Насыщенный пар используется во многих областях промышленности, поэтому для работы различных устройств важно поддерживать состояние насыщения пара.
Рассмотрим, как определить насыщенный пар или нет. Также в статье даны способы определения насыщенности пара, формула и примеры расчета.
Содержание
- Данные для определения насыщенности
- Методы
- Как найти?
- Как рассчитать?
- Несколько примеров
- Где эти расчеты могут пригодиться на практике?
- Заключение
Данные для определения насыщенности
Насыщенный пар или нет, можно определить, зная условия его возникновения и зависимость от различных факторов:
- Этот тип пара образуется только в закрытых сосудах.
- Образуется только над поверхностью исходной жидкости или льдом.
- Имеет свойство конденсации.
- Насыщен влагой.
- Температура пара всегда равна температуре его жидкости.
- Плотность и давления такого пара не зависят от объема.
- Насыщенный пар имеет прямую зависимость от температуры и давления.
Насыщенный пар находится в термодинамическом равновесии с жидкостью из которой он образован. На это указывает равенство массы испарения и последующей конденсации.

Методы
Математический способ определения насыщенного пара используется при вычислении на основе имеющихся данных о его давлении, температуре, влажности и по иным параметрам.
Также есть метод определения на основе отдельных данных:
- Замер температуры пара. Указывает на состояние насыщенного пара при условии равенства температур газа и жидкости. Любое отклонение от равенства укажет на потерю динамического равновесия и уровня влажности.
- По давлению. Измеряется давление пара и сравнивается с табличной величиной при актуальной температуре.
- По степени конденсации. Рассчитывается температура конденсата и скорость его образования.
- По уровню влажности. Влажность насыщенного пара всегда равна 100%.
Также существует метод определения по точке кипения. Он основан на расчете скорости парообразования при актуальном давлении. Например, при давлении 101 кПа, точкой парообразования является температура 100 градусов.
Существуют также некоторые лабораторные методы определения:
- статический,
- динамический,
- кинетический.
Они также основаны на замерах температуры, давления, плотности, влажности и конденсации при определенных условиях и сравнении полученных данных с таблицей насыщенного пара по температуре и давлению.
Как найти?
Свойства насыщенного пара не позволяют приравнивать его к идеальному газу, поэтому для его расчета используется формула Менделеева-Клапейрона.
Как рассчитать?
Расчет выполнятся по формуле: pV=vRT.
 Уравнение состоит из:
Уравнение состоит из:
- «p» — давление насыщенного пара (Па);
- «V» — его объем (м3);
- «v» — общее количество вещества (моль);
- «R» — газовая постоянная (8,31 м2);
- «T» — температура среды (К).
Данная формула помогает рассчитать не только параметры насыщенного пара, но и их изменения при изменении плотности, объема или давления.
Несколько примеров
Задача:
- В цилиндре находится насыщенный пар и вода при постоянной температуре.
- Поршень сдвигается, уменьшая свободный объем пространства.
- Выяснить, как повлияет уменьшение объема на общую массу жидкости.
Ответ: масса жидкости увеличится, по причине обратного фазового перехода пара в жидкость.
Согласно уравнению pV=m/u*Rt, при снижении общего объема пара не последует снижения его давления, а значит пар конденсируется обратно в воду, увеличив ее общую массу.
Задача:
- Температура насыщенного пара 100 градусов.
- Давление 101 кПа.
- Плотность неизвестна.
Решение: P=pu/Rt=105*18*10-3/8,31*373=0,5 кг/м3.
Ответ: насыщенный пар при температуре 100 градусов по Цельсию и при давлении 101 кПа имеет плотность 0,5 кг/м3. При решении данной задачи использовались табличные величины молярной массы, газовой постоянной и давлении при данной температуре.
Где эти расчеты могут пригодиться на практике?
 Расчет состояния насыщенного пара используется во многих сферах:
Расчет состояния насыщенного пара используется во многих сферах:
- при проектировании бытовых систем вентиляции и кондиционирования;
- для эффективной работы отопительных систем;
- при проектировании и поддержании работы паровых турбинных установок.
На основе этих расчетов строятся «умные» датчики влажности, которые реагируют на количество молекул воды или иных веществ в воздухе. Свойства насыщенного пара также применяются при выпаривании летучих веществ с их очисткой за счет последующей конденсации их насыщенных паров.
Заключение
Свойства насыщенного пара не делают его идеальным газом, но позволяют использовать в быту и в промышленности. Этот пар является идеальным источником тепла, влажности и помогает разделять химические элементы за счет способности к конденсации.
Формула расчета по уравнению Менделеева-Клапейрона позволяет рассчитать основные параметры пара и определить степень его схожести с насыщенным.
-
Давление насыщенного пара.
И что будет происходить с насыщенным
паром, если уменьшить занимаемый им
объем? Например, если сжимать пар,
находящийся в равновесии с жидкостью
в цилиндре под поршнем, поддерживая
температуру содержимого цилиндра
постоянной.
При сжатии пара равновесие
начнет нарушаться. Плотность пара в
первый момент немного увеличится, и из
газа в жидкость начнет переходить
большее число молекул, чем из жидкости
в газ. Ведь число молекул, покидающих
жидкость в единицу времени, зависит
только от температуры, и сжатие пара
это число не меняет. Процесс продолжается
до тех пор, пока вновь не установится
динамическое равновесие и плотность
пара, а значит, и концентрация его молекул
не примут прежнее значение. Следовательно,
концентрация молекул
насыщенного пара при постоянной
температуре не зависит от его объема.
Так как давление пропорционально
концентрации молекул (p
= nkT),
то из этого определения
следует, что давление
насыщенного пара не зависит oт
занимаемого им объема.
Давление пара
![]() ,
,
при котором жидкость
находится в равновесии со своим паром,
называют давлением насыщенного пара.
-
Ненасыщенный пар.
Мы много раз употребляли
слова газ и
пар. Никакой
принципиальной разницы между газом и
паром нет. Но если при
неизменной температуре газ простым
сжатием можно превратить в жидкость,
то мы называем его паром, точнее,
ненасыщенным паром.
-
Зависимость давления насыщенного пара от температуры.
Состояние
насыщенного
пара, как говорит опыт, приближенно
описывается уравнением
состояния идеального газа,
а его давление определяется формулой
![]()
С ростом температуры давление
растет.
Так как д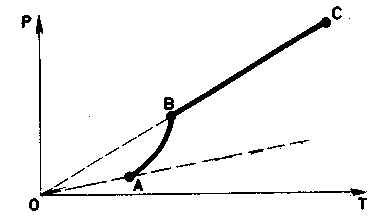 авление
авление
насыщенного
пара не зависит от объема, оно
зависит только от
температуры.
Однако
эта зависимость ро(Т),
найденная
экспериментально, не является
прямо пропорциональной, как
у идеального газа при постоянном
объеме. С увеличением температуры
давление насыщенного пара растет
быстрее, чем давление идеального
газа (рис. 30, участок кривой АВ).
Это становится
особенно очевидным,
если провести изохору через точку
А
(пунктирная
прямая) Почему
это происходит?
Однако эта зависимость
р(Т), найденная
экспериментально, не является
прямо пропорциональной, как
у идеального газа при постоянном
объеме. С увеличением температуры
давление насыщенного парабыстрее,
чем давление идеального
газа (рис. 30).Почему это
происходит?
При
нагревании жидкости в закрытом
сосуде часть жидкости превращается
в пар. В результате согласно
формуле
![]()
давление
насыщенного
пара растет не только вследствие
повышения температуры жидкости,
но и вследствие увеличения
концентрации молекул (плотности)
пара.
В основном
увеличение давления при повышении
температуры определяется именно
увеличением концентрации. Главное
различие в поведении идеального газа
и насыщенного пара состоит в том, что
при изменении температуры пара в закрытом
сосуде (или при изменении объема при
постоянной температуре) меняется масса
пара. Жидкость частично превращается
в пар или, напротив, пар частично
конденсируется. Когда вся жидкость
испарится, пар при дальнейшем нагревании
перестанет быть насыщенным и его давление
при постоянном объеме будет возрастать
прямо пропорционально абсолютной
температуре (см. рис. 30, участок ВС).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Это пар, находящийся в термодинамическом равновесии с жидкой (или твёрдой) фазой одного и того же вещества.
Одним из параметров, характеризующим насыщенный пар, является его давление.
Давление насыщенного пара зависит от температуры и не зависит от объема.
Разберемся подробнее, почему так происходит.
Почему давление насыщенного пара не зависит от объема?
Рассмотрим этот вопрос на примере дистиллированной воды.
Возьмем цилиндр с поршнем, в полости которого находится дистиллят в термодинамическом равновесии с паром. Начинаем двигать поршень вниз, объем цилиндра начинает уменьшаться, происходит сжатие насыщенного пара, при этом мы поддерживаем постоянную температуру.
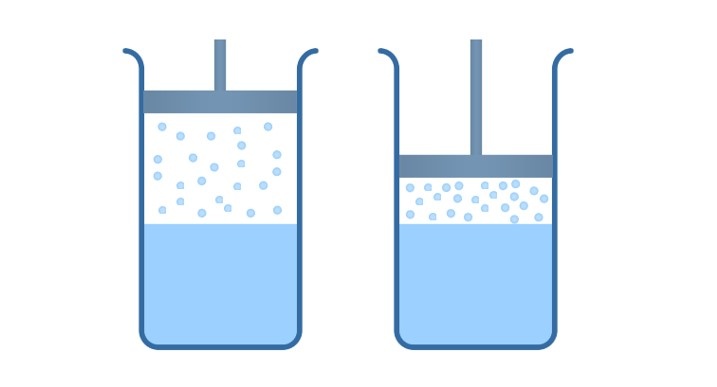
Система начнёт выходить из равновесия, плотность пара будет увеличиваться, и из газообразной фазы в жидкую будет переходить молекул больше, чем из жидкой в газообразную.
Другими словами, мы будем наблюдать процесс превращения насыщенного пара обратно в жидкость, этот процесс называется конденсация.
Если мы начнем поднимать поршень, объем полости увеличится, концентрация водяных паров над жидкостью начнет уменьшаться, вследствие чего, вода в сосуде начнет испаряться до тех пор, пока давление и концентрация насыщенного пара над жидкостью не придет в исходное состояние, то есть пока не наступит термодинамическое равновесие.
Из выше сказанного мы делаем вывод, что концентрация молекул насыщенного пара над жидкостью при постоянной температуре не зависит от его объема.
P=nkT,P=nkT,
где PP – давление пара (Па), nn – концентрация молекул пара (м-3), kk – постоянная Больцмана (равна 1,380649 Дж/К), ТТ – температура (К).
Из приведенной формулы мы видим, что давление насыщенного пара прямо пропорционально концентрации молекул и температуре паров над жидкостью (или твердым веществом) и, следовательно, не зависит от занимаемого им объема.
Как давление насыщенного пара зависит от температуры?
Из формулы, приведенной выше, мы наблюдаем, что давление насыщенного пара прямо пропорционально температуре термодинамической системы.
Несмотря на это, экспериментальная зависимость отличается от описанной уравнением, и давление пара увеличивается с большей скоростью с повышением температуры, нежели по линейному закону. Почему так происходит?
Всё дело в том, что во время увеличения подведенной температуры растёт и скорость испарения жидкости (или сублимации твёрдого вещества), вследствие этих факторов, увеличивается и концентрация испарённых (или сублимированных) молекул в газообразном состоянии над жидкой (или твёрдой) фазой. Поэтому и давление насыщенных паров изменяется быстрее. Плотность пара будет возрастать до тех пор, пока термодинамическое равновесие для данной температуры вновь не восстановится.
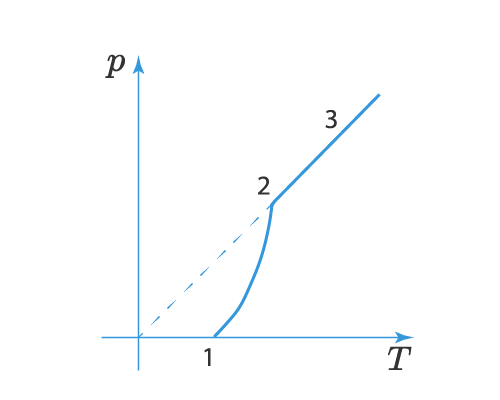
На участке 1-2 мы как раз видим влияние двух факторов – увеличение температуры и концентрации паров. В точке 2 вся жидкость испаряется (или твердое вещество сублимируется) и пар становится ненасыщенным, тогда давление начинает расти по линейному закону, что видно на участке 2-3.
Значения давления насыщенного пара для воды и других веществ при различных температурах получены эмпирическим методом. Эти данные можно найти в справочных материалах.
Тест по теме «Давление насыщенного пара»
Насыщенные и ненасыщенные пары.
Рассмотрим процессы, происходящие в закрытом сосуде:
- процесс испарения, скорость которого постепенно уменьшается
- конденсации, скорость которого постепенно возрастает
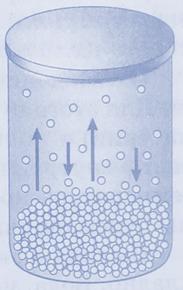
С течением времени в сосуде закрытом крышкой между жидкостью и её паром устанавливается состояние динамического (подвижного) равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, то есть когда скорости процессов испарения и конденсации одинаковы. Такую систему называютдвухфазной.
Пар, находящийся в динамическом равновесии со своей жидкостью, называютнасыщенным.
Название «насыщенный» подчеркивает, что в данном объеме при данной температуре не может находиться большее количество пара.
Ненасыщенный пар – это пар, не достигший динамического равновесия со своей жидкостью. При данной температуре давление ненасыщенного пара всегда меньше давления насыщенного пара. При наличии над поверхностью жидкости ненасыщенного пара процесс парообразования преобладает над процессом конденсации, и потому жидкости в сосуде с течением времени становится все меньше и меньше.
Рассмотрим некоторые свойства насыщенного пара:
1. Концентрация молекул насыщенного пара не зависит от его объёма при постоянной температуре. Если уменьшить объем насыщенного пара, то сначала концентрация его молекул увеличится и из газа в жидкость начнет переходить больше молекул до тех пор, пока опять на установится динамическое равновесие.
2. Давление насыщенного пара при постоянной температуре не зависит от его объёма.
p = n*k*T, т.к. n не зависит от V , то и р не зависит от V.
Независимое от объёма давление пара, при котором жидкость находится в равновесии со своим паром, называется давлением насыщенного пара. Это наибольшее давление, которое может иметь пар при данной температуре.
3. Давление насыщенного пара зависит от температуры. Чем выше будет температура жидкости, тем больше молекул будет испаряться, динамическое равновесие нарушится, но концентрация молекул пара будет расти до тех пор, пока равновесие не установится опять, а значит, больше станет и давление насыщенного пара. С увеличением температуры давление насыщенных паров возрастает.
В атмосферном воздухе всегда присутствуют пары воды, которая испаряется с поверхности морей, рек, океанов и т.п.
Воздух, содержащий водяной пар, называют влажным.
Влажность воздуха оказывает огромное влияние на многие процессы на Земле: на развитие флоры и фауны, на урожай сельхоз. культур, на продуктивность животноводства и т.д. Влажность воздуха имеет большое значение для здоровья людей, т.к. от неё зависит теплообмен организма человека с окружающей средой. При низкой влажности происходит быстрое испарение с поверхности и высыхание слизистой оболочки носа, гортани, что приводит к ухудшению состояния.
Значит, влажность воздуха надо уметь измерять. Для количественной оценки влажности воздуха используют понятия абсолютной и относительной влажности.
Абсолютная влажность – величина, показывающая, какая масса паров воды находится в 1 м³ воздуха. Она равна парциальному давлению пара при данной температуре.
Парциальное давление пара – это давление, которое оказывал бы водяной пар, находящийся в воздух , если бы все остальные газы отсутствовали.
Относительная влажность воздуха – это величина, показывающая, как далек пар от насыщения. Это отношение парциального давления p водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного пара p0 при той же температуре, выраженное в процентах:
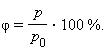
Если воздух не содержит паров воды, то его абсолютная и относительная влажность равны 0.
Если влажный воздух охлаждать, то находящийся в нем пар можно довести до насыщения, и далее он будет конденсироваться.
Примеры:
выпадение росы под утро,

запотевание холодного стекла, если на него подышать,

образование капли воды на холодной водопроводной трубе,

сырость в подвалах домов.

Точка росы – это температура, при которой водяной пар, содержащийся в воздухе, становится насыщенным.
Точка росы также характеризует влажность воздуха.
|
C° |
Точка россы при относительной влажности воздуха в % |
|||||||||||||
|
30% |
35% |
40% |
45% |
50% |
55% |
60% |
65% |
70% |
75% |
80% |
85% |
90% |
95% |
|
|
30 |
10,5 |
12,9 |
14,9 |
16,8 |
18,4 |
20 |
21,4 |
22,7 |
23,9 |
25,1 |
26,2 |
27,2 |
28,2 |
29,1 |
|
29 |
9,7 |
12 |
14 |
15,9 |
17,5 |
19 |
20,4 |
21,7 |
23 |
24,1 |
25,2 |
26,2 |
27,2 |
28,1 |
|
28 |
8,8 |
11,1 |
13,1 |
15 |
16,6 |
18,1 |
19,5 |
20,8 |
22 |
23,2 |
24,2 |
25,2 |
26,2 |
27,1 |
|
27 |
8 |
10,2 |
12,2 |
14,1 |
15,7 |
17,2 |
18,6 |
19,9 |
21,1 |
22,2 |
23,3 |
24,3 |
25,2 |
26,1 |
|
26 |
7,1 |
9,4 |
11,4 |
13,2 |
14,8 |
16,3 |
17,6 |
18,9 |
20,1 |
21,2 |
22,3 |
23,3 |
24,2 |
25,1 |
|
25 |
6,2 |
8,5 |
10,5 |
12,2 |
13,9 |
15,3 |
16,7 |
18 |
19,1 |
20,3 |
21,3 |
22,3 |
23,2 |
24,1 |
|
24 |
5,4 |
7,6 |
9,6 |
11,3 |
12,9 |
14,4 |
15,8 |
17 |
18,2 |
19,3 |
20,3 |
21,3 |
22,3 |
23,1 |
|
23 |
4,5 |
6,7 |
8,7 |
10,4 |
12 |
13,5 |
14,8 |
16,1 |
17,2 |
18,3 |
19,4 |
20,3 |
21,3 |
22,2 |
|
22 |
3,6 |
5,9 |
7,8 |
9,5 |
11,1 |
12,5 |
13,9 |
15,1 |
16,3 |
17,4 |
18,4 |
19,4 |
20,3 |
21,1 |
|
21 |
2,8 |
5 |
6,9 |
8,6 |
10,2 |
11,6 |
12,9 |
14,2 |
15,3 |
16,4 |
17,4 |
18,4 |
19,3 |
20,2 |
|
20 |
1,9 |
4,1 |
6 |
7,7 |
9,3 |
10,7 |
12 |
13,2 |
14,4 |
15,4 |
16,4 |
17,4 |
18,3 |
19,2 |
|
19 |
1 |
3,2 |
5,1 |
6,8 |
8,3 |
9,8 |
11,1 |
12,3 |
13,4 |
14,5 |
15,3 |
16,4 |
17,3 |
18,2 |
|
18 |
0,2 |
2,3 |
4,2 |
5,9 |
7,4 |
8,8 |
10,1 |
11,3 |
12,5 |
13,5 |
14,5 |
15,4 |
16,3 |
17,2 |
|
17 |
-0,6 |
1,4 |
3,3 |
5 |
6,5 |
7,9 |
9,2 |
10,4 |
11,5 |
12,5 |
13,5 |
14,5 |
15,3 |
16,2 |
|
16 |
-1,4 |
0,5 |
2,4 |
4,1 |
5,6 |
7 |
8,2 |
9,4 |
10,5 |
11,6 |
12,6 |
13,5 |
14,4 |
15,2 |
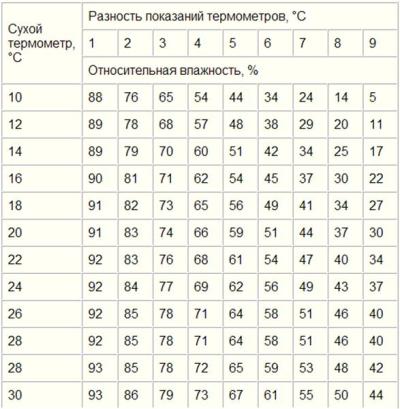
Для измерения влажности воздуха используют приборы гигрометры и психрометры.
1. Конденсационный гигрометр.

Состоит из укрепленной на подставке металлической круглой коробочки с отполированной плоской поверхностью. В коробочке сверху имеются два отверстия. Через одно из них в коробочку наливают эфир и вставляют термометр, а другое соединяют с резиновой грушей. Действие конденсационного гигрометра основано на определении точки росы.
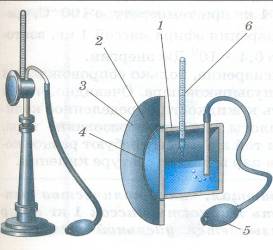
Продувают воздух через эфир (с помощью резиновой груши), при этом эфир быстро испаряется и охлаждает коробочку. При определенной температуре на отполированной поверхности коробочки появляются капельки воды (роса). По термометру определяют эту температуру, это и будет точка росы. В специальной таблице по точке росы находят абсолютную влажность.
Чтобы найти относительную влажность, надо давление насыщенного пара при температуре точки росы разделить на давление насыщенного пара при температуре окружающего воздуха и умножить на 100%.
2. Волосной гигрометр.

Его работа основана на том, что обезжиренный человеческий волос при увеличении влажности воздуха удлиняется, а при уменьшении влажности укорачивается. Волос оборачивают вокруг легкого блока, прикрепив один конец к раме, а к другому подвешивают груз. При изменении длины волоса указатель (стрелка), прикрепленный к блоку, будет двигаться, перемещаясь по шкале. Шкалу градуируют по эталонному прибору.
3. Психрометр. (от греч «психриа» – холод).

Состоит из двух одинаковых термометров. Резервуар одного из них обернут марлей, опущенной в сосуд с водой. Вода смачивает резервуар термометра и при её испарении он охлаждается. По разности температур сухого и влажного термометров по психрометрической таблице определяют влажность воздуха.