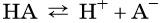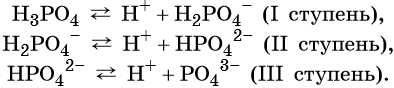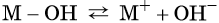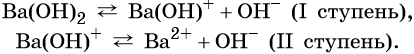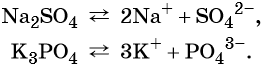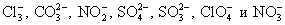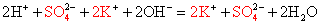Анионы и катионы. Как правильно посчитать количество анионов и катионов.
Андрей Ломакин
Профи
(530),
закрыт
6 лет назад
Лучший ответ
Людмила Фролова
Мыслитель
(7488)
6 лет назад
это зависит от формулы всего соединения, например:
NaCl – 1 катион и 1 анион
Al2(SO4)3 -2 катиона и 3 аниона
Остальные ответы
Тугеус Владимир
Искусственный Интеллект
(174779)
6 лет назад
Взвесить образец вещества, поделить на молярную массу и найти количество вещества. Ну а теперь то, что написала Людмила, умножить на число Авогадро 6·10²³
Похожие вопросы
Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей (средних)
Катионами называют положительно заряженные ионы.
Анионами называют отрицательно заряженные ионы.
В процессе развития химии понятия «кислота» и «основание» претерпели серьёзные изменения. С точки зрения теории электролитической диссоциации кислотами называют электролиты, при диссоциации которых образуются ионы водорода H + , а основаниями — электролиты, при диссоциации которых образуются гидроксид-ионы OH – . Эти определения в химической литературе известны как определения кислот и оснований по Аррениусу.
В общем виде диссоциацию кислот представляют так:
где A – — кислотный остаток.
Такие свойства кислот, как взаимодействие с металлами, основаниями, основными и амфотерными оксидами, способность изменять окраску индикаторов, кислый вкус и т. д., обусловлены наличием в растворах кислот ионов H + . Число катионов водорода, которые образуются при диссоциации кислоты, называют её основностью. Так, например, HCl является одноосновной кислотой, H2SO4 — двухосновной, а H3PO4 — трёхосновной.
Многоосновные кислоты диссоциируют ступенчато, например:
От образовавшегося на первой ступени кислотного остатка H2PO4 – последующий отрыв иона H + происходит гораздо труднее из-за наличия отрицательного заряда на анионе, поэтому вторая ступень диссоциации протекает гораздо труднее, чем первая. На третьей ступени протон должен отщепляться от аниона HPO4 2– , поэтому третья ступень протекает лишь на 0,001%.
В общем виде диссоциацию основания можно представить так:
где M + — некий катион.
Такие свойства оснований, как взаимодействие с кислотами, кислотными оксидами, амфотерными гидроксидами и способность изменять окраску индикаторов, обусловлены наличием в растворах OH – -ионов.
Число гидроксильных групп, которые образуются при диссоциации основания, называют его кислотностью. Например, NaOH — однокислотное основание, Ba(OH)2 — двухкислотное и т. д.
Многокислотные основания диссоциируют ступенчато, например:
Большинство оснований в воде растворимо мало. Растворимые в воде основания называют щелочами.
Прочность связи М—ОН возрастает с увеличением заряда иона металла и увеличением его радиуса. Поэтому сила оснований, образуемых элементами в пределах одного и того же периода, уменьшается с возрастанием порядкового номера. Если один и тот же элемент образует несколько оснований, то степень диссоциации уменьшается с увеличением степени окисления металла. Поэтому, например, у Fe(OH)2 степень основной диссоциации больше, чем у Fe(OH)3.
Электролиты, при диссоциации которых одновременно могут образовываться катионы водорода и гидроксид-ионы, называют амфотерными. К ним относят воду, гидроксиды цинка, хрома и некоторые другие вещества. Их полный перечень приведён в уроке 6, а их свойства рассмотрены в уроке 16.
Солями называют электролиты, при диссоциации которых образуются катионы металлов (а также катион аммония NH4 + ) и анионы кислотных остатков.
Химические свойства солей будут описаны в уроке 18.
Тренировочные задания
1. К электролитам средней силы относится
2. К сильным электролитам относится
3. Сульфат-ион в значительном количестве образуется при диссоциации в водном растворе вещества, формула которого
4. При разбавлении раствора электролита степень диссоциации
1) остается неизменной
2) понижается
3) повышается
4) с начала повышается, потом понижается
5. Степень диссоциации при нагревании раствора слабого электролита
1) остается неизменной
2) понижается
3) повышается
4) с начала повышается, потом понижается
6. Только сильные электролиты перечислены в ряду:
7. Водные растворы глюкозы и сульфата калия соответственно являются:
1) с ильным и слабым электролитом
2) неэлектролитом и сильным электролитом
3) слабым и сильным электролитом
4) слабым электролитом и неэлектролитом
8. Степень диссоциации электролитов средней силы
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03—0,3
4) менее 0,03
9. Степень диссоциации сильных электролитов
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03—0,3
4) менее 0,03
10. Степень диссоциации слабых электролитов
1) больше 0,6
2) больше 0,3
3) лежит в пределах 0,03—0,3
4) менее 0,03
11. Электролитами являются оба вещества:
1) фосфорная кислота и глюкоза
2) хлорид натрия и сульфат натрия
3) фруктоза и хлорид калия
4) ацетон и сульфат натрия
12. В водном растворе фосфорной кислоты H3PO4 наименьшая концентрация частиц
13. Электролиты расположены в порядке увеличения степени диссоциации в ряду
14. Электролиты расположены в порядке уменьшения степени диссоциации в ряду
15. Практически необратимо диссоциирует в водном растворе
1) уксусная кислота
2) бромоводородная кислота
3) фосфорная кислота
4) гидроксид кальция
16. Электролитом, более сильным по сравнению с азотистой кислотой, будет
1) уксусная кислота
2) сернистая кислота
3) фосфорная кислота
4) гидроксид натрия
17. Ступенчатая диссоциация характерна для
1) фосфорной кислоты
2) соляной кислоты
3) гидроксида натрия
4) нитрата натрия
18. Только слабые электролиты представлены в ряду
1) сульфат натрия и азотная кислота
2) уксусная кислота, сероводородная кислота
3) сульфат натрия, глюкоза
4) хлорид натрия, ацетон
19. Каждое из двух веществ является сильным электролитом
1) нитрат кальция, фосфат натрия
2) азотная кислота, азотистая кислота
3) гидроксид бария, сернистая кислота
4) уксусная кислота, фосфат калия
20. Оба вещества являются электролитами средней силы
1) гидроксид натрия, хлорид калия
2) фосфорная кислота, азотистая кислота
3) хлорид натрия, уксусная кислота
4) глюкоза, ацетат калия
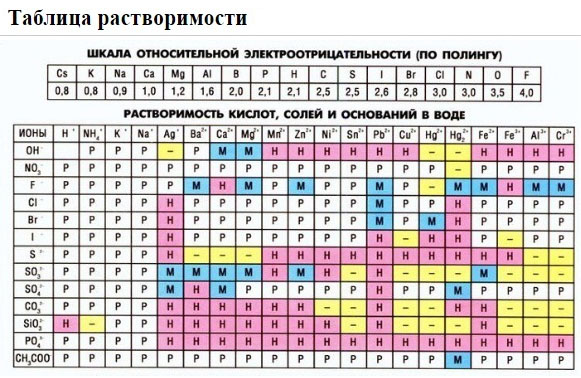
Катионы и анионы в химии, таблица растворимости
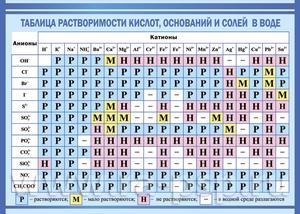
Показатели растворимости в воде
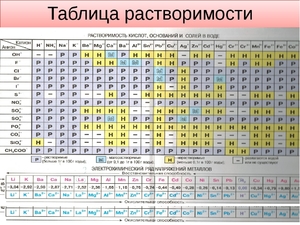
Она помогает при решении химических уравнений, где участвуют ионные реакции. Если результатом будет получение нерастворимого вещества, то реакция возможна. Существует несколько вариантов:
- Вещество хорошо растворяется;
- Малорастворимо;
- Практически не растворяется;
- Нерастворимо;
- Гидрализуется и не существует в контакте с водой;
- Не существует.
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
Электролиты
Это растворы или сплавы, проводящие электрический ток. Электропроводность их объясняется мобильностью ионов. Электролиты можно поделить на 2 группы:
- Сильные. Растворяются полностью, независимо от степени концентрации раствора.
- Слабые. Диссоциация проходит частично, зависит от концентрации. Уменьшается при большой концентрации.
Теория электролитической растворимости
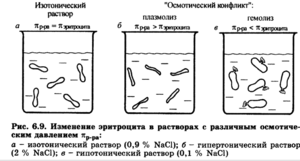
Одновременно с диссоциацией проходит противоположный процесс – соединение ионов в молекулы. Кислоты – это такие электролиты, при распаде которых образуется катион – ион водорода. Основания – анионы – это гидроксид ионы. Щелочи – это основания, которые растворяются в воде. Электролиты, которые способны образовывать и катионы и анионы, называются амфотерными.
Это такая частица, в которой больше протонов или электронов, он будет называться анион или катион, в зависимости от того, чего больше: протонов или электронов. В качестве самостоятельных частиц они встречаются во многих агрегатных состояниях: газах, жидкостях, кристаллах и в плазме. Понятие и название ввёл в обиход Майкл Фарадей в 1834 году. Он изучал воздействие электричества на растворы кислот, щелочей и солей.
Простые ионы несут на себе ядро и электроны. Ядро составляет почти всю атомную массу и состоит из протонов и нейтронов. Количество протонов совпадает с порядковым номером атома в периодической системе и зарядом ядра. Ион не имеет определённых границ из-за волнового движения электронов, поэтому невозможно измерить их размеры.
Отрыв электрона от атома требует, в свою очередь, затрат энергии. Она называется энергия ионизации. Когда присоединяется электрон, происходит выделение энергии.
Катионы
Это частицы, носящие положительный заряд. Могут иметь разную величину заряда, например: Са2+ — двузарядный катион, Na+ — однозарядный катион. Мигрируют к отрицательному катоду в электрическом поле.
Анионы
Это элементы, имеющие отрицательный заряд. А также обладает различным количеством величины зарядов, например, CL- — однозарядный ион, SO42- — двухзарядный ион. Такие элементы входят в состав веществ, обладающих ионной кристаллической решёткой, в поваренной соли и многих органических соединениях.
- Натрий. Щелочной металл. Отдав один электрон, находящийся на внешнем энергетическом уровне, атом превратится в положительный катион.
- Хлор. Атом этого элемента принимает на последний энергетический уровень один электрон, он превратится в отрицательный хлорид анион.
- Поваренная соль. Атом натрия отдаёт электрон хлору, вследствие этого в кристаллической решётке катион натрия окружён шестью анионами хлора и наоборот. В результате такой реакции образуется катион натрия и анион хлора. Благодаря взаимному притяжению формируется хлорид натрия. Между ними образуется прочная ионная связь. Соли — это кристаллические соединения с ионной связью.
- Кислотный остаток. Это отрицательно заряженный ион, находящийся в сложном неорганическом соединении. Он встречается в формулах кислот и солей, стоит обычно после катиона. Практически для всех таких остатков есть своя кислота, например, SO4 – от серной кислоты. Кислот некоторых остатков не существует, и их записывают формально, но они образуют соли: фосфит ион.
Химия – наука, где возможно творить практически любые чудеса. Катион вы можете узнать по ссылке.
Ионные уравнения
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации. Разберем историю вопроса, алгоритм составления ионных уравнений и примеры задач.
ИСТОРИЯ ВОПРОСА
Еще древние алхимики, проводя нехитрые химические реакции в поисках философского камня и записывая в толстые фолианты результаты своих исследований, использовали определенные знаки для химических веществ. У каждого ученого была своя система, что неудивительно: каждый хотел защитить свои тайные знания от происков завистников и конкурентов. И лишь в VIII веке появляются единые обозначения для некоторых элементов.
В 1615 году Жан Бегун в своей книге «Начала химии», что по праву считается одним из первых учебников в этом разделе естествознания, предложил использовать условные обозначения для записи химических уравнений. И лишь в 1814 году шведский химик Йонс Якоб Берцелиус создал систему химических символов на основе одной или двух первых букв латинского названия элемента, подобную той, с которой ученики знакомятся на уроках.
В восьмом классе (параграф 12, учебник «Химия. 8 класс» под редакцией В.В. Еремина) ребята научились составлять молекулярные уравнения реакций, где и реагенты, и продукты реакций представлены в виде молекул.
Однако это упрощенный взгляд на химические превращения. И об этом задумывались ученые уже в XVIII веке.
Аррениус в результате своих экспериментов выяснил, что растворы некоторых веществ проводят электрический ток. И доказал, что вещества, обладающие электропроводностью, в растворах находятся в виде ионов: положительно заряженных катионов и отрицательно заряженных анионов. И именно эти заряженные частицы вступают в реакции.
ЧТО ТАКОЕ ИОННЫЕ УРАВНЕНИЯ
Ионные уравнения реакций — это химические равенства, в которых вещества, вступающие в реакцию, и продукты реакций обозначены в виде диссоциированных ионов. Уравнения данного типа подходят для записи химических реакций замещения и обмена в растворах.
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации (тема подробно разбирается в параграфе 10, учебник «Химия. 9 класс» под редакцией В.В. Еремина). В виде молекул записывают газы, вещества, выпадающие в осадок, и слабые электролиты, которые практически не диссоциируют. Газы обозначаются стрелкой вверх (↑), субстанции, выпадающие в осадок, стрелкой вниз (↓).
ОСОБЕННОСТИ ИОННЫХ УРАВНЕНИЙ
1. Реакции ионного обмена, в отличие от окислительно-восстановительных реакций, протекают без нарушения валентности веществ, вступающих в химические превращения.

2. Реакции между ионами протекают при условии образования в ходе реакции плохорастворимого осадка, выделения летучего газа или образования слабых электролитов.
Удивительно, что реакции обмена могут проходить даже с нерастворимыми солями слабых кислот. В этом случае сильная кислота вытесняет слабую из ее солей. В качестве примера можно привести сокращенное ионное уравнение разведения карбоната кальция в сильных кислотах.
АЛГОРИТМ СОСТАВЛЕНИЯ ИОННОГО УРАВНЕНИЯ
Записываем молекулярное уравнение химического процесса.
Балансируем молекулярное уравнение с помощью коэффициентов.
Чтобы правильно сбалансировать равенство, нужно вспомнить закон сохранения массы веществ (параграф 12, «Химия. 8 класс» под редакцией В.В. Еремина), согласно которому в ходе химических превращений новые атомы не появляются, а старые не разрушаются. Т.е. число атомов в продуктах реакции равно числу атомов в исходных веществах. Помним, что водород и кислород уравниваем в последнюю очередь.
Определяем, какие вещества в химической реакции диссоциируют, т.е. распадаются на ионы.
Записываем в виде ионов:
- растворимые соли;
- сильные кислоты (H2SO4, HNO3, HCl и др.);
- растворимые в воде основания.
Записываем в виде молекул:
- нерастворимые соли;
- слабые кислоты, щелочи, вода;
- оксиды;
- газы;
- простые вещества;
- большинство органических соединений.
Если есть сомнения в растворимости реагента или продукта реакции, можно проверить по специальной таблице, которая является справочным материалом, ей можно пользоваться на различных экзаменах.
В таблице, помимо растворимости соединений, представлены также заряды катионов и анионов, участвующих в реакциях.
Определяем многоатомные ионы.
Это необходимо сделать, т.к. данные соединения не разлагаются на отдельные атомы и имеют свой заряд. Чаще всего в химических превращениях участвуют следующие многоатомные ионы:
Записываем равенство таким образом, чтобы все диссоциирующие субстанции были представлены в виде катионов и анионов.
Проверяем, чтобы уравнение было сбалансировано, т.е. количество различных атомов в частях с реагентами и продуктами реакции совпадало.
На данном этапе мы получили полное ионное уравнение.
Вычеркиваем идентичные ионы в обеих частях равенства, т.е. катионы и анионы с одинаковыми нижними индексами и зарядами, и переписываем равенство без данных ионов.
Проверяем, чтобы количество атомов элементов совпадало в правой и левой частях уравнения. Таким образом получаем краткое ионное уравнение.
ПРИМЕРЫ
Задача 1
Выясните, произойдет ли химическое взаимодействие между растворами гидроксида калия и хлорида аммония. (Записать для реакции молекулярное, полное ионное и сокращенное ионное уравнение.)
Записываем молекулярное уравнение, проверяем коэффициенты.
Помним, что гидроксид аммония — нестабильное соединение и разлагается на аммиак и воду.
Записываем окончательное уравнение:
NB! Благодаря летучести и резкому раздражающему запаху 3%-й раствор NH3 называется «нашатырный спирт» и используется в медицине.
Подсматривая в таблицу растворимости, помечаем полное ионное уравнение, не забывая о зарядах ионов.
Вычеркивая идентичные катионы и анионы в обеих частях реакции, составляем краткое ионное уравнение.
Делаем вывод: химическая реакция между гидроксидом калия и хлоридом аммония протекает с образованием воды и выделением аммиака — летучего газа с резким запахом.
Задача 2
А сейчас выполним задание из учебника «Химия. 9 класс» под редакцией В.В. Еремина.
Налейте в пробирку 1 мл раствора карбоната натрия и аккуратно прилейте к нему пару капелек соляной кислоты.
Составьте уравнение реакции, напишите полное и сокращенное ионные уравнения.
Записываем реакцию в молекулярном виде, расставляем коэффициенты, если это необходимо.
Подсматривая в таблицу растворимости, записываем полное ионное уравнение, не забывая отмечать заряды ионов.
Вычеркивая одинаковые катионы и анионы в правой и левой частях равенства, составляем краткое ионное уравнение.
Вопрос «Что происходит?» остался без ответа. К сожалению, в домашних условиях этот опыт осуществить трудновато, так как стиральной содой уже давно никто не пользуется, да и соляную кислоту в аптеке уже не продают. Но примерно такой же визуальный эффект можно наблюдать, если смешать раствор пищевой соды с раствором уксусной кислоты.
источники:
http://obrazovanie.guru/himiya/kationy-i-aniony-tablitsa-rastvorimosti.html
http://rosuchebnik.ru/material/ionnye-uravneniya/
Результаты (отдельно
для катионов и отдельно для анионов)
запишите в соответствующие строки
второй вертикальной колонки таблицы
(рис.9). Суммы катионов и анионов должны
быть равны или могут незначительно
отличаться друг от друга, так как
некоторые ионы (А13+
СОз2+
и другие) не были учтены. Если
суммы катионов (К) и анионов (А) различаются
более чем на 5%, т.е. если 5%,
то допущена ошибка в расчетах или при
переписывании исходных данных.
Эту ошибку необходимо найти и исправить.
Рис 9. Химический
состав той же пробы, что и на рис.8,
пересчитанный в эквивалентную форму
(по Гречину П.И. и др. 2003).
|
Ионы |
мг/л |
мг-экв/л |
%-экв |
|
|
Катионы |
NH4l+ |
– |
– |
|
|
NaI++KI+ |
21,2 |
0,9 |
||
|
Mg2+ |
19,4 |
1,6 |
||
|
Са2+ |
68,0 |
3,4 |
||
|
Fe |
0,1 |
– |
||
|
A13+ |
– |
– |
||
|
Сумма |
108,7 |
5,6 |
||
|
Анионы |
||||
|
CI1– |
6,0 |
0,2 |
||
|
SO42– |
33,2 |
0,7 |
||
|
HCO31– |
298,0 |
4,9 |
||
|
СО22– |
– |
– |
||
|
NO3l– |
0,06 |
– |
||
|
Сумма |
338,1 |
5,8 |
||
|
Общая |
446,7 |
– |
5. Определить
процент-эквивалентное содержание ионов.
Для этого сумму
отдельно катионов (и, соответственно,
отдельно анионов) принимают за 100% и
вычисляют «долю» каждого катиона
(аниона). Точность – до целых единиц. При
одинаковом содержание двух катионов
(или анионов), точность следует повысить
и определить какого иона больше.
Результат записать в третью вертикальную
колонку таблицы (рис.10). Обязательно
проверьте, составляет ли содержание
катионов (анионов) в сумме 100
процент-эквивалентов.
Рис.10. Заполнение
таблицы химического состава воды
(окончание).
|
Ионы |
мг/л |
мг-экв/л |
%-экв |
|
|
Катионы |
NH4l+ |
– |
– |
– |
|
NaI++KI+ |
21,2 |
0,9 |
15 |
|
|
Mg2+ |
19,4 |
1,6 |
27 |
|
|
Са2+ |
68,0 |
3,4 |
58 |
|
|
Fe |
0,1 |
– |
– |
|
|
A13+ |
– |
– |
– |
|
|
Сумма |
108,7 |
5,6 |
100 |
|
|
Анионы |
||||
|
CI1– |
6,0 |
0,2 |
3 |
|
|
SO42– |
33,2 |
0,7 |
12 |
|
|
HCO31– |
298,0 |
4,9 |
85 |
|
|
СО22– |
– |
– |
– |
|
|
NO3l– |
0,06 |
– |
– |
|
|
Сумма |
338,1 |
5,8 |
100 |
|
|
Общая |
446,7 |
– |
– |
Примечание:
по указанию преподавателя при составлении
таблицы кроме основных могут быть учтены
и другие ионы, например F1–.
Задание 2. Составить
формулу Курлова и дать характеристику
воды по
классификации
Алекина.
Здравствуйте дорогие читатели. Сегодня вам разберу что такое электролите и неэлектролиты. И как решить задание где нужно найти сколько молей катионов или анионов надо найти в данном веществе.
Давайте сперва разберем что такое электролиты и неэлектролиты и какие вещества относятся к электролитам, а какие вещества не относятся к электролитам.
Электролиты — вещества, водные растворы которых или расплавы проводят электрический ток.
Неэлектролиты — вещества, водные растворы которых не проводят электрический ток.
К электролитам относятся соли, кислоты, основания. Так, типичными электролитами являются:
— кислоты (НСl, HNO3, H2SO4, Н3РO4, СН3СООН, HF и др.);
— основания (КОН, NaOH, Са(ОН)2, Ва(ОН)2, NH3 ∙ Н2O и др.);
— соли (NaCl, K2SO4, Ca(NO3)2, CH3COONa, NH4Cl и др.).
Большинство органических веществ электролитами не являются. Так, не относятся к электролитам углеводороды, спирты, альдегиды, углеводы и другие.
А электропроводность электролитов обусловлена присутствием в их растворах (или расплавах) ионов, которые и обеспечивают прохождение электрического тока. Для объяснения электропроводности водных растворов кислот, солей и оснований С. Аррениус выдвинул в 1887 г. теорию электролитической диссоциации.
В соответствии с теорией электролитической диссоциции, электролиты при растворении в воде распадаются (диссоциируют) на ионы, которые являются положительно заряженными и отрицательно заряженными. Положительно заряженные ионы называются катионами, отрицательно заряженные — анионами.
В общем виде диссоциация электролита KatAn может быть записана так:
Все электролиты можно разделить на сильные и слабые. Сильные электролиты в разбавленных водных растворах полностью диссоциируют на ионы. К сильным электролитам относятся все щёлочи, многие кислоты (такие как НСlO4, НСlO3, НСl, HNO3, H2SO4, HMnO4 и некоторые другие), а также практически все соли (даже если они малорастворимы, т.к. в водном растворе не существуют “молекулы” солей). Слабые электролиты лишь в малой степени диссоциируют на ионы. К слабым электролитам относятся вода, органические кислоты (уксусная, щавелевая, лимонная и тогдалее ), многие неорганические кислоты (сернистая, сероводородная, плавиковая, азотистая, хлорноватистая и другие). В отличие от сильных электролитов, диссоциация слабых электролитов обратима.
Начнем разбор с электролитической диссоциации солей.
Электролитическая диссоциация солей
С точки зрения теории электролитической диссоциации соли — сложные вещества, при диссоциации которых образуются катионы металлов и анионы кислотных остатков. Практически все соли относятся к сильным электролитам, полностью распадаясь в водных растворах на ионы:
Если рассмотреть малорастворимые соли, как AgCl или BaSO4 (их растворимость мизерна и не превышает 10-5 моль/л), та часть их, которая перешла в раствор, полностью распадается на ионы:
А кислые и основные соли диссоциируют ступенчато.
Например, давайте рассмотрим задание из ОГЭ.
Задание из ОГЭ: 3 моль анионов образуется при полной диссоциации 1 моль
1) фосфата калия (K3PO4)
2) нитрата алюминия (Al(NO3)3)
3) нитрата натрия (NaNO3)
4) сульфата меди(II) (CuSO4)
5) хлорида железа(III) (FeCl3)
Нам нужно найти в каком из соединений при диссоциации 1 моль вещества образуется 3 моль аниона, то есть если разложить вещества на положительно заряженные ионы (катионы) и на отрицательно заряженные ионы (анионы). При разложении первого вещества (фосфата калия) на положительные и отрицательные ионы образуется 3 моль катиона калия и 1 моль фосфат анионов. При разложении второго вещества ( нитрата алюминия) образуется 1 моль катиона алюминия и 3 моль нитрат анионов. При разложении третьего вещества ( сульфата меди(II)) образуется 1 моль катиона меди и 1 моль сульфат анионов. При разложении четвертого вещества (хлорида железа(III)) образуется у моль катиона железа и 3 моль хлорид анионов. Из всех веществ подходят два вещества, это нитрат алюминия и хлорида железа(II), и при этом оба вещества растворимы, что говорит о том что они диссоциируются полностью. Из этого следует что приведенном мною примере два ответа.
В следующей статье я продолжу разбирать тему где в задании по ОГЭ нужно найти сколько анионов и катионов образуются. И в следующей статье разберу диссоциацию кислот и оснований, а также амотерных гидроксидов.
Certain kinds of atoms form regular three-dimensional repeating structures when they bond with other elements. These repeating patterns are called crystal lattices, and they are characteristic of ionic solids, or compounds that contain ionic bonds, such as table salt (much more below).
These crystals have tiny repeating sections that boast cations, or positively charged atoms, at their center. This central atom is geometrically associated with a certain number of anions via one of a number of familiar patterns. Each anion in turn can be envisioned as sitting at the center of its own repeating unit and associating with a certain number of cations, which may be the same number or a different number as in the cation-at-center example.
This number, called the coordination number or ligancy, applies to ions rather than “native” atoms and determines the greater three-dimensional shape of the solid in predictable ways that relate to fundamental atomic architecture. It also determines the color owing to specific and unique distances between electrons and other components of the crystal lattice.
Determining the Coordination Number
If you happen to have access to three-dimensional models of common crystal lattice patters, you can visually inspect one “unit” from the perspective of both the anion and the cation and see how many “arms” reach out to the ion of opposite charge. In most cases, however, you will have to rely on a combination of online research and using molecular formulas.
Example: The formula for the ionic compound sodium chloride, or table salt, is NaCl. This means that every cation should have exactly one anion associated with it; in the language of ligancy, this means that the cation Na+ and the anion Cl− have the same coordination number.
Upon inspection, the structure of NaCl shows each Na+ ion having a Cl− neighbor above and below, to the left and to the right, and ahead and behind. The same is true from the Cl− perspective. The coordination number for both ions is 6.
Coordination Number of a Heavier Ion
Cations and anions present a 1:1 molecular ratio in a crystal, which means that they have the same coordination number, but this does not mean that the number is fixed at 6. The number 6 is a convenient number in three-dimensional space because of the up-down-right-left-forward-backward symmetry. But what if these “connections” were oriented diagonally, as if pointing away from the center of a cube toward all its corners?
In fact, this is how the lattice of cesium chloride, or CsCl, is arranged. Cesium and sodium have the same number of valence electrons, so in theory NaCl and CsCl might exhibit similar crystals. However, a cesium ion is far more massive than a sodium ion, and because it takes up more space, it is better accommodated with a coordination number of 8. Now, neighboring ions are found purely along diagonals; they are more distant than in NaCl, but also more numerous.
Because cesium and chlorine exist in a 1:1 ratio in this compound, the coordination number for the chloride ion in this instance is 8.
Unequal Coordination Number Example
Titanium oxide (TiO2) is an example of a crystal structure containing anions and cations in a 2:1 ratio. So, the fundamental unit of the lattice is tetrahedral: Each Ti4+ cation is amid six O2-ions, while every O2-ion has three immediate Ti4+ neighbors.
The coordination number for Ti4+ is 6, while that of the O2-ion is 3. This makes chemical sense since the formula TiO2 implies that twice as many oxygen ions exist in this compound as do titanium ions.