Загрузить PDF
Загрузить PDF
Протоны, нейтроны и электроны – основные частицы, из которых состоит атом. Протоны заряжены положительно, электроны – отрицательно, а нейтроны и вовсе не имеют заряда.[1]
Масса электронов очень мала, а масса протонов и нейтронов практически одинакова.[2]
На самом деле, найти в атоме количество протонов, нейтронов и электронов довольно просто, нужно только научиться ориентироваться по периодической таблице химических элементов Д.И.Менделеева.
-

1
Возьмите периодическую таблицу элементов. Это система, в которой элементы организованы в зависимости от их атомной структуры. Цветное одно- или двухбуквенное сокращение – это название элемента в сокращенном виде. В таблице также представлена информация об атомном номере элемента и атомной массе.[3]
- Таблицу Менделеева можно найти в учебнике по химии или в Интернете.
- Во время контрольных работ периодическую таблицу обычно предоставляют.
-

2
Найдите в таблице нужный вам элемент. Каждый элемент в таблице располагается под своим номером. Все элементы можно разделить на металлы, неметаллы и метоллоиды (полуметаллы). В этих группах элементы классифицируются еще на несколько групп: щелочные металлы, галогены, инертные газы.[4]
- Группы (столбцы) и периоды (строки) нужны для систематизации, по ним легко найти нужный вам элемент.
- Если вы ничего не знаете о нужном вам элементе, просто найдите его в таблице.
-

3
Найдите атомный номер элемента. Атомный номер обозначает число протонов в ядре атома.[5]
Атомный номер располагается над символом элемента, обычно в левом верхнем углу клетки. Он покажет вам, сколько протонов содержится в одном атоме элемента.- Например, Бор (В) обозначен в таблице под номером 5, поэтому у него 5 протонов.
-

4
Определите количество электронов. Протоны – это положительно заряженные частицы в ядре атома. Электроны представляют собой частицы, которые несут отрицательный заряд. Поэтому когда элемент находится в нейтральном состоянии, то есть его заряд будет равен нулю, число протонов и электронов будет равным.
- Например, Бор (В) обозначен в таблице под номером 5, поэтому можно смело утверждать, что у него 5 электронов и 5 протонов.
- Однако если элемент содержит отрицательный или положительный ион, то протоны и электроны не будут одинаковыми. Вам придется вычислить их. Число ионов выглядит как маленький, верхний индекс после элемента.
-

5
Найдите атомную массу элемента. Чтобы найти число нейтронов, вам сначала нужно вычислить атомную массу элемента. Атомная масса – это средняя масса атомов данного элемента, ее нужно рассчитывать. Имейте в виду, что у изотопов атомная масса отличается.[6]
. Атомная масса указана под символом элемента.- Округляйте атомную массу до ближайшего целого числа. Например, атомная масса бора = 10,811, соответственно, ее можно округлить до 11.
-

6
Вычтите из атомной массы атомный номер. Чтобы определить количество нейтронов, нужно вычесть атомный номер из атомной массы. Помните, что атомный номер – это число протонов, которое вы уже определили.[7]
- Возьмем наш пример с бором: 11 (атомная масса) – 5 (атомный номер) = 6 нейтронов.
Реклама
-

1
Определите число ионов. Ион – это атом, состоящий из положительно заряженного ядра, в котором находятся протоны и нейтроны, и отрицательно заряженных электронов. Атом несет нейтральный заряд, но заряд может быть положительным и отрицательным из-за электронов, которые атом может отдавать и принимать.[8]
Поэтому число протонов в атоме не меняется, а число электронов в ионе может меняться.- Электрон несет отрицательный заряд, поэтому если атом отдает электроны, то сам становится заряженным положительно. Когда атом принимает электроны, он становится отрицательно заряженным ионом.
- Например, у N3- заряд -3, а у Ca2+ заряд +2.
- Помните, если число ионов не указано в таблице, вам не нужно делать подобные вычисления.
-

2
Вычтите заряд из атомного номера. Если ион положительно заряжен, нужно вычесть из атомного номера заряд. Если у иона положительный заряд, значит, он отдал электроны. Чтобы подсчитать оставшееся число электронов, нужно вычесть заряд от атомного номера. Если ион заряжен положительно, значит, в нем больше протонов, чем электронов.
- Например, у Ca2+ заряд +2, поэтому можно сказать, что он отдал два электрона. Атомный номер кальция = 20, поэтому у его иона 18 электронов (20-2=18).
-

3
Если ион заряжен отрицательно, чтобы узнать число электронов, нужно добавить заряд к атомному номеру. Потому что ион стал отрицательным из-за того, что принял лишние электроны. Так что нужно просто прибавить заряд к атомному номеру, тогда вы получите число электронов. Разумеется, если ион заряжен отрицательно, то электронов в нем больше, чем протонов.
- Например, у N3- заряд -3, значит, азот получил три дополнительных электрона. Атомный номер азота 7, поэтому число электронов у азота = 10. (то есть 7+3=10).
Реклама
Об этой статье
Эту страницу просматривали 950 363 раза.
Была ли эта статья полезной?
Химический элемент
Химический элемент – совокупность атомов с одним и тем же зарядом ядра, числом протонов в ядре и электронов
в электронной оболочке. Закономерную связь химических элементов отражает периодическая таблица Д.И. Менделеева.
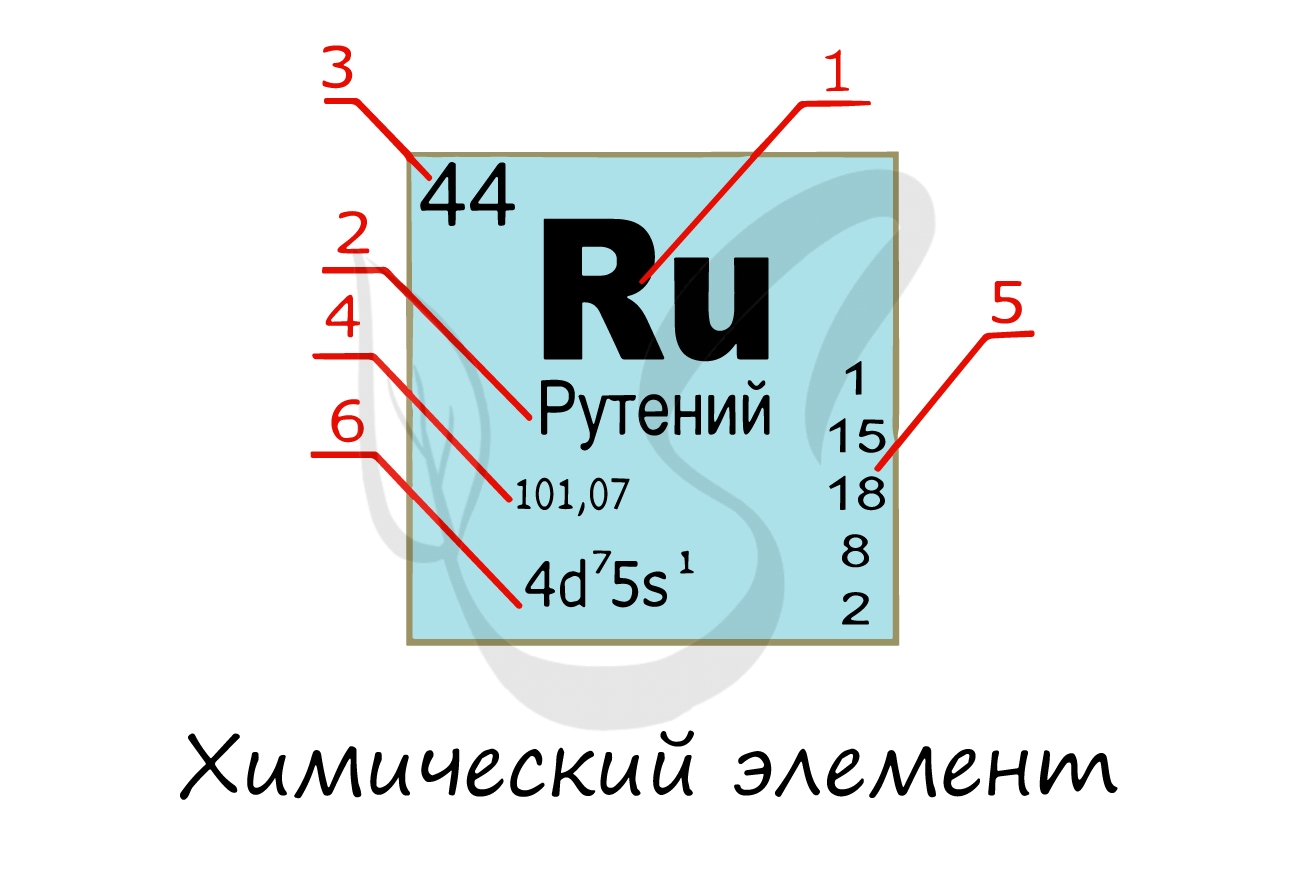
Изучая подобную карточку химического элемента, можно узнать о нем многое:
- Обозначение химического элемента
- Русское наименование
- Порядковый номер = заряд атома = число электронов = число протонов
- Атомная масса
- Распределение электронов по энергетическим уровням
- Электронная конфигурация внешнего уровня
Надо заметить, что на экзамене часто из карточки элемента скрывают распределение электронов и конфигурацию внешнего
уровня. Тем не менее, если вы успешно освоили предыдущую тему, то для вас не составит труда написать электронную
конфигурацию атома зная его порядковый номер в таблице Д.И. Менделеева (номер уж точно не тронут!))
Протоны, нейтроны и электроны
Вы уже знаете, что порядковый номер элемента в периодической таблице Д.И. Менделеева равен числу протонов, а число протонов
равно числу электронов.
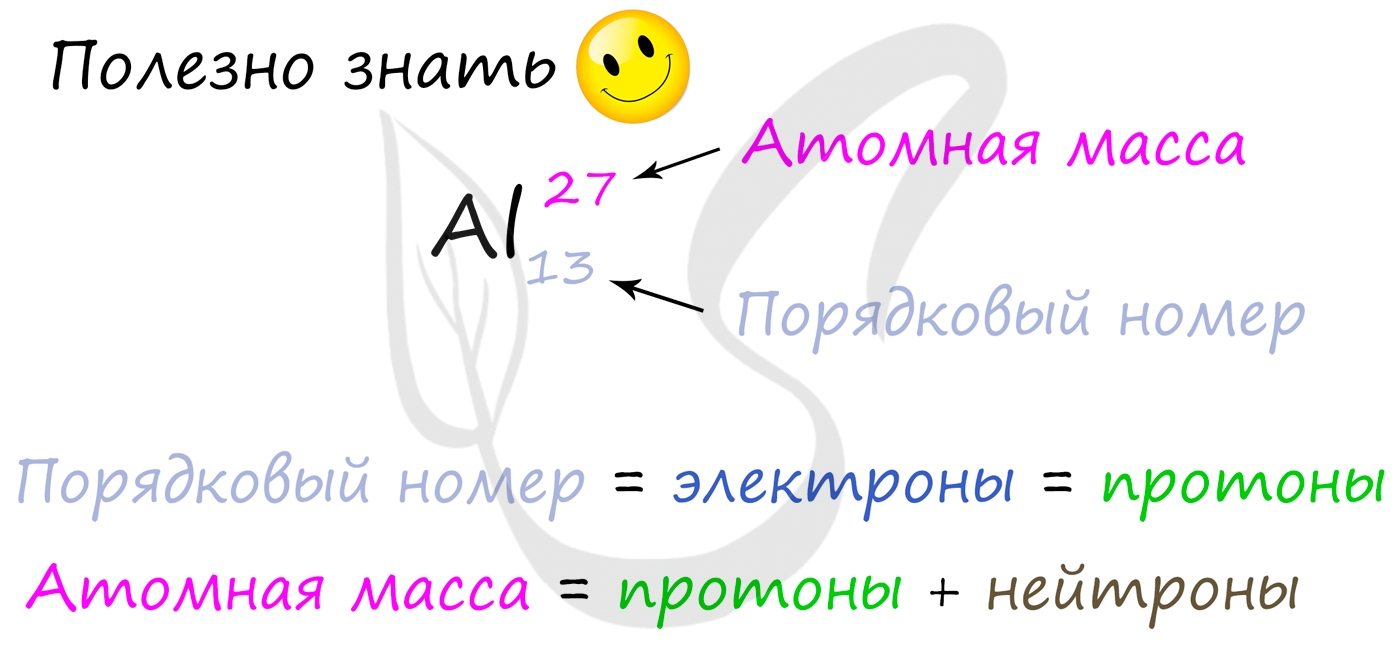
Для того чтобы найти число нейтронов в атоме алюминия, необходимо вычесть из атомной массы число протонов:
27 – 13 = 14
Получается, что в атоме алюминия 14 нейтронов. Посчитайте число нейтронов, электронов и протонов самостоятельно для атомов бериллия,
кислорода, меди. Решение вы найдете ниже.

Если вы поняли суть и научились считать протоны, нейтроны и электроны, самое время приступать к следующей теме.
Изотопы
Изотопы (греч. isos – одинаковый + topos – место) – общее название разновидностей одного и того же химического элемента,
имеющих одинаковый заряд ядра (число протонов), но разное число нейтронов.
Вероятно, вы не задумывались, но вся таблица Д.И. Менделеева и представленные в ней химические элементы – это самые распространенные
на земле изотопы.
Лучше всего объяснить, что такое изотопы наглядным примером. Широко известны три изотопа водорода: протий, дейтерий и тритий.
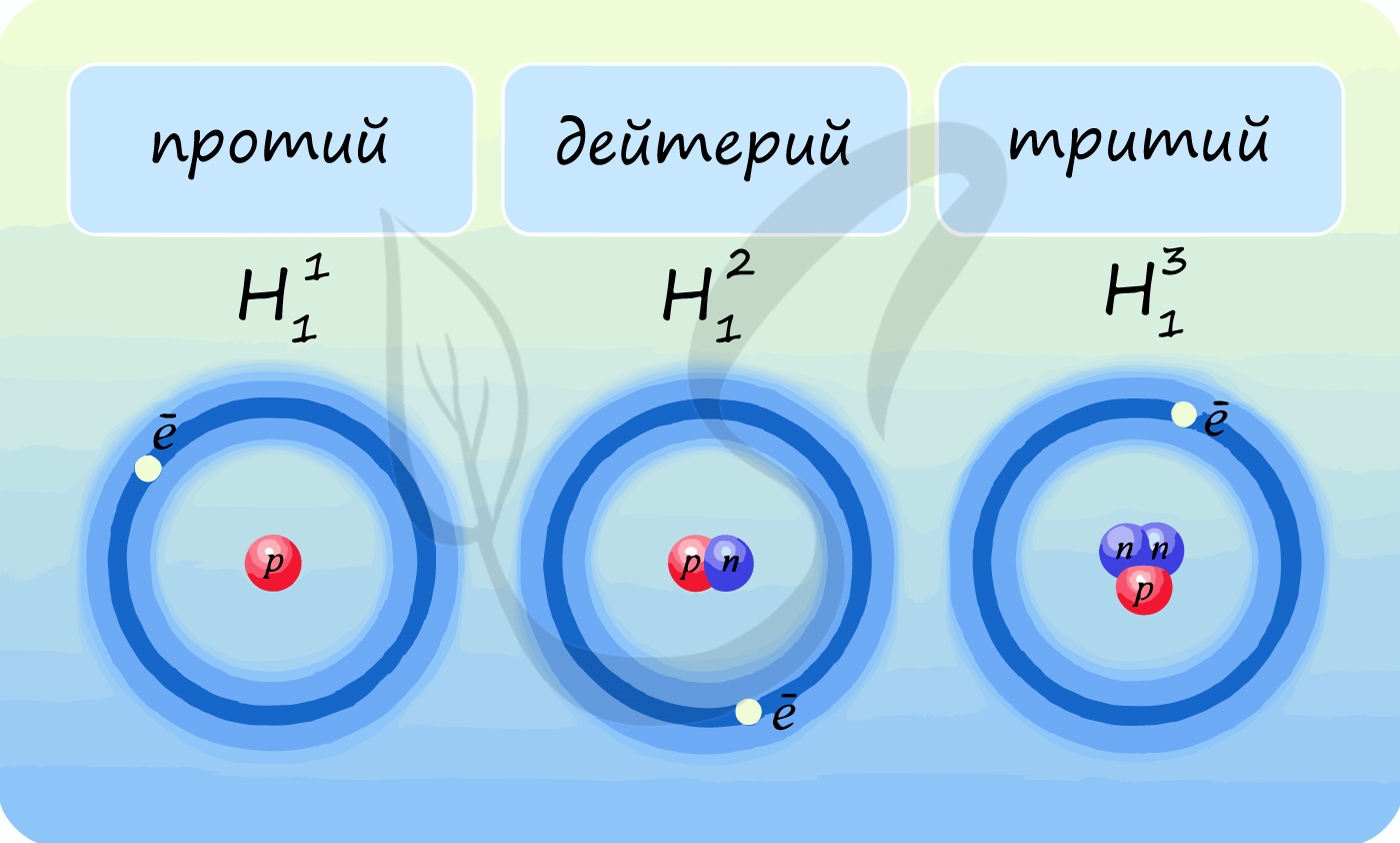
В таблице Д.И. Менделеева представлен самый распространенный из трех – протий. Он содержит 1 протон и 1 электрон, нейтроны отсутствуют. У
дейтерия 1 протон, 1 нейтрон и 1 электрон. У трития 1 протон, 2 нейтрона, 1 электрон.
Теперь очевидно, что изотопы – атомы одного и того же химического элемента, различающиеся числом нейтронов.
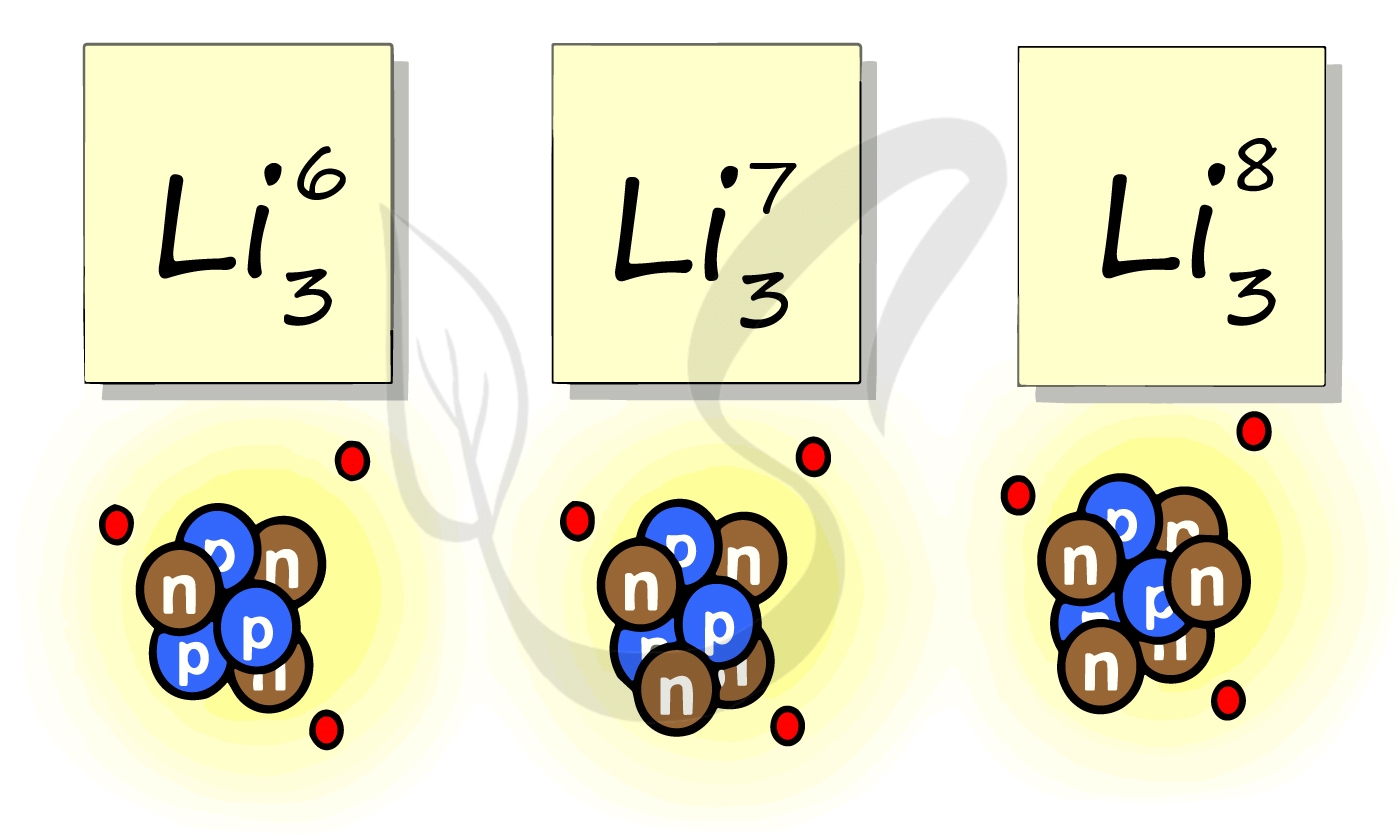
Рассмотрим пример с изотопами лития. Самостоятельно посчитайте количество нейтронов у каждого изотопа. Найдите тот, который
включен в таблицу Д.И. Менделеева.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
| Протон (p, p+) | |
|---|---|
 |
|
| Семья | фермион |
| Группа | адрон, барион, N-барион, нуклон |
| Участвует во взаимодействиях | Сильное, слабое, электромагнитное и гравитационное |
| Античастица |
антипротон  |
| Масса |
938,272 088 16(29) МэВ[1] 1,672 621 923 69(51)⋅10−27 кг[2] 1,007 276 466 621(53) а. е. м.[3] |
| Время жизни | ∞ (не менее ⋅1034 лет[4]) |
| Обнаружена | Эрнест Резерфорд в 1919 году |
| В честь кого или чего названа | от др.-греч. πρῶτος «первый» |
| Квантовые числа | |
| Электрический заряд |
+1e +1,6021766208(98)⋅10−19 Кл |
| Барионное число | 1 |
| Спин | ½ ħ |
| Магнитный момент | 2,792 847 344 63(82) ядерного магнетона[5] или 1,410 606 797 36(60)×10-26 Дж/Тл[6] |
| Внутренняя чётность | 1 |
| Изотопический спин | ½ |
| Странность | 0 |
| Очарование | 0 |
| Другие свойства | |
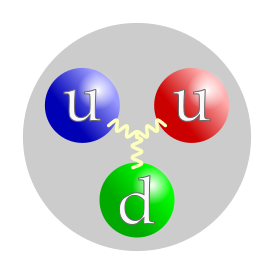
| Кварковый состав | uud |
| Схема распада | нет |
Прото́н (от др.-греч. πρῶτος «первый»[7]) — одна из трёх (вместе с нейтроном и электроном) элементарных частиц, из которых построено обычное вещество. Протоны входят в состав атомных ядер; порядковый номер химического элемента в таблице Менделеева равен количеству протонов в его ядре.
В физике протон обозначается 

Масса протона составляет 1,6726⋅10−27 кг или 938,27 МэВ, что примерно в 1836 раз больше массы электрона. Спин равен ½, поэтому протон является фермионом. Внутренняя чётность положительна.
В классификации элементарных частиц протон относится к адронам.
Он обладает способностью ко всем четырём фундаментальным взаимодействиям — сильному,
электромагнитному, слабому и гравитационному.
Электрический заряд его положителен и равен по модулю заряду электрона: e = +1,6022⋅10−19 Кл.
В отличие от, например, электрона, протон не является точечной частицей, а имеет внутреннюю структуру и конечные размеры.
Фундаментальные частицы, из которых построен протон — кварки и глюоны.
Какую именно величину считать размером протона, зависит от договорённости, но в любом случае это будет величина порядка 1 фм.
Наиболее точно измерен так называемый электрический радиус — 0,841 фм.
Протон стабилен, многочисленные эксперименты не выявили никаких свидетельств его распада.
Для объяснения этого факта было введено сохраняющееся барионное число (протону приписывается барионное число +1).
Название «протон» предложено Э. Резерфордом в 1920 году.
Свойства[править | править код]
Структура[править | править код]
Первоначально протон считался бесструктурной частицей.
Однако постепенно накапливались экспериментальные факты
(большая величина аномального магнитного момента,
результаты опытов по упругому и глубоко неупругому рассеянию), говорящие о том, что это не так.
По современным представлениям, элементарными единицами, из которых построены все сильно взаимодействующие частицы,
и протон в том числе, являются кварки.
В первоначальной версии кварковой модели считалось (и до сих пор часто говорят), что протон состоит из трёх кварков — двух верхних и одного нижнего (uud).
Хотя эта (так называемая «наивная») кварковая модель и позволяет неплохо описать некоторые свойства протона
(так, отношение магнитных моментов протона и нейтрона получается равным −3/2, что близко к экспериментальному значению −1,47[8]), на самом деле она не совсем правильна.
В действительности протон содержит, кроме этих трёх — валентных — кварков, множество глюонов и кварк-антикварковых пар (так называемых морских кварков).
Согласно данным, полученным в экспериментах по глубоко неупругому рассеянию, лишь около 40% импульса протона приходится на валентные кварки, 50% на глюоны и 10% на морские кварки[9].
Исследование коллаборации NNPDF[en] показало, что в состав протона могут временно входить очарованные кварки[10].
Кварки не могут покинуть протон из-за явления конфайнмента.
Физические характеристики[править | править код]
Масса[править | править код]
Масса протона, выраженная в разных единицах, составляет[11]:
- 938,272 088 16(29) МэВ[12];
- 1,007 276 466 621(53) а. е. м.[3];
- 1,672 621 923 69(51)⋅10−27 кг[2];
- 1836,152 673 43(11) массы электрона[13].
Магнитный момент[править | править код]
Магнитный момент протона определяется путём измерения отношения резонансной частоты прецессии магнитного момента протона
в заданном однородном магнитном поле и циклотронной частоты обращения протона по круговой орбите в том же самом
поле[14][обновить данные]. Он равен 2,792 847 344 63(82) ядерного магнетона[5]
или 1,410 606 797 36(60)×10-26 Дж/Тл[6].
Размер[править | править код]
Протон, как и любая квантовомеханическая система, не имеет чётких границ — составляющие его кварки размазаны в пространстве
в соответствии со своей волновой функцией. Поэтому нельзя однозначно сказать, что такое размер протона — это вопрос соглашения.
В качестве размера можно выбрать радиус твёрдого кора ядерных сил, электрический либо магнитный радиус
или другую характерную величину размерности длины. Однако чаще всего за размер элементарной частицы принимают
среднеквадратический радиус распределения электрического заряда (электрический радиус)[15].
Измерения электрического радиуса протона с помощью атомов обычного водорода, проводимые разными методами с 1960-х годов, привели
(CODATA-2014) к результату 0,8751 ± 0,0061 фм[16].
Первые эксперименты с атомами мюонного водорода дали для этого радиуса на 4 %
меньший результат 0,84184 ± 0,00067 фм[17][18].
Причины этого различия окончательно не выяснены. Измерения лэмбовского сдвига в атоме обычного водорода, проведённые в 2019 году,
дали значение 0,833±0,010 фм, что хотя и согласуется с данными, полученными из мюонного водорода, но по-прежнему противоречит
данным старых экспериментов[19].
Позже в 2019 году были опубликованы результаты эксперимента PRad, выполненного в Лаборатории Джефферсона группой учёных под руководством
А. Гаспаряна, в котором для определения радиуса протона использовалось рассеяние электронов.
Результат оказался равен 0,831±0,007±0.012 фм[20].
В наборе данных CODATA-2018 было зафиксировано значение радиуса, близкое к измеренному на основе спектроскопии мюонного водорода — 0,8414 ± 0.0019 фм[21], и в целом проблема зарядового радиуса протона считается решённой, однако отдельные нестыковки в измерениях всё ещё существуют и обсуждаются[22].
Слабый заряд[править | править код]
Так называемый слабый заряд протона 
определяющий его участие в слабых взаимодействиях путём обмена Z-бозоном
(аналогично тому как электрический заряд частицы определяет её участие в электромагнитных взаимодействиях путём обмена фотоном),
составляет 0,0719 ± 0,0045, согласно экспериментальным измерениям нарушения чётности при рассеянии поляризованных электронов
на протонах[23]. Измеренная величина в пределах экспериментальной погрешности согласуется с теоретическими предсказаниями
Стандартной модели (0,0708 ± 0,0003)[23].
Время жизни[править | править код]
Свободный протон стабилен, экспериментальные исследования не выявили никаких признаков его распада.
Нижнее ограничение на время жизни — 2,9⋅1029 лет независимо от канала распада[4],
1,6⋅1034 лет для распада на позитрон и нейтральный пион, 7,7⋅1033 лет для
распада на положительный мюон и нейтральный пион[24].
Поскольку протон является наиболее лёгким из барионов, стабильность протона является следствием
закона сохранения барионного числа — протон не может распасться на какие-либо более лёгкие частицы (например, позитрон и нейтрино) без нарушения этого закона. Однако многие теоретические расширения Стандартной модели предсказывают процессы (пока не наблюдавшиеся), в которых барионное число не сохраняется и, следовательно, протон может распадаться.
Взаимодействия[править | править код]
Протон участвует во всех известных взаимодействиях — сильном, электромагнитном, слабом и гравитационном.
Благодаря сильному взаимодействию, протоны и нейтроны соединяются в атомные ядра.
Благодаря электромагнитному взаимодействию, ядра и электроны образуют атомы, из которых, в свою очередь, состоят молекулы и макроскопические тела.
Слабое взаимодействие протонов приводит, например, к процессам бета-распада.
Сильное[править | править код]
При низких энергиях сильное взаимодействие протонов проявляется как ядерные силы, связывающие протоны и нейтроны в атомных ядрах[7].
В отличие, например, от электромагнитных, ядерные силы нецентральны и зависят от спинов частиц (поэтому, в частности, протон и нейтрон с параллельно направленными спинами образуют связанное состояние — дейтрон, а с антипараллельными — нет).
Как показывает эксперимент, ядерные силы обладают свойством изотопической симметрии: они не меняются при замене протонов на нейтроны и наоборот.
Поэтому в теории ядерных сил протон и нейтрон часто рассматривают как состояния одной частицы
с изотопическим спином 1/2 (нуклона), отличающиеся его проекцией (у протона +1/2, у нейтрона −1/2)[7].
Ядерные силы можно описать как обмен пионами (модель Юкавы) и в меньшей степени также другими, более тяжёлыми мезонами[7].
Эмпирически найденный потенциал ядерных сил соответствует притяжению на больших расстояниях и сильному отталкиванию на меньших (около 0,5 фм)[25].
В рамках этой модели протон состоит из тяжёлой сердцевины (кора, от англ. core),
и окружающего его облака виртуальных мезонов (на больших расстояниях — пионов, ближе к центру ро-мезонов, омега-мезонов и других).
С другой стороны, при глубоко неупругом рассеянии частиц высоких энергий на протонах дело выглядит так,
как будто рассеяние происходит на некоторых точечных частицах, находящихся внутри протона. Фейнман назвал их партонами.
Это и есть кварки[7].
При столкновениях протонов высоких энергий друг с другом или с ядрами возникает сильно разогретая ядерная материя и, возможно, кварк-глюонная плазма.
Электромагнитное[править | править код]
Электрический заряд протона равен по абсолютной величине и противоположен по знаку заряду электрона.
Тот факт, что сумма зарядов протона и электрона равна нулю, проверен с большой точностью, поскольку он означает электрическую нейтральность обычной материи[26].
Разноимённые заряды притягиваются, поэтому протон и электрон могут образовать связанное состояние — атом водорода.
Если электрон заменить отрицательно заряженным мюоном, образуется похожая на водород система, но примерно в 200 раз меньших размеров — мюонный водород.
Вообще, атомы обычного вещества обязаны своим существованием электромагнитному притяжению между протонами ядра и электронами.
Электрически заряженные элементарные частицы со спином 1/2 описываются уравнением Дирака.
Согласно этому уравнению, магнитный момент такой частицы должен быть равнен 

называется ядерным магнетоном).
Однако магнитный момент протона, как было установлено ещё в 1930-х годах, сильно отличается от предсказания теории Дирака (он в 2,79 раза больше). Уже это подсказывает, что протон не является точечной частицей, а имеет какую-то внутреннюю структуру[7][27].
Прямое доказательство было получено в опытах Хофштадтера (Нобелевская премия по физике 1961 года)[28].
При помощи упругого рассеяния электронов большой энергии на протонах (что является своего рода аналогом электронного микроскопа)
было показано, что электрический заряд протона не сосредоточен в одной точке, а распределён в области радиусом около 0,8 фм[7]. То же самое относится и к магнитному моменту.
В теории электромагнитное взаимодействие протона описывается двумя функциями — электрическим и магнитным формфакторами, которые представляют собой фурье-образ распределения плотности заряда и магнитного момента внутри протона[29]. Можно рассмотреть среднеквадратические радиусы этих распределений — это так называемые электрический и магнитный радиусы протона.
Слабое[править | править код]
Протон, как и все адроны, участвует также в слабом взаимодействии.
Известным примером этого является электронный захват — процесс, когда протон, связанный в атомном ядре,
захватывает электрон с K-, L- или M-оболочки атома, превращаясь при этом в нейтрон и испуская нейтрино:

«Дырка» в K-, L- или M-слое, образовавшаяся при электронном захвате, заполняется электроном одного из вышележащих электронных слоев атома
с излучением характеристических рентгеновских лучей, соответствующих атомному номеру 
и/или оже-электронов. Известно свыше 1000 изотопов от 7
4Be до 262
105Db,
распадающихся путём электронного захвата. При достаточно высоких доступных энергиях распада
(выше 
позитронный распад 
Ещё один слабый процесс с участием протона — обратный бета-распад, при помощи которого детектируют нейтрино:

В основе вышеприведённых процессов лежит обмен W-бозоном.
Возможен также обмен Z-бозоном, который приводит к нарушающим чётность эффектам в упругом рассеянии
(например, асимметрии упругого рассеянния продольно поляризованных электронов на неполяризованном протоне).
Роль протонов[править | править код]
В астрофизике[править | править код]
Протон — одна из часто встречающихся во Вселенной частиц. Они содержатся как в звёздах,
так и в межзвёздном пространстве.
Первые протоны образовались в эпоху адронизации — спустя 10-6—1 cек после Большого Взрыва. Сначала количество протонов и антипротонов во Вселенной было примерно одинаковым, с небольшим избытком протонов; к концу этой эпохи почти все они аннигилировали, а оставшиеся протоны существуют по сей день. В эпоху первичного нуклеосинтеза (3—20 минут спустя) часть из них вошла в состав ядер элементов тяжелее водорода (дейтерия, гелия, лития)[30].
Протоны принимают участие в термоядерных реакциях, которые являются основным источником энергии, генерируемой звёздами.
В частности, реакции pp-цикла, который является источником почти всей энергии, излучаемой Солнцем, сводятся к
соединению четырёх протонов в ядро гелия-4 с превращением двух протонов в нейтроны.
В большом количестве протоны содержатся в солнечном ветре.
Также протоны являются основным компонентом первичных космических лучей — более 90% их составляют протоны.
В космических лучах встречаются протоны с энергиями до 1020 эВ, — на много порядков больше, чем можно достичь на современных ускорителях.
В химии[править | править код]
С точки зрения химии, протон есть положительный ион водорода (точнее, его лёгкого изотопа — протия) — H+.
Он отличается от остальных химически значимых ионов тем, что не содержит ни одного электрона.
Поэтому его размер на несколько порядков меньше.
Отсюда, например, его способность проникать вглубь других молекул, образуя водородные связи[31].
Протон является мощным акцептором электронов и, соответственно, участвует в реакциях
донорно-акцепторного взаимодействия.
Протонирование — присоединение протона к молекуле — имеет важное
значение во многих химических реакциях, например, при нейтрализации, электрофильном присоединении
и электрофильном замещении, образовании ониевых соединений[32].
Источником протонов в химии являются минеральные и органические кислоты.
В водном растворе кислоты способны к диссоциации с отщеплением протона, образующего катион гидроксония.
В газовой фазе протоны получают ионизацией — отрывом электрона от атома водорода.
Потенциал ионизации невозбуждённого атома водорода составляет 13,595 эВ.
При ионизации молекулярного водорода быстрыми электронами при атмосферном давлении и комнатной температуре
первоначально образуется молекулярный ион водорода (H2+) — физическая система, состоящая из двух протонов,
удерживающихся вместе на расстоянии 1,06 Å одним электроном. Стабильность такой системы, по Полингу,
вызвана резонансом электрона между двумя протонами с «резонансной частотой»,
равной 7⋅1014 Гц[33]. При повышении температуры
до нескольких тысяч градусов состав продуктов ионизации водорода изменяется в пользу протонов.
В экспериментальной физике частиц[править | править код]
Ввиду стабильности и простоты получения (из водорода), протоны
часто используются в экспериментальной физике элементарных частиц как в качестве мишени, так и в качестве частиц пучка.
В первом случае мишенью может служить какой-нибудь богатый водородом материал, например, жидкий водород, парафин или полиэтилен[34].
Пучки протонов высокой энергии создаются на ускорителях.
Они используются для изучения всевозможных процессов рассеяния, а также для получения пучков нестабильных частиц, таких, как пионы, каоны и гипероны[7].
Большая часть открытий в физике элементарных частиц до 1980-х годов сделана на протонных синхротронах[35]. Наиболее мощный на сегодня ускоритель — Большой адронный коллайдер (англ. Large hadron collider, LHC) — разгоняет протоны до энергии 6,5 ТэВ[36].
В медицине[править | править код]
Пучки ускоренных протонов применяются для лечения онкологических заболеваний (протонная терапия)[37][38].
История открытия[править | править код]
Идея о водородоподобной частице как составной части других атомов развивалась в течение долгого времени.
В 1815 году английский химик Уильям Праут предположил, что все атомы состоят из атомов водорода (которые он назвал «protyle»),
исходя из того, что атомные массы элементов приблизительно кратны массе атома водорода (гипотеза Праута)[39].
В 1886 году Ойген Гольдштейн открыл каналовые лучи (известные также как анодные лучи) и показал, что это —
положительно заряженные частицы. Вильгельм Вин в 1898 году доказал, что самые лёгкие из них — ионы водорода (то есть протоны).
Действуя на движущиеся протоны электрическими и магнитными полями, Вин измерил отношение заряда протона
к его массе[40].
В 1917 году Резерфорд заметил, что когда альфа-частицы попадают в воздух,
на сцинтилляционных детекторах появляются вспышки от других, более лёгких (судя по длине пробега) частиц.
В чистом азоте они появлялись чаще. В 1919 году Резерфорд сделал вывод:
Исходя из полученных до сих пор результатов, трудно избежать заключения, что атомы с большой длиной пробега,
появившиеся при столкновении α-частиц с атомами азота, суть не атомы азота, а, по-видимому, атомы водорода или атомы с массой 2.
Если это действительно так, то нам следует сделать вывод, что под действием мощных сил, возникающих при столкновении
с быстрой α-частицей, атом азота расщепляется и что освободившийся при этом атом водорода является составной частью ядра азота.
Это событие часто называют открытием протона[41].
Название «протон» предложил Резерфорд в 1920 году[42].
Примечания[править | править код]
- ↑ http://physics.nist.gov/cuu/Constants/Table/allascii.txt Архивная копия от 8 декабря 2013 на Wayback Machine Fundamental Physical Constants — Complete Listing
- ↑ 1 2 2018 CODATA Recommended Values: proton mass. Дата обращения: 16 января 2009. Архивировано 30 ноября 2015 года.
- ↑ 1 2 2018 CODATA Recommended Values: proton mass in u. Дата обращения: 16 января 2009. Архивировано 30 марта 2009 года.
- ↑ 1 2 Ahmed S. et al. Constraints on Nucleon Decay via Invisible Modes from the Sudbury Neutrino Observatory (англ.) // Physical Review Letters : journal. — 2004. — Vol. 92, no. 10. — P. 102004. — doi:10.1103/PhysRevLett.92.102004. — Bibcode: 2004PhRvL..92j2004A. — arXiv:hep-ex/0310030. — PMID 15089201.
- ↑ 1 2 CODATA 2018 recommended values: proton magnetic moment to nuclear magneton ratio. Дата обращения: 12 августа 2019. Архивировано 21 октября 2019 года.
- ↑ 1 2 CODATA 2018 recommended values: proton magnetic moment. Дата обращения: 12 августа 2019. Архивировано 21 июля 2019 года.
- ↑ 1 2 3 4 5 6 7 8 Протон // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1994. — Т. 4: Пойнтинга — Робертсона — Стримеры. — 704 с. — 40 000 экз. — ISBN 5-85270-087-8.
- ↑ К. Н. Мухин. Экспериментальная ядерная физика. — М., 1993. — Т. 2. — С. 327.
- ↑ Кварки // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Советская энциклопедия, 1990. — Т. 2: Добротность — Магнитооптика. — 704 с. — 100 000 экз. — ISBN 5-85270-061-4.
- ↑ Evidence for intrinsic charm quarks in the proton | Nature
- ↑ Рекомендованные значения CODATA 2018 года, в скобках указана погрешность величины в единицах последней значимой цифры, одно стандартное отклонение
- ↑ 2018 CODATA Recommended Values: proton mass energy equivalent in MeV. Дата обращения: 16 января 2009. Архивировано 30 июня 2015 года.
- ↑ 2018 CODATA Recommended Values: proton-electron mass ratio. Дата обращения: 16 января 2009. Архивировано 22 апреля 2020 года.
- ↑ Бете, Г., Моррисон Ф. Элементарная теория ядра. —
М: ИЛ, 1956. — С. 48. - ↑ «Размер» элементарной частицы // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1994. — Т. 4: Пойнтинга — Робертсона — Стримеры. — 704 с. — 40 000 экз. — ISBN 5-85270-087-8.
- ↑ Proton rms charge radius (англ.). Fundamental Physical Constants. NIST (2014). Дата обращения: 3 апреля 2016. Архивировано 21 июля 2019 года.
- ↑ Pohl R. et al. The size of the proton (англ.) // Nature. — 2010. — 8 July (vol. 466, no. 7303). — P. 213—216. — doi:10.1038/nature09250. — Bibcode: 2010Natur.466..213P. — PMID 20613837.
- ↑ Proton Structure from the Measurement of 2S-2P Transition Frequencies of Muonic Hydrogen. Дата обращения: 26 января 2013. Архивировано 27 января 2013 года.
- ↑ N. Bezginov et al. A measurement of the atomic hydrogen Lamb shift
and the proton charge radius (англ.) // Science. — 2019. — Vol. 365. — P. 1007—1012. — doi:10.1126/science.aau7807. - ↑ New measurement yields smaller proton radius: Physicists get closer to solving the proton radius puzzle with unique new measurement of the charge radius of the proton (англ.). ScienceDaily. Дата обращения: 9 ноября 2019. Архивировано 7 ноября 2019 года.
- ↑ CODATA Value: proton rms charge radius. physics.nist.gov. Дата обращения: 2 февраля 2022. Архивировано 16 мая 2021 года.
- ↑ H. Gao, M. Vanderhaeghen. The proton charge radius (англ.) // Reviews of Modern Physics. — 2022-01-21. — Vol. 94, iss. 1. — P. 015002. — ISSN 1539-0756 0034-6861, 1539-0756. — doi:10.1103/RevModPhys.94.015002.
- ↑ 1 2 The Jefferson Lab Qweak Collaboration. Precision measurement of the weak charge of the proton (англ.) // Nature. — 2018. — May (vol. 557, no. 7704). — P. 207—211. — doi:10.1038/s41586-018-0096-0.
- ↑ K. Abe et al. (Super-Kamiokande Collaboration). Search for proton decay via
and
in 0.31 megaton
years exposure of the Super-Kamiokande water Cherenkov detector (англ.) // Physical Review D. — 2017-01-06. — Vol. 95, iss. 1. — P. 012004. — doi:10.1103/PhysRevD.95.012004. Архивировано 20 апреля 2019 года.
- ↑ Ядерные силы // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1999. — Т. 5: Стробоскопические приборы — Яркость. — 692 с. — 20 000 экз. — ISBN 5-85270-101-7.
- ↑ А. И. Ахиезер, М. П. Рекало. Электродинамика адронов. — К., 1977. — С. 12-13.
- ↑ К. Н. Мухин. Экспериментальная ядерная физика. — М., 1993. — Т. 1. — С. 85.
- ↑ Хофштадтер P. Структура ядер и нуклонов
// УФН. — 1963. — Т. 81, № 1. — С. 185—200. — ISSN. — URL: http://ufn.ru/ru/articles/1963/9/e/ Архивная копия от 17 сентября 2016 на Wayback Machine - ↑ В. Б. Берестецкий, Е. М. Лифшиц, Л. П. Питаевский. Квантовая электродинамика. — М., 1980. — С. 677-682.
- ↑ Галактики / ред.-сост. В. Г. Сурдин. — М.: Физматлит, 2013. — С. 12-13.
- ↑ Межатомное взаимодействие // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1992. — Т. 3: Магнитоплазменный — Пойнтинга теорема. — 672 с. — 48 000 экз. — ISBN 5-85270-019-3.
- ↑ Химический энциклопедический словарь / гл. редактор И.Л.Кнунянц. — М.: «Советская энциклопедия», 1983. — С. 484. — 792 с.
- ↑ Л. Паулинг. Природа химической связи. — Госхимиздат, 1947. — С. 26. — 440 с.
- ↑ К. Н. Мухин. Экспериментальная ядерная физика. — М., 1993. — Т. 2. — С. 64.
- ↑ Ускорители заряженных частиц // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1999. — Т. 5: Стробоскопические приборы — Яркость. — 692 с. — 20 000 экз. — ISBN 5-85270-101-7.
- ↑ Accelerator physics of colliders Архивная копия от 28 сентября 2020 на Wayback Machine — Particle Data Group.
- ↑ Гольдин Л. Л., Джелепов В. П., Ломанов М. Ф., Савченко О. В., Хорошков В. С. Применение тяжелых заряженных частиц высокой энергии в медицине // Успехи физических наук. — Российская академия наук, 1973. — Т. 110. — С. 77—99.
- ↑ Кокурина E. Лечебная подводная лодка // В мире науки. — 2017. — № 8/9. — С. 40—48.
- ↑ Department of Chemistry and Biochemistry UCLA Eric R. Scerri Lecturer. The Periodic Table : Its Story and Its Significance: Its Story and Its Significance (англ.). — Oxford University Press, 2006. — ISBN 978-0-19-534567-4.
- ↑ Wien, Wilhelm. Über positive Elektronen und die Existenz hoher Atomgewichte (нем.) // Annalen der Physik : magazin. — 1904. — Bd. 318, Nr. 4. — S. 669—677. — doi:10.1002/andp.18943180404. — Bibcode: 1904AnP…318..669W.
- ↑ Petrucci, R. H.; Harwood, W. S.; Herring, F. G. General Chemistry. — 8th. — Upper Saddle River, N.J. : Prentice Hall, 2002. — С. 41.
- ↑ Pais, A. Inward Bound (англ.). — Oxford University Press, 1986. — P. 296. — ISBN 0198519974.;
утверждается, что термин «протон» был впервые использован в статье Physics at the British Association (англ.) // Nature. — 1920. — Vol. 106, no. 2663. — P. 357—358. — doi:10.1038/106357a0. — Bibcode: 1920Natur.106..357..
Литература[править | править код]
- Многие известные свойства протона систематически изложены в публикации Particle Data Group. [1] (англ.)
- Широков Ю. М., Юдин Н. П. Ядерная физика. — М.: Наука, 1972. — 670 с.
- Резерфорд Э. Избр. научные труды. Кн. 2 — Строение атома и искусственное превращение элементов, пер. с англ. М., 1972.
- Жакоб М., Ландшофф П. Внутренняя структура протона // Успехи физических наук. — Российская академия наук, 1981. — Т. 133, вып. 3. — С. 505—524. — doi:10.3367/UFNr.0133.198103d.0505.
- Дрелл С. Д., Захариазен Ф. Электромагнитная структура нуклонов. — М.: ИЛ, 1962. — 175 с.
- Шелест В. П. Лекции о структуре и свойствах адронов. — М.: Атомиздат, 1976. — 248 с.
В древние времена считалось, что все состоит из земли, воды и воздуха, другого — нет. И сравнительно недавно люди смогли показать всю составляющую нашего мира. Важным вопросом было: что из себя представляет вещество?
Вещество — это материя, которая есть во всех физических телах на нашей планете.
Оно может быть простым и сложным.
Различие этих двух групп состоит в том, что простые вещества состоят из одного вида атомов, а сложные — из нескольких, поэтому впервые в ходе реакций не могут раскладываться на другие атомы, как это делают вторые.

Образцом сложного вещества можно назвать воду (H2O). Если провести химическую реакцию, то оно образует 2 элемента — водород (Н) и кислород (О). То, что получилось, — простые вещества, без последующего разложения.
В 19 веке считалось, что сами элементы не поддаются изменениям и независимы от объединения. Но такие высказывания были опровергнуты русским химиком Дмитрием Ивановичем Менделеевым, который доказал обратное, при этом указав на то, что качественная характеристика каждого элемента влияет на его атомный вес, из-за чего происходит повтор их свойств. Это умозаключение он олицетворил в своей периодической системе, назвав в честь себя.

Атом
Атом — мелкая частица, которая не разлагается в реакции на другие компоненты.
Есть что-то меньше вещества — это атомы.
Атомы можно различать по нескольким параметрам (приведем самые распространенные):
- Масса;
- Размер;
- Физические хар-ки;
- Химические хар-ки;
- Энергия;
- Вес атома.
Любой атом отличается от частицы другого элемента. Если сравнить атом водорода (Н) с атомом кислорода (О), то, очевидно, что у них будет несоответствие по многим характеристикам.
Размер атома
Если сравнить размеры атома и составляющих его частиц, то первый преобладает по своим масштабам. Ядро атома — ничто, по сравнению с ним самим. Взяв один кубический метр платины (Pt) и сплюснув его до такого состояния, где атомные расстояния просто бы исчезли, то он его кубический метр превратился бы в кубический миллиметр.
Из определения атома следует, что это маленькая частица. По форме они напоминают шар, а размер их поперечников составляет стомиллионную долю сантиметра. Чтобы это было нагляднее, рассмотрим поперечник атома водорода (Н), считающийся самым маленьким. Его размер составляет 10-8 доле сантиметра. Большим атомом является уран (U), чья величина составляет 3 х10-8 долей сантиметра.
Масштаб и вес атомов небольшие.
Вес атома
Чтобы посчитать вес какого-либо элемента, принято использовать 0,0625 долю кислорода (О), которая показывает насколько значение этого элемента больше. Если обратиться к таблице Менделеева, то можно увидеть под номерами всех элементов цифру, обозначающую атомный вес. Например, у водорода (Н) он составляет 1,008 (значение округляется, поэтому 1),а у радия — 226,025 (или же 226).Тут можно проследить разницу веса.
На заметку: при работе с периодической таблицей учтите, что если у вещества номер выше, тем вес атома будет больше.
Чаще всего у многих их вес будет дробный. Это объясняется тем, что они вмещают определенное количество частиц со своим весом, но признаки у всех абсолютно идентичны. Но такое не только у атомов. То же самое есть и самих элементов. Их называют изотопами.
Изотопы — химические элементы, занимающие один порядковый номер, но разную массу ядер.
Изотопы есть практически у каждого элемента (у кальция (Са) их целых четыре), при этом, чаще всего, их выводят искусственным путем.

Элементарные частицы
Протоны, нейтроны
Протоны — положительно заряженные части ядра. Заряд равен заряду электрона. Вес составляет 0,0625 грамм.
Нейтроны — нейтральная часть ядра. Чтобы узнать их значение, нужно из атомного веса элемента вычесть значение протонов (= электронов).
Поскольку электроны отделены от своих “напарников”, кружась вокруг них, стоит уделить им отдельное внимание.
Электроны
Электроны — частицы, у которых самый маленький отрицательный электрический заряд.
До настоящего времени считалось, что атомы, разложенные из элементов, являются конечным продуктом. На сегодняшний день эта мысль была развеяна учеными, которые доказали, что даже эти разложенные атомы содержат в себе крохотные молекулы.
Обратимся к одной из гипотез, объясняющую вещественную структуру. Там говорится, что элементный атом — некая совокупность, где есть центр, вокруг которого происходит вращение других крупинок.
Начнем с рассмотрения окраин центра, а именно с электронных уровней и электронов.
Как и говорилось ранее, значение электронов такое же, как и у протонов.
Их можно сравнить с шаром , а диаметр 40-13 сантиметров (что доказывает свою мизерность по сравнению с обычными атомами).
Электроны способны находиться в бездействии. Их масса при этом составляет 91-27 грамм. Это подчеркивает скудность инертных свойств, благодаря которым электроны способны быстро вращаться вокруг свой оси.
Масса электрона зависит от его скорости. Поговорив про массу “покоя”, которая есть у всех тел на Земле, нужно посмотреть и на массу “скорости”. Когда электрон занимается перемещением, то он образовывает электромагнитное поле. Оно играет большую роль, ибо именно из-за проявления ее инертных свойств набирается масса и энергия, передавая это все частицам. Сделаем вывод, что ускоренный динамизм этой частицы, приводит к набору его веса.
Но перемещение электронов не происходит ровно. Научно доказано, что эти частицы двигаются волнообразно из-за интерференции и дифракции.
Интерференция электронов — слияние нескольких волн электронов.
Дифракция электронов — волновое обтекание области места, через которое проходит ток.
Помимо того, что электроны двигаются волнами, так еще они крутят вокруг самих себя. Крутящееся и волновое движение говорит о нем (электроне) как о некоем магните.
Все три вида элементарных частиц фигурируют в постоянном обменивающемся контакте. Между электроном и протоном возникает связь, заставляющая их содействовать, поскольку их заряды противоположны, а вот две одинаковые частицы (например, два электрона) отталкиваются, т.к. заряды одинаковы (так же и у протона).
Нахождение частиц у элемента
Найти у какого-либо элемента эти частицы несложно. Разберем это на примере алюминия (Al).

Его порядковый номер — 13, соответственно, это есть ядро. Атомная масса алюминия составляет 26,98154 (значение округляется, поэтому 27). Протоны равны массе заряда (р=13), так же и электроны (е=13). Чтобы узнать значение нейтронов, нужно из атомной массы вычесть значение заряда ядра (n=27-13=14).
Взаимосвязь частиц
Каждая частица имеет свое электрическое поле, через которое оно “соприкасается” с остальными. Такие поля можно обозначить определенной материей, в которой, помимо этих частиц, есть и другие, наполняющие эту материю — фотоны.
Фотон — частица, не имеющая массы. Является переносчиком электромагнитного “общения”.

Все они имеют конкретный запас энергии. Именно через фотоны происходит коммуникация частиц. В такой связи происходит “бартер” фотонами, что служит для хорошей энергетической силы, то есть взаимосвязи частиц.
И в самом ядре происходит “общение” протона и нейтрона, но здесь уже нет электрического поля, поскольку нейтрон его не образовывает. Здесь все проходит при помощи особого поля, исходящего от ядра.
Ядерное поле — вид материи, который состоит из протонов, нейтронов и мезонов.
Мезон — частица, которая способствует взаимодействию протонов и нейтронов, а также влияет на то, чтобы эти частицы оставались в ядре.
Благодаря мезонам, протоны и нейтроны способны внутри своего ядра передавать определенную информацию путем ядерной силы. Ее работа в ядре происходит на определенной дистанции (приблизительно сантиметров).
Ядерная сила — сила влияния протона и нейтрона друг на друга.
Ядерные силы, происходящие внутри ядра, способны делать из протонов нейтроны и наоборот при помощи мезонов.
Можно сказать, что ядерные силы намного мощнее электрических, но вместе они не дают протонам выйти за границы ядра. Несмотря на то, что частицы сопротивляются, объединение двойной силы подавляет их, при этом создавая крепкое ядро. Из-за них и зависит его прочность.
Все три частицы называются элементарными, потому что их невозможно разложить на другие упрощенные элементы, но они могут становиться и образовываться друг из друга.
Химическое строение атомов
Работа электрона
Структура водорода (Н) заслуживает внимания. Это единственный элемент, который содержит в себе две частицы — один протон, находящийся в ядре, и один электрон, вращающийся вокруг него. Но даже тут есть нюанс: у электрона нет определенного барьера, отгораживающего его от окружающей среды.
Путь электрона вокруг ядра достаточно пластичен и поддается изменениям (причиной может стать увеличение массы электрона). А поскольку в ядре и на оболочке противоположно заряженные частицы, то они имеют свойство присоединяться. Но есть один момент: когда отрицательно заряженная частица облетает ядро, то образовывается центробежная сила, которая пытается максимально отдалить частицу. Все эти моменты создают спорную ситуацию.
Самое важное, чтобы была стабильность, тогда электрон будет спокойно находиться на своем месте. Поскольку вес орбитальной частицы небольшой, то для стабилизации ему придется летать возле ядра намного быстрее (примерно 60 15 облетов).
Получается, что электрон водорода (Н) находится неподалеку от протона, сохраняя минимум своей энергии. Но если какая-либо частица вторгнется в данную схему, и водород (Н) отдалится от ядра, то его энергия станет больше, но не надолго. Дело в том, что электрон все равно будет пытаться вернуться на место, приближенное к ядру. Электрон таким действием (переходом на другую орбиту) предоставил определенную часть своей энергии — лучистой энергии.
Если электрону дадут энергию, то он перейдет на другое место (чем больше энергии, тем дальше от протона). При этом, когда он будет возвращаться к ядру, то будет происходить активная выработка электромагнитной энергии с последующем излучением.
Когда ученые наблюдали за такими переходами этой частицы, они сделали вывод, что как и в любом элементе, так и в водороде (Н) электрон может совершать отойти только на конкретный круг, опираясь на полученное извне питание.Слои, на которых электрон способен перемещаться, называют дозволенными.
Работа протона и нейтрона в ядре
Как говорилось ранее, протон и электрон водорода (Н) — разноименные и аналогичные по значениям, поэтому их совместный заряд составляет — ноль. Из этого выходит, что водород (в обычном его состоянии) — нейтральная частица.
Такой вывод относится ко всем элементам из таблицы Менделеева. Все их атомы в нормальном состоянии нейтральны из-за равновесия разных зарядов.
Вернемся к ядру водорода (Н). Известно, что в нем находится только один протон. Обратимся к массе ядра.
Масса ядра — общее число протонов и нейтронов внутри ядра. Ее можно найти у всех элементов периодической таблицы.
Согласно этому, масса ядра водорода тоже будет составлять один (так как есть 1 протон и полностью отсутствуют нейтроны).
Что говорилось выше, относилось к природному водороду (Н), равному единице. Но существует еще и тяжелый водород (Н) — он же изотоп дейтерий (2H, имеет название тяжелого водорода). Масса равна двум. Если в ядре простого водорода (Н) всего лишь один протон, то у дейтерия — дейтоны.
Дейтон — объединение протона и нейтрона в ядре.
Водород и его изотопы
В природе обычный водород (Н) может вмещать в себя дейтерий, но в очень маленьком количестве (на 6 000 атомов Н один 2H). Но есть еще более тяжелый изотоп водорода (Н) — тритий (³Н, сверхтяжелый водород). В его ядре уже не одна, и не две частицы, а три — два нейтрона и один протон, между которыми есть ядерная сила. Масса трития составляет три. Получается, что он в целых три раза превосходит самый легкий водород.

Несмотря на то, что вес водорода и его изотопов различается, их объединяют некоторые общие свойства. Например, если самый простой водород (Н) вступит в связь с кислородом (О), то получится вода (Н2О). То же самое происходит и в цепи дейтерия ( 2H) и кислорода (О). У этого изотопа тоже на выходе получается вода, но тяжелая, которая пользуется спросом в производстве атомной энергии.
Читайте про свойства магнитного поля.
Из примера можно сделать вывод, главную роль в химических свойствах играет электронная оболочка и ее устройство, а не массу ядра. Водород и его изотопы несут в себе разную массу, но общее у них — это электроны возле ядра, которые и сохраняют идентичные свойства.
Водород (Н) взял первое место в менделеевской таблице. Такое решение было неслучайным. Как мы знаем, порядковый номер напрямую зависит от числа заряда ядра. То же самое и у водорода (Н) (номер в таблице — один = заряд ядра — один). Если правильно сказать, то: всякое вещество, занимающее место в периодической таблице Менделеева, имеет свой порядковый номер, соотносящийся заряду ядра и числу электронов на его оболочках.
Из всего сказанного получается, что водород (Н), занимающий первое место, имеет заряд ядра — +1 и один электрон на орбите.
Гелий и его изотопы
На втором месте в таблице стоит гелий (Не). Как и говорилось ранее про все элементы, его номер и заряд ядра однозначны, поэтому второй будет равен +2 (внутри ядра два протона), а оболочка будет содержать два электрона.
Как и все составляющие таблицы, гелий (Не) имеет изотопы. Их целых девять, но самыми стабильными из них считаются легкий и тяжелый, поэтому ими пользуются чаще. Рассмотрим первый.
Легкий гелий (³Не, еще имеет название гелион). Масса его ядра составляет 3, состоит из двух протонов, одного нейтрона и трех электронов на оболочке. Считается, что содержание гелиона в природном гелии 1/1 000 000 тяжелого гелия. Выводится искусственным путем.
Тяжелый гелий (⁴Не). Считается самым востребованным из всех изотопов гелия (Не). Ядро содержит два протона и два нейтрона, а на орбитах расположены четыре электрона.Образовывает около 99% гелия на нашей планете. Есть забавный факт про это вещество: если охладить его (-271 ºС) и поместить в открытую емкость, то этот изотоп вытечет из нее.
Затруднение состава атома в элементе обусловлено возрастанием объема элементарных частиц: протонов и нейтронов в ядре и электронов на оболочке. При помощи таблицы Менделеева можно узнать все эти необходимые данные об элементе (а именно про частицы).
В науке доказано, что легкие элементы имеют большое преимущество: их ядра, содержащие одинаковое количество протонов и нейтронов, считаются самыми крепкими, поскольку ядерная сила превышена, чем у остальных. Рассмотрим тяжелый гелий (⁴Не). В его составе располагаются два протона и два нейтрона, соответственно, у него неплохая прочность, точно так же, как и возникающая сила ядра.
Такие тяжелые вещества содержат разное количество частиц (протонов, нейтронов и электронов), из-за чего в ядре контакт между ними теряется, чего не происходит в легких. В тяжелых элементах возможно расщепить их ядра при разрыве атомных бомб.
Радиоактивные элементы
У тяжелых элементов есть и подразделение радиоактивных. Они отличаются тем, что их ядра настолько непрочны, что они способны самостоятельно расщепляться на отдельные частицы. Радий (Ra) — самый известный радиоактивный химический элемент. Его порядковый номер — 88. Масса атома равна 226 (если быть точнее, то 226,025).
Состав протонов в ядре — 88, а нейтронов — 138. Все они занимаются распадом, где позже они трансформируются в атомы радона (Rn, радиоактивный газ, номер в периодической таблице — 86). Все происходит точно так же: атомы радона (Rn) занимаются распадом, после чего тоже преобразовываясь в другие элементы.
Электронные оболочки
Электронные оболочки — это тоже важная часть, без которой представление какого-то химического элемента просто не было бы. Как было рассмотрено ранее, электроны единственные, кто размещен за ядром, при этом крутится вокруг него, собираясь определенными группами по разным “отсекам”.
Познание с ядрами и их частицами подошло к концу, поэтому теперь стоит уделить внимание тому, что находится за пределами этой главной точки.
Нахождение электронных оболочек и его содержимого
Чтобы определить количество электронных слоев элемента, нужно обратиться к его номеру периода. Например, алюминий (Al) с порядковым номером 13, находится в третьем периоде, поэтому число его слоев равно 3.
Еще одной удивительной характеристикой оболочек является закрепленное число электронов, которые могут находиться на слое. На первой орбите могут расположиться два электрона, на втором — восемь, на третьем — 16 и т.д. (с каждым разом нужно умножать на четыре).

Завершенным считается тот слой, который достиг окончательного предела. Электроны, которые расположены дальше всего от ядра, более активны, поэтому предпочитают вступать в контакт с другими атомами (научно это можно назвать валентностью). Число электронов на внешней оболочке зависит от номера группы. Например, бор (В) имеет заряд — +5, он находится во втором периоде, поэтому количество электронных слоев равно двум. Первый слой равен двум, а второй — трем, поскольку бор (В) находится в 3 группе.
Когда электронный слой полностью заполнен, то он считается стабилизированным. Это говорит о том, что атому не требуется брать дополнительные силы (электроны) из окружающей среды или других веществ. Если взять гелий (Не), у которого два электрона, находящиеся на одной оболочке, а у неона (Ne) электронов десять, располагающиеся на двух электронных слоях(на первом — 2, на втором — 8). Из этого выходит, что и гелий, и неон полностью заполнены, поэтому они не нуждаются в посторонней помощи, так как их оболочки завершенные. Такие элементы являются инертными в химическом плане (не идут на контакт с другими элементами, чтобы “занять” или “обменяться” этими частицами).
Но таких самодостаточных элементов достаточно мало, больше всего тех, где на внешней оболочке будет не хватать электронов, поэтому такие элементы охотнее прибегают к воздействию с другими. Калий (К) имеет 19 электронов, находящихся на четырех слоях (первый — 2, второй — 8, третий — 8, четвертый — 1). Больше всего интересует последняя оболочка. Поскольку там всего лишь один электрон, который очень далеко от ядра, то последнее не в силах удержать электрон, поэтому он с легкостью может перейти к другому элементу.
Если же взять кислород (О), у которого восемь электронов и две электрические оболочки (на первом — 2, на втором — 6). Как видно, второй слой является незавершенным, до предела ему не хватает еще двух частиц. Кислород пытается сохранить недостающее число, а также найти два электрона, чтобы завершить свой последний круг. Это может произойти в реакции с другими элементами, у которых внешний слой тоже является незавершенным и достаточно отдаленным от ядра, чтобы тот, в свою очередь, не пытался что-либо удержать.
Элементы с проблемой недостатка электронов довольно энергичны в реакциях друг с другом, поскольку у них есть потребность в присоединении или отдаче нужного числа электронов.
Распределение электронов по слоям
Размещение электронов на оболочках происходит в установленном для них порядке. Если же получается, что частица изменяет свое местонахождение или число, то электронный слой просто меняется (а именно его физические и химические свойства).
Одинаковое число протонов и электронов в элементе является доказательством того, что общий заряд (электрический) равняется нулю.
Ионы
Изменение количества двух этих частиц способно привести к тому, что атом преобразуется в электрически заряженный.
Если же у атома возникает проблема с большим объемом электронов, он меняется на отрицательный ион.
Ион — заряженная молекула. Ионы бывают катионами и анионами. Есть во всех веществах.
Катион — положительный ион.
Анион — отрицательный ион.
Хлор (Cl), который вобрал в себя всего лишь один электрон, превращается отрицательным ионом (или же анионом). Такой ион будет считаться однозарядным, так как вместил в себя одну частицу. Писаться он будет уже так: Cl⁻.
Кислороду (О), чтобы стать отрицательным ионом, нужно присоединить два электрона. Он будет считаться двухзарядным. Записываться будет вот так: О⁻.
Когда атом превращается в ион, то для окружающего мира он является системой, которая электрически заряжена, что подразумевает появление определенного электрического поля, объединяющее и сам атом, и все происходящее в его зоне контроля. Это электрическое поле позволяет атому контактировать с другими такими же частицами, имеющими заряженность (ионы, электроны и т.д.).

Как и в остальных случаях, ионы, обладающие разными зарядами, притягиваются химически, что приводит к появлению новых, сложных частиц. Ими считаются молекулы.
Окисление
Степень окисления — заряд элемента, находящегося в соединении, который вычислен путем того, что в соединении ковалентная полярная связь превратилась в ионную.
Окисление — важная часть в образовании новых соединений.
Частицы в реакциях
Когда происходит химическая реакция, электроны либо объединяются, либо переходят к более отрицательному атому, чтобы стать заряженными.
Если бы вещества состояли только из ионов, то их заряды имели целые числа, которые равнялись бы количеству электронов (отданных или не отданных). Рассмотрим хлорид натрия (NaCl). Хлор (Cl) отнимает у натрия (Na) один электрон, при этом два элемента становятся ионами, но с разными зарядами. Натрий (Na) становится положительным, то есть катионом (записывается Na⁺¹), а хлор (Cl) — отрицательным, то есть анионом (записывается Cl⁻¹). Перейдем к соляной кислоте (HCl).
В этой паре хлор (Cl) считается самым отрицательным в электрическом плане, поэтому все два электрона (от водорода (Н) и от него) больше направлены к хлору (Cl), а если электрон водорода (Н) перейдет к хлору, что заряды будут полными, а не частичными как в первом случае. Правильная запись выглядит вот так: H+1CI-1.
Эти надстрочные значки и являются степенью окисления.
Правила записи степени окисления
Чтобы правильно записать степень окисления, нужно знать несколько правил:
- Степень окисления располагается над элементом справа;
- Первым делом записывается знак заряда (плюс или минус), не записывать его нельзя, это считается грубой ошибкой;
- После знака следует само значение;
- Даже если степень окисления равна +1 или -1, то она так и записывается без сокращения ( с сокращением, то есть + или -, пишутся только ионы);
- Заряд ионов записывается над ними справа;
- На первом месте в написании заряда стоит значение, а уже только потом знак.
Пример степени окисления: H+2O-2
Пример заряда иона: AL3+ii.
Вычисление степени окисления
Вычисление степени окисления проводится по некоторым пунктам, которых стоит придерживаться:
1.Есть элементы, у которых степень окисления неизменна, к ним относятся:
- щелочные металлы (степень окисления всегда +1);
- металлы из 2А группы (+2);
- алюминий (FI+3) и бор (B+3);
- фтор (F-1);
- часто кислород (О) имеет степень окисления — 2, но есть исключение у пероксидов, где у кислорода (О) -1;
- водород (Н). С неметаллами его степень равна +1, с металлами — -2.
2. Остальное в периодической таблице с плавающей степенью. Если рассмотреть хлор (Cl), то его значения нечетны: начиная от -1, заканчивая +7 (сюда входит +1, +3, +5). А вот у серы (S) все наоборот — она имеет лишь четные: от -2 до +6 (входит +2, +4).
Главное правило: если сложить все степени из соединения, то должен получиться ноль. Также, если состав какого-либо вещества из одного элемента, то его степень будет нулем.
Бывает такое, что соединение из трех составляющих. Ни в коем случае нельзя делать так, как в соединении двух элементов. Значение первого и последнего элементов известны, а значение третьего нужно считать по специальной формуле.
Пример
Возьмем Н3РО4 (фосфорная кислота).
Из правила водород (Н) будет +1, а кислород (О) — -2, осталось узнать о фосфоре (Р). Мы должны сложить все известные значения.
Здесь будем использовать уравнение.
(+1) × 3 + Х + (-2) × 4 = 0
Х = +5
Мы знаем, что сумма всех элементов должна быть нулем, поэтому приравниваем весь пример ему. Перед водородом (Н) стоит цифра 3, поэтому его степень умножаем на это число, то же самое и с кислородом (О). Фосфор (Р) у нас неизвестен, поэтому обозначаем его иксом. Дальше решаем обычным уравнением и вписываем полученное значение над ним.
Если говорить про степень окисления и валентность, то это абсолютно разные вещи. Первое имеет отрицательное или нулевое значения, а второе только положительное.
Ключевые мометы
Эта тема переплела два ответвления — физику и химию, показывая всю многогранность нашей природы и взаимосвязь этих наук. Как мы поняли, некоторые моменты до сих пор непонятны нам, но ученые не останавливаются на достигнутом, продвигаясь дальше. Данный предмет обсуждения, находящийся в этой работе — базовые понятия, написанные доступным языком.
Этот материал разбирал такие маленькие, но важные для нас моменты — атомы, которых мы не видим, хотя они влияют на все вокруг, даже на нас самих.
Чтобы лучше усвоить материал, здесь собраны ключевые моменты из текста, требующие особого внимания:
- Вещества бывают простыми и сложными;
- Атомы — это неразлагающиеся мелкие частицы;
- Чем выше порядковый номер у элемента, тем больше его атомный вес;
- Изотопы — химические элементы под одним порядковым номером, но с разной массой ядер. Есть у любого элемента;
- У атомов есть частицы (элементарные): протоны, нейтроны, электроны;
- Протоны — положительно заряженные частицы, находящиеся в ядре;
- Нейтроны — беззарядные частицы;
- Электроны — частицы, с самым маленьким отрицательным электрическим зарядом;
- Значение протона равно значению электрона;
- Чем быстрее скорость электрона, тем его масса больше;
- Движение электрона волнообразное, упорядоченное, при этом он вращается;
- Интерференция электронов — слияние нескольких волн электронов;
- Дифракция электронов — волновое обтекание области места, через которое проходит ток;
- Порядковый номер — это заряд ядра;
- У каждой частицы есть электрическое поле, позволяющее взаимодействовать с другими частицами;
- Фотон — переносчик электромагнитного “общения” частиц;
- Ядерное поле — вид материи, который состоит из протонов, нейтронов и мезонов.
- Мезон — частица, позволяющая протонам и нейтронам контактировать, а также удерживает их внутри ядра ядерной силой;
- Ядерная сила — сила влияния протона и нейтрона друг на друга;
- Ядерные силы могут из протонов нейтроны и наоборот при помощи мезонов;
- Ядерные силы мощнее электрических;
- Протон, нейтрон и электрон называются элементарными, потому что их невозможно разложить на более простые частицы, но они могут становиться друг другом и образовываться друг из друга;
- Если электрон отдалится от ядра, то он ненадолго образует энергию, но все равно вернется на свое место, тоже образовывая энергию, переходящую в излучение;
- Дозволенные слои — орбиты, на которые электрон может переходить;
- Дейтон — объединение протона и нейтрона в ядре;
- Легкие элементы считаются лучше, потому что их ядра прочнее из-за одинакового числа частиц;
- Число электронных слоев = номер периода;
- У каждой электронной оболочки есть определенное конечное число электронов, которое оно способно вместить;
- Те элементы, у которых оболочки не полностью заполнены, лучше вступают в контакт с другими элементами;
- Ион — заряженная молекула.
- Катион — положительный ион.
- Анион — отрицательный ион;
- Степень окисления — заряд элемента, который вычислен путем того, что в соединении ковалентная полярная связь превратилась в ионную;
- Есть элементы, чья степень окисления постоянна, а есть те, у кого она изменяется;
- Если сложить все степени окисления в соединении, то всё будет равно нулю.
Короткое, но познавательное видео про элементарные частицы:
Элементарные частицы: нейтроны, протоны, электроны. Действительно элементарные?
Когда речь заходит о том, из чего состоят различные окружающие нас объекты, мы сразу начинаем говорить о молекулах, затем об атомах. А из чего же состоят сами атомы? Так ли просто они устроены, как шарик, который мы видели на уроках химии и физике в школе? На самом деле, все не так уж и просто. Для простоты в самом начале скажем, что абсолютное большинство всех вещей в мире состоит из элементарных частиц. Почему не все? Дело в том, что далеко не вся Вселенная изучена человеком, поэтому мы не можем однозначно сказать, все ли состоит из частиц.
Например, свет — это волна, состоящая из элементарных частиц — фотонов, но раньше наука не могла такое сказать.
Теперь об этих самых частицах. Элементарные частицы — это такие частицы, которые человек сейчас расщепить на более маленькие не может, поэтому пока считается, что из них все и состоит. Таких частиц бывает огромное множество, но сегодня же мы будем больше говорить о наиболее популярных из них, а именно — нейтроны, протоны, электроны.
Где встречаются нейтроны, протоны, электроны?
Почему мы сказали выше, что эти три элементарные частицы считаются наиболее популярными? Все просто — из них состоит абсолютно любой атом. Если говорить об этом чуть более подробно, то атом состоит из двух частей:
- ядро атома
- электроны
В свою же очередь ядро атома включает в себя протоны и нейтроны. Таким образом, атом состоит из трех элементарных частиц, две из которых составляют ядро, а множество третьих вращается вокруг этого ядра.
Классификация элементарных частиц
Чтобы получше разобраться в том, какие бывают элементарные частицы и как они взаимодействуют друг с другом, нам нужно разделить их на группы по принципу схожести определенных свойств. Это и называется классификация. Сейчас все поймете.
Разделим по времени жизни
Делить какие-то там частицы по времени жизни звучит очень странно, ведь это неодушевленные предметы и о жизни здесь речь идти не должна. Вы будете абсолютно правы, имея такую точку зрения. Однако в данном случае имеется в виду не жизнь, как существование живого организма, а скорей пребывание в одном и том же состоянии. Если говорить проще, то не все из элементарных частиц могут сохранять свои свойства в течение большого отрезка времени, поэтому мы и решили их так разделить. Итак, разделить в данном случае можно на две группы:
- стабильные (это те частицы, которые как раз могут очень долго сохранять свойства, некоторые даже говорят бесконечно долго). Сюда относятся электроны, фотоны, протоны и другие частицы)
- нестабильные (а это те, которые через некоторый промежуток времени меняют свои свойства и переходят в другие формы). Сюда относятся все остальные виды частиц.
Разделим по тому, как они взаимодействуют
Интересно, что при довольно схожем строении, разные частицы могут взаимодействовать друг с другом совсем по-разному. Давайте посмотрим, как можно разделить элементарные частицы по такому принципу:
- составные
- бесструктурные
Действительно, частицы тоже бывают составные и фундаментальные (по сути самые простые), и от этого многое зависит. Давайте подробно разберемся с каждым из этих видов.
Составные частицы, которые по-другому еще называются адронами (вы наверняка слышали про Адронный коллайдер в Швейцарии) взаимодействуют со всеми частицами. Такое взаимодействие еще называют фундаментальным. Они в свою очередь тоже подразделяются на мезоны и барионы.
Теперь давайте поговорим о фундаментальных частицах. Здесь все гораздо более интересно, ведь таких частиц в мире открыто великое множество. Давайте для начала узнаем, на какие виды разделяются фундаментальные или же бесструктурные частицы:
- кварки
- лептоны
- калибровочные бозоны
Теперь давайте остановимся на каждом виде отдельно и поговорим о нем более подробно. А начать предлагаем с кварков.
Кварки — это такие частицы, которые находятся в составе адронов. Отдельно их встретить ученым пока не удавалось, только в составе других частиц. Для того, чтобы их изучать, ученым приходится использовать различные хитрые методы. Они подразделяются еще на шесть подтипов, но о них сегодня мы говорить не будем. Интересной особенностью кварков является то, что они, являясь фундаментальными частицами, все же участвуют в сильных взаимодействиях.
Теперь давайте перейдем к лептонам (точечным частицам). Это тоже довольно важный вид бесструктурных частиц. Они в отличие от кварков уже не участвуют в сильных взаимодействиях. Однако именно заряженные лептоны все же могут принимать участие в взаимодействии электромагнитном. Здесь так же, как и в кварках, отмечается целых шесть подтипов.
Ну а теперь последний тип с довольно странным для многих названием — калибровочные бозоны. Это тоже немаловажный тип, ведь именно он служит своего рода посредником в различных взаимодействиях между частицами. Чтобы вам было легче запомнить, приведем несколько примеров таких частиц: фотон, гравитон и глюон.
Ядро протон нейтрон электрон
Отлично, когда мы уже знаем довольно много про то, как устроены остальные элементарные частицы, давайте вернемся обратно к протону, нейтрону и электрону. Теперь самое время поговорить об устройстве ядра атома.
Начнем с того, что в ядре атома собран весь его положительный заряд, который обеспечивается протонами. Несмотря на большой заряд, размеры ядра очень малы по сравнению с электронными орбитами (орбиты, по которым вращается электрон вокруг ядра). В среднем они колеблются от 10 в минус 15 степени до 10 в минус 14 степени. Как мы помним из школьного курса химии количество протонов атома — это номер Z атома и порядковый номер элемента в таблице Менделеева. Примечательно также то, что количество протонов и электронов в атоме всегда одинаково.
Наверняка вам очень интересно, почему ядро атома, которое тоже состоит из элементарных частиц, такое плотное. Дело в том, что связь между протонами и нейтронами не является ни гравитационной, и электромагнитной, но при этом она в несколько раз сильнее, чем связь между ядром и электроном.
Число протонов нейтронов и электронов
Как мы уже поняли выше, в атоме абсолютно всегда количество протонов и электронов равно. Это обусловлено тем, что заряд должен быть нейтрален, а значит и количество положительных должно равняться количеству отрицательных частиц (отметим, что заряд протона +1, а заряд электрона -1). Также напомним, что количество протонов дает нам порядковый номер в таблице Менделеева этого атома. Теперь поговорим о нейтронах. Можно ли каким-то образом определить их количество внутри атома? Конечно можно. Это можно сделать, зная массу атома и количество протонов. Нужно просто вычесть из массы атома количество протонов и мы получим количество нейтронов (иногда нужно округлять). Для примера возьмем Медь (Cu). Ее атомная масса примерно равна 64, а номер в таблице 29, значит количество нейтронов будет равно 64 — 29 = 35. Все очень просто.
3 протона 3 нейтрона 3 электрона
Теперь для того, чтобы получше разобраться в этой теме, давайте попробуем все понять на примере другого атома. Это, как вы могли уже догадаться, атом Лития. У него 3 протона, 3 нейтрона и 3 электрона. По той формуле, которую мы уже узнали выше, тут сразу можно понять, что примерная масса атома Лития будет равна 6 (3 нейтрона + 3 протона). Также мы сходу можем сказать, что номер Лития в таблице Менделеева тоже 3 (количество протонов).

Теперь давайте посмотрим на таблицу Менделеева, представленную выше. Действительно, у Лития именно 3 номер и масса равна 6,941.
Видите, как все легко и просто. Однако особенно внимательный читатель уже давно заметил ошибку. Действительно, округлив массу Лития мы понимаем, что здесь количество нейтронов будет равно 4. Как же так получается, что у нас 3 нейтрона. Это подводит нас к следующей теме, о которой мы сейчас и поговорим.
Протон изотоп нейтрон электрон
Наверное, на одном из школьных уроков вы слышали такой термин, как изотоп. В школе это была та самая тема, после которой я полюбил естественные науки. Сейчас я не могу дать однозначный ответ, почему, просто было очень интересно. Итак, изотопы.
Что такое изотоп
Если говорить просто, то Изотопы представляют собой измененную модель обычного атома какого-то вещества. То есть возьмем любой атом какого-то вещества. У него есть фиксированное количество электронов, протонов и электронов. Однако, как мы уже заметили выше, это количество может быть и другим благодаря существованию изотопов. У изотопов такой же порядковый номер элемента в таблице Менделеева, а значит, как мы уже поняли, у них точно такое же количество протонов. Однако, есть отличия в массе элемента, а значит и в количестве нейтронов. Теперь давайте узнаем, как нам пригодится эта информация и как определить, что перед нами изотоп какого-то элемента.
Как определить, что перед нами изотоп
Наверняка самые догадливые и внимательные из вас уже догадались, что обычная формула с определением количества нейтронов с изотопами не работает от слова совсем, ведь это уже измененная модель обыкновенного элемента. Раз так, то мы можем просто попробовать подставить данные по атому в нашу формулу и понять, работает она или нет. Если нет, то перед нами изотоп. Но естественно, для удобства ученые придумали специальные обозначения для изотопов, чтобы нам, обычным людям, было удобнее с ними работать и изучать их. Как же эти обозначения работаю. А очень просто!
У изотопов после названия еще дописывается количество нуклонов в ядре (то есть количество элементарных частиц внутри ядра, сумма протонов и нейтронов). Давайте разберемся на примере очень популярного изотопа урана-235, радиоактивного урана. Обычный же уран по сути называется уран-238.
Зачем нам это знать?
Как вы уже могли понять, все многообразие элементарных частиц не ограничивается таблицей Менделеева и элементами, которые в ней представлены. У некоторых элементов бывает сразу несколько популярных изотопов, поэтому если вы хотите действительно хорошо разбираться в этой теме, то и запоминание всех популярных изотопов не будет лишним. А эта таблица вам в этом поможет:

Отлично, теперь мы уже неплохо разобрались с массой атома, таблицей Менделеева и разобрали основные типы элементарных частиц. Пришло время поговорить о более серьезных вещах. О чем же?
Радиоактивность
Для многих, кто в школе проходил эту тему лишь вскользь, это понятие выглядит очень страшным и непонятным. Кроме того, у многих на ум приходят различные катастрофы, косвенно связанные с этим понятием. Ну кто из вас сейчас не подумал о Хиросиме или о Чернобыле? Однако мы сейчас будем развеивать все эти мифы и стереотипы и хорошенько разберемся в этой далеко не легкой, но при этом очень интересной теме.

Как это работает?
Для того, чтобы разобраться в чем-либо, нужно сначала понять, с чего все начинается. В данном случае все идет от превращения атомов, а точнее от превращения их ядер. Интересно здесь то, что процесс этот самопроизвольный, то есть для того, чтобы он начался, нужно все-таки воздействовать извне, но как только превращения ядер начались, их уже не остановить! Да, далее произойдет именно то, о чем вы думаете. Ядро, с которого и начнется этот необыкновенно интересный с одной стороны и ужасно опасный с другой процесс называется материнским. Соответственно, если радиоактивный процесс затрагивает какое-то ядро помимо материнского, оно будет считаться дочерним, а 2 ядра, между которыми произошел обмен, называют генетически связанными — все как у людей.
Что такое радиоактивный распад?
Разумеется, радиоактивный распад встречается и в природе, однако происходит он крайне редко и не приносит никакого весомого вреда. А вот искусственный распад — штука очень опасная, если уметь ей управлять. Вся суть в том, что самопроизвольно меняется количество элементарных частиц. Существует несколько типов распадов и зависит этот тип от того, какие частицы будет испускать наш атом. Если это будут 2 протона и 2 нейтрона, то это положительно заряженная частица, называемая альфа-частицей. Соответственно, такой распад будет называться альфа-распадом. А вот с бета-частицами все немного посложнее.
Существует сразу 2 типа таких частиц: электроны и позитроны. Если эта частица электрон, то она обязательно образована нейтроном, распавшимся на протон и электрон. Если же эта бета-частица позитрон, то она всегда образована протоном, который распался на нейтрон и электрон. Распад, при котором из атома вылетает бета-частица — это уже бета-распад. Существует еще и менее популярный тип распада (изомерный переход или гамма-распад), при котором из атома вылетают гамма-кванты. Тут все еще сложнее, ведь такой изомерный переход никогда не бывает один. О чем я говорю? Дело в том, что гамма-распад очень часто сопровождают и другие типы распада. Это происходит в тот момент, когда частица распадается в первый раз. На этом этапе могут произойти другие виды распадов, а уж только потом процесс переходит непосредственно к гамма-распаду.
А в природе где это все можно встретить?
Как мы уже сказали выше, в природе тоже встречается радиоактивность. Если немного подумать, то оказывается, что радиоактивны по сути все вещества, у которых нет стабильных изотопов (кто еще не знает, что это, почитайте о них выше). Так вот, ученые пошли еще дальше и подошли к этому вопросу системно. В итоге они получили, что оказывается по таблице менделеева радиоактивны по своей природе вещества, у которых номер 83 или больше. Однако это если мы говорим о тех веществах, которые однозначно радиоактивны.
А ведь встречаются и немного другие. Например среди элементов с атомной массой поменьше встречаются такие, у изотопов которых очень большой период полураспада. Для примера возьмем теллур-128. У обычного теллура номер в таблице Менделеева 52, а значит он не подходит под первую группу, верно? И это неудивительно, ведь его изотоп теллур-128 так стабилен, что его период полураспада примерно в 2 раза больше, чем( 10 в степени 15 миллиардов лет). Неплохо, верно? Спешим вас успокоить, это элемент с самым большим периодом полураспада, но все-таки это очень много, ведь наша земля в миллиарды раз моложе. А для чего нужны все эти цифры? Это как-то практически применимо? Ну конечно, с помощью этих данных можно определять возраст многих минералов, горных пород и даже возраст планет в космосе! А ведь вы еще не знаете, что же такое период полураспада. Давайте разберемся с этим важнейшим понятием.
А что такое период полураспада?
Говоря о том, где можно встретить радиоактивность в природе, мы затронули такой термин, о котором еще не говорили. Что-ж, это неплохой повод, что это сделать сейчас. Так вот, период полураспада — это такое время, за которое частица распадается.

Но почему же именно ПОЛУраспад? Ну да, здесь все не так просто. Если говорить точнее, то это время, за которое она (частица) распадается с вероятностью 50 процентов. Теперь более понятно, верно?
Как вы уже могли догадаться у одной и той же частицы периоды полураспада могут отличаться в зависимости от изотопов. Однако для изотопа частицы это число постоянно.
Заключение
Как вы уже поняли, об элементарных частицах можно говорить очень много и говорить о них можно бесконечно много. Однако на этом наше небольшое вводное повествование о них предлагаем закончить. Если вам понравилась эта статья и вы хотите, чтобы мы публиковали больше материала на эту тему, то не забудьте проявить немного активности ниже. Напомним также, что на нашем сайте есть множество статей на смежные тематики, поэтому предлагаем вам с ними ознакомиться. До скорых встреч!
Download Article
Download Article
Finding the number of protons, neutrons, and electrons in a given element isn’t as hard as it sounds. Oftentimes part of your answer will be right in front of you in the periodic table! Once you know where to look, finding the number of protons, neutrons, and electrons will be a breeze.
-

1
Get a periodic table of elements. The periodic table is a chart that organizes elements by their atomic structure. It is color-coded and assigns each element a unique 1 or 2-letter abbreviation. Other elemental information includes atomic weight and atomic number.[1]
- You can find a periodic table online or in a chemistry book.
- In tests, normally, a periodic table will be provided.
-

2
Find your element on the periodic table. The table orders elements by atomic number and separates them into three main groups: metals, non-metals, and metalloids (semi-metals). Further elemental groupings include alkali metals, halogens, and noble gases.[2]
- Using the group (columns) or period (rows) can make the element easier to locate on the table.
- You can also search the table for the symbol of the element if you don’t know any other properties.
Advertisement
-

3
Locate the element’s atomic number. The atomic number is located above the element symbol, in the upper left-hand corner of the square. The atomic number will tell you how many protons make up a single atom of an element.[3]
- For example, boron (B) has an atomic number of 5, therefore it has 5 protons.
-

4
Determine the number of electrons. Protons are particles in the nucleus of an atom that have a positive charge equal to +1. Electrons are particles that have a negative charge equal to -1. Therefore, an element in a neutral state will have the same number of protons and electrons.[4]
- For example, boron (B) has an atomic number of 5, therefore it has 5 protons and 5 electrons.
- However, if the element includes a negative or positive ion, then the protons and electrons will not be the same. You will have to calculate them. The ion number will appear as a small superscript after the element.
-

5
Look for the atomic mass of the element. To find the number of neutrons, you will first need to find the atomic mass. An element’s atomic mass (also known as the atomic weight) is the weighted average mass of atoms of an element.[5]
The atomic mass can be found underneath the symbol for the element.- Make sure that you round the atomic mass to the nearest whole number. For example, the atomic mass of boron is 10.811, but you can just round the atomic mass up to 11.
-

6
Subtract the atomic number from the atomic mass. To find the number of neutrons, you will need to subtract the atomic number from the atomic mass. Remember that the atomic number is the same as the number of protons, which you have already identified.[6]
- For our boron example, 11 (atomic mass) – 5 (atomic number) = 6 neutrons
Advertisement
-

1
Identify the net charge. The net charge of an ion will appear as a small superscript number following the element. An ion is an atom that has a positive or negative charge due to the addition or removal of electrons.[7]
Although the number of protons in the atom remains the same, the number of electrons is altered in an ion.- Because an electron has a negative charge, when you remove electrons, the ion becomes positive. When you add more electrons, the ion becomes negative.
- For example, N3- has a -3 charge while Ca2+ has a +2 charge.
- Keep in mind that you do not have to do this calculation if there is no superscripted ion number following the element.
-

2
Subtract the charge from the atomic number. When an ion has a positive charge, the atom has lost electrons. To calculate the remaining number of electrons, you subtract the amount of extra charge from the atomic number. In the case of a positive ion, there are more protons than electrons.[8]
- For example, Ca2+ has a +2 charge so it has lost 2 electrons from the neutral state. Calcium’s atomic number is 20, therefore the ion has 18 electrons.
-

3
Add the charge to the atomic number for negative ions. When an ion has a negative charge, the atom has gained electrons. To calculate the total number of present electrons, you simply add the amount of extra charge to the atomic number. In the case of a negative ion, there are fewer protons than electrons.[9]
- For example, N3- has a -3 charge; therefore, it has gained 3 electrons compared to the neutral state. Nitrogen’s atomic number is 7, therefore this ion has 10 electrons.
Advertisement
Add New Question
-
Question
How do I find the number of protons when an atom has a -ve or +ve charge?

Meredith Juncker is a PhD candidate in Biochemistry and Molecular Biology at Louisiana State University Health Sciences Center. Her studies are focused on proteins and neurodegenerative diseases.

Scientific Researcher
Expert Answer
The number of protons will never change. Atoms with negative or positive charges just indicate a gain or loss of electrons.
-
Question
How can I find the electron and proton numbers of actinium?

Meredith Juncker is a PhD candidate in Biochemistry and Molecular Biology at Louisiana State University Health Sciences Center. Her studies are focused on proteins and neurodegenerative diseases.

Scientific Researcher
Expert Answer
You will find actinium in group 3, period 7 of the periodic table. The atomic number of actinium is 89, which means there are 89 protons. Because there is no net charge, we know that # protons = # electrons, so there are 89 electrons as well.
-
Question
How do I find the number of protons are in a nucleus when given the atomic mass?

All the protons are present in the nucleus, or centre of an atom. You need the atomic number to find the amount of protons and/or electrons, unless you have the amount of neutrons and the atomic mass, in which case you can simply subtract the amount of neutrons from the atomic mass, leaving the amount of protons in the atom. The atomic number (number at the top) is the amount of protons and the amount of electrons. So if an element has an atomic number of 5, you know that it has 5 protons and 5 electrons. The atomic mass (number at the bottom) is the amount of protons and neutrons added together. Whichever you know, you subtract from the atomic mass.
See more answers
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
Video
About This Article
Article SummaryX
The easiest way to find the number of protons, neutrons, and electrons for
an element is to look at the element’s atomic number on the periodic table.
That number is equal to the number of protons. The number of protons is
equal to the number of electrons, unless there’s an ion superscript listed
after the element. To find the number of neutrons, subtract the element’s
atomic number from its atomic mass (the number listed underneath the
element).
Did this summary help you?
Thanks to all authors for creating a page that has been read 2,837,860 times.
