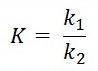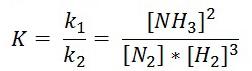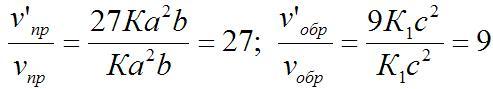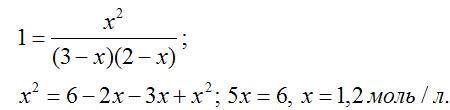Скорость
химической реакции (v)
характеризуется изменением концентрации
реагирующих веществ (моль/л или
моль/см3) в единицу времени (сек.,
мин., ч.).
Для
гомогенной (однородной) системы
скорость химической реакции измеряется
количеством веществ, вступивших в
реакцию или образовавшихся в результате
реакции за единицу времени в единице
объема системы. Для гетерогенной
системы скорость химической реакции
измеряется количеством веществ,
вступивших в реакцию или образовавшихся
в результате реакции за единицу времени
на единице поверхности раздела фаз.
Факторы,
влияющие на скорость химической
реакции
1)
Природа реагирующих веществ (характер
связи в молекулах реагентов);
2)
Концентрация реагентов;
3)
Температура;
4)
Катализатор;
5)
Давление (для газов);
6)
Излучение (ИК-, УФ-, рентгеновское,
радиоактивное и др.);
7)
Площадь поверхности раздела фаз (для
гетерогенных реакций).
Влияние
концентрации реагирующих веществ
выражается законом действия масс: при
постоянной температуре скорость
химической реакции, протекающей в
однородной среде, пропорциональна
произведению концентраций реагирующих
веществ, возведенных в степени их
стехиометрических коэффициентов.
Например,
для обратимой гомогенной реакции,
выражающейся уравнением aA +
bB ↔ cC + dD, в соответствии
с законом действия масс, можно записать
выражение скорости прямой и обратной
реакций:
где
k1 и k2 – константы скоростей
прямой и обратной реакций.
Физический
смысл константы скорости заключается
в том, что она показывает численное
значение скорости химической реакции,
с которой реагируют вещества при их
концентрации (или произведении
концентраций), равной единице. Константа
скорости реакции зависит от природы
реагентов, температуры, наличия
катализатора, но не зависит от
концентрации реагентов.
Химическое
равновесие
Химические
реакции по признаку обратимости
делятся на необратимые и обратимые.
К необратимым реакциям относятся
такие реакции, которые протекают до
тех пор, пока один из реагентов полностью
не израсходуются. Признаками необратимых
реакций, протекающих в растворах,
являются: а) выпадение осадка, б)
образование газа, в) образование
слабого электролита.
Обратимыми
реакциями называются такие реакции,
которые протекают одновременно в двух
взаимно противоположных направлениях.
Для подобных реакций вместо знака
равенства пользуются противоположно
направленными стрелками (↔).
С
течением времени скорость любой
реакции, измеряется по убывающим
концентрациям исходных веществ, будет
уменьшаться, так как по мере взаимодействия
веществ их концентрации уменьшаются
(скорость прямой реакции). Если реакция
является обратимой, то по мере увеличения
концентрации продуктов ее скорость
будет возрастать (скорость обратной
реакции). Как только скорости прямой
и обратной реакций становятся
одинаковыми, в системе устанавливается
химическое равновесие и дальнейшее
изменение концентраций всех веществ,
находящихся в системе, прекращается.
Количественной
характеристикой состояния равновесия
является константа химического
равновесия К, которая определяется
отношением констант скоростей прямой
и обратной реакцией
В
подавляющем большинстве случаев
константы скоростей прямой и обратной
реакций не равны. Константа равновесия
– постоянная при данной температуре
величина и определяет соотношение
между равновесными концентрациями
продуктов реакции и исходных веществ,
возведенных в степени их стехиометрических
коэффициентов.
Например,
для процесса N2 +
3H2 ↔ 2NH3
Квадратной
скобкой обозначена концентрация
каждого вещества в момент равновесия,
так называемая равновесная
концентрация.
Константа
равновесия зависит от природы
реагирующих веществ и температуры.
Катализатор не влияет на состояние
равновесия. Присутствие катализатора
в системе лишь изменяет время его
достижения. В состоянии равновесия
система может находиться до тех пор,
пока не изменится хотя бы одно из
внешних воздействий: температура,
концентрация одного из реагентов,
давление (для газов). Изменения,
происходящие в равновесной системе
в результате внешних воздействий,
определяются принципом подвижного
равновесия (принцип Ле-Шателье): внешнее
воздействие на систему, находящуюся
в состоянии равновесия, приводит к
смещению этого равновесия в направлении,
при котором эффект произведенного
воздействия ослабляется.
На
смещение равновесия оказывает влияние:
1)
изменение температуры:
эндотермический процесс ускоряется
в большей степени при повышении
температуры и, наоборот, при понижении
температуры ускоряется экзотермический
процесс;
2)
изменение давления
(для реакций, протекающих в газовой
фазе): при повышении давления равновесие
реакции смещается в направлении
образования веществ, занимающих
меньший объем, и, наоборот, понижение
давления способствует процессу,
сопровождающемуся увеличением объема.
Если реакция протекает без изменения
объема, то изменение давления в системе
не оказывает влияние на
химическое равновесие.
3)
изменение концентрации:
увеличение концентрации исходных
веществ приводит к увеличению скорости
прямой реакции, при этом протекающий
в системе процесс завершится, когда
скорости прямой и обратной реакций
станут равны и установится новое
равновесие. Уменьшение концентрации
одного из продуктов реакции (вывод из
системы) приводит к смещению равновесия
в сторону его образования.
Критерием
принципиальной осуществимости реакций
является неравенство ΔGp,
T
< 0. Но это неравенство не
является еще полной гарантией
фактического течения процесса в данных
условиях, не является достаточным для
оценки кинетических возможностей
реакции. Так, ΔGо298,
H2O(г) = – 228,59 кДж/моль, а ΔGо298,
AlI3(к) = -313;8 кДж/моль и,
следовательно, при Т = 298 К и р
= 1,013 • 105 Па возможны реакции,
идущие по уравнениям:
Н2(г)
+ ½О2(г) = Н2О (1)
2Аl(к)
+ 3l2(к) = 2Аll3(к)
(2)
Однако
эти реакции при стандартных условиях
идут только в присутствии катализатора
(платины для первой и воды для второй).
Катализатор как бы снимает кинетический
“тормоз”, и тогда проявляется
термодинамическая природа вещества,
Скорость химических реакций зависит
от многих факторов, основные из которых
– концентрация (давление) реагентов,
температура и действие катализатора.
Эти же факторы определяют и достижение
равновесия в реагирующей системе.
Пример
1. Во сколько раз изменится скорость
прямой и обратной реакции в системе:
2SO2(г)
+ O2(г) = 2SO3(г)
если
объем газовой смеси уменьшить в три
раза? В какую сторону сместится
равновесие системы?
Решение.
Обозначим концентрации реагирующих
веществ: [SO2]= a,
[О2] = b,
[SO3] = с. Согласно
закону действия масс скорости v
прямой и обратной реакции до
изменения объема:
vпр
= Ка2b;
vобр = К1с2.
После
уменьшения объема гомогенной системы
в три раза концентрация каждого из
реагирующих веществ увеличится в три
раза: [SO2] = 3а,
[О2] = 3b;
[SO3] = 3с.
При новых концентрациях скорости v’
прямой и обратной реакции:
v’пр
= К(3а)2(3b)
= 27Ка2b;
v’обр
= К1(3с)2 = 9К1с2.
Отсюда:
Следовательно,
скорость прямой реакции увеличилась
в 27 раз, а обратной – только в девять
раз. Равновесие системы сместилось в
сторону образования SO3.
Пример
2. Вычислите, во сколько раз
увеличится скорость реакции, протекающей
в газовой фазе, при повышении температуры
от 30 до 70оС, если температурный
коэффициент реакции равен 2.
Решение.
Зависимость скорости химической
реакции от температуры определяется
эмпирическим правилом Вант-Гоффа по
формуле:
Следовательно,
скорость реакции νТ2
при температуре 70оС больше
скорости реакции νТ1
при температуре 30оС в 16 раз.
Пример
3. Константа равновесия гомогенной
системы:
СО(г)
+ Н2О(г) = СО2(г) + Н2(г)
при
850оС равна 1. Вычислите концентрации
всех веществ при равновесии, если
исходные концентрации: [СО]исх
=3 моль/л, [Н2О]исх = 2 моль/л.
Решение.
При равновесии скорости прямой и
обратной реакций равны, а отношение
констант этих скоростей постоянно и
называется константой равновесия
данной системы:
vпрК1
[СО][Н2О]; vобр
= К2[СО2][Н2];
В
условии задачи даны исходные
концентрации, тогда как в выражение
Кр входят только равновесные
концентрации всех веществ системы.
Предположим, что к моменту равновесия
концентрации [СО2]р = х
моль/л. Согласно уравнению системы
число молей образовавшегося водорода
при этом будет также х моль/л. По
столько же молей (х моль/л) СО и
Н2О расходуется для образования
по х молей СО2 и Н2.
Следовательно, равновесные концентрации
всех четырех веществ:
[СО2]р
= [Н2]р = х моль/л; [СО]р
= (3 – х) моль/л;
[Н2О]р
= (2 – х) моль/л.
Зная
константу равновесия, находим значение
х, а затем исходные концентрации
всех веществ:
Таким
образом, искомые равновесные
концентрации:
[СО2]р
= 1,2 моль/л;
[Н2]р=
1,2 моль/л;
[СО]р
= 3 – 1,2 = 1,8 моль/л;
[Н2О]р
= 2 – 1,2 = 0,8 моль/л.
Пример
4. Эндотермическая реакция
разложения пентахлорида фосфора
протекает по уравнению:
PCl5(г)
= РСl3(г) + Сl(г);
ΔН = + 92,59 кДж.
Как
надо изменить: а) температуру; б)
давление; в) концентрацию, чтобы
сместить равновесие в сторону прямой
реакции – разложения PCl5?
Решение.
Смещением или сдвигом химического
равновесия называют изменение
равновесных концентраций реагирующих
веществ в результате изменения одного
из условий реакции. Направление, в
котором сместилось равновесно,
определяется по принципу Ле Шателье:
а) так как реакция разложения PCl5
эндотермическая (ΔН > 0) то для
смещения равновесия в сторону прямой
реакции нужно повысить температуру;
б) так как в данной системе разложение
РСl5 ведет к увеличению объема
(из одной молекулы газа образуются
две газообразные молекулы), то для
смещения равновесия в сторону прямой
реакции надо уменьшить давление; в)
смещения равновесия в указанном
направлении можно достигнуть как
увеличением концентрации РСl5,
так и уменьшением концентрации РСl3
или Сl2.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 сентября 2020 года; проверки требуют 23 правки.
Свобо́дная эне́ргия Ги́ббса (или просто эне́ргия Ги́ббса, или потенциа́л Ги́ббса, или изобарно-изотермический потенциал, или термодинами́ческий потенциа́л в узком смысле) — это величина, изменение которой в ходе химической реакции равно изменению внутренней энергии системы. Энергия Гиббса показывает, какая часть от полной внутренней энергии системы может быть использована для химических превращений или получена в их результате в заданных условиях и позволяет установить принципиальную возможность протекания химической реакции в заданных условиях. Математически это термодинамический потенциал следующего вида:
Энергию Гиббса можно понимать как полную потенциальную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (


Определение[править | править код]
Классическим определением энергии Гиббса является выражение
где 




Дифференциал энергии Гиббса для системы с постоянным числом частиц, выраженный в собственных переменных — через давление 

Для системы с переменным числом частиц этот дифференциал записывается так:
Здесь 
Связь с термодинамической устойчивостью системы[править | править код]
Покажем, что минимум потенциала Гиббса соответствует устойчивому равновесию термодинамической системы с фиксированными температурой, давлением и числом частиц.
Запишем обобщённое уравнение первого и второго начал термодинамики:
При 
Таким образом в системе при постоянных температуре и давлении энергия Гиббса достигает минимального значения.
Применение в химии[править | править код]
Связь с химическим потенциалом[править | править код]
Используя свойства экстенсивности термодинамических потенциалов, математическим следствием которых является соотношение Гиббса-Дюгема, можно показать, что химический потенциал для системы с одним типом частиц есть отношение энергии Гиббса к числу молей вещества n в системе:
Если система состоит из частиц нескольких сортов 

Химический потенциал применяется при анализе систем с переменным числом частиц, а также при изучении фазовых переходов. Так, исходя из соотношений Гиббса — Дюгема и из условий равенства химических потенциалов 

Энергия Гиббса и направление протекания реакции[править | править код]
a) эндотермическая реакция
б)экзотермическая реакция
Энергетический профиль реакции[2]
В химических процессах одновременно действуют два противоположных фактора — энтропийный (


уравнению Гиббса — Гельмгольца :
Из этого выражения следует, что 


Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса.

|
процесс может протекать — самопроизвольный процесс, |

|
система находится в состоянии химического равновесия. |

|
процесс протекать не может — несамопроизвольный процесс |
Иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может. Речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенства 
Изотерма Вант-Гоффа[править | править код]
Изотерма Вант-Гоффа — соотношение, связывающее изменение свободной энергии Гиббса 

где 

Solid — твердое
Liquid — жидкое
Gas — газообразное
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как
где 

Историческая справка[править | править код]
Энергия Гиббса названа в честь одного из основателей термодинамики, Джозайи Уилларда Гиббса.
Примечания[править | править код]
- ↑ Стромберг А. Г., Семченко Д. П. Физическая химия: учебник для хим. спец. вузов. — 6-е изд. — М.: Высшая школа, 2006. — 527 с.
- ↑ Desmos.
Литература[править | править код]
- Ахметов Н. С. Актуальные вопросы курса неорганической химии. — М.: Просвещение, 1991. — 495 с. — ISBN 5-09-002630-0.
- Базаров И. П. Термодинамика. — М.: Высшая школа, 1991. — 376 с. — ISBN 5-06-000626-3.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1. — Издание 3-е, доп. — М.: Наука, 1976. — 584 с. — («Теоретическая физика», том V).
См. также[править | править код]
- Термодинамический потенциал
- Свободная энергия Гельмгольца
…
Здесь вы найдете примеры задач на вычисление таких термодинамических параметров как энтальпия, энтропия, энергия Гиббса. Определение возможности самопроизвольного протекания процесса, а также составление термохимических уравнений.
Задачи к разделу Основы термодинамики с решениями
Задача 1. Рассчитайте стандартную энтальпию и стандартную энтропию химической реакции. Определите в каком направлении при 298 °К (прямом или обратном) будет протекать реакция. Рассчитайте температуру, при которой равновероятны оба направления реакции.
Fe2O3 (к) + 3H2 = 2Fe(к) + 3H2O(г)
Показать решение »
Решение.
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
Используя справочные данные стандартных энтальпий веществ, находим:
ΔHр-ции = 2·ΔH0Fe+3·ΔH0H2O— ΔH0Fe2O3 — 3·ΔH0H2= 2·0 + 3·(- 241,82) – (-822,16) — 3·0 = 96,7 кДж/моль
ΔSр-ции=ΣS0кон – ΣS0исх Дж/(моль·K)
Используя справочные данные стандартных энтропий веществ, находим:
ΔSр-ции = 2·ΔS0Fe + 3·ΔS0H2O — ΔS0Fe2O3 — 3·ΔS0H2= 2·27,15 + 3·188,7 – 89,96 — 3·131 = 137,44 Дж/(моль·K)
ΔG = ΔH – TΔS= 96,7 – 298 ·137,44 /1000 = 55,75 кДж/моль
При Т=298°К, ΔG > 0 – реакция не идет самопроизвольно, т.е. реакция будет протекать в обратном направлении.
Чтобы рассчитать температуру, при которой равновероятны оба направления реакции, надо ΔG приравнять к нулю:
ΔG = ΔH – TΔS = 0, тогда
T= — (ΔG – ΔH) / ΔS= — (0-96,7)/0,137 = 705,83 K
При Т = 705,83 К реакция будет идти равновероятно как в прямом так и в обратном направлении.
Задача 2. Вычислите энергию Гиббса и определите возможность протекания реакции при температурах 1000 и 3000 К.
| Cr2O3 (т) + 3C (т) = 2Cr (т) + 3CO (г) | |||||
| ΔH298, кДж/моль | — 1141 | 0 | 0 | — 110,6 | |
| ΔS298, Дж/(моль×К) | 81,2 | 5,7 | 23,6 | 197,7 |
Показать решение »
Решение.
Вычисления энергии Гиббса проводим согласно выражению:
ΔGр-ции = ΔHр-ции – TΔSр-ции
Необходимо рассчитать энтальпию и энтропию химической реакции.
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
Используя справочные данные стандартных энтальпий веществ, находим:
ΔHр-ции= 2·ΔH0Cr + 3·ΔH0CO — ΔH0Cr2O3 — 3·ΔH0C= 2·0 + 3·(- 110,6) – (-1141) — 3·0 = 809,2 кДж/моль
ΔSр-ции=ΣS0кон – ΣS0исх Дж/моль·K
Аналогично, используя справочные данные стандартных энтропий веществ, находим:
ΔSр-ции= 2·ΔS0Cr + 3·ΔS0CO — ΔS0Cr2O3 — 3·ΔS0C= 2·23,6 + 3·197,7 – 81,2 — 3·5,7 = 542 Дж/(моль·K)
Найдем энергию Гиббса при 1000 К
ΔG1000 = ΔH – TΔS= 809,2 – 1000 ·542 /1000 = 267,2 кДж/моль
ΔG1000 > 0, следовательно, реакция самопроизвольно не идет.
Найдем энергию Гиббса при 3000 К
ΔG3000= ΔH – TΔS = 809,2 – 3000 ·542 /1000 = — 816,8 кДж/моль
ΔG3000 ˂ 0, следовательно, реакция протекает самопроизвольно.
Задача 3. Определите тепловой эффект сгорания жидкого CS2(ж) до образования газообразных СО2 и SO2. Сколько молей CS2 вступят в реакцию, если выделится 700 кДж тепла?
Показать решение »
Решение.
Уравнение реакции сгорания жидкого сероуглерода следующее:
CS2(ж) + 3O2 = СО2 + 2SO2
Тепловой эффект реакции вычислим подставляя справочные данные стандартных энтальпий веществ в выражение:
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
ΔHр-ции= 2·ΔH0SO2 + ΔH0CO2 — ΔH0CS2 — 3·ΔH0O2 = 2·(-296,9) + 3·(- 393,5) – 87 — 3·0 = -1075,1 кДж/моль
Т.е. при сгорании 1 моля сероуглерода выделяется 1075,1 кДж тепла
а при сгорании x молей сероуглерода выделяется 700 кДж тепла
Найдем х:
x = 700·1/1075,1 = 0,65 моль
Итак, если в результате реакции выделится 700 кДж тепла, то в реакцию вступят 0,65 моль CS2
Задача 4. Вычислите тепловой эффект реакции восстановления оксида железа (II) водородом, исходя из следующих термохимических уравнений:
1. FeO (к) + CO (г) = Fe (к) + CО2 (г); ΔH1 = -18,20 кДж;
2. СO (г) + 1/2O2 (г) = СO2 (г) ΔН2 = -283,0 кДж;
3. H2 (г) + ½ O2 (г) = H2O (г) ΔН3 = -241,83 кДж.
Показать решение »
Решение.
Реакция восстановления оксида железа (II) водородом имеет следующий вид:
4. FeO (к) + H2 (г) = Fe (к) + H2O (г)
Чтобы вычислить тепловой эффект реакции необходимо применить закон Гесса, т.е. реакцию 4. можно получить, если сложить реакции 1. и 2. и вычесть реакцию 1.:
ΔHр-ции = ΔH1 + ΔH3 – ΔH2 = -18,2 – 241,3 + 283 = 23 кДж
Таким образом, тепловой эффект реакции восстановления оксида железа (II) водородом равен
ΔHр-ции = 23 кДж
Задача 5. Реакция горения бензола выражается термохимическим уравнением:
С6Н6(ж) + 7½ О2(г) = 6СО2(г) + 3Н2О(г) – 3135,6 кДж.
Вычислите теплоту образования жидкого бензола. Определите теплотворную способность жидкого бензола при условии, что стандартные условия совпадают с нормальными.
Показать решение »
Решение.
Тепловой эффект реакции равен:
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
В нашем случае ΔHр-ции = – 3135,6 кДж, найдем теплоту образования жидкого бензола:
ΔHр-ции= 6·ΔH0СO2 + 3·ΔH0H2O — ΔH0C6H6 – 7,5·ΔH0O2
-ΔH0C6H6 = ΔHр-ции — 3·(-241,84) + 6·(- 393,51) – 7,5·0 = — 3135,6 — 3·(-241,84) + 6·(- 393,51) – 7,5·0 = — 49,02 кДж/моль
ΔH0C6H6 = 49,02 кДж/моль
Теплотворная способность жидкого бензола вычисляется по формуле:
QТ = ΔHр-ции · 1000 / М
М(бензола) = 78 г/моль
QТ = – 3135,6· 1000 / 78 = — 4,02·104 кДж/кг
Теплотворная способность жидкого бензола QТ = — 4,02·104 кДж/кг
Задача 6. Реакция окисления этилового спирта выражается уравнением:
С2Н5ОН(ж) + 3,0 О2(г) = 2СО2(г) + 3Н2О(ж).
Определить теплоту образования С2Н5ОН(ж), зная ΔН х.р. = — 1366,87 кДж. Напишите термохимическое уравнение. Определите мольную теплоту парообразования С2Н5ОН(ж) → С2Н5ОН(г), если известна теплота образования С2Н5ОН(г), равная –235,31 кДж·моль-1.
Показать решение »
Решение.
Исходя из приведенных данных, запишем термохимическое уравнение:
С2Н5ОН(ж) + 3О2(г) = 2СО2(г) + 3Н2О(ж) + 1366,87 кДж
Тепловой эффект реакции равен:
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
В нашем случае ΔHр-ции = – 1366,87 кДж.
Используя справочные данные теплот образования веществ, найдем теплоту образования С2Н5ОН(ж):
ΔHр-ции= 2·ΔH0СO2 + 3·ΔH0H2O — ΔH0C2H5OH(ж) – 3·ΔH0O2
– 1366,87 =2·(-393,51)+ 3·(-285,84) — ΔH0C2H5OH – 3·0
ΔH0C2H5OH(ж) = -277,36 кДж/моль
ΔH0C2H5OH(г) = ΔH0C2H5OH(ж) + ΔH0парообразования
ΔH0парообразования = ΔH0C2H5OH(г) — ΔH0C2H5OH(ж)
ΔH0парообразования = — 235,31 + 277,36 = 42,36 кДж/моль
Мы определили, что теплота образования С2Н5ОН(ж) равна
ΔH0C2H5OH(ж) = -277,36 кДж/моль
и мольная теплота парообразования С2Н5ОН(ж) → С2Н5ОН(г) равна
ΔH0парообразования = 42,36 кДж/моль
Задача 7. Чем можно объяснить, что при стандартных условиях, невозможна экзотермическая реакция:
СО2 (г)+Н2 (г) ↔ СО (г)+Н2О (ж)?
Рассчитайте ΔG данной реакции. При каких температурах данная реакция становится самопроизвольной?
Показать решение »
Решение.
Рассчитаем ΔG данной реакции:
ΔG = ΔH – TΔS
Для этого сначала определим ΔH и ΔS реакции:
ΔHр-ции = ΣH0кон – ΣH0исх кДж/моль
Используя справочные данные стандартных энтальпий веществ, находим:
ΔHр-ции= ΔH0H2O(ж) + ΔH0CO — ΔH0CО2 — ΔH0Н2 = -110,5 + (-285,8) – (393,5) — 0 = -2,8 кДж/моль
ΔSр-ции=ΣS0кон – ΣS0исх Дж/(моль·K)
Аналогично, используя справочные данные стандартных энтропий веществ, находим:
ΔSр-ции= ΔS0H2O(ж) + ΔS0CO — ΔS0CО2 — ΔS0Н2 = 197,5 + 70,1 — 213,7 — 130,52 = -76,6 Дж/(моль·K)
Найдем энергию Гиббса при стандартных условиях
ΔGр-ции= ΔH – TΔS= -2,8 + 298 · 76,6 /1000 = 20 кДж/моль> 0,
следовательно, реакция самопроизвольно не идет.
Найдем при каких температурах данная реакция становится самопроизвольной.
В состоянии равновесия ΔGр-ции= 0, тогда
T = ΔH/ΔS = -2,8/(-76,6·1000) = 36,6 К
Задача 8. Рассчитав на основании табличных данных ΔG и ΔS, определите тепловой эффект реакции:
2 NO (г) + Cl2 (г) ↔ 2 NOCl(г).
Показать решение »
Решение.
При постоянных температуре и давлении, изменение энергии Гиббса связано с энтальпией и энтропией выражением:
ΔG = ΔH – TΔS
На основании табличных данных рассчитаем ΔG и ΔS
ΔG0р-ции = Σ ΔG0прод — Σ ΔG0исх
ΔGр-ции = 2·ΔG0NOCl(г) — 2·ΔG0NO(г) — ΔG0Cl2(г)
ΔGр-ции = 2· 66,37 — 2· 89,69 – 0 = — 40,64 кДж/моль
ΔGр-ции < 0, значит реакция самопроизвольна.
ΔSр-ции=ΣS0кон – ΣS0исх Дж/(моль·K)
ΔSр-ции = 2·ΔS0NOCl(г) — 2·ΔS0NO(г) — ΔS0Cl2(г)
ΔSр-ции = 2· 261,6 — 2· 210,62 – 223,0 = -121,04 Дж/(моль·K)
Найдем ΔH:
ΔH = ΔG + TΔS
ΔH = — 40,64 + 298 · (-121,04/1000) = — 76,7 кДж/моль
Тепловой эффект реакции ΔH = — 76,7 кДж/моль
Задача 9. С чем будет более интенсивно взаимодействовать газообразный хлористый водород (в расчете на 1 моль): с алюминием или с оловом? Ответ дайте, рассчитав ΔG0 обеих реакций. Продуктами реакций являются твердая соль и газообразный водород.
Показать решение »
Решение.
Рассчитаем ΔG0 для реакции взаимодействия газообразного хлористого водорода (в расчете на 1 моль) с алюминием
2Al(т) + 6HCl (г) = 2AlCl3 (т) + 3H2
ΔG0р-ции = Σ ΔG0прод — Σ ΔG0исх кДж/моль
ΔG0р-ции1 = 2·ΔG0AlCl3 (т) + 3·ΔG0H2 — 2·ΔG0Al (т) — 6·ΔG0HCl(г)
ΔG0р-ции1 = 2· (-636,8) + 3·0— 2·0— 6·(-95,27) = -701,98 кДж/моль
В реакции принимает участие 2 моль Al(т), тогда ΔGр-ции1 1 моля Al(т) равно
ΔG0р-ции 1 = -701,98 / 2 = -350,99 кДж/моль
Рассчитаем ΔG0 для реакции взаимодействия газообразного хлористого водорода (в расчете на 1 моль) с оловом:
Sn(т) + 2HCl (г) = SnCl2(т) + H2
ΔG0р-ции2 =ΔG0SnCl2 (т) + ΔG0H2 — ΔG0Sn (т) — 2·ΔG0HCl(г)
ΔG0р-ции 2 = -288,4 + 0- 0- 2·(-95,27) = -97,86 кДж/моль
Обе реакции имеют ΔG0<0, поэтому они протекают самопроизвольно в прямом направлении, но более интенсивно взаимодействовать газообразный хлористый водород будет с алюминием, т.к
ΔG0р-ции 1 ˂ ΔG0р-ции 2
Задача 10. Не прибегая к вычислениям, определите, какие знаки (>0, <0, ≅0) имеют ΔG, ΔH и ΔS для протекающей в прямом направлении реакции:
4 НBr (г) + O2(г) ↔ 2 H2O(г) + 2 Br2(г)
Как повлияет повышение температуры на направленность химической реакции?
Показать решение »
Решение.
При постоянных температуре и давлении изменение энергии Гиббса связано с энтальпией и энтропией выражением:
ΔG = ΔH – TΔS
Энтропия – мера беспорядочности системы. Значение энтропии тем больше, чем больше беспорядок в системе (больше газообразных веществ). В данной реакции количество молей газов в правой части равно – 5, а в левой – 4, значит энтропия системы уменьшается ΔS˂0.
По условию задачи реакция протекает в прямом направлении, следовательно ΔG˂0.
В обычных условиях TΔS ˂˂ ΔH, поэтому в данном случае ΔH˂0 – реакция экзотермическая.
При повышении температуры может настать момент, когда значения TΔS и ΔH станут одинаковыми, тогда система придет в равновесие ΔG=0. Если температуру повысить значительно, то будет преобладать энтропийный фактор TΔS, тогда реакция самопроизвольно протекать уже не будет ΔG>0.
Материалы из методички: Сборник задач по теоретическим основам химии для студентов заочно-дистанционного отделения / Барботина Н.Н., К.К. Власенко, Щербаков В.В. – М.: РХТУ им. Д.И. Менделеева, 2007. -155 с.
Понятие энтропии
Абсолютная энтропия веществ и изменение энтропии в процессах
Стандартная энтропия
Стандартная энтропия образования
Энергия Гиббса
Стандартная энергия Гиббса образования
Энтальпийный, энтропийный фактор и направление процесса
Примеры решения задач
Задачи для самостоятельного решения
Понятие энтропии
Энтропия S – функция состояния системы. Энтропия характеризует меру неупорядоченности (хаотичности) состояния системы. Единицами измерения энтропии являются Дж/(моль·К).
Абсолютная энтропия веществ и изменение энтропии в процессах
При абсолютном нуле температур (Т = 0 К) энтропия идеального кристалла любого чистого простого вещества или соединения равна нулю. Равенство нулю S при 0 К позволяет вычислить абсолютные величины энтропий веществ на основе экспериментальных данных о температурной зависимости теплоемкости.
Изменение энтропии в процессе выражается уравнением:
ΔS = S(прод.) – S(исх.)
где S(прод.) и S(исх.) – соответственно абсолютные энтропии продуктов реакции и исходных веществ.
На качественном уровне знак S реакции можно оценить по изменению объема системы ΔV в результате процесса. Знак ΔV определяется по изменению количества вещества газообразных реагентов Δnг. Так, для реакции
CaCO3(к) = CaO(к) + CO2(г)
(Δnг = 1) ΔV > 0, значит, ΔS > 0.
Для реакции:
С(графит) + 2Н2(г) = СН4(г)
(Δnг = -1) ΔV < 0, следовательно и ΔS < 0.
Стандартная энтропия
Величины энтропии принято относить к стандартному состоянию. Чаще всего значения S рассматриваются при Р = 101,325 кПа (1 атм) и температуре Т = 298,15 К (25оС). Энтропия в этом случае обозначается Sо298 и называется стандартной энтропией при Т = 298,15 К. Следует подчеркнуть, что энтропия вещества S (Sо) увеличивается при повышении температуры.
Стандартная энтропия образования
Стандартная энтропия образования ΔSоf,298 (или ΔSообр,298) – это изменение энтропии в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии.
Энергия Гиббса
Энергия Гиббса G – функция состояния системы. Энергия Гиббса равна:
G = Н – ТS.
Абсолютное значение энергии Гиббса определить невозможно, однако можно вычислить изменение δG в результате протекания процесса.
Критерий самопроизвольного протекания процесса: в системах, находящихся при Р, Т = const, самопроизвольно могут протекать только процессы, сопровождающиеся уменьшением энергии Гиббса (ΔG < 0). При достижении равновесия в системе ΔG = 0.
Стандартная энергия Гиббса образования
Стандартная энергия Гиббса образования δGоf,298 (или δGообр,298) – это изменение энергии Гиббса в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии, причем простые вещества пристутствуют в наиболее термодинамически устойчивых состояниях при данной температуре.
Для простых веществ, находящихся в термодинамически наиболее устойчивой форме, δGоf,298 = 0.
Энтальпийный, энтропийный фактор и направление процесса
Проанализируем уравнение ΔGоТ = ΔНоТ — ΔТSоТ. При низких температурах ТΔSоТ мало. Поэтому знак ΔGоТ определяется в основном значением ΔНоТ (энтальпийный фактор). При высоких температурах ТΔSоТ – большая величина, знак Δ GоТ определяется и энтропийным фактором. В зависимости от соотношения энтальпийного (ΔНоТ) и энтропийного (ТΔSоТ) факторов существует четыре варианта процессов.
-
-
- Если ΔНоТ < 0, ΔSоТ > 0, то ΔGоТ < 0 всегда (процесс может протекать самопроизвольно при любой температуре).
- Если ΔНоТ > 0, ΔSоТ < 0, то ΔGоТ > 0 всегда (процесс не протекает ни при какой температуре).
- Если ΔНоТ < 0, ΔSоТ < 0, то ΔGоТ < 0 при Т < ΔНо/ΔSо (процесс идет при низкой температуре за счет энтальпийного фактора).
- Если ΔНоТ > 0, ΔSоТ > 0, то ΔGоТ < 0 при Т > ΔНо/ ΔSо (процесс идет при высокой температуре за счет энтропийного фактора).
-
Примеры решения задач
Задача 1. Используя термодинамические справочные данные, вычислить при 298,15 К изменение энтропии в реакции:
4NH3(г) + 5O2(г) = 4NО(г) + 6H2O(ж)
Объяснить знак и величину ΔSо.
Решение. Значения стандартных энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | NH3(г) | O2(г) | NО(г) | H2O(ж) |
| Sо298,
Дж/(моль·К) |
192,66 | 205,04 | 210,64 | 69,95 |
ΔSох.р.,298 = 4Sо298(NО(г) ) + 6Sо298(H2O(ж)) — 4Sо298(NH3(г)) — 5Sо298(O2(г)) = 4× 210,64 + 6× 69,95 — 4× 192,66 — 5× 205,04 = — 533,58 Дж/К
В данной реакции ΔV < 0 (Δnг = — 5), следовательно и ΔSoх.р.,298 < 0, что и подтверждено расчетом.
Задача 2. Используя справочные термодинамические данные, рассчитать стандартную энтропию образования NH4NO3(к). Отличается ли стандартная энтропия образования NH4NO3(к) от стандартной энтропии этого соединения?
Решение. Стандартной энтропии образования NH4NO3 отвечает изменение энтропии в процессе:
N(г) + 2H2(г) + 3/2O2(г) = NH4NO3(к); δSоf,298(NH4NO3(к)) = ?
Значения стандартных энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | N2(г) | H2(г) | O2(г) | NH4NO3(к) |
| Sо298,
Дж/(моль·К) |
191,50 | 130,52 | 205,04 | 151,04 |
ΔSох.р.,298 = ΔSоf,298(NH4NO3(к)) = Sо298(NH4NO3(к)) — Sо298(N2(г)) — 2Sо298(H2(г)) – 3/2Sо298(O2(г)) = 151,04–191,50 —— 2× 130,52–3/2× 205,04 = — 609,06 Дж/(моль·К).
Стандартная энтропия образования NH4NO3(к), равная — 609,06 Дж/(моль·К), отличается от стандартной энтропии нитрата аммония Sо298(NH4NO3(к)) = +151,04 Дж/(моль·К) и по величине, и по знаку. Следует помнить, что стандартные энтропии веществ Sо298 всегда больше нуля, в то время как величины ΔS0f,298, как правило, знакопеременны.
Задача 3. Изменение энергии Гиббса реакции:
2Н2(г) + О2(г) = 2 Н2О(ж)
равно δGо298= –474,46 кДж. Не проводя термодинамические расчеты, определить, за счет какого фактора (энтальпийного или энтропийного) протекает эта реакция при 298 К и как будет влиять повышение температуры на протекание этой реакции.
Решение. Поскольку протекание рассматриваемой реакции сопровождается существенным уменьшением объема (из 67,2 л (н.у.) исходных веществ образуется 36 мл жидкой воды), изменение энтропии реакции ΔSо<0. Поскольку ΔGо298 реакции меньше нуля, то она может протекать при температуре 298 К только за счет энтальпийного фактора. Повышение температуры уменьшает равновесный выход воды, поскольку ТΔSо<0.
Задача 4. Используя справочные термодинамические данные, определить может ли при 298,15 К самопроизвольно протекать реакция:
С4Н10(г) = 2С2Н4(г) + Н2(г)
Если реакция не будет самопроизвольно протекать при 298,15 К, оценить возможность ее протекания при более высоких температурах.
Решение. Значения стандартных энергий Гиббса и энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | С4Н10(г) | С2Н4(г) | Н2(г) |
| ΔGоf,298× , кДж/моль | — 17,19 | 68,14 | 0 |
| Sо298, Дж/(моль·К) | 310,12 | 219,45 | 130,52 |
ΔGох.р.,298 = 2ΔGоf,298(С2Н4(г)) + ΔGоf,298(Н2(г)) — ΔGоf,298(С4Н10(г)) = 2× 68,14 + 17,19 = 153,47 кДж.
ΔGох.р.,298 > 0, следовательно, при Т = 298,15 К реакция самопроизвольно протекать не будет.
ΔSох.р.,298 = 2Sо298(С2Н4(г)) + Sо298(Н2(г)) — Sо298(С4Н10(г)) = 2× 219,45 + 130,52 – 310,12 = +259,30 Дж/К.
Поскольку ΔSох.р.,298 > 0, то при температуре Т>ΔНо/ΔSо величина ΔGох.р.,298 станет величиной отрицательной и процесс сможет протекать самопроизвольно.
Задача 5. Пользуясь справочными данными по ΔGоf,298 и Sо298, определите ΔHо298 реакции:
N2O(г) + 3H2(г) = N2H4(г) + H2O(ж)
Решение. Значения стандартных энергий Гиббса и энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | N2O(г) | H2(г) | N2H4(г) | H2O(ж) |
| ΔGоf,298, кДж/моль | 104,12 | 0 | 159,10 | -237,23 |
| Sо298, Дж/(моль·К) | 219,83 | 130,52 | 238,50 | 69,95 |
ΔGох.р.,298 = ΔGоf,298(N2H4(г)) + ΔGоf,298(H2O(ж)) – ΔGоf,298(N2O(г)) – 3ΔGоf,298(H2(г)) = 159,10 + (–237,23) – 104,12 – 0 = –182,25 кДж.
ΔSох.р.,298 = Sо298(N2H4(г)) + Sо298(H2O(ж)) – Sо298(N2O(г)) — 3Sо298(H2(г)) = 238,50 + 69,95 – 219,83 –3× 130,52 = –302,94 Дж/К.
ΔGо298 = ΔНо298 – ТΔSо298. Подставляя в это уравнение величины ΔНо298 и ТΔSо298, получаем:
ΔНо298 = –182,25× 103 + 298·(–302,94) = –272526,12 Дж = – 272,53 кДж.
Следует подчеркнуть, что поскольку ΔSо298 выражена в Дж/(моль× К), то при проведении расчетов ΔG0298 необходимо также выразить в Дж или величину ΔS0298 представить в кДж/(мольK).
Задачи для самостоятельного решения
1. Используя справочные данные, определите стандартную энтропию образования ΔSоf,298 NaHCO3(к).
2. Выберите процесс, изменение энергии Гиббса которого соответствует стандартной энергии Гиббса образования NO2(г):
а) NO(г) + 1/2O2(г) = NO2(г);
б) N2(г) + 2O2(г) = 2NO2(г);
в) 1/2N2(г) + O2(г) = NO2(г);
г) N(г) + O2(г) = NO2(г).
3. Используя справочные данные, вычислите при 298,15 К изменение энтропии в реакции:
2NH4NO3(к) = 2N2(г) + 4H2O(г) + О2(г).
Объясните знак и величину ΔSº реакции.
-
- .
|
δSох.р.,298 =1040,84 Дж/К. В данной реакции δV > 0 (D nг = 7), |
4. Используя справочные данные, определите принципиальную возможность протекания реакции при 298,15 К:
NiO(к) + C(графит) = Ni(к) + CO(г)
Если реакция не будет самопроизвольно протекать при 298,15 К, оценить возможность ее протекания при более высоких температурах.
|
ΔGох.р.,298 = 74,45 кДж > 0, следовательно, при Т = 298,15 К |
5. Рассчитайте стандартную энергию Гиббса образования ΔGоf,298 C2H5OH(ж), используя справочные данные о величинах ΔНоf,298 и Sо298.
6. Используя справочные данные, определите стандартную энтропию образования ΔSоf,298 K2Cr2O7(к).
7. На основе расчетов термодинамических величин покажите, чем эффективнее восстанавливать при 298 К Cr2O3(к) до металла — алюминием или магнием:
1) Cr2O3(к) + 3Mg(к) = 3MgO(к) + 2Cr(к); ΔGо1;
2) Cr2O3(к) + 2Al(к) = Al2O3(к) + 2Cr(к); ΔGо2.
|
ΔGо1=-648,9 кДж; ΔGо2=-523,3 кДж. |
8. Используя справочными данными по величинам Sо298, определите возможность самопроизвольного протекания в изолированной системе при 298 К процесса:
KClO3(к) = KCl(к) + 3/2O2(к)
|
ΔSо298=247,1 Дж/К. |
9. Используя справочные данные, вычислите при 298 К изменение энтропии в процессе:
Н2(г) + 1/2О2(г) = Н2О(г)
10. На основе справочных данных оценить температуру восстановления WO3(к) водородом:
WO3(к) + 3H2(г) = W(к) + 3H2O(г).
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке “Файлы работы” в формате PDF
Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции; это термодинамический потенциал следующего вида:
G = U + PV – TS
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста её энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж).
1 Основные понятия энергии Гиббса
Классическим определением энергии Гиббса является выражение:
G = U + PV – TS,
где U – внутренняя энергия, P – давление, V – объем, T – абсолютная температура, S – энтропия.
Дифференциал энергии Гиббса для системы с постоянным числом частиц, выраженный в собственных переменных — через давление p и температуру T:
dG = – S dT + VdP.
Для системы с переменным числом частиц этот дифференциал записывается так:
dG = – S dT + V dP + dN.
Здесь – химический потенциал, который можно определить как энергию, которую необходимо затратить, чтобы добавить в систему еще одну частицу.
Правило фаз Гиббса в термодинамике: число равновесно сосуществующих в какой-либо системе фаз не может быть больше числа образующих этих фаз.
Эенергия Гиббса: (изобарно-изотермический потенциал, свободная энтальпия), один из потенциалов термодинамических системы. Обозначается G, определяется разностью между энтальпией H и произведением энтропии S на термодинамическую температуру Т: G = H — T·S. Изотермический равновесный процесс без затраты внешних сил может протекать самопроизвольно только в направлении убывания энергии Гиббса до достижения ее минимума, которому отвечает термодинамическое равновесное состояние системы. Названа по имени Дж. У. Гиббса.
Термодинамические потенциалы , функции объема, давления, температуры, энтропии, числа частиц и других независимых макроскопических параметров, характеризующих состояние термодинамической системы. К потенциалам термодинамическим относятся внутренняя энергия, энтальпия, изохорно-изотермический потенциал (Гельмгольца энергия), изобарно-изотермический потенциал (Гиббса энергия). Зная какие-либо потенциалы термодинамические как функцию полного набора параметров, можно вычислить любые макроскопические характеристики системы и рассчитать происходящие в ней процессы.
Распределение Гиббса: каноническое, распределение вероятностей различных состояний макроскопической системы с постоянным объемом и постоянным числом частиц, находящейся в равновесии с окружающей средой заданной температуры; если система может обмениваться частицами со средой, то распределение Гиббса называется большим каноническим. Для изолированной системы справедливо Гиббса распределение микроканоническое, согласно которому все микросостояния системы с данной энергией равновероятны. Названо по имени открывшего это распределение Дж. У. Гиббса.
2 Значение энергии Гиббса
Самопроизвольность протекания процессов в системах открытого и закрытого типов описывается через специальный критерий, получивший название энергии Гиббса. Он является функцией состояния. Д.У. Гиббс, работая с термодинамическими системами, сумел вывести ее через энтропию и энтальпию. Энергия Гиббса, в частности, позволяет предсказывать направленность протекания самопроизвольных биологических процессов и оценивать их теоретически достижимый КПД.
Если применить выводы Гиббса ко второму термодинамическому закону, то формулировка будет следующей: при постоянных (const) давлении и температуре без внешнего воздействия система может поддерживать самопроизвольное протекание лишь таких процессов, следствием которых является уменьшение уровня энергии Гиббса до значения, которое наступает при достижении ею установившегося минимума. Равновесие любой термодинамической системы означает неизменность указанной энергии (минимум). Поэтому энергия Гиббса представляет собой потенциал (свободную энтальпию) в изобарно-изотермических системах. Поясним, почему указан именно минимум. Дело в том, что это одно из важнейших постулатов равновесия в термодинамике: данное состояние при неизменности температуры и давления означает, что для очередного изменения необходимо увеличить уровень энергии, а такое возможно лишь при смене каких-либо внешних факторов.
Буквенное обозначение – G. Численно равна разности между известной энтальпией и значением произведения температуры на энтропию. То есть энергия Гиббса может быть выражена через следующую формулу:
где S – энтропия системы, t – температура термодинамическая, H – энтальпия.
Энтропия системы в данную формулу включена для того, чтобы учитывать тот факт, что высокая температура приводит к уменьшению упорядоченного состояния системы (беспорядок), а низкая же – наоборот.
Так как и Гиббсова энергия, и энтальпия – одни из функций системы в термодинамике, то посредством изменения G или H можно охарактеризовать протекающие химические превращения. Если приводится уравнение реакции и изменение энергии Гиббса, то его относят к классу термохимических.
Применительно к этой энергии может быть сформулировано Правило Гесса: если давление и температура неизменны, то создание новых веществ из первоначальных (базовых реагентов) приводит к тому, что энергия в системе изменяется, при этом вид происходящих реакций и их количество на результат никак не влияют.
Так как энергия, о которой говорится в представленном докладе, является изменчивой величиной, то для выполнения расчетов было введено понятие «стандартная энергия Гиббса». Эта величина присутствует в любом химическом справочнике, численно равна 298 кДж/моль (обратите внимание, что размерность точно такая же, как для любой другой молярной энергии). Это значение позволяет рассчитать изменение практически для любого химического процесса.
Если в процессе протекания химической реакции на систему оказывается внешнее воздействие (совершается работа), то значение энергии Гиббса увеличивается. Такие реакции относят к эндергоническим. Соответственно, если сама система совершает работу, затрачивая энергию, то речь идет о экзергонических проявлениях.
Понятие Гиббсовой энергии нашло широчайшее применение в современной химии. К примеру, синтез полимеров основан на реакциях присоединения. При их проведении несколько частиц объединяются в одну, при этом значение энтропии уменьшается. Основываясь на формуле Гиббса, можно утверждать, что внешнее воздействие (например, высокотемпературное) может обратить подобную экзотермическую реакцию присоединения, что и подтверждается на практике [2].
3 Методы измерения энергии Гиббса
Существует значительное число способов расчета изобарно- изотермического потенциала. Это объясняется тем, что для расчета Δσot необходимо в соответствии с уравнением (1.6) знать ΔН оt и ΔS оt. Если учесть, что эти величины в свою очередь связаны с температурой уравнением теплоемкости (Ср = f(Т)), то становится понятным, что вычисление Δσot является довольно сложной задачей и требует знания этих величин для каждого компонента, входящего в уравнение реакции. Следует отметить, что для большинства веществ величины Δσot, ΔSot, ΔНot, а также коэффициенты уравнения Ср = а + bТ + с/Т2 обобщены и приведены в таблицах различных справочников [1]. Поскольку в данных справочниках все величины даны в калориях, расчеты выполнены с учетом этих величин. В связи с изложенным рассмотрим расчет Δσo t реакции окисления сернистого ангидрида в серный SО2 + 0.5О2 ↔ SО3 наиболее распространенным методом. В таблице1 приведены исходные термодинамические данные для всех компонентов реакции:
Т а б л и ц а 1 – Термодинамические величины реакции окисления
Компонент реакции ΔНо 298 ккал/моль Δσо 298 Ккал/моль Sо 298 Кал/(моль*град) Ĉр кал /(моль *град 298 – 600
SO2 70,96 71,748 59,30 10,76
O2 0 0 49,03 7,22
SO3 94,45 88,69 61,24 14,84
По значениям стандартных величин ΔНo 298 и So 298
Δσo298 = ΔНo298 – ТΔSo298
Изобарно-изотермический потенциал реакции
Δσo298 = [–94.45 – (–70.96) – 0.298 (61.24 – 0.5 · 49.03 – 59.30] = –16.76 ккал,
что хорошо согласуется с расчетом по закону Гесса:
Δσo298 = –88.69 – (–71.748) = –16.94 ккал
При наличии в справочниках величины средней теплоемкости ΔĈр в исследуемом температурном интервале Δσo 298 определяют
Δσot = ΔНo298 + Δ Ĉр( Т – 298) – Т ΔSo298 – Т ĈрlnТ/298 (1)
Это уравнение неприменимо для расчета Δσo Т в растворах, даже в узком температурном интервале.
Пример 1. Определить Δσ600 для вышеприведенной реакции, если значения Ĉр600 для SО2 О2, SО3 составляют 10.76; 7.22; 18.84 кал/(моль*град). Для решения использовать значение ΔН0 298 и S0 298 из таблицы 1.
Решение.
Δσ600 = [–94.45 –(–70.96) ] +[(18.84 – 0.5 · 7.22 – 10.76) · (600 – 298)] – – 600 (61.24 – 0.5 · 49.03 – 59.30) – 600 · 4.47 ln400/298 = = –23.49 + 1.349 + 13.545 – 1.876 = –10.472 ккал/моль.