.
Порядок составления формул оксидов
Формулы
оксидов можно составлять по правилу креста:

Рис.1
 Запомни при составлении
Запомни при составлении
формул первым ставят
элемент степень окисления. которого со знаком +, а
вторым элемент с отрицательной степенью окисления. Для оксидов это
всегда кислород.
Далее
необходимо:
1. расставить степени
окисления
(с.о.) для каждого атома. Кислород в оксидах всегда имеет с.о. -2
(минус два).
2. Для того чтобы
правильно
определить степень окисления. второго элемента необходимо познакомится
с таблицей возможных степеней окисления некоторых элементов:
Таблица.1 Степени окисления некоторых элементов
|
Элемент |
Возможные степени окисления |
| N (азот) | -3, 0, +1, +2, +3, +4,+5. |
| P (фосфор) | -3, 0, +3, +5. |
| S (сера) | -2, 0, +4, +6. |
| C (углерод) | -4, 0, +2, +4. |
Степень окисления «0» –
ноль имеют:
1. Простые вещества: Н2,
Са, О2 …
2. Сложные в-ва (в сумме): Са+2О-2 (+2 – 2 =0)
Степень окисления со знаком +
характерна для элементов которые отдают свои электроны в соединениях
другим атомам или от которых оттянуты общие электронные пары, т.е.атомы
менее электроотрицательных элементов. например металлы
всегда имеют положительную степени окисления.
Подсказка: Узнать степени окисления для металлов
можно в таблице “растворимости…“.
В ней представлены заряды ионов металлов они обычно совпадают со
степенью окисления.
С неметаллами кислород образует оксид, если только этот неметалл менее
электроотрицательный, чем сам кислород см. таблицу
электроотрицательности.

рис.2
 Запомни если степени
Запомни если степени
окисления.
элементов в бинарных соединениях равны по модулю, то индексы в формуле
не ставятся: Сa+2О-2.
Составим формулу
оксида натрия:
По
таблице растворимости заряд иона натрия +,
соответственно степень окисления натрия имеет значение +1 (Na+1),
с.о. кислорода в оксидах всегда -2.
Натрий
имеет положительный заряд, значит, его ставим первым, а вторым
ставим кислород и по правилу креста получим: Na2+1O-2
или Na2O.
Правило
наименьшего общего кратного
это способ наиболее универсальный для составления формул. Как им
пользоваться рассмотрим на примере.
Составить формулу
оксида серы (VI).
1.
У кислорода с.о. -2 следовательно в формуле он ставиться вторым, а
первым элементом будет сера ее с.о. указана в названии оксида VI, т. е
+6. S+6O-2.
2.
Найдем наименьшее общее кратное. Для чисел 2 и 6 это будет 6.
3.
Находим индексы и расставляем для каждого элемента. См. рисунки ниже.
6 : 6 = 1 это индекс для серы.
Индексы со значением 1 в формулах не ставятся.
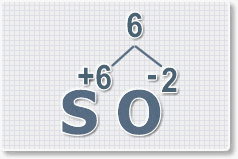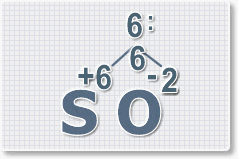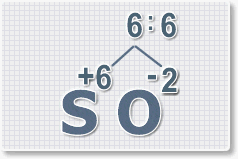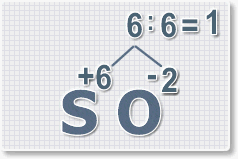
Рис.3
6 : 2 = 3
это индекс для кислорода
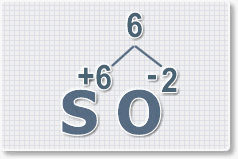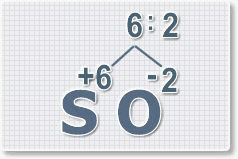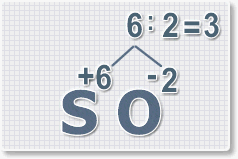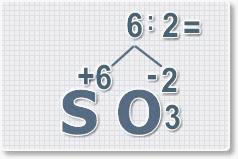
Рис.4
В результате получим
формулу оксида серы (VI):

* * *
Инфоурок
›
Химия
›Другие методич. материалы›Алгоритм составления формул основных классов неорганических соединений
Алгоритм составления формул основных классов неорганических соединений
Скачать материал
без ожидания
Скачать материал
без ожидания


- Сейчас обучается 118 человек из 49 регионов


- Сейчас обучается 426 человек из 64 регионов


- Сейчас обучается 69 человек из 31 региона


Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 256 881 материал в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Материал подходит для УМК
Другие материалы
- 04.11.2022
- 75
- 3

- 04.11.2022
- 86
- 0
- 04.11.2022
- 66
- 0
- 04.11.2022
- 76
- 0

- 04.11.2022
- 97
- 0




Вам будут интересны эти курсы:
-
Курс повышения квалификации «Химия окружающей среды»
-
Курс профессиональной переподготовки «Химия: теория и методика преподавания в образовательной организации»
-
Курс повышения квалификации «Методика написания учебной и научно-исследовательской работы в школе (доклад, реферат, эссе, статья) в процессе реализации метапредметных задач ФГОС ОО»
-
Курс повышения квалификации «Нанотехнологии и наноматериалы в биологии. Нанобиотехнологическая продукция»
-
Курс повышения квалификации «Особенности подготовки к сдаче ОГЭ по химии в условиях реализации ФГОС ООО»
-
Курс повышения квалификации «Правовое регулирование рекламной и PR-деятельности»
-
Курс профессиональной переподготовки «Биология и химия: теория и методика преподавания в образовательной организации»
-
Курс профессиональной переподготовки «Организация маркетинга в туризме»
-
Курс повышения квалификации «Финансы предприятия: актуальные аспекты в оценке стоимости бизнеса»
-
Курс профессиональной переподготовки «Управление ресурсами информационных технологий»
-
Курс повышения квалификации «Психодинамический подход в консультировании»
-
Курс повышения квалификации «Современные образовательные технологии в преподавании химии с учетом ФГОС»
-
Курс профессиональной переподготовки «Организация деятельности специалиста оценщика-эксперта по оценке имущества»
-
Курс профессиональной переподготовки «Техническое сопровождение технологических процессов переработки нефти и газа»
-
Курс профессиональной переподготовки «Организация системы учета и мониторинга обращения с отходами производства и потребления»
-
Скачать материал (медленно)
Настоящий материал опубликован пользователем Федотова Елена Геннадьевна. Инфоурок является
информационным посредником и предоставляет пользователям возможность размещать на сайте
методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них
сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайтЕсли Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.Удалить материал
-

- На сайте: 7 лет и 10 месяцев
- Подписчики: 0
- Всего просмотров: 18938
-
Всего материалов:
11
|
§ 17 |
Валентность. Составление формул оксидов |
Вы, наверное, обратили внимание на то, что оксиды различных химических элементов по составу отличаются друг от друга. Например, на один атом кислорода в воде H2O приходятся два атома водорода, а в оксиде магния MgO — один атом магния. Как это можно объяснить?
В XIX в. учёные предположили, что атомы разных элементов обладают различной способностью присоединять к себе другие атомы. Так, атом водорода может присоединить лишь один атом другого химического элемента, кислород — два атома, азот — три. В настоящее время известно, что атомы, входящие в состав молекул, соединены между собой химическими связями в определённой последовательности. Чтобы показать это, используют структурные формулы, выражающие не только число атомов, но и последовательность их соединения. Химические связи между атомами в молекулах принято обозначать чёрточками.
Число связей, которые данный атом образует с другими атомами, называют валентностью.
Слово «валентность» в переводе с латинского означает «сила, способность».
Изобразим структурную формулу воды:

Обратите внимание на то, что атомы водорода в молекуле воды не связаны друг с другом, а соединены только с атомом кислорода. Каждый атом водорода образует одну химическую связь (от символа H отходит одна чёрточка) — он одновалентен. Атом кислорода образует две связи — он двухвалентен. Число чёрточек, отходящих от символа химического элемента в структурной формуле, и есть валентность данного атома.
Установлено, что и в других соединениях водород всегда одновалентен, т. е. атомы водорода образуют лишь одну связь. Валентность кислорода всегда равна двум.
В молекуле углекислого газа CO2 атом углерода образует с каждым атомом кислорода две двойные связи, которые равноценны четырём одинарным (четыре чёрточки в структурной формуле), следовательно, углерод в этом веществе четырёхвалентен:
O C
C O.
O.
Зная валентность одного химического элемента в соединении, можно определить валентность другого. Так, хлор в хлороводороде HCl одновалентен, азот в аммиаке NH3 трёхвалентен, а валентность углерода в метане CH4 равна четырём:

Для обозначения валентности обычно используют римские цифры, которые ставят в формуле над символом химического элемента:

Чтобы подсчитать валентность, нет необходимости каждый раз рисовать структурные формулы. Легко заметить, что в соединении общее число единиц валентности всех атомов одного элемента всегда равно общему числу единиц валентности всех атомов другого элемента. Иными словами, произведение числа атомов одного элемента на его валентность равно произведению числа атомов второго элемента на его валентность.
Таблица 4
|
Последовательность действий |
Составление формулы |
|
|
Указать валентность кислорода |
|
|
|
Умножить число атомов кислорода на численное значение его валентности (II) |
3•2 = 6 |
2•2 = 4 |
|
Разделить полученное значение на индекс, показывающий число атомов другого элемента |
6 : 2 = 3 |
4 : 1 = 4 |
|
Записать значение валентности над символом этого элемента |
|
|
Например:
 .
.
Для углерода (число атомов равно 1): IV•1 = 4;
для кислорода (число атомов равно 2): II•2 = 4.
Чтобы определить валентность элемента в оксиде по формуле, необходимо провести следующие математические вычисления (табл. 4).
Некоторые химические элементы проявляют в соединениях постоянную валентность (табл. 5), её надо запомнить, другие — переменную.
Химические элементы с постоянной валентностьюТаблица 5
|
Валентность |
Химические элементы |
|
I |
H, Na, K, Ag |
|
II |
O, Mg, Ca, Ba, Zn |
|
III |
Al |
Таблица 6
|
Последовательность действий |
Составление формулы |
|
|
Записываем символы химических элементов (кислород на втором месте) и указываем их валентность (кислород двухвалентен, валентность второго элемента либо дана в названии, либо постоянна и приведена в таблице 5) |
Оксид алюминия
|
Оксид углерода(IV)
|
|
Находим наименьшее общее кратное двух числовых значений валентности |
III и II ⇒ 6 |
IV и II ⇒ 4 |
|
Находим индексы, поделив наименьшее общее кратное на численные значения валентности данного элемента |
6 : 3 = 2 (Al) 6 : 2 = 3 (O) |
4 : 4 = 1 (C) 4 : 2 = 2 (O) |
|
Записываем индексы после знаков химических элементов |
Al2O3 |
CO2 |
Обратите внимание, что значения валентности многих металлов совпадают с номерами групп Периодической системы химических элементов Д. И. Менделеева, в которых они находятся.
Значение переменной валентности принято указывать в скобках в названии соединения, например:  — оксид углерода(IV),
— оксид углерода(IV),  — оксид углерода(II).
— оксид углерода(II).
Рассмотрим, как можно составить формулу оксида по его названию (табл. 6).
Понятие о валентности возникло на заре современной химии, поэтому его использование в настоящее время вызывает много вопросов. Как, например, определить валентность атомов в простых веществах? В железе при комнатной температуре у каждого атома 8 ближайших соседей (см. рис. 23, а). Означает ли это, что железо восьмивалентно? Как быть с другими веществами немолекулярного строения? Так, оксиды металлов, как правило, не образуют молекул. Строение того же оксида алюминия Al2O3 лишь формально можно изобразить структурной формулой O Al
Al O
O Al
Al O, на самом деле в этом веществе каждый атом алюминия находится в окружении шести атомов кислорода. Поэтому приведённую формулу принято называть графической. В общем, надо помнить, что валентность имеет реальный смысл лишь в случае веществ молекулярного строения.
O, на самом деле в этом веществе каждый атом алюминия находится в окружении шести атомов кислорода. Поэтому приведённую формулу принято называть графической. В общем, надо помнить, что валентность имеет реальный смысл лишь в случае веществ молекулярного строения.
1.Дайте определение понятия «валентность».
2.Зная, что водород одновалентен, определите валентность химических элементов по формулам соединений: NaH, CaH2, AlH3, CH4, PH3, H2S, HF.
3.Определите валентность элементов по формулам оксидов и назовите вещества: P2O5, SO2, SO3, NO, Na2O, CaO, Mn2O7, SnO2, I2O5, H2O.
4.Напишите формулы следующих оксидов: оксида магния, оксида фосфора(III), оксида калия, оксида хлора(IV), оксида железа(III), оксида меди(II), оксида кремния(IV), оксида хлора(VII), оксида цинка, оксида алюминия, оксида водорода, оксида золота(III).
5.В соединениях с кислородом марганец проявляет валентности II, III, IV, VII. Составьте формулы этих оксидов и назовите их.
6.Хлор образует четыре оксида, в которых он проявляет валентности I, III, V и VII. Составьте формулы этих соединений и назовите их.
7.При горении магния, цинка и алюминия в кислороде образуются их оксиды. Составьте формулы этих соединений, напишите уравнения реакций.
Как написать формулы оксидов, соответствующих гидроксидам
Гидроксиды – это сложные вещества, к которым относятся кислоты и основания. Название состоит из двух частей – «гидро» (вода) и оксид. Если оксид кислотный, в результате его взаимодействия с водой получится гидроксид – кислота. Если же оксид основный (не основной, как иногда ошибочно называют), то и гидроксид будет представлять собой основание.

Инструкция
Для того чтобы правильно писать формулы, которые соответствуют гидроксидам – кислотам и основаниям, необходимо иметь представление об оксидах. Оксиды – это сложные вещества, состоящие из двух элементов, одним из которых является кислород. Гидроксиды в своем составе имеют еще и атомы водорода. Формулы оксидов очень легко написать, используя упрощенную схему. Для этого достаточно от соответствующего гидроксида «вычесть» все молекулы воды, которые входят в состав гидроксида. Если составной частью кислоты или основания является одна молекула воды, то нужно уменьшить количество атомов водорода на 2, а атомов кислорода на 1. Если же в состав гидроксида входят две молекулы воды, то и количество атомов водорода и кислорода нужно будет уменьшить на 4 и 2 соответственно.
H2SO4, серная кислота. Отнимите 2 атома водорода и 1 атом кислорода – получите SO3 или оксид серы (VI).
H2SO3, сернистая кислота. По аналогии с предыдущим примером получается SO2 или оксид серы (IV).
H2CO3, угольная кислота. Образуется CO2 или оксид углерода (IV).
H2SiO3, кремниевая кислота. Следовательно, получится SiO2 или оксид кремния.
Ca(OH)2, гидроксид кальция. Вычтите молекулу воды и останется CaO или оксид кальция.
В некоторых формулах гидроксидов имеется нечетное количество атомов водорода, а потому требуется удвоение. Кроме этого, удвоению подвергаются и остальные элементы, входящие в состав гидроксида, после чего, по аналогии, вычитаются все образовавшиеся молекулы воды.
NaOH, гидроксид натрия. Удвойте количество атомов каждого элемента и получите Na2O2H2. Вычтите молекулу воды и останется Na2O или оксид натрия.
Al(OH)3, гидроксид алюминия. Удвойте количество атомов – Al2O6H6. Вычтите три образовавшиеся молекулы воды и получится Al2O3, оксид алюминия.
HNO3, азотная кислота. Удвойте количество каждого элемента – получите H2N2O6. Вычтите из нее одну молекулу воды и получится N2O5 – оксид азота (V).
HNO2, азотистая кислота. Произведите удвоение числа каждого элемента – получите H2N2O4. Вычтите из нее одну молекулу воды и получится N2O3 – оксид азота (III).
H3PO4, ортофосфорная кислота. Удвойте количество каждого элемента – получите H6P2O8. Вычтите из нее три молекулы воды и получится P2O5 – оксид фосфора (V).
HMnO4, марганцовая кислота. Выполните удвоение количества атомов и получите H2Mn2O8. Вычтите молекулу воды (2 атома водорода и 1 атом кислорода), в результате будет Mn2O7 – оксид марганца (VII).
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Методические
рекомендации для учащихся первого курса
по теме: «Основные классы неорганических
соединений»
1. ОКСИДЫ
– сложные вещества, состоящие из двух
элементов, одним из которых является
кислород в степени окисления -2.
Элементом
может быть как металл, так и неметалл.
2. КИСЛОТЫ
– сложные вещества, состоящие из атомов
водорода, способных
замещаться атомами металла,
и кислотных остатков. Водород в формулах
кислот всегда пишется на первом месте.
Кислоты – это
гидроксиды неметаллов.
3. ОСНОВАНИЯ
– сложные вещества, состоящие из атомов
металла и одной или нескольких
гидроксогрупп ОН.
Основания – это
гидроксиды металлов.
4. СОЛИ
– сложные вещества, состоящие из атомов
металла и кислотных остатков.
II Классификация оксидов
Все оксиды делят
на две группы: солеобразующие
и несолеобразующие.
Несолеобразующие
– это оксиды, которые не образуют солей
ни с кислотами, ни
с основаниями. К
ним относятся оксиды: CO,
NO,
N2O,
SiO.
Все эти оксиды –
оксиды неметаллов.
Солеобразующие
оксиды –
это оксиды, которые образуют соли
либо с кислота-
ми,
либо с основаниями.
Солеобразующие
оксиды делят
на три группы: кислотные,
основные и амфо-
терные.
КИСЛОТНЫЕ
ОКСИДЫ – это
оксиды, которым соответствуют кислоты.
К
ним относятся все
оксиды неметаллов
(за исключением несолеобразующих) и
оксиды металлов
с валентностью 4 и больше.
Например:
SO3
– H2SO4
SO2
– H2SO3
CO2
– H2CO3
SiO2
– H2SiO3
P2O5
– H3PO4
и
HPO3
N2O5
– HNO3
CrO3
– H2CrO4
SeO2
– H2SeO3
(Оксиды S,
C,
Si,
P,
N
– это оксиды неметаллов, а оксиды Cr
(VI)
и Se
(IV)
– это
оксиды металлов.
Однако и те и другие – это кислотные
оксиды).
Таким образом,
надо иметь в виду, что оксиды неметаллов
– это всегда кислотные
оксиды, а оксиды
металлов могут быть как основными, так
и кислотными.
ОБРАТИТЕ ВНИМАНИЕ!
Валентность (и степень окисления)
элемента в оксиде
и кислоте должны
быть ОДИНАКОВЫМИ.
Формулу кислоты
легко записать по формуле оксида Для
этого надо мысленно
(или на черновике)
прибавить
воду Н2О
к оксиду и
(если в этом есть необходи-
мость) сократить.
Например:
формула оксида N2O3.
Прибавляем к N2O3
воду Н2О.Получаем
–
Н2
N2O4;
сокращаем на 2 – получаем Н
NO2.
Второй пример:
формула оксида V2O5.
Прибавляем к V2O5
воду Н2О.
Получаем – Н2
V2O6;
сокращаем на 2 – получаем Н
VO3.
Третий пример:
формула оксида Cl2O7.
Прибавляем к Cl2O7
воду Н2О.
Получаем – Н2
Cl2O8;
сокращаем на 2 – получаем Н
ClO4.
Четвертый пример:
формула оксида МоO3.
Прибавляем к МоO3
воду Н2О.
Получаем – Н2
МоO4;
естественно, сокращать в этом случае
просто нечего.
ОСНОВНЫЕ
ОКСИДЫ – это
оксиды, которым соответствуют основания.
К
ним относятся
только оксиды
металлов
(за исключением тех, которые относятся
к кислотным, то-есть
с валентностью металла 4 и больше.
НАПРИМЕР: К2О
– КОН Na2O
– NaOH
BaO
– Ba(OH)2
FeO –
Fe(OH)2
Fe2O3
– Fe(OH)3
CrO – Cr(OH)2
Ag2O
– AgOH
ПОМНИТЕ!
Валентность гидроксогруппы
ОН равна 1.
Валентность металла
может быть не
только постоянной, но и переменной.
АМФОТЕРНЫЕ
ОКСИДЫ – это
оксиды, которые проявляют свойства как
основных, так и
кислотных оксидов. К ним относятся
только
некоторые оксиды
металлов –
Al2O3,
ZnO,
BeO,
Cr2O3
(эти оксиды надо запомнить) и ряд других.
Если амфотерный
оксид реагирует с кислотой, то он
реагирует как обычный
основный оксид.
Если же амфотерный оксид реагирует со
щелочью, то в этом
случае он реагирует
как кислотный оксид и ему соответствует
кислота, формулу
которой находим
так же, как и с любым кислотным оксидом,
то-есть прибавляя
Н2О.
НАПРИМЕР:
Al2O3
– Н2Al2O4;
сокращаем на 2, получаем НАlО2.
Если же Al2O3
реагирует с
кислотой, то, естественно, ему соответствует
гидроксид Аl(ОН)3.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #







