Содержание
- Актуальность
- Что такое СКФ?
- Причины изменения скорости клубочковой фильтрации
- Как определить СКФ?
- Норма и отклонения
- Значение СКФ для диагностики заболеваний

Нефрон – это основной элемент, из которого состоят почки. Это своеобразный клубок, состоящий из сосудов и каналов, по которым проходит жидкость. Благодаря нефронам почкам удаётся выполнять свою работу и обеспечивать грамотную деятельность всего организма, так как именно они вместе с мочой удаляют все продукты обмена, скапливающиеся в крови.
Подобное действие гарантирует избавление от большинства вредных веществ и грамотную работу почек, не вызывающих проблем. При этом в кровь через нефроны отправляется очищенная вода.
Происходит всасывание и за 24 часа в сумме нефроны успевают обработать до 120 литров жидкостей.
Актуальность
Скорость клубочковой фильтрации – это, как раз, количество обработанной жидкости. Именно благодаря измерению скорости клубочковой фильтрации или СКФ удаётся узнать, насколько эффективно почки выполняют свою работу и не нужна ли им помощь. Всё дело в том, что при заболевании почек нефроны начинают погибать.
Чем больше их погибает, тем большая нагрузка ложится на оставшихся и тем быстрее погибают они. В результате, почки начинают гораздо хуже справляться со своей работой и в скором времени можно будет на себе ощутить наличие заболевания, от которого срочно требуется избавиться.
Что такое СКФ?

Скорость клубочковой фильтрации – один из наиболее важных показателей, определяющих функционирование почечного аппарата. Если данное значение вышло за пределы нормы, значит в почках появилось какое-то заболевание, от которого нужно избавиться.
Именно поэтому многие нефрологи, после обращения к ним с жалобами на боль в области почек, в первую очередь назначают именно этот анализ, ведь специалисты обладают необходимым опытом, и знают, что анализ крови на СКФ может прояснить картину.
В нормальном состоянии этот показатель должен составлять от 80 до 120 миллилитров в минуту. С возрастом естественные процессы в организме замедляются, и показатель может стать ниже. Если же фильтрационная функция в почках начала давать сбой без каких-либо видимых причин, стоит задуматься.
Важно понимать, что фильтрационная способность почек является одним из важнейших показателей всего организма в целом. Если вредные вещества в моче не будут выводиться из организма, то это станет причиной возникновения заболеваний не только в почках, но и в других органах.
Единицы измерения СКФ складываются из нескольких показателей. Несмотря на то, что ориентиром считается количество миллилитров в минуту, определение этого показателя – сложный процесс, доступный только специалистам.
Диагностика заболевания, в результате которой и возникли подозрения, определяет, каким методом стоит действовать. В большинстве случаев берётся анализ крови, а непосредственным процессом, в результате которого и происходит анализ, является клиренс инсулина.
Клиренс инсулина находится в плазме и спокойно фильтруется, не подвергаясь никаким реакциям. Это позволяет без лишних усилий получить необходимые данные, определив количество функционирующих нефронов функционируют, и их работоспособность. Тем не менее, получение клиренса инсулина подразумевает наличие соответствующего оборудования, которое есть далеко не везде.
Это приводит к дороговизне процесса и появлению ряда альтернативных методик, в том числе и анализу мочи, который, в свою очередь, менее эффективен, но некоторая часть полученных данных позволяет определить общую картину.
Причины изменения скорости клубочковой фильтрации
Скорость клубочковой фильтрации у каждого человека более-менее постоянна. Разумеется, она варьируется в зависимости от обстоятельств, но если нет заболеваний почек, то резких изменений не происходит.
Единственный допустимый процесс, приводящий к уменьшению данного показателя – старение, в результате которого не только этот, но и все естественные показатели становятся ниже.
Причин для изменения клубочковой фильтрации почек несколько, и каждая из них – повод обратиться к специалисту. Если говорить об уменьшении данного показателя, то это:
- Сигнал к проявлению недостаточности в хронической форме. Возможно, заболевание только назревает, а возможно, оно уже появилось.
- Рост в моче концентрации креатинина и мочевины. Иными словами, почки просто начинают не справляться с поставленной задачей и не удаляют все вредные вещества из крови, так как скорость работы клубочков почек снизилась.
- Пиелонефрит. Серьёзное заболевание, определить наличие которого можно далеко не сразу. При пиелонефрите сначала начнут страдать канальцы нефронов и только после этого снизится скорость фильтрации. Вовремя обнаружить проблему можно при помощи анализа мочи по методу Зимницкого.
- Наличие патологических изменений, таких как сердечная недостаточность или снижение артериального давления.
В свою очередь повышение скорости клубочковой фильтрации может быть связано с такими заболеваниями как сахарный диабет, волчанка или гипертензия.
В любом случае, если вы заботитесь о здоровье почек и желаете обеспечить их эффективную работу на долгий срок, не испытывая проблем, рекомендуется регулярно проверять показатели скорости клубочковой фильтрации, чтобы оперативно среагировать на любые возможные изменения.
Как определить СКФ?

Наиболее эффективным вариантом определить скорость клубочковой фильтрации является клиренс инсулина, так как этот элемент позволяет получить наиболее точные значения. Однако определение скорости клубочковой фильтрации подобным методом довольно дорого стоит, поэтому этот расчёт можно проводить и альтернативными методами, такими как:
Проба Ребрга-Тареева. Эта методика позволяет определить скорость клубочковой фильтрации почек благодаря суточному клиренсу креатинина. Чтобы рассчитать необходимые данные, пациент должен собрать всю мочу за 24 часа, что далеко не так просто, как может показаться на первый взгляд.
Среди недостатков метода стоит отметить, что больные с часто меняющимися показателями не получат эффективных результатов. Существуют ситуации, когда клиренс креатинина падает, что также не даёт точного результата. Однако существуют и преимущества: подобный анализ на СКФ можно будет без проблем проводить при наличии беременности, особых диет и в любом возрасте.
Проба Кокрофта. В этом случае скорость фильтрации определяется при помощи специальных измерений, для чего были определены соответствующие формулы.
Подробно ознакомиться с существующими методиками и признаками действия специальных калькуляторов вы сможете, обратившись за помощью к специалисту.
Опытный врач знает, как получить необходимые данные при помощи биохимических и других видов анализов. Если же положиться исключительно на собственные силы, можно не только не добиться необходимого результата, но и серьёзно усугубить ситуацию.
Норма и отклонения

Нормой при клубочковой фильтрации у взрослого здорового человека считается показатель в районе 100 миллилитров в минуту. При этом показатель одинаков как у мужчин, так и у женщин. Значение этой характеристики заключается в количестве жидкости, обрабатываемой почками. Снижение клубочковой фильтрации указывает на тот факт, что в организме возникла проблема, которую необходимо срочно устранить, пока она не перетекла в хроническую форму. Особенно опасно отклонение от нормы у детей, так как в их возрасте данное значение должно стабильно расти.
Как только появилось беспокойство в области почек, следует тут же обратиться к специалисту. Он сможет провести необходимые исследования, определить нормальные значения СКФ и дать подробную расшифровку полученных данных, описывающую текущую ситуацию.
Значение СКФ для диагностики заболеваний
Скорость клубочковой фильтрации – показатель, напрямую влияющий на состояние здоровья. Данное значение характеризуют функцию почек и может говорить о развитии того или иного заболевания, в случае отклонения показателя от нормы. Современная медицина способна точно определить значение СКФ в почках и устранить возможные проблемы.
Существует множество методов диагностики и некоторые из них можно назвать настоящими прорывами в области медицины. Врач может назначить диализ или какие-либо иные процедуры, всё зависит от конкретной ситуации, к каждой из которых найдётся подходящий подход.
Опубликовано: 20.07.2021 11:38:00 Обновлено: 20.07.2021 Просмотров: 370408

Почечная недостаточность – острое или хроническое заболевание, при котором нарушаются фильтрационная, выделительная и другие функции почек с развитием многочисленных сбоев в работе всего организма. При этом происходит отравление собственными токсичными продуктами обмена веществ, попавшими в кровь – уремия. Патология, особенно при стремительном развитии, может угрожать жизни больного и требует скорейшего лечения.
Распространенность хронической болезни почек во всем мире в среднем составляет 13,4%. В России почечная недостаточность встречается у 36% лиц старше 60 лет и у 16% граждан трудоспособного возраста.
Причины
Хроническая форма заболевания чаще всего развивается как осложнение других патологий. Ранее основной причиной почечной недостаточности считался гломерулонефрит. В настоящее же время ведущее место занимают гипертоническая болезнь и сахарный диабет, приводящие к поражению мелких сосудов, питающих почки, и стойкому нарушению кровообращения в них.
Острая почечная недостаточность (ОПН) более чем в половине случаев связана с травмой или перенесенными операциями на органах малого таза. Развивается она также при неправильном приеме лекарственных препаратов, нарушении работы сердца, кровотечениях и шоке, генерализованной аллергической реакции, обезвоживании, циррозе, отравлении, аутоиммунных и инфекционных болезнях, онкологии, переливании несовместимой крови.
Предрасполагают к нарушению работы почек следующие факторы:
- плохая экология;
- особенности питания;
- мужской пол;
- возраст старше 60 лет;
- избыточный вес;
- вредные привычки – табакокурение, злоупотребление алкоголем;
- генетическая предрасположенность;
- прием некоторых медикаментов;
- инфекционные и паразитарные поражения;
- хронические заболевания сердечно-сосудистой (в том числе – повышенное артериальное давление), мочевыделительной и эндокринной систем;
- нарушение жирового обмена, дислипидемия, гиперхолестеринемия, метаболический синдром.
Симптомы почечной недостаточности
Почки не только очищают кровь от токсинов и выводят их из организма, но также регулируют водно-солевой баланс, контролируют уровень артериального давления, тонус сосудов, концентрацию гемоглобина, помогают в сохранении здоровья опорно-двигательного аппарата и сердца. Учитывая такое многообразие функций органа, почечная недостаточность проявляется многочисленными симптомами, выраженность которых зависит от стадии и формы заболевания.
При остром повреждении почек на начальной стадии имеются лишь проявления основного заболевания. Далее следует самая тяжелая, олигурическая стадия, продолжительностью до 3-х недель, со снижением суточного объема мочи менее 500 мл. Первым признаком болезни становится резкое уменьшение или прекращение мочеиспускания.
Состояние часто обратимо (если обратимо основное заболевание или состояние, приведшее к ОПН) и при правильном лечении переходит в полиурическую стадию почечной недостаточности с восстановлением объема мочи. При этом самочувствие пациента нормализуется, но может развиваться обезвоживание организма и присоединиться инфекция. Стадия полного восстановления продолжается от шести месяцев до года. При выраженных нарушениях состояние переходит в хроническую форму.
Хроническая почечная недостаточность (ХПН) развивается медленно, в течение нескольких месяцев и даже лет, и приводит к стойким изменениям в органе. На начальном этапе специфических симптомов обычно не бывает, но иногда человек может заметить снижение объема выделяемой мочи. Либо единственным проявлением патологии может быть никтурия – частое ночное мочеиспускание.
По мере прогрессирования заболевания и присоединения уремии появляются и другие симптомы:
- апатия, общая слабость;
- жажда;
- неприятный вкус во рту;
- расстройство сна;
- ухудшение памяти;
- тошнота.
При отсутствии эффективного лечения присоединяются неврологические расстройства – непроизвольные подергивания мышц, снижение скорости реакций, а также обильная рвота, диарея, одышка, раздражение кожи и слизистых оболочек.
Осложнения
Болезнь осложняется появлением артериальной гипертензии, анемии, перикардита, аритмии и сердечной недостаточности, остеопороза, подагры, энцефалопатии, язвенной болезни желудка и двенадцатиперстной кишки, атеросклероза сосудов с развитием инфаркта и инсульта, синдрома беспокойных ног.
У детей почечная недостаточность приводит к задержке роста костной ткани.
Развитие почечной недостаточности у женщин во время беременности сопряжено с невынашиванием плода или формированием у него врожденных пороков.
Без лечения ХПН может закончиться смертью пациента от сердечно-сосудистых осложнений или уремической комы.
Диагностика
При первичном обследовании врач собирает анамнез заболевания, уточняя жалобы и давность симптомов. Далее проводятся осмотр кожных покровов, пальпация и поколачивание пальцами поясничной области.
Диагноз почечной недостаточности выставляется на основании следующих лабораторных и инструментальных исследований:
- Общий анализ мочи. Метод позволяет установить причину заболевания. Примесь крови, наличие эритроцитов в биоматериале свидетельствуют о мочекаменной болезни, гломерулонефрите, инфекции, новообразовании или травме. Лейкоциты указывают на инфекционный либо аутоиммунный процесс. Также может снижаться плотность мочи, присутствовать белок и восковидные цилиндры в ней.
- Клинический анализ крови. Повышение лейкоцитов и СОЭ говорит об инфекционном процессе, а уменьшение количества эритроцитов и гемоглобина в крови свидетельствует о сопутствующей почечной недостаточности анемии.
- Биохимический анализ крови. Увеличение в сывороточной крови мочевины и креатинина служит основным признаком почечной недостаточности. Эти вещества образуются в процессе распада белков и могут выводиться из организма исключительно с мочой. Прогрессирующий рост концентрации креатинина является главным диагностическим критерием тяжести заболевания. Сахарный диабет – одна из наиболее частых причин ХПН, однако и без эндокринных заболеваний при дисфункции почек есть склонность к умеренному повышению глюкозы в крови. Значительное увеличение уровня калия сопровождает выраженное нарушение функции почек, а высокая концентрация мочевой кислоты характерна для подагры и может привести к развитию мочекаменной болезни. Также в анализах крови при почечной недостаточности часто снижены альбумин, кальций, повышены триглицериды, щелочная фосфатаза, фосфор и холестерин.
- Биопсия почек. В сложных диагностических случаях может осуществляться забор небольшой части почечной ткани, которая подвергается последующему осмотру через микроскоп. Метод позволяет обнаружить характерные гистологические признаки ХПН – замещение клубочков почек рубцовой тканью.
- Ультразвуковое исследование органов малого таза. Важное место в диагностике почечной недостаточности занимает УЗИ почек. При ХПН отмечается их уменьшение (сморщивание) вместе с истончением наружного слоя. Также метод применяется для обнаружения новообразований, камней или кист.
- Компьютерная и магнитно-резонансная томография брюшной полости. Более точный способ визуализации опухолей, кист и конкрементов размером даже менее 5 мм.
Лечение почечной недостаточности
Обязательно проводятся диагностика и лечение патологии, послужившей причиной почечной недостаточности, а также устранение факторов риска.
Важную роль в терапии заболевания играют общие мероприятия, направленные на сохранение функции пораженного органа:
- Ограничение потребления жидкости.
- Отказ от приема ряда медикаментов.
- Коррекция питания. Диета при почечной недостаточности предполагает ограничение продуктов и напитков с повышенным содержанием натрия, фосфора, калия. Это поваренная соль, молочные продукты, печень, бобовые, орехи. Количество потребляемого белка также строго дозируется.
Консервативное лечение почечной недостаточности назначается врачом по результатам анализов. Для восстановления водно-солевого баланса внутривенно через капельницу вводятся специальные растворы. При задержке жидкости могут применяться мочегонные препараты. Также проводится терапия средствами, улучшающими кровообращение в органах малого таза, препаратами эритропоэтина, витамином D.
При выраженном или длительном нарушении фильтрационной функции почек пациенту показано аппаратное очищение крови – гемодиализ. Процедура проводится регулярно и позволяет убрать из организма токсичные вещества. Альтернативой выступает перитонеальный диализ, при котором в брюшную полость вводится с последующим удалением специальный раствор, забирающий на себя вредные вещества.
В случае тяжелого течения хронической почечной недостаточности выполняется операция по трансплантации почки. После пересадки проводится курс терапии препаратами, подавляющими иммунитет, чтобы не произошло отторжения донорской ткани.
Дата публикации 25 марта 2022Обновлено 12 декабря 2022
Определение болезни. Причины заболевания
Хроническая болезнь почек (ХБП, chronic kidney disease) — это комплекс симптомов, которые развиваются при прогрессирующих заболеваниях почек и присутствуют не меньше трёх месяцев. Такие симптомы возникают на фоне постепенной и необратимой гибели нефронов — структурных единиц почки [15].
Раньше эту болезнь называли хронической почечной недостаточностью (ХПН), но сейчас таким термином обозначают только тяжёлую стадию заболевания.
Проявления ХБП зависят от степени поражения почек. Вначале симптомов может не быть и пациента беспокоят только признаки основного заболевания, например высокое артериальное давление. Позже пациенты отмечают, что участилось мочеиспускание по ночам, повысилось артериальное давление или привычные препараты для его снижения перестали действовать. Типичные признаки терминальной, или конечной, стадии ХБП — резкая слабость, запах аммиака изо рта, сухость и зуд кожи [3][16].
Распространённость ХБП
Хронической болезнью почек страдает около 13 % людей в мире [3]. Данные одинаковы для стран с высоким уровнем жизни и для развивающихся стран. При этом с каждым годом таких пациентов становится больше на 10 %. ХБП встречается практически так же часто, как гипертония, сахарный диабет, метаболический синдром и ожирение. Те или иные признаки повреждения почек обнаруживают у каждого 10-го пациента [3][4].
У детей частота развития терминальной стадии болезни зависит от возраста: чаще всего она встречается в 15–19 лет, но может возникнуть и у детей младше 5 лет. ХБП II–V стадии чаще выявляют у мальчиков. Вероятно, это связано с большей распространённостью среди них врождённых патологий мочевыделительной системы, например обструктивной уропатии и дисплазии почки [5].
Факторы риска ХБП
Термин ХБП объединяет в себе поражения почек, вызванные инфекционными, атеросклеротическими, аутоиммунными и другими причинами [3].
Факторы риска развития хронической болезни почек подразделяют на модифицируемые и немодифицируемые, т. е. на те, на которые повлиять можно, и на которые нельзя.
К немодифицируемым факторам относят пожилой возраст, наследственную предрасположенность, врождённое низкое количество нефронов, например при дефиците веса при рождении, перенесённое острое повреждение почек, расовые и этнические факторы.
Модифицируемые факторы включают гипертонию, сахарный диабет, табакокурение, токсическое воздействие лекарств, хронические воспаления или системные инфекции, обструкцию мочевыводящих путей, беременность и высокое потребление белка [14].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы хронической болезни почек
Вначале ХБП можно диагностировать только по наличию в моче белка, чаще альбумина. При этом наблюдаются признаки основного заболевания: повышенное давление, высокий уровень глюкозы в крови и т. д.
В дальнейшем усиливается образование мочи (полиурия), её суточный объём достигает 2–3 литров. Больной чаще мочится, но, в отличие от симптома учащённого мочеиспускания, каждый раз отделяется много мочи. Также отмечается никтурия — два и более ночных позывов к мочеиспусканию. При этом ночью выделяется больше мочи, чем днём.
Полиурия и никтурия, особенно в сочетании с анемией, должны насторожить в отношении возможной ХБП [1]. Заподозрить её также можно при появлении отёков на лице, руках или стопах, постоянной жажде, общей слабости, плохом аппетите и повышенном артериальном давлении. С прогрессированием заболевания снижается вес, нарастает слабость и ухудшается работоспособность. Гипертония при этом становится неконтролируемой, т. е. лекарства перестают помогать.
На поздних сроках заболевания выделение мочи сильно снижается, вплоть до полного отсутствия на конечной стадии. Пациенты становятся вялыми и заторможенными. Часто жалуются на выраженную слабость, тошноту, сухость и неприятный вкус во рту, отвращение к пище, особенно мясной, желтушность, бледность и сероватый оттенок кожи, кожный зуд, зябкость и судороги в икроножных мышцах. Повышенное артериальное давление сменяется гипотонией, могут болеть суставы, кости и позвоночник, возникает ощущение жжения и ползания мурашек в ногах [1][2][8].
Все симптомы ХБП, за исключением изменения количества выделяемой мочи, неспецифические. Они встречаются при заболеваниях, которые приводят к развитию ХБП, например при гипертонии или сахарном диабете. Поражение почек при наличии таких симптомов можно заподозрить, когда возникает боль и дискомфорт в пояснице, изменяется цвет мочи — она становится красной, бурой, пенистой, содержит хлопья и осадок.
Патогенез хронической болезни почек
Нефроны состоят из маленьких фильтров, называемых клубочками, которые фильтруют жидкость. Белки и клеточные элементы крови остаются в крови, а отфильтрованная первичная моча выводится по небольшим трубочкам.
Несмотря на многообразие причин, вызывающих ХБП, морфологические изменения в почках при этом одинаковы. При болезнях почек количество действующих нефронов уменьшается, из-за чего ускоряется и повышается объём фильтруемой крови в единицу времени. Кроме того, давление в клубочках оставшихся нефронов увеличивается, из-за чего усиливается проницаемость капилляров и растёт уровень альбумина в моче. Этот белок может откладываться в межкапиллярном пространстве клубочка. В результате оно расширяется и в нём накапливается плотный, похожий на хрящевую ткань, белок гиалин. В дальнейшем нефроны замещаются соединительной тканью и почка сморщивается — порочный круг замыкается.
Снижение количества здоровых нефронов приводит к тому, что почки не успевают выводить конечные продукты азотистого обмена, такие как креатинин, мочевина, мочевая кислота, аммиак и др. Это приводит к уремии, которая проявляется слабостью, апатией, отсутствием аппетита, тошнотой, рвотой, зудом кожи и отвращением к пище, особенно к мясу.
К уремическим токсинам относят также паратиреоидный гормон. Его повышенная выработка сначала позволяет снизить уровень кальция и повысить содержание фосфора, т. е. скорректировать нарушения, свойственные уремии. Затем этого гормона становится слишком много, и он превращается в токсичное вещество, которое усиливает уремию.
В дальнейшем избыток паратгормона приводит к почечной остеодистрофии, при которой:
- костная ткань становится пористой и хрупкой, возникают деформации и переломы костей;
- повышается уровень триглицеридов;
- усиливается анемия;
- соли кальция откладываются в тканях, в том числе в миокарде и сердечных клапанах [1][10].
Оставшимся здоровым нефронам приходится выводить в минуту гораздо больше веществ. При этом возникает полиурия и никтурия — повышается объём мочи и учащаются позывы к мочеиспусканию по ночам.
Даже при значительном снижении скорости клубочковой фильтрации почки способны поддерживать образование и выведение мочи (диурез). Это достигается за счёт изменения концентрации мочи — способности почек выводить необходимое количество электролитов и органических веществ. Относительная плотность мочи при этом снижается до плотности безбелкового фильтрата плазмы (1010–1012 г/л). В результате конечные продукты обмена и электролиты задерживаются в крови и симптомы уремии нарастают [1][4].
В норме почки способны выводить столько натрия, сколько потребляет человек. При прогрессировании ХБП натрий хуже фильтруется почечными клубочками и плохо выводится с мочой. Но может возникать и другая ситуация: способность почки к обратному захвату натрия резко падает, из-за чего его концентрация в моче снижается. В этом случае развивается солевое истощение с резкой гипотонией, выраженной слабостью и быстрым прогрессированием ХБП.
На поздних стадиях ХБП из-за выраженного снижения диуреза и низкой скорости клубочковой фильтрации уровень калия в крови увеличиваться до 5 ммоль/л. Такое состояние называют гиперкалиемией. В некоторых случаях, например при диабетической нефропатии и тубулоинтерстициальных заболеваниях почек, гиперкалиемия проявляется раньше. Усиливать её могут инфекции, травмы, повышенная температура и приём калийсберегающих мочегонных средств (Спиронолактона, Триамтерена, Амилорида) [1].
При гиперкалиемии ухудшается проведение электрических импульсов по нервно-мышечным клеткам, что может привести к параличу и замедлению сердцебиения, вплоть до полной остановки сердца.
Классификация и стадии развития хронической болезни почек
В Международной классификации болезней (МКБ-10) ХБП кодируется как N18. Она выделена в отдельную нозологическая форму из-за того, что механизм поражения почек, факторы прогрессирования болезни и меры профилактики схожи при различных заболеваниях [3].
Классификация ХБП основана на изменении скорости клубочковой фильтрации (СКФ) — объёма жидкости, отфильтрованного из почечных клубочковых капилляров в капсулу за единицу времени.
Стадии ХБП по СКФ:
- I — нормальная или повышенная СКФ (≥ 90 мл/мин.);
- II — незначительно сниженная СКФ (60–89 мл/мин.);
- IIIа — умеренно сниженная СКФ (45–59 мл/мин.);
- IIIб — существенно сниженная СКФ (30–44 мл/мин.);
- IV — резко сниженная СКФ (15–29 мл/мин.);
- V — терминальная почечная недостаточность (СКФ ˂ 15 мл/мин.) [3][13].
Признаки поражения почек присутствуют на всех стадиях, начиная с самой первой.
Кроме хронической, выделяют ещё острую болезнь почек (или острую почечную недостаточность, как её называли раньше). При острой форме симптомы развиваются стремительно, но чаще всего это состояние обратимо в течение трёх месяцев. Если выздоровление за этот период не произошло, то почка погибает [3].
Стадии ХБП по клинической картине:
- I стадия — начальная (или латентная). Усиливается образование мочи, у половины пациентов повышается артериальное давление, может наблюдаться небольшая анемия. Скорость клубочковой фильтрации составляет 40–80 мл/мин. Эта стадия примерно соответствует II–IIIа стадии предыдущей классификации [6].
- II стадия — консервативная. У пациентов продолжает усиленно образовываться моча, повышено давление, появляются ночные позывы к мочеиспусканию. Анемия нарастает до умеренной, уровень креатинина в крови повышается до 145–700 мкмоль/л. Скорость клубочковой фильтрации составляет 10–40 мл/мин. Консервативная стадия примерно соответствует IIIб–IV стадиям ХБП по СКФ.
- III стадия — терминальная. Усиленное образование мочи сменяется резким снижением. Выражена анемия, повышен уровень фосфатов, калия, натрия и магния. Содержание креатинина превышает 700–800 мкмоль/л. Скорость клубочковой фильтрации составляет менее 10 мл/мин. Соответствует V стадии классификации по СКФ [6][8].
Осложнения хронической болезни почек
Хроническая болезнь почек приводит к сердечно-сосудистым осложнениям, дефициту витамина D, патологиям костной системы и множеству других осложнений.
Осложнения со стороны сердечно-сосудистой системы:
- Задержка натрия у 80 % пациентов приводит к артериальной гипертензии, которая может протекать длительно, плохо поддаваться терапии, вызывать поражение сетчатки, головного мозга, почек и сердца. Гипертония также может привести к инсульту, энцефалопатии, судорожным припадкам, ретинопатии (поражению сетчатки глаза, оболочки сосудов и зрительных нервов). Кроме того, артериальная гипертензия в сочетании с анемией и другими патологическими факторами вызывает перегрузку левых отделов сердца и гипертрофию миокарда левого желудочка [1][3][9].
- На фоне повышенного выведения белка с мочой, изменения инсулинового обмена и высокого уровня паратиреоидного гормона растёт содержание атерогенных фракций липидов: триглицеридов, аполипопротеинов В и др. В результате развивается атеросклероз коронарных артерий, они не полностью обеспечивают кровью увеличенный миокард и возникают инфаркты.
- В терминальных стадиях ХБП может развиваться выпотной или фибринозный перикардит. Сердечная мышца при этом сдавливается, что служит дополнительным фактором развития хронической сердечной недостаточности.
У больных с ХБП нарушается синтез гормонально-активного витамина D (кальцитриола). Это вещество образуется в почечной ткани, его дефицит нарастает по мере сморщивания почек. В сочетании с высоким уровнем кальция и фосфатов дефицит витамина D приводит к вторичному гиперпаратиреозу — заболеванию паращитовидных желёз. Этим тяжёлым осложнением страдает 30 % пациентов на гемодиализе [10].
Повышение паратиреоидного гормона нарушает работу многих органов. Отложения кальция в клапанах сердца, его проводящей системе, в сердечных и несердечных сосудах способствуют возникновению кардиомиопатии, прогрессированию атеросклероза, гипертонии и сердечной недостаточности [10].
Осложнения со стороны костной системы, связанные с гиперпаратиреозом, сильнее выражены у детей. У них может развиваться почечный рахит, который протекает как и обычный рахит. В фалангах пальцев, длинных костях и отдалённых от центра концах ключиц возникают поднадкостничные эрозии, костная ткань рассасывается и разрушается, костный мозг перерождается и заменяется на соединительную ткань. Часть костной ткани уплотняется, и развивается остеосклероз. На фоне этих нарушений учащаются переломы костей, чаще рёбер и шейки бедра.
К осложнениям ХБП также относят анемию, ацидоз и гипоальбуминемию. На первых стадиях ХБП анемией страдает 4–8 % пациентов, с развитием болезни — до 50–80 % [3].
Гипоальбуминемия возникает из-за потери альбумина с мочой, снижения поступления белка в организм на фоне потери аппетита и нарушения всасывания белка в ЖКТ, а также повышенного распада белка. В результате развивается белково-энергетическая недостаточность.
Повышенный распад белков усиливает метаболический ацидоз — увеличение кислотности крови. Ацидоз приводит к тахикардии, аритмии, фибрилляции желудочков, сердце начинает хуже сокращаться [3][19].
В терминальной стадии болезни почки практически перестают выделять мочу и в крови сохраняются уремические токсины: мочевина и креатинин. Задержка токсинов вызывает тошноту, рвоту, кожный зуд, иногда мучительный, ощущение жжения и ползания мурашек, подкожные кровоизлияния, кровотечения из носа, дёсен, матки и желудочно-кишечного тракта. Рвота бывает длительной, часто возникает повторно и плохо поддаётся лечению. Она вызывает обезвоживание и препятствует приёму пищи, из-за чего снижается вес [1][2].
Диагностика хронической болезни почек
Для постановки диагноза врач собирается анамнез и проводит осмотр. Полученная информация позволяет заподозрить болезнь на ранних стадиях [3]. Затем пациенту нужно будет сдать анализы мочи, крови и пройти инструментальную диагностику.
Сбор анамнеза
Врач-терапевт или нефролог обращает внимание на следующие симптомы: частые позывы к мочеиспусканию, особенно ночью, изменение цвета мочи или появление в ней посторонних примесей, отёки и боли в поясничной области.
Врач уточняет:
- когда появились эти симптомы;
- как долго они наблюдаются;
- страдает ли пациент болезнями, которые относятся к факторам риска ХБП, например сахарным диабетом или гипертонией;
- какие препараты принимает пациент.
На ранних стадиях ХБП может протекать с крайне слабыми симптомами или совсем без них. Поэтому диагноз устанавливают по данным лабораторных исследований.
Анализ крови
При подозрении на ХБП и при наличии факторов риска, даже если нет симптомов, необходимо оценить уровень креатинина и скорость клубочковой фильтрации. Эти показатели определяют по биохимическому анализу крови. Его сдают натощак: перед сдачей анализа нельзя есть 8 часов.
Один из клинических синдромов ХБП — это нарушение водно-электролитного баланса. На начальных стадиях уровень калия в крови снижается, на поздних стадиях — возрастает.
Содержание натрия в крови может долго оставаться нормальным, вплоть до развития терминальных стадий. С ухудшением работы почек у одних пациентов уровень натрия в крови снижается, у других он, наоборот, задерживается в организме. В первом случае возникает слабость и снижается давление, во втором — развивается натрий-зависимая гипертония [1][3][8].
При ХБП часто наблюдается нормоцитарная, нормохромная анемия, т. е. снижается именно число эритроцитов, при этом их размер и содержание в них гемоглобина остаётся нормальным.
Анализы мочи
При подозрении на ХБП следует контролировать уровень протеина, альбумина и эритроцитов в суточной или утренней моче [2].
Маркеры повреждения почек по анализу мочи:
- появление белка;
- избыток альбумина;
- наличие лейкоцитов и эритроцитов.
Проводится общий анализ мочи с микроскопией осадка, анализ мочи на микроальбуминурию и определение белка в суточной моче. Из-за сниженной способности почек к концентрации мочи увеличивается её суточный объём. При этом относительная плотность мочи в течение дня не изменяется, а в дальнейшем плотность мочи снижается и не превышает 1008 г/л.
Чтобы определить количество суточной мочи, её относительную плотность, а также выявить динамику этих показателей в течение суток, проводится анализ мочи по Зимницкому. Для этого пациенту нужно собрать восемь порций мочи через каждые три часа в разные контейнеры. Хранить пробы необходимо в холодном месте.
Рентгенография и УЗИ почек
Эти исследования позволяют определить размер почек. Обычно на поздних стадиях они уменьшаются, их ткань уплотняется. Нормальные размеры почки при нарастающей ХБП могут указывать на обострение патологического процесса. В таких случаях при правильном лечении можно добиться улучшения работы почек.
Ультразвуковое исследование также позволяет увидеть очаговые изменения: опухоль, абсцесс, нефролитиаз и туберкулёз почки [1].
Биопсия
С помощью биопсии можно определить причины поражения почки и её тяжесть, а также подобрать лечение. Это исследование показано, если у пациента с ХБП более чем в 2 анализах мочи на протяжении 3 месяцев определяется белок и кровь. Также биопсию проводят при снижении скорости клубочковой фильтрации, которую невозможно объяснить клиническими данными.
Дифференциальная диагностика
Следует различать хроническую и острую почечную недостаточность. Оба состояния сопровождаются повышением уровня креатинина и снижением скорости клубочковой фильтрации, но при острой почечной недостаточности изменения происходят быстро, а при хронической форме болезни — постепенно.
Лечение хронической болезни почек
При ХБП нужно лечить основное заболевание, которое вызвало развитие болезни почек. Кроме того, обязательно применяются препараты, влияющие на различные звенья патогенеза. Такое комбинированное лечение позволяет затормозить развитие терминальной почечной недостаточности [3].
Диета при ХБП
Лечение ХБП начинается с диеты. Пациентам следует снизить потребление белка в сутки до 0,6–0,5 г/кг, при тяжёлой ХБП (СКФ 10–25 мл/мин) — до 0,25–0,3 г/кг.
Много белка содержится в мясе, рыбе, сыре, твороге, орехах и бобовых. К низкобелковым продуктам относятся овощи, фрукты, рис, мёд, сливочное и растительное масло [3][14].
Низкобелковая диета позволяет уменьшить симптомы и скорость развития уремии.
Если по анализу крови содержание калия более 5 ммоль/л, нужно ограничить его потребление до 2–3 г/сут. Также рекомендуется снизить поступление с пищей фосфатов. Воду можно пить почти без ограничений, но её количество не должно превышать суточный диурез более чем на 500 мл.
Пациентам с гипертонией и/или признаками задержки натрия нужно ограничить соль до 5 г/сут. Необходимо исключить из рациона соленья, маринады, копчёности, колбасы и т. д. Также следует есть меньше жирной, жареной пищи и продуктов с рафинированными сахарами (конфеты, выпечку).
Лечение артериальной гипертензии
Оптимальное артериальное давление (АД) у пациентов с ХБП — меньше 135–140/80–85 мм рт. ст. При концентрации белка в моче 1 г/сут. и более АД должно быть меньше 130/80 мм рт. ст.
Лечение гипертонии при ХБП должно быть длительным и непрерывным. Необходимо сочетать лекарства разных групп: диуретики и препараты, блокирующие активность РААС (ренин-ангиотензин-альдостероновой системы).
Диуретики. У 80 % пациентов с ХБП давление повышается из-за задержки натрия [1]. Чтобы вывести натрий и избыточную жидкость, а также снизить давление, применяют салуретики (разновидность диуретиков, или мочегонных средств): Фуросемид, Этакриновую кислоту и др. Эти препараты повышают скорость клубочковой фильтрации, выводят натрий и калий.
На начальных стадиях хронической болезни почек с осторожностью могут применяться тиазидные диуретики (например, Гипотиазид) и калийсберегающие диуретики (Спиронолактон, Верошпирон, Триамтерен). При развитии ХПН (СКФ ˂ 30 мл/мин) их не применяют совсем или назначают в комбинации с петлевыми диуретиками.
При V стадии ХБП рекомендуется не менее трёх месяцев применять калийсберегающие диуретики. Они снижают риск развития инфаркта, инсульта и других острых сердечно-сосудистых заболеваний. При этом нужно тщательно следить за уровнем калия в крови [3].
Диуретики могут усугублять нарушения пуринового и фосфорно-кальциевого обмена и ускорять развитие гиперпаратиреоза. Поэтому при постоянном приёме необходимо контролировать не только объём циркулирующей крови и электролиты, но и уровень мочевой кислоты, кальция, паратиреоидного гормона и кальцитриола в крови [1][8][13].
Препараты, блокирующие активность РААС (ренин-ангиотензин-альдостероновой системы). Учитывая активацию ренина и повышение в плазме альдостерона, применяются следующие лекарства:
- β-блокаторы (Пропранолол, Метопролол, Пиндолол и др.);
- ингибиторы АПФ (Эналаприл, Рамиприл, Фозиноприл и др.);
- блокаторы АТ1-рецепторов ангиотензина (Валсартан, Лозартан и др.);
- блокаторы кальциевых каналов (Верапамил, Нифедипин, Дилтиазем и др.) — всё чаще применятся для лечения почечной артериальной гипертензии; они не ухудшают почечный кровоток, а в ряде случаев способны увеличивать клубочковую фильтрацию [1][2][3][13].
В соответствии с Федеральными клиническими рекомендациями по диагностике и лечению ХБП 2021 года, ингибиторы АПФ и блокаторы АТ1-рецепторов ангиотензина назначаются при ХБП III–V стадии независимо от наличия артериальной гипертензии и сахарного диабета. Эти препараты позволяют уменьшить содержание белка в моче, замедлить нарушение работы почек, снизить риски сердечно-сосудистых заболеваний. Если нет противопоказаний, препараты можно применять постоянно [3].
Другое медикаментозное лечение
При ХБП также необходимо:
- Нормализовать фосфорно-кальциевый обмен. Для этого нужно ограничить содержание фосфатов в пище, принимать фосфат-связывающие вещества (Карбонат или Ацетат кальция, гидроксид алюминия) и препараты активированного витамина D (Кальцитриол, Парикальцитол и др.).
- Корректировать метаболический ацидоз, ежедневно вводя гидрокарбонат натрия или карбонат кальция.
- Лечить анемию. При снижении гемоглобина до 90–100 г/л рекомендуется принимать лекарства, стимулирующие образование эритроцитов (Эпоэтин бета, Эпоэтин альфа и др.) и препараты железа [3][4][13].
- Нормализовать углеводный и липидный обмен. Применяются препараты, снижающие сахар (бигуаниды, производные сульфонилмочевины и др.). Если достичь оптимального уровня глюкозы не удаётся, добавляют инсулин. При повышенном уровне липидов могут применяться статины или фибраты.
Лечение терминальной стадии ХБП
При V стадии ХБП потребуется заместительная почечная терапия: гемодиализ или перитонеальный диализ. При СКФ ≤ 6 мл/мин. диализ проводится обязательно независимо от наличия симптомов. При СКФ 10–15 мл/мин. диализ может быть назначен пожилым пациентам и детям до 18 лет.
Во время диализа кровь пропускают через избирательно проницаемую мембрану и удаляют уремические токсины, избыток воды, натрия и калия.
Детям может быть назначен как гемодиализ, так и перитонеальный диализ. Перитонеальный диализ считается предпочтительным методом для детей, поскольку он безболезненный, легче переносится, может проводиться родителями дома. Осложнения, связанные с катетером, как правило, не опасны для жизни. Но перитонеальный диализ противопоказан при гнойном процессе, опухолях, спайках в брюшной полости, перитоните, негерметичности брюшной полости (илеостоме, дренажах и т. д.) [5].
Гемодиализ не проводят при дефиците массы у младенцев и невозможности сформировать доступ с адекватным потоком крови. Также процедура противопоказана при сердечно-сосудистой недостаточности и повышенной кровоточивости.
Прогноз. Профилактика
ХБП может нарастать с различной скоростью или внезапно, иногда даже без лечения, переходить в стадию ремиссии. Также неожиданно под влиянием инфекции, обезвоживания (например, из-за поноса и рвоты) или травмы болезнь может очень быстро, буквально за несколько дней, привести к гибели пациента.
ХБП быстрее прогрессирует у мужчин, причины этого до конца не ясны [3][11][12].
Ожидаемая продолжительность жизни пациентов в возрасте 44 лет составляет 7,1–11,5 лет, в возрасте 60–64 лет — 2,7–3,9 лет. Однако прогноз во многом зависит от характера основного заболевания, его прогрессирования, стадии ХБП и проводимого лечения [10].
Пациенты погибают в основном не от почечных причин, а от других заболеваний: сердечно-сосудистых осложнений (инфаркта миокарда, инсульта, хронической сердечной недостаточности), сахарного диабета и артериальной гипертензии [3][20]. Самая частая причина смерти при ХБП — это сердечно-сосудистые заболевания. От них умирает 40–60 % пациентов [9][11].
Профилактика хронической болезни почек
Для профилактики ХБП нужно устранить или уменьшить воздействие факторов риска. Для этого следует бросить курить, снизить избыточный вес, корректировать повышенный уровень глюкозы и лечить гипертонию.
Чтобы замедлить развитие ХБП, необходимо:
- лечить заболевания почек, например пиелонефрит и гломерулонефрит;
- своевременно хирургически устранять обструкцию мочевыводящих путей и стеноз почечных артерий;
- проводить адекватную терапию тонзиллита, ангины, бронхита, периодонтита, рожистого воспаления и инфекций кожи на месте расчёсов.
При развитии ХБП на фоне других заболеваний, например сахарного диабета и гипертонии, пациенты должны наблюдаться совместно эндокринологом или кардиологом с нефрологом. Частота осмотров зависит от стадии ХБП и уровня концентрации белка в моче. Врача нужно посещать раз в год на I стадии ХБП и не меньше одного раза в шесть недель на IV–V стадиях. Чтобы своевременно назначить заместительную почечную терапию, пациенты с IV–V стадиями должны наблюдаться нефрологом диализного центра [3].
Фильтрация мочи в почках
Содержание
- Что собой представляет?
- От чего зависит скорость клубочковой фильтрации почек?
- Когда нужна диагностика?
- Патологические причины повышения или снижения
Характеристика, отражающая деятельность выделительной системы, называется «клубочковая фильтрация почек». Она выявляет способность крови очищаться от вредных и ненужных веществ путем выделения первичной мочи. Этот процесс зависит от скорости кровотока и наличия функционирующих нефронов.

Что собой представляет?
Клубочковая фильтрация — это один из показателей функции почек, а изменение ее скорости является признаком патологических изменений в клубочках, их повреждения или функционального отклонения. Клубочек мелких капилляров и канальцевого аппарата является структурной единицей нефрона — почечной клетки. Благодаря ему из организма выводятся вредные вещества и продукты обмена, которые находятся в кровяном русле. В почках происходит два процесса — фильтрация и обратное всасывание или реабсорбция. Именно скорость и качество этих процессов являются показателями общего состояния организма. На этапе клубочковой фильтрации формируется первичная моча.
От чего зависит скорость клубочковой фильтрации почек?
Фильтрационная функция почек определяется множеством показателей. В первую очередь это скорость протекания крови в органе, который зависит от состояния сосудистого русла, его проходимости. Уровень жидкости в сосудах определяет фильтрационное давление, в случае когда оно ниже чем необходимо, процесс фильтрации не происходит. Огромное значение имеет количество способных к функционированию нефронов. Если их масса значительно снижена, орган не сможет нормально функционировать. С возрастом под влиянием различных физиологических факторов скорость выделения мочи в нефроне несколько снижается.
Элементы крови фильтруются в клубочке почки со скоростью 80—125 мл/мин.
Когда нужна диагностика?
Определять скорость, с которой компоненты отсеиваются из крови в парном органе нужно, если у пациента наблюдаются гнойно-воспалительные процессы, а также при различных серьезных хронических заболеваниях. Недостаточность работы почек бывает после шока, обширной кровопотери или в результате обезвоживания. Поэтому если присутствует подобного рода патология, нужно обязательно делать анализ на СКФ мочи. Если уровень фильтрационной способности клубочков подает ниже 60, это главный признак развивающейся почечной недостаточности.
Проводимые анализы
Для определения этого показателя проводят анализ мочи по формуле MDRD. Кроме этого, проводят исследование на клиренс креатинина, который также поможет выявить нарушение почечного кровотока. Для этого анализа используют две различные пробы. Если норма при проведении одной из них не соблюдается, то для достоверности результатов проводят еще одну. Отклонение может иметь физиологические причины, таким образом, когда организм стареет, количество функционирующий нефронов в нем уменьшается, а повышает скорость клубочковой фильтрации употребление белка в больших объемах.
СКФ по формуле MDRD
Этот анализ учитывает пол и возраст человека, поэтому является очень точным. Чаще применяется для диагностики процесса выработки первичной урины у беременных. Для определения показателя нужно знать количество креатинина в крови, а получившееся значение нужно разделить на 1000. Однако если повысить уровень фильтрации значительно, то результаты исследований будут недостоверными.
Проба Реберга-Тареева

Поможет выявить нарушение в почечном кровотоке путем исследования уровня клиренса креатинина, выработанного организмом человека. Он представляет собой объем крови, из которого почки могут изъять 1 мг креатинина в течение 1 минуты. Этот анализ проводят в плазме крови и в урине. Кроме этого, для правильного расчета результатов требуется измерить диурез минутный. На основе этих данных вычисляется скорость клубочковой фильтрации.
Анализ Кокрофта-Голда
При этом анализе забор биологического материала для исследования проводится утром в отличие от предыдущего, однако, имеет с ним много общего. Для достоверности результатов пациент с утра и натощак пьет 2 стакана воды, что запустит выработку мочи. Первое мочеиспускание во время этого теста не используется, так как является результатом работы почек ночью. Забор мочи осуществляется не раньше, чем через час после выпитой воды. А также собирается урина от следующего мочеиспускания. Еще больному производится забор крови из вены. Это позволяет в точности определить 2 показателя, необходимые для расчетов скорости фильтрации почек.
Нагрузочные пробы
В их основе стоит выявление способности почек при необходимости ускорять свою работу, используя резерв почечной функциональной способности и клубочковой фильтрации. Для этого применяется большая нагрузка белками, чаще аминокислотами. Иногда применяют введение «Допамина». Белковая нагрузка состоит в изменении рациона с увеличением количества мяса и яиц. У здорового человека норма СКФ значительно возрастет, так как весь белок фильтруется. Но если наблюдается повышенная проницаемость сосудистого фильтра, то клубочковая фильтрация не поменяется.
Патологические причины повышения или снижения
Заболевания, поражающие паренхиму, способны нарушить уровень клубочковой фильтрации.

Падение показателя означает ухудшение функциональной способности почек и наблюдается при хроническом гломерулонефрите или почечной недостаточности. Такое явление обнаруживается при воспалительных заболеваниях почек, в том числе аутоиммунной природы. Вызвать его могут нарушение обмена веществ, сахарный диабет, амилоидоз или другие нефропатии.
Оценка статьи:




 (пока оценок нет)
(пока оценок нет)
![]() Загрузка…
Загрузка…
Похожие публикации
Распространенность ренальной дисфункции сегодня сопоставима с такими социально значимыми заболеваниями, как артериальная гипертензия и сахарный диабет, а также с ожирением и метаболическим синдромом. Признаки повреждения почек и/или снижение скорости клубочковой фильтрации обнаруживают как минимум у каждого десятого представителя общей популяции. При этом на ранних стадиях заболевание малосимптомно. А позднее выявление ограничивает возможности в лечении — линией спасения таких пациентов становится заместительная почечная терапия.

 В минувшем году в Беларуси количество впервые выявленных пациентов с терминальной хронической почечной недостаточностью составило 83 (годом ранее — 58), согласно данным доклада руководителя Республиканского центра нефрологии, почечно-заместительной терапии и трансплантации почки Олега Калачика на республиканском совещании по итогам работы нефрологической службы Беларуси за 2021 год.
В минувшем году в Беларуси количество впервые выявленных пациентов с терминальной хронической почечной недостаточностью составило 83 (годом ранее — 58), согласно данным доклада руководителя Республиканского центра нефрологии, почечно-заместительной терапии и трансплантации почки Олега Калачика на республиканском совещании по итогам работы нефрологической службы Беларуси за 2021 год.
Хроническая болезнь почек (ХБП) — это персистирующее в течение трех месяцев или более поражение почек вследствие действия различных этиологических факторов (см. табл. 1).
Таблица 1. Основные признаки или маркеры, позволяющие предполагать наличие ХБП.
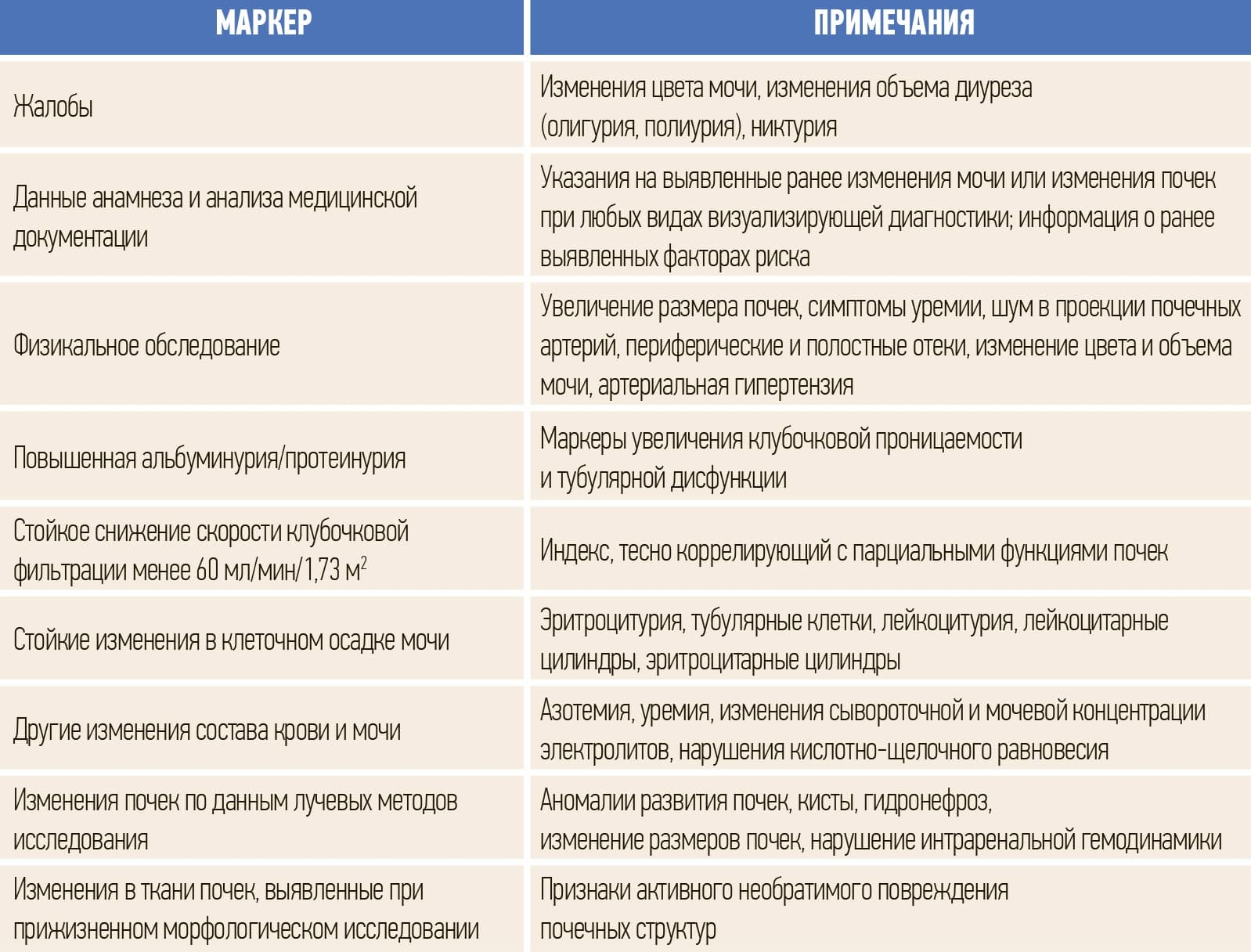
ХБП признана ООН патологией особого внимания как один из индикаторов достижения глобальных целей по сокращению преждевременной смертности от неинфекционных заболеваний к 2030 году.
В отделении нефрологии ГрУК на лечении в 2021 году находились 539 пациентов (в 2020 году — 315) с ХБП 3–5-й стадии. Среди причин, приведших к развитию ХБП, выделяются:
- хронический тубулоинтерстициальный нефрит — 188;
- хронический нефритический синдром — 118;
- сахарный диабет — 114;
- поликистоз почек — 39;
- артериальная гипертензия — 38;
- мочекаменная болезнь — 24.
Таким образом, широко распространенные причины вторичного повреждения почек — сахарный диабет, артериальная гипертензия, метаболические нарушения. В связи с этим понятным и логичным является алгоритм ведения нефрологических пациентов: ранний скрининг ХБП, коррекция факторов риска, изменение в лечении коморбидных состояний с учетом нарушенной скорости клубочковой фильтрации (СКФ), назначение нефропротективной терапии и динамическое наблюдение за пациентом.
К настоящему времени ХБП признана существенным фактором риска сердечно-сосудистой заболеваемости и смертности.
Взаимоотношения дисфункции почек и изменений сердечно-сосудистой системы носят многогранный характер и выстраиваются по типу обратной связи. С одной стороны, почка может выступать как орган-мишень для действия большинства известных факторов, связанных с сердечно-сосудистыми изменениями. С другой стороны, она может активно вмешиваться в формирование системных метаболических и сосудистых патологических процессов, являясь генератором и традиционных, и нетрадиционных факторов риска, тем самым замыкая сложный патогенетический круг, определяющий судьбу пациентов.
Подобный взгляд на взаимообусловленность патологических процессов в сердечно-сосудистой системе и почках, двунаправленность действия факторов риска, клиническая предсказуемость конечных результатов такого сочетания, с одной стороны, позволяет представлять данные взаимоотношения как непрерывную цепь событий, составляющих кардиоренальный континуум, а с другой — открывает дополнительные перспективы первичной и вторичной профилактики не только сердечно-сосудистых заболеваний, но и ХБП.
По данным Европейской ассоциации диализа и трансплантации, почечных реестров США и Японии, Российского регистра хронической почечной недостаточности, сердечно-сосудистые осложнения являются ведущей причиной смертности среди пациентов с терминальной стадией заболеваний почек на заместительной почечной терапии (в структуре общей смертности данной категории больных — от 30 % до 52 %).
В то же время в общей популяции населения в возрасте 45–74 лет снижение скорости клубочковой фильтрации ниже 60 мл/мин/1,73 м2 выступает в качестве независимого фактора риска инфаркта миокарда.
В канадском регистре GRACE (Global Registry of Acute Coronary Events) показано, что у больных с инфарктом миокарда с подъемом сегмента ST, не Q-инфарктом и нестабильной стенокардией при скорости клубочковой фильтрации 30–60 мл/мин/1,73 м2 риск смерти увеличивается в 2,09 раза, а при СКФ менее 30 мл/мин/1,73 м2 — почти в 4 раза.
Смертность от ХБП в 2016 году и прогноз на 2040 год.
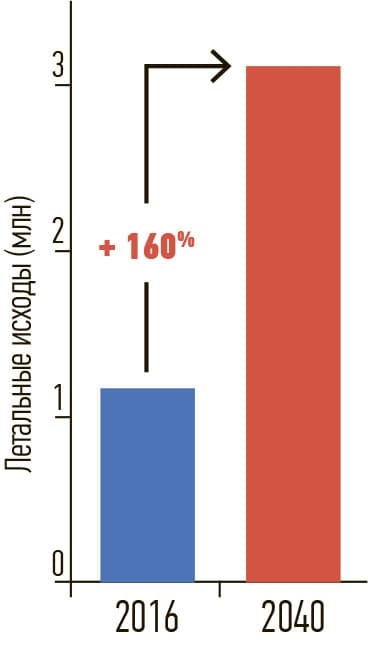 Ежегодно от ХБП умирает более 1,2 млн человек.
Ежегодно от ХБП умирает более 1,2 млн человек.
Летальность при инфаркте миокарда в популяции с терминальной стадией ХБП составляет около 59 % в течение первого года, достигая 70 % к концу второго. По данным другого анализа, включающего более 500 тысяч человек, нижний порог снижения скорости клубочковой фильтрации, при котором отмечается рост относительного риска сердечно-сосудистой смертности, равнялся 75 мл/мин/1,73 м2.
Кроме того, у людей старше 55 лет с исходным уровнем скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2 риск развития ИБС и ее осложнений, в т. ч. фатальных, превышал риск формирования терминальной почечной недостаточности.
Высокий риск кардио-васкулярных осложнений возникает не только в терминальной стадии почечной недостаточности, но и на ранних стадиях снижения функции почек. Это обусловлено комплексным влиянием на миокард и сосуды гемодинамических, метаболических и эндокринных нарушений, сопровождающих почечную дисфункцию.
В связи с этим логичной выглядит рекомендация Ассоциации нефрологов (клинические рекомендации «Хроническая болезнь почек», 2021) о том, чтобы в клинической практике у пациента с вероятными признаками поражения почек врачи любых специальностей проводили диагностику ХБП и классифицировали ее в медицинской документации с указанием:
1) стадии в зависимости от значений скорости клубочковой фильтрации, вида заместительной почечной терапии (ЗПТ), факта трансплантации (см. табл. 2);
2) градации выраженности альбуминурии/протеинурии для систематизации статистических данных, оценки прогноза и планирования лечебно-профилактических мероприятий.
Таблица 2. Классификация и стратификация стадий ХБП по уровню СКФ.
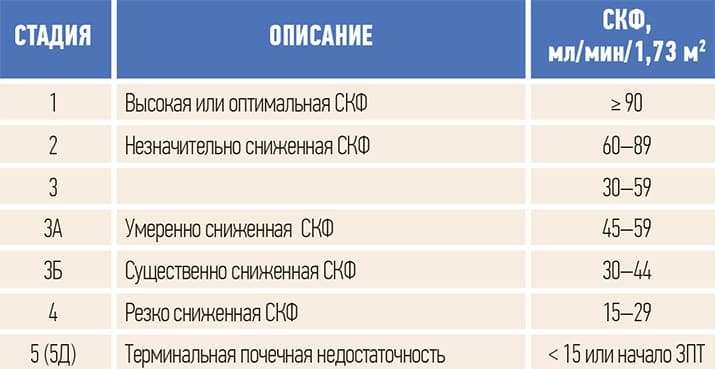
Оценка функции почек осуществляется по формулам:
1) CKD-EPI (Chronic Kidney Di-sease Epidemiology Collabora-tion) — наиболее рекомендованная формула;
2) MDRD (Modification of Diet in Renal Disease);
3) формула Кокрофта — Голта используется для оценки клиренса креатинина, используется для расчета СКФ перед назначением новых оральных антикоагулянтов.
Запоминать формулы не нужно, в настоящее время есть калькуляторы — в онлайн-доступе или в виде приложений для смартфона. Следует подчеркнуть, что на сегодняшний день идеально точной формулы нет.
Более того, существует ряд клинических ситуаций, когда использование вышеуказанных формул не рекомендовано в связи с высоким риском получения ошибочных значений СКФ:
- острое почечное повреждение;
- пациенты на диализе;
- определенное диетическое питание (вегетарианская диета, высокобелковая диета, креатиновые добавки);
- экстремальные размеры тела (выраженные истощение и ожирение (ИМТ <15 кг/м2 и >40 кг/м2);
- заболевания скелетной мускулатуры (миодистрофии), параплегия или ампутированные конечности;
- высокая мышечная масса (может занижать СКФ);
- возраст до 18 лет;
- тяжелое поражение печени;
- беременность;
- прием препаратов, способных повышать продукцию креатинина (фенофибрат, альфакальцидол, кальцитриол, парикальцитол, преднизолон); подавлять тубулярную секрецию креатинина (сульфаметоксазол + триметоприм), вступающих в реакцию Яффе (диуретики в высоких дозах, некоторые цефалоспорины) либо снижающих концентрацию креатинина за счет неустановленных механизмов, прямо не связанных с влиянием на деятельность почек (ацетилцистеин).
Следует помнить, что незначительные изменения СКФ могут быть физиологичными.
В настоящее время для определения СКФ используется новый эндогенный маркер цистатин С, по своим диагностическим характеристикам значительно превосходящий креатинин.
Цистатин С — это белок, который:
1) с постоянной скоростью синтезируется всеми клетками, содержащими ядра;
2) свободно фильтруется через клубочковую мембрану, полностью метаболизируется в почках;
3) не секретируется проксимальными почечными канальцами.
Согласно ряду исследований, уровень цистатина С, в отличие от уровня креатинина, не зависит от роста, массы тела, мышечной массы и пола человека.
Показания к назначению измерения цистатина С
1. Рутинный скрининг ренальной дисфункции и связанных с ней ССЗ у всех лиц 55 лет и старше.
2. Оценка ренальной дисфункции любой этиологии и стратификации ее тяжести при:
- гипертензии;
- сахарном диабете и/или метаболическом синдроме;
- патологии почек;
- диабетической нефропатии;
- трансплантации почек и печени;
- операциях с применением аппарата искусственного кровообращения,
- у детей.
3. Быстрая диагностика и стратификация пациентов в отделении интенсивной терапии.
4. При беременности — для оценки риска преэклампсии. (Применение цистатина С для расчета СКФ у беременных сегодня является спорным: одни авторы утверждают, что цистатин С можно использовать для ранней диагностики ренальных нарушений при беременности, другие — что измерение СКФ у здоровых беременных женщин по цистатину С и креатинину дает разные результаты и разница зависит от срока беременности.
Поэтому при определении СКФ у беременных следует учитывать, что разные маркеры имеют разные референтные уровни, которые, в случае цистатина С, например, сильно зависят от срока беременности).
5. При сердечной недостаточности (особенно в сочетании с NT-proBNP и тропонином), в т. ч. ОКС и инфаркте миокарда.
При наличии у пациента тиреоидной патологии, злокачественных новообразований или же на фоне приема высоких доз глюкокортикоидов концентрация цистатина С может меняться.
Что делать, если формульные методы неинформативны, а цистатин С недоступен?
В классическом варианте определение СКФ по клиренсу эндогенного креатинина возможно по пробе Реберга — Тареева: собирается суточная моча, определяется содержание креатинина в крови и моче, минутный диурез и рассчитывается СКФ по формуле:

Поскольку минутный объем фильтрации в почках зависит от роста и веса человека, для нормирования показателя у людей, значительно отклоняющихся в размерах от средних значений, клиренс креатинина пересчитывают на условную величину стандартной средней поверхности тела (1,7 м2).
Для этого нужно знать рост и вес человека. Нормальные значения СКФ (объем крови, очищаемой почками от креатинина за одну минуту) по пробе Реберга — Тареева составляют 80–120 мл/мин/1,73 м2. Начиная с возраста 30–40 лет СКФ постепенно уменьшается (примерно на 1 % в год) и к 80–90 годам составляет лишь половину той величины, которая определяется в 30 лет.
Критерием диагноза ХБП является скорость клубочковой фильтрации менее 60 мл/мин/1,73 м2 продолжительностью 3 месяца и более независимо от наличия других признаков повреждения почек.
При этом ХБП не ставится:
- если уровень СКФ в пределах 60–89 мл/мин/1,73 м2 при отсутствии признаков почечного повреждения, что обозначается как «начальное снижение СКФ» и требует динамического наблюдения и скрининга факторов риска;
- возраст обследуемого 65 лет и старше — это вариант возрастной нормы. Лицам моложе этого возраста рекомендуют контроль состояния почек не реже 1 раза в год и активную профилактику ХБП.
Формулирование диагноза ХБП не должно носить формальный характер. Скорость клубочковой фильтрации нужно динамично отслеживать, что влияет на медикаментозную терапию и ее своевременную корректировку.
Пациентам с ФП рекомендован регулярный контроль функции почек, даже если у них нет диагноза ХБП (см. табл. 3).
Таблица 3. Практические рекомендации Европейской ассоциации аритмологов (EHRA) по применению новых ОАК у пациентов с ФП.
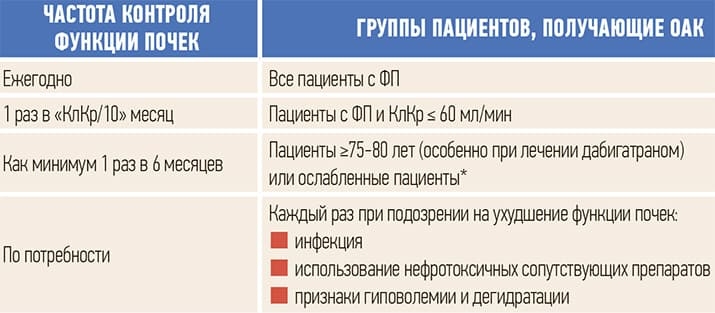
* Определяется при наличии 3 или более критериев: беспричинная потеря веса; жалобы на утомляемость; снижение мышечной силы рук; замедленная ходьба или низкая физическая активность.
ФП — фибрилляция предсердий; ХБП — хроническая болезнь почек; ОАК — оральные антикоагулянты; КлКр — клиренс креатинина.
Правило «делим на 10» описывает условную частоту пересмотра значений СКФ. Например, полученные значения СКФ составили 60 мл/мин/1,73 м2, делим данное значение на 10 и получаем 6, что означает: раз в 6 месяцев пациенту следует пересчитывать уровень СКФ.
Также следует помнить о ситуациях, которые автоматически сопряжены с расчетом значений СКФ, — это инфекции, использование нефротоксичных препаратов, гиповолемия и дегидратация, в т. ч. при назначении диуретиков.





