Дата публикации 7 ноября 2018Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Дислипидемия (ДЛ) — патологический синдром, связанный с нарушением обмена липидов и липопротеидов, т.е. изменением соотношения их концентрации в крови.[1] Он является одним из главных факторов риска атеросклероз зависимых заболеваний.
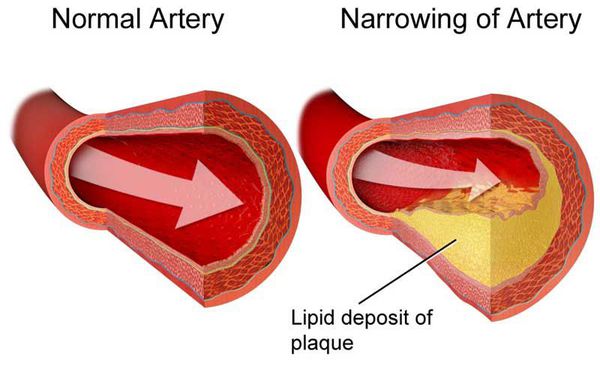
Липиды и липопротеиды — одни из источников энергии, необходимой организму человека. Они представляют собой жироподобные органические соединения. Липиды входят в состав липопротеидов.
Причины, приводящие к развитию дислипидемии, можно разделить на неизменяемые (эндогенные) и изменяемые (экзогенные).
К первым относится возраст, пол, гормональный фон и наследственная предрасположенность.
Группа изменяемых факторов риска ДЛ более многочисленна. К основным причинам относятся:
- нерациональное питание (избыточное потребление калорий, насыщенных жиров, простых углеводов);
- курение табака;
- избыточный вес (висцеральное ожирение);
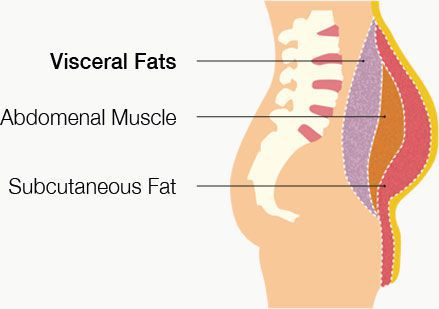
- сахарный диабет;
- злоупотребление алкоголем;
- повышенное артериальное давление;
- длительный стресс;
- малоподвижный образ жизни;
- систематическое физическое перенапряжение;
- хроническое субклиническое воспаление.
Также причинами ДЛ могут быть различные заболевания, патологические синдромы и приём некоторых медикаментов.
От внешних факторов больше зависит содержание в крови таких жировых субстанций, как хиломикроны и триглицериды. До 80% холестерина липопротеинов низкой плотности синтезируется в организме, главным образом, в печени и в меньшей степени зависит от внешних факторов. Семейно-генетический формы ДЛ полностью зависят от наследственных факторов.[1][9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы дислипидемии
Так как ДЛ является лабораторным синдромом, то её проявления связаны с атеросклерозом артерий тех органов и тканей, которые они кровоснабжают:
- ишемия головного мозга;
- ишемическая болезнь сердца;
- облитерирующий атеросклероз артерий нижних конечностей и т. д.
Ишемическая болезнь сердца – наиболее распространённое и грозное атеросклероз зависимое заболевание. От него погибает больше людей, чем от всех видов рака. Чаще всего это заболевание проявляется в виде стенокардии или инфаркта миокарда.
Стенокардию раньше называли “грудной жабой”, что точно характеризует симптомы заболевания — давящие или сжимающие ощущения за грудиной на высоте физической или эмоциональной нагрузки, продолжающиеся несколько минут и прекращающиеся после прерывания нагрузки или приёма нитроглицерина.
Инфаркт миокарда связан с разрывом атеросклеротической бляшки в сердечной артерии и формированием тромба на бляшке. Это приводит к быстрому перекрытию артерии, острой ишемии, повреждению и некрозу миокарда.
От хронической и острой ишемии может страдать головной мозг, что проявляется головокружением, потерей сознания, выпадением речевой и двигательной функции. Это не что иное, как мозговой инсульт или прединсультное состояние — транзиторная ишемическая атака. При облитерирующем атеросклерозе нижних конечностей происходит снижение кровоснабжение ног. Стоит отметить, что долгое время атеросклероз остаётся бессимптомным, клинические проявления начинаются при сужении артерии на 60-75%.
Семейно-генетические дислипидемии могут проявляться стигматами, такими как ксантомы кожи и ксантелазмы век.
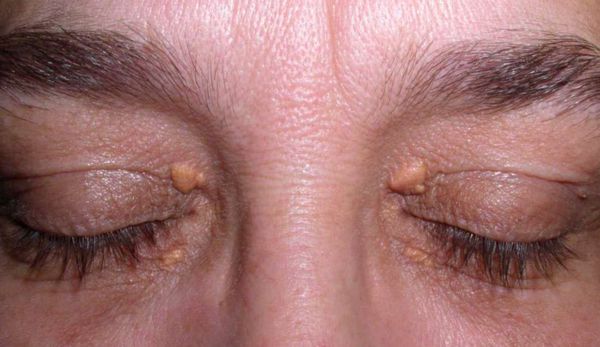
Значительное повышение концентрации триглицеридов крови (более 8 ммоль/л) может приводить к острому панкреатиту, который сопровождается сильной болью в верхнем отделе живота, тошнотой, рвотой, учащённым сердцебиением и общей слабостью.
Патогенез дислипидемии
Основными липидами плазмы крови являются:
- холестерин (ХС) — предшественник желчных кислот, половых гормонов и витамина Д;
- фосфолипиды (ФЛ) — основные структурные компоненты всех клеточных мембран и внешнего слоя липопротеиновых частиц;
- триглицериды (ТГ) — липиды, образующиеся из жирных кислот и глицерина, которые поступают в организм с пищей, затем транспортируются в жировые депо или включаются в состав липопротеинов.
Жирные кислоты (ЖК) плазмы крови — источник энергии и структурный элемент ТГ и ФЛ. Они бывают насыщенными и ненасыщенными. Насыщенные ЖК входят в состав животных жиров. НенасыщенныеЖК составляют растительные жиры и делятся на моно- и полиненасыщенные жирные кислоты. Мононенасыщенные ЖК в большом количестве содержаться в оливковом масле, а полиненасыщенные — в рыбьем жире и других растительных маслах. Считается, что все эти жиры необходимы человеку, их сбалансированное количество должно составлять до 30% суточного каллоража пищи и распределяться примерно на три равные части между моно-, полиненасыщенными и насыщенными ЖК.
Соединение жиров с белками называют липопротеинами или липопротеидами.
| Основные липопротеиды крови | Размер | Атерогенность (вклад в уровень ХС плазмы) |
|---|---|---|
| Хиломикроны | 500 нМ | Незначительный |
| Липопротеины очень низкой плотности (ЛОНП) | 40 нМ | 13% |
| Липопротеины низкой плотности (ЛНП) | 10-20 нМ | 70% |
| Липопротеины промежуточной плотности (ЛПП) | 8-10 нМ | Незначительный |
| Липопротеины высокой плотности (ЛВП) | 7 нМ | 17% |
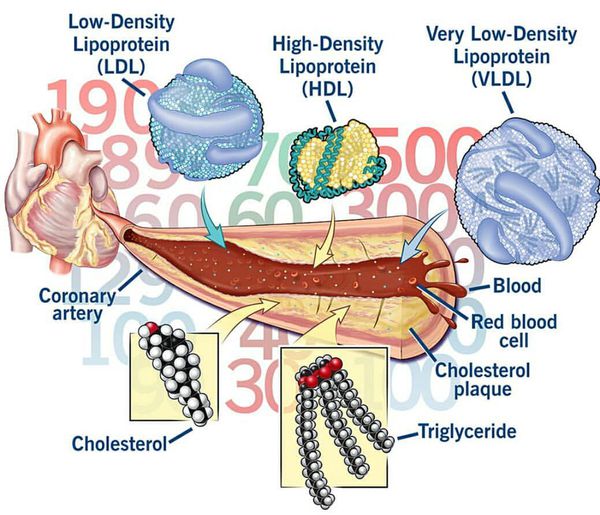
Хиломикроны — самые крупные липопротеиновые частицы, тесно связанные с жирной пищей. Они, как и липопротеины промежуточной плотности, не оказывают значительного влияния на атеросклероз.
Липопротеины высокой плотности способствуют обратному переносу ХС из сосудистой стенки в печень. В последнее время клиническое значение этих липопротеинов снизилось, так как появились данные о том, что более важным фактором является не их концентрация в крови, а функциональность.
Липопротеины низкой плотности обладают особой атерогенностью. Они, находясь в крови в повышенном количестве и будучи в модифицированном (окисленном) состоянии, проникают под повреждённый эндотелий артерий мышечного и эластического типа, формируя атеросклеротические бляшки и способствуя их деструкции. Именно ЛНП являются целью гиполипидемической и антиатеросклеротической терапии.[2][6]
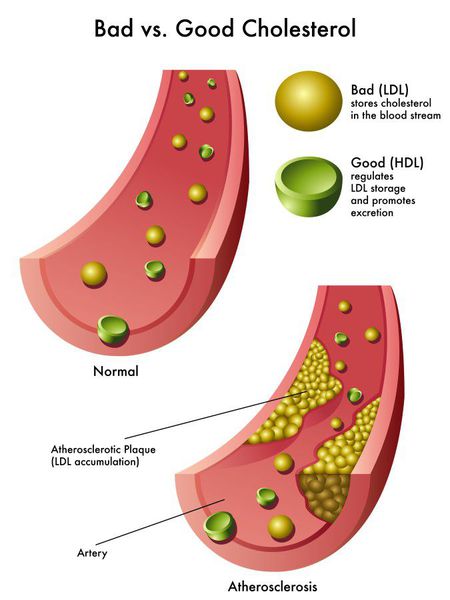
Помимо прочего выделяют липопротеин(а) — Лп(а). Это атерогенная липопротеиновая частица с диаметром 26 нМ. По своей структуре она похожа на ЛНП, но отличается наличием в своём составе уникального апобелка — апо(а). Данный белок имеет 98% сходство с молекулой плазминогена, что обеспечивает участие частицы в процессах атеротромбоза. Концентрация Лп(а) в крови имеет прямую связь с тяжестью атеросклероза и рассматривается как независимый биохимический маркер его развития.
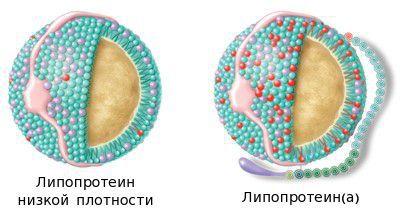
Существует также липопротеин ассоциированная фосфолипаза 2 типа, играющая существенную роль в обмене липидов и липопротеидов.
Под воздействием различных эндогенных и экзогенных факторов происходит изменение соотношения концентрации в крови перечисленных липидов и липопротеидов, что и приводит к ДЛ.
Классификация и стадии развития дислипидемии
Различают семейно-генетические, вторичные и смешанные дислипидемии.
Семейно-генетическая ДЛ бывает:
- гомозиготной — встречается довольно редко (1 случай на 1 млн человек), ХС у таких пациентов с детского возраста превышает 20 ммоль/л, а ЛНП составляет 12-15 ммоль/л;
- гетерозиготной — встречаются гораздо чаще (1 случай на 300-500 человек), у таких пациентов ХС превышает 12-15 ммоль/л, а ЛНП равен 5-7 ммоль/л.
Если при данном виде дислипидемии не проводить специфическое лечение (например, интенсивную статинотерапию, инъекции блокаторов моноклональных антител к PCSK9 и ЛПНП-аферез), то у пациентов наблюдается бурный атерогенез и сердечно-сосудистые события в молодом и среднем возрасте.[1]
Вторичные гиперлипидемии являются причиной какой-либо конкретной болезни или фактора риска. Вторичные изменения липидного обмена затрагивают все ветви жирового обмена в организме и наблюдаются при различных заболеваниях и состояниях:
- вторичная гиперхолестеринемия (высокий уровень ХС) может сформироваться при диетических погрешностях (чрезмерное употребление насыщенных жиров и простых углеводов), гипотиреозе, нефротическом синдроме, биллиарном циррозе, холестазе, синдроме Кушинга, неврогенной анорексии, приёме оральных контрацептивов, кортикостероидов, прогестерона, андрогенов и иммуносупрессоров (циклоспорин);
- вторичная гипертриглицеридемия (высокий уровень ТГ) может возникнуть по причине диетических погрешностей (чрезмерное употребление пищи с обилием легкоусвояемых углеводов и жиров, злоупотребление алкоголем), сахарного диабета, гипотиреоза, хронической болезни почек, панкреатита, булимии, синдрома Кушинга, болезни Гоше, липодистрофии, подагры, полицитемии, ожирения, приёма эстрогенов, глюкокортикоидов, бета-блокаторов и диуретиков;
- гипоальфахолестеринемия (низкий уровень ХС липопротеинов высокой плотности) встречается при систематических диетических погрешностях и вредных привычках (диета, обогащённая полиненасыщенными жирами, курение), сахарном диабете, циррозе печени, холестазе, болезни Крона, лимфоматозе, кахексии, ожирении, приёме прогестерона, анаболических стероидов, тестостерона, бета-блокаторов, а также при беременности.
В случае вторичных ДЛ следует параллельно лечить основное заболевание и корректировать дислипидемию медикаментозными и немедикаментозными средствами.
Чаще всего встречаются смешанные ДЛ, связанные как с генетическим факторами, так и с болезнями и модифицируемыми (поведенческими) факторами риска.
Формы смешанной ДЛ по Фредриксону в модификации ВОЗ и их вклад в атерогенез.[15]
| Фенотип | Общий холестирин |
ТГ | Повышение липопротеинов (ЛП) |
Атерогенность |
|---|---|---|---|---|
| I | Повышены | Повышены или в норме | Хиломикроны | Неатерогенен |
| IIa | Повышены | В норме | ЛНП | Высокая |
| IIb | Повышены | Повышены | ЛНП и ЛОНП | Высокая |
| III | Повышены | Повышены | ЛПП | Высокая |
| IV | Чаще в норме | Повышены | ЛОНП | Умеренная |
| V | Повышены | Повышены | Хиломикроны и ЛОНП | Низкая |
Нормы показателей липидов и липопротеинов крови зависят от индивидуального сердечно-сосудистого риска человека:
- при низком и среднем риске ХС < 5 ммоль/л, ЛНП< 3 ммоль/л;
- при высоком риске ХС < 4,5 ммоль/л, ЛНП < 2,5 ммоль/л;
- при очень высоком риске ХС < 4 ммоль/л, ЛНП < 1,5 ммоль/л.
ТГ у всех должны быть < 1,7 ммоль/л, ЛВП у мужчин > 1,0 ммоль/л, а у женщин > 1,2 ммоль/л.
Стадийность ДЛ:
- ЛНП умеренно повышенные (3-4 ммоль/л), высокие (4,1-4,8 ммоль/л), очень высокие (≥ 4,9 ммоль/л);
- ХС умеренно повышенный (5-6 ммоль/л), высокий (6,1-6,9 ммоль/л), очень высокий (≥ 7,0 ммоль/л);
- ЛВП низкий (< 1 ммоль/л), высокий (≥ 1,6 ммоль/л);
- ТГ умеренно повышенные (1,7-2,2 ммоль/л), высокие (2,3-4,4 ммоль/л), очень высокие (≥ 4,5 ммоль/л).
Осложнения дислипидемии
Осложнения ДЛ связаны с развитием атеросклероза. Считается, что его первичные проявления в виде липидных полосок у значимой части населения формируются ещё в подростковом и молодом возрасте. В дальнейшем прогноз зависит от активности атерогенеза и целостности атеросклеротических бляшек. При отсутствии тромботической деструкции этих бляшек и гемодинамически не значимом атеросклерозе качество и продолжительность жизни не изменятся.
Если атеросклероз приобретёт стенозирующий характер (обычно это происходит при сужении сосуда более чем на 75%), то появляются клинические проявления в той области, которую кровоснабжают эта артерия: ишемия головного мозга, миокарда, нижних конечностей и т. д.
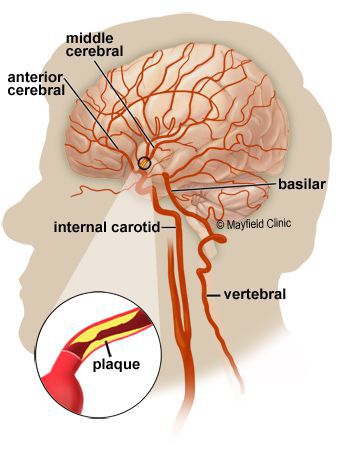
Если же произойдёт разрыв атеросклеротической бляшки, то сформируется тромб или тромбоэмболия с возможным развитием инфаркта миокарда или мозгового инсульта.
Диагностика дислипидемии
Диагностика начинается со сбора анамнеза (истории болезни) и выяснения жалоб. Если у кровных родственников отмечалась ранняя смерть от сердечно-сосудистых заболеваний или сердечно-сосудистые события, необходимо проверить липидный спектр пациента. Жалобы при ДЛ появляются на клинических стадиях атеросклероза и говорят о далеко зашедшем заболевании.
При подозрении на семейно-генетическую ДЛ целесообразно проведение генетического анализа крови для выявления генов, отвечающих за развитие наследственной ДЛ, в том числе и у близких родственников пациента.
В клинической практике ДЛ диагностируют лабораторным способом. О заболевании свидетельствует превышение референсных значений в повторных анализах крови. Для определения показателей липидов и липопротеидов крови используется ряд формул:
- формула Фридвальда (верна, пока уровень ТГ не выше 4,5 ммольл);
- формула Климова или коэффициент (индекс) атерогенности;
- соотношение атерогенных и антиатерогенных апобелков.
В последние годы широко используется такой показатель, как холестерин-не-липопротеины высокой плотности (ХС-не-ЛПВП), который определяется по формуле: ХС − ЛВП.
Важно выявлять сопутствующие заболевания ДЛ, такие как сахарный диабет, ожирение, метаболический синдром и другие эндокринные дисфункции.
При правильной интерпретации лабораторных показателей диагностика ДЛ чаще всего не вызывает трудности. Сложнее проводить дифференциальную диагностику между различными ДЛ (первичная, вторичная, приобретённая, семейная).
Лечение дислипидемии
Лечение ДЛ начинаются с немедикаментозных мероприятий, таких как:
- рационализация питания;
- оптимизация массы и параметров тела;
- повышение физической активности;
- отказ от хронических интоксикаций.[8]
При недостаточной эффективности немедикаментозных мероприятий показано назначение лекарственных средств гиполипидемического и антисклеротического действия, подобранных пациенту с учётом индивидуального общего сердечно-сосудистого риска.
В клинической практике используется последние генерации фибратов:
- ципрофибрат («Липанор») по 100 мг 1-2 раза в сутки;
- фенофибрат («Липантил-М») по 200 мг в сутки;
- новая лекарственная форма фенофибрата («Трайкор») по 145 мг в сутки.
Препараты никотиновой кислоты в клинической практике применяют редко из-за большого количества нежелательных явлений и отсутствия положительного влияния на прогноз. Секвестранты желчных кислот также оказывают незначительное клиническое воздействие.
Омега-3 ПНЖК представлены в России единственным рецептурным препаратом этой группы — «Омакором». В 1 капсуле препарата содержится 90% незаменимых омега-3 ПНЖК в виде эйкозопентаеновой и докозагексаеновой кислот. «Омакор» способен незначительно снижать ТГ и ЛОНП.
В нашей стране зарегистрирован один ингибитор, поглощающий ХС в кишечнике — «Эзетимиб» («Эзетрол»). Механизм его действия заключается в снижении всасывания экзогенного холестерина из кишечника, что может снизить концентрацию ЛНП в крови дополнительно на 15-20%. Положительное влияние на прогноз этих препаратов крайне мало, однако, учитывая их безопасность, они всё шире применяются для снижения ЛНП в случае недостижения целевых показателей при статинотерапии или непереносимости статинов.[8][14]
Основными препаратами, снижающим концентрацию липидов, ХС и липопротеидов, способствующих развитию атеросклероза, являются статины. Они блокируют ферменты, участвующие в синтезе ХС в клетках печени, тем самым вызывая стимуляцию внутрипечёночного образования рецепторов к ЛПН. Это, в свою очередь, значительно снижает ЛНП в крови (на 50-60%). Препараты хорошо переносятся и положительно влияют на прогноз, т.е. снижают число инфарктов миокарда, ишемических мозговых инсультов, сердечно-сосудистую и общую смертность.
Статины обладают дополнительными положительными эффектами — стабилизация атеросклеротических бляшек и регресс атеросклероза.
Практическое значение имеют симвастатин («Зокор»), аторвастатин («Липримар»), розувастатин («Крестор») и питавастатин («Ливазо»). Эти препараты, а также большое количество дженерических статинов зарегистрированы в России.
Статинотерапия для первичной и вторичной профилактики проводится в следующих дозах:
- симвастатин по 10-40 мг в сутки;
- аторвастатин по 10-80 мг в сутки;
- розувастатин по 5-40 мг в сутки;
- питавастатин по 1-4 мг в сутки.
В 2015 году были зарегистрированы два препарата новой группы — алирокумаб и эволокумаб. Они предназначены для лечения семейно-генетической и смешанной ДЛ. Исследования показали достоверное значительное снижение ЛПНП в крови (на 60-70%) и их стабильный низкий уровень на протяжении длительного времени при хорошей переносимости. Эволокумаб применяют по 420 мг 1 раз в месяц, алирокумаб — по 75 мг 1 раз в две недели в подкожных инъекция шприц-ручкой. Недостатки этой группы медикаментов — высокая стоимость терапии по сравнению со статинами и другими средствами.
Комбинированная терапия дислипидемии решает задачи, которые не под силу монотерапии. Каждый препарат, снижающий концентрацию фракций липидов, влияет на определённый элемент метаболизма липидов и липопротеидов:
- статины и комбинация статинов с «Эзетролом» преимущественно снижают ЛНП, незначительно влияют на содержание ТГ и умеренно повышают концентрацию ЛВП;
- фибраты снижают уровень ТГ и повышают ЛВП, почти не оказывая влияния на ЛНП;
- никотиновые кислоты умеренно действуют на все звенья метаболизма липидов, но их применение ограничено в связи с высокой частотой побочных эффектов.
В России с 2008 года зарегистрирован комбинированный препарат «Инеджи», содержащий фиксированные дозы симвастатина и эзетимиба.
К комбинации статинов с фибратами всё чаще прибегают при лечении пациентов с сахарным диабетом 2 типа и с метаболическим синдромом при повышенном содержании ТГ в крови. Статины в такой комбинации эффективно предупреждают развитие макрососудистых осложнений (инфаркт миокарда, стенокардия), а фибраты способствуют предупреждению диабетической микроангиопатии.
Всё чаще статины сочетают с «Омакором» и кумабами.[7][14][15]
Прогноз. Профилактика
Прогноз ДЛ зависит от формы и выраженности синдрома, степени развития атеросклероза и наличия атеросклероз зависимых заболеваний.
Профилактика ДЛ основывается на поведенческих мероприятиях.
Рациональное питание способно снизить ЛНП лишь до 20%, однако отмечается влияние диеты на ТГ и ЛПОН. Кроме того, здоровое питание является выраженным фактором снижения общей смертности.
Количество калорий, потребляемых с пищей, должно способствовать поддержанию нормального веса тела. В связи с этим рекомендуется ограничить потребление животных жиров (не более 10%), а общее количество жира не должно превышать 20-30% от всего суточного каллоража. Ежедневное поступление ХС с пищей не должно превышать 300 мг у лиц без ДЛ и атеросклероза, а при наличии этих состояний – не более 200 мг.
Необходимо сокращать потребление насыщенных жиров и не преувеличивать важность ограничения некоторых жирных продуктов, например яиц, поскольку они служат ценным источником многих полезных веществ. Особо атерогенные насыщенные жиры — это трансжиры, содержащиеся в твёрдых маргаринах и полуфабрикатах.[9][13]
Фрукты и овощи (не считая картофель) следует потреблять не менее 400-500 г в день. Употребление мясных продуктов, субпродуктов и красного мяса следует ограничить. Лучше использовать в пищу больше других белковых продуктов: бобовые, рыба или птица. Каждый день нужно употреблять молочные продукты с низким содержанием жира и соли (кефир, кислое молоко, сыр, йогурт).
В ежедневной пище необходимы простые сахара, но их доля не должна превышать 10% от общей калорийности рациона. Общее количество потребляемой соли, включая соль, содержащуюся в готовых продуктах, не должно превышать 5 г в сутки, особенно это важно для людей с артериальной гипертензией.
Глубоководную рыбу северных морей (сель, сардины, скумбрия, лосось) полезно употреблять не реже 2-3 раз в неделю. Это связано с высоким содержанием в этих сортах ω-З ПНЖК, способствующих профилактике атеросклероза. Растительные стеролы/станолы содержатся в семенах растений, орехах и растительных маслах. В дозах около 2 г в сутки они не позволяют ХС всасываться в кишечнике.[2][4]

Снижение избыточного веса — обязательное условие профилактики ДЛ и сердечно-сосудистых осложнений. Снижение массы тела достигается назначением низкокалорийной диеты и регулярными адекватными физическими нагрузками. Для антропометрической оценки следует использовать показатель индекс массы тела (ИМТ) = вес в кг/рост м2. Нормальный ИМТ — 18,5-25 кг/м2. Для оценки типа ожирения используют измерение окружности талии (ОТ). Норма ОТ у мужчин — не более 94 см, у женщин — не более 80 см. ОТ свыше 102 см у мужчин и 88 см у женщин — показатель абдоминального ожирения, что ассоциируется с повышенным риском сердечно-сосудистых осложнений.[15]
Всем пациентам с ДЛ, избыточной массой тела и другими факторами риска рекомендуется повысить повседневную физическую активность с учётом возраста, тренированности и имеющихся заболеваний. Наиболее физиологичное, безопасное и доступное для всех аэробное физическое упражнение — ходьба. Ею рекомендуется заниматься 5-6 раз в неделю не менее 30-45 минут с достижением пульса 60-75% от максимального для человека. Максимальная частота сердцебиения рассчитывается по формуле: 220 – возраст (лет). Людям с ИБС и другими заболеваниями сердечно-сосудистой системы следует разрабатывать индивидуальный режим тренировок, учитывая показатели нагрузочного теста (велоэргометр или тредмил).[2][3]
Физические тренировки — важная составляющая профилактики ДЛ. Они снижают частоту сердцебиения и артериальное давление, позволяют адаптироваться к условиям ишемии, стабилизируют гормональный фон и оксигенацию тканей. Более эффективны аэробные, динамические, адекватные по интенсивности нагрузки циклического типа — ходьба, туризм, плавание, прогулки на лыжах и велосипеде.
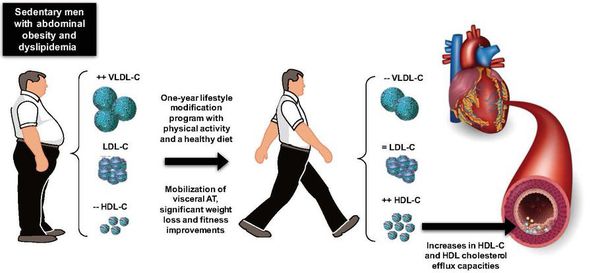
Важно отказаться от курения в любой форме, в том числе от пассивного. Алгоритм программы отказа от курения состоит из нескольких принципов:
- выявление курильщиков;
- оценка выраженности привычки и готовности избавиться от неё;
- объяснение вреда курения и рекомендация отказа от него;
- при необходимости — врачебная помощь, включающая комплексную терапию;
- регулярное наблюдение врачом пациента-курильщика.
Наиболее эффективным медикаментом для отказа от табакокурения считается варениклин («Чампикс»). Он является блокатором никотиновых рецепторов головного мозга, в результате чего подавляется тяга к курению, снижается удовольствие от процесса и уменьшаются абстинентные проявления.
Ряд исследований показал, что умеренное потребление алкоголя может положительно воздействовать на ДЛ. Безопасным для здоровья считается употребление не более 150 мл алкоголя в неделю для мужчин и 100 мл для женщин при условии суточного употребления не более 20 г для мужчин и 15 г для женщин. Однако любые дозы алкоголя не рекомендованы людям с артериальной гипертензией, гипертриглицеридемией, заболеваниями гепато-биллиарной и панкреатической зоны, подагрой и ожирением. Злоупотребление алкоголем при статинотерапии может привести к миопатии и рабдомиолизу.[6]
Превентивная статинотерапия также является действенным направлением профилактики ДЛ. Для этого чаще используют низкие дозы современных статинов:
- симвастатин 10-20 мг в сутки;
- аторвастатин 10-20 мг в сутки;
- розувастатин 5-10 мг в сутки;
- питавастатин 1-2 мг в сутки.
Д. А. Иткин
С. В. Черкесова
РМАПО, Москва
Необходимость коррекции нарушений липидного обмена в настоящее время не вызывает сомнений. Многочисленными исследованиями, проведенными до начала 90-х годов, доказана возможность снижения уровня холестерина (ХС), триглицеридов (ТГ) и нормализации показателей липидного обмена на фоне гипохолестеринемической терапии.
Но всегда ли выраженное снижение общего холестерина (ОХ) и холестерина липопротеидов низкой плотности (ХС-ЛПНП) способствует улучшению жизненного прогноза?
В исследовании CARE было показано, что снижение ХС-ЛПНП ниже уровня 3,2 ммоль/л не влекло за собой дальнейшего снижения уровня смертности. В то же время, согласно исследованию POST-CABGT, куда включались больные после операции аортокоронарного шунтирования (АКШ), при снижении холестерина ЛПНП до уровня менее 2,6 ммоль/л (по сравнению с больными с уровнем 3,4-3,5 ммоль/л) необходимость в повторных операциях АКШ сокращается на 29%. Аналогичные результаты были получены в ходе исследования CARS, куда включались больные с ИБС, относительно нормальным уровнем ОХ (от 4,1 до 5,6 ммоль/л) и средним уровнем ХС-ЛПНП (3,17 ммоль/л). В настоящее время целью гипохолестеринемической терапии при вторичной профилактике ИБС европейские кардиологи считают достижение уровня холестерина ЛПНП менее 3,0 ммоль/л, а американские — менее 2,6 ммоль/л.
Показана эффективность как медикаментозных, так и немедикаментозных методов коррекции уровня дислипидемий. При этом любую коррекцию следует начинать с устранения факторов риска, способствующих прогрессированию атеросклероза, таких как курение, гиподинамия, а также с нормализации индекса массы тела.
В случаях возникновения дислипидемии на фоне таких заболеваний, как гипотиреоз, нефротический синдром и др., необходимо прежде всего начать лечение основного заболевания.
 |
| Рисунок. Нормализация уровня липопротеидов в крови позволяет уменьшить потребность в хирургическом лечении |
Одним из основных методов немедикаментозного лечения является соблюдение диеты с ограничением употребления жиров животного происхождения и легкоусваиваемых углеводов, ограничение калорийности питания. В ходе исследования Veterans Administrations больным была предписана диета с увеличенным содержанием полиненасыщенных жирных кислот и уменьшенным содержанием животных жиров (по сравнению с пациентами, соблюдавшими стандартную североамериканскую диету). Диетотерапия на протяжении восьми лет привела к снижению уровня ОХ на 12,7% и уменьшению частоты развития инфарктов миокарда (ИМ) на 20%. При этом не было отмечено снижения общей смертности в какой-либо из групп больных. В исследовании Finnish Mental Hospital Study за шестилетний период наблюдения у 450 больных обоего пола в возрасте 34—64 лет на фоне диеты с низким содержанием холестерина отмечено снижение его уровня в крови на 15%. При этом достижение среднего уровня ОХ в 5,8 ммоль/л не вызывало достоверного снижения общей смертности или смертности от сердечно-сосудистых заболеваний. В исследовании DART, включавшем более 2000 больных, средний возраст которых был 56,5 лет, соблюдение диеты на протяжении двух лет повлекло за собой недостоверное снижение уровня общей смертности и смертности от ИБС. Однако ишемические события (нефатальные ИМ) встречались даже чаще в группе больных, соблюдавших диету. Наиболее крупное исследование Minnesota Coronary Survey, включавшее около 5000 пациентов обоего пола и любого возраста со средним исходным уровнем ОХ 5,3 ммоль/л, выявило, что соблюдение только гипохолестериновой диеты привело к снижению уровня ОХ на 14,5% за 4,5 года по сравнению с контрольной группой, придерживавшейся стандартной диеты. Это исследование также не показало уменьшения развития сердечно-сосудистых заболеваний и снижения общей смертности.
На наш взгляд, лечение больных с гиперхолестеринемией и гипертриглицеридемией необходимо во всех случаях начинать с устранения факторов риска и назначения гипохолестеринемической диеты. При этом, если диета эффективна, то рассматривать ее в качестве монотерапии можно только в том случае, если больной действительно в состоянии соблюдать диету в течение всей оставшейся жизни. Однако больным с ИБС в период обострения заболевания и при наличии выраженной гиперхолестеринемии показано, наряду с соблюдением диеты, одновременное назначение гипохолестеринемических препаратов в адекватных дозах. Нормализация уровня показателей липидного обмена только на фоне диеты у таких больных не представляется возможной, а несвоевременное начало лечения может привести к развитию неблагоприятных осложнений.
При отсутствии «острой» ситуации неэффективность немедикаментозной терапии в течение трех месяцев является показанием к подключению медикаментозной терапии. Следует отметить, что применение гиполипидемических препаратов, к какому бы классу они ни относились, ни в коем случае не означает отказа от соблюдения диеты. Наоборот, любая гипохолестеринемическая терапия будет эффективна при условии соблюдения диеты.
В настоящее время используются пять основных классов лекарственных средств, применяемых с учетом механизма их действия, эффективности и наличия побочных эффектов, а также противопоказаний при том или ином типе дислипидемии.
I Статины.
II Никотиновая кислота и ее производные.
III Фибраты.
IV Секвестранты желчных кислот.
V Антиоксиданты.
На сегодняшний день влияние на общую смертность, смертность от сердечно-сосудистых заболеваний и риск развития сердечно-сосудистых осложнений доказано только для препаратов из группы статинов. Действие этих препаратов основано на ингибировании фермента 3-гидрокси-3-метилглутарил-коэнзим-А (ГМГ-ко-А)-редуктазы. Благодаря торможению биосинтеза холестерина в печени и кишечнике статины уменьшают внутриклеточные запасы холестерина. Это вызывает образование повышенного количества рецепторов к ЛПНП и ускоряет удаление их из плазмы.
Другие механизмы действия статинов на эндотелий сосудов, агрегацию тромбоцитов окончательно не изучены.
Эффект статинов преимущественно направлен на снижение уровня холестерина ЛПНП и общего холестерина. В работах последних лет показано, что применение высоких доз статинов может заметно снижать уровень триглицеридов, и конкурировать с эффектом фибратов.
На сегодняшний день в России зарегистрированы следующие препараты из группы статинов:
- ловастатин (мевакор, фирма Merck Sharp & Dohme)
- симвастатин (зокор, той же фирмы)
- правастатин (липостат, Bristol Mayer Scweeb)
- флювастатин (лескол, Novartis)
- аторвастатин (липримар, Pfizer)
- церивастатин (липобай, Bayer)
По данным W. C. Roberts (1997), доза симвастатина в 10 мг приблизительно эквивалентна 20 мг ловастатина или правастатина и 40 мг флювастатина. Согласно его исследованиям, двукратное повышение дозы статинов по отношению к начальной дозе приводит к дополнительному снижению ОХ приблизительно на 5% и ХС-ЛПНП на 7%. При этом повышение уровня холестерина липопротеидов высокой плотности (ХС-ЛПВП) не зависит от увеличения дозы препарата.
Препараты из группы статинов используются для первичной и вторичной профилактики ИБС. Под вторичной профилактикой понимают применение препаратов у больных с доказанной ИБС.
Нам представляется, что наибольшая эффективность при назначении статинов должна определяться не только по уровню исходных показателей липидного обмена, но и по сочетанию суммарного риска развития сердечно-сосудистых осложнений и клиническому течению заболевания. Так, у больных с острым коронарным синдромом клинический эффект применения статинов может быть более выраженным, чем у больных со стабильной стенокардией, а тактика должна быть более агрессивной. Однако эти выводы основаны на нашем практическом опыте, они не получили пока подтверждения в ходе многоцентровых рандомизированных исследований.
Статины, так же как аспирин и β-блокаторы, относятся к средствам, влияющим на прогноз заболевания у больных с ИБС.
Эффективность применения статинов доказана также в ходе исследований, посвященных первичной профилактике.
Исследования 4S, CARE, LIPID, WOSCOPS, AFCAPS/TEXCAPS и другие демонстрируют действенность терапии статинами для вторичной и первичной профилактики ИБС. При этом влияние статинов на «конечные точки» при вторичной профилактике более выражено и экономически более оправданно. Поэтому применение статинов у больных с диагностированной ИБС в сочетании с дислипидемиями может быть рекомендовано всем больным. Эффективность терапии статинами выше в группе больных с более выраженными нарушениями липидного обмена. Развитие «коронарных событий» у ряда больных ИБС на фоне нормальных значений показателей липидного обмена указывает на многофакторность генеза этих осложнений и подчеркивает значение не только уровня дислипидемии, но и совокупности ряда факторов, важнейшими из которых являются клинические проявления обострения заболевания.
Одной из возможных причин эффективности гипохолестеринемических препаратов в профилактике ИБС является продемонстрированная в ряде работ их способность к замедлению прогрессирования и даже возможность регресса атеросклеротического процесса. Эти эффекты изучались путем измерения диаметра сосудов с помощью артериографии или внутрисосудистого ультразвукового исследования.
В исследовании MAAS у больных с ИБС лечение симвастатином в дозе 20 мг в течение четырех лет позволило выявить статистически достоверное уменьшение развития новых стенозов коронарных артерий и регресс уже имевшихся коронарных стенозов; просвет сосудов увеличивался от 0,06 до 0,17 мм при наличии исходного стеноза более 50%.
Замедление прогрессирования или регресс атеросклероза достигаются благодаря интенсивной и агрессивной гипохолестеринемической терапии при значительном снижении уровня ХС-ЛПНП. Наибольшей гипохолестеринемической активностью в одинаковой дозировке обладают симвастатин и аторвастатин. В исследовании SMAC применение аторвастатина и симвастатина в дозе 10-20 мг в сутки позволило почти у 50% больных с ИБС и исходным уровнем ХС-ЛПНП от 4,2 до 7,8 ммоль/л достичь целевого уровня на фоне 52 недель лечения. При этом эффект аторвастатина наступал несколько быстрее, и через 16 недель лечения он был достигнут у 46% больных по сравнению с 27% на фоне лечения симвастатином. К концу года эта разница нивелировалась, составив 50% при лечении аторвастатином и 48% на фоне лечения симвастатином, и была статистически недостоверной. Это исследование показало выраженную гипохолестеринемическую эффективность обоих статинов и примерно одинаковый эффект через год лечения тем и другим препаратами. При этом в большинстве европейских стран стоимость симвастатина была несколько ниже, чем аторвастатина. В данном исследовании не наблюдалось каких-либо серьезных побочных эффектов, потребовавших отмены препаратов.
Другим важным гиполипидемическим средством, используемым для нормализации липидного обмена, является никотиновая кислота и ее производные (ниацин). По мнению В. Парсона, преимущество этой группы препаратов в том, что «они все делают так, как надо». Наряду со снижением уровня ОХ и ХС-ЛПНП препараты этой группы снижают уровень триглицеридов и успешнее, чем любые другие гиполипидемические средства, увеличивают уровень ХС-ЛПВП. Эти препараты обладают и рядом других преимуществ. Например, они снижают уровень липопротеина «а», которому придается большое значение в качестве важного самостоятельного фактора риска развития таких осложнений, как инфаркт и инсульт. Препараты никотиновой кислоты и ее производные уменьшают уровень ЛПНП, воздействуя преимущественно на мелкие, наиболее атерогенные их частицы. Эти лекарственные средства увеличивают уровень ХС-ЛПВП за счет фракции ЛПВП2, которая является наиболее активной в плане удаления липидов из бляшек, и тем самым препятствуют прогрессированию атеросклероза.
В ряде работ показана возможность уменьшения сердечно-сосудистых осложнений и общей смертности при применении ниацина.
В программе сердечно-сосудистых препаратов (США) сравнивался ряд лекарственных средств, изменяющих уровень холестерина. Исследование проводилось у мужчин 30—65 лет, имевших в анамнезе хотя бы один сердечный приступ. Изучалось влияние эстрогенов, тироксина, клофибрата и ниацина. Каждая группа состояла приблизительно из 1100 больных, а группа плацебо была в два раза больше. Предполагаемая продолжительность исследования составляла 5 лет, но для первых двух средств оно было досрочно прекращено в связи с развитием большого количества инфарктов и других осложнений. Клофибрат не оказывал благоприятного воздействия на уровень смертности и количество сердечно-сосудистых осложнений. Таким образом, никотиновая кислота была единственным средством, при применении которого удалось уменьшить число нефатальных инфарктов примерно на 27%, инсультов — на 24%, количество госпитализаций по поводу сердечно-сосудистых осложнений — на 12% и необходимость в хирургическом лечении на сердце и сосудах — на 46%.
Тенденция к снижению смертности, отмечавшаяся за 5 лет наблюдения на фоне приема ниацина, оказалась статистически недостоверной.
Важным преимуществом этой группы лекарственных средств является относительно низкая их стоимость по сравнению с другими гиполипидемическими препаратами. В настоящее время чаще всего применяются медленно высвобождающиеся формы никотиновой кислоты. Они обеспечивают более длительное и постепенное высвобождение активного соединения и обусловливают значительное снижение побочных эффектов. К этим препаратам относятся:
- соединение никотиновой кислоты с полигелем;
- никотиновая кислота в капсулах с инертным наполнителем;
- никотиновая кислота в матрице из тропического воска (препарат эндурацин, который нашел наиболее широкое применение в дозе 500 мг три раза в день.
Эффективность этих препаратов также несколько различается. По данным Figge с соавт. (1988), биодоступность препаратов ниацина пролонгированного действия, имеющих восковую матрицу, почти в два раза выше, чем с дозированным высвобождением. Поэтому эффективность эндурацина в дозе 1500 мг в сутки в отношении ХС-ЛПНП, ХС-ЛПВП, по данным Д. Кинана, была даже несколько большей, чем при приеме 3000 мг ниацина с пролонгированным высвобождением.
Крупномасштабные исследования по сравнению характеристик эффективности, дозировки, побочных эффектов различных пролонгированных форм никотиновой кислоты до настоящего времени отсутствуют.
Максимальная суточная доза препаратов никотиновой кислоты не должна превышать 6 г, а для эндурацина — 3 г. Увеличение дозы не привело к улучшению результатов, а количество побочных эффектов при этом может увеличиваться. Общая особенность всех препаратов никотиновой кислоты — это необходимость постепенного повышения дозы под контролем уровня показателей липидного обмена даже при хорошей их переносимости. Чаще всего лечение начинается с дозы 500 мг в сутки в течение недели, затем 500 мг два раза в день в течение еще 1-3 недель, а затем происходит корректирование дозы в зависимости от показателей липидного обмена. Для уменьшения побочных реакций препараты применяют во время еды, ограничивают употребление горячих напитков, а также при появлении первых признаков гиперемии добавляют небольшие дозы аспирина (100—325 мг), что помогает уменьшить эти проявления в первые 3-4 дня до последующего полного их исчезновения.
Наиболее часто встречающиеся побочные эффекты при приеме ниацина — это чувство жара в виде «приливов» и кожный зуд, а также чувство гиперестезии и парестезии; запоры, диарея, головокружение, сердцебиение, нарушение аккомодации, сухость кожных покровов или нарушение ее пигментации. Все эти побочные эффекты составляют от 2 до 7%
(Д. Кинан) и достоверно не отличаются от побочных эффектов в группе плацебо. Обычно для контроля за нежелательными осложнениями со стороны печени каждые четыре недели проводятся биохимические исследования. Появление тошноты, рвоты или других недомоганий требует временной отмены препарата и дополнительного исследования печеночных проб. При этом незначительное повышение уровня АСТ, АЛТ, ЛДГ, ГГТП при лечения ниацином допускается. Кроме печеночных проб, при лечении препаратами никотиновой кислоты должны регулярно контролироваться уровень сахара, мочевой кислоты.
Использование других групп лекарственных препаратов, таких как фибраты, ионообменные смолы (секвестранты желчных кислот) и антиоксиданты, также позволяет в целом ряде случаев улучшить нарушенные показатели липидного обмена. Однако до настоящего времени не получены данные об их влиянии на общую смертность, смертность от сердечно-сосудистых заболеваний, развитие сердечно-сосудистых осложнений, необходимость в хирургических методах лечения, частоту госпитализаций и т. д. Ведущиеся в последнее время крупномасштабные исследования по применению фибратов и антиоксидантов, возможно, позволят более точно определить их роль и место в лечении дислипидемий у широкого контингента пациентов.
По вопросу литературы обращайтесь на кафедру терапии и подростковой медицины РМАПО по тел. (095) 945-48-70
Цель обзора. Описать возможности воздействия на атерогенную дислипидемию у больных с метаболическим синдромом.
Последние данные литературы. Метаболический синдром (МС) играет значимую роль в развитии и прогрессировании сердечно-сосудистых заболеваний (ССЗ), смертность от которых занимает лидирующие позиции среди причин смерти людей трудоспособного возраста. Среди больных с МС риск развития ишемической болезни сердца (ИБС) в 3–4 раза выше, смертность от ИБС в 3 раза выше, риск развития ишемического инсульта в 2 раза выше по сравнению с пациентами без метаболических нарушений. Атерогенная дислипидемия представляет собой не только модифицируемый фактор риска развития и прогрессирования атеросклероза, но и одно из основных звеньев «порочного круга» МС. Поэтому главной «мишенью» в комплексе мер, направленных на максимальное снижение риска развития ССЗ и их осложнений у больных с МС представляется дислипидемия. Известно, что только достижение целевых уровней липидов наряду с коррекцией всех компонентов МС может гарантировать снижение сердечно-сосудистого риска. В настоящее время в арсенале врача-интерниста достаточно широкий спектр гиполипидемических средств. В статье рассматриваются немедикаментозные и медикаментозные подходы к лечению нарушений липидного обмена. Перспективным представляется применение комбинированной липидкорригирующей терапии.
Заключение. Своевременное выявление МС имеет большое клиническое и прогностическое значение, поскольку данное состояние при адекватной терапии потенциально обратимо. Одной из важнейших задач в лечении атерогенной дислипидемии в рамках МС служит достижение целевых уровней липидов путём изменения образа жизни и применения гиполипидемической терапии.
Ещё в прошлом столетии известные клиницисты объединяли повышение артериального давления (АД), избыточную массу тела, повышение уровня глюкозы и нарушения липидного обмена в звенья одной цепи, предполагая, что в основе всех этих нарушений лежит единый процесс. Каждая его составляющая представляет собой, по сути, модифицируемый фактор риска развития атеросклероза, а наличие тесной патогенетической связи между ними послужило основанием для выделения их в самостоятельный синдром – метаболический. Компоненты метаболического синдрома по своей клинической масштабности уже давно вышли за рамки понятия «синдром», однако до сих пор не найдена формулировка нозологии, способной объединить все его составляющие.
Метаболический синдром (МС) в последние годы стал центром дискуссий среди врачей многих специальностей: кардиологов, эндокринологов, гастроэнтерологов, гинекологов и др. Повышенное внимание к данной проблеме обусловлено, прежде всего, нарастающей распространённостью МС. За последние 15 лет было проведено более 20 эпидемиологических исследований, посвященных распространенности МС. Мета-анализ широкомасштабных исследований показал, что в популяции взрослого населения МС выявляется от 10% в Китае до 24% в США. Эксперты ВОЗ назвали МС пандемией XXI века, и в ближайшие 25 лет прогнозируют увеличение темпов роста МС на 50% [1, 2].
Одним из важных аргументов изучения МС служит его атерогенный потенциал. Согласно данным скандинавского исследования KIHD (Kuopio Ischaemic Heart Disease Risk Factor Study) продолжительностью 11 лет, среди больных с МС риск развития ИБС оказался в 3–4 раза выше, смертность от ИБС в 3 раза выше по сравнению с пациентами без метаболических нарушений [3]. В исследовании ARIC (Atherosclerosis Risk in Communities) было показано, что у лиц с МС инциденты развития ишемического инсульта были в 2 раза выше по сравнению с контрольной группой [4]. Таким образом, актуальность проблемы обусловлена, прежде всего, тем, что МС играет значимую роль в развитии и прогрессировании сердечно-сосудистых заболеваний (ССЗ), смертность от которых занимает лидирующие позиции среди причин смерти людей трудоспособного возраста [5-8]. Своевременное выявление МС имеет большое клиническое и прогностическое значение, поскольку данное состояние при адекватной терапии потенциально обратимо.
Нарушения липидного обмена служат важной причиной развития атеросклероза и его клинических осложнений. Дислипидемия в тоже время представляет собой модифицируемый фактор риска и одно из основных звеньев «порочного круга» МС. Поэтому главной «мишенью» в комплексе мер, направленных на максимальное снижение риска развития ССЗ и их осложнений у больных с МС, представляется атерогенная дислипидемия. Целью проводимой терапии должно быть достижение целевых уровней липидов наряду с коррекцией всех компонентов МС, что может гарантировать снижение сердечно-сосудистого риска. Оптимальные значения липидных параметров, которые были приняты секцией атеросклероза ВНОК в соответствии с Европейскими рекомендациями по профилактике ССЗ, представлены в табл. 1 [9].
Таблица 1. Оптимальные значения липидных параметров плазмы для больных с документированным атеросклерозом, лиц высокого и очень высокого риска осложнений атеросклероза, пациентов с сахарным диабетом 2 типа
| Липидные параметры | ммоль/л | мг/дл |
| ОХС | < 4,5 желательно < 4,0 |
< 175 желательно < 155 |
| ХС ЛПНП | < 2,0 | < 80 |
| ХС ЛПВП | > 1,0 (муж.) > 1,2 (жен.) |
> 40 (муж.) > 45 (жен.) |
| ТГ | < 1,7 | < 150 |
ОХС – общий холестерин
ХС ЛПНП – холестерин липопротеинов низкой плотности
ХС ЛПВП – холестерин липопротеидов высокой плотности
ТГ – триглицериды
Первым шагом в лечении нарушений липидного обмена должны быть немедикаментозные методы: диета, физические нагрузки, отказ от курения и алкоголя. Изменение образа жизни благотворно влияет на липидный спектр: на каждый 1кг снижения массы тела концентрация общего холестерина (ОХС) снижается на 0,05 ммоль/л, липопротеидов низкой плотности (ЛПНП) – на 0,02 ммоль/л, триглицеридов (ТГ) – на 0,015 ммоль/л, а уровень липопротеидов высокой плотности (ЛПВП) повышается на 0,009 ммоль/л [10]. Снижение веса на 5,6кг снижает на 58% риск дальнейшего прогрессирования нарушений углеводного обмена – развитие сахарного диабета 2 типа у больных с нарушением толерантности к глюкозе [11-13].
Основная цель диеты при дислипидемии – снижение уровня атерогенных липидов в крови при сохранении физиологической полноценности пищевого рациона. В настоящее время существует огромное количество диетических рекомендаций. Многие пациенты под словом «диета» подразумевают голодание и стремятся как можно быстрее сбросить лишний вес данным способом. Основным аргументом противников данного способа снижения массы тела служит рикошетный набор веса, наступающий после его окончания. Однако не стоит забывать и о том, что голодание может усугублять течение неалкогольной жировой болезни печени (НАЖБП) у больных с МС [14].
Основные принципы диетотерапии при наличии атерогенной дислипидемии у больных с МС включают:
- общий энергетический расклад принимаемой пищи с учётом рекомендаций, представленных ниже: белки – 15%, жиры – 30%, сложные углеводы – 55% общей калорийности;
- количество жира (включая растительные жиры), содержащегося во всех потребляемых в течение суток продуктах < 30%, доля насыщенных жиров < 7%;
- поступление холестерина с пищей в сутки < 200 мг;
- разнообразные свежие продукты и овощи более 400 г/сут;
- мясные продукты с высоким содержанием жира целесообразно заменять бобовыми, рыбой, птицей;
- молоко и молочные продукты с низким содержанием жира и соли (кефир, сыр, йогурт) – ежедневно;
- углеводы 55% (преимущественное употребление сложных углеводов, содержащихся в овощах, фруктах, цельнозерновых);
- сахар < 10%;
- соль 2-5 г/день;
- омега-3-полиненасыщенные жирные кислоты 1-2% – содержатся в жирной морской рыбе (лосось, тунец, скумбрия) не реже 2 раз в неделю;
- добавление в пищевой рацион растительных станолов (не менее 3г в день), которые благодаря уменьшению абсорбции холестерина позволяют снизить уровень ОХС в плазме крови на 10%, а в сочетании с диетой – на 15% [15].
- Клетчатка более 25г/сут; прием дополнительных 14г клетчатки ассоциируется с 10 % снижением общей калорийности и потерей веса на 1,9кг за 4 месяца [16-20].
Следует помнить, что даже строгое соблюдение диеты, которое, безусловно, необходимо, позволяет снизить уровень ОХС не более чем на 10%.
Залогом успеха немедикаментозных мер служат регулярные дозированные физические нагрузки с периодичностью не менее 30-45 мин 4-5 раз в неделю. Увеличение физической активности является высокоэффективным методом лечения абдоминального ожирения (АО), нарушений липидного обмена, способствует значительному уменьшению инсулинорезистентности (ИР) [18, 21-23]. Основную часть физической активности должны составлять аэробные нагрузки (кардиотренировки: ходьба, плавание, велосипед, спортивные танцы, лыжи, занятия на тренажерах «бегущая дорожка» и др.), поскольку особенностью главной мышцы организма – сердца – является постоянный полностью аэробный обмен. Положительный эффект аэробных физических нагрузок состоит в повышении функциональных резервов сердечно-сосудистой и дыхательной систем, в нормализации АД и массы тела, улучшении углеводного обмена, увеличении ЛПВП и снижении ЛПНП и триглицеридов [24, 25].
В настоящее время вред курения неоспорим. Курение в 3,5 раза повышает риск развития инсульта, приводит к прогрессированию атеросклероза. Доказано, что курение является независимым фактором риска развития и прогрессирования ССЗ, а также фактором риска внезапной смерти [26, 27]. Так, выкуривание одной сигареты вызывает повышение АД на 8-10мм рт.ст. минимум на 15 минут. Кроме того, курение снижает эффективность антигипертензивной терапии. В зарубежной литературе имеются данные отрицательного воздействия курения на липидный спектр, степень АО, степень ИР, что в целом демонстрирует более тяжёлое течение болезни у курящих в сравнении с некурящими больными с МС [28, 29]. Установлен вред не только активного, но и пассивного курения, поэтому отказ или сокращение курения должны быть неотъемлемой мерой профилактики и лечения больных с МС.
Как известно, потребление алкоголя в безопасных для здоровья дозах (не более 30г чистого алкоголя в сутки для мужчин и 20г для женщин) способствует уменьшению смертности от ССЗ преимущественно за счёт повышения уровня ХС ЛПВП. Злоупотребление алкоголем у больных с МС, помимо общеизвестного вреда, способно оказать выраженное отрицательное действие: во-первых, усугубить течение НАЖБП; во-вторых, может спровоцировать миопатию или рабдомиолиз у пациентов, принимающих статины. Поэтому целесообразно рекомендовать отказ даже от умеренных доз алкоголя [16].
При недостаточной эффективности немедикаментозных мер, а также у лиц с высоким и очень высоким риском смертельного исхода от ССЗ необходимо начинать медикаментозную терапию. За последние 20 лет арсенал липидкорригирующих средств увеличился и в наши дни представлен следующими классами препаратов:
- Ингибиторы ГМГ-КоА редуктазы (статины);
- Производные фиброевой кислоты (фибраты);
- Ингибитор абсорбции ХС в кишечнике (эзетимиб);
- Секвестранты желчных кислот (ионно-обменные смолы);
- Никотиновая кислота (ниацин);
- Омега-3-полиненасыщенные жирные кислоты (?-3 ПНЖК).
Для лечения атерогенной дислипидемии «золотым стандартом» во всём мире служит высокоэффективный класс препаратов, полностью подавляющий гидрокси-метилглутарил-КоА редуктазу (ГМГ-КоА-редуктазу) – статины [30]. Основной механизм действия статинов заключается в умеренном снижении содержания ОХС в клетках печени за счет обратимого подавления ключевого фермента синтеза холестерина – ГМГ-КоА-редуктазы, что приводит к увеличению количества рецепторов для ЛПНП и повышению выведения их из кровотока. В зависимости от дозы и химической структуры статины снижают уровень ОХС на 22–48% и ХС ЛПНП на 27–60%. В зависимости от исходной концентрации ТГ снижаются на 10–30%, тогда как уровень ХС ЛПВП увеличивается на 6–12%. Наряду с гиполипидемическим действием, статины обладают плейотропными эффектами. В экспериментальных исследованиях было показано, что статины способствуют стабилизации атеросклеротической бляшки за счет уменьшения объема липидного ядра, укрепления её оболочки и улучшения локальной функции эндотелия. Существует мнение, что плейотропные эффекты статинов наступают при снижении ХС ЛПНП на 25% [31, 32].
Многочисленные клинические исследования (4S, CARE, PROSPER, LIPID, WOSCOPS, AF CAPS/TexCAPS, HPS, CARDS, AVERT, MIRACL, REVERSAL и др.) доказали высокую эффективность статинов при атерогенной дислипидемии в аспекте снижения частоты сердечно-сосудистых осложнений, в том числе снижения риска преждевременной смерти у больных с клиническими проявлениями атеросклероза [9, 33].
Результаты эпохального исследования 4S (Scandinavian Simvastatin Survival Study) в значительной мере способствовали развитию препаратов статинов как класса.
Это было самое первое длительное плацебо-контролируемое исследование с использованием симвастатина (использовался препарат “Зокор”) 20–40 мг/сут, в котором участвовало 4444 человека с ИБС. В этой работе впервые изучалось влияние лечения симвастатином на сердечно-сосудистую и общую смертность. Исследуемая популяция – больные ИБС после инфаркта миокарда в анамнезе, в возрасте 35–70 лет, с исходным уровнем ОХС 213–309 мг/дл. Снижение уровня ХС ЛПНП за 5 лет наблюдения составило 36%, что привело к снижению общей смертности на 30% (p=0,0003). Возможность существенно снижать сердечно-сосудистую смертность (по результатам исследования на 42%) развеяла сомнения о необходимости гиполипидемической терапии у больных ИБС с целью профилактики ее осложнений, и ответило на многие вопросы по безопасности такого лечения [34].
Самое крупное исследование последнего времени – HPS (Heart Protection Study), в котором участвовало 20 536 пациентов (50% больных принимали симвастатин -использовался препарат “Зокор”, 50% – плацебо). По основным результатам HPS, прием cимвастатина в дозе 40 мг/сут в течение 5 лет позволил достоверно снизить сердечно-сосудистую смертность на 17%, частоту любого большого сердечно-сосудистого осложнения на 24% (p<0,0001) и общую смертность на 13% (p=0,0003). Среди сердечно-сосудистых причин смерти наибольшая польза от лечения симвастатином была получена при снижении комбинированной конечной точки (риск первого нефатального инфаркта и внезапной смерти) на 27% (p<0,0001). Терапия симвастатином оказала существенное влияние на частоту фатального и нефатального инсульта независимо от этиологии (-25%) и необходимость операций реваскуляризации (-24%). Впервые было показано, что снижение уровня ХС ЛПНП на 1 ммоль/л связано со снижением общей смертности, как в первичной, так и вторичной профилактике ИБС и эта польза не зависит от пола, возраста, исходных значений липидов и степени снижения ХС ЛПНП. Впервые в проспективном исследовании была убедительно показана клиническая польза применения симвастатина у больных с АГ, СД 2 типа и экстракоронарным атеросклерозом [35, 36].
На липидный профиль благоприятно влияют и фибраты – агонисты подкласса ядерных рецепторов – PPARs-?, внутриклеточных компонентов, содержащих набор ферментов, активация которых интенсифицирует процессы в ядре клетки, регулирующие синтез апобелков, окисление жирных кислот. Реализация этих механизмов активизирует печёночную липопротеидлипазу, ферменты, регулирующие гидролиз хиломикронов, ЛПОНП, ЛППП. Фибраты снижают уровни ТГ на 30-50%, ХС ЛПНП на 10-15% и повышают концентрацию ХС ЛПВП на 10-20% [37]. Дериваты фиброевой кислоты достаточно хорошо изучены в контролируемых клинических исследованиях. В исследовании WHO Cooperative Trial on Primary Prevention 10 627 мужчин в возрасте 30-59 лет без признаков ИБС были рандомизированы на прием клофибрата 1,6г в день или плацебо в течение 5 лет. Снижение уровня ОХС в плазме крови в группе больных, получавших клофибрат, составило 8%, что сопровождалось достоверным снижением количества нефатальных инфарктов на 25% (p<0,05) [38].
В другом исследовании по первичной профилактике HHS (Helsinki Heart Study) был использован другой фибрат – гемфиброзил 1200 мг/сут, который был назначен в суточной дозе 1200 мг мужчинам 40-55 лет с различными типами дислипидемий [39]. Количество инфарктов миокарда в группе гемфиброзила снизилось на 35% (p<0,02); общая смертность в группах была одинаковой.
В исследовании по вторичной профилактике VA-HIT (Veterans Affairs High-density lipoprotein cholesterol Intervention Trial) проверяли гипотезу о снижении коронарных событий у мужчин с документированной ИБС и низким уровнем ХС ЛПВП при повышении уровня ХС ЛПВП и снижении ТГ. [40]. В исследование были включены 2531 пациент со средним уровнем ХС ЛПВП 0,8 ммоль/л, которые получали гемфиброзил 1200 мг в сутки или плацебо в течение 5 лет. Первичными конечными точками в VA-HIT были количество нефатальных ИМ и сердечно-сосудистая смертность. Уровень ТГ в ходе исследования был снижен на 31%, ОХС – на 4%, уровень ХС ЛПВП достоверно увеличился на 6%, концентрация ХС ЛПНП достоверно не изменилась. К концу исследования отмечено достоверное снижение количества сердечно-сосудистых смертей, нефатальных ИМ и инсультов (комбинированная конечная точка) на 24% (p<0,001).
Результаты многоцентрового рандомизированного исследования FIELD (Fenofibrate Intervention and Event Lowering Diabetes Study) по применению фенофибрата у больных СД 2 типа в течение 5 лет показали, что препарат уменьшает число микрососудистых осложнений. В частности, было зарегистрировано достоверное снижение необходимости лазерной терапии на 30%, нетравматических ампутаций нижних конечностей на 38% и снижение прогрессирования альбуминурии в группе лечения фенофибратом [41]. Согласно основным результатам исследования при лечении фенофибратом не было достигнуто достоверного снижения нефатального ИМ и сердечно-сосудистой смертности (относительный риск 11%, p=0,16). Однако с учетом активного назначения статинов в обеих группах в ходе исследования при вторичном анализе было установлено достоверное снижение общего количества кардиоваскулярных событий на 15%(p=0,01).
Ингибитор абсорбции ХС в кишечнике (эзетимиб) – новый класс гиполипидемических средств. Основным местом действия является ворсинчатый эпителий тонкой кишки: глюкуронид эзетимиба, локализуясь на поверхности энтероцита, блокирует специфический белок Ньюмана-Пика 1 (белок способствует транспорту холестерина из просвета кишки). Предварительные результаты, проведенные в России и за рубежом показывают, что при монотерапии эзетимиб в дозе 10мг/сут снижает уровень ХС ЛПНП на 17-19%, повышает содержание ХС ЛПВП на 1,5%. Однако, основная сфера применения эзетимиба – комбинированная терапия с невысокими дозами различных статинов [42]. Исследование Двух Столиц, проведенное в нашей стране, показало, что добавление эзетимиба в дозе 10мг/сут к любому из статинов даёт дополнительное снижение уровня ХС ЛПНП на 20-30% по сравнению с монотерапией статинами [16, 43].
Недавно завершены исследования ENHANCE и SEAS, изучавшие комбинацию эзетимиба и симвастатина. В исследовании ENHANCE (Ezetimibe and Simvastatin in Hypercholesterolemia enhances atherosclerosis regression) у 720 больных с семейной гиперхолестеринемией сравнивали два режима гиполипидемической терапии: симвастатин 80мг (монотерапия) против комбинации эзетимиба 10мг с симвастатином 80мг. К концу исследования достоверной разницы по толщине комплекса интима-медиа между исследуемыми группами получено не было. Однако отмечено достоверно большее снижение уровня ХС ЛПНП в группе больных, получавших комбинацию препаратов, в связи с чем, в январе 2009 года Food and Drug Administration (FDA, USA) опубликовало официальное заявление по анализу безопасности данного исследования. В настоящее время продолжается исследование IMPROVE-IT, изучающее комбинацию симвастатина и эзетимиба в плане снижения риска сердечно-сосудистых осложнений.
В исследовании SEAS (Simvastatin and Ezetimibe in Aortic Stenosis) основной гипотезой работы было изучение влияния комбинированной терапии (эзетимиб 10мг и симвастатин 40мг) по сравнению с плацебо на количество больших коронарных событий в течение 4-х лет у 1873 больных с аортальным стенозом. Комбинация эзетимиба и симвастатина позволила добиться снижения уровня ХС ЛПНП на 61% (абсолютное снижение на 2 ммоль) [9].
К настоящему времени имеются лишь единичные данные по эффективности и безопасности эзетимиба в комбинации с фибратами. Необходимы дальнейшие клинические исследования эзетимиба и вариантов его комбинации с другими препаратами, нормализующими липидный обмен.
Секвестранты желчных кислот (ионно-обменные смолы) используются в качестве гиполипидемических средств уже более 30 лет. Ионно-обменные смолы – сложные полимерные соединения – связывают желчные кислоты, содержащие холестерин, в просвете тонкой кишки и усиливают их экскрецию с фекалиями. В результате развивается дефицит холестерина, для компенсации которого увеличивается количество мембранных рецепторов к ЛПНП, обеспечивающих дополнительный клиренс ХС ЛПНП из плазмы крови. Представителями смол являются холестирамин, колестипол и колесевелам. Эти препараты показаны больным с IIа типом гиперлипидемии. В настоящее время проходит клиническое исследование CHIPS (Controling Hypertension and Hypotension Immediately Post-Stroke) с применением колесевелама в комбинированной терапии со статинами или эзетимибом [16]. Секвестранты желчных кислот в России в настоящее время не зарегистрированы.
Никотиновая кислота (ниацин) относится к витаминам группы В, однако в высоких дозах (3-5 г/сут.) она обладает гиполипидемическим действием. Никотиновая кислота снижает синтез ЛПОНП в печени и частично блокирует высвобождение жирных кислот из жировой ткани, создавая их дефицит в плазме. В длительном исследовании CDP (Coronary Drug Project) было показано, что только в группе больных, принимавших никотиновую кислоту, в отдаленном периоде смертность от всех причин была на 11% ниже по сравнению с группой плацебо (исследование проходило в тот период, когда статины ещё не вошли в клиническую практику). Никотиновая кислота увеличивает ЛПВП на 20–30%, снижает уровень ТГ на 40–50% и ЛПНП на 20–30%, и считается эффективным препаратом для повышения уровня ЛПВП [44].
Рандомизированное исследование HATS (HDL – Atherosclerosis Treatment Study) показало эффективность комбинированной терапии ниацином замедленного высвобождения 2-4г с симвастатином 10-20мг в сутки в течение 3 лет в снижении риска смерти, инфаркта миокарда, инсульта или необходимости в операциях реваскуляризации. В настоящее время никотиновая кислота не нашла широкого применения в медицине ввиду многих противопоказаний, предостережений. Пациентам с МС, страдающих СД 2 типа, назначение ниацина нежелательно. Следует отметить, что на сегодняшний день убедительных данных о применении комбинации статинов с никотиновой кислотой недостаточно для того, чтобы рекомендовать её в клинической практике.
Омега-3-полиненасыщенные жирные кислоты (O-3 ПНЖК) в больших дозах (2-4 г/ сутки) применяют для лечения IIb – V фенотипов гиперлипидемии. В настоящее время в России зарегистрирован препарат Омакор, состоящий из высокоочищенных и высококонцентрированных ?-3 ПНЖК (около 90%). В 1997 году были опубликованы результаты исследования, свидетельствующие о том, что Омакор в дозе 2-4 г/сутки снижает уровень ТГ в крови на 45% (р<0,0001). В 1999 году результаты многоцентрового исследования GISSI – Prevenzione (Gruppo Italiano per lo Studio della Sopravvivenza nell,Infarcto miocardico Prevenzione) показали положительное влияние высокоочищенных ?-3 ПНЖК на клинические исходы у больных, перенесших инфаркт миокарда. Оказалось, что применение высокоочищенных O-3 ПНЖК (Омакор) в дозе 1000 мг/ день в сочетании со стандартной терапией достоверно снижает концентрацию ТГ на 4,6%, общую смертность на 21% и риск внезапной смерти на 45% у постинфарктных пациентов по сравнению с группой контроля [45].
В 2008 году закончилось рандомизированное плацебо-контролируемое исследование GISSI – HF (Gruppo Italiano per lo Studio della Sopravvivenza neH,Insufficienza Cardiaca Heart Failure Study) у больных с сердечной недостаточностью, которые получали 1г ?-3 ПНЖК (n=3494) или плацебо (n=3481) в дополнение к стандартной терапии в течение 3,9 лет. По результатам этого исследования было отмечено достоверное снижение общей смертности на 9% в группе пациентов, принимавших Омакор [9]. Необходимы дальнейшие исследования эффективности ?-3 ПНЖК, а пока пациентам необходимо рекомендовать употреблять 2-3 раза в неделю рыбу северных морей (скумбрия, тунец, лосось, палтус и т.д.).
Как видно, терапевтические возможности в борьбе с нарушениями липидного обмена у больных с МС достаточно широки. Конечно, самым назначаемым гиполипидемическим классом служат статины. Однако несмотря на большое количество крупных клинических исследований, доказавших высокую эффективность ингибиторов ГМГ-КоА-редуктазы, сохраняется тенденция отсутствия адекватного лечения и профилактики ССЗ. Среди множества возможных причин недостаточного использования статинов основными служат: переоценка риска побочных эффектов и осложнений терапии статинами, формальное отношение врачей и больных к профилактике и лечению нарушений липидного обмена, а также недооценка эффективности использования статинов как средств профилактики и лечения атеросклероза и других ССЗ.
В настоящее время внимание исследователей привлекает новое направление в лечении атерогенной дислипидемии у больных с НАЖБП при МС – использование комбинации статинов и урсодезоксихолевой кислоты (УДХК). С одной стороны, назначение УДХК является патогенетически обоснованным при НАЖБП благодаря её цитопротективному, иммуномодулирующему и антиапоптотическому механизмам действия [46, 47, 48]. Известно, что применение УДХК при НАЖБП в дозе 10-15 мг/кг в сутки, длительностью 6 месяцев и более оказывает положительное влияние на биохимические показатели, ведёт к снижению активности трансаминаз, щелочной фосфатазы (ЩФ), гамма-глютмилтранспептидазы (ГГТ) и уменьшению выраженности стеатоза и воспаления по данным гистологического исследования печени [49, 50]. После нормализации активности трансаминаз на фоне приёма УДХК больному можно назначать статины.
С другой стороны, гипохолестеринемический механизм действия УДХК можно использовать в лечении дислипидемии у данной категории больных. В литературе имеются данные о том, что эффективность комбинации малых доз статинов и УДХК выше, чем использование удвоенной дозы статинов. В испанском исследовании при комбинированной терапии симвастатином 20мг/сут и УДХК 300мг/сут в течение 4 месяцев, по сравнению с монотерапией симвастатином 40мг/сут, было достигнуто более выраженное снижение уровня ЛПНП (р=0,0034). Аналогичный результат был получен в этом же исследовании в группе больных, принимавших аторвастатин в дозе 20мг/сут и УДХК 300мг/сут в течение 4 месяцев, по сравнению с монотерапией аторвастатином 40мг/сут (р=0,0037). [51].
На базе кафедры пропедевтики внутренних болезней и клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии имени В.Х. Василенко (заведующий кафедрой и директор клиники – академик РАМН, профессор В.Т. Ивашкин) под руководством профессора О.М. Драпкиной была выполнена диссертационная работа, посвящённая изучению нарушений липидного обмена у больных с метаболическим синдромом, а также оценке эффективности и безопасности липидкорригирующей терапии. 77 пациентов с МС, учитывая цели и задачи проводимого исследования, после лабораторно-инструментального обследования были рандомизированы в 3 группы лечения:
- 1 – группа больных с дислипидемией, получавшая УДХК в дозе 1250мг в сутки (n=22),
- 2 – группа больных с дислипидемией, получавшая симвастатин 40-60мг в сутки (n=27),
- 3 – группа больных с дислипидемией и повышенным уровнем печёночных трансаминаз, получавшая симвастатин и УДХК (n=28).
Результаты этой работы продемонстрировали возможность назначать статины у больных с повышенным уровнем сывороточных трансаминаз в рамках НАЖБП при МС после курса УДХК, а самое главное, высокую эффективность комбинированной терапии атерогенной дислипидемии статинами и УДХК у больных с выраженным абдоминальным ожирением. При проведении сравнительного анализа влияния симвастатина, УДХК и их комбинации на липидный обмен статистически значимые изменения были обнаружены для следующих показателей липидного спектра: 1. уровень ОХС: при лечении комбинацией препаратов уже через 3 месяца выявлено достоверно большее снижение в сравнении с группой больных, получавших симвастатин (р<0,05); 2. уровень ТГ: при лечении комбинацией препаратов через 6 месяцев выявлено достоверно большее снижение в сравнении с группой больных, получавших УДХК (р<0,05); 3. уровень ЛПНП: при лечении комбинацией препаратов через 3 месяца выявлено достоверно большее снижение в сравнении с группой больных, получавших симвастатин (р<0,05). [52]. Таким образом, комбинация статина и УДХК оправдана в лечении атерогенной дислипидемии у больных с МС.
Добиться значимого успеха в лечении МС возможно, только воздействуя на все его патогенетические звенья: АО, ИР, АГ. Интересно, что многие из препаратов, направленных на коррекцию основных компонентов МС благотворно влияют и на липидный обмен. Так, эффективный для лечения ожирения ингибитор обратного захвата серотонина и норадреналина – сибутрамин – продемонстрировал себя с положительной стороны во многих клинических исследованиях [53]. В 2004 году на 13 Европейском конгрессе по ожирению (Прага, Чешская республика, 26 мая 2004 года) были представлены данные о благоприятном влиянии препарата на липидный профиль [54]. Однако необходимо дальнейшее изучение влияния лекарственных средств для снижения массы тела на весь комплекс нарушений при МС.
Поскольку ключевую связующую роль между компонентами МС играет ИР, в качестве патогенетического лечения применяются препараты, улучшающие инсулиночувствительность тканей – инсулиносенситайзеры. Одним из препаратов выбора фармакотерапии МС является метформин, относящийся к группе бигуанидов. Основное действие метформина направлено на преодоление ИР на всех уровнях: в печени, в скелетной мускулатуре, в жировой ткани [55, 56]. Клинические исследования продемонстрировали высокую эффективность метформина, в том числе и в отношении дислипидемии: он улучшает показатели липидного спектра (снижает ЛПНП, ЛПОНП, повышает ЛПВП). Уменьшение ИР на фоне применения метформина обуславливает эффективность его применения при НАЖБП, улучшая клинико-лабораторные и гистологические показатели [57].
Своевременная диагностика МС и правильное ведение пациента с использованием немедикаментозных и медикаментозных средств, направленных на все звенья патогенеза, позволит продлить жизнь и значительно улучшить её качество. Но только достижение целевых уровней липидов наряду с коррекцией других факторов может гарантировать значимое снижение сердечно-сосудистого риска. Сегодня в арсенале врача-интерниста имеется широкий спектр средств, улучшающих липидный обмен. Снижение высокого атерогенного потенциала МС позволит предотвратить развитие сердечно-сосудистых осложнений.
Литература
1. Mamedov M, Suslonova N, Lisenkova I. et al. Metabolic syndrome prevalence in Russia: Preliminary results of a cross-sectional population study. Diabetic and Vascular Disease research. 2007; 4(1):46-47.
2. Zimmet P., Shaw J., Alberti G. Preventing type 2 diabetes and the dysmetabolic syndrome in the real world: a realistic view. Diabetic medicine. 2003; 20 (9):693-702.
3. Lakka H. M., Laaksonen D. E., Lakka T. A., Niskanen L. K., Kumpusalo E. The metabolic syndrome and total cardiovascular disease mortality in middle-aged men. JAMA. 2002; 4; 288 (21):2709–16.
4. Rodriquez-Colon S., Mo J., Duan Y. et al. Metabolic syndrome clusters and the risk of incident stroke: the atherosclerosis risk in communities (ARIC) study. Stroke. 2009; 40(1):200-5.
5. Cornier M.-A., Dabelea D., Hernandez T. L. et al. The Metabolic Syndrome. Endocr. Rev. 2008; 29(7):777-822.
6. Kohli P, Greenland P. Role of the metabolic syndrome in risk assessment for coronary heart disease. JAMA. 2006; 295:819–21.
7. Protopsaltis I., Korantzopoulos P. et al. Metabolic Syndrome and Its Components as Predictors of Ischemic Stroke in Type 2 Diabetic Patients Stroke. Stroke. 2008; 39(3):1036-8.
8. Wannamethee SG, Shaper AG, Lennon L, Morris RW. Metabolic syndrome vs Framingham risk score for prediction of coronary heart disease, stroke, and type 2 diabetes mellitus. Arch Intern Med. 2005; 165:2644–50.
9. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации (IV пересмотр). Кардиоваскулярная терапия и профилактика. 2009; 8(6):Приложение 3.
10. Долженко М.Н. Пациент с ишемической болезнью сердца и хроническим стеатогепатитом: как проводить гиполипидемическую коррекцию. Украинский Мед Журнал. 2007; 57(1):8-11.
11. Kelley D., et al. Relative effects of calorie restriction and weight loss in noninsulin-depended diabetes mellitus. J Clin Endocrinol Metab. 1993; 77:1287-93.
12. Klein S, Fontana L, et al. Absence of an effect of liposuction on insulin action and risk factors for coronary heart disease. N Engl J Med. 2004; 350:2549-57.
13. Wing R, Blair E et al. Caloric restriction per se is a significant factor in improvements in glycemic control and insulin sensitivity during weight loss in obese NIDDM patients. Diabetes Care. 1994; 17:30-6.
14. Буеверов А.О., Маевская М.В. Некоторые патогенетические и клинические вопросы неалкогольного стеатогепатита. Клинические перспективы гастроэнтерологии, гепатологии. 2003; 3:2-7.
15. Драпкина О.М., Клименков А.В., Ивашкин В.Т. Новые методы лечения дислипидемии. Российские медицинские вести. 2007; 2:18-25.
16. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза: Российские рекомендации III пересмотр 2007. ВНОК, секция атеросклероза. М., 2007; 44с.
17. Драпкина О.М., Ашихмин Я.И., Ивашкин В.Т. Питание и сердечно-сосудистые заболевания. Трудный пациент. 2006; 4 (8):43-8.
18. Chipkin S., Black S., Braun B. The balance between exercise and diet: impact on insulin sensitivity. Current Opinion in Endocrinology and Diabetes. 2005; 12:152-6.
19. European Guidelines on cardiovascular disease prevention in clinical practice. European Heart Journal. 2003; 24:1601-10.
20. World Health Organisation. Diet, nutrition and the prevention chronic disease. Report of a Joint/FAO Expеrt Consultation. Geneva. WHO. 2003.
21. Ross R., Dagnone D., et al. Reduction in obesity and related co morbid conditions after diet-induced weight loss or exercise-induced weight loss in men: a randomized controlled trial. Ann Intern Med. 2000; 133:92-103.
22. Ross R., Yanssen I., et al. Exercise-induced reduction in obesity and insulinresistent in women: a randomised controlled trial. Obes Res. 2004; 12:789-98.
23. Ryan D. Risk and benefits of weight loss: challenges to obesity research. European Heart Journal Supplements (Supplement L). 2005; 7:27-31.
24. Корнеева О.Н. Регуляция чувствительности к инсулину: диета и физические нагрузки. Российские медицинские вести. 2007; 2:36-43.
25. Houmard J., Shaw C., Tanner C. Effect of short-term exercise training on insulin-stimulated PI 3-kinase activity in human skeletal muscle. Am J Physiol Endocrinol Metab. 1999; 277:1055-60.
26. Bazzano L., He J. et al. Relationship between cigarette smoking and novel risk factors for cardiovascular disease in the United States. Ann Intern Med. 2003; 138(11):891-7.
27. Goldenberg I., Jonas M. et al. Current smoking, smoking cessation, and the risk of sudden cardiac death in patients with coronary artery disease. Arch Intern Med. 2003; 163(19):2301-5.
28. Berlin I. Smoking-induced metabolic disorders: a review. Diabetes Metab. 2008; 34(4Pt 1):307-14.
29. Chouraki V., Wagner A. et al. Smoking habits, waist circumference and coronary artery disease risk relationship: the PRIME study. Eur J Cardiovasc Prev Rehabil. 2008; 15(6):625-30.
30. Eidelman R.S., Lamas G.A., Hennekens C.H. The New National Cholesterol Education Program Guidelines. Clinical Challenges for More Widespread Therapy of Lipids to Treat and Prevent Coronary Heart Disease. Arch Intern Med. 2002; 162:2033-6.
31. Мамедов М.Н. Проблемы использования статинов в России. Consilium Medicum. 2007; 9: 5.
32. Davidson M. The mobil lipid clinic. Lippincott Williams&Wilkins: Philadelphia, 2002; 61–133.
33. Сусеков А.В. Ингибиторы ГМГ-КоА-редуктазы при вторичной профилактике атеросклероза: 30 лет спустя. Consilium Medicum. 2006; 7(11):24-7.
34. Scandinavian Simvastatin Survival Study Group: Randomized trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet. 1994; 344:1383–9.
35. Collins R. Heart Protection Study – Main results. Late-breaking clinical trails. American Heart Association. Scientific Sessions, 2001. 13 November 2001. Anaheim. California. USA.
36. Heart Protection Study Collaborative Group: Lifetime cost-effectiveness of simvastatin in a range of risk groups and age groups derived from a randomised trial of 20536 people. BMJ. 2006; 333:1145-48.
37. Chapman MJ. Fibrates: therapeutic review. Brit J Diabet Vascul Dis. 2006; 6:11-20.
38. Committee of Principal Investigators. A cooperative trial in the primary prevention of ischemic heart disease using clofibrate. Br Heart J. 1978; 40:1069-118.
39. Frick M., Elo O., Haapa K. et al. Helsinki Heart Study: Primary prevention trial with gemfibrozil in middle aged men with dyslipidemia. Safety of treatment, changes in risk factors and incidence of coronary heart disease. N Engl J Med. 1987; 317:1237-45.
40. Rubins H., Robins S., Collins D. et al. for the Veterans Affaires High – Density Lipoprotein Cholesterol Intervention Trial Study Group. Gemfibrozil for the Secondary prevention of coronary heart disease in men with low levels of high density lipoprotein cholesterol. N Engl J Med. 1999; 341:410-8.
41. Keech A. et al. FIELD study investigators. Effects of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomized controlled trial. Lancet. 2005; 366:1849-61.
42. Сусеков А.В. Место эзетимиба в лечении дислипидемий и атеросклероза. Фарматека. 2004; 14(91):1-5.
43. Ballantyne C., Abate N. et al. Dose-comparison study of the combination of ezetimibe and simvastatin (Vytorin) versus atorvastatin in patients with hypercholesterolemia: the Vytorin Versus Atorvastatin (VYVA) study. Am. Heart J. 2005; 149:464-73.
44. Singh I.M., Shishehbor M.H., Ansell B.J. High-Density Lipoprotein as a Therapeutic Target A Systematic Review. JAMA. 2007; 298(7):786-98.
45. Studer M., Briel M., Leimenstoll B. et al. Effect of Different Antilipidemic Agents and Diets on Mortality. A Systematic Review. Arch Intern Med. 2005; 165:725-30.
46. Драпкина О.М. Неалкогольный стеатогепатит. Рациональная гепатопротекция. Медицинский вестник. 2006; 42:14-5.
47. Angulo P. Treatment of nonalcoholic fatty liver disease. Ann Hepatol. 2002; 1(1):12-9.
48. Siebler J., Gall P. Treatment of nonalcoholic fatty liver disease. World J Gastroenterol. 2006; 12(14):2161-7.
49. Буеверов А.О. Возможности клинического применения урсодезоксихолевой кислоты. Consilium Medicum. 2005; 7 (6):18-22.
50. Корнеева О.Н., Драпкина О.М., Буеверов А.О., Ивашкин В.Т. Неалкогольная жировая болезнь печени как проявление метаболического синдрома. Клинические перспективы гастроэнтерологии, гепатологии. 2005; 4:24-7.
51. Cabezas Gelabert R. Effect of ursodeoxycholic acid combined with statins in hypercholesterolemia treatment: a prospective clinical trial. Rev Clin Esp. 2004; 204(12):632-5.
52. Буеверова Е.Л. Нарушения липидного обмена у больных с метаболическим синдромом: Дис….канд. мед. наук. Москва, 2009; 174с.
53. Stock M.J. Sibutramine: a review of the pharmacology of a novel anti-obesity agent. Int. J. Obes. 1997; 21:25-9.
54. Sabuncu T. et al. The effect of 1-yr sibutramine treatment on glucose tolerance, insulin sensivity and serum lipid profiles in obese subjects. Diabetes Nutr Metab. 2004; 17(2):103-7.
55. Gianarelli R., Aragona M. et al. Reducing insulin resistance with metformin: the evidence today. Diabetes and metabolism. 2003; 29:6S28-6S35.
56. Urso R. Metformin in non-alcoholic steatohepatitis. Lancet. 2002; 359:355-6.
57. Marchesini G. Metformin in non-alcoholic steatohepatitis. Lancet. 2001; 358:893-4.
Нарушения липидного обмена

Версия: Клинические рекомендации РФ 2023 (Россия)
Категории МКБ:
Гиперхиломикронемия (E78.3), Другие гиперлипидемии (E78.4), Смешанная гиперлипидемия (E78.2), Чистая гиперглицеридемия (E78.1), Чистая гиперхолестеринемия (E78.0)
Разделы медицины:
Гериатрия, Кардиология, Эндокринология
Общая информация
Краткое описание
Разработчик клинической рекомендации:
- Общероссийская общественная организация «Российское кардиологическое общество» (РКО)
При участии:
- Автономная некоммерческая организация “Национальное общество по изучению атеросклероза” (НОА)
- Российская ассоциация эндокринологов (РАЭ)
- Российское общество кардиосоматической реабилитации и вторичной профилактики (РосОКР)
- Общероссийская общественная организация “Российское научное медицинское общество терапевтов” (РНМОТ)
- Евразийская ассоциация кардиологов
- Евразийского общества терапевтов (ЕАТ)
- Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров»
Одобрено на заседании Научно-практического совета Министерства здравоохранения Российской Федерации (заседание от 27.12.2022г)
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Клинические рекомендации
Нарушения липидного обмена
Возрастная группа: Взрослые
Год утверждения: 2023 г.
Пересмотр не позднее: 2025
Дата размещения: 14.02.2023
Статус: Действует
ID: 752
Применение отложено
Определение заболевания или состояния (группы заболеваний или состояний)
Дислипидемии (ДЛП) — состояния, когда концентрации липидов и липопротеидов крови выходят за пределы нормы, могут быть вызваны как приобретенными (вторичными), так и наследственными (первичными) причинами [8].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
E78.0 Чистая гиперхолестеринемия
Семейная гиперхолестеринемия
Гиперлипопротеидемия Фредриксона, тип IIa
Гипер-бета-липопротеидемия
Гиперлипидемия, группа A
Гиперлипопротеидемия с липопротеидами низкой плотности
E78.1 Чистая гиперглицеридемия
Эндогенная гиперглицеридемия
Гиперлипопротеидемия Фредриксона, тип IV
Гиперлипидемия, группа B
Гипер-пре-бета-липопротеидемия
Гиперлипопротеидемия с липопротеидами очень низкой плотности
E78.2 Смешанная гиперлипидемия
Обширная или флотирующая бета-липопротеидемия
Гиперлипопортеинемия Фредриксона, типы IIb или III
Гипербеталипопротеидемия с пре-бета-липопротеидемией
Гиперхолестеринемия с эндогенной гиперглицеридемией
Гиперлипидемия, группа C
Тубоэруптивная ксантома
Ксантома туберозная
E78.3 Гиперхиломикронемия
Гиперлипопротеидемия Фредриксона, типы I или V
Гиперлипидемия, группа D
Смешанная гиперглицеридемия
E78.4 Другие гиперлипидемии
Семейная комбинированная гиперлипидемия
Облачная МИС “МедЭлемент”
Облачная МИС “МедЭлемент”

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место – 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
ДЛП классифицируют в зависимости от того, уровень каких именно липидов и липопротеидов выходит за пределы нормы. Крайне важно дифференцировать первичные и вторичные дислипидемии, так как в этих случаях принципиально отличается тактика лечения. В настоящее время ВОЗ принята классификация Fredrickson (1976), согласно которой выделяют несколько ее фенотипов (Таблица 1, Приложение А3). Следует подчеркнуть, что данная классификация не устанавливает диагноз, а лишь фиксирует тип ДЛП, вне зависимости от того, является ли она приобретенной или наследственной. Класификация также позволяет определить риск развития атеросклероза в зависимости от типа ДЛП. Так, IIа, IIb и III типы являются атерогенными, в то время как I, IV и V типы – «относительно» атерогенными. Классификация наследственных (семейных) дислипидемий приведена в таблице 2, приложение А3.
Принципы формулировки диагноза
Примеры формулировки диагноза
Гиперлипидемия (Гиперлипопротеидемия – ГЛП) IIa типа. Гиперлипопротеидемия(а).
Смешанная гиперлипидемия.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Первичные дислипидемии имеют генетическую природу, развиваются в результате аномалий генов, которые регулируют функции рецепторов, ферментов или транспортных белков, участвующих в липидном обмене. В этих случаях они проявляются как семейные (наследственные) нарушения липидного метаболизма и относятся к первичным моногенным ДЛП. СГХС – это наследственное аутосомно-доминантное заболевание, обусловленное мутациями генов, кодирующие рецептор липопротеидов низкой плотности (LDLR), аполипопротеин В-100 (APOB) и профермента пропротеин-конвертаза субтилин/кексин типа 9 (PCSK9), сопровождающееся стойким повышением уровня холестерина (ХС) липопротеидов низкой плотности (ЛНП) и ранним развитием атеросклероза. Заболевание проявляется в виде двух форм: менее тяжелой гетерозиготной и более тяжелой гомозиготной [9]. Но в подавляющем большинстве случаев они развиваются как первичные полигенные ДЛП, т.е. являются следствием сочетания слабых генетических влияний с факторами внешней среды: курением, нарушением диеты, малоподвижным образом жизни. Наиболее атерогенными ДЛП являются изолированная гиперхолестеринемия (ГХС) (фенотип IIа), представленная семейной и полигенной ГХС, комбинированная гиперлипидемия (различные фенотипы гиперлипидемии в одной семье). Менее атерогенна изолированная гипертриглицеридемия (ГТГ) (фенотип IV или V). ГТГ натощак может быть связана с рядом факторов, внешних и внутренних. К внешним факторам, способствующим развитию ГТГ и, соответственно, высокой ее распространенности в популяции, относятся избыточное питание с преобладанием жирной пищи, простых углеводов с высоким гликемическим индексом (сахар, глюкоза), а также избыточное потребление алкоголя, длительный прием ряда лекарств, в первую очередь глюкокортикоидов, неселективных бета-адреноблокаторов. Вторичная ГТГ встречается значительно чаще первичной и может быть обусловлена, в первую очередь, инсулинорезистентностью и связанными с ней состояниями: СД 2 типа, метаболическим синдромом и ожирением. К метаболическим факторам, способствующим формированию ГТГ, относится низкая активность липолитических ферментов, в частности, периферической липопротеинлипазы (ЛПЛ), которая определяется или генетическими особенностями фермента, или повышением содержания в липопротеидах ингибиторов ЛПЛ в первую очередь апоCIII [10, 11]. Среди первичных причин повышения ТГ следует упомянуть наследственные механизмы (гиперпродукция ЛОНП, дефект гидролиза ТГ, дефект клиренса ремнантов ТГ в печени). [12]. Основными причинами вторичных ДЛП являются сахарный диабет (СД), гипотиреоз, хроническая болезнь почек (ХБП).
Патогенез атеросклероза, ассоциированного с ДЛП
Атеросклероз проявляется уплотнением сосудистой стенки и образованием атеросклеротических бляшек. Это динамичный процесс, для которого характерно как прогрессирование, так и обратное развитие изменений в стенке артерии. Однако со временем атеросклероз прогрессирует, приводя, в итоге, к клиническим проявлениям заболевания. К настоящему времени сложилось четкое представление об атеросклерозе как мультифакториальном заболевании, в основе которого лежат сложные нарушения в биохимических, иммунологических и молекулярно-генетических процессах. Сегодня доминируют две гипотезы развития и становления атеросклероза: гипотеза «ответ на повреждение» и липидно-инфильтрационная гипотеза. Гипотеза «Ответ на повреждение» ставит во главу угла нарушение целостности эндотелия в качестве инициирующего фактора атеросклеротического процесса. Факторы, вызывающие повреждение эндотелия, весьма многообразны, но наиболее распространены окись углерода, поступающая в кровь при активном и «пассивном» курении, повышение артериального давления, дислипидемия, в особенности ГХС, обусловленная либо семейной предрасположенностью, либо вредными привычками, в первую очередь, диетическими погрешностями. В качестве повреждающих агентов могут выступать модифицированные (окисленные, десиалированные) липопротеиды и целый ряд других, как эндогенных, так и экзогенных факторов. На месте повреждения эндотелия происходит адгезия моноцитов и тромбоцитов, сопровождающаяся миграцией моноцитов в интиму. Прогрессирующее утолщение интимы ведет к развитию гипоксии внутри бляшки и в близлежащих участках сосуда. Гипоксия является возможной причиной развития некротических изменений в ядре бляшки и усиленной васкуляризации бляшки из системы ваза вазорум адвентиции. Эти сосуды в сердцевине бляшки являются источником микрогеморрагий (апоплексии) в ней, что в свою очередь ведет к усилению ее тромбогенной активности. В результате ослабления мышечно-эластического слоя сосуда в коронарных артериях происходит их ремоделирование с дилатацией, причем внутренний диаметр просвета сосуда какое-то время поддерживается «нормальным», до тех пор, пока прогрессирующий рост бляшки не превысит компенсаторные возможности медиального слоя артерии, и не приведет к прогрессирующему сужению ее просвета. Именно на этом этапе бляшки приобретают характер нестабильных и играют основную роль в развитии осложнений атеросклероза. Кроме того, происходит изменение фенотипа гладклмышечных клеток, который при поврежедении сосудистой стенки, из сократительного переходит в секреторный с высвобождением провоспалительных цитокинов и активацией молекул адгезии.
Липидная теория атеросклероза предполагает пусковым моментом в развитии атеросклероза инфильтрацию интимы и субэндотелия липидами и липопротеидами. По мере накопления липидов в сердцевине бляшки, происходит увеличение ее размеров, в результате чего фиброзная покрышка бляшки под действием специфических энзимов (эластаз, металлопротеиназ) истончается и при определенных условиях (повышение артериального давления, значительная физическая нагрузка) разрывается. Разрыв сопровождается активацией каскада коагуляции крови, агрегации тромбоцитов с образованием тромба, блокирующего просвет сосуда. Клинически этот процесс проявляется, в зависимости от локализации либо нестабильной стенокардией, либо инфарктом миокарда (ИМ), либо ишемическим инсультом.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Наиболее актуальные данные о распространенности нарушений липидного обмена в РФ получены в ходе многоцентрового исследования ЭССЕ-РФ, проведенного в 13 регионах РФ с включением 21048 человек [13]. Распространенность ГХС (уровень общего холестерина (ОХС) ≥5,0 ммоль/л) в среднем составила 58,4±0,34%. Существенных различий уровня ХС у мужчин и женщин не выявлено. С возрастом распространенность ГХС увеличивается практически в 2 раза: от 37,7±0,73% в возрастной группе 25—34 года до 74,5±0,54% среди лиц в возрасте от 55 до 64 лет (p <0,01). Независимо от пола среди жителей сельской местности ГХС встречается чаще, чем среди горожан (63,2±0,82 и 57,4±0,38% соответственно; p <0,001). Атерогенные сдвиги в липидном профиле в виде ГХС обусловлены в основном повышенным (≥3,0 ммоль/л) уровнем ХС ЛНП. Достоверно более высокая распространенность повышенного уровня ХС ЛНП у жителей села по сравнению с горожанами (62,4±0,60% против 59,2±0,38%; p<0,05) обусловлена в основном более высокими значениями этого показателя среди женщин (61,3±1,08% против 56,5±0,48%; p<0,05). Повышенный уровень ТГ обнаружен у 30,2±0,52% мужчин всей выборки, что достоверно выше, чем у женщин (20,1±0,34%; p<0,0001). Распространенность высокого уровня ТГ связана с возрастом, особенно это харакерно для женщин: 8,8±0,59% в младшей возрастной группе (25-34 года) и 34,4±0,71% среди женщин в возрасте 55-64 лет (p<0,0001). В то же время, частота гипертриглицеридемии достоверно выше у мужчин с низким уровнем благосостояния по сравнению с мужчинами с высоким уровнем благосостояния (30,9±0,66% против 23,8±3,41%; p<0,05). У жителей села распространенность ГТГ незначительно, но достоверно выше, чем у горожан (p<0,05 для всех случаев). Низкий уровень ХС ЛВП (меньше 1,0 ммоль/л для мужчин и 1,2 ммоль/л для женщин) обнаружен в 19,5% случаев.
Так же, результаты исследования ЭССЕ-РФ, показали, что 23% лиц из популяции имели выраженное повышение уровня ОХС >6,2 ммоль/л, а выраженное повышение уровня ХС ЛНП >4,2 ммоль/л встречалось в 20,6%[152].
Взаимосвязь ДЛП с риском развития сердечно-сосудистых осложнений
Крупнейшим проспективным исследованием было исследование MRFIT (Multiple Risk Factor Intervention Trial). У 361662 обследованных мужчин 35-57 лет были определены основные факторы риска ИБС, включая липиды сыворотки крови. Впервые был определен пороговый уровень ОХС (5,2 ммоль⁄л), с которого регистрируется значительный прирост смертности от ИБС. Абсолютный риск ИБС при самых высоких средне-популяционных значениях ОХС был в 20 раз выше, чем при наиболее низких уровнях, равных 4,7 ммоль⁄л [14].
Мета-анализ 4-х проспективных эпидемиологических исследований (Фремингемское, MRFIT, Coronary Primary Prevention Trial, Lipid Research Clinic) выявил зависимость повышения уровня ХС ЛВП на 1 мг⁄дл и снижением на 2-3% риска ИБС, независимо от других ФР, включая ХС ЛНП [15].
В мета-анализе 17 проспективных популяционных исследований было показано, что повышение ТГ сыворотки крови на 1 ммоль⁄ л ассоциируется с увеличением новых случаев ИБС на 32% у мужчин и на 76% – у женщин [15]. По данным крупнейшего эпидемиологического исследования (Framingham Study), уровень ТГ более 1,7 ммоль/л означает достоверно более высокий риск развития ССО [15]. При достижении целевого уровня (ЦУ) ХС ЛНП <1,8 ммоль/л риск ССО у пациентов с ХС ЛВП <1,0 ммоль/л на 64% выше, чем пациентов с ХС ЛВП ≥1,4 ммоль/л [16]. Повышенные уровни ТГ и низкий уровень ХС ЛВП синергично увеличивают риск сердечно-сосудистых событий у пациентов с уже достигнутыми ЦУ ХС ЛНП (<2,1 ммоль/л) [17]. Показано, что у пациентов с ТГ более 2,3 ммоль/л и одновременно ХС ЛВП менее 0,8 ммоль/л, риск ССО увеличивается в 10 раз по сравнению с пациентами с нормальными значениями ТГ и ХС ЛВП [17, 18].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
К клиническим проявлениям заболевания приводят прогрессия атеросклеротического процесса, вызванного ДЛП. В зависимости от преимущественно пораженного сосудистого бассейна комплекс симптомов и синдромов широко варьирует. Основным осложнением атеросклероза коронарных артерий является ИБС, которая клинически проявляется стенокардией, ИМ, с частым исходом в хроническую сердечную недостаточность. Поражение магистральных артерий головного мозга проявляется симптомами его хронической ишемии с последующим развитием атеросклеротической энцефалопатии и/или инсульта. Атеросклероз артерий нижних конечностей сопровождается клинической картиной перемежающей хромоты. При отсутствии соответствующего лечения заболевание прогрессирует и может закончиться развитием гангрены нижних конечностей.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза:
Диагноз ДЛП на основании значения липидных параметров устанавливается в соответствии с пороговыми значениями, указанными в таблице 2, Приложение А3.
Современный алгоритм обследования состоит из следующих основных этапов:
-
выявление основных факторов риска (ФР) (таблица 3, Приложение А3)
-
выявление клинических симптомов атеросклероза (данные опроса и осмотра);
-
определение липидного профиля (венозная кровь) с расчетом ХС ЛНП, ХС неЛВП;
-
оценка сердечно-сосудистого риска по шкале SCORE2;
-
исключение/верификация субклинического и клинически значимого атеросклероза (инструментальные методы обследования).
Жалобы и анамнез
Многие пациенты с повышенным уровнем липидов сыворотки крови могут не иметь никаких жалоб. Симптомы зависят от локализации атеросклеротического процесса – сосудистого бассейна, который преимущественно вовлечен в процесс. Поражение коронарного русла приводит к появлению болей в левой половине грудной клетки, загрудинной области при физической нагрузке или в покое, нарушениям сердечного ритма (жалобы на неритмичное, резко учащенное сердцебиение или ощущение «замирания», «перебоев в работе сердца»), одышки, отеков нижних конечностей. При локализации атеросклеротического процесса преимущественно в цереброваскулярном бассейне превалируют жалобы на головную боль, субъективное чувство головокружения, снижение памяти, внимания, работоспособности, появление «шума в ушах», «шума в голове». Развитие облитерирующего атеросклероза артерий нижних конечностей приводит к перемежающей хромоте, в тяжелых случаях – появлению интенсивных болей в нижних конечностях в покое, больше в ночное время, в горизонтальном положении пациента (интенсивность болевого синдрома может снижаться после пациента перехода в положение сидя/стоя).
На первом этапе обследования собирается анамнез, во время которого выясняется наличие у пациента ИБС, АГ, СД, атеросклероза периферических артерий, семейной гиперхолестеринемии (СГХС), метаболического синдрома, ожирения, ХБП. При сборе семейного анамнеза, особое внимание должно уделяться раннему проявлению ССЗ у родственников пациента 1-й линии родства.
Физикальное обследование
-
Всем пациентам для выявления клинических признаков нарушений липидного обмена и признаков состояний/заболеваний, обусловленных нарушениями липидного обмена, рекомендовано проводить физикальное обследование в объеме: осмотр (липоидная дуга роговицы у лиц моложе 45 лет, ксантелазмы, ксантомы); пальпация основных магистральных артерий верхних и нижних конечностей, сонных артерий; определение характера пульса; аускультация сердца и магистральных сосудов; измерение окружности талии [153-154].
ЕОК/ЕОА нет (УУР C, УДД 5)
Комментарии. Ксантомы (xanthomata) – это очаговые образования различного цвета (от нормального до желто-коричневого, оранжевого или розового); чаще всего располагаются в области сухожилий, суставов, на ладонях, стопах, ягодицах, бёдрах. Гистологически ксантомы представляют собой скопление ксантомных (пенистых) клеток, клеток-макрофагов, нагруженных липидами. Ксантомные клетки обычно имеют одно ядро, но встречается и многоядерные клетки типа инородных тел (клетки Тутона); среди них могут быть гистиоциты и лимфоидные клетки. Фиброз обычно не наблюдается. В старых очагах преобладают фибробласты и новообразованные коллагеновые волокна, окружающие группы пенистых клеток. В дальнейшем фиброзная ткань замещает пенистые клетки. Различают 4 клинические разновидности ксантом- плоскую, множественную узелковую (эруптивные ксантомы), туберозную, сухожильную. Плоские ксантомы (xanthoma planes) наблюдаются чаще у пожилых людей, представляют собой желтовато-оранжевые плоские или слегка выпуклые полосы в складках ладони и пальцев. Эруптивные ксантомы (син.: xanthoma papulosum multiplex, множественные узелковые ксантомы) характеризуются множественными плоскими или полусферическими узелками от 2 до 6 мм в диаметре, желтоватого или желтовато-оранжевого цвета с розово-синюшным венчиком у основания. Элементы высыпаний могут быть рассеянными по всему кожному покрову, но чаще – на разгибательных поверхностях конечностей, в области суставов, спины, ягодиц. Туберозные ксантомы (син.: xanthoma tuberosum, туберкулёзная ксантома, узловатая ксантома) встречаются у больных с семейной гиперхолестеринемией в области разгибательных поверхностей коленных и локтевых суставов, на ягодицах. Высыпания симметричны – безболезненные, плотной консистенции узлы величиной от 1,5 до 3,5 см в диаметре, желтоватого цвета с буроватым или синюшным оттенком. Сухожильные ксантомы (син.: xanthoma tendinеа, ксантома сухожилий) – плотные, медленно увеличивающиеся, опухолевидные образования желтого цвета, располагающиеся в области ахилловых сухожилий и сухожилий разгибателей пальцев.
Ксантелазмы – это плоские, желтые, образования на коже век Величина их колеблется от нескольких миллиметров до 3-5 см и более.
Липидная дуга роговицы имеет диагнстическое значение у лиц моложе 40-45 лет.
Лабораторные диагностические исследования
- Всем лицам старше 40 лет рекомендуется скрининг, включающий анализ крови по оценке нарушений липидного обмена биохимический (липидный профиль) с целью стратификации сердечно-сосудистого риска по шкале SCORE2 [50, 241].
ЕОК/ЕОА I C (УУР С, УДД 5)
-
Пациентам с дислипидеией рекомендуется лабораторное исследование с определением уровня глюкозы, креатинина, мочевины, общего билирубина в крови, определение активности АЛТ, АСТ, КФК в крови и общий (клинический) анализ крови [154].
ЕОК/ЕОА I C (УУР С, УДД 5)
-
Определение уровеня ХС ЛВП в крови рекомендовано всем пациентам для дополнительной оценки риска в системе SCORE2 [50, 241].
ЕОК/ЕОА I C (УУР С, УДД 5)
-
У всех пациентов старше 40 лет рекомендовано определять уровень ХС ЛНП как главный показатель оценки сердечно-сосудистого риска [19, 20, 21].
ЕОК/ЕОА I C (УУР С, УДД 4)
-
Пациентам высокого/очень высокого риска рекомендуется, кроме уровня ХС ЛНП, ХС неЛВП в крови [155, 156].
ЕОК/ЕОА IIa C (УУР B, УДД2)
-
У пациентов с ГТГ, СД, ожирением, метаболическим синдромом рекомендовано проводить лабораторную оценку ХС неЛВП – для более точной оценки сердечно-сосудистого риска [20, 21, 22].
ЕОК/ЕОА I C (УУР А, УДД 1)
-
В случаях, когда трактовка сердечно-сосдистого риска вызывает затруднения(сомнения) в особенности у пациентов с ГТГ, СД, ожирением, метаболическим синдромом рекомендовано лабораторное исследование уровня атерогенного аполипопротеина В100[20].
ЕОК/ЕОА I C (УУРС, УДД 5)
-
Хотя бы раз в жизни у любого взрослого рекомендовано измерить уровень Лп(а) в крови. При значении Лп(а)>180 мг/дл риск эквивалентен гетерозиготной СГХС [20].
ЕОК/ЕОА IIa C (УУР С, УДД 5)
-
У пациентов с отягощённым семейным анамнезом рекомендовано измерять уровень Лп(а) в крови. Уровень Лп(а)>50 мг/дл ассоциируется с увеличением сердечно-сосудистого риска. [20].
ЕОК/ЕОА IIa C (УУРС, УДД 5)
Комментарии. Принципы определения уровня липидов сыворотки крови: традиционно образцы крови для анализа липидов берутся натощак, однако последние исследования говорят о том, что колебания концентрации липидов плазмы крови незначительны в зависимости от приема пищи [23, 24].Однако у лиц с ГТГ забор крови рекомендуется проводить натощак.
Референсный метод определения уровня ХС ЛНП является многостадийным:
1) ультрацентрифугирование в плотности 1,006 г/мл в течение 18 часов для удаления липопротеидов, богатых ТГ (ХМ и ЛОНП);
2) выделение донной фракции (плотности 1,006 г/мл) и преципитация в ней липопротеидов, содержащих апоВ смесью гепарин и MnCl2 для выделения ЛВП;
3) определение концентрации ХС в донной фракции и супернатанте референсным методом для определения ХС (модифицированный метод Абеля-Кендалла);
4) вычисление ХС ЛНП как разности для значений ХС в донной фракции и ХС ЛВП. Препаративное выделение методом ультрацентрифугирования в солевом растворе определенной плотности позволяет изолировать ЛНП и определить их состав.
Длительность и трудоемкость ультрацентрифугирования привела к разработке методов, более доступных для лабораторной практики. Самым распространенным способом определения уровня ХС ЛНП в клинических лабораториях является расчетный. В этом случае необходимо определить уровень ХС, ТГ и ХС ЛВП в крови и концентрацию ХС ЛВП в супернатанте после преципитации липопротеидов, содержащих апоВ (ЛОНП и ЛНП), и вычислить значение концентрации ХС ЛНП по формуле Фридвальда:
ХС ЛНП (в мг/дл) = общий ХС – ХС ЛВП – ТГ/5
ХС ЛНП (в ммоль/л) = общий ХС – ХС ЛВП – ТГ/2,2
В основе этой формулы лежат два допущения: 1) большая часть ТГ плазмы находится в ЛОНП; 2) массовое отношение ТГ/ХС в ЛОНП равно 5:1.
Формула Фридвальда позволяет получить значения ХС ЛНП, сопоставимые с полученными референсным методом при ТГ < 200 мг/дл, при концентрации 200–400 мг/дл возможна ошибка рассчетов. Применение этой формулы при концентрации ТГ> 400 мг/дл, наличии хиломикронов (ХМ), ДЛП III типа приводит к завышению содержания ХС ЛОНП и занижению ХС ЛНП и не позволяет получить сопоставимые результаты. В настоящее время разработаны прямые методы выделения ЛНП, пригодные для использования в клинико-диагностической лаборатории [5]. Исследовать уровень липидов с целью скрининга для определения риска не обязательно натощак. Однако при таком определении уровня липидов риск может быть недооценен у больных сахарным диабетом, так как в одном исследовании пациенты с диабетом имели на 0,6 ммоль/л ниже ХС ЛНП после приема пищи [8]. В последующем, для уточненной и дальнейшей характеристики тяжелых ДЛП, а также для наблюдения пациентов, рекомендуется определять уровень липидов натощак.
-
Пациентам с клиническими проявлениями СГХС (ССЗ у мужчин моложе 55 лет и женщин моложе 60 лет, ксантоматоз, гиперхолестеринемия (ХС ЛНП >5 ммоль/л. у взрослых, >4 ммоль/л. у детей) для установления клинического диагноза СГХС рекомендуется использовать диагностические критерии Голландских липидных клиник (Dutch Lipid Clinic Network – DLCN) (Таблица 3/А3) [50, 153].
ЕОК/ЕОА I C (УУР C, УДД 5)
Инструментальные диагностические исследования
Неинвазивные методы визуализации могут обнаружить наличие, оценить степень и оценить клинические последствия атеросклеротического повреждения сосудов. Визуализация коронарных артерий с помощью компьютерной томографии (КТ) сердца и сонных артерий методом дуплексного сканирования экстракраниальных отделов брахиоцефальных артерий являются информативными в выявлении атеросклеротического поражения артерий. Обнаружение кальцификации коронарной артерии с помощью неконтрастной КТ дает хорошую оценку атеросклеротической нагрузки и тесно связано с ССО. КТ-ангиография имеет высокую чувствительность 95-99% и специфичность 64-83% для диагностики ИБС [25]. Для скрининга атеросклероза коронарных артерий может использоваться кальциевый индекс (КИ), определяемый при КТ по Agatston [26]. Это исследование позволяет обеспечить дополнительную стратификацию риска [27], имеет меньшую стоимость, не требует внутривенного введения контрастных веществ (Таблица 4, Приложение А3). Использование КИ улучшает как дискриминацию, так и реклассификацию категории риска [28, 29]. Оценка атеросклеротических бляшек в сонной или бедренной артерии с помощью ультразвука является прогностическим фактором сердечно-сосудистых событий, сравнимым с КИ [30, 31], в то время как измерение толщины интимы-медиа сонной артерии уступает КИ и наличию бляшек в сонной артерии [32, 33] и не используется в качестве стратификатора риска.
У бессимптомных лиц с умеренным риском наличие КИ > 100 единиц по Agatston и наличие атеросклеротических бляшек в сонной или бедренной артерии по данным дуплексного сканирования может перевести их в категорию более высокого риска. При этом КИ невысок и имеет низкую специфичность у пациентов моложе 45 лет с тяжелой СГХС, включая гомозиготную СГХС (гоСГХС).
-
Всем пациентам с дислипидемией рекомендовано дуплексное сканирование брахиоцефальных артерий [34]
ЕОК/ЕОА IIaВ (УУР А, УДД1)
-
У пациентов с выявленными атеросклеротическими бляшками в сонной или бедренной артерии по данным дуплексного сканирования рекомендовано реклассифицировать категорию риска от низкого и умеренного до высокого с целью эффективного управления определяющими риск факторами [34, 35, 50].
ЕОК/ЕОА IIaВ (УУР А, УДД1)
-
У пациентов с коронарным атеросклерозом и значением КИ выше 100 единиц по данным КТ сердца рекомендовано реклассифицировать категорию риска от низкого и умеренного до высокого с целью эффективной корекции факторов риска [36, 33].
ЕОК/ЕОА IIaВ (УУР В, УДД 2)
Иные диагностические исследования
Иные диагностические исследования в рамках диагностики ДЛП не предусмотрены, возможно расширение диагностических исследований по решению врача в зависимости от клинической ситуации и состояния пациента.
Оценка сердечно-сосудистого риска
-
У всех бессимптомных взрослых старше 40 лет, без ССЗ, СД, ХБП, СГХС, с ХС ЛНП < 4,9 ммоль/л рекомендуется проведение скрининга для оценки общего риска с использованием шкалы SCORE2 [50, 241, 254].
ЕОК/ЕОА IC (УУР C, УДД 5)
-
Пациентов с установленными ранее ССЗ, СГХС, СД, ХБП 3-5 стадий, очень высоким риском по шкале SCORE2 или уровнем ХС ЛНП >4,9 ммоль/л рекомендовано относить к категории высокого или очень высокого риска с целью эффективного управления определяющими ФР [8, 50].
ЕОК/ЕОА IC (УУР C, УДД 5)
Комментарии. В РФ для расчета риска фатальных и нефательных сердечно-сосудистых осложнений в процентах в течение ближайших 10 лет следует использовать шкалу SCORE2 для стран с высоким сердечно-сосудистым риском (приложение Г2) [254]. Для оценки риска по шкале SCORE2 следует выбрать квадрат в зависимости от пола, возраста и статуса курения пациента. В найденном квадрате следует отыскать ячейку, наиболее соответствующую уровню систолического АД и ХС неЛВП данного пациента. Оценка риска по шкале SCORE2 не рекомендована у лиц с подтвержденным ССЗ, СД, ХБП, с единственным, но выраженным ФР (например, тяжелая АГ), с СГХС. Такие пациенты автоматически относятся к группе очень высокого и высокого риска ССО и требуют интенсивной коррекции ФР. Наличие стеноза более 50% в крупных (магистральных) артериях любого сосудистого бассейна по данным любых инструментальных методов исследования, даже в отсутствие клинических симптомов, также переносит пациента в категорию очень высокого риска.
Категории сердечно-сосудистого риска, согласованные со шкалой SCORE2, представлены в Приложении Г2.
Следует обратить особое внимание на выделение внутри категории очень высокого риска категории экстремального риска. К экстремальному риску следует относить: наличие 2 и более сердечно-сосудистых осложнений в течение 2 лет, несмотря на оптимальную гиполипидемическую терапию и/или достигнутый уровень ХС ЛНП <1,4 ммоль/л.
Под атеросклеротическим сердечно-сосудистым заболеванием (АССЗ) подразумевают все проявления ИБС, ишемический инсульт или транзиторное нарушение мозгового кровообращения, атеросклероз артерий нижних конечностей.
-
Пациентов с СГХС и АССЗ рекомендовано относить к категории очень высокого риска с целью эффективного управления определяющими ФР [37].
ЕОК/ЕОА IC (УУР В, УДД 2)
-
Пациентов с СГХС без АССЗ рекомендовано относить к категории высокого риска с целью эффективного управления определяющими ФР [37].
ЕОК/ЕОА IC (УУР В, УДД 2)
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Решение о тактике лечения рекомендуется принимать в зависимости от исходного уровня сердечно-сосудистого риска. Тактика немедикаментозной и медикаментозной терапии суммирована в таблице 1, Приложение Б4.
1. Целевые уровни ХС ЛНП
-
У пациентов очень высокого риска рекомендовано достижение целевого уровня ХС ЛНП <1,4 ммоль/л и снижение по меньшей мере на 50% от исходного через 8±4 недель терапии как для первичной, так и вторичной профилактики ССО [39, 42, 50].
ЕОК/ЕОА IС (УУР С, УДД 5)
-
У пациентов с подтвержденным АССЗ, перенесших повторное сосудистое событие в течение 2 лет (в любом сосудистом бассейне), несмотря на прием максимально переносимой дозы ингибитора гидроксиметилглутарил-кофермента А (ГМГ-КоА) редуктазы, рекомендован целевой уровень ХС ЛНП <1,0 ммоль/л [40, 41, 50].
ЕОК/ЕОА IIbB (УУРС, УДД 5)
-
У пациентов высокого риска рекомендован целевой уровень ХС ЛНП <1,8 ммоль/л и его снижение по меньшей мере на 50% от исходного [39, 42, 50].
ЕОК/ЕОА IA (УУР С, УДД 5)
-
У пациентов умеренного риска рекомендован целевой уровень ХС ЛНП <2,6 ммоль/л для первичной профилактики ССЗ [39, 50].
ЕОК/ЕОА IIaА (УУРС, УДД 5)
-
У пациентов низкого риска рекомендован целевой уровень ХС ЛНП <3,0 ммоль/л [42, 50].
ЕОК/ЕОА IIbA (УУРС, УДД 5)
Комментарии. Статины – C10AA ингибиторы ГМГ-КоА-редуктазы.
2. Немедикаментозное лечение ДЛП
Для профилактики ССЗ доказала свое преимущество диета [44] с высоким уровнем употребления фруктов, овощей, цельнозерновых злаков и клетчатки, орехов, рыбы, птицы и молочных продуктов с низким содержанием жира и ограниченным потреблением сладостей, сладких напитков и красного мяса. Рекомендуется использовать жиры растительных масел. Такая диета является эффективным средством первичной и вторичной профилактики атеросклероза [45]. В частности, многоцентровое рандомизированное исследование PREDIMED, выполненное в Испании, у лиц из группы высокого риска, но без ССЗ, доказало снижение частоты основных ССО (ИМ, инсульт или смерть от сердечно-сосудистой причины) на 28-31% при ежедневном употреблении оливкового масла или орехов [46]. Наблюдательные исследования подтверждают рекомендации о том, что потребление рыбы, по крайней мере, дважды в неделю и омега-3 полиненасыщенных жирных кислот в низких дозах в качестве пищевой добавки могут снижать риск сердечно-сосудистой смерти и инсульта в первичной профилактике без влияния на метаболизм липопротеидов плазмы [47]. Оценка биологически активных добавок и функциональных продуктов питания должна в обязательном порядке включать в себя не только доказательства полезных свойств по влиянию на липидный профиль и атеросклероз, но, также и хорошую переносимость. Важным является производственный стандарт для указанных продуктов, гарантирующий стандартизацию и качество. К пищевым добавкам, влияющим на липидный профиль относится красный дрожжевой рис (монаколин), действие которого, как и статинов, связано с ингибированием ГМГ-КоА-редуктазы. В крупном исследовании, выполненном в Китае у больных с ИБС, монаколин снижал частоту ССО на 45% [48]. Гипохолестеринемический эффект (снижение ХС ЛНП на 15-25%) наблюдается при ежедневном приеме монаколина K в дозе 10 мг. [49]. Монаколин К можно применять, с учетом доказанной клинической эффективности и безопасности, у лиц низкого и умеренного риска с умеренно повышенным ХС ЛНП и отсутствием показаний для приема статинов. Влияние изменения образа жизни на уровень липидов и рекомендации по диете для улучшения общего профиля липопротеидов представлены в Приложении В («Информация для пациентов») и таблице П2, приложении Б4.
Немедикаментозные методы для снижения ТГ включают в себя снижение избыточной массы тела [ИМТ 20-25 кг/м2, окружность талии <94 см (мужчины) и <80 см (женщины)], уменьшение потребления алкоголя (пациентам с ГТГ следует полностью воздержаться от приема алкоголя), увеличение регулярной физической активности (физические упражнения минимум 30 мин каждый день), ограничение в потреблении легко всасываемых углевовдов [50].
3. Медикаментозная терапия ДЛП
3.1 Общие принципы медикаментозной терапии
Комментарии: при планировании гиполипидемической терапии рекомендуется придерживаться следующей схемы:
– оценить общий риск развития ССЗ;
– обсудить с пациентом особенности профилактики ССЗ;
– определить ЦУ ХС ЛНП в соответствии с категорией риска;
– подсчитать в процентах степень снижения уровня ХС ЛНП, необходимого для достижения целевого значения;
– выбрать из группы статинов препарат, который может обеспечить такой уровень снижения ХС ЛНП;
-эффективность и переносимость терапии статинами вариабельны, поэтому может потребоваться титрация дозы препарата;
– если монотерапия статином не позволяет достичь цели, следует рассмотреть возможность комбинированной терапии, в том числе статина с эзетимибом, предпочтительно в одной таблетке или капсуле (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб) (у лиц очень высокого риска возможно начать гиполипидемическую терапию сразу с комбинации статина с эзетимибом).
– врачу убедить пациента в необходимости непрерывной (пожизненной) гиполипидемической терапии.
3.2 Основные классы препаратов для лечения дислипидемий
К средствам, корригирующим ДЛП, относятся статины, эзетимиб, фибраты, другие гиполипидемические средства (эзетимиб, омега-3 триглицериды, включая другие эфиры и кислоты (омега-3 ПНЖК), алирокумаб**, эволокумаб**, инклисиран**).
Статины являются одними из наиболее изученных классов препаратов в профилактике ССЗ. Результаты многочисленных клинических исследований свидетельствуют о том, что статины значительно снижают заболеваемость и смертность от ССЗ при первичной и вторичной профилактике во всех возрастных группах, как у мужчин, так и у женщин. В клинических исследованиях статины замедляли прогрессирование и даже вызывали регрессию атеросклеротической бляшки. Крупнейший метаанализ 19 исследований с различными статинами показал снижение смертности от всех причин на 14%, частоты сердечно-сосудистых событий на 27%, нефатальных и фатальных коронарных осложнений на 27%, инсульта на 22% при снижении уровня ХС ЛНП на 1,0 ммоль/л [51]. Относительное снижение риска при первичной профилактике сопоставимо с таковым во вторичной профилактике. Доступные данные позволяют предположить, что клинический эффект в значительной степени зависит не от препарата, а от степени снижения ХС ЛНП. В РФ представлены (в порядке убывания гиполипидемического эффекта) розувастатин в дозах 5, 10, 15, 20 и 40 мг, аторвастатин** — 10, 20, 30, 40 и 80 мг/сут, питавастатин — 1, 2 и 4 мг, симвастатин** — 10, 20 и 40 мг. Максимальное снижение ХС ЛНП на 50–55% возможно при применении высоких доз розувастатина и аторвастатина**. Статины различаются по своим свойствам всасывания, биодоступности, связывания с белками плазмы, выведения и растворимости. Всасывание препаратов варьирует от 20 до 98%. Многие статины в значительной степени подвергаются метаболизму в печени с участием изоферментов цитохрома P450, за исключением правастатина, розувастатина и питавастатина. Препараты, потенциально взаимодействующие с статинами, представлены в таблице П3, приложении Г4 [52, 53, 54, 55, 56, 57, 58, 59, 60]. Важно отметить, что по данным опубликованного в 2014 году метаанализа 8 важнейших рандомизированных клинических исследований с статинами (n=38153, 6286 ССО у 5387 человек) была продемонстрирована меньшая частота ССО при уровне ХС ЛНП <1,3 ммоль/л (50 мг/дл). При сравнении с участниками с уровнем ХС ЛНП >4,5 ммоль/л (175 мг/дл) было отмечено прогрессивное снижение относительного риска развития сердечно-сосудистых осложнений в зависимости от уровня ХС ЛНП: 2,0–2,6 ммоль/л (75–100 мг/дл), 1,3–2,0 ммоль/л (50–75 мг/дл), и <1,3 ммоль/л (50 мг/дл): 0,56 (95% ДИ 0,46–0,67), 0,51 (0,42–0,62) и 0,44 (0,35–0,55), соответственно [61]. В настоящее время для достижения ЦУ ХС ЛНП и снижения риска ССО оправдано использования трех статинов: розувастатина, аторвастатина**, питавастатина, симвастатина.
Фибраты. Механизм их действия заключается в активации альфа-рецепторов, активируемых активатором пероксисом (РРARα), расположенных в печени, мышцах, жировой ткани, сердце, почках, макрофагах и тромбоцитах. Основная роль PPARα-рецепторов заключается в регуляции метаболизма липидов и липопротеидов, воспаления, функции эндотелия. Активированные PPARα-рецепторы связываются со специфическими участками ДНК, стимулируя или угнетая основные гены, кодирующие метаболические процессы. При этом необходимо отметить, что из класса фибратов только фенофибрат** может использоваться в комбинации со статинами [44]. Фенофибрат** увеличивает синтез апоА1, апоА2, активность ЛПЛ и снижает синтез апоСIII, апоВ100 и концентрацию малых плотных частиц ЛНП на 50%. Это ведет к увеличению уровня ХС ЛВП на 10–30%, ускорению превращения ХМ в их ремнанты, снижению уровня ХС ЛНП на 25%, уменьшению синтеза ТГ и ЛОНП. Уровень ТГ может снижаться до 50% [62, 63]. Помимо влияния на обмен липидов, фенофибрат** снижает уровень мочевой кислоты в среднем на 25%, фибриногена на 21%, С-реактивного белка на 34% [62, 63].
Ингибиторы абсорбции холестерина. Эзетимиб ингибирует всасывание в кишечнике холестерина, поступающего с пищей и из желчи, не влияя на всасывание других жирорастворимых пищевых веществ. Ингибируя всасывание ХС на уровне ворсинок слизистой тонкого кишечника (путем взаимодействия с белком NPC1L1), эзетимиб снижает количество холестерина, поступающего в печень. В ответ на снижение поступления ХС печень активирует на своей поверхности рецепторы ЛНП, что ведет к увеличению клиренса ХС ЛНП из крови. В клинических исследованиях монотерапия эзетимибом сопровождалась снижением уровня ХС ЛНП на 15–22%. Комбинация эзетимиба с статинами обеспечивала дополнительное снижение уровня ХС ЛНП на 15-20%. В исследовании SHARP (Study of Heart and Renal Protection) у пациентов с ХБП было отмечено снижение частоты развития ССЗ в основной группе, получавшей терапию эзетимибом в сочетании с симвастатином** по сравнению с группой, получавшей плацебо, на 17% [64]. Исследование IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) — самое крупное и продолжительное рандомизированное клиническое исследование по применению эзетимиба, включившее 18144 больных, госпитализированных по поводу острого коронарного синдрома [38]. На момент включения больные не получали эзетимиба или максимальной дозы любого статина, но должны были иметь относительно невысокий уровень ХС ЛНП (1,3-3,2 ммоль/л или 50-125 мг/дл). Период наблюдения за больными достигал 7 лет. Через 1 год наблюдения средний уровень ХС ЛНП в группе эзетимиба составил 1,4 ммоль/л (54 мг/дл), что на 0,4 ммоль/л (14 мг/дл) меньше, чем в группе симвастатина**. В группе комбинированного лечения было продемонстрировано значимое снижение суммарного количества смертельных исходов вследствие сердечно-сосудистых причин, ИМ, госпитализации по поводу нестабильной стенокардии, коронарной реваскуляризации и инсульта на 6,4% (относительный риск (ОР)=0,936; 95% доверительный интервал (ДИ)=0,89–0,99, р=0,016), снижение абсолютного риска — на 2,0% [38]. Таким образом, эзетимиб может быть использован в качестве средства второй линии в комбинации со статинами, когда монотерапия статинами не позволяет достичь целевого уровня даже при их назначении в максимальных дозах, а также при непереносимости статинов или наличии противопоказаний к их применению.
Ингибиторы пропротеиновой конвертазы субтилизин-кексина типа 9 (PCSK9) Алирокумаб ** и эволокумаб ** (по АТХ — C10AX Другие гиполипидемические средства) являются ингибиторами (моноклональными антителами к) PCSK9 — белка, контролирующего экспрессию рецепторов к ХС ЛНП гепатоцитов [65]. Повышенные уровень/функция PCSK9 снижают экспрессию рецепторов ЛНП и увеличивают концентрацию ХС ЛНП в плазме, в то время как снижение уровня/функции PCSK9 вызывает снижение ХС ЛНП в плазме крови [66]. Алирокумаб** в дозировках 75 и 150 мг и эволокумаб** в дозировке 140 мг подкожно с частотой введения 1 раз в 2 недели в клинических исследованиях показали возможность снижения уровня ХС ЛНП на 60% и риска сердечно-сосудистых осложнений на 15% у больных с АССЗ в комбинации с умеренной и высокоинтенсивной терапией статинами. Исследование FOURIER (Further cardiovascular OUtcomes Research with PCSK9 Inhibition in subjects with Elevated Risk) включило 27564 пациентов с атеросклеротическим поражением различных сосудистых бассейнов: 22040 пациентов (81%) в прошлом перенесли ИМ (из них 5500 в сроки от 4 недель до 1 года перед включением в исследование), у 5330 (19%) в анамнезе был негеморрагический инсульт и у 3640 (13%) — периферический атеросклероз. Пациенты находились на адекватной гиполипидемической терапии: 69,2% получали статины в режиме высокой интенсивности и 30,4% — умеренной интенсивности, у 5,1% дополнительно к статину назначали эзетимиб. Участники, рандомизированные в группу активного лечения, получали эволокумаб** подкожно в дозе 140 мг 1 раз в 2 недели или 420 мг в месяц, тогда как пациентам в группе контроля на протяжении исследования подкожно вводили плацебо [40]. Медиана наблюдения в исследовании составила 2,2 года. Была подтверждена высокая гиполипидемическая эффективность эволокумаба**: уровень ХС ЛНП снизился на 59% с 2,40 ммоль/л до 0,78 ммоль/л. Впервые было продемонстрировано положительное влияние терапии эволокумабом** на сердечно-сосудистые исходы: частота событий, оцениваемых по первичной конечной точке, в группе эволокумаба** была ниже на 15% (ОР=0,85, 95% ДИ=0,79-0,92, p <0,001), а по вторичной точке — ниже на 20% (ОР=0,80, 95% ДИ=0,73–0,88, p <0,001), чем в группе плацебо. Чуть позднее были представлены результаты дополнительного, заранее спланированного анализа, целью которого было определение связи между границами и степенью снижения уровня ХС ЛНП и частоты ССО [67]. В этот анализ были включены 25982 человека (94% от общего количества рандомизированных, 13013 — на эволокумабе**, 12969 — плацебо). Их ранжировали по уровню достигнутого к 4-й неделе лечения ХС ЛНП на 5 подгрупп: <0,5 ммоль/л (n=2669), 0,5–1,3 ммоль/л (n=8003), 1,4–1,8 ммоль/л (n=3444), 1,9–2,6 ммоль/л (n=7471), >2,6 ммоль/л (n=4395). Было отмечено, что при снижении ХС ЛНП вплоть до 0,2 ммоль/л (7,7 мг/дл) уменьшается частота ССО без увеличения риска нежелательных явлений. Однако статистически значимое снижение частоты событий из первичной и вторичной конечных точек было показано только в первых двух подгруппах низких значений ХС ЛНП, т.е. менее 0,5 и 1,3 ммоль/л: на 24% и 15% [ОР=0,76 (0,64–0,90) и 0,85 (0,76–0,96)] для первичной точки и на 31% и 25% [0,69 (0,56–0,85)] и [0,75 (0,64–0,86)] для вторичной точки, соответственно. В связи с этими данными авторы отметили целесообразность пересмотра целевого уровня ХС ЛНП в современных рекомендациях для лиц очень высокого сердечно-сосудистого риска. Исследование ODYSSEY OUTCOMES (Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment With Alirocumab) с участием 18 924 пациентов с перенесенным 1–12 месяцев назад ОКС продемонстрировало, что алирокумаб** статистически значимо снижает риск крупных сердечно-сосудистых событий. Они отмечались у 903 пациентов (9,5%) в группе терапии препаратом алирокумаб** и у 1052 пациентов (11,1%) в группе плацебо, что соответствует снижению относительного риска на 15% (ОР 0,85; 95% ДИ, 0,78–0,93; p<0,001). Кроме того, на фоне алирокумаба ** снижался риск смерти от всех причин на 15%. У пациентов с исходно более высоким уровнем ХС ЛНП (≥100 мг/дл/2,6 ммоль/л) при применении алирокумаба ** отмечалось более выраженное снижение риска сердечно-сосудистых событий на 24% ниже (ОР 0,76; 95% ДИ, 0,65–0,87), а смерти от всех причин — на 29% (ОР 0,71; 95% ДИ, 0,56–0,90), в сравнении с плацебо [41].
Инклисиран** — это химически модифицированная двухцепочечная малая интерферирующая рибонуклеиновая кислота (миРНК). В гепатоцитах инклисиран** использует механизм РНК-интерференции, чтобы нацелиться на матричную РНК PCSK9 и запустить процесс ее деградации, тем самым увеличивая рециркуляцию и экспрессию рецепторов ЛНП, с последующим увеличением его захвата и уменьшением уровня ХС ЛНП в крови [157–160]. Инклисиран** вводится подкожно 3 раза в первый год, а затем два раза в год.
В группе клинических исследований ORION (A Randomized Trial Assessing the Effects of Inclisiran on Clinical Outcomes Among People With Cardiovascular Disease) 9, 10, 11 была подтверждена долгосрочная гиполипидемическая эффективность инклисирана** для следующих групп пациентов: СГХС, АССЗ и эквиваленты сердечно-сосудистого риска, такие как как СД 2 типа, СГХС или 10-летний риск ССО >20% по Фрамингемской шкале или эквивалентной ей. Было установлено, что назначение инклисзирана приводит к снижению уровня ХС ЛНП у указанных категорий больных на 50–58%, как в краткосрочной, так и в долгосрочной перспективе [161, 162]. Профиль безопасности инклисирана** сопоставим с плацебо [161, 162], не было получено данных о возникновении специфических серьезных нежелательных явлений, возникших в ходе лечения [50]. В метаанализе по результатам трех рандомизированных клинических исследований было показано снижение частоты серьезных неблагоприятных сердечно-сосудистых событий на 24% (отношение рисков = 0,76; 95% доверительный интервал, 0,61–0,92) [252].
Омега-3 ПНЖК в соответствии с современными воззрениями являются основными препаратами для снижения уровня ТГ. Недавно завершившееся исследование REDUCE-IT (Cardiovascular Risk Reduction with Icosapent Ethyl for Hypertriglyceridemia) с участием 8179 пациентов доказало влияние омега-3 ПНЖК на твердые конечные точки [68]. Критериями включения были: установленные в анамнезе ССЗ (~70% пациентов) или СД 2-го типа + >1 ФР, уровень ТГ ≥2,3 ммоль/л и <5,6 ммоль/л, достигнутый целевой уровень ХС ЛНП >1,03 ммоль/л и ≤2,6 ммоль/л. Первичной конечной точкой являлось время от рандомизации до первого события: сердечно-сосудистая смерть, нефатальный ИМ, нефатальный ишемический инсульт, реваскуляризация, нестабильная стенокардия. Было продемонстрировано снижение относительного риска развития серьезных неблагоприятных СС событий на 25% (р <0,001), в группе пациентов, принимавших омега-3 ПНЖК (форма эйкозопентаеновой кислоты 4 г/сут) в сравнении с плацебо. Таким образом, Омега-3 триглицериды, включая другие эфиры и кислоты, могут использоваться для терапии ГТГ в дозе 2–4 г/сут.
Сравнение эффективности статинов, фибратов и эзетимиба представлено в таблице П4, приложении Г4.
Сводные данные по эффективности, дозам, побочным эффектам гиполипидемических препаратов приведены в таблице П8, приложении Г4.
3.3 Медикаментозная терапия ДЛП для достижения целевого уровня ХС ЛНП
-
Всем пациентам с ДЛП рекомендована терапия статином в дозах, необходимых для достижения целевого уровня ХС ЛНП [39, 69, 70].
Комментарии: дозы статинов для интенсивного и умеренного снижения ХС ЛНП приведены в таблице П4, приложение Б3. При непереносимости высокоинтенсивной терапии статинов следует рассмотреть снижение дозы препарата с последующей переоценкой переносимости.
ЕОК/ЕОА IA (УУР В, УДД 1)
-
Пациентам, не достигшим целевого уровня ХС ЛНП на фоне максимально переносимых доз статинов, следует рассмотреть возможность комбинированной терапии, в том числе статин с эзетимибом, предпочтительно в одной таблетке или капсуле (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб) [38].
ЕОК/ЕОА IВ (УУР А, УДД 2)
-
У пациентов с очень высоким риском и недостижением целевого уровня ХС ЛНП на фоне максимально переносимых доз статина в комбинации с эзетимибом рекомендовано добавить алирокумаб** (ЕОК/ЕОА I A), эволокумаб**(ЕОК/ЕОА I A) или инклисиран** (ЕОК/ЕОА нет) с целью вторичной профилактики ССЗ [40, 41, 67, 243].
(УУР А, УДД 1)
-
В случае значительного повышения уровня ХС ЛНП у больных очень высокого риска (выше 4,0 ммоль/л), рекомендуется рассмотреть возможность инициального назначения статина и эзетимиба, предпочтительно в одной таблетке или капсуле (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб) [244].
ЕОК/ЕОА нет (УУР А, УДД 1)
-
В случае значительного повышения уровня ХС ЛНП у больных экстремального или очень высокого риска (выше 5,0 ммоль/л), рекомендуется рассмотреть возможность инициального назначения статина максимально переносимой дозе+эзетимиб+ингибитора PCSK9: алирокумаба** (ЕОК/ЕОА I A), эволокумаба** (ЕОК/ЕОА I A) или инклисирана** (ЕОК/ЕОА нет) [243, 245, 246,255].
(УУР А, УДД 1)
-
У пациентов с очень высоким риском, без СГХС, и недостижением целевого уровня ХС ЛНП на фоне максимально переносимых доз статина с/без эзетимибом рекомендовано добавить алирокумаб**, эволокумаб** или инклисиран** [40, 41, 67, 243] с целью первичной профилактики ССЗ.
ЕОК/ЕОА IIbC (УУР А, УДД 2)
-
Пациентам с непереносимостью любой дозы статина рекомендован прием эзетимиба [71, 72].
ЕОК/ЕОА IIаC (УУР А, УДД 2)
-
Пациентам с непереносимостью любой дозы статина, которые на фоне приема эзетимиба не достигли целевого уровня ХС ЛНП, рекомендовано добавление к терапии алирокумаба**, эволокумаба** или инклисирана** [71, 72, 73, 243].
ЕОК/ЕОА IIbC (УУР А, УДД 2)
Комментарии: степень снижения уровня ХС ЛНП при различных вариантах гиполипидемической терапии указан в таблице А3.11. Алгоритм медикаментозной терапии достижения целевого уровня ХС ЛНП приведен в Приложении Б2.
3.4 Медикаментозная терапия гипертриглицеридемии
- Пациентам любой категории риска рекомендован целевой уровень ТГ <1,7 ммоль/л [16, 156, 163].
ЕОК/ЕОА IIaC (УУР B, УДД 2)
Комментарии: важными причинами остаточного риска являются высокий уровень ТГ и низкий уровень ХС ЛВП в плазме крови. Даже при достижении целевого уровня ХС ЛНП у пациентов сохраняется остаточный риск ССО. По данным крупнейшего эпидемиологического исследования (Framingham Study), уровень ТГ<1,7 ммоль/л (< 150 мг/дл) указывает на более низкий риск ССО, более высокие уровни указывают на необходимость поиска причин повышения уровня ТГ. Повышенные уровни ТГ и низкий уровень ХС ЛВП синергично увеличивают риск ССО у пациентов с уже достигнутыми ЦУ ХС ЛНП [16, 156, 163].
-
Пациентам высокого и очень высокого риска, достигшим на терапии статином уровня ТГ 1,7–2,3 ммоль/л, рекомендовано добавить препарат омега-3 ПНЖК в дозе до 2 г 2 раза в день [68].
ЕОК/ЕОА IIaВ (УУР В, УДД 2)
-
Пациентам с уровнем ТГ> 2,3 ммоль/л на терапии статином, рекомендовано добавить фенофибрат** (предпочтительно в одной таблетке (зарегистрирован розувастатин+фенофибрат) или препарат омега-3 ПНЖК в дозе до 2 г 2 раза в день [68, 77, 78, 79].
Комментарии: В исследовании ECLIPSE-REAL к концу 12 недель терапии комбинацией фенофибрата** и статина значительно снизили ОХС, ТГ, ХС ЛНП, ХС ЛОНП, но более значимым и статистически значимым снижение было в группе, получавшей комбинацию розувастатина и фенофибрата** [164–166].
ЕОК/ЕОА IIaВ (УУР С, УДД 5)
-
Пациентам с уровнем ТГ > 5,0 ммоль/л, рекомендовано назначить фенофибрат** и препарат омега-3 ПНЖК в дозе до 2 г 2 раза [242].
ЕОК/ЕОА IIaВ (УУР В, УДД 2)
Алгоритм выбора медикаментозной терапии ГТГ представлен в приложении Б1.
4. Аппаратное лечение ДЛП
Подразумевает такие экстракорпоральные методы удаления атерогенных липопротеидов как плазмаферез, плазмосорбция. Они назначаются пациентам, у которых после 6 месяцев комбинированной гиполипидемической терапии в максимально переносимых дозах не достигнуты целевые уровни ХС ЛНП. Помимо этого, плазмаферез, плазмосорбция проводятся по следующим показаниям: гомозиготная СГХС и ХС ЛНП >7,8 ммоль/л, или гетерозиготная СГХС и ХС ЛНП >7,8 ммоль/л + 1 дополнительный фактор сердечно-сосудистого риска, или гетерозиготная СГХС и ХС ЛНП > 5,0 ммоль/л + 2 фактора риска или уровень Лп(а) >50 мг/дл; гетерозиготная СГХС и ХС ЛНП >4,1 ммоль/л у лиц очень высокого риска; СГХС при отмене гиполипидемической терапии в связи с беременностью при высоком риске сердечно-сосудистых осложнений [8].
Плазмаферез, плазмосорбция проводятся еженедельно или 1 раз в две недели. Во время процедуры из плазмы крови пациента удаляется до 80% уровня ХС ЛНП, при этом концентрация уровня ХС ЛНП в плазме крови пациента в зависимости от объема обработанной плазмы снижается на 70–80%. В настоящее время существует ряд методов плазмафереза, плазмосорбции ХС ЛНП: каскадная плазмофильтрация, гепарин-преципитация ЛНП (HELP), аффинная плазмо- и гемосорбция липопротеидов, иммуносорбция ЛНП.
Плазмаферез, плазмосорбция проводятся только в специализированных отделениях больниц и клиник.
Показания к ЛНП и Лп(а) плазмаферезу, плазмосорбции приведены в таблице П3, приложении Б.
5. Лечение ДЛП в отдельных клинических ситуациях
5.1 Семейная гиперхолестеринемия
Определение. Эпидемиология
Семейная гиперхолестеринемия (СГХС) — генетически детерминированное моногенное нарушение липидного обмена с преимущественно аутосомно-доминантным типом наследования, сопровождающееся значительным повышением уровня ХС ЛНП в крови и, как следствие, преждевременным развитием и прогрессирующим течением атеросклероза, как правило, в молодом возрасте [9, 220]. Различают две формы: гетерозиготную (геСГХС) и гомозиготную (гоСГХС). В структуре моногенных дислипидемий геСГХС занимает первое место по распространенности и составляет в среднем 1 на 200–250 человек [9, 220]. Согласно результатам эпидемиологического исследования, проведенного в ряде регионов Российской Федерации, распространенность геСГХС колеблется от 1:108–1:173 лиц [221]. ГоСГХС встречается значительно реже, распространенность составляет 1 случай на 160–300 тыс. населения Европы [222].
Этиология и патогенез
Генетические основы заболевания
Развитие СГХС обусловлено дефектами генов белков, участвующих в метаболизме липопротеидов, в результате которых нарушается захват клетками ЛНП-частиц и в крови повышается уровень ХС ЛНП [223, 224].
Самая частая генетическая причина СГХС — мутация в гене рецептора липопротеидов низкой плотности (LDLR), который расположен главным образом на поверхности гепатоцитов и играет ключевую роль в связывании и выведении из кровотока циркулирующих ЛНП-частиц [225, 226]. На сегодняшний день известно более 1600 мутаций LDLR, способных нарушить функцию рецептора и вызывать развитие СГХС. Мутации в гене LDLR обуславливают от 85 до 90% случаев СГХС [227].
Вторая по частоте причина — мутация в гене аполипопротеина В (APOB), кодирующего апобелок В100, входящий в состав ЛНП-частиц и ответственный за связывание ЛНП с рецептором. В результате изменений в гене половина ЛНП-частиц не способна связаться с ЛНП-рецептором [228]. Мутации гена APOB обеспечивают от 5 до 10% случаев СГХС [229]. Показано, что носители мутаций гена LDLR имеют более высокий уровень ОХС и ХС ЛНП и более выраженные проявления атеросклероза артерий, чем носители мутаций гена APOB [230].
Третий ген, мутации в котором способны приводить к развитию СГХС, — это ген, кодирующий пропротеинконвертазу субтилизин/кексин тип 9 (PCSK9 — ПКСК9) — сериновую протеазу, участвующую в разрушении ЛНП-рецептора [231, 232, 233]. Мутации гена PCSK9 обеспечивают меньше 5% случаев СГХС [227]. Уровни ХС ЛНП у носителей миссенс-мутаций PCSK9 очень варьируют от относительно умеренных до очень высоких [234].
Диагностические критерии заболевания
Потенциальную вероятность наличия СГХС необходимо оценивать в случаях [235, 236]:
-
ОХС ≥8 ммоль/л и/или ХС ЛНП ≥5 ммоль/л без терапии для взрослых и ОХС> 6,7 ммоль/л или ХС ЛНП ≥3,5 ммоль/л у детей,
-
Ранний дебют ССЗ атеросклеротического генеза (у мужчин <55 лет; у женщин <60 лет),
-
Кожные / сухожильные ксантомы,
-
Случай внезапной сердечной смерти члена семьи.
С учетом генетической предиспозиции быстрая прогрессия атеросклероза у пациентов с СГХС приводит к раннему дебюту ССЗ атеросклеротического генеза, чаще всего — ИБС. Длительное бессимптомное течение заболевания диктует необходимость опираться в первую очередь на лабораторные показатели и семейный анамнез при выявлении новых случаев СГХС для своевременного старта терапии в зоне первичной профилактики.
Для клинической диагностики заболевания целесообразно использование специализированных критериев, разработанных для взрослых и детей с геСГХС и для пациентов с гоСГСХ. Крайне важно проведение дообследования с целью исключения вторичных дислипидемий и их вклада в повышенные значения ХС ЛНП у лиц с подозрением на СГХС.
Диагностические критерии геСГХС
Ø Для диагностики геСГХС у взрослых пациентов 18 лет и старше рекомендовано использовать диагностические критерии Dutch Lipid Clinic Network (DLCN) — шкалы Голландских липидных клиник (Приложение Г1) [50, 235].
ЕОК/ЕОА I С (УУРС, УДД 5)
- Диагноз устанавливается на основании суммы баллов, полученных в каждой группе. Внутри группы баллы не суммируются, учитывается только один признак, дающий максимальное количество баллов внутри каждой из групп.
-
В соответствии с набранной суммой баллов геСГХС может быть определенной, вероятной или возможной. При этом диагноз геСГХС выставляется только при наличии определенной или вероятной формы.
-
Для определения 95-го перцентиля уровня ХС ЛНП в зависимости от пола и возраста следует использовать значения, приведенные в Таблице П6/А3 (Популяционные показатели ХС ЛНП в зависимости от пола и возраста, по данным исследования ЭССЕ-РФ) [152].
Ø Для диагностики геСГХС у взрослых пациентов 18 лет и старше только в случаях отсутствия возможности определения ХС ЛНП, а также у детей рекомендовано использовать диагностические критерии Simon Broome Registry — Саймона Брума (Таблица 7/А3) [235, 237].
ЕОК/ЕОА I С (УУРС, УДД 5)
Ø Диагноз геСГХС выставляется в случае соответствия пациента критериям определенного или вероятного диагноза СГХС.
Диагностические критерии гоСГХС
Ø Для диагностики гоСГХС и у взрослых, и у детей рекомендовано использовать критерии, предложенные экспертами европейского общества по атеросклерозу (Таблица 8/А3) [222].
ЕОК/ЕОА I С (УУР А, УДД 3)
-
Согласно данным критериям, диагноз гоСГХС выставляется у детей и взрослых при наличии одного из двух условий.
Таким образом, диагностика СГХС возможна без выполнения молекулярно-генетического исследования по клиническим критериям, однако выявление конкретной мутации существенно облегчает постановку диагноза СГХС и последующее проведение каскадного скрининга, а также позволяет точнее стратифицировать сердечно-сосудистый риск [238].
Выполнение молекулярно-генетического исследования для верификации СГХС показано лицам с суммой баллов 6 и более согласно клиническим критериям DLCN или при постановке диагноза геСГХС согласно критериям Саймона Брума [239, 240].
ЕОК/ЕОА I С (УУРА, УДД 2)
Каскадный скрининг
Каскадный скрининг рекомендован к проведению родственникам первой, второй, и если возможно, третьей степени родства пациента с установленным диагнозом СГХС, а в случае, если у пробанда выявлен патогенный или вероятно-патогенный вариант нуклеотидной последовательности генов LDLR, APOB, PCSK9, — проведение генетического каскадного скрининга у родственников пробанда с целью определения у них наличия или отсутствия данного генетического варианта. При подтверждении наличия патогенных или вероятно-патогенных вариантов у родственника рекомендовано выставление диагноза СГХС, даже если уровень ХС ЛНП ниже диагностических значений согласно клиническим критериям [235, 237].
ЕОК/ЕОА I С (УУРС, УДД 5)
Лечение
Целевые уровни ХС ЛНП
-
У пациентов очень высокого риска с СГХС рекомендовано достижение целевого уровня ХС ЛНП <1,4 ммоль/л и снижение по меньшей мере на 50% от исходного для первичной профилактики ССО [37, 43, 50]
ЕОК/ЕОА IIaС (УУР С, УДД 5)
-
У пациентов очень высокого риска с СГХС и АССЗ рекомендовано достижение целевого уровня ХС ЛНП <1,4 ммоль/л и снижение по меньшей мере на 50% от исходного для вторичной профилактики ССО [37, 43]
ЕОК/ЕОА IС (УУР С, УДД5)
-
У пациентов высокого риска с СГХС рекомендовано достижение целевого уровня ХС ЛНП <1,8 ммоль/л и его снижение по меньшей мере на 50% от исходного [39, 42, 50].
ЕОК/ЕОА IA (УУР С, УДД 5)
Медикаментозная терапия
Гиполипидемическую терапию рекомендовано инициировать сразу после установления диагноза.
-
Всем пациентам с СГХС рекомендована стартовая терапия статином в дозах, необходимых для достижения целевого уровня ХС ЛНП [39, 69, 70].
ЕОК/ЕОА IA (УУР В, УДД 1)
Комментарии: дозы статинов для интенсивного и умеренного снижения ХС ЛНП приведены в таблице 4, приложение Б3. При непереносимости высокоинтенсивной терапии статинами следует рассмотреть снижение дозы препарата с последующей переоценкой переносимости.
-
Пациентам, не достигшим целевого уровня ХС ЛНП на фоне максимально переносимых доз статина, рекомендуется комбинированная терапия статином с эзетимибом предпочтительно в одной таблетке (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб) [38].
ЕОК/ЕОА IВ (УУР А, УДД 2)
-
У пациентов с очень высоким риском и недостижением целевого уровня ХС ЛНП на фоне максимально переносимых доз статина в комбинации с эзетимибом рекомендовано добавить алирокумаб**(ЕОК/ЕОА I A), инклисиран**(ЕОК/ЕОА нет) или эволокумаб**(ЕОК/ЕОА I A) с целью вторичной профилактики ССЗ [40, 41, 67, 243].
(УУР А, УДД 2)
-
Пациентам с непереносимостью любой дозы статина рекомендован прием эзетимиба для достижения целевого уровня ХС ЛНП [71, 72].
ЕОК/ЕОА IIаC (УУР А, УДД 2)
-
Пациентам с непереносимостью любой дозы статином, которые на фоне приема эзетимиба не достигли целевого уровня ХС ЛНП, рекомендовано добавление к терапии алирокумаба**(ЕОК/ЕОА IIbC), инклисирана**(ЕОК/ЕОА нет) или эволокумаба**(ЕОК/ЕОА IIbC) [71, 72, 73, 243]
ЕОК/ЕОА IIbC (УУР А, УДД 1)
-
Пациентам очень высокого риска с СГХС, если не достигнут целевой уровень ХС ЛНП на максимально переносимых дозах статина в комбинации с эзетимибом, рекомендовано добавление к терапии алирокумаба** (ЕОК/ЕОА IC), инклисирана** (ЕОК/ЕОА нет) или эволокумаба** (ЕОК/ЕОА IC) [9, 74, 75, 243, 247]
(УУР A, УДД 1)
5.2 ДЛП и сахарный диабет
-
У пациентов с СД 2-го типа и категории очень высокого риска рекомендовано снижение ХС ЛНП ≥50% и < 1,4 ммоль/л [39, 80, 81].
ЕОК/ЕОА IА (УУР В, УДД 1)
-
У пациентов с СД 2-го типа и категории высокого риска рекомендовано снижение ХС ЛНП ≥50% и < 1,8 ммоль/л [50, 80, 167].
ЕОК/ЕОА IА (УУР С, УДД 5)
-
Пациентам с СД 1-го типа и высоким/очень высоким риском рекомендована терапия статином [50, 82].
ЕОК/ЕОА IА (УУР С, УДД 5)
-
Пациентам с СД, которым начата терапия ингибитором ГМГ-КоА-редуктазы, но целевой уровень ХС ЛНП не достигнут, рекомендована интенсификация терапии [50].
ЕОК/ЕОА IIaС (УУР С, УДД 5)
-
Пациентам с СД2, на фоне терапии статином, но с уровнем ТГ ≥ 2,3 ммоль/л, рекомендовано добавление фенофибрата** к терапии статиом, предпочтительно в одной таблетке (зарегистрирован розувастатин+фенофибрат) [79, 167].
ЕОК/ЕОА IIa B (УУР В, УДД 2)
Комментарии: длительное наблюдение за больными СД на фоне комбинированной терапии фенофибратом** и статином позволило доказать состоятельность такой стратегии в плане долгосрочного прогноза — выявлено снижение общей и сердечно-сосудистой смертности. На протяжении всех трех временных срезов было получено достоверное снижение количества больших ССО на 34–36% [248].
-
Пациентам с СД, у которых после интенсификации терапии статином целевой уровень ХС ЛНП не достигнут, рекомендовано статину добавить эзетимиб [38, 83], в том числе статин с эзетимибом в одной таблетке или капсуле (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб).
ЕОК/ЕОА IА (УУР А, УДД 2)
-
Рекомендуется назначение других гиполипидемических средств, таких как ингибиторы PCSK9 — алирокумаба**, эволокумаба** или инклисирана** всем пациентам с СД2 высокого и очень высокого сердечно-сосудистого риска с недостаточным снижением ХС ЛНП на фоне приема максимально переносимых доз статинов и эзетимиба для достижения ЦУ ХС ЛНП и снижения риска ССО [50, 249].
ЕОК/ЕОА IА (УУР С, УДД 5)
-
Пациенткам с СД до наступления менопаузы и планирующим беременность или не принимающим контрацептивы не рекомендована терапия статином [8, 50].
ЕОК/ЕОА IIIC (УУР C, УДД 5)
-
Пациентам с СД 1-го типа и СД 2-го типа в возрасте ≤30 лет с повреждением органов-мишеней и/или ХС ЛНП>2,5 ммоль/л рекомендована терапия статином [8, 50, 81].
ЕОК/ЕОА IIbC (УУР C, УДД 5)
Комментарии. Согласно Российским рекомендациям по лечению сахарного диабета 2019 года (IX пересмотр), рекомендациям ESC по лечению дислипидемии 2019 г, терапию АССЗ в сочетании с СД 2-го типа следует начинать с ингибиторов натрий-зависимого переносчика глюкозы 2-го типа или с аналогов глюкагоноподобного пептида-1. У пациентов с СД 2-го типа и ССЗ, имеющих очень высокий и высокий сердечно-сосудистый риск, в качестве гипогликемической терапии рекомендованы эмпаглифлозин** для снижения риска новых сердечно-сосудистых событий или дапаглифлозин** для снижения риска госпитализаций по причине сердечной недостаточности [87].
Для ведения пациентов с ССЗ с целью снижения сердечно-сосудистого риска рекомендуются:
-
Ингибиторы натрийзависимого переносчика глюкозы 2-го типа: эмпаглифлозин**, дапаглифлозин**. Аналоги глюкагоноподобного пептида 1 (аГПП-1): лираглутид, дулаглутид, семаглутид.
-
Бигуаниды: метформин** (как препарат второго ряда).
Ингибиторы натрийзависимого переносчика глюкозы 2-го типа
По итогам исследования EMPA-REG Outcome было на фоне эмпаглифлозина(**) продемонстрировано снижение частоты достижения первичной конечной точки на 14% (p=0,038), при этом результаты по каждому из компонентов комбинированной точки были различными: общая смертность снизилась на 32% (p<0,001), сердечно-сосудистая смертность — на 38% (p<0.0001) [84].
Аналоги ГПП-1. В 2016 г. опубликованы результаты исследования LEADER, посвященного эффективности и безопасности лираглутида. Данное многоцентровое двойное слепое плацебо-контролируемое исследование проводилось в 410 центрах 32 стран и включало 9340 пациентов, из которых 4668 были рандомизированы в группу лираглутида, 4672 — в группу плацебо. Частота сердечно-сосудистой смерти была ниже в группе лираглутида (4,7%), чем в группе плацебо (6.0%, ОР 0,78, ДИ 0,66–0,93, p=0,007), общей смертности — 8,2% и 9,6%, соответственно, (ОР 0,85, ДИ 0,74-0,97, p=0,02). Было продемонстрировано снижение риска достижения первичной комбинированной тройной конечной точки на 13%, сердечно-сосудистой смерти — на 22%, композитной конечной точки (коронарная реваскуляризация, нестабильная стенокардия, госпитализация по поводу сердечной недостаточности) — на 20%, риска смерти от всех причин — на 15%, увеличение времени до наступления микрососудистого события (нефропатии) — на 22% [85]. Влияние терапии семаглутидом на сердечно-сосудистые исходы изучалось в исследовании SUSTAIN-6. 3297 пациентов с СД 2-го типа и высоким сердечно-сосудистым риском были рандомизированы в группы семаглутида (0,5 или 1 мг 1 раз в неделю) или плацебо в дополнение к стандартной противодиабетической и сердечно-сосудистой терапии. У 83% включенных пациентов было установлено наличие сердечно-сосудистых заболеваний и/или ХБП III–V стадии. Срок наблюдения составил 104 недели. Выявлено уменьшение риска комбинированной тройной конечной точки на фоне приема семаглутида на 26%, инсультов на 38%, при этом препарат не уменьшал частоты общей и сердечно-сосудистой смертности, нефатального ИМ и госпитализации по поводу сердечной недостаточности [86].
Для снижения количества ССО и улучшения прогноза больных СД 2-го типа рекомендуется отдавать приоритет препаратам с подтвержденными сердечно-сосудистыми преимуществами. С учетом имеющихся доказательств благоприятного влияния эмпаглифлозина** и лираглутида на ССО, данные препараты следует рассматривать, наряду с метформином**, в качестве первой линии терапии больных СД 2-го типа высокого и очень высокого риска. При наличии ХСН предпочтение отдается эмпаглифлозину**.
-
У пациентов с СД 2-го типа и ССЗ, имеющих очень высокий и высокий сердечно-сосудистый риск, в качестве гипогликемической терапии рекомендованы эмпаглифлозин** или дапаглифлозин** для снижения риска новых сердечно-сосудистых событий [87].
ЕОК/ЕОА IА (УУР А, УДД 1)
-
У пациентов с СД 2-го типа и ССЗ в качестве гипогликемической терапии рекомендован эмпаглифлозин** для снижения риска смерти [88].
ЕОК/ЕОА IB (УУР A, УДД 1)
-
У пациентов с СД 2-го типа и ССЗ, имеющих очень высокий и высокий сердечно-сосудистый риск, в качестве гипогликемической терапии рекомендован лираглутид для снижения риска как новых ССО, так и риска смерти [85].
ЕОК/ЕОА IB (УУР А, УДД 2)
-
У пациентов с СД 2-го типа без ССЗ рекомендован метформин** для снижения сердечно-сосудистого риска [89].
ЕОК/ЕОА IIaС (УУР А, УДД 2)
5.3 ДЛП и хроническая болезнь почек
На начальных стадиях ХБП повышены уровни ТГ, а уровни ХС ЛВП снижены. Для ХБП характерен увеличение уровня Лп(a). Пациенты с ХБП 3–5-й стадии имеют высокий или очень высокий сердечно-сосудистый риск [90, 91].
-
У диализ-независимых пациентов ХБП 3–5-й стадии рекомендуется применение статина или комбинации статин / эзетимиб [92, 93, 94, 95].
ЕОК/ЕОА IА (УУР В, УДД 1)
-
У пациентов с ХБП 5-й стадии с атеросклеротическим ССЗ, уже получающих статин, эзетимиб, или комбинацию статин / эзетимиб, при начале диализа, рекомендовано продолжить исходную гиполипидемическую терапию [92, 93, 96, 97, 98].
ЕОК/ЕОА IIaC IА (УУР В, УДД 1)
-
Пациентам с ХБП 1-4 стадии и уровнем ТГ >1,7 ммоль/л рекомендовано рассмотреть назначение омега-3 ПНЖК с целью снижения уровня ТГ [168-170].
ЕОК/ЕОА IIaВ (УУР А, УДД 2)
-
У пациентов c диализ-зависимой ХБП и не имеющих атеросклеротических ССЗ, не рекомендуется начало терапии статином [99, 100]
ЕОК/ЕОА IIIA (УУР А, УДД 2)
5.4 ДЛП и ОКС/чрескожные коронарные вмешательства
-
У всех пациентов с ОКС при отсутствии противопоказаний или установленной непереносимости рекомендовано начать или продолжить терапию статином в высоких дозах как можно раньше, вне зависимости от исходных значений ХС ЛНП [101, 102, 103].
ЕОК/ЕОА IА (УУР А, УДД 2)
-
Всем пациентам через 4–6 недель после ОКС рекомендовано оценить достижение целевых показателей ХС ЛНП (снижение на 50% от исходного и <1,4 ммоль/л), безопасность терапии статином и, при необходимости, скорректировать дозы препаратов [8, 50, 101, 102, 171].
ЕОК/ЕОА IIaC (УУР А, УДД 1)
-
Пациентам, через 4–6 недель после ОКС не достигшим целевых уровней ХС ЛНП на фоне максимально переносимых доз статином, рекомендована комбинация статина с эзетимибом [38], в том числе статин с эзетимибом в одной таблетке или капсуле (зарегистрированы розувастатин+эзетимиб и аторвастатин+эзетимиб).
ЕОК/ЕОА IА (УУР А, УДД 2)
-
Пациентам после ОКС при недостижении целевых уровней ХС ЛНП через 4–6 недель на фоне максимально переносимых доз статином с и без эзетимиба рекомендовано присоединение алирокумаба** или эволокумаба** [40, 41, 250–252].
ЕОК/ЕОА IВ (УУР А, УДД 2)
-
Пациентам с противопоказаниями к терапии статином или подтвержденной непереносимостью статинов рекомендована терапия эзетимибом [71, 72].
ЕОК/ЕОА IIaC (УУР А, УДД 2)
-
У пациентов с ОКС, которые при поступлении имеют уровень ХС ЛНП выше целевого, несмотря на терапию максимально переносимыми дозами статина и эзетимибом, рекомендовано раннее назначение (во время госпитализации в связи с коронарным событием) алирокумаба** или эволокумаба** [104, 105].
ЕОК/ЕОА IIaC (УУР А, УДД 2)
Комментарий: если на фоне терапии статинами в максимально переносимых дозах уровень ХС ЛНП остается значительно повышенным (> 2,5 ммоль/л), можно рассмотреть блокаторы PCSK9 без предварительного применения эзетимиба.
5.5 ДЛП у пожилых
-
У пожилых лиц с АССЗ рекомендована терапия статином так же, как и у более молодых пациентов [106].
ЕОК/ЕОА IА (УУР А, УДД 1)
-
У пожилых лиц при наличии высокого и очень высокого риска для первичной профилактики рекомендована терапия статином [106].
ЕОК/ЕОА IА (УУР А, УДД 1)
-
Пациентам старше 75 лет при наличии высокого и очень высокого риска для первичной профилактики рекомендована терапия статином [106].
ЕОК/ЕОА IIbВ (УУР А, УДД 1)
-
У пожилых пациентов при наличии потенциального риска лекарственного взаимодействия рекомендуется назначать статин в низкой дозе с последующей титрацией до достижения целевого уровня ХС ЛНП [107, 108, 109]. При необходимости достижения более низкого целевого уровня ХС ЛНП у пациентов очень высокого и экстремального риска рассмотреть возможность комбинированной терапии низкими дозами статина и эзетимибом [50].
ЕОК/ЕОА IС (УУР С, УДД 5)
5.6 ДЛП у женщин, при беременности и лактации
-
Назначение гиполипидемических средств не рекомендуется при планировании беременности, во время беременности и в период грудного вскармливания. Пациенткам с тяжелой СГХС возможно назначение секвестрантов желчных кислот (не адсорбируемых) и/или применение плазмафереза, плазмосорбции [50].
ЕОК/ЕОА нет (УУР С, УДД 5)
-
У женщин группы высокого риска вне беременности и вне периода грудного вскармливания рекомендуется назначение статинов для первичной профилактики ИБС [39, 42].
ЕОК/ЕОА нет (УУР С, УДД 1)
-
Женщинам с целью вторичной профилактики вне беременности и вне периода грудного вскармливания рекомендованы статины по тем же показаниям и с теми же целевыми уровнями ХС ЛНП, что и мужчинам [39, 42].
ЕОК/ЕОА нет (УУР С, УДД 1)
Комментарии: использование современных низкодозированных комбинированных гормональных пероральных контрацептивов у женщин в репродуктивном возрасте не приводит к увеличению риска острых коронарных событий [110]. Их применение возможно у женщин после оценки липидных показателей, при нормальном уровне холестерина. При наличии ГХС (уровень ХС ЛНП выше 4 ммоль/л) и/или множественных факторах сердечно-сосудистого риска и/или высоком риске тромбоэмболических осложнений следует рассмотреть альтернативные гормональные пероральные контрацептивы [111]. Заместительная терапия эстрогенами, несмотря на положительное влияние на показатели липидного профиля, не продемонстрировала возможности снижения сердечно-сосудистого риска и не может быть рекомендована для сердечно-сосудистой профилактики у женщин [112].
Прием липидснижающих препаратов при подготовке к беременности, во время беременности и лактации запрещен. У пациенток с тяжелой СГХС во время беременности/лактации следует использовать плазмаферез, плазмосорбцию.
Женщины репродуктивного возраста:
– во время лечения должны пользоваться адекватными методами контрацепции;
– женщины с СГХС должны получить консультацию перед беременностью и инструкции по отмене гиполипидемических средств не позднее, чем за 4 недели до прекращения предохранения от беременности и не должны принимать эти препараты до окончания грудного вскармливания;
– в случае незапланированной беременности женщина с СГХС должна незамедлительно прекратить прием любых гиполипидемических средств и срочно проконсультироваться со своим лечащим врачом;
– в связи с результатами нескольких пилотных клинических исследований о негативном влиянии статинов на фертильную функцию у мужчин можно рекомендовать пациенту с СГХС воздержаться от приема статинов на период планируемого зачатия.
5.7 ДЛП и цереброваскулярная болезнь
-
Пациентам с перенесенным ишемическим инсультом рекомендована интенсивная липидснижающая терапия для достижения целевого уровня ХС ЛНП менее 1,4 ммоль/л [38, 50, 113, 114, 203, 204, 205].
ЕОК/ЕОА IA (УУР В, УДД 1)
Комментарий: дополнительные преимущества от снижения уровня ХС ЛНП ниже 1,8 ммоль/л были продемонстрированы в исследовании TST (Treat Stroke to Target): у пациентов с ранее перенесенным ИИ выбор такой тактики лечения позволял уменьшать риск развития повторных сердечно-сосудистых событий событий на 22%. Результаты исследования IMPOVE-IT и двух метаанализов показали дополнительное снижение риска развития СС событий при снижении уровня ХС ЛНП<1,4%, позволив определить формулу «чем ниже ХС ЛНП, тем ниже риск CC событий».
-
Рекомендуется большинству пациентам с ИИ или ТИА назначение высокоинтенсивной терапии статинами в максимально переносимых дозах для достижения целевого уровня ХС ЛНП [76, 204, 207].
ЕОК/ЕОА I A (УУР В, УДД 1)
Комментарий: под высокоинтенсивной терапией статинами подразумевается назначение аторвастатина** в дозах 40–80 мг/сут или розувастатина в дозах 20–40 мг/сут. При повышении уровня ТГ выше целевого значения (2,3 ммоль/л) назначение статинов также является терапией первой линии.
-
Рекомендуется пациентам старше 75 лет, перенесшим ИИ или ТИА, начинать умеренно-интенсивную терапию статинами [207, 208, 209].
ЕОК/ЕОА I A (УУР А, УДД 1)
Комментарий: под умеренно интенсивной терапией статинами подразумевают назначение аторвастатина** 10–20 мг/сут, розувастатина 5–10 мг/сут, питавастатина 4 мг.
-
Рекомендуется пациентам старше 75 лет с ИИ или ТИА, ранее получавшим высокоинтенсивную терапию статинами, продолжить ее, не изменяя режим интенсивности [210, 211].
ЕОК/ЕОА нет (УУР С, УДД 4)
-
Рекомендуется пациентам с ИИ или ТИА, не достигшим целевых значений ХС ЛНП на фоне терапии максимально переносимыми дозами статинами в течение 4-12 недель, добавление к терапии эзетимиба [203, 212].
ЕОК/ЕОА 1 А (УУР В, УДД 4)
-
Рекомендуется пациентам с ИИ или ТИА и непереносимостью статинаов назначение эзетимиба с целью достижения целевого значения ХС ЛНП [72, 73].
ЕОК/ЕОА I B (УУР С, УДД 5)
Комментарий: под непереносимостью статинов понимается развитие побочных эффектов после отмены и повторного рестарта терапии, в том числе с назначением другого статина и/или в сниженной дозе.
-
Рекомендуется пациентам с ИИ или ТИА добавление к проводимой терапии статинами и эзетимибом алирокумаба**, инклисирана** или эволокумаба**, с целью достижения целевого значения ХС ЛНП [40, 206, 250-252].
ЕОК/ЕОА 1 А (УУР A, УДД 1)
-
Рекомендуется пациентам с ИИ и ТИА оценка эффективности проводимой гиполипидемической терапии, ее безопасности и приверженности пациента к проводимому лечению (включая изменение образа жизни) [213, 214].
ЕОК/ЕОА нет (УУР С, УДД 4)
Комментарий: целесообразно проводить оценку лабораторных параметров (измерение уровня липидов натощак, АЛТ, АСТ) спустя 4–12 недель после начала приема статинов или увеличения их дозы. После достижения целевого уровня ХС ЛНП и ТГ (целевое значение для ТГ — менее 2,3 ммоль/л) рекомендован ежегодный лабораторный контроль (при отсутствии проблем с приверженностью пациента или других конкретных причин более частого мониторинга). Рутинный контроль печеночных ферментов во время лечения статинами не рекомендуется, за исключением наличия симптомов, свидетельствующих о патологии печени.
5.8 ДЛП и клапанные пороки сердца
-
Пациентам с аортальным стенозом без сопутствующей ИБС не рекомендовано начинать гиполипидемическую терапию с целью замедления прогрессирования аортального стеноза в отсутствие других показаний к такому лечению [115, 116, 117, 118].
ЕОК/ЕОА IIIА (УУР А, УДД 2)
Медицинская реабилитация
Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
-
Для всех пациентов с нарушениями липидного обмена рекомендована разработка индивидуального плана реабилитационных мероприятий, включающая в себя рекомендации по достижению ЦУ ХС ЛНП, повышению приверженности к лечению, питанию, физической активности, контролю веса [108].
ЕОК/ЕОА нет (УУР B, УДД 2)
-
С целью снижения риска ССО всем пациентам с ДЛП рекомендованы по крайней мере 3,5–7 ч умеренной физической активности в неделю или 30–60 мин большинство дней в неделю [119, 120, 121].
ЕОК/ЕОА нет (УУР А, УДД 1)
Прогноз
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Достижение и удержание ЦУ ХС ЛНП, ТГ является ключевым фактором, влияющим на прогноз и улучшающим сердечно-сосудистые исходы у пациентов как с ССЗ, так и СД.
Важными целями при лечении ДЛП являются:
– максимальное снижение риска развития ССО и смертельных исходов;
– коррекция всех модифицируемых ФР (курение, избыточная масса тела, ожирение, гипергликемия, АГ).
Госпитализация
Организация оказания медицинской помощи
Показания для плановой госпитализации: не предусмотрены
Показания для экстренной госпитализации: не предусмотрены
Показания к выписке пациента из стационара: не предусмотрены
Иные организационные технологии
При анализе работы медицинской организации с пациентами с нарушениями липидного обмена целесообразно анализировать следующие показатели:
-
процент пациентов высокого риска, достигших ЦУ ХС ЛНП менее 1,8 ммоль/л через 8 и 52 недели наблюдения;
-
процент пациентов, получающих комбинированную гиполипидемическую терапию.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Курение
-
Рекомендовано прекратить курение в любой форме [173]
ЕОК/ЕОА I A (УУР В, УДД 2)
-
Курильщикам рекомендуется назначение никотинзаместительной терапии или варениклина [174,175]
ЕОК/ЕОА IIa A (УУР A, УДД 1)
-
Отказ от курения рекомендован вне зависимости от набора веса, так как прибавка в весе не уменьшает пользы прекращения курения для АССЗ [176].
ЕОК/ЕОА I B (УУР B, УДД 3)
Комментарии: несмотря на то, что в сигаретах по типу «нагревание без горения» содержится меньше токсичных веществ, чем в обычных сигаретах, они содержат табак, поэтому их использование не рекомендуется. Долгосрочное влияние электронных сигарет на сердечно-сосудистую и дыхательную системы требует дополнительных исследований [177].
Физическая активность
-
Взрослым любого возраста для снижения общей смертности, СС заболеваемости и смертности рекомендовано стремиться по крайней мере к 150–300 мин аэробной физической активности умеренной интенсивности в неделю или 75–150 мин интенсивных нагрузок или эквиваленту из их сочетания [178]
ЕОК/ЕОА I A (УУР С, УДД 5)
-
Взрослым, которые не могут выполнять 150 минут физической активности средней интенсивности в неделю, рекомендуется оставаться настолько активными, насколько позволяют их способности и состояние здоровья [179]
ЕОК/ЕОА I A (УУР В, УДД 2)
Питание
-
Для снижения риска ССЗ рекомендовано использование cредиземноморской диеты и ее аналогов [46], замена насыщенных жиров на ненасыщенные [180] и ограничение употребления соли [181].
ЕОК/ЕОА I A (УУР B, УДД 1)
-
Рекомендовано употребление большего количества растительной пищи, богатой клетчаткой, включая цельнозерновые, фрукты, овощи, бобовые и орехи [182], рыбы, преимущественно жирных сортов, по крайней мере 1 раз в неделю и ограничение обработанного мяса [183] Рекомендуется ограничить потребление простых углеводов, в частности сахаросодержащих напитков, максимум до 10% от потребляемой энергии [184].
ЕОК/ЕОА I B (УУР С, УДД 5)
-
Рекомендовано ограничение употребления алкоголя до 100 г (чистого алкоголя) в неделю [185].
ЕОК/ЕОА I B (УУР B, УДД 2)
Ожирение
-
Людям с избыточным весом и лицам c ожирением рекомендуется снижение веса для уменьшения АД, дислипидемии и риска СД 2-го типа, и, таким образом, улучшения профиля ССР [186].
ЕОК/ЕОА I A (УУР А, УДД 1)
-
Следует рассмотреть возможность бариартрической хирургии при морбидном ожирении и отсутствии эффекта от немедикаментозных мер [187].
ЕОК/ЕОА IIa B (УУР А, УДД 1)
Сахарный диабет
-
Для скрининга сахарного диабета у лиц с АССЗ или без нее рекомендуется оценить HbA1c (который можно брать не натощак) или уровень глюкозы в крови натощак [188].
ЕОК/ЕОА IIa A (УУР С, УДД 5)
-
Рекомендуемый уровень HbA1c для снижения ССР и микроваскулярных осложнений СД у большинства пациентов 1-го и 2-го типов СД равен <7.0% [189].
ЕОК/ЕОА I A (УУР А, УДД 2)
Артериальное давление
-
Рекомендуется достижение уровня АД <140/90 мм рт. ст. у всех пациентов, индивидуальные целевые уровни зависят от возраста и наличия сопутствующей патологии [190].
ЕОК/ЕОА I A (УУР А, УДД 1)
-
Рекомендуется для пациентов 18–69 лет поддерживать САД в интервале 120–130 мм рт. ст. [191]. У пациентов ≥70 лет, получающих терапию, рекомендовано целевое значение САД <140 мм рт. ст. со снижением до 130 мм рт. ст. при удовлетворительной переносимости [192]. У всех пациентов, получающих терапию, рекомендовано снижение ДАД <80 мм рт. ст. [193]
ЕОК/ЕОА I A (УУР А, УДД 1)
Антитромботическая терапия
-
Антитромботическая терапия рекомендована для вторичной профилактики ССЗ [194].
ЕОК/ЕОА I A (УУР А, УДД 1)
Профилактика при различных клинических состояниях
-
Пациентам с онкологическими заболеваниями рекомендуется выявление и контроль факторов риска АССЗ [196].
ЕОК/ЕОА I С (УУР С, УДД 4)
-
Всем пациентам с ХОБЛ рекомендовано обследование на АССЗ и факторы риска АССЗ [197].
ЕОК/ЕОА I С (УУР В, УДД 2)
-
У взрослых с ревматоидным артритом рекомендуется умножение имеющегося риска сердечно-сосудистых осложнений на 1,5 [198].
ЕОК/ЕОА IIa B (УУР B, УДД 3)
-
У пациентов с АССЗ, ожирением и гипертонической болезнью, рекомендуется регулярный скрининг на полноценность сна (например, с помощью вопроса: «Как часто вас беспокоили проблемы с засыпанием, сонливостью или слишком долгого сна?») [199].
ЕОК/ЕОА I С (УУР С, УДД 5)
-
У мужчин с эректильной дисфункцией следует оценивать ССР [200, 201].
ЕОК/ЕОА IIa С (УУР В, УДД 3)
Динамическое наблюдение — чрезвычайно важная составляющая медицинской помощи пациентам с ДЛП, задачами которого являются: поддержание ЦУ ЛНП, ТГ, контроль выполнения врачебных рекомендаций по коррекции ФР, контроль за соблюдением режима приема медикаментозной терапии. Все рекомендации, даваемые пациенту, должны быть ясными, четкими и соответствовать его интеллектуальному уровню. С целью обеспечить осознанное участие пациента в лечебно-профилактическом процессе и повысить эффективность лечения целесообразно для ряда пациентов, для которых устных рекомендаций недостаточно, продублировать их в письменном виде.
После старта или изменения дозировок гиполипидемической терапии необходим контроль липидов сыворотки через 8 (±4) недель до достижения целевого уровня липидов, далее ежегодно (если нет проблем с приверженностью или других причин для более частого контроля). Контроль АЛТ, АСТ, билирубин, КФК проводится через 4–6 недель после изменения гиполипидемической терапии, после достижения целевого уровня липидов рутинный контроль не требуется, только при наличии жалоб, характерных для поражения печени или мышц.
Согласно рекомендациям по диспансерному наблюдению пациентов с АГ, стабильной ИБС, перенесенным ОНМК в анамнезе требуется контроль уровня ХС ЛНП и АД дважды в год. При гиперхолестеринемии выше 8,0 ммоль/л рекомендован контроль ХС ЛНП не реже 1 раза в год. У пациентов со стенозом сонной артерией более 50% требуется контроль ХС ЛНП дважды в год [202].
Регулярный мониторинг HbA1c и/или уровня глюкозы плазмы должен проводиться пациентам с высоким риском развития СД и при высокодозной терапии статинами.
С целью своевременной модификации сердечно-сосудистого риска у больных с ДЛП рекомендуется динамическое наблюдение за выраженностью атеросклеротического процесса. Согласно консенсусу российких экспертов [256], при отсутствии АСБ в сонных и бедренных артериях пациенту должно быть рекомендовано повторное УЗИ через 3 года. При наличии АСБ высотой <1,5 мм и максимальном стенозе <25% в сонных артериях, а также при максимальном стенозе <25% в бедренных артериях повторное УЗИ артерий следует провести через 2 года. При АСБ высотой ≥1,5 мм и максимальном стенозе <50% в сонных артериях, а также при максимальном стенозе 25-49% в бедренных артериях повторное УЗИ рекомендуется проводить через 1 год, при отсутствии динамики атеросклеротического процесса частоту исследований можно сократить до 1 исследования в 2–3 года. При выявлении максимального стеноза ≥50% в сонных артериях следует ежегодно проводить стандартное дуплексное сканирование экстракраниального отдела брахиоцефальных артерий, частоту которого можно сократить до 1 раза в 2 года при отсутствии динамики атеросклеротического процесса.
Информация
Источники и литература
-
Клинические рекомендации Российского кардиологического общества
- Rosenberg WM, Gray JA et al. Evidence based medicine: what it is and what it isn”t. BMJ 1996, January; 312 (7023): 71–72.
Федеральный закон от 21.11.2011 № 323-ФЗ (ред. от 03.04.2017) «Об основах охраны здоровья граждан в Российской Федерации».
Эпидемиологический словарь, 4-е издание. Под ред. Джона М. Ласта для Международной эпидемиологической ассоциации. М, 2009. 316 с.
Федеральное агентство по техническому регулированию и метрологии. Национальный стандарт Российской Федерации. ГОСТР 52379–2005. Надлежащая клиническая практика. Москва, 2005.
Федеральный закон от 12.04.2010 № 61-ФЗ (ред. от 03.07.2016) «Об обращении лекарственных средств».
Малая медицинская энциклопедия. М.: Медицинская энциклопедия, 1991—96 гг. [Электронный ресурс]. Режим доступа:http://dic.academic.ru/dic.nsf/enc_medicine/28878/Синдром.
Андреева Н. С, Реброва О. Ю, Зорин Н. А. и др. Системы оценки достоверности научных доказательств и убедительности рекомендаций: сравнительная характеристика и перспективы унификации. Медицинские технологии. Оценка и выбор. 2012. №. 4. С. 10–24.
Кухарчук В. В. и др. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, VII пересмотр //Атеросклероз и дислипидемии. 2020. Т. 11. №. 1 (38).
Nordestgaard BG et al. Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society. //European heart journal. 2013. Vol. 34. №. 45. P. 3478–3490.
Yao Z. Human apolipoprotein C-III — a new intrahepatic protein factor promoting assembly and secretion of very low density lipoproteins. Cardiovasc Hematol Disord Drug Targets. 2012;12(2):133–140.
Sacks FM, Alaupovic P, Moye LA, et al. VLDL, apolipoproteins B, CIII, and E, and risk of recurrent coronary events in the Cholesterol and Recurrent Events (CARE) trial. Circulation. 2000;102:1886–1892.
Hegele RA, Ginsberg HN, Chapman MJ et al. The polygenic nature of hypertriglyceridaemia: implications for definition, diagnosis, and management. Lancet Diabetes Endocrinol. 2014. 2(8): 655–666. doi:10.1016/S2213-8587(13)70191-8
Метельская В. А. и др. Анализ распространенности показателей, характеризующих атерогенность спектра липопротеидов, у жителей Российской Федерации (по данным исследования ЭССЕ-РФ) //Профилактическая медицина. 2016. Т. 19. №. 1. P. 15–23.
Caggiula AW et al. The multiple risk factor intervention trial (MRFIT): IV. Intervention on blood lipids //Preventive Medicine. 1981. Vol. 10. №. 4. P. 443–475.
Castelli WP. Epidemiology of triglycerides: A view from Framingham. Am J Cardiol. 1992. 70(19): H3–H9. doi:10.1016/0002-9149(92)91083-g
Carey VJ et al. Contribution of high plasma triglycerides and low high-density lipoprotein cholesterol to residual risk of coronary heart disease after establishment of low-density lipoprotein cholesterol control //The American journal of cardiology. 2010. Vol. 106. №. 6. P. 757–763.
Barter P, Gotto AM, LaRosa JC et al. HDL Cholesterol, Very Low Levels of LDL Cholesterol, and Cardiovascular Events. New England Journal of Medicine. 2007. 357(13): 1301–1310. doi:10.1056/nejmoa064278
Aguiar C et al. A review of the evidence on reducing macrovascular risk in patients with atherogenic dyslipidaemia: A report from an expert consensus meeting on the role of fenofibrate–statin combination therapy //Atherosclerosis Supplements. 2015. Vol. 19. P. 1–12.
Prospective Studies Collaboration et al. Blood cholesterol and vascular mortality by age, sex, and blood pressure: a meta-analysis of individual data from 61 prospective studies with 55 000 vascular deaths //The Lancet. 2007. Vol. 370. №. 9602. P. 1.
Catapano AL et al. 2016 ESC/EAS Guidelines for the Management of Dyslipidaemias. // Eur Heart J. 2016. Vol. 37. №. 39. P. 2999–3058.
Holewijn S et al. Apolipoprotein B, non-HDL cholesterol and LDL cholesterol for identifying individuals at increased cardiovascular risk // Journal of internal medicine. 2010. Vol. 268. №. 6. P. 567–577.
Boekholdt SM et al. Association of LDL cholesterol, non–HDL cholesterol, and apolipoprotein B levels with risk of cardiovascular events among patients treated with statins: a meta-analysis // Jama. 2012. Vol. 307. №. 12. P. 1302–1309.
Langsted A, Nordestgaard BG. Nonfasting versus fasting lipid profile for cardiovascular risk prediction. Pathology. 2019. 51(2): 131–141. doi:10.1016/j.pathol.2018.09.062
Farukhi Z, Mora S. The Future of Low-Density Lipoprotein Cholesterol in an Era of Nonfasting Lipid Testing and Potent Low-Density Lipoprotein Lowering. Circulation. 2018. 137(1): 20–23. doi:10.1161/CIRCULATIONAHA.117.031857
Meijboom WB, Meijs MF, Schuijf JD et al. Diagnostic accuracy of 64-slice computed tomography coronary angiography: a prospective, multicenter, multivendor study. J Am Coll Cardiol. 2008. 52(25): 2135–2144. doi:10.1016/j.jacc.2008.08.058
Agatston AS, Janowitz WR, Hildner FJ et al. Quantification of coronary artery calcium using ultrafast computed tomography. J Am Coll Cardiol. 1990. 15(4): 827–832. doi:10.1016/0735-1097(90)90282-t
Serrano CV, de Mattos FR, Pitta FG et al. Association between Neutrophil-Lymphocyte and Platelet-Lymphocyte Ratios and Coronary Artery Calcification Score among Asymptomatic Patients: Data from a Cross-Sectional Study. Mediators Inflamm. 2019. 2019: 1–8. doi:10.1155/2019/6513847
Piepoli MF et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice, (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR) // European heart journal. 2016. Vol. 37. №. 29. P. 231.
Mortensen MB, Falk E, Li D et al. Statin Trials, Cardiovascular Events, and Coronary Artery Calcification. JACC: Cardiovascular Imaging. 2018. 11(2): 221–230. doi:10.1016/j.jcmg.2017.01.029
McDermott MM, Kramer CM, Tian L et al. Plaque Composition in the Proximal Superficial Femoral Artery and Peripheral Artery Disease Events. JACC: Cardiovascular Imaging. 2017. 10(9): 1003–1012. doi:10.1016/j.jcmg.2016.08.012
Sillesen H, Sartori S, Sandholt B et al. Carotid plaque thickness and carotid plaque burden predict future cardiovascular events in asymptomatic adult Americans. European Heart Journal — Cardiovascular Imaging. 2017. 19(9): 1042–1050. doi:10.1093/ehj
Perrone-Filardi P, Achenbach S, Mohlenkamp S et al. Cardiac computed tomography and myocardial perfusion scintigraphy for risk stratification in asymptomatic individuals without known cardiovascular disease:, a position statement of the Working Group on Nuclear Cardiology and Cardiac CT of the European Society of Cardiology //European heart journal. 2011. Vol. 32. №. 16. P. 1986–1993.
Den Ruijter HM, Peters SAE, Anderson TJ et al. Common Carotid Intima-Media Thickness Measurements in Cardiovascular Risk Prediction. JAMA. 2012. 308(8): 796–803. doi:10.1001/jama.2012.9630
Inaba Y, Chen JA, Bergmann SR. Carotid plaque, compared with carotid intima-media thickness, more accurately predicts coronary artery disease events: a meta-analysis // Atherosclerosis. 2012. Vol. 220. №. 1. P. 128–133.
Lorenz MW et al. Carotid intima-media thickness progression to predict cardiovascular events in the general population (the PROG-IMT collaborative project): a meta-analysis of individual participant data // The Lancet. 2012. Vol. 379. №. 9831. P. 2053–2062.
Pletcher MJ et al. Using the coronary artery calcium score to predict coronary heart disease events: a systematic review and meta-analysis // Archives of internal medicine. 2004. Vol. 164. №. 12. P. 1285–1292.
Akioyamen LE et al. Risk factors for cardiovascular disease in heterozygous familial hypercholesterolemia: A systematic review and meta-analysis // Journal of clinical lipidology. 2019. Vol. 13. №. 1. P. 15–30.
Cannon C. P et al. Ezetimibe added to statin therapy after acute coronary syndromes // New England Journal of Medicine. 2015. Vol. 372. №. 25. P. 2387–2397.
Trialists CT et al. Efficacy and safety of LDL-lowering therapy among men and women: meta-analysis of individual data from 174 000 participants in 27 randomised trials // The Lancet. 2015. Vol. 385. №. 9976. P. 1397–1405.
Sabatine MS et al. Evolocumab and clinical outcomes in patients with cardiovascular disease // New England Journal of Medicine. 2017. Vol. 376. №. 18. P. 1713–1722.
Jukema JW et al. ODYSSEY OUTCOMES Committees and Investigators. Alirocumab in patients with polyvascular disease and recent acute coronary syndrome: ODYSSEY OUTCOMES trial // J Am Coll Cardiol. 2019. Vol. 74. №. 9. P. 1167–1176.
Trialists CT et al. The effects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomised trials // The Lancet. 2012. Vol. 380. №. 9841. P. 581–590.
Santos RD et al. Defining severe familial hypercholesterolaemia and the implications for clinical management: a consensus statement from the International Atherosclerosis Society Severe Familial Hypercholesterolemia Panel // The lancet Diabetes & endocrinology. 2016. Vol. 4. №. 10. P. 850–861.
Eckel RH, Jakicic JM, Ard JD et al. 2013 AHA/ACC Guideline on Lifestyle Management to Reduce Cardiovascular Risk. Circulation. 2013. 129(25 suppl 2): S76–S99. doi:10.1161/01.cir.0000437740.48606.d1
de Lorgeril M, Salen P, Martin J-L et al. Mediterranean Diet, Traditional Risk Factors, and the Rate of Cardiovascular Complications After Myocardial Infarction. Circulation. 1999. 99(6): 779–785. doi:10.1161/01.cir.99.6.779.
Estruch R, Ros E, Salas-Salvado J, et al. Primary Prevention of Cardiovascular Disease with a Mediterranean Diet Supplemented with Extra-Virgin Olive Oil or Nuts. N Engl J Med. 2018. 378(25): e34. doi:10.1056/NEJMoa1800389.
Mozaffarian D, Lemaitre RN, King IB et al. Plasma Phospholipid Long-Chain ω-3 Fatty Acids and Total and Cause-Specific Mortality in Older Adults. Ann Intern Med. 2013. 158(7): 515–525. doi:10.7326/0003-4819-158-7-201304020-00003
Lu Z, Kou W, Du B, et al. Effect of Xuezhikang, an Extract From Red Yeast Chinese Rice, on Coronary Events in a Chinese Population With Previous Myocardial Infarction. Am J Cardiol. 2008. 101(12): 1689–1693. doi:10.1016/j.amjcard.2008.02.056
Li Y, Jiang L, Jia Z, et al. A Meta-Analysis of Red Yeast Rice: An Effective and Relatively Safe Alternative Approach for Dyslipidemia. PLoS One. 2014. 9(6): e98611. doi:10.1371/journal.pone.0098611
Mach F, Baigent C, Catapano A.L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2019. doi:10.1093/eurheartj/ehz455
- Rosenberg WM, Gray JA et al. Evidence based medicine: what it is and what it isn”t. BMJ 1996, January; 312 (7023): 71–72.
Информация
Список сокращений
АГ артериальная гипертония
АД артериальное давление
АЛТ аланинаминотрансфераза
АСБ атеросклеротическая бляшка
АСТ аспартатаминотрансфераза
АССЗ атеросклеротическое сердечно-сосудистое заболевание
ВГН верхняя граница нормы
ДЛП дислипидемия
геСГХС гетерозиготная семейная гиперхолестеринемия
гоСГХС гомозиготная семейная гиперхолестеринемия
ГТГ гипертриглицеридемия
ГХС гиперхолестеринемия
ДИ доверительный интервал
ДЛП дислипидемия
ЕОК Европейское общество кардиологов
ЕОА Европейское общество атеросклероза
ЖНВЛП жизненно-необходимые важнейшие лекарственные препараты
ИБС ишемическая болезнь сердца
ИМ инфаркт миокарда
ИМТ индекс массы тела
КИ кальциевый индекс
КТ компьютерная томография
КФК креатинфосфокиназа
ЛВП липопротеиды высокой плотности
ЛНП липопротеиды низкой плотности
Лп(а) липопротеид(а)
ЛПП липопротеиды промежуточной плотности
ЛОНП липопротеиды очень низкой плотности
миРНК малая интерферирующая рибонуклеиновая кислота
неЛВП липопротеиды невысокой плотности
омега-3 ПНЖК омега-3 триглицериды, включая другие эфиры и кислоты
ОКС острый коронарный синдром
ОР относительный риск
ОХС общий холестерин
РНК рибонуклеиновая кислота
СГХС семейная гиперхолестеринемия
СД сахарный диабет
СКФ скорость клубочковой фильтрации
ССЗ сердечно-сосудистые заболевания
ССО сердечно-сосудистые осложнения
ТГ триглицериды
ТИА транзиторная ишемическая атака
УЗИ ультразвуковое исследование
ФР факторы риска
ХБП хроническая болезнь почек
ХМ хиломикроны
ХС холестерин
ЦУ целевой уровень
РЛНП рецептор к липопротеидам низкой плотности
APOB ген аполипопротеина В
DLCN Dutch Lipid Clinic Network
LDLR ген рецептора липопротеидов низкой плотности
PCSK9 пропротеин-конвертаза субтилин/кексин типа 9 (C10AX Другие гиполипидемические средства)
SCORE системная оценка коронарного риска (Systemic Coronary Risk Evaluation)
Термины и определения
Дислипидемии (ДЛП) — состояния, когда концентрации липидов и липопротеидов крови выходят за пределы нормы.
Доказательная медицина — надлежащее, последовательное и осмысленное использование современных наилучших доказательств (результатов клинических исследований) в сочетании с индивидуальным клиническим опытом и c учетом ценностей и предпочтений пациента в процессе принятия решений о состоянии здоровья и лечении пациента [1].
Заболевание — состояние, возникающее в связи с воздействием патогенных факторов, нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма [2].
Исход — любой возможный результат, возникающий от воздействия причинного фактора, профилактического или терапевтического вмешательства, все установленные изменения состояния здоровья, возникающие как следствие вмешательства [3].
Клиническое исследование — любое исследование, проводимое с участием человека в качестве субъекта для выявления или подтверждения клинических и/или фармакологических эффектов исследуемых продуктов и/или выявления нежелательных реакций на исследуемые продукты, и/или изучения их всасывания, распределения, метаболизма и выведения с целью оценить их безопасность и/или эффективность [4].
Конфликт интересов — ситуация, при которой у медицинского или фармацевтического работника при осуществлении ими профессиональной деятельности возникает личная заинтересованность в получении лично либо через представителя компании материальной выгоды или иного преимущества, которое влияет или может повлиять на надлежащее исполнение ими профессиональных обязанностей вследствие противоречия между личной заинтересованностью медицинского работника или фармацевтического работника и интересами пациента [2].
Лекарственные препараты — лекарственные средства в виде лекарственных форм, применяемые для профилактики, диагностики, лечения заболевания, реабилитации, для сохранения, предотвращения или прерывания беременности [5].
Медицинское вмешательство — выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинской деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследований и (или) медицинских манипуляций, а также искусственное прерывание беременности [2].
Изменение образа жизни — мероприятия, направленные на нормализацию веса и характера питания, двигательной активности, целью которых является снижение сердечно-сосудистого риска.
Пациент — физическое лицо, которому оказывается медицинская помощь или которое обратилось за оказанием медицинской помощи независимо от наличия у него заболевания и от его состояния [2].
Пожилые пациенты — пациенты, которым от 60 до 75 лет.
Рабочая группа по разработке/актуализации клинических рекомендаций — коллектив специалистов, работающих совместно и согласованно в целях разработки/актуализации клинических рекомендаций и несущих общую ответственность за результаты данной работы.
Синдром — устойчивая совокупность ряда симптомов с единым патогенезом [6].
Состояние — изменения организма, возникающие в связи с воздействием патогенных и (или) физиологических факторов и требующие оказания медицинской помощи [2].
Уровень достоверности доказательств — степень уверенности в том, что полученный эффект от применения медицинского вмешательства является истинным [7].
Уровень убедительности рекомендаций — степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда, в конкретной ситуации [7].
Хроническая болезнь почек — наднозологическое понятие, объединяющее всех пациентов с признаками повреждения почек и/или снижением функции, оцениваемой по величине скорости клубочковой фильтрации, которые сохраняются в течение 3 и более месяцев.
Целевой уровень — уровень того или иного лабораторного, инструментального, клинического показателя, различный для разных групп пациентов с тем или иным заболеванием, достижение которого в процессе лечения позволяет добиться наиболее благоприятного соотношения польза (снижение сердечно-сосудистого риска) — риск (неблагоприятные эффекты).
Критерии оценки качества медицинской помощи
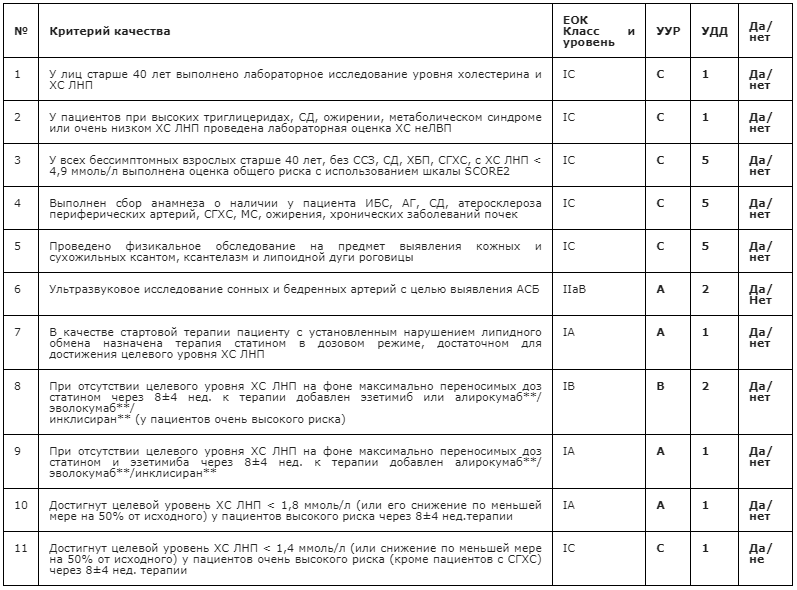
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Президиум рабочей группы:
Ежов М. В.
Кухарчук В. В.
Сергиенко И. В.
Другие члены рабочей группы:
Алиева А. С.
Анциферов М. Б.
Аншелес А. А.
Арабидзе Г. Г.
Аронов Д. М.
Арутюнов Г. П.
Ахмеджанов Н. М.
Балахонова Т. В.
Барбараш О. Л.
Бойцов С. А.
Бубнова М. Г.
Воевода М. И.
Галстян Г. Р.
Галявич А. С.
Горнякова Н. Б.
Гуревич В. С.
Дедов И.И.
Драпкина О. М.
Дупляков Д. В.
Ерегин С. Я.
Ершова А. И.
Иртюга О. Б.
Карпов Р. С.
Карпов Ю. А.
Качковский М. А.
Кобалава Ж. Д.
Козиолова Н. А.
Коновалов Г. А.
Константинов В. О.
Космачева Е. Д.
Котовская Ю. В.
Мартынов А. И.
Мешков А. Н.
Небиеридзе Д. В.
Недогода С. В.
Обрезан А. Г.
Олейников В. Э.
Покровский С. Н.
Рагино Ю. И.
Ротарь О. П.
Скибицкий В. В.
Смоленская О. Г.
Соколов А. А.
Сумароков А. Б.
Ткачева О. Н.
Филиппов А. Е.
Халимов Ю. Ш.
Чазова И. Е.
Шапошник И. И.
Шестакова М.В.
Шляхто Е. В.
Члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов. В случае сообщения о наличии конфликта интересов член(ы) рабочей группы был(и) исключен(ы) из обсуждения разделов, связанных с областью конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Представленные Рекомендации разработаны на основе Рекомендаций по лечению нарушений липидного обмена Европейского общества кардиологов и Европейского общества по изучению атеросклероза 2019 года [50].
В Рекомендациях, основанных на результатах крупнейших эпидемиологических, рандомизированных клинических исследований и метаанализов, обобщены и изложены основные принципы лечения пациентов с нарушениями липидного обмена в целом и в особых клинических ситуациях. Основная цель Рекомендаций — облегчить принятие решения при выборе оптимальной стратегии лечения конкретного пациента с дислипидемией. Тем не менее окончательное решение о лечении должно быть принято с учетом индивидуальных особенностей механизмов развития и течения заболевания.
Целевая аудитория данных клинических рекомендаций:
1. Врач-кардиолог.
2. Врач-терапевт.
3. Врач общей практики.
4. Врач-эндокринолог.
5. Врач-невролог.
Вследствие того, что члены Российского кардиологического общества входят в состав Европейского общества кардиологов и также являются его членами, все рекомендации Европейского общества кардиологов (ЕОК) формируются с участием российских экспертов, которые являются соавторами европейских рекомендаций. Таким образом, существующие рекомендации ЕОК отражают общее мнение ведущих российских и европейских кардиологов. В связи с этим формирование Национальных рекомендаций проводилось на основе рекомендаций ЕОК, с учетом национальной специфики, особенностей обследования, лечения, учитывающих доступность медицинской помощи. По этой причине в тексте настоящих клинических рекомендаций, одновременно использованы две шкалы оценки достоверности доказательств тезисов рекомендаций: уровни достоверности доказательств ЕОК с УУР и УДД. Добавлены классы рекомендаций ЕОК, позволяющие оценить необходимость выполнения тезиса рекомендаций (Таблицы 1, 2, 3, 4, 5).
Таблица 1. Шкала оценки классов рекомендаций Европейского общества кардиологов (ЕОК)
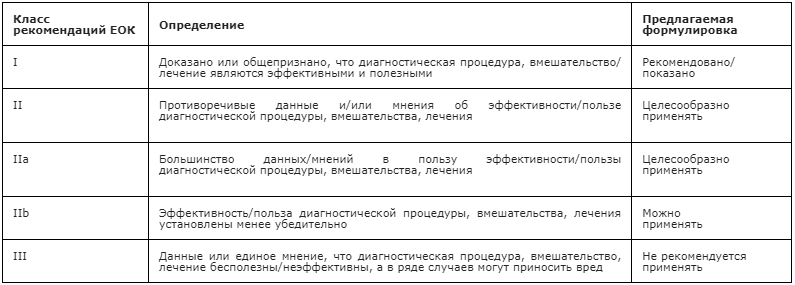
Таблица 2. Шкала оценки уровней достоверности доказательств Европейского общества кардиологов (ЕОК)

Таблица 3. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)

Таблица 4. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
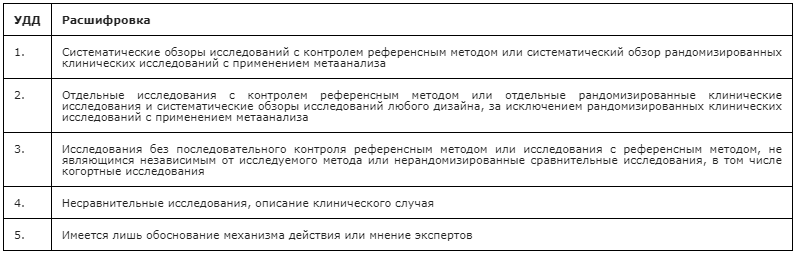
Таблица 5. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)

Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию — не реже чем один раз в три года или при появлении новой информации о тактике ведения пациентов с данным заболеванием. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими некоммерческими профессиональными организациями. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
1. Приказ Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. № 918н «Об утверждении Порядка оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями».
2. Приказ Минестерства здравоохранения Российской Федерации от 10 мая 2017 г. № 203н «Об утверждении критериев оценки качества медицинской помощи».
3. Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 № 103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации» (Зарегистрирован 08.05.2019 № 54588)
Таблица А3.1. Классификация дислипидемий (ВОЗ, адаптировано из классификации Fredrickson)
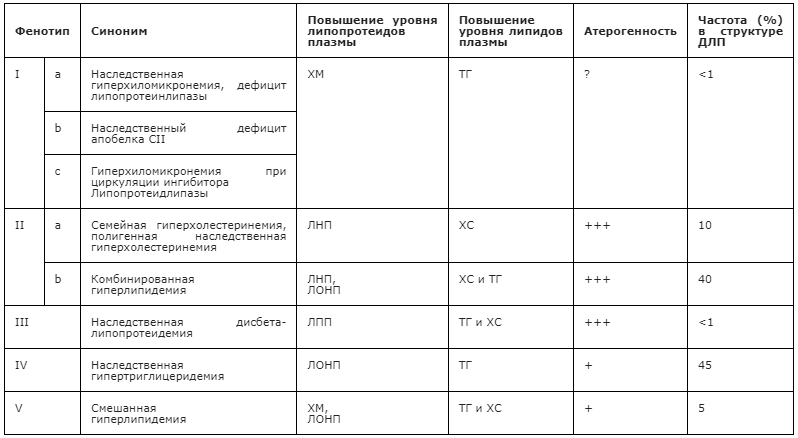
ДЛП — дислипидемия, ОХС — общий холестерин, ЛВП — липопротеиды высокой плотности, ЛНП — липопротеиды низкой плотности, ТГ — триглицериды, ЛОНП — липопротеиды очень низкой плотности, ХМ — хиломикроны.
Таблица А3.2. Оптимальные значения липидных параметров в зависимости от категории риска

* И снижение ХС ЛНП >50% от исходного уровня.
ЛВП — липопротеиды высокой плотности, ЛНП — липопротеиды низкой плотности, ТГ — триглицериды, Лп(а) — липопротеид(а).
Таблица А3.3. Факторы риска развития и прогрессирования атеросклероза
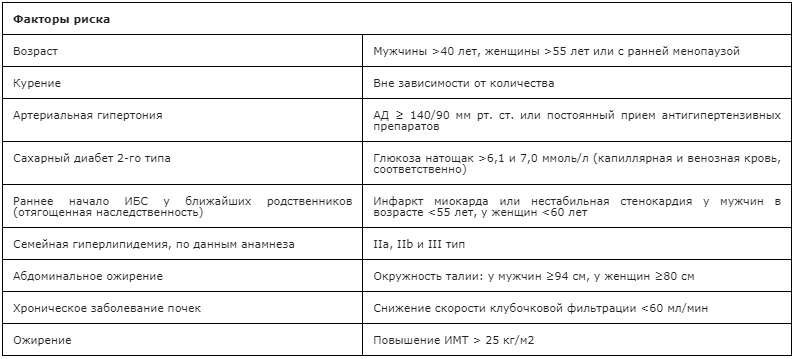
Приложение А3.1. Принципы диагностики и оценки сердечно-сосудистого риска
Таблица А3.4. Количественная оценка индекса коронарного кальция

Таблица А3.5. Основные наследственные (генетические) дислипидемии [9]
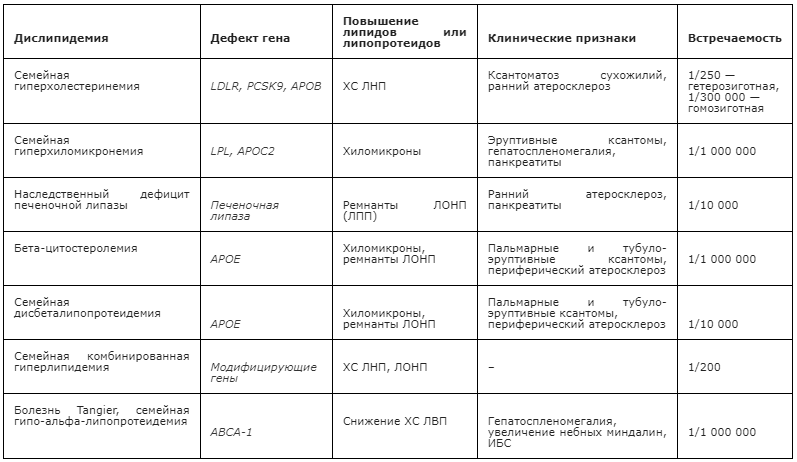
ХС ЛНП — холестерин липопротеидов низкой плотности; ХС ЛОНП — холестерин липопротеидов очень низкой плотности; ХС ЛПП — холестерин липопротеидов промежуточной плотности ХС ЛВП — холестерин липопротеидов высокой плотности; ИБС — ишемическая болезнь сердца.
Таблица А3.6 Популяционные показатели ХС ЛНП в зависимости от пола и возраста для РФ.
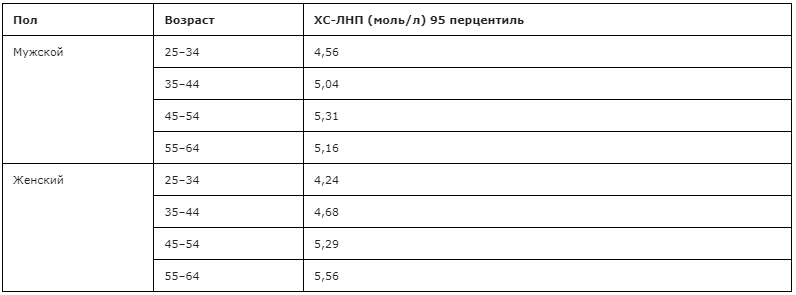
Таблица А3.7. Диагностические критерии Simon Broome Registry — Саймона Брума

Таблица А3.8. Диагностические критерии гоСГХС

Таблица А3.9. Препараты, потенциально взаимодействующие с статинами
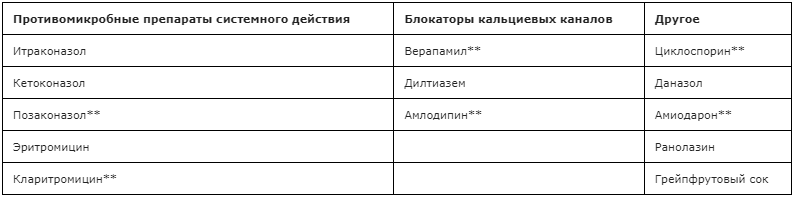
Таблица А3.10. Сравнение эффективности фенофибрата**, статинов и эзетимиба [38, 62, 63, 148, 8]
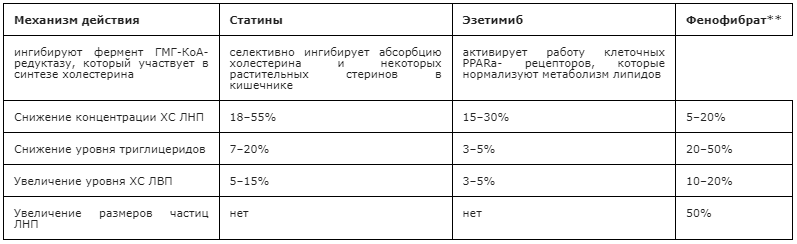
Таблица А3.11. Расчет степени снижения ХС ЛНП при различных вариантах гиполипидемической терапии

Таблица А3.12. Показания к плазмаферезу, плазмосорбции
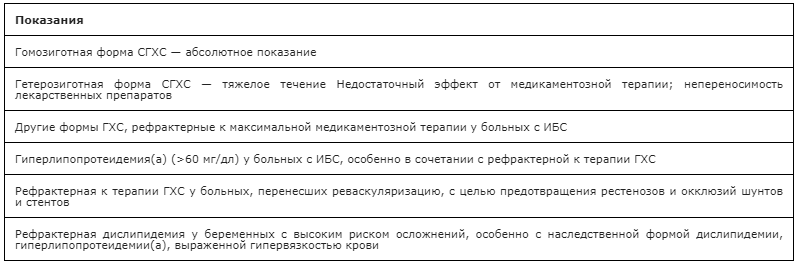
СГХС — семейная гиперхолестеринемия.
Таблица А3.13. Сводные данные по эффектам гиполипидемических препаратов [149]
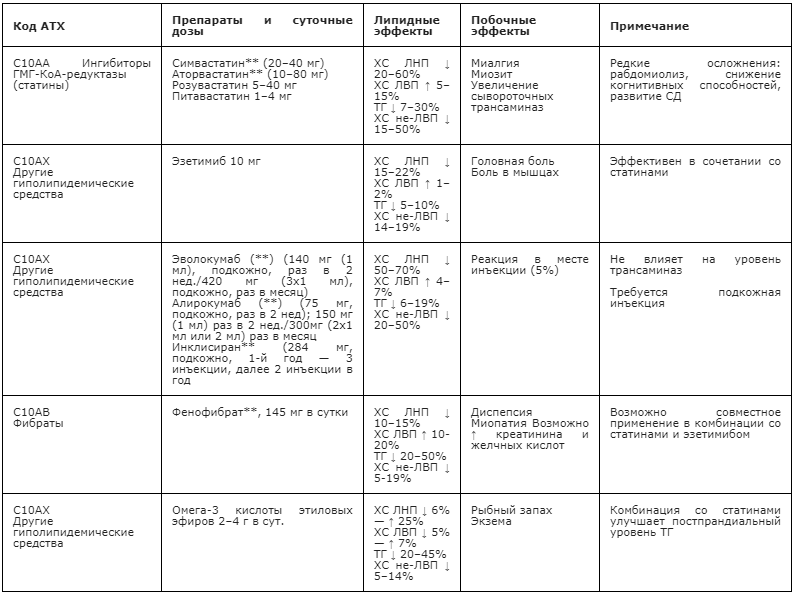
Приложение Б. Алгоритмы действий врача
Приложение Б1. Алгоритм лечения гипертриглицеридемии
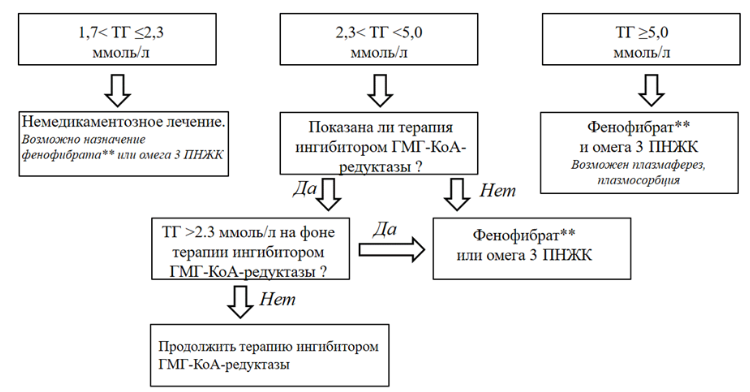
Примечание. Омега3 ПНЖК — Омега-3 кислоты этиловых эфиров, включая другие эфиры и кислоты, в дозе 2–4 г/сут. При тяжелой гипертриглицеридемии рассмотреть вопрос использования плазмафереза, плазмосорбции.
Приложение Б2. Алгоритм медикаментозной терапии для достижения целевого уровня ХС ЛНП
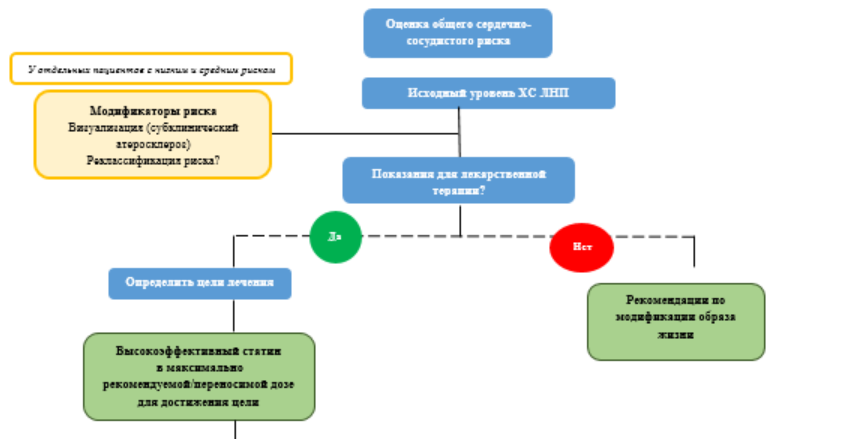
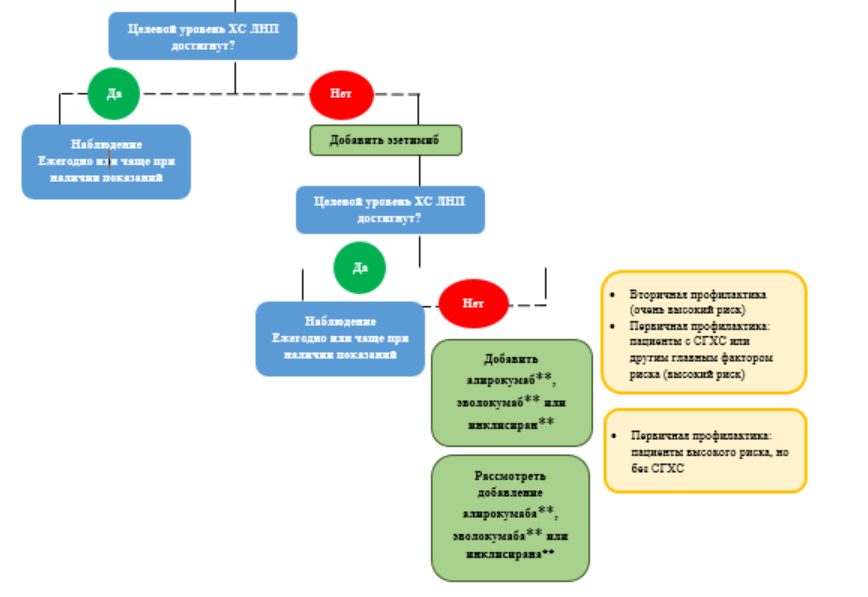
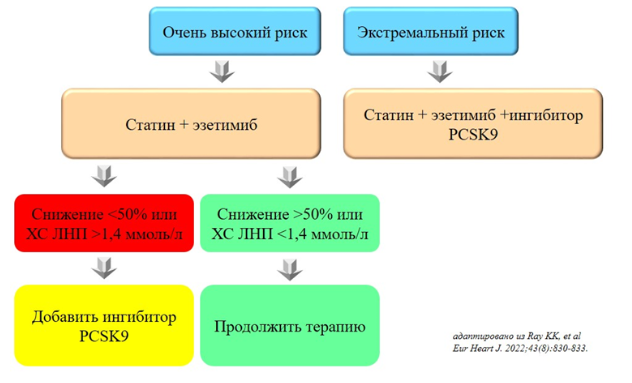
Таблица Б1. Лабораторный контроль безопасности и эффективности (показатели, кратность) до и во время гиполипидемической терапии
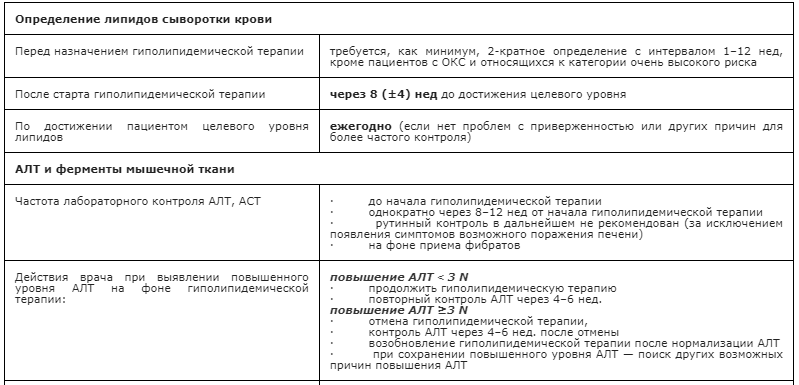

Таблица Б3/4. Интенсивность терапии статинами
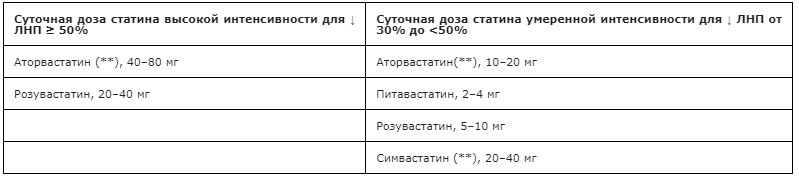
Приложение Б4: принципы гиполипидемической терапии и диспансерное наблюдение больных с ДЛП
Таблица Б4/1. Тактика ведения в зависимости от сердечно-сосудистого риска и уровня холестерина [50]
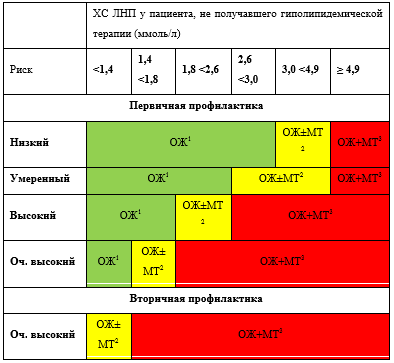
Примечание: ХС ЛНП — холестерин липопротеидов низкой плотности. У больных ССЗ терапия статинами назначается вне зависимости от уровня ХС.
1. ОЖ: лечение не требуется, рекомендуется поддержание здорового образа жизни и контроль факторов риска.
2. ОЖ±МТ: рекомендуется поддержание здорового образа жизни и, возможно (по решению врача), назначение липидснижающей терапии, если целевой уровень ХС ЛНП не достигнут.
3. ОЖ+МТ: рекомендуется поддержание здорового образа жизни и одновременное назначение липидснижающей терапии.
Таблица Б4/2 Влияние изменения образа жизни на уровень липидов [50]
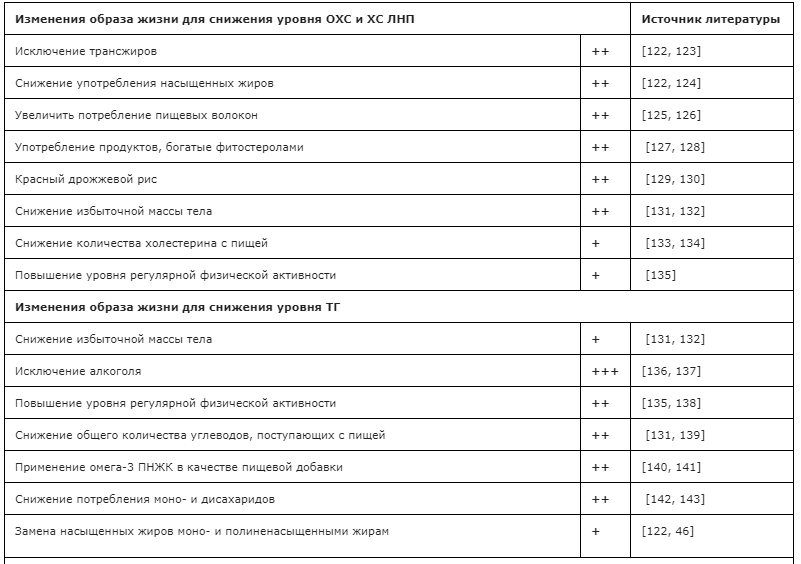

Примечание: +++ Общее соглашение об эффективности влияния на уровень липидов. ++ Менее выраженное влияние на уровень липидов; имеющиеся свидетельства/мнения специалистов указывают на эффективность мероприятий. + Противоречивые сведения.
Приложение В. Информация для пациента
Таблица В1. Рекомендации по диете для улучшения общего профиля липопротеидов
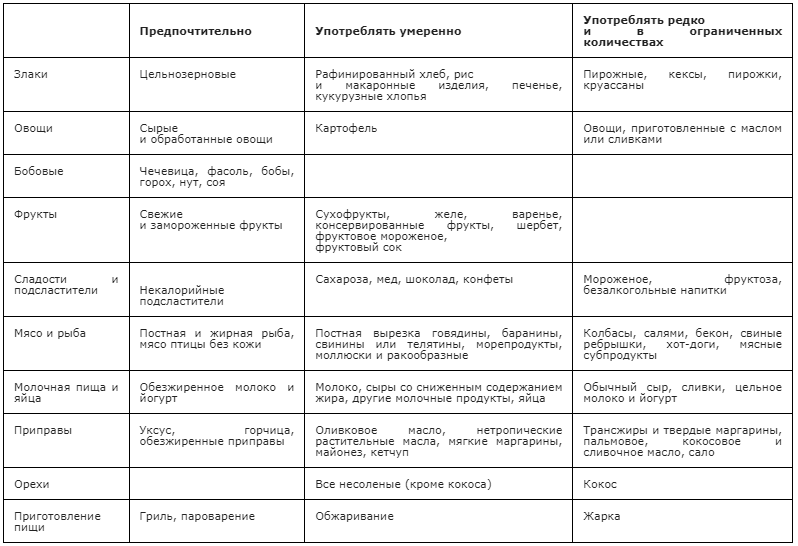
Примечание: умеренное употребление алкоголя (не более 50 мг в день крепких напитков, 200 мг красного или белого вина и не более 350 мл пива во время приема пищи) является приемлемым, при условии, что уровень ТГ не повышен, отсутствует гипертоническая болезнь и/или печеночная недостаточность.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Голландские диагностические критерии гетерозиготной семейной гиперхолестеринемии
Название на русском языке: Голландские диагностические критерии гетерозиготной семейной гиперхолестеринемии
Оригинальное название (если есть): Dutch Lipid Clinic Network criteria
Источник (официальный сайт разработчиков, публикация с валидацией): [9]
Тип (подчеркнуть): шкала оценки
Назначение: постановка клинического диагноза гетерозиготной семейной гиперхолестеринемии
Содержание (шаблон):
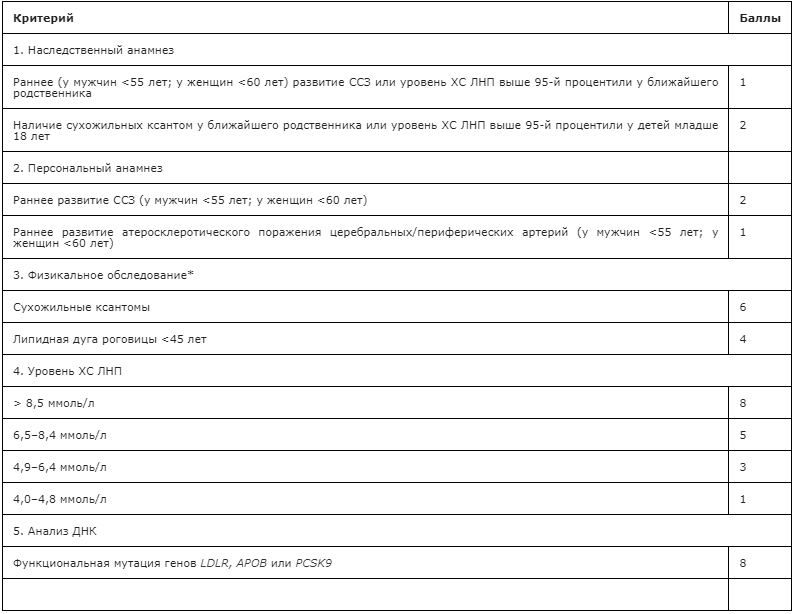
* исключают друг друга (т. е. максимум 6 баллов). ССЗ — сердечно-сосудистое заболевание, ХС ЛНП — холестерин липопротеидов низкой плотности, СГХС — семейная гиперхолестеринемия.
Ключ (интерпретация): Диагноз ставится на основании суммы баллов: «определенная» СГХС — >8 баллов, «предположительная» ИЛИ «вероятная» СГХС — 6–8 баллов, «возможная» СГХС — 3–5 баллов, «маловероятная» СГХС — 0–2 баллов.
Таблица Г2. Шкала SCORE2 расчета нефатальных СС осложнений для стран очень высокого риска.
Название на русском языке: Шкала SCORE2
Оригинальное название (если есть): Systematic COronary Risk Evaluation model
Источник (официальный сайт разработчиков, публикация с валидацией): escardio.org. SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe // European heart journal. 2021. Vol. 42. №. 25. P. 2439–2454.
Тип (подчеркнуть): шкала оценки
Назначение: расчет риска нефатальных сердечно-сосудистых осложнений
Содержание (шаблон) и интерпретация:
SCORE2 для пожилых лиц 70–89 лет в популяции очень высокого риска
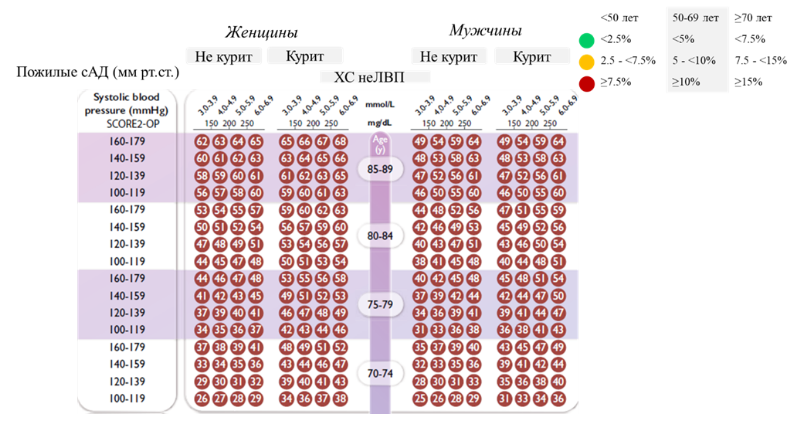
SCORE2 для лиц 40–69 лет в популяции очень высокого риска
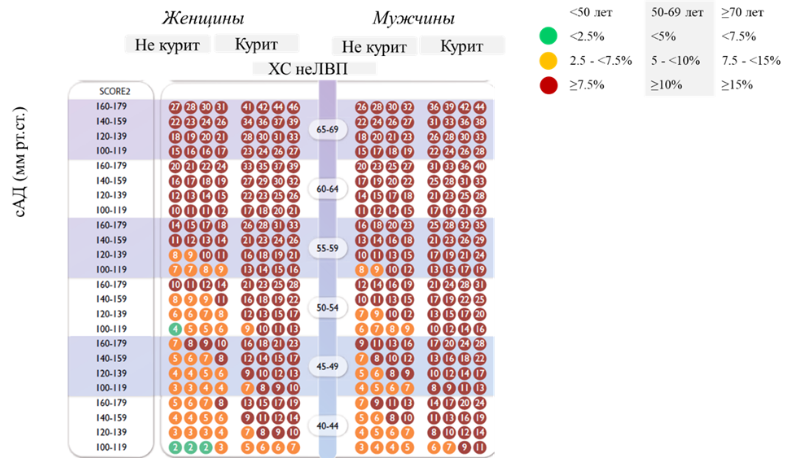
Пояснения: ХС не ЛВП=ОХС-ЛВП
Таблица Г3. Шкала глобальной оценки 10-летнего сердечно-сосудистого риска
Название на русском языке: Шкала глобальной оценки 10-летнего сердечно-сосудистого риска
Оригинальное название (если есть): нет
Источник (официальный сайт разработчиков, публикация с валидацией): escardio.org. SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe // European heart journal. 2021. Vol. 42. №. 25. P. 2439–2454.
Тип (подчеркнуть): шкала оценки
Назначение: оценка 10-летнего сердечно-сосудистого риска
Содержание (шаблон) и интерпретация:
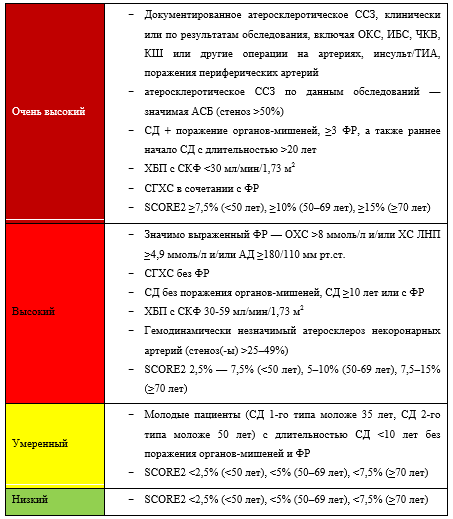
АГ — артериальная гипертензия, ХБП — хроническая болезнь почек, СКФ — скорость клубочковой фильтрации, ТИА — транзиторная ишемическая атака, CCЗ — сердечно-сосудистые заболевания, АСБ — атеросклеротическая бляшка, СГХС — семейная гиперхолестеринемия, ФР — фактор риска.
Прикреплённые файлы
Мобильное приложение “MedElement”

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение “MedElement”

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях “MedElement (МедЭлемент)”, “Lekar Pro”,
“Dariger Pro”, “Заболевания: справочник терапевта”, не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения “MedElement (МедЭлемент)”, “Lekar Pro”,
“Dariger Pro”, “Заболевания: справочник терапевта” являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Среди них есть полностью зависящие от человека и его образа жизни. Но на некоторые он повлиять не в силах.
- Несбалансированное питание с высоким содержанием жиров животного происхождения.
- Курение и употребление спиртных напитков.
- Сидячий образ жизни.
- Постоянное нервное перенапряжение.
- Болезни, связанные с нарушением метаболизма: сахарный диабет I и II типа, болезнь Кушинга.
- Болезни ЖКТ, связанные с нарушением всасывания и усвоения питательных веществ.
- Наследственные особенности.
В группе риска находятся люди старше 40 лет (преимущественно мужчины) и беременные женщины.
Проявления дислипидемии

Зависят от локализации холестериновых бляшек. Именно поэтому они могут выглядеть по-разному у людей с одинаковым диагнозом.
Основные симптомы нарушения липидного обмена:
- артериальная гипертония;
- стенокардия покоя и напряжения (давящие боли, жжение в области сердца в спокойном состоянии или при выполнении физических работ);
- внезапные головокружения, шум и гул в ушах, ухудшение памяти, резкое снижение концентрации внимания;
- боли в ногах при ходьбе;
- образование отложений жира в коже (ксантомы) или в области век (ксантелазмы).
Если у человека совпадает большинство пунктов, то с большой долей вероятности можно предположить, что у него липидный обмен нарушен.
Записаться к кардиологу
Диагностика и лечение
Для выявления нарушений используются некоторые специфические анализы. Они необходимы для выяснения, как нормализовать липидный обмен в организме:
- Биохимия крови, измеряющая показатели липидного обмена.
- Определение коэффициента атерогенности — определение соотношения липопротеинов высокой и низкой плотности.
- Ультразвуковое дуплексное сканирование сосудов цвете при помощи УЗ-аппарата. С его помощью врач определяет очаги плохого кровообращения и сравнивает кровоток в парных органах.
- Магнитно-резонансная ангиография — позволяет оценить анатомические и функциональные особенности кровотока.
- Компьютерная ангиография — применяется для визуализации крупных кровеносных сосудов и выявления их патологических изменений.
Не все анализы и методы обязательны. Они назначаются по усмотрению врача и отсутствии противопоказаний.
Специалисты, к которым следует обратиться с конечными результатами:
- кардиолог;
- невролог;
- сосудистый хирург..
После ознакомления с анализами пациента, сбора анамнеза и осмотра врач разрабатывает индивидуальную схему лечения. Терапия включает в себя лечение лекарственными препаратами (например, статинами). К таковым относятся диета с ограниченным содержанием жиров животного происхождения и посильные физические нагрузки.
Иногда требуется экстракорпоральная гемокоррекция, целью которой является очищение крови от патогенных элементов (излишков холестерина, продуктов метаболического распада, токсических веществ и антител).
Как методы экстракорпоральной гемокоррекции помогают при гиперхолестеринемии
Для коррекции нарушения липидного обмена используется ряд методик, таких как:
- криоаферез (H.E.L.P.-афереза);
- плазмофильтрация (каскадный плазмаферез);
- иммуносорбция.
Методики способствуют восстановлению адекватного уровня холестерина. После процедуры уменьшается объем холестериновых бляшек на стенках сосудов и снижается вязкость крови.

Также наблюдаются другие положительные эффекты:
- Увеличивается восприимчивость клеток к лекарствам.
- Работа внутренних органов становится эффективней за счет усиления кровоснабжения.
- Улучшаются память, концентрация внимания, настроение.
- Нормализуется сон.
- Снижается вероятность развития инсульта.
- Усиливается кровоснабжение миокарда, что уменьшает количество приступов стенокардии и риск развития инфаркта миокарда.
- Физические нагрузки легче переносятся.
- Улучшается циркуляция крови в нижних конечностях, позволяя трофическим язвам быстрее заживать. Уменьшает вероятность развития гангрены.
- Стимулируются процессы регенерации в коже за счет усиления кровообращения.
- Достигается видимый омолаживающий эффект.
Показания к экстракорпоральной гемокоррекции
Врачи назначают гемокоррекцию для лечения липидного обмена в следующих случаях:
- повышенное артериальное давление;
- высокий уровень общего холестерина;
- противопоказания к определенному веществу в лекарственных препаратах, снижающих холестерин;
- необходимость уменьшение дозировок из-за развития осложнений;
- недостаточная эффективность препаратов;
- повышенные индекс атерогенности > 3 и уровень липопротеина а (ЛП(а));
- унаследованные патологии, связанные с выраженным повышением количества ЛПНП в кровотоке и высоким риском раннего развития ИБС;
- наличие ИБС, цереброваскулярной болезни, облитерирующего атеросклероза;
- перенесенные инфаркт миокарда, острое нарушение мозгового кровообращения, оперативные вмешательства на сердечно-сосудистой системе.

При желании остановить развитие атеросклероза можно. Для этого надо записаться на приём к кардиологу в медицинский центр на Яузе. Специалисты проведут тщательный осмотр, назначат необходимые анализы, выставят диагноз и назначат адекватное лечение.
Помимо остановки развития болезни можно добиться омолаживающего эффекта, который напрямую связан с улучшением кровоснабжения всех внутренних органов и систем.
Записаться на консультацию
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
