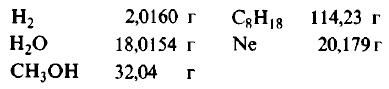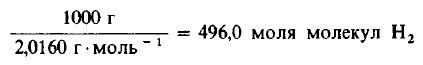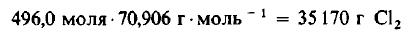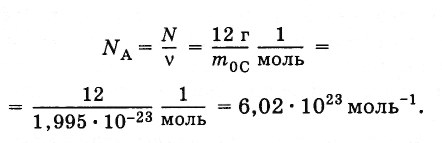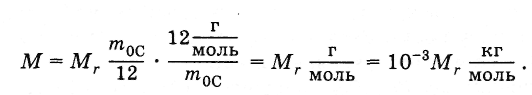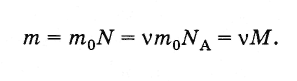В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·1023 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·1023 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·1023).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·1023 атомов. Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·1023 молекул. Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
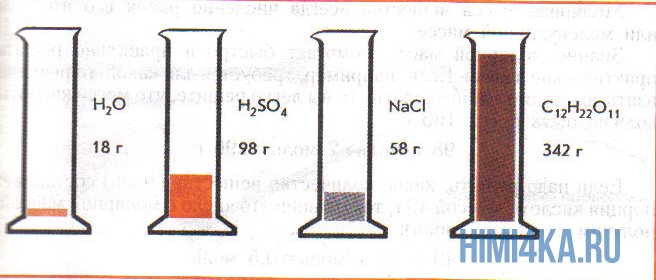
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·1023; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·1023 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·1023 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·1023 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·1023 × 0,25 = 1,505·1023 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·1023 молекул/моль, что равно 2,99·1026 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Число́ Авога́дро, конста́нта Авогадро, постоянная Авогадро — физическая величина, численно равная количеству специфицированных структурных единиц (атомов, молекул[1], ионов, электронов или любых других частиц) в 1 моле вещества[2]. Ранее определялось как количество атомов в 12 граммах (точно) чистого изотопа углерода-12. Обозначается обычно как NA[3], а иногда и L[4].
Постоянная Авогадро в Международной системе единиц СИ согласно изменениям определений основных единиц СИ есть целое число, точно равное
- NA ≡ 6,022 140 76⋅1023 моль−1.
Иногда в литературе проводят различие между постоянной Авогадро NA, имеющей размерность моль−1, и численно равным ей безразмерным целым числом Авогадро А[5][K 1].
Моль — количество вещества, которое содержит NA структурных элементов (то есть столько же, сколько атомов содержится в 12 г 12С, согласно старому определению), причём структурными элементами обычно являются атомы, молекулы, ионы и др. Масса 1 моля вещества (молярная масса), выраженная в граммах, численно равна его молекулярной массе, выраженной в атомных единицах массы.
Например:
- 1 моль натрия имеет массу 22,9898 г и содержит примерно 6,02⋅1023 атомов;
- 1 моль фторида кальция CaF2 имеет массу (40,08 + 2 · 18,998) = 78,076 г и содержит 6,02⋅1023 ионов кальция и 12,04⋅1023 ионов фтора;
- 1 моль тетрахлорида углерода CCl4 имеет массу (12,011 + 4 · 35,453) = 153,823 г и содержит 6,02⋅1023 молекул тетрахлорида углерода;
- и т. п.
В конце 2011 года на XXIV Генеральной конференции по мерам и весам единогласно принято предложение[7] определить моль в будущей версии Международной системы единиц (СИ) таким образом, чтобы избежать его привязки к определению килограмма. Предполагалось, что моль в 2018 году будет определён на основе числа Авогадро, которому будет приписано точное значение без погрешности, базирующееся на результатах измерений, рекомендованных CODATA. До 20 мая 2019 года число Авогадро являлось измеряемой величиной, не принимаемой по определению. В 2015 году из наиболее прецизионных измерений получено рекомендованное значение числа Авогадро NA = 6,022 140 82(11)⋅1023 моль−1, полученное в результате усреднения результатов различных измерений[8][9][10].
Закон Авогадро[править | править код]
На заре развития атомной теории (1811) А. Авогадро выдвинул гипотезу, согласно которой при одинаковых температуре и давлении в равных объёмах идеальных газов содержится одинаковое количество молекул. Позже было показано, что эта гипотеза есть необходимое следствие кинетической теории, и сейчас она известна как закон Авогадро. Его можно сформулировать так: один моль любого газа при одинаковых температуре и давлении занимает один и тот же объём, при нормальных условиях равный 22,41383 литра. Эта величина известна как молярный объём газа.
История измерения константы[править | править код]
Сам Авогадро не делал оценок числа молекул в заданном объёме, но понимал, что это очень большая величина. Первую попытку найти число молекул, занимающих данный объём, предпринял в 1865 году Йозеф Лошмидт. Из вычислений Лошмидта следовало, что для воздуха количество молекул на единицу объёма составляет 1,81⋅1018 см−3, что примерно в 15 раз меньше истинного значения. Через 8 лет Максвелл привёл гораздо более близкую к истине оценку «около 19 миллионов миллионов миллионов» молекул на кубический сантиметр, или 1,9⋅1019 см−3. По его оценке число Авогадро было приблизительно 
В действительности в 1 см³ идеального газа при нормальных условиях содержится около 2,68675⋅1019 молекул. Эта величина была названа числом (или постоянной) Лошмидта. С тех пор было разработано большое число независимых методов определения числа Авогадро. Превосходное совпадение полученных значений является убедительным свидетельством реального количества молекул.
В 1908 г. Перрен даёт приемлемую оценку 6,8·1023, вычисленную из параметров броуновского движения.
Современные оценки[править | править код]
Один из оптиков австралийского ACPO держит однокилограммовый монокристаллический шар из кремния для проекта International Avogadro Coordination.
|
|
Данные в этой статье приведены по состоянию на декабрь 2011 года. Вы можете помочь, обновив информацию в статье. |
Официально принятое в 2010 году значение числа Авогадро было измерено при использовании двух сфер, изготовленных из монокристалла кремния-28, выращенного методом Чохральского. Сферы были выточены в Институте кристаллографии имени Лейбница и отполированы в австралийском Центре высокоточной оптики настолько гладко, что при диаметре около 93,75 мм высоты выступов на их поверхности не превышали 98 нм; радиальные координаты поверхности измерены методом оптической интерферометрии с погрешностью 0,3 нм (порядка толщины одного атомного слоя)[11]. Для их производства был использован высокочистый кремний-28, выделенный в нижегородском Институте химии высокочистых веществ РАН из высокообогащённого по кремнию-28 тетрафторида кремния, полученного в Центральном конструкторском бюро машиностроения в Санкт-Петербурге.
Располагая такими практически идеальными объектами, можно с высокой точностью подсчитать число атомов кремния в шаре и тем самым определить число Авогадро. Согласно полученным результатам, оно равно 6,02214084(18)·1023 моль−1[12].
Однако в январе 2011 года были опубликованы результаты новых измерений, считающиеся более точными[13]: NA = 6,02214078(18)⋅1023 моль−1.
На 24-й Генеральной конференции по мерам и весам 17—21 октября 2011 года была единогласно принята резолюция[7], в которой, в частности, предложено в будущей ревизии СИ переопределить моль таким образом, чтобы число Авогадро было равным точно 6,02214X⋅1023 моль−1, где Х заменяет одну или более значащих цифр, которые будут определены в окончательном релизе на основании наиболее точных рекомендаций CODATA[14]. В этой же резолюции предложено таким же образом определить как точные значения постоянную Планка, элементарный заряд, постоянную Больцмана и максимальную световую эффективность монохроматического излучения для дневного зрения.
Значение числа Авогадро, рекомендованное CODATA в 2010 году, составляло:
- NA = 6,022 141 29(27)⋅1023 моль−1.
Значение числа Авогадро, рекомендованное CODATA в 2014 году, составляло[15]:
- NA = 6,022 140 857(74)⋅1023 моль−1
Связь между константами[править | править код]
См. также[править | править код]
- Универсальная газовая постоянная
- Постоянная Больцмана
- Уравнение состояния идеального газа
- Молярный объём газа
Комментарии[править | править код]
- ↑ Число Авогадро A есть кратная единица измерения очень больших целых безразмерных величин, численно равная постоянной Авогадро, то есть A в NA раз больше исходной величины — 1-й штуки. Число Авогадро используют для количественного описания систем, содержащих настолько большое число любых объектов (обычно частиц и групп частиц вещества), что указывать количество этих объектов в штуках становится малоудобно и малонаглядно. Например, 1 А теннисных мячей покроют поверхность планеты Земля слоем толщиной 100 км; 1 А долларовых банкнот закроют все материки Земли плотным двухкилометровым слоем; в пустыне Сахара содержится немногим менее 3 А песчинок[6].
Примечания[править | править код]
- ↑ Ранее выводилось как количество молекул в грамм-молекуле или атомов в грамм-атоме.
- ↑ Авогадро постоянная // Физическая энциклопедия / Гл. ред. А. М. Прохоров. — М.: Советская энциклопедия, 1988. — Т. 1. — С. 11. — 704 с. — 100 000 экз.
- ↑ в отличие от N, обозначающее количество частиц (англ. Particle number)
- ↑ http://www.iupac.org/publications/books/gbook/green_book_2ed.pdf
- ↑ Пресс И. А., Основы общей химии для самостоятельного изучения, 2012, с. 22—23.
- ↑ Пресс И. А., Основы общей химии для самостоятельного изучения, 2012, с. 23.
- ↑ 1 2 On the possible future revision of the International System of Units, the SI. Resolution 1 of the 24th meeting of the CGPM (2011).
- ↑ Точная оценка числа Авогадро поможет дать новое определение килограмма : Наука: Наука и техника: Lenta.ru
- ↑ The Correlation of the NA Measurements by Counting 28Si Atoms
- ↑ More Precise Estimate of Avogadro’s Number to Help Redefine Kilogram | American Institute of Physics. Дата обращения: 15 июля 2015. Архивировано из оригинала 16 июля 2015 года.
- ↑ Алексей Понятов. Последний сдался килограмм // Наука и жизнь. — 2019. — № 3.
- ↑ Физики уточнили число Авогадро для будущего эталона килограмма. РИА Новости (20 октября 2010). Дата обращения: 20 октября 2010. Архивировано из оригинала 23 октября 2010 года.
- ↑ B. Andreas et al., Determination of the Avogadro Constant by Counting the Atoms in a 28Si Crystal, Phys. Rev. Lett. 106, 2011, 030801
- ↑ Agreement to tie kilogram and friends to fundamentals — physics-math — 25 October 2011 — New Scientist
- ↑ CODATA Value: Avogadro constant
- ↑ Больцмана постоянная, 1988.
- ↑ Фарадея постоянная, 1998.
Литература[править | править код]
- Больцмана постоянная // Физическая энциклопедия. — Советская Энциклопедия, 1988. — Т. 1. — С. 222.
- Мейлихов Е. З. Число Авогадро. Как увидеть атом. — Долгопрудный, Московская обл.: Интеллект, 2017. — 86 с. — (Истоки современной физики). — 500 экз. — ISBN 978-5-91559-233-8.
- Пресс И. А. Основы общей химии для самостоятельного изучения. — 2-е изд., перераб. — СПб.: Лань, 2012. — 496 с. — ISBN 978-5-8114-1203-7.
- Фарадея постоянная // Физическая энциклопедия. — Советская Энциклопедия, 1998. — Т. 5. — С. 275.
- Число Авогадро // Большая советская энциклопедия
И молекулярная физика, и термодинамика изучают свойства вещества, но при этом пользуются разными методами.
Молекулярная физика рассматривает свойства вещества с точки зрения его внутренней структуры (движение молекул вещества, их взаимодействие).
Термодинамика не рассматривает внутреннюю структуру вещества, а интересуется его энергией, передачей энергии. Так, она рассматривает как за счёт тепла, полученного при сгорании топлива, можно получить работу (работа тепловой машины). О термодинамике будем говорить позднее, а пока речь пойдёт о молекулярной физике, которую ещё называют молекулярно-кинетической теорией или статистической физикой.
Молекулярная физика говорит о том, что любое вещество состоит из молекул. Металлы, имеющие кристаллическое строение,
состоят из атомов, но атомы можно считать одноатомными молекулами. Молекулы вещества находятся в непрерывном хаотическом движении (обладают кинетической энергией) и взаимодействуют друг с другом – одновременно притягиваются и отталкиваются (обладают потенциальной энергией взаимодействия).
На рисунке показан график зависимости силы взаимодействия молекул от расстояния между ними. Пунктирные линии относятся к силам притяжения и отталкивания, сплошная линия даёт результирующую силу взаимодействия молекул. При
эта сила равна нулю, что соответствует наиболее устойчивому состоянию молекул (наименьшему значению потенциальной энергии их взаимодействия).
Агрегатные состояния вещества определяются соотношением потенциальной и кинетической энергий молекул.
В газах молекулы находятся далеко друг от друга, их потенциальная энергия мала, а кинетическая велика., то есть
В кристаллических телах молекулы (атомы) располагаются вплотную друг к другу, их потенциальная энергия взаимодействия очень велика. Они обладают и кинетической энергией, совершая колебания около своих положений равновесия, но для них
В жидкостях, плотность которых меньше плотности твёрдых тел, молекулы и колеблются около положений равновесия, и время от времени совершают и поступательное движение. Кинетическая и потенциальная энергии молекул жидкости соизмеримы между собой
Так как молекулярная физика говорит о молекулах, то надо ввести понятия, связанные с молекулой – это масса молекулы, концентрация молекул и другие.
Один кг (или грамм) очень крупные для молекулы единицы массы, поэтому в молекулярной физике за единичную массу приняли 1/12 часть массы атома углерода (раньше единичную массу связывали с атомом водорода, кислорода):
Количество единичных масс в атоме назвали относительной атомной массой или просто атомной массой А, а количество единичных масс в молекуле – молекулярной массой М. Тогда молекула углерода содержит 12 единичных масс, так как
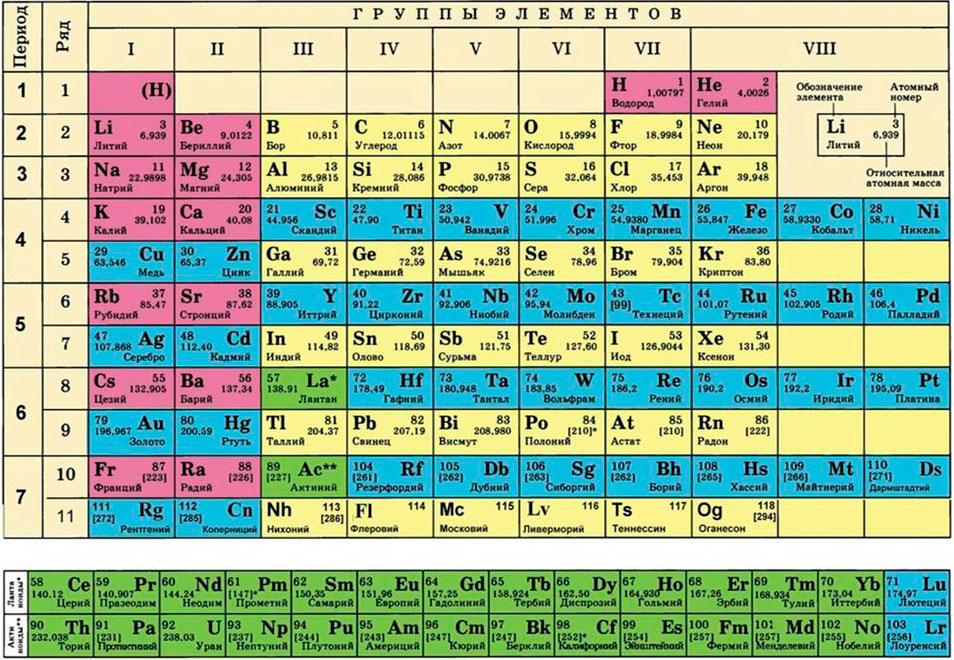
Для водорода А = 1, для кислорода А = 16 и так далее (см. таблицу Менделеева).
Молекулярная масса М складывается из атомных масс А. Так,
Атомная и молекулярная массы – безразмерные величины.
Единицей количества вещества в молекулярной физике является моль. Моль – это количество вещества, в котором содержится число молекул (атомов), равное числу атомов в 0,012 кг изотопа углерода.
Таким образом, молярная масса углерода равна 0,012 кг/моль.
Масса моля водорода (молярная масса водорода):
Молярная масса воды:
то есть если взять 0,018 кг воды, то это будет моль воды.
Моль любого вещества содержит одинаковое количество молекул, названное числом Авогадро
Объём моля для твёрдых и жидких тел находится путём деления молярной массы вещества на его плотность:
Объём моля любого газа при нормальных условиях равен
Задачи
Подписывайтесь на канал и сообщите о нём своим друзьям, одноклассникам. Здесь непременно найдёте много полезного для себя.
Посмотрите занятия 32 и 33.
Ссылки на другие занятия даны в Занятии 1.
Обновлено: 23.05.2023
В химических процессах участвуют мельчайшие частицы – молекулы, атомы, ионы, электроны. Число таких частиц даже в малой порции вещества очень велико. Поэтому, чтобы избежать математических операций с большими числами, для характеристики количества вещества, участвующего в химической реакции, используется специальная единица – моль .
Моль – это такое количество вещества, в котором содержится определенное число частиц (молекул, атомов, ионов), равное постоянной Авогадро
Постоянная Авогадро N A определяется как число атомов, содержащееся в 12 г изотопа 12 С:
Таким образом, 1 моль любого вещества содержит 6,02 • 10 23 частиц этого вещества.
1 моль железа содержит 6,02 • 10 23 атомов Fe.
1 моль серы содержит 6,02 • 10 23 атомов S.
2 моль серы содержит 12,04 • 10 23 атомов S.
0,5 моль серы содержит 3,01 • 10 23 атомов S.
Исходя из этого, любое количество вещества можно выразить определенным числом молей ν ( ню ). Например, в образце вещества содержится 12,04 • 10 23 молекул. Следовательно, количество вещества в этом образце составляет:
где N – число частиц данного вещества;
N а – число частиц, которое содержит 1 моль вещества (постоянная Авогадро).
Молярная масса вещества (M) – масса, которую имеет 1 моль данного вещества.
Эта величина, равная отношению массы m вещества к количеству вещества ν , имеет размерность кг/моль или г/моль . Молярная масса, выраженная в г/моль, численно равна относительной относительной молекулярной массе M r (для веществ атомного строения – относительной атомной массе A r ).
Например, молярная масса метана CH 4 определяется следующим образом:
M(CH 4 )=16 г/моль, т.е. 16 г CH 4 содержат 6,02 • 10 23 молекул.
Молярную массу вещества можно вычислить, если известны его масса m и количество (число молей) ν , по формуле:
Моль
Моль — это количество вещества из 6,02214076⋅10 23 атомов или молекул. Оно не имеет физического смысла и изначально было привязано к массе определенного количества (12 граммов) углерода-12, но позже переопределено, как и многие другие единицы системы СИ. В школьных расчетах количество структурных единиц в моле, которое также называется постоянной Авогадро, обычно округляют до 6,022⋅10 23 и обозначают NA.
Примеры
В стакане содержится 2 моль воды. Сколько молекул воды находится в стакане?
N = ν⋅ NA =2 ⋅ 6,022⋅10 23 = 12,044⋅10 23 молекул воды.
Также можно решить обратную задачу. Сколько молей вещества составляют 24,088⋅10 23 молекул воды?
ν⋅ = N / NA = 24,088⋅10 23 / 6,022⋅10 23 = 4 моля.
Моль и молярная масса: простое объяснение с примерами
Молярная масса
Итак, молярная масса равна массе порции вещества m к количеству молекул ν в его порции:
Вооружившись этим знанием, мы можем переводить граммы в число молекул и наоборот. При этом следует учесть, что молярная масса численно идентична молекулярной массе (то есть массе молекулы), выраженной в атомных единицах массы, и относительной молекулярной массе.
Пример
Найдем массу 5 моль воды.
Чтобы решить эту задачу, обратимся к формуле молярной массы и выразим из нее массу:
В этой формуле мы знаем количество вещества ν = 5 моль, а молярную массу сложной молекулы нужно определить, как сумму молярных масс составляющих ее химических элементов:
Моль и молярная масса: простое объяснение с примерами
Где взять молярные массы кислорода и водорода (в соединение входит два атома водорода, поэтому его молярную массу умножаем на 2)?
M (H2O) = 2 ⋅M (H) + M (O) = 2 ⋅ 1 + 16 = 18 г/моль.
То есть масса 1 моль воды составляет 18 граммов. Теперь можем подсчитать массу 5 моль воды:
m = М ⋅ ν = 18 ⋅ 5 = 90 г.
Аналогичным образом мы можем подсчитать количество вещества, которое содержится в определенном образце заданной массы. Для примера возьмем оксид алюминия Al2O3 и узнаем, сколько моль в 400 граммах этого вещества. Для этого выразим количество вещества через молярную массу и подставим исходные данные:
ν = m / М = 400 / (2 ⋅ М (Al) + 3 ⋅ (O)) = 400 / (2 ⋅ 75 + 3 ⋅ 16) = 400 / (150 + 48) = 400 / 198 ≈ 2,02 моль.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·10 23 × 0,25 = 1,505·10 23 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
На предыдущих двух вступительных уроках в курс молекулярной физики речь шла об основных положениях МКТ. Сейчас же мы подробнее остановимся на первом положении (все тела состоят из маленьких частиц), а именно поговорим о численных оценках некого тела, некой порции вещества. Введём понятие массы молекулы, количества вещества, молярной массы и относительной атомной и молекулярной массы.
Читайте также:
- Детский сад проект архикад
- Связь педагогики с другими науками взаимосвязь педагогической науки и практики кратко
- Как устроены телескопы рефрактор и рефлектор кратко
- Что такое азот в биологии 6 класс определение кратко
- В чем состоит особенность энергии информации и социальных объектов как предметов труда кратко
Количество вещества
Чем больше атомов
или молекул в макроскопическом теле,
тем, очевидно, больше вещества содержится
в нем. Число молекул в макроскопических
телах огромно. Поэтому удобно указывать
не абсолютное число атомов, а относительное.
Принято
сравнивать число молекул или атомов в
данном теле с числом атомов, содержащихся
в углероде массой 12 г. Относительное
число атомов или молекул в теле
характеризуется особой физической
величиной, называемой количеством
вещества.
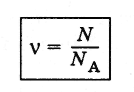
Количеством
вещества v
называют отношение числа молекул N
в
данном теле к числу атомов NA
в
12 г углерода*.
(2.2.2)
* Если вещество
состоит из отдельных атомов, не
объединенных в молекулы, то здесь и в
дальнейшем под числом молекул надо
подразумевать число атомов.
Зная
количество вещества v
и число NA,
мы
тем самым знаем число молекул N
в
веществе. Количество вещества выражают
в молях.
Моль
— это количество вещества, содержащего
столько же молекул, сколько атомов
содержится в углероде массой 12 г.
Если
количество вещества равно, например,
2,5 моль, то это означает, что число молекул
в теле в 2,5 раза превышает число атомов
в 12 г углерода, т. е. равно 2,5
NA.
Постоянная Авогадро
Число
молекул или атомов в моле вещества
называют постоянной Авогадро. Это
название дано в честь итальянского
ученого XIX
в. А. Авогадро**.
** А. Авогадро
(1776—1856) — итальянский физик и химик;
автор четырехтомного труда, который
был первым руководством по молекулярной
физике.
Согласно определению
моля постоянная Авогадро одинакова для
всех веществ. Она равна, в частности,
числу атомов в моле углерода, т. е. в 12 г
углерода.
Для
вычисления постоянной Авогадро надо
найти массу одного атома углерода (или
любого другого атома). Грубую оценку
массы можно сделать так, как это было
выполнено для массы молекулы воды.
Наиболее точные методы определения
массы основаны на отклонении пучков
ионов электромагнитным полем. Измерения
дают для массы атома углерода т0С
=
1,995·10-23
г. Отсюда постоянная Авогадро равна
(2.2.3)
Наименование
моль-1
указывает, что NA
—
число атомов любого вещества, взятого
в количестве одного моля. Если количество
вещества v
= 2,5 моль, то число молекул в теле N
= vNA
= 1,5·1024.
Существует много
других методов определения постоянной
Авогадро, не связанных с нахождением
масс атомов. Все они приводят к одним и
тем же результатам. Постоянная Авогадро
играет важнейшую роль во всей молекулярной
физике и является универсальной
постоянной.
Огромная величина
постоянной Авогадро показывает, насколько
малы микроскопические масштабы по
сравнению с макроскопическими. Тело,
обладающее количеством вещества 1 моль,
имеет привычные для нас макроскопические
размеры.
Молярная масса
Наряду
с относительной молекулярной массой
Мr,
в
физике и химии широко используется
понятие молярной массы М.
Молярной
массой называют массу
вещества,
взятого в количестве одного моля.
Согласно этому
определению молярная масса равна
произведению массы молекулы на постоянную
Авогадро:

(2.2.4)
Молярная
масса простым образом связана с
относительной молекулярной массой.
Подставив в формулу (2.2.4) выражения т0
из
(2.2.2) и NA
из
(2.2.3), получим:
(2.2.5)
Например,
молярная масса воды Н2О
равна 18 г/моль, или 0,18 кг/моль, так как
относительная молекулярная масса воды
приближенно равна 18.
Масса
m
произвольного
количества вещества v
и молярная масса М
связаны
соотношением:
(2.2.6)
Так,
масса 3 моль воды равна: m
= 3
моль·0,018 кг/моль = 0,054 кг.
Используя
формулы (2.2.6) и (2.2.2), можно получить
формулу для числа молекул в теле в
зависимости от массы тела m
и
молярной массы М:
(2.2.7)
Нужно
запомнить значение постоянной Авогадро:
достаточно знать порядок величины 1023.
Столько
молекул содержится в
12 г углерода,
в
18 г воды
и т. д. Формулы (2.2.1),
(2.2.2) и
(2.2.4)
дают
определения новым физическим величинам:
относительной молекулярной массе,
количеству вещества и молярной массе.
Вывести их нельзя, их надо просто
запомнить. Остальные формулы можно
вывести, и запоминать их необязательно.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #