Загрузить PDF
Загрузить PDF
В атомах одного и того же элемента число протонов неизменно, в то время как число нейтронов может меняться. Зная, сколько нейтронов содержится в конкретном атоме, вы сможете определить, является ли он обычным атомом или изотопом, который будет иметь меньшее или большее количество нейтронов.[1]
Определить количество нейтронов в атоме — довольно просто. Все, что вам нужно сделать для расчета количества нейтронов в атоме или изотопе, — это следовать нашим инструкциям и держать под рукой периодическую таблицу.
-
1
Найдите элемент в периодической таблице. Для примера мы будем рассматривать осмий (Os), который находится в шестом периоде (шестой ряд сверху).
-
2
Найдите атомный номер элемента. Это, как правило, наиболее заметное число в ячейке элемента и обычно находится над его символом (в варианте периодической системы, которую мы используем в нашем примере, других номеров и нет). Атомный номер — это количество протонов в одном атоме этого элемента. Для осмия это число 76, то есть в одном атоме осмия содержится 76 протонов.
- Число протонов неизменно, именно оно и делает элемент элементом.
-
3
Найдите атомную массу элемента. Это число обычно находится под символом элемента. Обратите внимание, что в варианте периодической системы в нашем примере атомная масса не приведена (это не всегда так; во многих вариантах периодической системы атомная масса указана). Атомная масса осмия — 190,23.
-
4
Округлите атомную массу до ближайшего целого числа. В нашем примере 190,23 округляется до 190.
- Атомная масса — среднее число изотопов конкретного элемента, обычно она не выражается целым числом.
-
5
Вычтите атомный номер из атомной массы. Поскольку абсолютная часть атомной массы приходится на протоны и нейтроны, вычитание числа протонов (то есть атомного номера, который равен числу протонов) из атомной массы дает число нейтронов в атоме. Цифры после десятичной запятой относятся к очень малой массе электронов в атоме. В нашем примере: 190 (атомный вес) – 76 (число протонов) = 114 (число нейтронов).
-
6
Запомните формулу. Чтобы найти число нейтронов в будущем, просто используйте эту формулу:
-
N = M – n
- N = количество нейтронов
- M = атомная масса
- n = атомный номер
Реклама
-
N = M – n
-
1
Найдите элемент в периодической таблице. В качестве примера мы будем рассматривать изотоп углерода 14С. Поскольку неизотопный углерод 14С есть просто углерод С, найдите углерод в периодической таблице (второй период или второй ряд сверху).
-
2
Найдите атомный номер элемента. Это, как правило, наиболее заметное число в ячейке элемента и обычно находится над его символом (в варианте периодической системы, которую мы используем в нашем примере, других номеров и нет). Атомный номер – это количество протонов в одном атоме этого элемента. Углерод находится под номером 6, то есть один атом углерода имеет шесть протонов.
-
3
Найдите атомную массу. В случае изотопов делать это очень просто, так как они названы в соответствии с их атомной массой. В нашем случае у углерода 14С атомная масса равна 14. Теперь мы знаем атомную массу изотопа; последующий процесс расчета такой же, как и для определения числа нейтронов в атомах (не изотопах).
-
4
Вычтите атомный номер из атомной массы. Поскольку абсолютная часть атомной массы приходится на протоны и нейтроны, вычитание числа протонов (то есть атомного номера, который равен числу протонов) из атомной массы дает число нейтронов в атоме. В нашем примере: 14 (атомная масса) – 6 (число протонов) = 8 (число нейтронов).
-
5
Запомните формулу. Чтобы найти число нейтронов в будущем, просто используйте эту формулу:
-
N = M – n
- N = количество нейтронов
- M = атомная масса
- n = атомный номер
Реклама
-
N = M – n
Советы
- Протоны и нейтроны составляют практически абсолютную массу элементов, в то время как электроны и прочие частицы составляют крайне незначительную массу (эта масса стремится к нулю). Так как один протон имеет примерно ту же массу, что и один нейтрон, а атомное число представляет собой число протонов, то можно просто вычесть число протонов от общей массы.
- Осмий — металл в твердом состоянии при комнатной температуре, получил свое название от греческого слова «osme» — запах.
- Если вы не уверены, что значит какое-то число в периодической таблице, запомните: таблица, как правило, строится вокруг атомного номера (то есть числа протонов), который начинается с 1 (водород) и растет на одну единицу слева направо, заканчиваясь на 118 (Оганесон). Это потому, что число протонов в атоме определяет сам элемент и такое число — наиболее легкий способ систематизации элементов (например, атом с 2 протонами — всегда гелий, так же, как и атом с 79 протонами — всегда золото).
Реклама
Об этой статье
Эту страницу просматривали 193 303 раза.
Была ли эта статья полезной?
Продолжаем наш разговор, посвящённый строению атома. В предыдущей серии мы узнали, как находить число протонов и электронов в атоме. Оно равно, как мы помним, порядковому номеру химического элемента в таблице Менделеева.
Таким образом, чтобы полностью определить состав атома, нам сталось ответить на вопрос, сколько в составе того или иного атома нейтронов?
Для этого вспомним, что частицами, входящими в состав атома и обладающими хоть сколько-нибудь значительной массой, являются протоны и нейтроны. Их масса условно принята равна одному. Это значит, что:
масса всего атома, так называемая атомная масса, есть сумма входящих в его состав протонов и нейтронов.
Число протонов мы знаем из таблицы Менделеева, оно равно порядковому номеру химического элемента, которому принадлежит атом. Там же, в таблице Менделеева, мы найдём и атомную массу! Так атомная масса серы (S) равна 32.
Итак, если нам известна атомная масса (её мы легко найдём в таблице Менделеева), если нам так же известно число протонов в атоме (оно равно порядковому номеру химического элемента в таблице), если атомная масса – это сумма протонов и нейтронов, можем ли мы найти число нейтронов? Ну, конечно, число нейтронов равно разнице между атомной массой и порядковым номером элемента:
То есть, число нейтронов в атоме кальция
будет: N = 40 (атомная масса) – 20 (порядковый номер) = 20.
Таким образом вторая серия нашего последовательного изложения химии подошла к концу. Подписывайтесь на канал. В следующей серии мы узнаем, почему атомная масса в таблице Менделеева имеет дробное значение.
Как определить число нейтронов?
Домашние заданияЗадания по химииНейтроны
Анонимный вопрос
6 марта 2019 · 286,2 K
Популяризатор науки, знаток химии и биологии, ценитель искусства. Меланхолик. Изучаю… · 10 нояб 2020
Число нейтронов определяется по формуле
N = A – Z, где N — кол-во нейтронов, A — атомная масса элемента, Z — кол-во протонов. Нейтроны и протоны составляют ядро, а масса электронов (e) не учитывается из-за ничтожного значения. Так, мы должны выяснить массу нейтронов, а она равна их количеству, так как масса частиц ядра равна 1.
Важно: масса не имеет единиц измерения.
Протоны и нейтроны имеют постоянную массу, но количество нейтронов может изменяться в зависимости от изотопа. В таких случаях меняется масса атома. Для атомов водорода такие изменения наиболее значимы, поэтому разделяется три изотопа: H, D, T — протий, дейтерий и тритий.30,6 K
> Важно: масса не имеет единиц измерения.
Это неверно. Масса вполне измеряется в граммах или их производными, но в… Читать дальше
Комментировать ответ…Комментировать…
Студент биологического факультета, активист молодежной общественной организации · 27 сент 2021
Число нейтронов = массовое число (атомная масса) – число протонов (число электронов). В таблице Менделеева число протонов определяется по заряда ядра, т.е. по номеру элемента
3,1 K
Комментировать ответ…Комментировать…
Как известно, атом любого химического элемента состоит из положительно заряженного ядра и отрицательно заряженных электронов. Ядро атома в свою очередь состоит из положительно заряженных протонов и имеющих нулевой заряд нейтронов.
Как определить количество электронов, протонов и нейтронов в атоме химического элемента? Для этого посмотрим в Периодическую систему… Читать далее
133,9 K
А откуда электроны в ядре атома?
Комментировать ответ…Комментировать…
рядом с символом элемента указывается не атомная масса изотопа а средняя масса изотопов по элементу. для никеля например указано масса 58,693, что вы подразумеваете как 59, но нет стабильного природного изотопа никеля-59. есть только 58,60,61,62,64. а 59 это стабильный изотоп кобальта! то же самое наблюдается с Cu,Zn,Ga,Se и другими элементами.
крч надо иметь под… Читать далее
3,8 K
Нужно вычесть число протонов из относительной атомной массы
Комментировать ответ…Комментировать…
Число нейтронов в атоме элемента условно обозначают латинской Z.
Z(Э) = Ar(Э) – p(Э), где p – число протонов (p=порядковому номеру элемента в системе Менделеева), Ar – относительная атомная масса элемента.
Например:
Z(О) = 16-8 = 8, значит атом кислорода содержит 8 нейтронов;
Z(S) = 32-16 = 16, атом серы содержит 16 нейтронов;
Z(V) = 51-23 = 28, атом ванадия содержит… Читать далее
1,5 K
Комментировать ответ…Комментировать…
ИП, Индивидуальный предприниматель · 27 апр
Верно, формула Z(Э) = Ar(Э) – p(Э) позволяет определить количество нейтронов в атоме элемента. Для этого необходимо вычесть из относительной атомной массы элемента (Ar) количество протонов (p), которое равно порядковому номеру элемента в системе Менделеева. Полученное значение будет равно количеству нейтронов в ядре атома данного элемента.
Например, для атома кислорода… Читать далее
Комментировать ответ…Комментировать…
Мы знаем, что масса атома определяется массой ядра. Ядро состоит из протонов и нейтронов, относительные массы которых равны (1). Масса ядра равна сумме масс протонов и нейтронов. Число протонов определяем по порядковому номеру элемента. Значит, число нейтронов в ядре можно найти, если от относительной атомной массы отнять порядковый номер.
Пример:
фтор — элемент № (9). Его относительная атомная масса равна (19).
В ядре атома фтора — (9) протонов и (19) (–) (9) (=) (10) нейтронов.
Рубидий — элемент № (37). Его относительная атомная масса равна (85).
В ядре атома рубидия — (37) протонов и (85) (–) (37) (=) (48) нейтронов.
Нуклиды
Вид атомов с определённым числом протонов и нейтронов в ядре называется нуклидом.
Нуклид обозначается следующим образом: внизу слева записывается число протонов (Z) (порядковый номер), вверху слева указывается массовое число (A) (сумма чисел протонов и нейтронов) —
RZA
, например:
C612
,
Se3479
.
Для обозначения нуклидов используют и другие способы записи:
углерод — (12),
C
— (12),
C12
;
селен — (79),
Se
— (79),
Se79
.
Изотопы
Атомы одного и того же химического элемента могут иметь разные массы. Существуют атомы водорода с массами (1), (2) и (3), атомы хлора с массами (35) и (37) и т. д.
Разновидности атомов одного химического элемента, имеющие разные атомные массы, называют изотопами.
С учётом знаний о строении ядра это определение можно сформулировать по-другому.
Изотопы — разновидности атомов с одинаковым числом протонов в ядре (зарядом ядра), но разным числом нейтронов.
Значит, изотопы отличаются только числом нейтронов.
Рис. (1). Изотопы водорода
Протоны определяют свойства атома, то есть придают ему индивидуальность. А нейтроны не влияют на свойства атома, а отражаются на его массе. Поэтому все изотопы одного и того же элемента химически неотличимы.
Химический элемент — это вид атомов с определённым зарядом ядра.
Относительная атомная масса элемента
Большинство химических элементов существуют в виде смеси изотопов. Приведённая в Периодической таблице относительная атомная масса элемента — это средняя величина атомных масс всех его изотопов.
Пример:
определим относительную атомную массу хлора. (25) % его атомов — это атомы с массой (37), а (75) % — с массой (35). Найдём среднее значение:
·25+35
·75)100
= 35,5.
Источники:
Рис. 1. Изотопы водорода © ЯКласс
Химический элемент
Химический элемент – совокупность атомов с одним и тем же зарядом ядра, числом протонов в ядре и электронов
в электронной оболочке. Закономерную связь химических элементов отражает периодическая таблица Д.И. Менделеева.
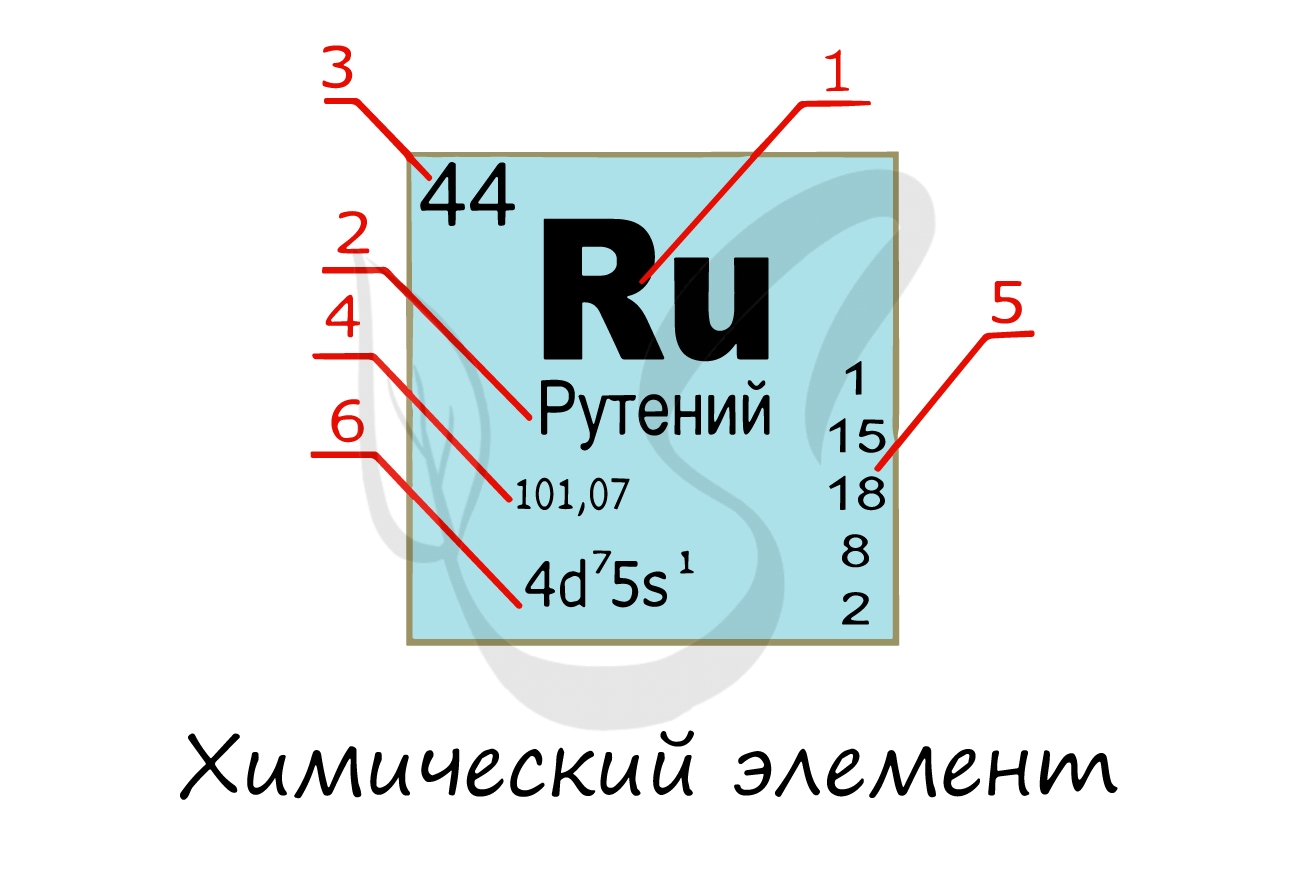
Изучая подобную карточку химического элемента, можно узнать о нем многое:
- Обозначение химического элемента
- Русское наименование
- Порядковый номер = заряд атома = число электронов = число протонов
- Атомная масса
- Распределение электронов по энергетическим уровням
- Электронная конфигурация внешнего уровня
Надо заметить, что на экзамене часто из карточки элемента скрывают распределение электронов и конфигурацию внешнего
уровня. Тем не менее, если вы успешно освоили предыдущую тему, то для вас не составит труда написать электронную
конфигурацию атома зная его порядковый номер в таблице Д.И. Менделеева (номер уж точно не тронут!))
Протоны, нейтроны и электроны
Вы уже знаете, что порядковый номер элемента в периодической таблице Д.И. Менделеева равен числу протонов, а число протонов
равно числу электронов.
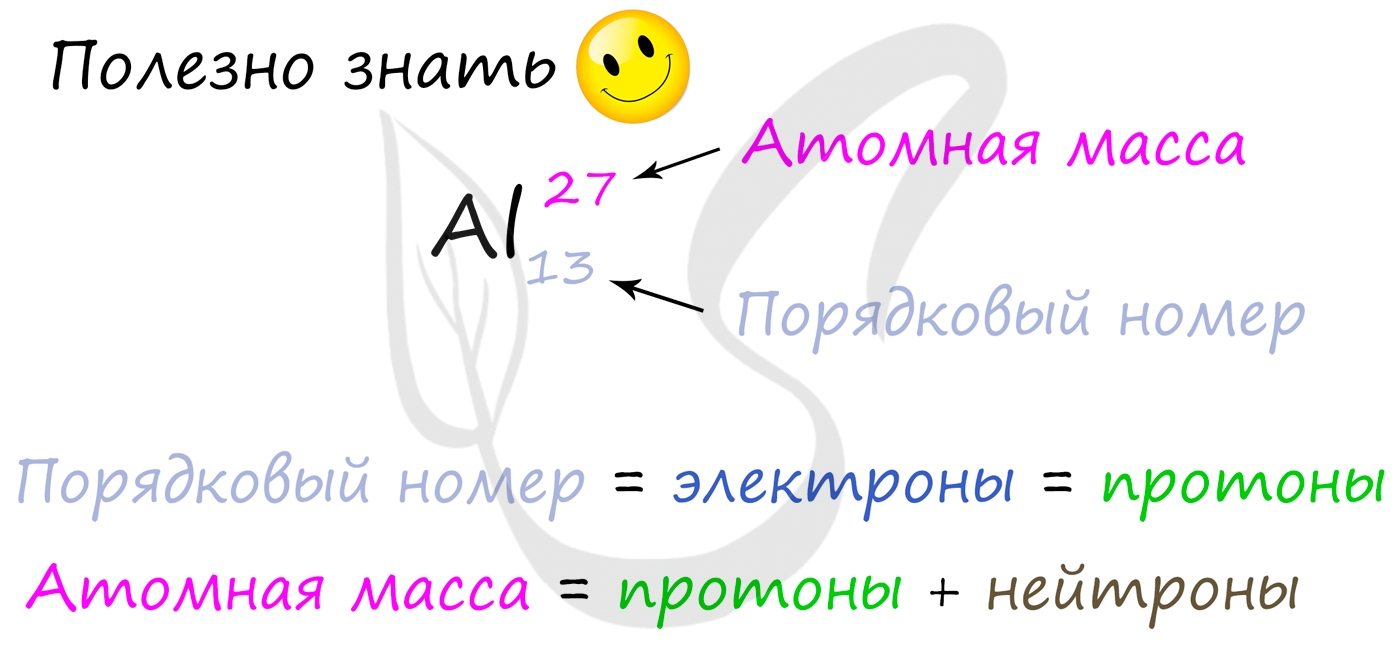
Для того чтобы найти число нейтронов в атоме алюминия, необходимо вычесть из атомной массы число протонов:
27 – 13 = 14
Получается, что в атоме алюминия 14 нейтронов. Посчитайте число нейтронов, электронов и протонов самостоятельно для атомов бериллия,
кислорода, меди. Решение вы найдете ниже.

Если вы поняли суть и научились считать протоны, нейтроны и электроны, самое время приступать к следующей теме.
Изотопы
Изотопы (греч. isos – одинаковый + topos – место) – общее название разновидностей одного и того же химического элемента,
имеющих одинаковый заряд ядра (число протонов), но разное число нейтронов.
Вероятно, вы не задумывались, но вся таблица Д.И. Менделеева и представленные в ней химические элементы – это самые распространенные
на земле изотопы.
Лучше всего объяснить, что такое изотопы наглядным примером. Широко известны три изотопа водорода: протий, дейтерий и тритий.
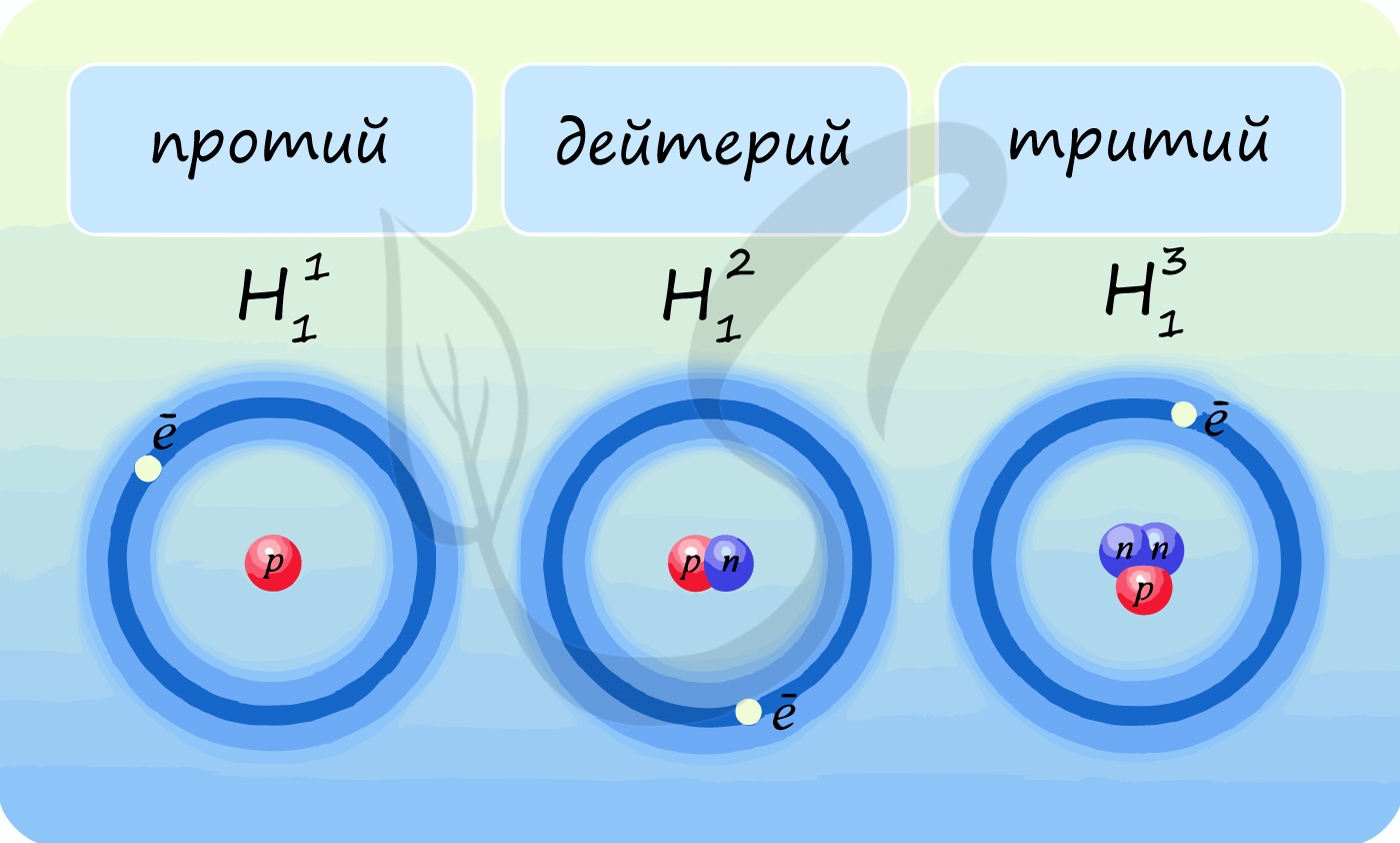
В таблице Д.И. Менделеева представлен самый распространенный из трех – протий. Он содержит 1 протон и 1 электрон, нейтроны отсутствуют. У
дейтерия 1 протон, 1 нейтрон и 1 электрон. У трития 1 протон, 2 нейтрона, 1 электрон.
Теперь очевидно, что изотопы – атомы одного и того же химического элемента, различающиеся числом нейтронов.
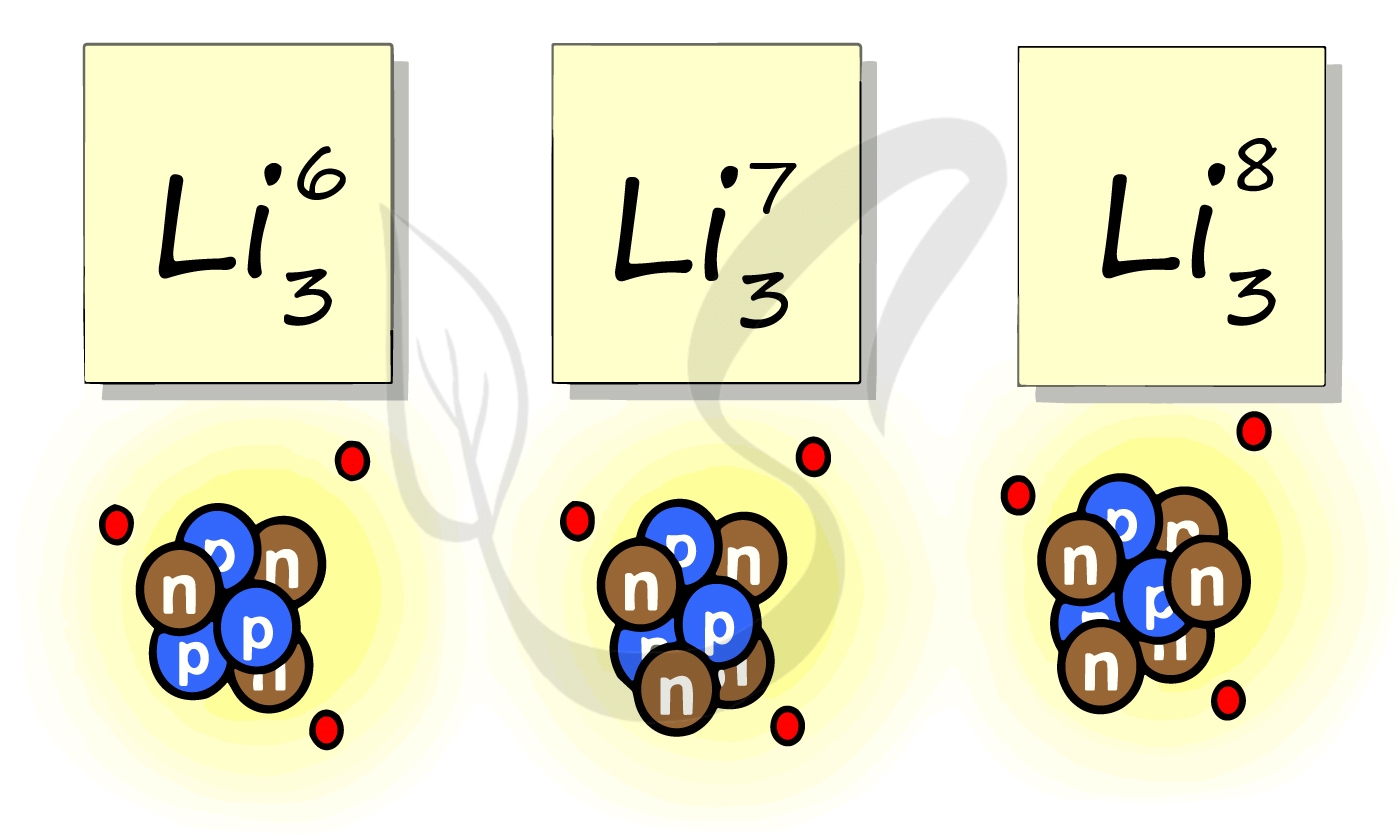
Рассмотрим пример с изотопами лития. Самостоятельно посчитайте количество нейтронов у каждого изотопа. Найдите тот, который
включен в таблицу Д.И. Менделеева.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.











