Решение залач на расчет ЭДС гальванического элемента и рН раствора
Определение ЭДС магний-алюминиевого гальванического элемента
Задача 147.
Рассчитайте ЭДС гальванического элемента Mg|Mg(NO3)2||Al(SO4)3|Al, если концентрация ионов магния и алюминия в растворах равны 0,01 моль/л и 0,001 моль/л соответственно.
Решение:
Алюминий, потенциал которого (-1,66 В) более электроположительный, чем у магния (-2,38 В) – катод, т. е. электрод, на котором протекает восстановительный процесс:
Al3+ + 3
Магний имеет меньший потенциал (-2,38 В) является анодом, на котором протекает окислительный процесс:
Mg0 – 2
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного и катодного процессов, получим:
2Al3+ + 3Mg0 = 2Al0 + 3Mg2+
Для расчета значения потенциалов, используем уравнение Нернста:
Е = Е0 + (0,059/n)lgC, где
Е0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; C – концентрация ионов металла в растворе.
Тогда
Е(Al) = -1,66 + (0,059/3)lg0,001 = -1,72 B.
Е(Mg) = -2,38 + (0,059/2)lg0,01 = -2,41 B;
Для определения ЭДС гальванического элемента необходимо из потенциала катода вычесть потенциал анода, т е. при вычислении ЭДС элемента меньший электродный потенциал вычитается из большего (в алгебраическом смысле), получим:
ЭДС = -1,72 – (-2,41) = +0,69 B.
Ответ: +0,69 B.
Определение pH исследуемого раствора, зная ЭДС гальванического элемента
Задача 148.
ЭДС гальванического элемента, составленного из водородного электрода, погружённого в исследуемый раствор, и электрода, имеющего потенциал Е = +0,337В, равна 0,54В. Определить pH исследуемого раствора. Ответы: 1) 3,5, 2) 7,00, 3) 3,44.
Решение:
Электродный потенциал водородного электрода, погруженного в исследуемый раствор, вычисляется из уравнения:
Е = -0,059pH.
Эная ЭДС гальванического элемента и электродный потенциал катода можно рассчитать электродный потенциал анода, получим:
ЭДС = E(катод) – Е(анод);
Е(анод) – ЭДС = 0,337 – 0,54 = -0.203B.
Теперь рассчитаем рН раствора, в который погружён анод, получим:
E = -0,059pH; pH = E(анод)/(-0,059) = -0.203/-0,059 = 3,44.
Ответ: 3); рН = 3,44.
Продукты коррозии железа покрыто висмутом
Задача 149.
Изделие из железа покрыто висмутом. Какой из металлов будет разрушаться при нарушении целостности покрытия? Напишите уравнения реакций происходящих процессов на катоде и аноде. Укажите продукты коррозии.
Решение:
Стандартные электродные потенциалы железа и висмута равны соответственно -0,44 В и +0,215 В. Окисляться, т.е. подвергаться коррозии, будет железо.
Железо имеет более электроотрицательный стандартный электродный потенциал (-0,44 В), чем висмут (+0,215 В), поэтому оно является анодом, висмут – катодом.
а) Коррозия пары металлов Fe/Bi в атмосфере влажного газа
Анод: Fe – 2
Катод: 1/2O2 + H2O + 2
Схема коррозии:
Fe + 1/2O2 + H2O = Fe(OH)2
Так как ионы Fe2+ с гидроксид-ионами ОН– образуют нерастворимый гидроксид, то продуктом коррозии будет Fe(OH)2:
Fе2+ + 2OH– = Fe(OH)2.
Воздух окисляет его и образуется ржавчина, гидратированный оксид железа(III):
2Fе(ОН)2(тв.) + 1/2О2(г.) + Н2О(ж.) = Fе2О3 . хН2О (тв.).
Таким образом, продуктом коррозии пары металлов Fe/Bi в атмосфере влажного газа является ржавчина Fе2О3 . хН2О.
…
Электродные потенциалы. ЭДС реакции
Окислительно — восстановительный потенциал является частным, узким случаем понятия электродного потенциала. Рассмотрим подробнее эти понятия.
В ОВР передача электронов восстановителями окислителям происходит при непосредственном контакте частиц, и энергия химической реакции переходит в теплоту.
Энергия любой ОВР, протекающей в растворе электролита, может быть превращена в электрическую энергию, если, например, окислительно-восстановительные процессы разделить пространственно, т.е. передача электронов восстановителем будет происходить через проводник электричества.
Это реализовано в гальванических элементах, где электрическая энергия получается из химической энергии окислительно-восстановительной реакции.
Элемент Даниэля-Якоби
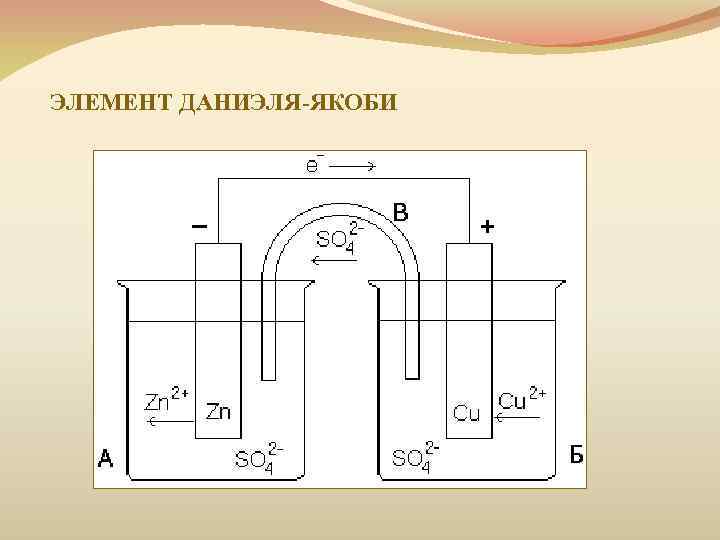
Рассмотрим гальванический элемент Даниэля-Якоби, в котором левый сосуд наполнен раствором сульфата цинка ZnSO4, с опущенной в него цинковой пластинкой, а правый сосуд – раствором сульфата меди CuSO4, с опущенным в него медной пластинкой.
Взаимодействие между раствором и пластиной, которая выступает в качестве электрода, способствует тому, чтобы электрод приобрел электрический заряд.
Возникающая на границе металл-раствор электролита разность потенциалов, называется электродным потенциалом. Значение и знак (+ или -) электродного потенциала определяются природой раствора и находящегося в нем металла.
При погружении металлов в растворы их солей более активные из них (Zn, Fe и др.) заряжаются отрицательно, а менее активные (Cu, Ag, Au и др.) положительно.
Результатом соединения цинковой и медной пластинки проводником электричества, является возникновение в цепи электрического тока за счет перетекания электронов с цинковой к медной пластинке по проводнику.
При этом происходит уменьшение количества электронов в цинке, что компенсируется переходом Zn2+ в раствор т.е. происходит растворение цинкового электрода — анода (процесс окисления).
Zn — 2e— = Zn2+
В свою очередь, рост количества электронов в меди компенсируется разряжением ионов меди, содержащихся в растворе, что приводит к накоплению меди на медном электроде – катоде (процесс восстановления):
Cu2+ + 2e— = Cu
Таким образом, в элементе Даниэля-Якоби происходит такая реакция:
Zn + Cu2+ = Zn2+ + Cu
Zn + CuSO4 = ZnSO4 + Cu
Количественно охарактеризовать окислительно-восстановительные процессы позволяют электродные потенциалы, измеренные относительно нормального водородного электрода (его потенциал принят равным нулю).
Чтобы определить стандартные электродные потенциалы используют элемент, одним из электродов которого является испытуемый металл (или неметалл), а другим является водородный электрод. По найденной разности потенциалов на полюсах элемента определяют нормальный потенциал исследуемого металла.
Окислительно-восстановительный потенциал
Значениями окислительно-восстановительного потенциала пользуются в случае необходимости определения направления протекания реакции в водных или других растворах.
Проведем реакцию
2Fe3+ + 2I— = 2Fe2+ + I2
таким образом, чтобы йодид-ионы и ионы железа обменивались своими электронами через проводник.
В сосуды, содержащие растворы Fe3+ и I—, поместим инертные (платиновые или угольные) электроды и замкнем внутреннюю и внешнюю цепь. В цепи возникает электрический ток.
Йодид-ионы отдают свои электроны, которые будут перетекать по проводнику к инертному электроду, погруженному в раствор соли Fe3+:
2I— — 2e— = I2
2Fe3+ + 2e— = 2Fe2+
Процессы окисления-восстановления происходят у поверхности инертных электродов. Потенциал, который возникает на границе инертный электрод – раствор и содержит как окисленную, так восстановленную форму вещества, называется равновесным окислительно-восстановительным потенциалом.
Факторы, влияющие на значение окислительно-восстановительного потенциала
Значение окислительно-восстановительного потенциала зависит от многих факторов, в том числе и таких как:
1) Природа вещества (окислителя и восстановителя)
2) Концентрация окисленной и восстановленной форм.
При температуре 25°С и давлении 1 атм. величину окислительно-восстановительного потенциала рассчитывают с помощью уравнения Нернста:
E = E° + (RT/nF)ln(Cок/Cвос), где
E – окислительно-восстановительный потенциал данной пары;
E°- стандартный потенциал (измеренный при Cок = Cвос);
R – газовая постоянная (R = 8,314 Дж);
T – абсолютная температура, К
n – количество отдаваемых или получаемых электронов в окислительно-восстановительном процессе;
F – постоянная Фарадея (F = 96484,56 Кл/моль);
Cок – концентрация (активность) окисленной формы;
Cвос– концентрация (активность) восстановленной формы.
Подставляя в уравнение известные данные и перейдя к десятичному логарифму, получим следующий вид уравнения:
E = E° + (0,059/n)lg(Cок/Cвос)
При Cок > Cвос, E > E° и наоборот, если Cок < Cвос, то E < E°
3) Кислотность раствора
Для пар, окисленная форма которых содержит кислород (например, Cr2O72-, CrO42-, MnO4—) при уменьшении pH раствора окислительно-восстановительный потенциал возрастает, т.е. потенциал растет с ростом H+. И наоборот, окислительно-восстановительный потенциал падает с уменьшением H+.
4) Температура
При увеличении температуры окислительно-восстановительный потенциал данной пары также растет.
Стандартные окислительно-восстановительные потенциалы представлены в таблицах специальных справочников. Следует иметь ввиду, что рассматриваются только реакции в водных растворах при температуре ≈ 25°С.
Такие таблицы дают возможность сделать некоторые выводы:
Что можно определить по значению окислительно-восстановительного потенциала
- Величина и знак стандартных окислительно-восстановительных потенциалов, позволяют предсказать какие свойства (окислительные или восстановительные) будут проявлять атомы, ионы или молекулы в химических реакциях, например
E°(F2/2F—) = +2,87 В – сильнейший окислитель
E°(K+/K) = — 2,924 В – сильнейший восстановитель
Окислительно-восстановительная пара будет обладать тем большей восстановительной способностью, чем больше числовое значение ее отрицательного потенциала, а окислительная способность тем выше, чем больше положительный потенциал.
- Возможно определить какое из соединений одного элемента будет обладать наиболее сильным окислительными или восстановительными свойствами.
- Возможно предсказать направление ОВР. Известно, что работа гальванического элемента имеет место при условии, что разность потенциалов имеет положительное значение. Протекание ОВР в выбранном направлении также возможно, если разность потенциалов имеет положительное значение. ОВР протекает в сторону более слабых окислителей и восстановителей из более сильных, например, реакция
Sn2+ + 2Fe3+ = Sn4+ + 2Fe2+
практически протекает в прямом направлении, т.к.
E° (Sn4+/Sn2+) = +0,15 В,
E° (Fe3+/Fe2+) = +0,77 В,
т.е. E° (Sn4+/Sn2+) < E° (Fe3+/Fe2+).
Реакция
Cu + Fe2+ = Cu2+ + Fe
невозможна в прямом направлении и протекает только справа налево, т.к.
E° (Сu2+/Cu) = +0,34 В,
E° (Fe2+/Fe) = — 0,44 В,
E° (Fe2+/Fe) < E° (Сu2+/Cu).
В процессе ОВР количество начальных веществ уменьшается, вследствие чего Е окислителя падает, а E восстановителя возрастает. При окончании реакции, т.е. при наступлении химического равновесия потенциалы обоих процессов выравниваются.
- Если при данных условиях возможно протекание нескольких ОВР, то в первую очередь будет протекать та реакция, у которой разность окислительно-восстановительных потенциалов наибольшая.
- Пользуясь справочными данными, можно определить ЭДС реакции.
Как определить электродвижущую силу (ЭДС) реакции?
Рассмотрим несколько примеров реакций и определим их ЭДС:
- Mg + Fe2+ = Mg2+ + Fe
- Mg + 2H+ = Mg2+ + H2
- Mg + Cu2+ = Mg2+ + Cu
E° (Mg2+/Mg) = — 2,36 В
E° (2H+/H2) = 0,00 В
E° (Cu2+/Cu) = +0,34 В
E° (Fe2+/Fe) = — 0,44 В
Чтобы определить ЭДС реакции, нужно найти разность потенциала окислителя и потенциала восстановителя
ЭДС = Е0ок — Е0восст
- ЭДС = — 0,44 — (- 2,36) = 1,92 В
- ЭДС = 0,00 — (- 2,36) = 2,36 В
- ЭДС = + 0,34 — (- 2,36) = 2,70 В
Все вышеуказанные реакции могут протекать в прямом направлении, т.к. их ЭДС > 0.
Связь константы равновесия и окислительно — восстановительного потенциала
Если возникает необходимость определения степени протекания реакции, то можно воспользоваться константой равновесия.
Например, для реакции
Zn + Cu2+ = Zn2+ + Cu
Применяя закон действующих масс, можно записать
K = CZn2+/CCu2+
Здесь константа равновесия К показывает равновесное соотношение концентраций ионов цинка и меди.
Значение константы равновесия можно вычислить, применив уравнение Нернста
E = E° + (0,059/n)lg(Cок/Cвос)
Подставим в уравнение значения стандартных потенциалов пар Zn/Zn2+ и Cu/Cu2+, находим
E0Zn/Zn2+ = -0,76 + (0,59/2)lgCZn/Zn2+
E0Cu/Cu2+ = +0,34 + (0,59/2)lgCCu/Cu2+
В состоянии равновесия E0Zn/Zn2+ = E0Cu/Cu2+, т.е.
-0,76 + (0,59/2)lgCZn2+ = +0,34 + (0,59/2)lgCCu2+, откуда получаем
(0,59/2)( lgCZn2 — lgCCu2+) = 0,34 – (-0,76)
lgK = lg (CZn2+/CCu2+) = 2(0,34 – (-0,76))/0,059 = 37,7
K = 1037,7
Значение константы равновесия показывает, что реакция идет практически до конца, т.е. до того момента, пока концентрация ионов меди не станет в 1037,7 раз меньше, чем концентрация ионов цинка.
Константа равновесия и окислительно-восстановительный потенциал связаны общей формулой:
lgK = (E10 -E20 )n/0,059, где
K — константа равновесия
E10 и E20 – стандартные потенциалы окислителя и восстановителя соответственно
n – число электронов, отдаваемых восстановителем или принимаемых окислителем.
Если E10 > E20, то lgK > 0 и K > 1.
Следовательно, реакция протекает в прямом направлении (слева направо) и если разность (E10 — E20) достаточно велика, то она идет практически до конца.
Напротив, если E10 < E20, то K будет очень мала.
Реакция протекает в обратном направлении, т.к. равновесие сильно смещено влево. Если разность (E10 — E20) незначительна, то и K ≈ 1 и данная реакция не идет до конца, если не создать необходимых для этого условий.
Зная значение константы равновесия, не прибегая к опытным данным, можно судить о глубине протекания химической реакции. Следует иметь ввиду, что данные значений стандартных потенциалов не позволяют определить скорость установления равновесия реакции.
По данным таблиц окислительно-восстановительных потенциалов возможно найти значения констант равновесия примерно для 85000 реакций.
Как составить схему гальванического элемента?
Приведем рекомендации ИЮПАК, которыми следует руководствоваться, чтобы правильно записать схемы гальванических элементов и протекающие в них реакции:
- ЭДС элемента — величина положительная, т.к. в гальваническом элементе работа производится.
- Значение ЭДС гальванической цепи – это сумма скачков потенциалов на границах раздела всех фаз, но, учитывая, что на аноде происходит окисление, то из значения потенциала катода вычитают значение потенциала анода.
Таким образом, при составлении схемы гальванического элемента слева записывают электрод, на котором происходит процесс окисления (анод), а справа – электрод, на котором происходит процесс восстановления (катод).
- Граница раздела фаз обозначается одной чертой — |
- Электролитный мостик на границе двух проводников обозначается двумя чертами — ||
- Растворы, в которые погружен электролитный мостик записываются слева и справа от него (если необходимо, здесь же указывается концентрация растворов). Компоненты одной фазы, при этом записываются через запятую.
Например, составим схему гальванического элемента, в котором осуществляется следующая реакция:
Fe0 + Cd2+ = Fe2+ + Cd0
В гальваническом элементе анодом является железный электрод, а катодом – кадмиевый.
Анод Fe0|Fe2+ || Cd2+|Cd0Катод
Типичные задачи на составление схем гальванического элемента и вычисление ЭДС реакции с решениями вы найдете здесь.
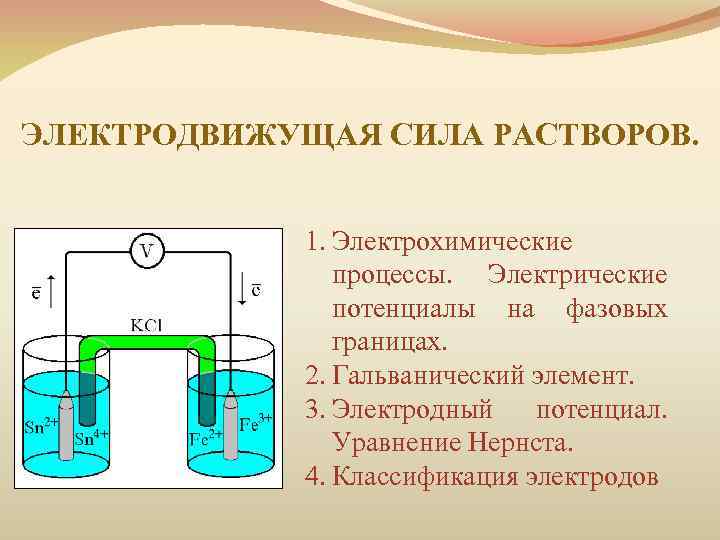
ЭЛЕКТРОДВИЖУЩАЯ СИЛА РАСТВОРОВ. 1. Электрохимические процессы. Электрические потенциалы на фазовых границах. 2. Гальванический элемент. 3. Электродный потенциал. Уравнение Нернста. 4. Классификация электродов
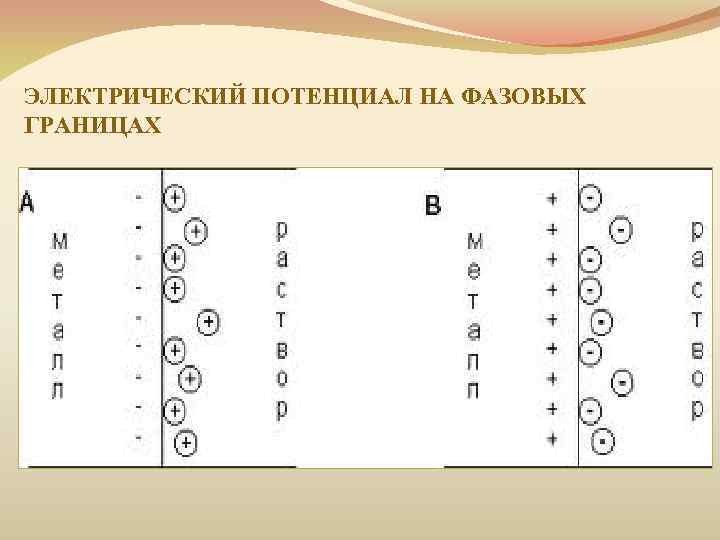
ЭЛЕКТРИЧЕСКИЙ ПОТЕНЦИАЛ НА ФАЗОВЫХ ГРАНИЦАХ
ГАЛЬВАНИЧЕСКИЙ ЭЛЕМЕНТ устройство, в котором энергия протекающих химических реакций превращается непосредственно в электрическую энергию ü Для осуществления такого превращения надо разбить ОВР на две полуреакции, для каждой полуреакции сконструировать полуэлемент (электрод) и объединить их в единый гальванический элемент.
ЭЛЕМЕНТ ДАНИЭЛЯ-ЯКОБИ
ЭЛЕМЕНТ ДАНИЭЛЯ-ЯКОБИ Zn + Cu 2+ → Zn 2+ + Cu 0 +65 -147 0 Zn 0→Zn 2+ + 2 e Cu 2+ + 2 e →Cu 0 Совокупность этих процессов приводит к возникновению электрического тока во внешней цепи.
ЭЛЕКТРОДВИЖУЩАЯ СИЛА между двумя полуэлементами существует разность потенциалов, ∆φ или ЭДС – электродвижущая сила. ü Работа, которую может совершить электрический ток, вырабатываемый гальваническим элементом, определяется разностью потенциалов между электродами ∆φ и количеством прошедшего по цепи электричества q: d. A = ∆φ dq
Работа тока гальванического элемента (и, следовательно, разность потенциалов), будет максимальна при его обратимой работе, когда процессы на электродах протекают бесконечно медленно и сила тока в цепи бесконечно мала!
УРАВНЕНИЕ НЕРНСТА Величина электродного потенциала металлического электрода зависит от: • температуры • активности (концентрации) иона металла в растворе, в который опущен электрод; Математически эта уравнением Нернста. зависимость выражается
УРАВНЕНИЕ НЕРНСТА
ЭДС ЭЛЕМЕНТА ДАНИЕЛЯ-ЯКОБИ
ЭЛЕКТРОДЫ § Электродом в электрохимии называется поверхность раздела между проводником электрического тока с электронной проводимостью и проводником электрического тока с ионной проводимостью, или, иными словами, место, где электронный механизм переноса электрического заряда изменяется на ионный (и наоборот). § В более узком смысле слова электродом часто называют проводник электрического тока с электронной проводимостью.
ЭЛЕКТРОДЫ Классификация электродов. 1). Электроды I рода. 2). Электроды неметаллической природы 3). Газовые электроды. 4). Электроды II рода. 5). Окислительно-восстановительные (ОХ – Rеd ). 6). Ионообменные электроды.
Электроды I рода. Ø состоят из металла, опущенного в раствор с теми же свойствами 1. Zn. SO 4 / Zn; Cu. SO 4 / Cu. 2. Амальгамный электрод (I рода). ü состоят из амальгамы металла, находящейся в контакте с раствором, содержащим ионы этого металла Сd 2+ / Cd(Hg)
Электроды I рода. 3. Газовые электроды ü состоят из инертного металла, который контактирует с газом и с раствором, содержащими ионы этого газа. Обратимы относительно катиона водородный электрод Pt (H 2) / H + Обратимы относительно аниона Хлоридный электрод Pt (Cl 2) / Cl-
ВОДОРОДНЫЙ ЭЛЕКТРОД Нормальный электрод (водородный) – где давление подачи газообразного водорода = 1 атмосфере; активность ионов водорода =1, и φ0 =0. Н 2 2 H+ + 2 e
Электроды II рода ü это металл, который покрыт трудно растворимой собственной солью и опущенный в раствор, содержащий ионы такие же как и в трудно растворимой соли. 1. Каломельный Нg / Hg 2 Cl 2 KCl 2. Хлорсеребряный Ag / Ag. Cl HCl
КАЛОМЕЛЬНЫЙ ЭЛЕКТРОД Hg 2 Cl 2 ↔ Hg 22+ + 2 Cl- Чем больше концентрация KCl, тем меньше скачок потенциала KCl – 0, 1 H φ0 = 0, 334 В КСl – 1 Н φ0 = 0, 282 В КСl – насыщ. φ0 = 0, 250 В
ХЛОРСЕРЕБРЯНЫЙ ЭЛЕКТРОД Ag 0 – ē + Cl- ↔ Ag. Cl Ø электрод компактный, Ø изготовлен в промышленных условиях, Ø обладает низким температурным коэффициентом, т. е. не зависит от t 0 C
III Окислительно-восстановительные электроды. Ø состоят из инертного металла, погруженного в раствор, содержащий вещества с различной степенью окисления Red и Oх. Пример: Pt/Fe. Cl 2 , Fe. Cl 3 Pt/ Co. Cl 3 , Co. Cl 4 продукты электронных реакций не выделяются на электродах, а остаются в растворе!
III Окислительно-восстановительные электроды. Хингидронный электрод С 6 Н 4(ОН)2 = С 6 Н 4 О 2 + 2 Н+ + 2 е RT a(хинон) * а (Н+)2 φ = φ0 + n. F * ln а(гидрогинон)
IV. Ионообменные электроды (Ионоселективные электроды)Ø состоят из ионита и раствора Ø потенциал на границе раздела фаз возникает за счет ионообменных процессов между ионитом и раствором Ионоселективные электроды (ИСЭ) ü электрохимические системы, в которых потенциал определяется процессами распределения ионов между мембраной и раствором
Ионоселективные электроды Исследуемый раствор А+ а. А+ В+ а. В+ Мембрана А+, В+ Стандартный раствор А+ а. А+
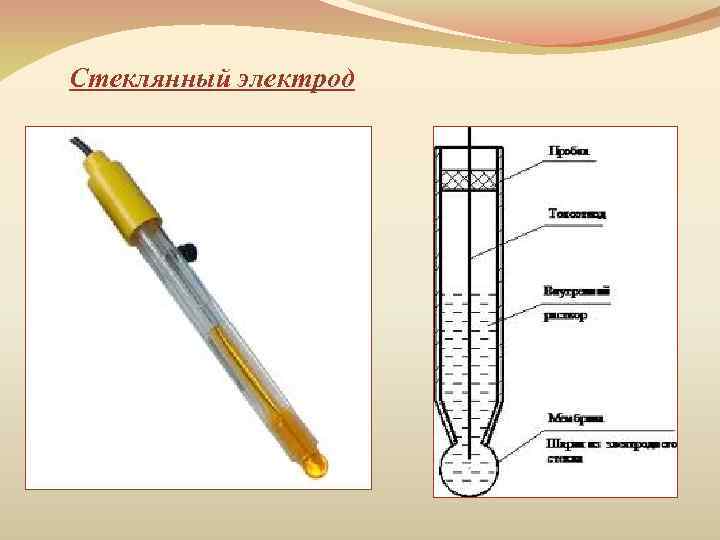
Стеклянный электрод
Стеклянный электрод ü состоит из стеклянного тонкостенного шарика, припаянного к стеклянной трубке. ü в шарик налит раствор HCl (внутренний раствор, моль∙л– 1), в который опущен хлорсеребряный электрод. Na+мр + H+р ↔ Na+р + H+мр
ЭЛЕКТРОДЫ СРАВНЕНИЯ Ø это такие электроды, потенциал которых известен и не изменяется во времени. ü водородный ü каломельный ü хлорсеребряный.
СПАСИБО ЗА ВНИМАНИЕ!
Тема 9. Электродные потенциалы. Электродвижущие силы. Электролиз
Лекция 9/1 Электродные потенциалы. Электродвижущие силы
Рассматриваемые вопросы:
1. Электродные потенциалы и механизм их возникновения.
2. Водородный электрод. Стандартные электродные потенциалы металлов. Ряд стандартных электродных потенциалов.
3. Принцип действия и электродвижущие силы гальванического элемента.
Для определения направления и полноты протекания окислительно-восстановительных реакций между окислительно-восстановительными системами в водных растворах используются значения электродных потенциалов этих систем.
Механизм возникновения электродных потенциалов, их количественное определение, процессы, которые сопровождаются возникновением электрического тока или вызваны электрическим током, изучаются особым разделом химии – электрохимией.
К электрохимическим относятся явления, возникающие на границе двух фаз с участием заряженных частиц (ионов и электронов), например, при погружении металлической пластинки в воду.
Рекомендуемые материалы
Для всех металлов характерно свойство в большей или меньшей степени растворяться в воде. При этом в воду переходят положительно заряженные ионы металла, в результате чего пластинка (из-за появления в ней избыточных электронов) заряжается отрицательно. Гидратированные катионы металла скапливаются возле поверхности пластинки на границе раздела двух фаз (металл-раствор). Возникает двойной электрический слой, характеризующийся некоторой разностью электростатических потенциалов. Как известно, энергию, которую необходимо затратить (положительный потенциал) или которую можно получить (отрицательный потенциал) при переносе единицы электричества из бесконечности в данную точку, называют электрическим потенциалом. Между пластинкой и раствором устанавливается окислительно-восстановительное равновесие:

При погружении металла в раствор его соли также возникает двойной
электрический слой, но в этом случае возможны два механизма его образования. Если концентрация катионов металла в растворе мала или металл довольно активный, вследствие чего равновесие процесса, указанного выше, сдвинуто вправо, то металлическая пластинка заряжается отрицательно:
В том случае, когда концентрация катионов металла в растворе велика или металл малоактивный, равновесие указанного процесса сдвигается влево и металлическая пластинка заряжается положительно:
В любом случае на границе раздела двух фаз образуется двойной электрический слой. Разность (скачок) потенциалов, возникающая между металлом и жидкой фазой, называется электродным потенциалом Е. Потенциалу металла приписывается тот знак, который возникает на его поверхности в двойном электрическом слое.
Пластинка металла и раствор его соли (т.е. катионы этого металла) вместе составляют единую окислительно-восстановительную систему, характеризующуюся определенным электродным потенциалом, который зависит от природы металла, концентрации его ионов в растворе, от температуры и рН среды.
При определении скачка потенциала в окислительно-восстановительных системах, не содержащих твердой фазы (например, MnO4–/Mn2+ или Cr2O72-/Cr3+), используют инертные электроды (благородные металлы, графит). В этом случае инертные электроды, адсорбируя из раствора молекулы, атомы или ионы, играют роль твердой фазы, обеспечивающей возникновение скачка потенциалов на межфазной границе.
Экспериментально определить абсолютное значение электродного потенциала невозможно. Поэтому на практике измеряется разность потенциалов между электродным потенциалом исследуемой системы и потенциалом электрода сравнения. В качестве стандартного электрода сравнения обычно используют водородный электрод. Он изготавливается из губчатой платины, погруженной в раствор H2SO4 c активностью ионов водорода, равной единице (что соответствует примерно их концентрации, равной 1 моль/л). Через раствор при 298 К (25 оС) под давлением в 101,325 кПа пропускается газообразный водород, который поглощается губчатой платиновой пластиной.
Рис.9.1 Гальваническая цепь для измерения электродного потенциала:
I – водородный электрод, II – солевой мостик, III – измеряемый электрод.
Таким образом, поверхность платинового электрода фактически насыщена водородом, в результате чего в системе устанавливается равновесие:

которое характеризуется определенным значением скачка потенциала на межфазной границе. Электродный потенциал, отвечающий данным условиям, получил название стандартного водородного потенциала 
Сочетая электрод, представляющий исследуемую окислительно-восстановительную систему, со стандартным водородным электродом, определяют электродный потенциал Е данной системы. Для того, чтобы можно было сравнивать окислительно-восстановительные свойства различных систем по их электродным потенциалам, необходимо, чтобы последние также были измерены при стандартных условиях. Таковыми обычно являются концентрация ионов, равная 1 моль/л, давление газообразных веществ 101,325 кПа и температура 298,15 К. Потенциалы, измеренные в таких условиях, носят название стандартных электродных потенциалов и обозначаются Ео. Они часто называются также окислительно-восстановительными или редокс-потенциалами, представляя собой разность между редокс-потенциалом системы при стандартных условиях и потенциалом стандартного водородного электрода.
Знак конкретного Ео соответствует заряду электрода по отношению к стандартному водородному электроду.
Стандартный электродный потенциал – это потенциал данного электродного процесса при концентрациях всех участвующих в нем веществ, равных единице.
Стандартные электродные потенциалы окислительно-восстановительных систем приводятся в справочной литературе. Эти системы записаны в форме уравнений полуреакций восстановления, в левой части которых находятся атомы, ионы или молекулы, принимающие электроны (окисленная форма):
Ox + n×
Эти системы в таблицах расположены в порядке возрастания величин их потенциалов, что соответствует падению восстановительной и росту окислительной активности. Система с большим электродным потенциалом всегда является окислителем по отношению к системе с меньшим потенциалом.
Выделяя из этого ряда окислительно-восстановительные системы типа Меn+/Me и располагая их в порядке возрастания стандартных электродных потенциалов, получают электрохимический ряд напряжений металлов: Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H2, Bi, Cu, Hg, Ag, Pd, Pt, Au.
Электрохимический ряд напряжений характеризует свойства металлов в водных растворах:
1. чем меньше электродный потенциал металла, тем легче он окисляется и труднее восстанавливается из своих ионов;
2. металлы, имеющие отрицательные электродные потенциалы, т.е. стоящие в ряду напряжений левее водорода, способны вытеснять его из разбавленных растворов кислот;
3. каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые имеют более высокий электродный потенциал.
При условиях, отличающихся от стандартных, численное значение равновесного электродного потенциала для окислительно-восстановительной системы, записанной в форме 

где 

С(Red) и C(Ox) – молярные концентрации соответственно восстановленной и окисленной форм соединения.

При подстановке численных значений R = 8,314 Дж/(моль×К), F=96494 Кл и Т (298 К) и замене натуральных логарифмов на десятичные уравнение упрощается:

Например, для окислительно-восстановительной системы
уравнение Нернста имеет вид

Ячейка для измерения электродного потенциала, например элемент Якоби-Даниэля, представляет собой пример электрохимического (гальванического) элемента – устройства, в котором химическая энергия окислительно-восстановительной реакции непосредственно преобразуется в электрический ток. Их называют также химическими источниками электрической энергии (ХИЭЭ).
Гальванический элемент состоит из двух полуэлементов (окислительно-восстановительных систем), соединенных между собой металлическим проводником и солевым мостиком. На каждом полуэлементе (часто называемом электродом) происходит полуреакция (электродный процесс). Процесс окисления (отдача электронов) осуществляется на аноде (отрицательный полюс), а восстановления (прием электронов) – на катоде (положительный полюс). Например, в представленном гальваническом элементе анодом является цинковый электрод:
а катодом – водородный или медный электрод:
2Н+ + 2


Электроны от анода по внешней цели протекают к катоду. Соответствующая схема такого гальванического элемента записывается следующим образом:

(-) Zn½Zn2+ êê
На схеме одна вертикальная линия изображает границу раздела фаз (элетрод-раствор), а две вертикальные линии – границу между растворами (на практике она обычно обеспечивается с помощью солевого мостика – U-образной трубки с раствором электролита, необходимого для замыкания цели между двумя электродами).
Причиной возникновения и протекания электрического тока в гальваническом элементе является разность электродных потенциалов (э.д.с) двух окислительно-восстановительных систем, соединенных между собой. Э.д.с (DЕ) любого гальванического элемента определяется общей формулой:
где Ек и Еа – электродный потенциал соответственно на катоде и на аноде.
Так как 
При таком осуществлении окислительно-восстановительной реакции ее энергия превращается в электрическую энергию, которую можно использовать, включив во внешнюю цель устройство, потребляющее электрическую энергию (например, электронагревательный прибор, электрическую лампу и т.п.).
Действие любого гальванического элемента основано на протекании в нем окислительно-восстановительной реакции. В простейшем случае гальванический элемент состоит из двух пластин или стержней, изготовленных из различных металлов и погруженных в раствор электролита. Такая система делает возможным пространственное разделение окислительно-восстановительной реакции: окисление протекает на одном металле, а восстановление – на другом. Таким образом, электроны передаются от восстановителя к окислителю по внешней цепи. Например, элемент Якоби-Даниэля:

В принципе электрическую энергию может дать любая окислительно-восстановительная реакция. Однако число реакций, практически используемых в химических источниках электрической энергии, невелико.
Все обычные ХИЭЭ не свободны от недостатков: стоимость веществ, необходимых для их работы (Pb, Cd и т.д.) высока; отношение количества энергии, которую может дать элемент, к его массе мало.
Протекание окислительно-восстановительных процессов в сильной степени зависит от различных условий, прежде всего от природы реагирующих веществ, их концентрации, температуры и характера среды.
Так, концентрированная и разбавленная HNO3 по-разному восстанавливается при взаимодействии с одним и тем же восстановителем:


Классическим примером различия характера протекания реакций с одними и теми же окислителями и восстановителями является восстановление KМnO4 в зависимости от реакции среды:
рН < 7
pH = 7
pH > 7
Как правило, для создания кислой среды используют относительно разбавленную Н2SO4 (реже HCl). Щелочная среда обычно создается с помощью растворов КОН и NaОН.
Изменение величины электродного потенциала каждой из двух полуреакций суммарного окислительно-восстановительного процесса и даже смена его направления могут быть достигнуты также за счет изменения температуры:

С помощью электродных потенциалов достаточно просто решается вопрос о составлении уравнений окислительно-восстановительных реакций, направлении и полноте их самопроизвольного протекания и т.п.
Как известно, термодинамическим условием самопроизвольного протекания химического процесса является отрицательное значение изменения изобарно-изотермического потенциала, т.е. DG < 0. Взаимосвязь между этой термодинамической функцией и э.д.с. гальванического элемента, составленного из двух окислительно-восстановительных систем, выражается формулой;
где n – число электронов, участвующих в суммарном окислительно-восстановительном процессе.
Из последнего выражения следует, что термодинамическим условием самопроизвольного протекания процесса в прямом направлении является положительное значение э.д.с (DЕ), когда система с более высоким значением электродного потенциала выступает в качестве окислителя, т.е. восстанавливается. Например, в гальваническом элементе, состоящем из двух электродов, характеризующихся следующими параметрами:


суммарный окислительно-восстановительный процесс самопроизвольно осуществляется при условии протекания восстановительной реакции только на медном электроде, а окислительной – на цинковом. Следовательно, в объединенном уравнении электродная реакция процесса с меньшим потенциалом записывается в обратном направлении, а процесса с большим потенциалом – в том виде, в каком она представлена в таблице, т.е. в форме процесса восстановления:

Если окислитель и восстановитель расположены достаточно далеко друг от друга в ряду стандартных электродных потенциалов, то направление окислительно-восстановительного процесса практически однозначно определяется их взаимным положением в этом ряду. При близких значениях Ео (разница меньше 0,3 В) необходимо учитывать, помимо рН среды и температуры, также концентрации реагирующих веществ, поскольку при изменении этих параметров процесса зачастую может изменяться и направление его протекания.
Применяя значение DЕо окислительно-восстановительной реакции, можно рассчитать ее константу равновесия. Для суммарного процесса типа 

Отношение концентраций представляет собой выражение константы равновесия окислительно-восстановительного процесса:
По мере протекания процесса концентрации Ох1 и Red2 уменьшаются, а Red1 и Ох2 – увеличиваются, что приводит в результате к значению DЕ = 0 и, следовательно, к DG = 0, характеризующему состояние равновесия:

откуда К можно рассчитать по выражению:

Литература
1. Глинка Н.Л. Общая химия. – Л.: Химия, 1978. – С. 270–290.
2. Шиманович И.Е., Павлович М.Л., Тикавый В.Ф., Малашко П.М. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. – С. 142 – 155.
3. Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 75-81.
Тема 9. Электродные потенциалы. Электродвижущие силы. Электролиз
Лекция 9/2 Электролиз
Рассматриваемые вопросы:
1. Электролиз с нерастворимыми и растворимыми электродами.
2. Законы Фарадея.
Электролиз – окислительно-восстановительный процесс, протекающий при прохождении постоянного электрического тока через раствор или расплав электролита.
При электролизе энергия электрического тока превращается в химическую энергию, иначе говоря, осуществляется процесс, обратный по характеру происходящему в гальваническом элементе. Как и в случае гальванического элемента, на аноде происходит окисление, а на катоде – восстановление. Но при электролизе анодом является положительный электрод, а катодом – отрицательный.
Характер протекания электродных процессов при электролизе зависит от многих факторов, важнейшими из которых являются состав электролита, материал электродов и режим электролиза (температура, плотность тока и т.д.).
Различают электролиз расплавов и растворов электролитов.
Электролиз расплавов электролитов.
Электролиз расплава соли с использованием инертных электродов показан на следующей схеме:
При высоких температурах расплав соли диссоциирует на ионы:

Прохождение электрического тока через расплав обусловлено тремя одновременно протекающими процессами:
1) направленное движение катионов Мg2+ к катоду, а анионов Cl– – к аноду;
2) восстановление, происходящее на катоде:
3) окисление, происходящее на аноде:
Суммарное уравнение электролиза после уравнивания числа отдаваемых и присоединенных электронов принимает вид:
Схематически весь процесс можно представить следующим образом:
Электролиз растворов электролитов
Электролиз растворов электролитов более сложен из-за возможности участия в электродных процессах молекул воды в восстановлении на катоде:
и окислении на аноде:

В тех случаях, когда на одном и том же электроде возможно протекание двух или большего числа процессов, наиболее вероятен тот, осуществление которого связано с минимальной затратой энергии. Это означает, что на катоде восстанавливаются в первую очередь окисленные формы окислительно-восстановительных систем с наибольшим электродным потенциалом, а на аноде окисляются восстановленные формы с наименьшим электродным потенциалом.
Для определения порядка протекания окислительно-восстановительных процессов на электродах при электролизе водных растворов можно руководствоваться следующими практическими правилами.
Катод.
1. В первую очередь восстанавливаются катионы металлов, имеющих стандартный электродный потенциал больший, чем у водорода, в порядке уменьшения Ео.
2. Катионы металлов с малым стандартным электродным потенциалом (от Li+ до Al3+ включительно) не восстанавливаются, а вместо них восстанавливаются молекулы воды (в кислой среде – ионы Н+).
3. Катионы металлов, имеющих стандартный электродный потенциал меньший, чем у водорода, но больший, чем у алюминия, восстанавливаются одновременно с молекулами воды.
Анод.
Характер окислительных процессов зависит также от материала электродов. Различают нерастворимые (инертные) и растворимые (активные) электроды.
Инертные электроды изготавливаются обычно из графита, угля, платины; в процессе электролиза они химически не изменяются, а служат лишь для передачи электронов во внешнюю цель.
При использовании инертных анодов следует учитывать следующее:
1. В первую очередь окисляются простые анионы в порядке возрастания их Ео, не превышающих + 1,5 В (S2-, J–, Br–, Cl–).
2. При электролизе водных растворов, содержащих анионы кислородосодержащих кислот (CO32-, NO3–, SO42-, PO43- и др.), на аноде окисляются не эти анионы, а молекулы воды.
3. В щелочных растворах на аноде окисляются ионы ОН–:
При использовании растворимых анодов (из Cu, Zn, Ag, Ni и др. металлов) электроны во внешнюю цель посылает сам анод за счет окисления атомов металла, из которого сделан анод:

Рассмотрим конкретные примеры.
Электролиз водных растворов солей (инертные электроды)
Количественные характеристики электролитических процессов устанавливаются двумя законами Фарадея:
I. Масса веществ, выделившихся на электродах при электролизе, прямо пропорциональна количеству электричества, прошедшего через раствор или расплав электролита.
II. При пропускании одинакового количества электричества через растворы или расплавы различных элементов масса веществ, выделяющихся на электродах, пропорциональна молярным массам их эквивалентов.
Экспериментально установлено, что для выделения на электроде одной молярной массы эквивалента вещества необходимо затратить одно и то же количество электричества, равное ~96500 Кл. Оно получило название постоянной Фарадея F.
Оба закона можно объединить общей формулой:

где m – масса окисленного или восстановленного вещества, г; Э – молярная масса его эквивалента, г/моль; Q – количество электричества, прошедшее через элемент (Q = Jt, где J – сила тока, А; t – время, с).
Если Q = Jt = 1 Кл, то

Величина К называется электрохимическим эквивалентом вещества. Она представляет собой массу вещества, окисляющегося или восстанавливающегося на электродах при прохождении через элемент 1 Кл электричества. Видно, что химический эквивалент связан с электрохимическим эквивалентом соотношением:

Показателем эффективности электролиза является выход по току η, %, определяемый как отношение массы вещества, фактически полученной в данных условиях электролиза mпракт, к массе вещества, теоретически вычисленной на основании закона Фарадея mтеор:

Области применения электролиза:
– получение металлов;
– очистка металлов от примесей (рафинирование);
– извлечение ценных компонентов;
– нанесение на поверхность металлических изделий слоев других металлов (гальваностегия);
– получение точных металлических копий с рельефных предметов электроосаждением металла (гальванопластика).
Пожарная опасность процессов электролиза.
– электролиз из расплавов предполагает присутствие высоких температур, что требует выполнения правил пожарной безопасности;
– процессы очень энергоемкие, с использованием электричества, что требует выполнения правил электробезопасности;
– возможность образования при протекании процессов водорода и кислорода, которые представляют собой пожароопасные и поддерживающие горение вещества;
Вам также может быть полезна лекция “6. Компетентность и оценка аудиторов”.
– возможность образования кислот и щелочей, способных вызвать активную коррозию металлических конструкций электролизера;
– возможность образования хлора, который является отравляющим веществом.
Литература
1. Глинка Н.Л. Общая химия. – Л.: Химия, 1978. – С. 285 – 293.
2. Шиманович И.Е. и др. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. – С. 155 – 159.
3. Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 65-84.
Измерение э. д. с. этой же пары металлов в обычной цепи осложняется тем, что величина электродвижущей силы будет зависеть также и от концентрации ионов металла в растворе. Электродвижущая сила будет обусловлена, кроме контактных потенциалов, переходом ионов из металла в раствор или обратно, т. е. теми явлениями, которые рассматривает теория Нернста. Это вызывает дополнительные скачки потенциалов. [c.384]
Стеклянный электрод (см. рис. 82). В 1909 г. Ф. Габер предложил стеклянный электрод для определения pH растворов. Электродвижущая сила электрода меняется в зависимости от pH. Он представляет собой тонкостенный (0,06—0,1 мм) стеклянный шарик, [c.498]
Общая ионная сила каждого раствора равна т, однако некоторая доля этой величины (х) обусловлена присутствием ионов хлора в левом растворе и ионов серебра в правом растворе. Электродвижущая сила элемента опре-де.тяется уравнением [c.307]
Водородный показатель pH экспериментально определяется различными методами, которые можно подразделить на потенциометрические и колориметрические. Потенциометрические методы основаны на измерении э. д. с. гальванического элемента, одной из электродных жидкостей которого является исследуемый раствор. Электродвижущая сила такого элемента функционально связана с концентрацией ионов Н+ в исследуемом растворе уравнением Нернста ( 79), по которому и вычисляется pH раствора. [c.486]
На двух поверхностях пленки (4) образуется два скачка потенциала, один из которых постоянен, другой меняется с изменением исследуемого раствора. Электродвижущая сила Е полученного таким образом стеклянно-каломельного элемента представляет собой разность потенциалов стеклянного и каломельного электродов Е— л — tp , где потенциал каломельного электрода, — потенциал стеклянного электрода, складывающийся из трех скачков потенциала на трех границах стеклянная мембрана — внешний (изменяемый) раствор, стеклянная мембрана — внутренний раствор, внутренний раствор — серебро. [c.25]
В титруемый раствор помещают серебряный электрод и погружают в этот раствор один конец сифона с азотнокислым калием. Другой конец сифона помещают в сосуд с хлористым калием. Туда же помещают отвод от каломельного электрода. Полученный серебряно-каломельный элемент присоединяют к потенциометру. Титруют испытуемый раствор, определяя компенсационным методом после перемешивания раствора электродвижущую силу (э. д. с.). после каждой порции добавляемого реагента. В начале титрования добавляют по 0,5 мл раствора, когда же изменения э. д. с. от каждой порции реагента становятся значительными, измерения э. д. с. производят по добавлении 0,1 мл. [c.80]
Как известно, в самой общей форме метод активностей представляет собой такой способ описания химических равновесий, в котором при сохранении обычного выражения термодинамического химического потенциала и условий гетерогенного равновесия, как равенства химического потенциала данного комнонента во всех фазах, в уравнении химического потенциала подставляется условная величина, но имеющая прямого физического смысла, но являющаяся аналогом концентрации. В растворах электролитов коэффициент пропорциональности между активностью и концентрацией а = / с зависит от состава и концентрации раствора. Его определяют различными методами, например, путем измерения упругости паров растворов, электродвижущей силы и т. д. Оказалось, что при больших разведениях коэффициент активности стремится к единице ио мере увеличения концентрации примерно до 0,5 М он падает на несколько десятых долей это дает некоторое основание формально сопоставлять коэффициент активности со степенью диссоциации. Затем по мере увеличения концентрации раствора он резко возрастает до нескольких единиц. [c.86]
Рассмотрим работу элемента Якоби (рис. 65)—одного из наиболее простых и наиболее старых гальванических элементов, состоящего из двух электродов—цинкового и медного, погруженных в соответствующие растворы сульфатов цинка и меди, которые разделены пористой перегородкой. Цинковый электрод заряжается отрицательно по отношению к медному электроду, и когда при их замыкании по гальванической цепи проходит ток, то на медном электроде осаждается медь, а цинковый электрод растворяется. Электродвижущая сила и вызванный ею ток [c.150]
При качественном анализе, как уже указывалось выше, большое значение имеет величина pH исследуемого раствора. В некоторых случаях предварительная проверка среды раствора при помош,и лакмуса не является достаточной. Поэтому в качественном анализе пользуются более точными методами определения концентрации ионов водорода, или pH. Для быстрого и точного определения pH применяют лабораторный рН-метр типа ЛЛПУ-2, предназначенный для измерения pH водных растворов неорганических и органических солей, кислот и оснований, если активная концентрация ионов водорода в них находится в пределах Ю – до 10- г-ион и (pH от 1 до 10). Действие прибора основано на измерении развиваемой электродной парой (датчиком), опускаемой в анализируемый раствор, электродвижущей силы (э. д. с.), которая зависит от величины pH раствора. Наиболее точные физико-химические методы определения pH ввиду их сложности малопригодны для повседневных студенческих работ в лаборатории качественного анализа. Одним из более простых является колориметрический метод определения pH. Этот метод основан на применении реактивов, меняющих свою окраску в зависимости от концентрации ионов водорода. Такие реактивы получили название индикаторов. [c.171]
Исследуемый гальванический элемент обычно состоит из индикаторного электрода и электрода сравнения. Индикаторным называют электрод, потенциал которого зависит от концентрации (активности) определяемого иона. Потенциал электрода сравнения должен оставаться постоянным независимо от протекания каких-либо реакций в анализируемом растворе. Электродвижущая сила исследуемого элемента выражается как разность между потенциалом электрода сравнения ( ср) и потенциалом индикаторного электрода (Еинд) [c.192]
Для определения средних коэффициентов активности [у] испо.тьзовалась гальваническая концентрационная ячейка с переносом, составленная из двух исследуемых растворов разной концентрации и Ag/Ag l-элeктpoдoв, имеющих общий нротивоион с исследуемыми растворами. Электродвижущая сила (эдс) такой ячейки определяется из уравнения [c.110]
Элементы, в которых в результате протекания на электродах химических процессов возникает разность потенциалов,-называются химическими или гальваническими. Каждый элемент состоит из двух электродов, на границе раздела которых с растворами возникают скачки потенциалов. Кроме скачков потенциала на границе металл—раствор электродвижущая сила элемента включает контактную разность потенциала между двумя разнородными металлами электродов и скачок потенциала на границе между двумя соприкасающимися растворами (диффузионный потенциал). Сначала ознакомимся с явлениями у отдельных электродов, а затем рассмотрим для примера работу элемента Якоби — Даниэля, один электрод которого состоит из цинка, погруженного в ZnS04, а другой — из меди, погруженный в раствор USO4. Оба раствора разделены такой перегородкой, [c.250]
При построении графика зависимости э. д. с., определенной на подходящем потенциометре, от объема израсходованного стандартного раствора обычно, хотя и не всегда, получают S-образную кривую титрования, причем точка ее перегиба соответствует точке эквивалентности. Потенциометрические измерения как в водной, так и в неводных средах производятся одинаковым способом при помощи одних и тех же приборов. Отличие состоит только в составе солевого мостика, устанавливаемого между электродом и исследуе-дп,1м раствором, а при титровании в инертных растворителях имеются различия в способах экранирования и заземления сосуда, в котором производится титрование. При проведении кис.потно-основного титрования потенциал индикаторного электрода, погруженного в исследуемый раствор, зависит от активности ионов водорода в растворе. Электродвижущая сила определяется трубчатым потенциометром с болыпим внутренним сопротивлением. [c.161]
Для измерения потенциалов необходимы чувствительный нуль-гальванометр, нормальный элемент Вестона, реохорд, батарея имага-зин сопротивлений. При измерениях потенциалов возможно также применение потенциометра. Измеряемый элемент составляется из электрода сравнения (например, насыщенного каломельного электрода) и электрода из исследуемого металла в определенном растворе. Электродвижущая сила неизвестного элемента пределяется из соотношения [c.321]