Электронное строение атома фосфора
Электронное строение нейтрального атома фосфора в основном состоянии.
Схема строения электронных оболочек
Распределение электронов по энергетическим уровням (или по электронным слоям) в атоме фосфора.
P
+15
2
8
5
Электронно-графическая схема
Распределение электронов по атомным орбиталям в атоме фосфора.
| 3 | ↑↓ | ↑ | ↑ | ↑ | ||
| 2 | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ||
| 1 | ↑↓ | |||||
| s | p |
Валентные орбитали атома фосфора выделены фиолетовым цветом.
Электронная конфигурация
Полная электронная конфигурация атома фосфора.
15P 1s2 2s2 2p6 3s2 3p3
Сокращённая электронная конфигурация атома фосфора.
15P [Ne] 3s2 3p3
Квантовые числа валентных электронов
Главное (n), орбитальное (l), магнитное (m) и спиновое (s) квантовые числа валентных электронов атома фосфора.
| Орбиталь | Квантовое число | |||
|---|---|---|---|---|
| n | l | m | s | |
| 3s | 3 | 0 | 0 | +½ |
| -½ | ||||
| 3p | 3 | 1 | -1 | +½ |
| 1 | +½ | |||
| 2 | +½ |
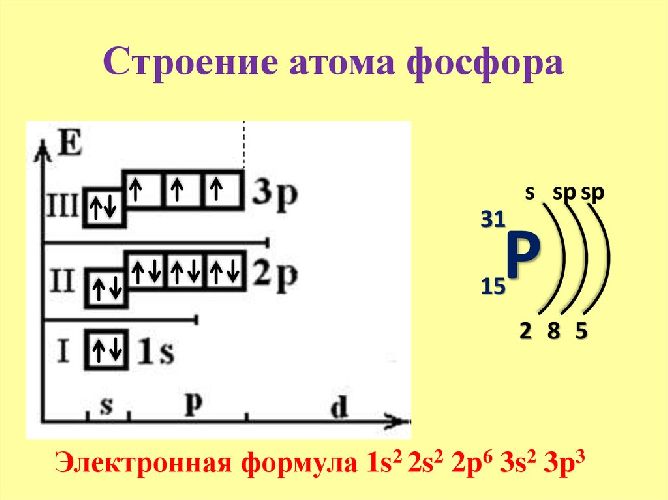
Строение атома фосфора


3.9
Средняя оценка: 3.9
Всего получено оценок: 381.
3.9
Средняя оценка: 3.9
Всего получено оценок: 381.
Фосфор (Р) – типичный неметалл с относительной атомной массой 31. Строение атома фосфора определяет его активность. Фосфор легко вступает в реакции с другими веществами и элементами.
Строение
Строение атома элемента фосфора отражено в периодической таблице Менделеева. Фосфор расположен под 15 номером в пятой группе, третьем периоде. Следовательно, атом фосфора состоит из положительно заряженного ядра (+15) и трёх электронных оболочек, на которых находится 15 электронов.
Графически расположение строение атома выглядит следующим образом:
- +15 P)2)8)5;
- 1s22s22p63s23p3.
Фосфор относится к р-элементам. На внешнем энергетическом уровне в возбуждённом состоянии располагается пять электронов, которые определяют валентность элемента. В обычном состоянии внешний уровень остаётся незавершённым. Три неспаренных электрона указывают на степень окисления (+3) и третью валентность. Фосфор легко переходит из обычного в возбуждённое состояние.
Ядро состоит из 15 протонов и 16 нейронов. Чтобы посчитать количество нейронов, необходимо вычесть из относительной атомной массы порядковый номер элемента – 31-15=16.
Аллотропия
Фосфор имеет несколько аллотропических модификаций, отличающихся строением кристаллической решётки:
- белый – ядовитое вещество, напоминающее воск, светится в темноте, т.к. окисляется при низких температурах;
- жёлтый – неочищенный белый фосфор (имеет примеси);
- красный – менее ядовитое вещество, чем белый или жёлтый фосфор, не воспламеняется и не светится;
- чёрный – похожее на графит вещество с металлическим блеском, проводит электрический ток, может переходить в металлический фосфор.

Белый фосфор – наиболее активная модификация элемента, которая быстро окисляется на воздухе, поэтому белый фосфор хранят под водой.
Свойства
Фосфор образует:
- фосфорную кислоту (H3PO4);
- оксиды P2O5 и P2O3;
- фосфин – летучее ядовитое соединение с водородом (PH3).
Фосфор реагирует c простыми веществами – металлами и неметаллами, проявляя окислительно-восстановительные свойства. Основные реакции с фосфором описаны в таблице.
|
Взаимодействие |
Что образуется |
Пример |
|
С кислородом |
Оксид (выделяется густой дым) |
– 4P + 5O2 → 2P2O5; – 4P + 3O2 → 2P2O3 |
|
С металлами |
Соль |
2P + 3Ca → Ca3P2 |
|
С неметаллами |
Соль |
– 2P + 3S → P2S3; – 2P + 3Cl2 → 2PCl3 |
|
С водой |
Кислота и фосфин |
4Р + 6Н2О → РН3 + 3Н3РО2 |
|
Со щелочами |
Фосфин и фосфит |
4Р + 3KOH + 3Н2О → РН3 + 3KH2PO2 |
|
С кислотами |
Фосфорная кислота |
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O |
Фосфор образует около 200 минералов, один из которых – апатит. Фосфор входит в состав жизненно важных соединений – фосфолипидов, которые составляют все клеточные мембраны.

Что мы узнали?
Рассмотрели схему строения атома фосфора. Формула атома – 1s22s22p63s23p3. Элемент может переходить в возбуждённое состояние с валентностью V. Известно несколько модификаций фосфора – белый, жёлтый, красный, чёрный. Самый активный – белый фосфор – способен самовоспламеняться в присутствии кислорода. Элемент реагирует со многими металлами и неметаллами, а также с кислотами, основаниями и водой.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
-

Danyal Murat
5/5
-

Дарья Селина
5/5
-

Иван Ткаченко
5/5
Оценка доклада
3.9
Средняя оценка: 3.9
Всего получено оценок: 381.
А какая ваша оценка?
Фосфор в таблице менделеева занимает 15 место, в 3 периоде.
| Символ | P |
| Номер | 15 |
| Атомный вес | 30.9737620 |
| Латинское название | Phosphorus |
| Русское название | Фосфор |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема фосфора
P: 1s2 2s2 2p6 3s2 3p3
Короткая запись:
P: [Ne]3s2 3p3
Одинаковую электронную конфигурацию имеют
атом фосфора и
Si-1, S+1, Cl+2
Порядок заполнения оболочек атома фосфора (P) электронами:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d →
5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ – до 6, на
‘d’ – до 10 и на ‘f’ до 14
Фосфор имеет 15 электронов,
заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
3 электрона на 3p-подуровне
Степень окисления фосфора
Атомы фосфора в соединениях имеют степени окисления 5, 4, 3, 2, 1, 0, -1, -2, -3.
Степень окисления – это условный заряд атома в соединении: связь в молекуле
между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается
заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается,
то степень окисления положительная.
Ионы фосфора
Валентность P
Атомы фосфора в соединениях проявляют валентность V, IV, III, II, I.
Валентность фосфора характеризует способность атома P к образованию хмических связей.
Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании
химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа P
Квантовые числа определяются последним электроном в конфигурации,
для атома P эти числа имеют значение N = 3, L = 1, Ml = 1, Ms = +½
Видео заполнения электронной конфигурации (gif):
Результат:

Энергия ионизации
Чем ближе электрон к центру атома – тем больше энергии необходимо, что бы его оторвать.
Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo.
Если не указано иное, то энергия ионизации – это энергия отрыва первого электрона, также существуют энергии
ионизации для каждого последующего электрона.
Энергия ионизации P:
Eo = 1012 кДж/моль
— Что такое ион читайте в статье.
Перейти к другим элементам таблицы менделеева
Где P в таблице менделеева?
Таблица Менделеева
Скачать таблицу менделеева в хорошем качестве
P (фосфор) – элемент с прядковым номером 15 в периодической системе.
Находится в III периоде. Температура плавления: 44 ℃. Плотность: 1.82 г/см3.
Электронная формула атома фосфора:
1s2 2s2 2p6 3s2 3p3
Сокращенная электронная конфигурация P:
[Ne] 3s2 3p3
Ниже приведена электронно-графическая схема атома фосфора

Распределение электронов по энергетическим уровням в атоме P
1-й уровень (K): 2
2-й уровень (L): 8
3-й уровень (M): 5

Валентные электроны фосфора
Количество валентных электронов в атоме фосфора – 5.
Ниже приведены их квантовые числа (N – главное, L – орбитальное, M – магнитное, S – спин)
| Орбиталь | N | L | M | S |
|---|---|---|---|---|
| s | 3 | 0 | 0 | +1/2 |
| s | 3 | 0 | 0 | -1/2 |
| p | 3 | 1 | -1 | +1/2 |
| p | 3 | 1 | 0 | +1/2 |
| p | 3 | 1 | 1 | +1/2 |
Степени окисления, которые может проявлять фосфор: -3, -2, -1, +1, +2, +3, +4, +5
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,655 -
гуманитарные
33,653 -
юридические
17,917 -
школьный раздел
611,939 -
разное
16,901
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
