поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,655 -
гуманитарные
33,653 -
юридические
17,917 -
школьный раздел
611,939 -
разное
16,901
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Расчет количества теплоты при нагревании и охлаждении:
Вы уже знаете, что изменить внутреннюю энергию тела можно передачей ему количества теплоты. Как связано изменение внутренней энергии тела, т. е. количество теплоты, с характеристиками самого тела?
Внутренняя энергия тела есть суммарная энергия всех его частиц. Значит, если массу данного тела увеличить в два или три раза, то и количество теплоты, необходимое для его нагревания на одно и то же число градусов, увеличится в два или три раза. Например, на нагревание двух килограммов воды от 20 °C до 80 °C потребуется в два раза больше теплоты, чем на нагревание одного килограмма воды (рис. 40, а).
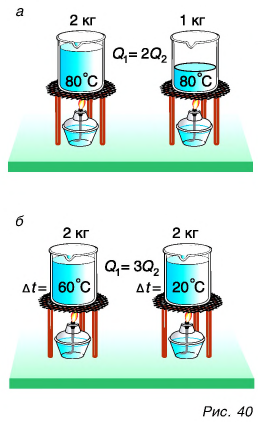
Очевидно также, что для нагревания воды на 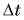
Из этих рассуждений следует подтвержденный опытами вывод. Количество теплоты, необходимое для нагревания тела, прямо пропорционально его массе и изменению температуры.
А зависит ли количество теплоты, идущее на нагревание, от рода вещества, которое нагревается?
Для ответа на этот вопрос проведем опыт. В два одинаковых стакана нальем по 150 г подсолнечного масла и воды. Поместим в них термометры и поставим на нагреватель (рис. 41).
Получив за одинаковое время от нагревателя равное с водой количество теплоты, масло нагрелось больше, чем вода. Значит, для изменения температуры масла на одну и ту же величину требуется меньше теплоты, чем для изменения температуры такой же массы воды.
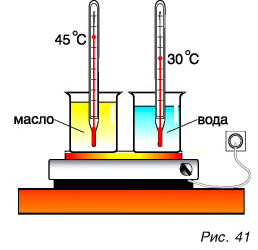
Поэтому для всех веществ вводят специальную величину — удельную теплоемкость вещества. Эту величину обозначают буквой с (от лат. capacite — емкость, вместимость). Теперь мы можем записать строгую формулу для количества теплоты, необходимого для нагревания:
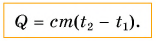
Выразим из этой формулы с: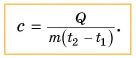
Удельная теплоемкость есть физическая величина, численно равная количеству теплоты, которое необходимо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C. Удельная теплоемкость измеряется в джоулях на килограмм-градус Цельсия 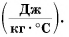
Для любознательных:
Часто формулу 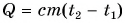 записывают в виде
записывают в виде 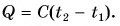 Здесь величина
Здесь величина 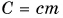 называется теплоемкостью тела (обратите внимание — не вещества). Она численно равна количеству теплоты, необходимому для нагревания всей массы тела на 1 °C. Измеряется теплоемкость тела в джоулях на градус Цельсия
называется теплоемкостью тела (обратите внимание — не вещества). Она численно равна количеству теплоты, необходимому для нагревания всей массы тела на 1 °C. Измеряется теплоемкость тела в джоулях на градус Цельсия 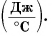
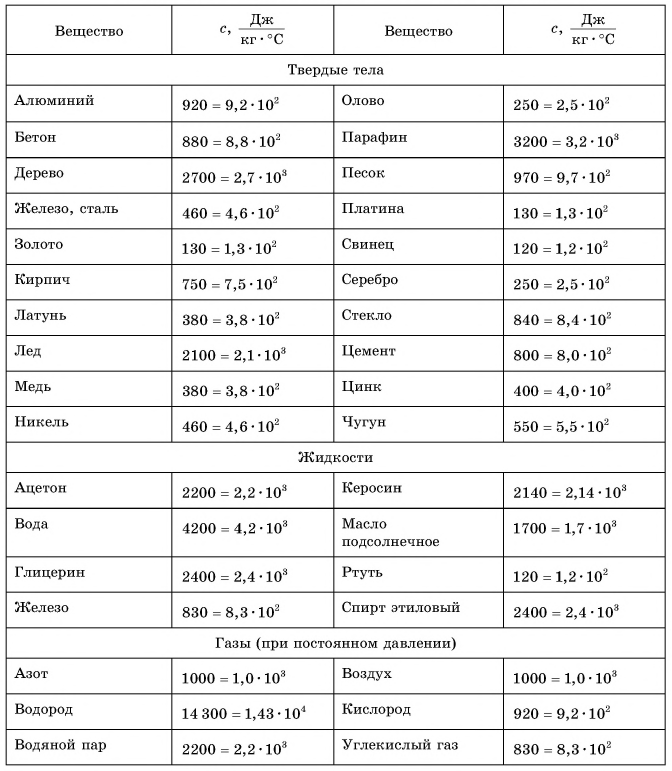
В таблице 1 представлены значения удельной теплоемкости различных веществ (в различных состояниях). Как следует из этой таблицы, среди жидкостей максимальное значение удельной теплоемкости имеет вода: для нагревания 1 кг воды на 1 °C требуется 4200 Дж теплоты — это почти в 2,5 раза больше, чем для нагревания 1 кг подсолнечного масла, и в 35 раз больше, чем для нагревания 1 кг ртути.
Формула 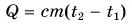 дает возможность найти и выделяемую при охлаждении тела теплоту. Так как конечная температура
дает возможность найти и выделяемую при охлаждении тела теплоту. Так как конечная температура 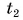 остывшего тела меньше начальной
остывшего тела меньше начальной 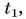 то изменение температуры оказывается отрицательным числом. Значит, и выделяемое телом количество теплоты выражается отрицательным числом, что обозначает не рост, а убыль внутренней энергии тела.
то изменение температуры оказывается отрицательным числом. Значит, и выделяемое телом количество теплоты выражается отрицательным числом, что обозначает не рост, а убыль внутренней энергии тела.
В заключение заметим, что при теплообмене двух или нескольких тел абсолютное значение количества теплоты, которое отдано более нагретым телом (телами), равно количеству теплоты, которое получено более холодным телом (телами):
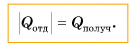
Это равенство называется уравнением теплового баланса и выражает, по сути, закон сохранения энергии. Оно справедливо при отсутствии потерь теплоты.
Таблица 1. Удельная теплоемкость некоторых веществ
Главные выводы:
- Количество теплоты, необходимое для нагревания тела (выделившееся при охлаждении), прямо пропорционально его массе, изменению температуры тела и зависит от вещества тела.
- Удельная теплоемкость вещества численно равна количеству теплоты, которое надо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C.
- При теплообмене количество теплоты, отданное более горячим телом, равно по модулю количеству теплоты, полученному более холодным телом, если нет потерь теплоты.
- Заказать решение задач по физике
Пример решения задачи:
Для купания ребенка в ванночку влили холодную воду массой 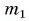 = 20 кг при температуре
= 20 кг при температуре 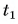 = 12 °C. Какую массу горячей воды при температуре
= 12 °C. Какую массу горячей воды при температуре 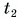 = 80 °C нужно добавить в ванночку, чтобы окончательная температура воды стала
= 80 °C нужно добавить в ванночку, чтобы окончательная температура воды стала 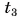 = 37 °C? Удельная теплоемкость воды с = 4200
= 37 °C? Удельная теплоемкость воды с = 4200 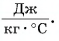
Дано:
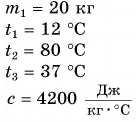
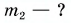
Решение
По закону сохранения энергии 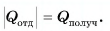
Отдавала теплоту горячая вода, изменяя свою температуру от 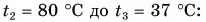
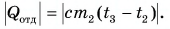
Холодная вода получила эту теплоту и нагрелась от 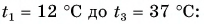
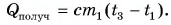
Так как нас интересует только модуль 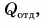 то можно записать:
то можно записать:
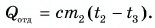
Тогда 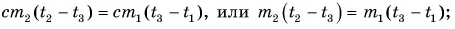
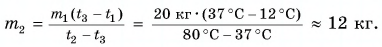
При решении мы пренебрегали потерями теплоты на нагревание ванночки, окружающего воздуха и т. д.
Возможен и другой вариант решения.
Рассчитаем сначала количество теплоты, которое было получено холодной водой:
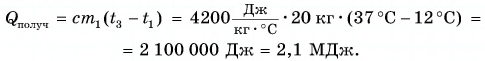
Полагая, что эта теплота отдана горячей водой, запишем: 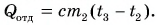 Выразим искомую массу:
Выразим искомую массу:
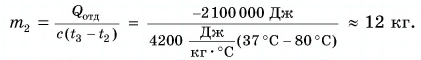
Ответ: 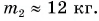
- Удельная теплота сгорания топлива
- Плавление и кристаллизация в физике
- Испарение жидкостей в физике
- Поверхностное натяжение жидкости
- Излучение тепла в физике
- Виды излучений в физике
- Инфракрасные излучения
- Количество теплоты в физике
Физика,
вопрос задал Fizica,
8 лет назад
Ответы на вопрос
Ответил InvisorTech
1
Дано: m = 2 кг, t₀ = 30°C, λ = 3.4 * 10⁵ Дж/кг
Найти: Q – ?
Решение:
Ответ: Q = 932 кДж
Предыдущий вопрос
Следующий вопрос
Новые вопросы
Литература,
5 лет назад
Написати власну детективну історія за схемою Конан Дойля…
География,
5 лет назад
Как называется прибор который использует при географических исследований…
Математика,
8 лет назад
две бригады должны изготовить 6930деталей. одна бригада-70деталей, другая-90 деталей. На сколько недель одна бригада опередит другую?
Математика,
8 лет назад
Задача На клумбе растет 7 роз, гладиолусов на 3 больше, чем роз, и на 2 цветка меньше чем колокольчиков. Сколько всего цветов на клумбе?
Алгебра,
8 лет назад
дана функция Y=f(X) где f(X)=х в квадрате. при каких значениях аргумента верно равенство f(X)=f(х+5)?
Математика,
8 лет назад
Який з виразів має таке саме значеннящо й вираз 7*4*40*25
а)4*25+7*40
б)(7+4+25)*40
в)(7*40)*(25*4)
*-це умножить (помножити)…
Содержание:
- Изменение внутренней энергии
- Внутренняя энергия тела
- Теплообмен
- Виды теплообмена
- Изменение внутренней энергии при нагревании и охлаждении
- Уравнение теплового баланса при теплообмене
- Подсчет теплоты, выделяемой при сжигании топлива. К. П. Д. нагревателя
- Изменение внутренней энергии при выполнении механической работы
- Закон сохранения и превращения энергии в механике
- Закон сохранения и превращения энергии в механических и тепловых процессах
- Первое начало термодинамики
- Применение первого начала термодинамики к изопроцессам в идеальном газе
- Адиабатный процесс
- Понятие о строении солнца и звезд
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе Q = ΔU · A
На странице -> решение задач по физике собраны решения задач и заданий с решёнными примерами по всем темам физики.
Изменение внутренней энергии
Внутренняя энергия тела – это полная энергия всех молекул, которые его составляют. Внутренняя энергия идеального газа пропорциональна его температуре.
Чтобы изменить внутреннюю энергию вещества, надо сообщить ему некоторое количество тепла или совершить работу.
Внутренняя энергия тела
Под внутренней энергией тела подразумевается сумма кинетической и потенциальной энергий всех частиц тела и энергии ядер его атомов. Возникает вопрос: какая же энергия не входит во внутреннюю энергию тела?
Пусть для примера таким телом является наша Земля. Известно, что Земля притягивается к Солнцу и движется по орбите вокруг него, т. е. обладает по отношению к Солнцу как потенциальной, так и кинетической энергией. Эта энергия не входит во внутреннюю энергию Земли, так как она связана с телом, находящимся вне Земли. Таким образом, во внутреннюю энергию тела не входит кинетическая и потенциальная энергия этого тела относительно всех тех тел, которые находятся вне его. Аналогично во внутреннюю энергию системы тел не входит кинетическая и потенциальная энергия этой системы относительно тех тел, которые не входят в эту систему.
Не менее важным является вопрос о том, как вычислять внутреннюю энергию тела или системы тел. Оказывается, что только для идеального газа имеется соответствующая формула . Во всех других случаях вычислять внутреннюю энергию мы не умеем. Однако для решения практических вопросов существенную роль играет не сама внутренняя энергия, а ее изменение, т. е. разность между ее значениями в начале и в конце того или иного процесса. А для этого не нужно знать числового значения всей внутренней энергии. Это относится не только к внутренней энергии. Примером сказанного может служить и разность температур, которая и по термодинамической шкале и по шкале Цельсия одинакова, т. е. не зависит от числового значения самой температуры, если ее единица не меняется.
Поскольку в молекулярной физике рассматриваются только такие явления, при которых молекулы не изменяются, то можно считать, что в этих явлениях изменяются только молекулярно-кинетическая и молекулярно-потенциальная энергии. Это упрощение значительно облегчает многие расчеты.
На основании закона сохранения энергии можно утверждать, что изменение внутренней энергии тела всегда связано с его взаимодействием с другими телами и с окружающей средой. В некоторых случаях, узнав, какое количество энергии теряют или получают при взаимодействии эти тела и окружающая среда, определяют изменение внутренней энергии тела. В других случаях, наоборот, по изменению внутренней энергии тела определяют, сколько энергии получила окружающая среда и другие взаимодействующие тела.
Одним из важнейших видов обмена энергией между телами и окружающей средой является теплообмен.
Теплообмен
Стоящий на столе горячий чайник через некоторое время остывает. Солнечные лучи летом заметно нагревают поверхность Земли. Металлическая ручка сковороды, стоящей на газовой плите, сильно нагревается. Все это примеры теплообмена. Обмен внутренней энергией между телами и окружающей средой или между частями тела без совершения механической работы называется теплообменом.
Обмен энергией при теплообмене обусловлен множеством актов отдельных взаимодействий между молекулами, иначе говоря, множеством микропроцессов. Например, остывание горячей воды в воздухе объясняется обменом энергией между молекулами воды и воздуха при их столкновениях. При этом нагревание воздуха и остывание воды обусловлено тем, что при большинстве таких столкновений молекулы воды теряют энергию, а молекулы воздуха приобретают ее. Однако при отдельных столкновениях молекулы воздуха могут терять энергию, а молекулы воды — приобретать, так как у некоторых молекул величина энергии может значительно отличаться от ее среднего значения (§3.4). Такие случаи будут происходить тем чаще, чем ближе станут температуры воды и воздуха. А при равенстве их температур случаи увеличения и уменьшения энергии молекул воздуха при столкновениях с молекулами воды будут равновероятны и никакой передачи энергии от воды к воздуху или обратно в целом происходить не будет.
Таким образом, при теплообмене большинство актов молекулярного взаимодействия способствует передаче энергии от тела с большей температурой к телу с меньшей температурой и ведет к выравниванию температур этих тел.
В силу исторических условий изменение внутренней энергии тела при теплообмене часто называют переданным или полученным количеством теплоты  . Если в процессе теплообмена внутренняя энергия тела увеличилась на
. Если в процессе теплообмена внутренняя энергия тела увеличилась на  , то говорят, что тело получило количество теплоты
, то говорят, что тело получило количество теплоты  . Если же при этом происходит уменьшение энергии тела на
. Если же при этом происходит уменьшение энергии тела на  , то говорят, что тело отдало количество теплоты
, то говорят, что тело отдало количество теплоты  . Следовательно, величина
. Следовательно, величина  является числовым выражением энергии, переданной или полученной телом в процессе теплообмена. Это означает, что количество теплоты
является числовым выражением энергии, переданной или полученной телом в процессе теплообмена. Это означает, что количество теплоты  должно измеряться в таких же единицах, как энергия или работа. В СИ единицей количества теплоты служит джоуль (Дж.) (Раньше единицей теплоты служили калория (кал) и килокалория (ккал) (§ 6.7).)
должно измеряться в таких же единицах, как энергия или работа. В СИ единицей количества теплоты служит джоуль (Дж.) (Раньше единицей теплоты служили калория (кал) и килокалория (ккал) (§ 6.7).)
Подчеркнем, что количество теплоты  является мерой изменения внутренней энергии тел в процессе теплообмена и существенно зависит от рода процесса. Это означает, что о количестве теплоты можно говорить только в связи с каким-либо процессом. Когда же тело находится в каком-то определенном состоянии, то ни о каком количестве теплоты в теле речи быть не может. В этом случае можно говорить лишь о внутренней энергии тела.
является мерой изменения внутренней энергии тел в процессе теплообмена и существенно зависит от рода процесса. Это означает, что о количестве теплоты можно говорить только в связи с каким-либо процессом. Когда же тело находится в каком-то определенном состоянии, то ни о каком количестве теплоты в теле речи быть не может. В этом случае можно говорить лишь о внутренней энергии тела.
Виды теплообмена
Теплообмен в природе осуществляется с помощью теплопроводности, конвекции и излучения (лучепоглощения и лучеиспускания).
Механизм теплопроводности фактически объяснен в предыдущем параграфе. Приведем еще одни пример. При нагревании конца металлического стержня его молекулы начинают двигаться быстрее, т. е. внутренняя энергия этого конца возрастает. Так как на другом конце стержня молекулы движутся медленнее, то внутри стержня с помощью хаотического движения атомов и электронов происходит передача внутренней энергии от горячего к холодному концу. Передача внутренней энергии от одних частей вещества к другим, обусловленная хаотическим движением молекул и других частиц вещества, называется теплопроводностью.
Среди различных видов вещества наилучшей теплопроводностью обладают металлы. Это объясняется тем, что в них находятся свободные электроны, Отметим еще, что теплопроводность вещества в твердом состоянии больше, чей в жидком, а в жидком больше, чей в газообразном. (Объясните, почему.)
Рассмотрим сущность конвекции. Чтобы показать плохую теплопроводность воды, обычно сосуд с водой нагревают сверху. При этом вверху вода может закипеть, а внизу останется холодной. Однако если сосуд нагревать снизу, то вода нагревается равномерно во всем объеме. Объясняется это тем, что вода при нагревании расширяется и ее плотность уменьшается. Если нагретая вода находится внизу, то верхние, более плотные слои воды под действием силы тяжести опускаются и вытесняют теплую воду вверх. Такое перемешивание воды будет происходить до тех пор, пока вся вода не закипит. Теплообмен, который происходит при перемешивании неравномерно нагретых слоев жидкости или газа под действием силы тяжести, называется конвекцией. Нетрудно сообразить, что в космическом корабле при состоянии невесомости конвекция отсутствует. (Подумайте, почему морозильная камера в холодильниках укрепляется вверху, а не внизу.)
Может показаться, что конвекцию нельзя причислять к теплообмену, так как она связана с работой силы тяжести. Однако при конвекции увеличение внутренней энергии жидкости или газа происходит только за счет подводимого извне тепла, а действие силы тяжести сводится только к ускорению равномерного прогрева жидкости или газа. Дополнительного вклада во внутреннюю энергию жидкости или газа действие силы тяжести при конвекции не дает. Поэтому конвекцию относят к теплообмену.
Теплообмен между Солнцем и Землей осуществляется посредством электромагнитного излучения. Электромагнитное излучение создается’ движением электрических зарядов и резко возрастает при повышении температуры. Излучение тела, которое определяется только его температурой, называется тепловым излучением.
Процесс излучения происходит за счет внутренней энергии тела. Когда излучение поглощается каким-либо другим телом, то внутренняя энергия тела увеличивается за счет энергии поглощенного излучения. Таким образом, посредством излучения происходит передача энергии от более нагретых тел к менее нагретым. Этот вид теплообмена происходит и при отсутствии вещества между телами.
Изменение внутренней энергии при нагревании и охлаждении
Выясним, как можно вычислять изменение внутренней энергии при теплообмене. Чтобы возможно точнее это сделать, нужно свести к минимуму неучтенные потери теплоты при теплообмене. Поэтому при научных исследованиях теплообмен осуществляют в калориметре (рис. 6.1), применение которого позволяет достаточно точно определять теплоту  , отданную или полученную телом в процессе теплообмена.
, отданную или полученную телом в процессе теплообмена.

Калориметр состоит из двух сосудов: внешнего и внутреннего. Внутренний сосуд делается из хорошего проводника тепла (латуни, меди), так как его температура должна быть такой же, как у налитой в него жидкости. Наружный сосуд предохраняет внутренний сосуд от потерь тепла путем конвекции и излучения. Поэтому его обычно окрашивают белой краской или делают из блестящей жести. Чтобы предохранить внутренний сосуд от потерь тепла путем теплопроводности, его ставят на деревянные подставки (у дерева плохая теплопроводность). Во внутренний сосуд помещают мешалку (из такого же материала, как сосуд) и термометр.
Теплообмен осуществляют следующим образом. С помощью весов определяют массу внутреннего сосуда калориметра и мешалки, а затем и массу налитой в него жидкости, например воды. После этого измеряют массу тела, нагревают его до известной температуры и, заметив начальную температуру жидкости, опускают нагретое тело в калориметр. Измерив конечную температуру жидкости, можно подсчитать, сколько теплоты отдало тело в процессе теплообмена.
С помощью таких опытов легко установить, что изменение внутренней энергии какого-либо тела прямо пропорционально его массе т и изменению температуры тела  :
:

здесь с — коэффициент пропорциональности. Поскольку изменение внутренней энергии при теплообмене оценивается количеством теплоты  , имеем
, имеем

Начальную температуру тела обычно обозначают  , а конечную
, а конечную  . Тогда в случае нагревания тела
. Тогда в случае нагревания тела  , а в случае охлаждения
, а в случае охлаждения  .
.
Опыты показывают, что  зависит от рода вещества, от внешних условий, от агрегатного состояния вещества. Эти зависимости и выражаются коэффициентом с в формулах (6.1) и (6.2).
зависит от рода вещества, от внешних условий, от агрегатного состояния вещества. Эти зависимости и выражаются коэффициентом с в формулах (6.1) и (6.2).
Величина с, характеризующая зависимость изменения внутренней энергии тела при нагревании или охлаждении от рода вещества и от внешних условий, называется удельной теплоемкостью вещества. Удельная теплоемкость вещества измеряется количеством теплоты, необходимым для нагревания единицы массы вещества на единицу температуры:

Выведем единицу удельной теплоемкости в СИ:

В СИ за единицу удельной теплоемкости принимается удельная теплоемкость такого вещества, для которого при нагревании массы в 1 кг на 1 К затрачивается 1 Дж энергии. При небольших изменениях температуры удельную теплоемкость можно считать постоянной. Для решения задач ее берут из таблиц.
Следует иметь в виду, что при определении количества теплоты, необходимой для нагревания или выделенной при охлаждении тела, иногда пользуются теплоемкостью тела С — величиной, измеряемой количеством теплоты, необходимым для нагревания тела на единицу температуры. Следовательно,

Пользоваться при расчетах теплоемкостью всего тела особенно удобно, когда отдельные части тела сделаны из разного вещества. В СИ за единицу теплоемкости тела принимается 1 Дж/К. (Покажите это с помощью формулы (6.3).)
Отметим еще, что удельная теплоемкость газа зависит от характера процесса, при котором происходит его нагревание. Например, удельная теплоемкость газа при постоянном давлении  больше его удельной теплоемкости при постоянном объеме
больше его удельной теплоемкости при постоянном объеме  , так как в первом случае нужно не только увеличить внутреннюю энергию газа, но и затратить энергию на выполнение работы, совершаемой газом над внешними телами в процессе его расширения (§ 5.10). Во втором же случае подведенная к газу теплота идет только на увеличение его внутренней энергии.
, так как в первом случае нужно не только увеличить внутреннюю энергию газа, но и затратить энергию на выполнение работы, совершаемой газом над внешними телами в процессе его расширения (§ 5.10). Во втором же случае подведенная к газу теплота идет только на увеличение его внутренней энергии.
Уравнение теплового баланса при теплообмене
Вспомним, что при отсутствии механической работы изменение внутренней энергии тела оценивают количеством теплоты  . Так как при чистом теплообмене никаких других видов изменений внутренней энергии нет, то на основании закона сохранения энергии можно утверждать, что в этом случае сколько теплоты отдадут одни тела, столько же приобретут другие. На этом основании составляется уравнение теплового баланса, c помощью которого делаются все расчеты. Итак, при теплообмене сумма количеств теплоты, отданных всеми телами, у которых внутренняя энергия уменьшается, равна сумме количеств теплоты, полученных всеми телами, у которых внутренняя энергия увеличивается:
. Так как при чистом теплообмене никаких других видов изменений внутренней энергии нет, то на основании закона сохранения энергии можно утверждать, что в этом случае сколько теплоты отдадут одни тела, столько же приобретут другие. На этом основании составляется уравнение теплового баланса, c помощью которого делаются все расчеты. Итак, при теплообмене сумма количеств теплоты, отданных всеми телами, у которых внутренняя энергия уменьшается, равна сумме количеств теплоты, полученных всеми телами, у которых внутренняя энергия увеличивается:

Теплообмен происходит до тех пор, пока температуры тел не сравняются. Общую температуру, которая получается после окончания теплообмена, обозначают  (греч. «тэта»).
(греч. «тэта»).
Для примера составим уравнение теплового баланса, которое используется при определении удельной теплоемкости вещества с помощью калориметра. Приближенно можно считать, что в этом случае в теплообмене участвуют три тела: калориметр, жидкость и тело, удельную теплоемкость вещества которого определяют. Это тело предварительно нагревают до известной температуры  и опускают в калориметр с жидкостью, температура которого
и опускают в калориметр с жидкостью, температура которого  . Через некоторое время в калориметре устанавливается общая конечная температура тел
. Через некоторое время в калориметре устанавливается общая конечная температура тел  . Тогда можно утверждать, что в процессе теплообмена тело отдало количество теплоты
. Тогда можно утверждать, что в процессе теплообмена тело отдало количество теплоты  , а калориметр и жидкость получили соответственно
, а калориметр и жидкость получили соответственно  и
и  . Поэтому
. Поэтому

Поскольку

имеем

или

Подставляя в правую часть последней формулы числовые значения величин, полученные из опыта, вычисляют удельную теплоемкость вещества тела.
Подсчет теплоты, выделяемой при сжигании топлива. К. П. Д. нагревателя
Внутренняя энергия тела частично может освобождаться, когда с веществом тела происходит химическая реакция. Особенно много теплоты выделяется при реакции горения. Вещества, которые используют для получения теплоты, называют топливом. Энергию, выделяемую при сгорании топлива, широко используют на производстве, на транспорте и в быту. Топливо бывает твердое, жидкое и газообразное.
Опыт показывает, что количество теплоты  , выделяемое при сжигании определенного сорта топлива, прямо пропорционально массе т сгоревшего топлива:
, выделяемое при сжигании определенного сорта топлива, прямо пропорционально массе т сгоревшего топлива:

Теплота  зависит от вида топлива. Эта зависимость выражается коэффициентом пропорциональности
зависит от вида топлива. Эта зависимость выражается коэффициентом пропорциональности  в (6.4).
в (6.4).
Величина  характеризующая зависимость теплоты, выделяющейся при сжигании топлива, от его вида, называется удельной теплотой сгорания или калорийностью топлива. Удельная теплота сгорания измеряется количеством теплоты, выделенным при полном сгорании единицы массы топлива:
характеризующая зависимость теплоты, выделяющейся при сжигании топлива, от его вида, называется удельной теплотой сгорания или калорийностью топлива. Удельная теплота сгорания измеряется количеством теплоты, выделенным при полном сгорании единицы массы топлива:

Найдем единицу удельной теплоты сгорания  в СИ:
в СИ:

Формула (6.4) удобна для вычисления теплоты, выделяемой при сжигании твердого и жидкого топлива. Расход газообразного топлива удобнее выражать не массой, а объемом сгоревшего газа. Поскольку давление газа в газопроводе повышено, газовые счетчики устраиваются так, что они показывают объем израсходованного газа, приведенный к нормальным условиям —  . Так как количество теплоты
. Так как количество теплоты  , выделенное при сжигании газа, прямо пропорционально
, выделенное при сжигании газа, прямо пропорционально  , то
, то

Здесь  (греч. «каппа») — удельная теплота сгорания газообразного топлива, которая зависит от природы газа. За удельную теплоту сгорания газообразного топлива принимают количество теплоты, выделенное при полном сгорании единицы объема газа, приведенного к нормальным условиям:
(греч. «каппа») — удельная теплота сгорания газообразного топлива, которая зависит от природы газа. За удельную теплоту сгорания газообразного топлива принимают количество теплоты, выделенное при полном сгорании единицы объема газа, приведенного к нормальным условиям:

(Покажите, что в СИ  измеряют в Дж/м3.)
измеряют в Дж/м3.)
Отметим, что потребность в топливе часто выражают в тоннах условного топлива, удельная теплота сгорания которого принята равной 29,3 .106 Дж/кг.
Топливо сжигают в печах, топках, форсунках и т. д., которые условно называют нагревателями. Тип устройства для сжигания топлива в основном определяется видом топлива и назначением выделенной теплоты. Полностью использовать теплоту, выделяющуюся в нагревателях, не удается, так как часть теплоты уносится с продуктами сгорания и рассеивается в окружающей среде.
Величина  , характеризующая эффективность устройства для сжигания топлива, называется коэффициентом полезного действия этого устройства (к. п. д.). Коэффициент полезного действия нагревателя показывает, какую часть количества теплоты выделенного при сжигании топлива, составляет полезно использованная теплота
, характеризующая эффективность устройства для сжигания топлива, называется коэффициентом полезного действия этого устройства (к. п. д.). Коэффициент полезного действия нагревателя показывает, какую часть количества теплоты выделенного при сжигании топлива, составляет полезно использованная теплота  :
:

Отметим, что величина  всегда находится по формулам (6.4) и (6.5), а
всегда находится по формулам (6.4) и (6.5), а  зависит от назначения устройства для сжигания топлива и может быть выражена различными формулами.
зависит от назначения устройства для сжигания топлива и может быть выражена различными формулами.
Изменение внутренней энергии при выполнении механической работы
Опыт Джоуля. Внутренняя энергия может изменяться не только при теплообмене, но и при выполнении механической работы. Например, при пилке дров происходит нагревание пилы. При сверлении механической детали сверло и деталь сильно нагреваются. Резец токарного станка при обработке деталей становится горячим. Такого рода примеров можно привести очень много. Все они показывают, что когда совершается механическая работа А по преодолению трения или разрушению материала, то происходит нагревание тел, т. е. увеличение их внутренней энергии, аналогичное тому, какое происходит при получении этими телами некоторого количества теплоты  . Поэтому говорят, что в приведенных выше примерах происходит превращение работы в теплоту, т. е. происходит превращение механической энергии тел (которая не входит в их внутреннюю энергию) во внутреннюю энергию.
. Поэтому говорят, что в приведенных выше примерах происходит превращение работы в теплоту, т. е. происходит превращение механической энергии тел (которая не входит в их внутреннюю энергию) во внутреннюю энергию.
Если с помощью механической работы можно получить неограниченное количество теплоты, то возникает вопрос: существует ли при этом между механической работой и теплотой определенное количественное соотношение? Иначе говоря, всегда ли за счет одинакового количества работы получается одно и то же количество теплоты? Для ответа на этот вопрос английский ученый Д. Джоуль выполнил серию опытов, которые дали утвердительный ответ. Свой первый опыт он произвел в 1843 г.
На рис. 6.2 изображена схема одного из опытов Джоуля. Установка состояла из калориметра с ртутью.

Через калориметр проходила ось, заканчивавшаяся валиком с ручкой. На валик наматывалась нить, к концам которой были прикреплены равные грузы массой т каждый. Рядом с грузами укреплялись линейки, с помощью которых измеряли перемещение грузов. Для усиления трения при движении грузов внутри калориметра делались выступы, а к оси прикреплялись лопасти.
Перед началом опыта с помощью ручки грузы поднимали в верхнее положение и измеряли температуру ртути. Затем ручка освобождалась, и при движении вниз грузы приводили во вращение лопасти внутри калориметра. При этом, вследствие большого трения между лопастями и ртутью, в калориметре выделялось тепло за счет работы, совершаемой при движении грузов на некотором пути h. Поскольку трение в других частях установки было ничтожно малым, можно считать, что в этом опыте увеличение внутренней энергии калориметра равно уменьшению механической энергии грузов в процессе их движения. В то время закон сохранения энергии еще не был твердо установлен, но Джоуль считал, что количество теплоты  , выделенное в калориметре, равно работе грузов
, выделенное в калориметре, равно работе грузов  .
.
Такого рода опытами Джоулю удалось доказать, что количество теплоты, выделенное при трении, прямо пропорционально произведенной работе.
По современным данным, для нагревания 1 кг воды от 292,5 К до 293,5 К, т. е. на 1 К, требуется 4186,8 Дж энергии. Это означает, что удельная теплоемкость воды

Отметим, что до опытов Джоуля с помощью теплообмена можно было находить только относительные удельные теплоемкости, т. е. узнавать, во сколько раз удельная теплоемкость одного вещества больше удельной теплоемкости другого. При этом удельная теплоемкость воды условно принималась за единицу. Количество теплоты, нужное для нагревания 1 кг воды на 1°С, было названо килокалорией (ккал). Удельная теплоемкость воды выражалась следующим образом:

Таким образом, на основании опытов Джоуля имеем

Из этого соотношения вытекает связь между килокалорией и джоулем:

В XVIII в. для объяснения тепловых явлений пользовались теорией теплорода. Ученые предполагали, что существует особый невесомый вид материи — теплород, количество которого в природе неизменно. Считалось,’ что при охлаждении тела теплород перетекает из тела в окружающую среду, а при нагревании тела в него перетекает теплород из других тел.
Одним из первых выступил против теории теплорода М. В. Ломоносов (1711— 1765 гг.), который объяснял тепловые явления движением невидимых частиц тела. В 1798 г. англичанин Б. Румфорд показал, что при сверлении пушечных стволов теплота может быть получена в неограниченном количестве (за счет механической работы). Эти исследования Румфорда доказали несостоятельность теории теплорода. Не менее важными для опровержения теории теплорода были и исследования французского ученого С. Карно, который создал теорию работы тепловых машин.
Закон сохранения и превращения энергии в механике
Назовем процессы, при которых не происходит превращения механического движения в другие формы движения материи, чисто механическими. Система, в которой происходят чисто механические процессы, называется консервативной. Эта система является идеализированной, так как в ней отсутствуют силы трения и другие сопротивления, приводящие к рассеянию механической энергии, т. е. к ее превращению в другие формы энергии. В консервативной системе может происходить только превращение кинетической энергии в потенциальную и обратно. Работа сил, действующих на тело в консервативной системе, не зависит от формы пути, а определяется только начальным и конечным положением тела. Напомним, что примером такого рода сил является сила тяжести. Из сказанного следует, что в консервативной системе работа силы на замкнутом пути равна нулю.
Для такой системы справедлив закон сохранения энергии в следующей форме: в замкнутой консервативной системе сумма кинетической и потенциальной энергий всех тел, составляющих систему, есть величина постоянная. Если обозначить эту сумму Е, то при отсутствии внешних воздействий на консервативную систему

Например, при свободном падении тела сумма его кинетической и потенциальной энергий остается постоянной.
Вспомним, что единственной мерой передачи механической энергии от одного тела к другому является работа А. Поэтому, если механическая энергия консервативной системы в каком-либо состоянии равна , а затем внешние силы совершают над этой системой работу А, то энергия системы увеличивается на А и в новом состоянии становится равной
, а затем внешние силы совершают над этой системой работу А, то энергия системы увеличивается на А и в новом состоянии становится равной  . Следовательно, в этом случае
. Следовательно, в этом случае

Напомним еще, что в более широком смысле механическая работа А при любых явлениях природы служит единственной мерой передачи и превращения механического движения в другие формы движения материи и обратно.
Закон сохранения и превращения энергии в механических и тепловых процессах
Было объяснено, что механическая энергия сохраняется только при отсутствии трения’ и других сопротивлений. Действие сил трения ведет к уменьшению механической энергии. Действительно, после выключения двигателя автомобиль постепенно теряет кинетическую энергию и останавливается; скатившись с горы, санки постепенно теряют скорость и т. д. Нетрудно сообразить, что бесследное исчезновение энергии в такого рода случаях является лишь кажущимся: при этом всегда происходит выделение некоторого количества теплоты. Таким образом, при трении и вообще при любом сопротивлении движению происходит превращение механической энергии во внутреннюю энергию.
Как известно, мерой уменьшения механической энергии в подобного рода случаях является работа А, а мерой увеличения внутренней энергии — полученная теплота  . Опыты Джоуля доказали, что А и
. Опыты Джоуля доказали, что А и  при этом прямо пропорциональны друг другу, а если их измерять в одинаковых единицах (в джоулях), то и равны друг другу. Следовательно, уменьшение механической энергии тел при действии сил трения в точности равно увеличению внутренней энергии всех тел, участвующих в таком процессе.
при этом прямо пропорциональны друг другу, а если их измерять в одинаковых единицах (в джоулях), то и равны друг другу. Следовательно, уменьшение механической энергии тел при действии сил трения в точности равно увеличению внутренней энергии всех тел, участвующих в таком процессе.
Это означает, что сумма механической и внутренней энергий всех тел, составляющих замкнутую систему, есть величина постоянная. Иначе говоря, суммарное изменение механической и внутренней энергий всех тел замкнутой системы в любом процессе, найденное по выполненной работе и переданной теплоте, равно нулю.
Изучение явлений природы показало, что изменение энергии тела происходит только при выполнении работы и при теплообмене. Следовательно, работа и количество теплоты — единственно возможные формы обмена энергией между телами. Таким образом, переданное телу количество теплоты  и выполненная этим телом работа А над другими телами однозначно определяют изменение его внутренней энергии в любом процессе.
и выполненная этим телом работа А над другими телами однозначно определяют изменение его внутренней энергии в любом процессе.
Немецкий врач Р. Майер в 1842 г. обратил внимание на взаимную превращаемость всех форм движения материи друг в друга и пытался распространить принцип сохранения энергии на все явления природы. Однако научно обосновал этот принцип в 1847 г. немецкий ученый Г. Гельмгольц.
Сформулируем теперь закон сохранения и превращения энергии: энергия замкнутой системы никогда не исчезает и не создается из ничего. При всех явлениях внутри системы она только превращается из одного вида в другой или передается от одного тела к другому, не изменяясь количественно.
Закон сохранения энергии является всеобщим законом природы, на котором базируется все современное естествознание. С его помощью проверяются новые теории и оцениваются результаты новых экспериментов. Нарушение этого закона в каких-либо явлениях природы привело бы к полной перестройке всех естественных наук и к изменению нашего миропонимания.
Первое начало термодинамики
Весьма важным способом изучения тепловых процессов служит термодинамический метод. Сущность этого метода заключается в следующем. При выполнении экспериментов измеряют числовые значения макроскопических величин, характеризующих изучаемый процесс. Их часто называют термодинамическими параметрами (§ 5.1). По результатам таких экспериментов находят закономерную связь между параметрами, а затем производят математический анализ этой связи на основе всеобщих законов природы, в справедливости которых нет никаких сомнений. Всеобщие законы природы, на основе которых проводят такой анализ, называют началами термодинамики.
Чтобы успешно проводить анализ связей между параметрами, математические выражения начал термодинамики должны иметь специфический, удобный для такого анализа вид. Поскольку все выводы термодинамики делают на основе экспериментов и незыблемых законов природы, они всегда оказываются верными. Термодинамический метод изучения природы позволяет предсказать ход многих явлений, но не дает наглядной модели, объясняющей физический смысл происходящих явлений. Этот недостаток термодинамического метода восполняет молекулярно-кинетическая теория, которая объясняет многие явления с помощью таких моделей. Таким образом, оба эти важнейших метода исследования явлений дополняют друг друга и совместно помогают нам глубоко осмыслить происходящие процессы.
Первым всеобщим законом природы, на основе которого строится термодинамика, является закон сохранения энергии. Его называют первым началом термодинамики и формулируют следующим образом: подведенное к системе количество теплоты  частично идет на увеличение внутренней энергии системы
частично идет на увеличение внутренней энергии системы  и частично — на совершение этой системой работы А:
и частично — на совершение этой системой работы А:

Отметим, что система, к которой применима формула (6.9), может состоять из одного тела. Напомним еще, что работа А в (6.9) численно равна энергии, переданной системой окружающим телам в форме механического движения.
Применение первого начала термодинамики к изопроцессам в идеальном газе
Выясним, какой вид принимает формула (6.9) для различных изопроцессов в идеальном газе. Мы уже знаем, что при изохорическом процессе работа газа А равна нулю. Следовательно, формула (6.9) для этого процесса принимает вид

Это означает, что при изохорическом процессе все подведенное к газу количество теплоты идет на увеличение его внутренней энергии.
Для изобарического процесса формула первого начала термодинамики имеет вид (6.9):

Действительно, в этом случае  отлично от нуля, так как объем газа непостоянен (§5.10). Изменение внутренней энергии
отлично от нуля, так как объем газа непостоянен (§5.10). Изменение внутренней энергии  , которое пропорционально приросту температуры, тоже отлично от нуля, поскольку температура газа в этом процессе изменяется. Таким образом, при изобарическом процессе подведенное к газу количество теплоты частично идет на увеличение его внутренней энергии, а частично тратится на выполнение работы газом в процессе его расширения.
, которое пропорционально приросту температуры, тоже отлично от нуля, поскольку температура газа в этом процессе изменяется. Таким образом, при изобарическом процессе подведенное к газу количество теплоты частично идет на увеличение его внутренней энергии, а частично тратится на выполнение работы газом в процессе его расширения.
При изотермическом процессе температура газа не изменяется. Поэтому на основании формул (5.22)—(5.24) можно утверждать, что в этом случае внутренняя энергия газа остается постоянной, т. е.  . Следовательно, формула (6.9) для этого процесса имеет вид:
. Следовательно, формула (6.9) для этого процесса имеет вид:

Это означает, что при изотермическом процессе все подведенное к газу количество теплоты идет на выполнение газом работы.
Анализ формулы (6.9) показывает, что с газом может происходить еще один важный процесс, при котором  =0. Этот процесс имеет большое практическое значение.
=0. Этот процесс имеет большое практическое значение.
Адиабатный процесс
Процесс в какой-либо системе, который происходит без обмена теплом с окружающей средой, называется адиабатным. Так как при таком процессе  =0, то формула (6.9) для него имеет вид
=0, то формула (6.9) для него имеет вид

Это означает, что при адиабатном процессе система может выполнять работу над внешними телами только за счет своей внутренней энергии. Наоборот, когда при адиабатном процессе внешние тела совершают работу над системой, то ее внутренняя энергия увеличивается.
Если газ при адиабатном расширении совершает работу над окружающей средой, то его внутренняя энергия уменьшается. Следовательно, в этом случае газ должен охлаждаться. (Подумайте, охладится ли газ, если он будет адиабат-но расширяться в вакуум.) Очевидно, что при адиабатном сжатии газ должен нагреваться. График адиабатного процесса в координатах р и V изображен на рис.6.3.

Он называется адиабатой. Для сравнения на рис. 6.3 изображена одна из изотерм для этой же массы идеального газа. С помощью формулы (4.9):  — нетрудно объяснить, почему адиабата идет круче, чем изотерма. При изотермическом сжатии газа р растет вследствие увеличения числа молекул в единице объема
— нетрудно объяснить, почему адиабата идет круче, чем изотерма. При изотермическом сжатии газа р растет вследствие увеличения числа молекул в единице объема  (Т не изменяется), а при адиабатном сжатии увеличиваются и
(Т не изменяется), а при адиабатном сжатии увеличиваются и  , и Т, поэтому р растет быстрее.
, и Т, поэтому р растет быстрее.
В реальных условиях адиабатный процесс осуществить невозможно, так как в природе не существуют идеальные тепловые изоляторы. Однако при хорошей тепловой изоляции процесс в газе может быть близок к адиабатному, особенно если он протекает в течение короткого времени, так как при этом заметного обмена теплотой между газом и окружающей средой не успеет произойти. Поэтому любой газ при быстром сжатии нагревается, а при быстром расширении охлаждается.
Это можно показать на следующем опыте. Возьмем стеклянную бутыль с узким горлом и нальем в нее немного воды. Заткнем бутыль резиновой пробкой, в которой имеется трубка, соединенная с нагнетающим насосом, и будем накачивать в бутыль воздух. При этом вода в бутыли исчезает. Следовательно, температура воздуха в бутыли повысилась. При достаточно большом давлении пробка вылетает и в бутыли появляется туман, что свидетельствует об охлаждении воздуха при расширении.
При быстром несильном сжатии газ может нагреваться очень сильно. Если при этом в газе находятся пары бензина или других горючих веществ, то они воспламеняются. Это явление используют в двигателях Дизеля для зажигания горючей смеси.
Понятие о строении солнца и звезд
Солнце является типичной звездой и представляет собой гигантский газовый шар. По своим физическим характеристикам Солнце — средняя звезда с массой около 2 . 1030 кг и радиусом 7 . 108 м.
Солнце состоит в основном из водорода (~70% по массе) и гелия (~29%). (Водорода по числу атомов в 10 раз больше, чем остальных элементов.) Масса Солнца в 330 ООО раз больше массы Земли, и огромное гравитационное притяжение сильно сжимает эти газы. Вычислив объем солнечного шара, можно подсчитать, что средняя плотность солнечного вещества составляет 1,4 . 103 кг/м3, т. е. больше плотности воды. По направлению к центру давление вышележащих слоев растет и плотность газа увеличивается, достигая в центре Солнца около 1,5 . 105 кг/м3, что более чем в 10 раз превышает плотность свинца.
Солнце излучает в мировое пространство ежесекундно огромное количество энергии. Источником этой энергии являются термоядерные реакции, которые протекают в его недрах. Температура в центре Солнца достигает 13 . 106 К и постепенно уменьшается по мере удаления от центра.
Передача энергии из недр Солнца осуществляется главным образом излучением. Излучение внутренних слоев поглощается вышележащими слоями, которые в свою очередь посредством излучения передают энергию следующим слоям, и так далее, до слоя, излучение которого прорывается, наконец, наружу, в космическое пространство.
Слой, в котором образуется видимое излучение Солнца, называемый фотосферой, мы наблюдаем как солнечный диск. Толщина фотосферы составляет несколько сотен километров, давление — порядка 0,1 атм. Температура внутренних слоев фотосферы около 6000 К и уменьшается до 4500 К в ее внешнем слое. Фотосфера составляет нижний слой атмосферы Солнца. Над ней расположена хромосфера, а самую наружную разреженную часть атмосферы называют короной (рис. 6.4).

Газ в хромосфере и короне очень сильно разрежен: в верхних слоях хромосферы содержится только около 1015 атомов/м3, а в короне — еще на порядок меньше (сравните с атмосферой Земли:  = 2,7 . 1025 молекул/м3).
= 2,7 . 1025 молекул/м3).
Теряя энергию на излучение в мировое пространство, газ в фотосфере быстро охлаждается, и в слое, лежащем под фотосферой, происходит вертикальное перемешивание — конвекция. При наблюдении в телескоп видно, что фотосфера состоит из множества гранул — небольших облаков более горячего газа, которые поднимаются из глубины, вытесняя остывший газ, и через несколько минут распадаются, заменяясь новыми. Иногда образуются устойчивые восходящие потоки горячих газов, которые называют факелами. Они видны в виде более ярких областей. Время от времени в фотосфере появляются темные пятна, представляющие собой более холодные области. Кстати, по движению этих пятен было обнаружено вращение Солнца.
Под действием мощных конвективных движений в солнечном веществе возникают механические колебания и образуются волны, похожие на звуковые. По мере распространения этих волн в верхние слои атмосферы, где газ сильно разрежен, амплитуда (размах) колебаний частиц газа увеличивается до нескольких километров и сильно увеличиваются скорости колебательного движения частиц. Однако такие колебания не могут долго сохранять правильный характер, и волнообразные движения протяженных областей газа разбиваются на отдельные мелкие беспорядочно движущиеся массы газа. В результате за счет механической энергии волн сильно возрастает средняя энергия хаотического движения частиц газа, и температура увеличивается в хромосфере до десятков тысяч Кельвинов, а в короне — до 106 К *).
*) См, замечание о кинетической температуре в § 3.10.
Вследствие очень низкой плотности вещества яркость короны в миллион раз меньше, чем фотосферы, и не превышает яркости Луны. Корону удобно наблюдать во время полного солнечного затмения, когда Луна закрывает от нас яркий диск фотосферы. Корона имеет лучистую структуру, причем длина лучей может более чем в десять раз превышать радиус фотосферы.
Кинетическая энергия частиц газа в короне- так велика, что многие из них преодолевают притяжение Солнца и улетают в межпланетное пространство. Поток этих частиц, движущихся со скоростью в сотни км/с, называют солнечным ветром. Заметим, что солнечный ветер, а также давление света вызывают образование «хвоста кометы», который всегда направлен в сторону от Солнца.
Услуги по физике:
- Заказать физику
- Заказать контрольную работу по физике
- Помощь по физике
Лекции по физике:
- Физические величины и их измерение
- Основные законы механики
- Прямолинейное равномерное движение
- Прямолинейное равнопеременное движение
- Сила
- Масса
- Взаимодействия тел
- Механическая энергия
- Импульс
- Вращение твердого тела
- Криволинейное движение тел
- Колебания
- Колебания и волны
- Механические колебания и волны
- Бегущая волна
- Стоячие волны
- Акустика
- Звук
- Звук и ультразвук
- Движение жидкости и газа
- Молекулярно-кинетическая теория
- Молекулярно-кинетическая теория строения вещества
- Молекулярно – кинетическая теория газообразного состояния вещества
- Теплота и работа
- Температура и теплота
- Термодинамические процессы
- Идеальный газ
- Уравнение состояния идеального газа
- Переход вещества из жидкого состояния в газообразное и обратно
- Кипение, свойства паров, критическое состояние вещества
- Водяной пар в атмосфере
- Плавление и кристаллизация
- Тепловое расширение тел
- Энтропия
- Процессы перехода из одного агрегатного состояния в другое
- Тепловое расширение твердых и жидких тел
- Свойства газов
- Свойства жидкостей
- Свойства твёрдых тел
- Изменение агрегатного состояния вещества
- Тепловые двигатели
- Электрическое поле
- Постоянный ток
- Переменный ток
- Магнитное поле
- Электромагнитное поле
- Электромагнитное излучение
- Электрический заряд (Закон Кулона)
- Электрический ток в металлах
- Электрический ток в электролитах
- Электрический ток в газах и в вакууме
- Электрический ток в полупроводниках
- Электромагнитная индукция
- Работа, мощность и тепловое действие электрического тока
- Термоэлектрические явления
- Распространение электромагнитных волн
- Интерференционные явления
- Рассеяние
- Дифракция рентгеновских лучей на кристалле
- Двойное лучепреломление
- Магнитное поле и электромагнитная индукция
- Электромагнитные колебания и волны
- Природа света
- Распространение света
- Отражение и преломление света
- Оптические приборы и зрение
- Волновые свойства света
- Действия света
- Линзы и получение изображений с помощью линз
- Оптические приборы и глаз
- Фотометрия
- Излучение и спектры
- Квантовые свойства излучения
- Специальная теория относительности в физике
- Теория относительности
- Квантовая теория и природа поля
- Строение и свойства вещества
- Физика атомного ядра
- Строение атома
- Подробности
- Обновлено 08.02.2019 16:27
- Просмотров: 463
Назад в “Оглавление” – смотреть
1. Что нужно знать, чтобы вычислить количество теплоты, полученное телом при нагревании или выделенное им при остывании?
Чтобы вычислить количество теплоты, полученное телом при нагревании или выделенное им при остывании, надо знать удельную теплоемкость вещества, массу тела, конечную и начальную температуру.
2.
Как рассчитывают количество теплоты, сообщённое телу при его нагревании или выделяющееся при его охлаждении?
Чтобы подсчитать количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость вещества умножить на массу тела и на разность между большей и меньшей его температурами:
Q = cm(t2-t1)
где с – удельная теплоемкость вещества (Дж/кг °С)
m – масса тела (кг)
(t2-t1) – разность конечной и начальной температур (°С)
Например:
Задача1
В железный котел массой 10 кг налита вода массой 20 кг.
Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100 °С?

Оба тела — и котел, и вода — будут нагреваться вместе.
Между ними происходит теплообмен, и их температуры можно считать одинаковыми, т. е. температура котла и воды изменяется на 100°С — 10°С=90°С.
Но количества теплоты, полученные котлом и водой, не будут одинаковыми, ведь их массы и удельные теплоемкости различны.
Задача 2
Смешали воду массой 0,8 кг, имеющую температуру 25°С, и кипяток массой 0,2 кг.
Температуру полученной смеси измерили, и она оказалась равной 40 °С.
Вычислить, какое количество теплоты отдал кипяток при остывании и получила холодная вода при нагревании.
Сравнить эти количества теплоты.

4. Какой вывод можно сделать из опыта по смешиванию холодной и горячей воды? Почему на практике эти энергии не равны?
Количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой, равны между собой.
То есть, если между телами происходит теплообмен, то внутренняя энергия всех нагревающихся тел увеличивается настолько, насколько уменьшается внутренняя энергия остывающих тел.
Однако на практике обычно получается, что отданная горячей водой энергия больше энергии, полученной холодной водой.
Это объясняется тем, что часть энергии передается окружающему воздуху, а часть энергии — сосуду, в котором смешивали воду.
Равенство отданной и полученной энергий будет тем точнее, чем меньше потери энергии.
Назад в “Оглавление” – смотреть
