.
Порядок составления формул оксидов
Формулы
оксидов можно составлять по правилу креста:

Рис.1
 Запомни при составлении
Запомни при составлении
формул первым ставят
элемент степень окисления. которого со знаком +, а
вторым элемент с отрицательной степенью окисления. Для оксидов это
всегда кислород.
Далее
необходимо:
1. расставить степени
окисления
(с.о.) для каждого атома. Кислород в оксидах всегда имеет с.о. -2
(минус два).
2. Для того чтобы
правильно
определить степень окисления. второго элемента необходимо познакомится
с таблицей возможных степеней окисления некоторых элементов:
Таблица.1 Степени окисления некоторых элементов
|
Элемент |
Возможные степени окисления |
| N (азот) | -3, 0, +1, +2, +3, +4,+5. |
| P (фосфор) | -3, 0, +3, +5. |
| S (сера) | -2, 0, +4, +6. |
| C (углерод) | -4, 0, +2, +4. |
Степень окисления «0» –
ноль имеют:
1. Простые вещества: Н2,
Са, О2 …
2. Сложные в-ва (в сумме): Са+2О-2 (+2 – 2 =0)
Степень окисления со знаком +
характерна для элементов которые отдают свои электроны в соединениях
другим атомам или от которых оттянуты общие электронные пары, т.е.атомы
менее электроотрицательных элементов. например металлы
всегда имеют положительную степени окисления.
Подсказка: Узнать степени окисления для металлов
можно в таблице “растворимости…“.
В ней представлены заряды ионов металлов они обычно совпадают со
степенью окисления.
С неметаллами кислород образует оксид, если только этот неметалл менее
электроотрицательный, чем сам кислород см. таблицу
электроотрицательности.

рис.2
 Запомни если степени
Запомни если степени
окисления.
элементов в бинарных соединениях равны по модулю, то индексы в формуле
не ставятся: Сa+2О-2.
Составим формулу
оксида натрия:
По
таблице растворимости заряд иона натрия +,
соответственно степень окисления натрия имеет значение +1 (Na+1),
с.о. кислорода в оксидах всегда -2.
Натрий
имеет положительный заряд, значит, его ставим первым, а вторым
ставим кислород и по правилу креста получим: Na2+1O-2
или Na2O.
Правило
наименьшего общего кратного
это способ наиболее универсальный для составления формул. Как им
пользоваться рассмотрим на примере.
Составить формулу
оксида серы (VI).
1.
У кислорода с.о. -2 следовательно в формуле он ставиться вторым, а
первым элементом будет сера ее с.о. указана в названии оксида VI, т. е
+6. S+6O-2.
2.
Найдем наименьшее общее кратное. Для чисел 2 и 6 это будет 6.
3.
Находим индексы и расставляем для каждого элемента. См. рисунки ниже.
6 : 6 = 1 это индекс для серы.
Индексы со значением 1 в формулах не ставятся.
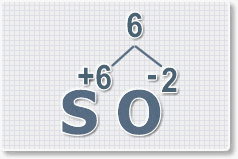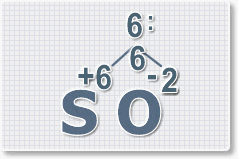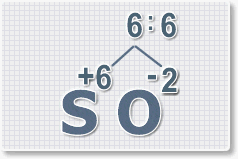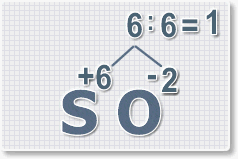
Рис.3
6 : 2 = 3
это индекс для кислорода
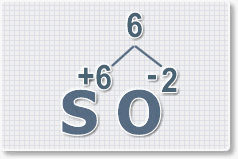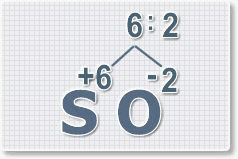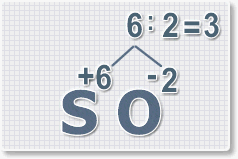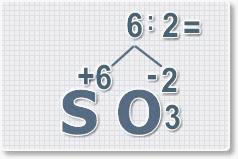
Рис.4
В результате получим
формулу оксида серы (VI):

* * *
|
§ 17 |
Валентность. Составление формул оксидов |
Вы, наверное, обратили внимание на то, что оксиды различных химических элементов по составу отличаются друг от друга. Например, на один атом кислорода в воде H2O приходятся два атома водорода, а в оксиде магния MgO — один атом магния. Как это можно объяснить?
В XIX в. учёные предположили, что атомы разных элементов обладают различной способностью присоединять к себе другие атомы. Так, атом водорода может присоединить лишь один атом другого химического элемента, кислород — два атома, азот — три. В настоящее время известно, что атомы, входящие в состав молекул, соединены между собой химическими связями в определённой последовательности. Чтобы показать это, используют структурные формулы, выражающие не только число атомов, но и последовательность их соединения. Химические связи между атомами в молекулах принято обозначать чёрточками.
Число связей, которые данный атом образует с другими атомами, называют валентностью.
Слово «валентность» в переводе с латинского означает «сила, способность».
Изобразим структурную формулу воды:

Обратите внимание на то, что атомы водорода в молекуле воды не связаны друг с другом, а соединены только с атомом кислорода. Каждый атом водорода образует одну химическую связь (от символа H отходит одна чёрточка) — он одновалентен. Атом кислорода образует две связи — он двухвалентен. Число чёрточек, отходящих от символа химического элемента в структурной формуле, и есть валентность данного атома.
Установлено, что и в других соединениях водород всегда одновалентен, т. е. атомы водорода образуют лишь одну связь. Валентность кислорода всегда равна двум.
В молекуле углекислого газа CO2 атом углерода образует с каждым атомом кислорода две двойные связи, которые равноценны четырём одинарным (четыре чёрточки в структурной формуле), следовательно, углерод в этом веществе четырёхвалентен:
O C
C O.
O.
Зная валентность одного химического элемента в соединении, можно определить валентность другого. Так, хлор в хлороводороде HCl одновалентен, азот в аммиаке NH3 трёхвалентен, а валентность углерода в метане CH4 равна четырём:

Для обозначения валентности обычно используют римские цифры, которые ставят в формуле над символом химического элемента:

Чтобы подсчитать валентность, нет необходимости каждый раз рисовать структурные формулы. Легко заметить, что в соединении общее число единиц валентности всех атомов одного элемента всегда равно общему числу единиц валентности всех атомов другого элемента. Иными словами, произведение числа атомов одного элемента на его валентность равно произведению числа атомов второго элемента на его валентность.
Таблица 4
|
Последовательность действий |
Составление формулы |
|
|
Указать валентность кислорода |
|
|
|
Умножить число атомов кислорода на численное значение его валентности (II) |
3•2 = 6 |
2•2 = 4 |
|
Разделить полученное значение на индекс, показывающий число атомов другого элемента |
6 : 2 = 3 |
4 : 1 = 4 |
|
Записать значение валентности над символом этого элемента |
|
|
Например:
 .
.
Для углерода (число атомов равно 1): IV•1 = 4;
для кислорода (число атомов равно 2): II•2 = 4.
Чтобы определить валентность элемента в оксиде по формуле, необходимо провести следующие математические вычисления (табл. 4).
Некоторые химические элементы проявляют в соединениях постоянную валентность (табл. 5), её надо запомнить, другие — переменную.
Химические элементы с постоянной валентностьюТаблица 5
|
Валентность |
Химические элементы |
|
I |
H, Na, K, Ag |
|
II |
O, Mg, Ca, Ba, Zn |
|
III |
Al |
Таблица 6
|
Последовательность действий |
Составление формулы |
|
|
Записываем символы химических элементов (кислород на втором месте) и указываем их валентность (кислород двухвалентен, валентность второго элемента либо дана в названии, либо постоянна и приведена в таблице 5) |
Оксид алюминия
|
Оксид углерода(IV)
|
|
Находим наименьшее общее кратное двух числовых значений валентности |
III и II ⇒ 6 |
IV и II ⇒ 4 |
|
Находим индексы, поделив наименьшее общее кратное на численные значения валентности данного элемента |
6 : 3 = 2 (Al) 6 : 2 = 3 (O) |
4 : 4 = 1 (C) 4 : 2 = 2 (O) |
|
Записываем индексы после знаков химических элементов |
Al2O3 |
CO2 |
Обратите внимание, что значения валентности многих металлов совпадают с номерами групп Периодической системы химических элементов Д. И. Менделеева, в которых они находятся.
Значение переменной валентности принято указывать в скобках в названии соединения, например:  — оксид углерода(IV),
— оксид углерода(IV),  — оксид углерода(II).
— оксид углерода(II).
Рассмотрим, как можно составить формулу оксида по его названию (табл. 6).
Понятие о валентности возникло на заре современной химии, поэтому его использование в настоящее время вызывает много вопросов. Как, например, определить валентность атомов в простых веществах? В железе при комнатной температуре у каждого атома 8 ближайших соседей (см. рис. 23, а). Означает ли это, что железо восьмивалентно? Как быть с другими веществами немолекулярного строения? Так, оксиды металлов, как правило, не образуют молекул. Строение того же оксида алюминия Al2O3 лишь формально можно изобразить структурной формулой O Al
Al O
O Al
Al O, на самом деле в этом веществе каждый атом алюминия находится в окружении шести атомов кислорода. Поэтому приведённую формулу принято называть графической. В общем, надо помнить, что валентность имеет реальный смысл лишь в случае веществ молекулярного строения.
O, на самом деле в этом веществе каждый атом алюминия находится в окружении шести атомов кислорода. Поэтому приведённую формулу принято называть графической. В общем, надо помнить, что валентность имеет реальный смысл лишь в случае веществ молекулярного строения.
1.Дайте определение понятия «валентность».
2.Зная, что водород одновалентен, определите валентность химических элементов по формулам соединений: NaH, CaH2, AlH3, CH4, PH3, H2S, HF.
3.Определите валентность элементов по формулам оксидов и назовите вещества: P2O5, SO2, SO3, NO, Na2O, CaO, Mn2O7, SnO2, I2O5, H2O.
4.Напишите формулы следующих оксидов: оксида магния, оксида фосфора(III), оксида калия, оксида хлора(IV), оксида железа(III), оксида меди(II), оксида кремния(IV), оксида хлора(VII), оксида цинка, оксида алюминия, оксида водорода, оксида золота(III).
5.В соединениях с кислородом марганец проявляет валентности II, III, IV, VII. Составьте формулы этих оксидов и назовите их.
6.Хлор образует четыре оксида, в которых он проявляет валентности I, III, V и VII. Составьте формулы этих соединений и назовите их.
7.При горении магния, цинка и алюминия в кислороде образуются их оксиды. Составьте формулы этих соединений, напишите уравнения реакций.
План урока:
Оксиды
Кислоты
Основания
Соли
Оксиды
В состав оксидов ВСЕГДА входит ТОЛЬКО два элемента, один из которых будет кислород. В этом классе соединений срабатывает правило, третий элемент лишний, он не запасной, его просто не должно быть. Второе правило, степень окисления кислорода равна -2. Из выше сказанного, определение оксидов будет звучать в следующем виде.

Оксиды в природе нас окружают повсюду, честно говоря, сложно представить нашу планету без двух веществ – это вода Н2О и песок SiO2.
Вы можете задаться вопросом, а что бывают другие бинарные соединения с кислородом, которые не будут относиться к оксидам.
Поранившись, Вы обрабатываете рану перекисью водорода Н2О2. Или для примера соединение с фтором OF2. Данные вещества вписываются в определение, так как состоят из 2 элементов и присутствует кислород. Но давайте определим степени окисления элементов.

Данные соединения не относятся к оксидам, так как степень окисления кислорода не равна -2.
Кислород, реагируя с простыми, а также сложными веществами образует оксиды. При составлении уравнения реакции, важно помнить, что элементу О свойственна валентность II (степень окисления -2), а также не забываем о коэффициентах. Если не помните, какую высшую валентность имеет элемент, советуем Вам воспользоваться периодической системой, где можете найти формулу высшего оксида.

Рассмотрим на примере следующих веществ кальций Са, мышьяк As и алюминий Al.

Подобно простым веществам реагируют с кислородом сложные, только в продукте будет два оксида. Помните детский стишок, а синички взяли спички, море синее зажгли, а «зажечь» можно Чёрное море, в котором содержится большое количество сероводорода H2S. Очевидцы землетрясения, которое произошло в 1927 году, утверждают, что море горело.

Чтобы дать название оксиду вспомним падежи, а именно родительный, который отвечает на вопросы: Кого? Чего? Если элемент имеет переменную валентность в скобках её необходимо указать.

Классификация оксидов строится на основе степени окисления элемента, входящего в его состав.

Реакции оксидов с водой определяют их характер. Но как составить уравнение реакции, а тем более определить состав веществ, строение которых Вам ещё не известно. Здесь приходит очень простое правило, необходимо учитывать, что эта реакция относиться к типу соединения, при которой степень окисления элементов не меняется.
Возьмём основный оксид, степень окисления входящего элемента +1, +2(т.е. элемент одно- или двухвалентен). Этими элементами будут металлы. Если к этим веществам прибавить воду, то образуется новый класс соединений – основания, состава Ме(ОН)n, где n равно 1, 2 или 3, что численно отвечает степени окисления металла, гидроксильная группа ОН- имеет заряд –(минус), что отвечает валентности I.При составлении уравнений не забываем о расстановке коэффициентов.

Аналогично реагируют с водой и кислотные оксиды, только продуктом будет кислота, состава НхЭОу. Как и в предыдущем случае, степень окисления не меняется, тип реакции – соединение. Чтобы составить продукт реакции, ставим водород на первое место, затем элемент и кислород.

Особо следует выделить оксиды неметаллов в степени окисления +1 или +2, их относят к несолеобразующим. Это означает, что они не реагируют с водой, и не образуют кислоты либо основания. К ним относят CO, N2O, NO.
Чтобы определить будет ли оксид реагировать с водой или нет, необходимо обратиться в таблицу растворимости. Если полученное вещество растворимо в воде, то реакция происходит.


Золотую середину занимают амфотерные оксиды. Им могут соответствовать как основания, так и кислоты, но с водой они не реагируют. Они образованные металлами в степени окисления +2 или +3, иногда +4. Формулы этих веществ необходимо запомнить.

Кислоты
Если в состав оксидов обязательно входит кислород, то следующий класс узнаваем будет по наличию атомов водорода, которые будут стоять на первом месте, а за ними следовать, словно нитка за иголкой, кислотные остатки.

В природе существует большое количество неорганических кислот. Но в школьном курсе химии рассматривается только их часть. В таблице 1 приведены названия кислот.

Валентность кислотного остатка определяется количеством атомов водорода. В зависимости от числа атомов Н выделяют одно- и многоосновные кислоты.

Если в состав кислоты входит кислород, то они называются кислородсодержащими, к ним относится серная кислота, угольная и другие. Получают их путём взаимодействия воды с кислотными оксидами. Бескислородные кислоты образуются при взаимодействии неметаллов с водородом.

Только одну кислоту невозможно получить подобным способом – это кремниевую. Отвечающий ей оксид SiO2 не растворим в воде, хотя честно говоря, мы не представляем нашу планету без песка.
Основания
Для этого класса соединений характерно отличительное свойство, их ещё называют вещества гидроксильной группы – ОН.

Чтобы дать название, изначально указываем класс – гидроксиды, потом добавляем чего, какого металла.

Классификация оснований базируется на их растворимости в воде и по числу ОН-групп.

Следует отметить, что гидроксильная группа, также как и кислотный остаток, это часть целого. Невозможно получить кислоты путём присоединения водорода к кислотному остатку, аналогично, чтобы получить основание нельзя писать уравнение в таком виде.
Na + OH →NaOH или H2 + SO4→ H2SO4
В природе не существуют отдельно руки или ноги, эта часть тела. Варианты получения кислот были описаны выше, рассмотрим, как получаются основания. Если к основному оксиду прибавить воду, то результатом этой реакции должно получиться основание. Однако не все основные оксиды реагируют с водой. Если в продукте образуется щёлочь, значит, реакция происходит, в противном случае реакция не идёт.

Данным способом можно получить только растворимые основания. Подтверждением этому служат реакции, которые вы можете наблюдать. На вашей кухне наверняка есть алюминиевая посуда, это могут быть кастрюли или ложки. Эта кухонная утварь покрыта прочным оксидом алюминия, который не растворяется в воде, даже при нагревании. Также весной можно наблюдать, как массово на субботниках белят деревья и бордюры. Берут белый порошок СаО и высыпают в воду, получая гашеную известь, при этом происходит выделение тепла, а это как вы помните, признак химического процесса.
Раствор щёлочи можно получить ещё одним методом, путём взаимодействия воды с активными металлами. Давайте вспомним, где они размещаются в периодической системе – I, II группа. Реакция будет относиться к типу замещения.

Напрашивается вопрос, а каким же образом получаются нерастворимые основания. Здесь на помощь придёт реакция обмена между щёлочью и растворимой солью.

Соли
С представителями веществ этого класса вы встречаетесь ежедневно на кухне, в быту, на улице, в школе, сельском хозяйстве.

Объединяет все эти вещества, что они содержат атомы металла и кислотный остаток. Исходя из этого, дадим определение этому классу.

Средние соли – это продукт полного обмена между веществами, в которых содержатся атомы металла и кислотный остаток (КО) (мы помним, что это часть чего-то, которая не имеет возможности существовать отдельно).
Выше было рассмотрено 3 класса соединений, давайте попробуем подобрать комбинации, чтобы получить соли, типом реакции обмена.

Чтобы составить название солей, необходимо указать название кислотного остатка, и в родительном падеже добавить название металла.
Ca(NO3)2– нитрат (чего) кальция, CuSO4– сульфат (чего) меди (II).
Наверняка многие из вас что-то коллекционировали, машинки, куклы, фантики, чтобы получить недостающую модель, вы менялись с кем-то своей. Применим этот принцип и для получения солей. К примеру, чтобы получить сульфат натрия необходимо 2 моль щёлочи и 1 моль кислоты. Допустим, что в наличии имеется только 1 моль NaOH, как будет происходить реакция? На место одного атома водорода станет натрий, а второму Н не хватило Na. Т.е в результате не полного обмена между кислотой и основанием получаются кислые соли. Название их не отличается от средних, только необходимо прибавить приставку гидро.

Однако бывают случаи, с точностью наоборот, не достаточно атомов водорода, чтобы связать ОН-группы. Результатом этой недостачи являются основные соли. Допустим реакция происходит между Ва(ОН)2 и HCl. Чтобы связать две гидроксильные группы, требуется два водорода, но предположим, что они в недостаче, а именно в количестве 1. Реакция пойдёт по схеме.

Особый интерес и некоторые затруднения вызывают комплексные соли, своим внешним, казалось,громоздким и непонятным видом, а именно квадратными скобками:K3[Fe(CN)6] или [Ag(NH3)2]Cl. Но не страшен волк, как его рисуют, гласит поговорка. Соли состоят из катионов (+) и анионов (-). Аналогично и с комплексными солями.

Образует комплексный ион элемент-комплексообразователь, обычно это атом металла, которого, как свита, окружают лиганды.

Источник
Теперь необходимо справиться с задачей дать название этому типу солей.

Попробуем дать название K3[Fe(CN)6]. Существует главный принцип, чтение происходит справа налево. Смотрим, количество лигандов, а их роль выполняют циано-группы CN−, равно 6 – приставка гекса. В комплексообразователем будут ионы железа. Значит, вещество будет иметь название гексацианоферрат(III) (чего) калия.

Образование комплексных солей происходит путём взаимодействия, к примеру, амфотерных оснований с растворами щелочей. Амфотерность проявляется способностью оснований реагировать как с кислотами, так и щелочами. Так возьмём гидроксид алюминия или цинка и подействуем на них кислотой и щёлочью.

В природе встречаются соли, где на один кислотный остаток приходится два разных металла. Примером таких соединений служат алюминиевые квасцы, формула которых имеет вид KAl(SO4)2. Это пример двойных солей.

Из всего вышесказанного можно составить обобщающую схему, в которой указаны все классы неорганических соединений.

Как составить реакции с оксидами (алгоритм)
методическая разработка по химии (8 класс) на тему

Этот алгоритм поможет легко и просто составить уравнения.
Скачать:
| Вложение | Размер |
|---|---|
| kak_sostavit_reakcii_s_oksidami.doc | 157 КБ |
Предварительный просмотр:
Как составить реакции с оксидами
Реакция 1. Основный оксид + кислотный оксид → соль
Тип реакции – реакция соединения .
Чтобы составить уравнение этой реакции, надо проделать следующие действия:
- Определить идёт ли реакция?
Реакция осуществима, если оксид металла образован элементами из IA и II A групп.
- Определить по формуле кислотного оксида химическую формулу соответствующей ему кислоты, формулу кислотного остатка и его валентность.
- Определить по формуле основного оксида валентность металла.
- Составить по валентностям формулу соли.
-
Записать уравнение реакции и подобрать в нем коэффициенты.
Пример: Написать уравнение реакции: MgO + N 2 О 5 → .
Действуем по плану:
- Складываем (в уме или на черновике) формулы кислотного оксида и воды:
- Определяем формулу кислотного остатка NO 3 , валентность I (равна количеству Н в кислоте).
- По формуле MgO легко находится валентность магния – II.
- Составляем формулу соли: Mg(NO 3 ) 2
- Записываем, уравнение реакции и подбираем в нем коэффициенты:
MgO + N 2 O 5 → Mg(NО 3 ) 2
Реакция 2. основный оксид + кислота → соль + вода
Тип реакции — реакция обмена .
Составить уравнение этой реакции проще, чем уравнение реакции 1, потому что формула кислоты нам уже известна; зная ее, просто получить и формулу кислотного остатка, и его валентность.
Дальше поступаем так же, как и в предыдущем примере. При составлении уравнения реакции не забудем, что выделяется вода!
Пример: Составьте уравнение реакции между оксидом алюминия и хлороводородной кислотой.
- Вспомним формулу хлороводородной кислоты — НСl, её остаток Сl (хлорид) имеет валентность I.
- По периодической системе Д.И. Менделеева установим, что валентность алюминия III и формула его оксида Аl 2 Оз.
- Составим формулу продукта реакции – соли (хлорида алюминия): АlСlз.
- Запишем уравнение реакции и подберем в нем коэффициенты:
Аl 2 Оз + 6HCl → АlСlз + 3H 2 O
Реакция 3. Кислотный оксид + основание → соль + вода
Тип реакции – реакция обмена .
Для составления уравнения такой реакции следует выполнить действия:
- По формуле кислотного оксида определить формулу его кислоты, формулу кислотного остатка и его валентность (точно так же, как и при составлении реакции 1).
- По формуле гидроксида найти валентность металла: это просто, ведь она равна числу гидроксогрупп (ОН). Если формула гидроксида неизвестна, ее придется составить, используя таблицу растворимости.
- Дальше поступаем, как и в предыдущих примерах: надо составить формулу соли, записать уравнение реакции (не забыть про воду!) и подобрать коэффициенты.
Пример: Составьте уравнение реакции, происходящей при пропускании углекислого газа через известковую воду.
- Вспомним, что углекислый газ — это оксид углерода (IV) СО 2 , а известковой водой называется водный раствор гидроксида кальция Са(ОН) 2 .
- Определим, что оксиду углерода (IV) соответствует угольная кислота Н 2 СО з ; ее кислотный остаток СОз (карбонат) имеет валентность II.
- Не представляет труда вывести формулу продукта реакции — карбоната кальция СаСОз.
- Осталось составить уравнение реакции: СаО + СО 2 → СаСОз.
Реакция 4. Основный оксид + вода → основание
Тип реакции — реакция соединения .
Определить идёт ли реакция?
Реакция осуществима, если оксид металла образован элементами из IA и II A групп.
Составить уравнение этой реакции не составит труда, если вы умеете составлять формулы оснований и оксидов.
Пример: Написать уравнение реакции: Н 2 O + Na 2 O → .
Н 2 O + Na 2 O → 2NaOH
Реакция 5. Кислотный оксид + вода → кислота
Тип реакции — реакция соединения .
Определить идёт ли реакция?
Реагируют все оксиды, кроме оксида кремния SiO 2 .
Составление уравнения этой реакции: п о формуле кислотного оксида определить формулу его кислоты, точно так же, как и при составлении реакции 1).
Пример: Написать уравнение реакции: Н 2 O + N 2 О 5 → .
По теме: методические разработки, презентации и конспекты
Как выполнить задание вида “составить уравнения возможных реакций” (на примере темы “Свойства оксидов”, 8 класс)
Предлагаемая презентация с анимационными эффектами и подсказками может помочь восьмикласснику научиться выполнять задания данного вида при изучении темы “Свойства оксидов”. Предназначена для.
Как выполнить задание вида “Составить уравнения возможных реакций (на примере темы “Химические свойства оснований”)
Предлагаемая презентация с помощью анимационных эффектров и “подсказок” поможет восьмиклассникам закрепить умение выполнять задания данного вида при изучении темы “Химические свойства оснований”. През.

Тема урока: «Классификация химических реакций. Реакции, идущие без изменения и с изменением состава вещества» в 11 классе.
Цели:Образовательная: продолжить формирование у учащихся понятия о классификации химических реакций в органической и неорганической химии.Развивающая: развитие аналитического и синтетического мышления.

Технологическая карта урока по химии « Типы химических реакций по числу и составу исходных и полученных веществ.»
Технологическая карта урока по химии « Типы химических реакций по числу и составу исходных и полученных веществ.».

Классификация химических реакций (по числу и составу исходных и полученных веществ) (урок изучения и первичного закрепления новых знаний и умений)
Создание условий для репродуктивного усвоения материала, умения сравнивать и анализировать.Организовать деятельность учащихся по изучению классификации химических реакций по количеству исх.

Определение состава смеси, в которой одно из исходных веществ, вступает в реакцию с соответствующим реагентом.
Алгоритм решения задач для обучающихся.

Урок “Классификация химических реакций по числу и составу исходных и полученных веществ”
План урока “Классификация химических реакций” содержит цели и задачи изучаемого материала. Описаны основные этапы и методы учебного процесса.
Тема урока: “Оксиды”. 8-й класс
Разделы: Химия
Класс: 8
Тип урока: изучение нового материала, обобщение и систематизация знаний и умений.
Цель: ввести понятие об оксидах; познакомить с важнейшими неорганическими классами; рассмотреть состав, названия, классификацию и физические свойства оксидов.
Задачи:
- Образовательная. Обобщить и закрепить знания обучающихся о физических свойствах оксидов, их нахождении в природе, применении; закрепить умения записывать уравнения реакций, характеризующих химические свойства оксидов.
- Развивающая. Развивать творческие способности при решении нестандартных задач. Развивать логическое мышление. Формировать умение представления при изучении состава, строения и свойств оксидов.
- Воспитательная. Воспитывать бережное отношение к окружающей среде. Формировать интерес к предмету, внимательность, трудолюбие, любознательность, наблюдательность.
Оборудование: Схема: «Классификация оксидов», карточки-задания, тесты, таблица «Химические свойства оксидов», таблица «Формулы и названия некоторых оксидов, схема 3, общие способы получения оксидов, карточки с формулами оксидов.
Основные формы ведения урока: рассказ, беседа, работа с учебником (общеклассная, групповая и индивидуальная), вопрос – ответ.
План урока:
- Проверка домашнего задания.
- Изучение нового материала.
- Определение и название оксидов.
- Классификация оксидов.
- Физические свойства оксидов.
- Химические свойства оксидов.
- Важнейшие оксиды.
- Способы получения оксидов.
- Способы получения оксидов.
- Закрепление изученного материала
В начале урока, мотивируя учебную деятельность учащихся, учитель рассказывает, что им предстоит изучить оксиды – вещества, образующие минералы; и на доске записывает формулу этих веществ:
SiO2 – кремнезёмы (IV),
Al2O3 – корунд,
CaO – негашеная известь,
Fe2O3 – красный железняк (гематит),
Fe3O4 – магнитный железняк (магнитит).
Их получают путём горения или разложения сложных веществ. В них 2 элемента, один – кислород. Я отнесу к ним также известь и лёд. Какие это вещества? (Оксиды.)
Проверка домашнего задания
Сценка «Кто я»
Я у древних химиков самым главным веществом считалась. «Начало всех начал» – говорил греческий учёный Фале, живший в VI в. до н.э. и утверждавший, что окружающий мир возник из меня – «первичной материи». Я в древности считалась матерью жизни и смерти. Мне поклонялись, а по преданиям древней Руси, во мне жили русалки и водяные. У древних народов Азии в прошлом я служила причиной войн и борьбы. Являюсь важным двигателем, который не ломается, не ржавеет, не горит, не гниёт и ни кем не уничтожается. Кто я? (Вода)
К какому классу веществ относится вода?
Какие классы неорганических веществ вы знаете?
Какие соединения (вещества) называются кислотами?
Подчеркните синим мелом формулы кислот и дайте им названия.
Как классифицируют кислоты?
Назовите кислородсодержащие и бескислородные кислоты.
Какие соединения называют основаниями?
Подчеркните жёлтым мелом формулы оснований и назовите эти вещества.
Как классифицируют основания?
Пользуясь таблицей растворимости, выберите из данных формул растворимые и нерастворимые основания.
Подчеркните красным мелом формулы солей и дайте им названия.
Какие соединения называют солями?
Как классифицируют соли?
Изучение нового материала
Итак, ребята, в 8 классе на уроках химии мы подробно разбирали состав и свойства неорганических соединений различных классов. Целью сегодняшнего урока является изучение и обобщение нового материала по теме «Оксиды».
Обращаем внимание учащихся на то, что на доске остались неподчёркнутые формулы веществ, с которыми они ещё не знакомы. Это формулы оксидов.
Вопрос 1. Какой газ необходим для фотосинтеза и выделяется при выдохе?
Ответ: углекислый газ CO2 – оксид углерода – (IV).
Вопрос 2. В стихотворении А.А. Ахматовой упомянут металл:
На рукомойнике моём
Позеленела медь
Но так играет луч на нём
Что весело глядеть.
С каким соединением реагирует водород с образованием данного металла и воды?
Ответ: оксид меди – CuO – (II)
Оксиды – сложные вещества, состоящие из двух элементов, один из которых – кислород в степени окисления – 2 и валентности – (II).
Поскольку оксиды образуют почти все химические элементы, необходимо каждому оксиду дать своё название. Названия оксидов состоят из слова «оксид» и названия химического элемента в родительном падеже. Если элемент имеет переменную степень окисления (переменную валентность), то её указывают римскими цифрами, взятыми в скобки, после названия химического элемента.
Элементы с постоянной степенью окисления – металлы главных подгрупп I, II, III групп. Элементы с переменной степенью окисления – остальные металлы.
Таблица № 1. Формулы и названия некоторых оксидов

Упражнение «Не прерви цепочку»
Для каждого ученика приготовлена карточка с формулой оксида. Ученик показывает карточку классу и называет оксид. Работу класса учитель организует по цепочке.
Схема 1. Классификация оксидов

Учитель напоминает формулы различных веществ.
Знак, какого элемента, металла или неметалла находится на первом месте?
Кислотные оксиды, как правило, – оксиды неметаллов.
Почему эти оксиды называют кислотными?
Оксиды, которым соответствуют кислоты (независимо от того, реагируют ли они с водой или не реагируют), называют кислотными.
Впишите в «схему 1» пример кислотного оксида. Сначала назовите любой неметалл, кислоту, а затем – кислотный оксид.
Знак какого элемента, металла или неметалла находится на первом месте в формуле оксидов магния, калия?
Основными оксидами являются оксиды металлов. Если оксид бария взаимодействует с водой, то получается новое вещество Ba(OH)2 – основание.
Теперь становится понятным название «основной оксид».
Оксиды, которым соответствуют основания (независимо от того, реагируют ли они с водой или нет), называют основными.
Основные оксиды реагируют с кислотами, образуя соли.
Кислотные оксиды реагируют со щелочами, образуя соли.
Основные и кислотные оксиды относят к солеобразующим. Но есть оксиды, для которых соответствующие соли не существуют, их называют несолеобразующими или безразличными. Пример: оксид азота (II) – NO
Таким образом, можно сделать вывод, что неметаллы образуют кислотные оксиды (искл. – несолеобразующие оксиды: CO, NO, N2O, SiO )

Физические свойства оксидов
В рамках изучения физических свойств оксидов учащиеся самостоятельно работают с учебником.
Оксиды имеют различные физические свойства: оксиды бывают твёрдые, жидкие и газообразные, различного цвета.
Агрегатные состояния оксидов:
Химические свойства оксидов
Следует акцентировать внимание учащихся на правиле: оксид взаимодействует с водой, если образуется растворимый гидроксид.

Важнейшие оксиды. Оксиды широко распространены в природе. Некоторые оксиды постоянно окружают нас и находят широкое применение. Познакомимся с некоторыми из них.
Вода H2O – оксид водорода. Вода – это самой распространённоё и самое необходимое вещество на нашей планете. Без воды не было бы жизни на Земле. Всё живое нуждается в воде. Так, если без пищи человек может прожить 50 суток, то без воды смерть наступает через 5-7 дней. Вода является и важнейшей составной частью клеток животных и растений. Организм человека на 65-70 % состоит из воды, а у некоторых медуз – до 99 % массы тела составляет вода. Содержание воды в огурцах и арбузах превышает 90 %. Велики затраты воды в сельском хозяйстве. Для того чтобы вырастить 1 т. пшеницы, требуется 1500 т. воды, 1 т. риса – 7000 т. воды. Общие запасы воды на Земле – огромны и составляют 138,6 млн. км 3 . Вода покрывает почти 3/4 поверхности земного шара.
Углекислый газ СО2 – оксид углерода (IV).
Около 0,03 % по объёму углекислый газ содержится в воздухе. В природе он образуется при гниении растительных и животных останков, дыхании, сжигании топлива, в больших количествах выделяется из вулканических трещин и вод минеральных источников.
При обычных условиях диоксид углерода бесцветен, не имеет запаха. Углекислый газ значительно тяжелее воздуха. Углекислый газ применяют при изготовлении шипучих напитков, в медицине – углекислотные ванны. «Сухой лёд» применяется для хранения скоропортящихся пищевых продуктов, для производства и хранения мороженого. Углекислый газ не горит и не поддерживает горение, поэтому его применяют для тушения пожаров.
Оксид кремния (IV) SiO2 в виде песка применяется в строительстве, в производстве стекла, керамики, цемента.
Некоторые оксиды (оксид серы (IV), оксид азота и др.) образуются в промышленном производстве. В больших количествах эти оксиды попадают в атмосферу, где парами воды образуют кислоты, и выпадают в виде так называемых кислотных дождей. Кислотные дожди наносят огромный вред окружающей среде, поэтому необходимо принимать меры, способствующие снижению попадания оксидов в атмосферу.
1) при горении простых и сложных веществ;
2) при разложении сложных веществ – нерастворимых оснований, кислот, солей (схема 4)

Закрепление полученного материала
С каким классом неорганических веществ вы сегодня познакомились?
Почему они имеют такое название?
Классификация оксидов.
Какими физическими свойствами обладают оксиды?
Какими химическими свойствами обладают оксиды?
Общие способы получения оксидов?
Назовите важнейшие оксиды.
Заканчиваем урок подведением итогов, выставляем отметки и предлагаем домашнее задание.
Литература:
1. / Неорганическая химия 7 – 10 класс, Москва «Просвещение 1980 г.» С.А. Балязин, Н.Г. Ключников, В.С. Полосин, § 19, стр. 25, § 26 – 29 стр. 31 – 36, § 44, стр. 53. /
2. / Химия 10 – 12 класс, Москва «Просвещение 1989 г.» Г.Е. Рудзитис, Ф.Г. Фельдман, § 1, стр. 43. /
3. / Химия 8 класс, Москва «Оникс 21 век 2003», И.И. Новошинский, Н.С. Новошинская, § 26 стр. 83, § 45, стр. 169 – 174. /
3. / Химия в школе № 2, 2010 г., стр. 30 – 33. /
4. / Химия в школе № 7, 2012 г., стр. 24 – 25. /
6. / Химия. Первое сентября № 18, 16 – 31 сентября 2009 г., стр. 30 – 41. /
Оксиды: классификация, получение и химические свойства
Оксиды — это сложные вещества, состоящие из атомов двух элементов, один из которых — кислород со степенью окисления -2. При этом кислород связан только с менее электроотрицательным элементом.
В зависимости от второго элемента оксиды проявляют разные химические свойства. В школьном курсе оксиды традиционно делят на солеобразующие и несолеобразующие. Некоторые оксиды относят к солеобразным (двойным).
Двойные оксиды — это некоторые оксиды , образованные элементом с разными степенями окисления.
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, обладающие характерными основными свойствами. К ним относят оксиды, образованные атомами металлов со степень окисления +1 и +2.
Кислотные оксиды — это оксиды, характеризующиеся кислотными свойствами. К ним относят оксиды, образованные атомами металлов со степенью окисления +5, +6 и +7, а также атомами неметаллов.
Амфотерные оксиды — это оксиды, характеризующиеся и основными, и кислотными свойствами. Это оксиды металлов со степенью окисления +3 и +4, а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO.
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO.
Классификация оксидов
Получение оксидов
Общие способы получения оксидов:
1. Взаимодействие простых веществ с кислородом :
1.1. Окисление металлов: большинство металлов окисляются кислородом до оксидов с устойчивыми степенями окисления.
Например , алюминий взаимодействует с кислородом с образованием оксида:
Не взаимодействуют с кислородом золото, платина, палладий.
Натрий при окислении кислородом воздуха образует преимущественно пероксид Na2O2,
Калий, цезий, рубидий образуют преимущественно пероксиды состава MeO2:
Примечания : металлы с переменной степенью окисления окисляются кислородом воздуха, как правило, до промежуточной степени окисления (+3):
Железо также горит с образованием железной окалины — оксида железа (II, III):
1.2. Окисление простых веществ-неметаллов.
Как правило, при окислении неметаллов образуется оксид неметалла с высшей степенью окисления, если кислород в избытке, или оксид неметалла с промежуточной степенью окисления, если кислород в недостатке.
Например , фосфор окисляется избытком кислорода до оксида фосфора (V), а под действием недостатка кислорода до оксида фосфора (III):
Но есть некоторые исключения .
Например , сера сгорает только до оксида серы (IV):
Оксид серы (VI) можно получить только окислением оксида серы (IV) в жестких условиях в присутствии катализатора:
2SO2 + O2 = 2SO3
Азот окисляется кислородом только при очень высокой температуре (около 2000 о С), либо под действием электрического разряда, и только до оксида азота (II):
Не окисляется кислородом фтор F2 (сам фтор окисляет кислород). Не взаимодействуют с кислородом прочие галогены (хлор Cl2, бром и др.), инертные газы (гелий He, неон, аргон, криптон).
2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д.
При окислении кислородом сложных веществ, состоящих, как правило, из двух элементов, образуется смесь оксидов этих элементов в устойчивых степенях окисления.
Например , при сжигании пирита FeS2 образуются оксид железа (III) и оксид серы (IV):
Сероводород горит с образованием оксида серы (IV) при избытке кислорода и с образованием серы при недостатке кислорода:
А вот аммиак горит с образованием простого вещества N2, т.к. азот реагирует с кислородом только в жестких условиях:
А вот в присутствии катализатора аммиак окисляется кислородом до оксида азота (II):
3. Разложение гидроксидов. Оксиды можно получить также из гидроксидов — кислот или оснований. Некоторые гидроксиды неустойчивы, и самопроизвольную распадаются на оксид и воду; для разложения некоторых других (как правило, нерастворимых в воде) гидроксидов необходимо их нагревать (прокаливать).
гидроксид → оксид + вода
Самопроизвольно разлагаются в водном растворе угольная кислота, сернистая кислота, гидроксид аммония, гидроксиды серебра (I), меди (I):
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
При нагревании разлагаются на оксиды большинство нерастворимых гидроксидов — кремниевая кислота, гидроксиды тяжелых металлов — гидроксид железа (III) и др.:
4. Еще один способ получения оксидов — разложение сложных соединений — солей .
Например , нерастворимые карбонаты и карбонат лития при нагревании разлагаются на оксиды:
Соли, образованные сильными кислотами-окислителями (нитраты, сульфаты, перхлораты и др.), при нагревании, как правило, разлагаются с с изменением степени окисления:
Более подробно про разложение нитратов можно прочитать в статье Окислительно-восстановительные реакции.
Химические свойства оксидов
Значительная часть химических свойств оксидов описывается схемой взаимосвязи основных классов неорганических веществ.
Химические свойства основных оксидов
Подробно про химические свойства оксидов можно прочитать в соответствующих статьях:
[spoiler title=”источники:”]
http://urok.1sept.ru/articles/642418
[/spoiler]






