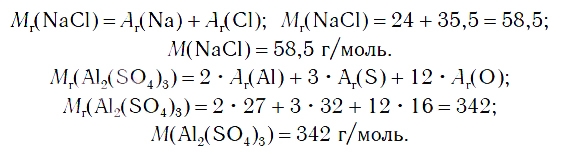В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.
Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4 и др. Это представители класса широко распространенных в химии соединений — солей (рис. 102).
Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4 c формулами солей ZnCl2 и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2 и FeSO4, относят к классу солей.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4 равна III.
Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
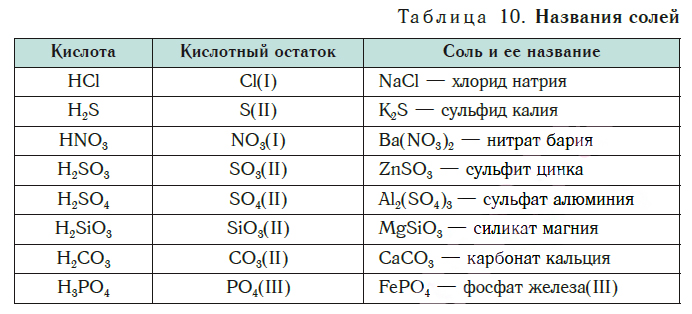
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
- Соли — сложные вещества, которые состоят из атомов металлов и кислотных остатков.
- Соли образуются при замещении атомов водорода в молекулах кислот на атомы металлов.
- Соли — вещества немолекулярного строения.
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Правила
составления формул основных солей по
названию.
Пример
1.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксохлорид
железа
(III)FeOHCl
Приставка
ГИДРОКСО означает, что соль основная,поэтому,
в составе – одна ОН группаНазвание
ХЛОРИД означает, что это соль солянойкислоты,
поэтому, в составе кислотного остатка
Cl
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( – 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксохлорид
железа
(III)+3
-1 -1FeOHCl
Валентность
железа равна III ( указано в названии
),поэтому,
заряд атома железа равен ( + 3 )Валентность
кислотного остатка Cl
равна
I , т.к. в НCl один атом водорода, поэтому,
заряд хлора равен ( – 1 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть – металл с ОН группой;
вторая часть – кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группа+3
-1(
FeOH )Заряд
первой части равен:+3
+ (-1) = +2+3
-1 -1FeOHCl
+2
-1Вторая
часть: кислотный остаток(
Cl )Заряд
второй части равен: -1
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа(
FeOH )Заряд
первой части равен:+3
+ (-1) = +2У
группы FeOH индекс1
не пишем+3
-1 -1FeOHCl2
+2
+ (-2) = 0Вторая
часть: кислотный остаток ( Cl )Для
равенства зарядов у кислотногоостатка
Cl пишем индекс: 2Заряд
второй части равен:-1
•
2 = – 2
¾
12 ¾
Пример
2.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
дигидроксохлорид
железа
(III)Fe(OH)2Cl
Приставка
ДИГИДРОКСО означает, что соль
основная,и
в её составе – две ОН группы“ДИ”
означает ДВЕ ( две ОН группы )Название
ХЛОРИД означает, что это соль солянойкислоты,
поэтому, в составе кислотного остатка
группа Cl
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( – 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
дигидроксохлорид
железа
(III)+3
-1 -1Fe(OH)2Cl
Валентность
железа равна III ( указано в названии
),поэтому,
заряд атома железа равен ( + 3 )Валентность
кислотного остатка Cl
равна
I , т.к. в НCl один атом водорода, поэтому,
заряд хлора равен ( – 1 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть – металл с ОН группой;
вторая часть – кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группы+3
-1(
Fe(OH)2
)Заряд
первой части равен:+3
+ ( -1 •
2
) = +1+3
-1 -1Fe(OH)2Cl
+1
-1Вторая
часть: кислотный остаток(
Cl )Заряд
второй части равен: -1
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа+3
-1(
Fe(OH)2
)Заряд
первой части равен:+3
+ ( -1 •
2
) = +1+3
-1 -1Fe(OH)2Cl
+1
+ ( -1 ) = 0Вторая
часть: кислотный остаток ( Cl )Заряд
второй части равен:-1
•
1 = – 1Заряды
частей равны, поэтому, индексы ставить
не надо, т.к. формула составлена.
¾
13 ¾
Пример
3.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксокарбонат
меди
(II)СuOHCO3
Приставка
ГИДРОКСО означает, что соль основная,поэтому,
в составе – одна ОН группаНазвание
КАРБОНАТ означает, что это соль
угольнойкислоты,
поэтому, в составе кислотного остатка
группа CО3
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( – 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксокарбонат
меди
(II)+2
-1 -2СuOHCO3
Валентность
меди равна II ( указано в названии ),поэтому,
заряд атома меди равен ( + 2 )Валентность
кислотного остатка CО3
равна
II , т.к.в
Н2CО3
два атома водорода, поэтому, заряд
CО3равен
( – 2 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть – металл с ОН группой;
вторая часть – кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группа+2
-1(
СuOH )Заряд
первой части равен:+2
+ (-1) = +1+2
-1 -2CuOHCO3
+1
-2Вторая
часть: кислотный остаток(
CO3
)Заряд
второй части равен: -2
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа(
CuOH )Заряд
первой части равен:+2
+ (-1) = +1У
группы CuOH запишите индекс 2+2
-1 -2(СuOH)2CO3
+1
+ (-2) = -1Вторая
часть: кислотный остаток ( Cl )Заряд
второй части равен:-1
•
2 = – 2У
кислотного остатка CO3индекс
1 не пишем
¾
14 ¾
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Краткий список
Выбрана категория:
Соли
со всеми вложенными подкадегориями
Общее число найденных записей: 1497.
Показано записей: 20.
1. Глюконат кальция
Брутто-формула:
C12H22CaO14
CAS# 299-28-5
Названия
Русский:
- Глюконат кальция [Wiki]
- кальция (2R,3S,4R,5R)-2,3,4,5,6-пентагидроксигексаноат(IUPAC)
;
;
English:
- Calcicol
- Calciofon
- Calcipur
- Calcium gluconate [Wiki]
- Calglucol
- Calglucon
- D-Gluconic acid, calcium salt (2:1)(CAS)
- Dragocal
- E 578
- Ebucin
- Glucal
- Glucobiogen
- calcium (2R,3S,4R,5R)- 2,3,4,5,6-pentahydroxyhexanoate(IUPAC)
- calcium;(2R,3S,4R,5R)-2,3,4,5,6-pentahydroxyhexanoate(IUPAC)
;
;
;
;
;
;
;
;
;
;
;
;
;
;
@:A()O^-`/|O`|`<`|wOH>`/<|wOH>`<`|wOH>`/<|dOH>“/HO@; Ca^2+<_(y-2,x-1,N0)@A()>_(x-1,y2,N0)@A()
HO/<|dOH>/<`|wOH><|wOH>/<`|wOH>|O`|/O^-$L(1.4)Ca^2+/0O`^-$L()|O`|/<`|dOH><|dOH>/<`|dOH><|wOH>/OH
2. Сульфат калия
Брутто-формула:
K2O4S
CAS# 7778-80-5
Названия
Русский:
- Сернокислый калий
- Сульфат калия(IUPAC) [Wiki]
- калия сульфат
;
;
;
English:
- Dipotassium sulfate
- E 515
- Potassium sulfate [Wiki]
- Sulfuric acid dipotassium salt
- dipotassium;sulfate(IUPAC)
;
;
;
;
;
K^+O`^-/S<_qq4O><_pp4O>/O^-K^+
3. Нитрат калия
Брутто-формула:
KNO3
CAS# 7757-79-1
Названия
Русский:
- Нитрат калия(IUPAC) [Wiki]
- азотнокислый калий
- калиевая селитра
- калийная селитра
- калия нитрат
;
;
;
;
;
English:
- EINECS:231-818-8
- Nitrate of potash
- Potassium nitrate(IUPAC) [Wiki]
- Saltpetre
;
;
;
;
O`^-/N^+`|O|O^-_(x1,N0)K^+
4. Хлорид калия
Брутто-формула:
ClK
CAS# 7447-40-7
Названия
Русский:
- Хлорид калия(IUPAC) [Wiki]
- калия хлорид
- хлористый калий
;
;
;
English:
- Chlorvescent
- E 508
- Enseal
- Kalitabs
- Kaochlor
- Klor-Con
- Klotrix
- Pfiklor
- Potassium chloride(IUPAC) [Wiki]
- Potavescent
- Slow-K
;
;
;
;
;
;
;
;
;
;
;
5. Карбонат калия
Брутто-формула:
CK2O3
CAS# 584-08-7
Названия
Русский:
- Карбонат калия(IUPAC) [Wiki]
- калия карбонат
- поташ
- углекислый калий
;
;
;
;
English:
- EINECS:209-529-3
- Potash
- Potassium carbonate(IUPAC) [Wiki]
- pearl ash
;
;
;
;
6. Гидрокарбонат калия
Брутто-формула:
CHKO3
CAS# 298-14-6
Названия
Русский:
- Гидрокарбонат калия(IUPAC) [Wiki]
- Углекислый калий, кислый
- бикарбонат калия
- калия гидрокарбонат
;
;
;
;
English:
- EINECS:206-059-0
- EPA Pesticide Chemical Code 073508
- Kaligreen
- Monopotassium carbonate
- Potassium bicarbonate [Wiki]
- Purple K
- compounds
- monopotassium salt;
- potassium acid carbonate
- potassium hydrogen carbonate(IUPAC)
;
;
;
;
;
;
;
;
;
;
7. Сульфат натрия
Брутто-формула:
Na2O4S
CAS# 7757-82-6
Названия
Русский:
- Сульфат натрия(IUPAC) [Wiki]
- натрий сернокислый
- натрия сульфат
;
;
;
English:
- Bisodium sulfate
- Disodium sulfate
- Disodium sulphate
- EINECS:231-820-9
- Salt cake
- Sodium sulfate(IUPAC) [Wiki]
- Sodium sulphate
- Sulfate, sodium
- Sulfuric acid disodium salt
- Sulfuric acid, disodium salt
- Thenardite
- disodium;sulfate(IUPAC)
;
;
;
;
;
;
;
;
;
;
;
;
$slope(15)Na^+/0O^-<Na^+>|S<`=O><=O>|O^-
$L(1.2)Na^+O`^-/S<_qq4O><_pp4O>/O^-Na^+
8. Нитрат натрия
Брутто-формула:
NNaO3
CAS# 7631-99-4
Названия
Русский:
- Натриевая селитра
- Нитрат натрия(IUPAC) [Wiki]
- азотнокислый натрий
- натрия нитрат
- натронная селитра
- чилийская селитра
;
;
;
;
;
;
English:
- Caliche
- Chile saltpeter
- E 251
- EINECS:231-554-3
- Nitrate of soda
- Nitratine
- Nitric acid monosodium salt
- Nitric acid sodium salt
- Nitric acid sodium salt (1:1)
- Peru saltpeter
- Soda niter
- Sodium nitrate(IUPAC) [Wiki]
- cubic niter
;
;
;
;
;
;
;
;
;
;
;
;
;
O`^-/N^+`|O|O^-_(x1,N0)Na^+
9. Хлорид натрия
Брутто-формула:
ClNa
Названия
Русский:
- Хлорид натрия(IUPAC)
- галит
- каменная соль
- натрия хлорид
- обычная соль
- пищевая соль
- поваренная соль
- столовая соль
;
;
;
;
;
;
;
;
English:
- Common salt
- Halite
- Rock salt
- Saline
- Sodium chloric
- Sodium chloride(IUPAC)
- Table salt
;
;
;
;
;
;
;
10. Карбонат натрия
Брутто-формула:
CNa2O3
CAS# 497-19-8
Названия
Русский:
- Карбонат натрия [Wiki]
- динатрий(IUPAC)
- кальцинированная сода
- натрия карбонат
- триоксокарбонат(IUPAC)
- углекислый натрий
;
;
;
;
;
;
English:
- EINECS:207-838-8
- Soda ash
- Soda crystals
- Sodium carbonate(IUPAC) [Wiki]
- Washing soda
;
;
;
;
;
Na^+|0O`^-/`|O|O^-`|0Na^+
11. Гидрокарбонат натрия
Брутто-формула:
CHNaO3
CAS# 144-55-8
Названия
Русский:
- Гидрокарбонат натрия(IUPAC)
- бикарбонат натрия
- натрий двууглекислый
- натрия гидрокарбонат
- питьевая сода
- пищевая сода
;
;
;
;
;
;
English:
- Baking soda, bicarbonate of soda
- Sodium bicarbonate
- Sodium hydrogen carbonate(IUPAC)
- nahcolite
- sodium hydrogencarbonate
;
;
;
;
;
12. Сульфат кальция
Брутто-формула:
CaO4S
CAS# 7778-18-9
Названия
Русский:
- Сульфат кальция(IUPAC) [Wiki]
- алебастр
- гипс
- кальций сернокислый
- кальция сульфат
- селенит
;
;
;
;
;
;
English:
- Anhydrite
- Anhydrous gypsum
- Calcium sulfate(IUPAC) [Wiki]
- Crysalba
- Drierite
- EINECS:231-900-3
- Gypsum
- Karstenite
- Muriacite
- Osteoset
- Sulfuric acid, calciumsalt (1:1)(CAS)
- Thiolite
;
;
;
;
;
;
;
;
;
;
;
;
Ca^2+O//S`|O|<_(A80,w+)O^->dO^-
Ca^++/0O`^-# -S`|O|<=O>|O^-
13. меди хлорокись
Брутто-формула:
H3ClCu2O3
CAS# 1332-65-6
Названия
Русский:
- Абига-Пик
- Куприкол
- Оксихлорид меди
- ХОМ
- меди хлорокись
;
;
;
;
;
English:
- Dicopper chloride trihydroxide(IUPAC)
- copper chloride hydroxide(CAS)
- copper oxychloride
;
;
;
$L(1.2)Cu^2+Cl^-|0O^-<H`>`/0Cu^2+`O^-<`/H>`|0O^-`H
14. Хлорид кальция
Брутто-формула:
CaCl2
Названия
Русский:
- Хлорид кальция(IUPAC) [Wiki]
- Хлористый кальций
- кальция хлорид
;
;
;
English:
- Anhydrous calcium chloride
- Calcium chloride(IUPAC) [Wiki]
- Calcium dichloride
- Calcium(II) chloride
- Calcosan
- Calplus
- Caltac
- Dowflake
- E509
- EINECS:233-140-8
- Liquidow
- Peladow
- Snomelt
- Superflake anhydrous
;
;
;
;
;
;
;
;
;
;
;
;
;
;
15. Карбонат кальция
Брутто-формула:
CCaO3
CAS# 471-34-1
Названия
Русский:
- Карбонат кальция(IUPAC)
- кальция карбонат
- углекислый кальций
;
;
;
English:
- Calcium carbonate(IUPAC)
- Limestone
- aragonite
- calcite
- chalk
- marble
- pearl
;
;
;
;
;
;
;
$slope(35)Ca^++`/0O^-C|O`|/O^-
16. Гидрокарбонат кальция
Брутто-формула:
C2H2CaO6
Названия
Русский:
- Гидрокарбонат кальция(IUPAC)
- кальция гидрокарбонат
;
;
English:
- Calcium bicarbonate
- Calcium hydrogen carbonate(IUPAC)
;
;
HO/`|O|O^-/0Ca^2+O`^-/`|O|OH
17. Сульфат магния
Брутто-формула:
MgO4S
CAS# 7487-88-9
Названия
Русский:
- Сернокислый магний
- Сульфат магния(IUPAC) [Wiki]
- магний сернокислый
- магния сульфат
- эпсомская соль
;
;
;
;
;
English:
- Magnesium sulfate(IUPAC) [Wiki]
- magnesium sulphate
;
;
Mg^2+O//S`|O|<_(A80,w+)O^->dO^-
Mg^2+/0O`^-# -S`|O|<||O>-O^-
18. Нитрат магния
Брутто-формула:
MgN2O6
CAS# 10377-60-3
Названия
Русский:
- Нитрат магния(IUPAC) [Wiki]
- магния нитрат
;
;
English:
- EINECS:233-826-7
- Magnesium dinitrate
- Magnesium nitrate(IUPAC)
- Magnesium(II) NItrate
- Magnesium(II) Nitrate (1:2)
- Magniosan
- Nitricacid, magnesium salt (8CI,9CI)
;
;
;
;
;
;
;
O`^-/N^+`|O|O^-/0Mg^2+O`^-/N^+`|O|O^-
O=N^+</O^->O^-_(x1.2,y#2,N0)Mg^2+_(x1.2,y#3,N0)O`^-N`^+<`/O`^->=O
19. Хлорид магния
Брутто-формула:
Cl2Mg
CAS# 7786-30-3
Названия
Русский:
- Хлорид магния(IUPAC)
- магния хлорид
- хлористый магний
;
;
;
English:
- Aerotex Accelerator MX
- C-TEK
- Catalyst G
- E 511
- Ekimac
- FIX-Mg
- Freecat MX
- HMC 23D
- Magnesium chloride(IUPAC)(CAS)
- Magnesium dichloride
- Magnesium(II) chloride
- Magnogene
- White Nigari NS
;
;
;
;
;
;
;
;
;
;
;
;
;
20. Карбонат магния
Брутто-формула:
CMgO3
Названия
Русский:
- Карбонат магния(IUPAC)
- Магния карбонат
- магний углекислый
;
;
;
English:
- Magnesite
- Magnesium carbonate(IUPAC)
;
;
Таблица и формулы солей.
Таблица и формулы солей (1 часть):
| Формула кислоты или основания | Название кислоты или основания | Формула кислотного остатка или остатка основания |
Название соли |
| HN3 | Азотистоводородная (Азоимид, Азидоводород) | N3– | Азид |
| HNO2 | Азотистая | NO2– | Нитрит |
| HNO3 | Азотная | NO3– | Нитрат |
| HBrO2 | Бромистая | BrO2– | Бромит |
| HBrO3 | Бромноватая | BrO3– | Бромат |
| HBrO | Бромноватистая (Гипобромистая кислота) | BrO– | Гипобромит |
| HBr | Бромоводород (Бромистоводородная кислота) | Br– | Бромид |
| HVO3 | Ванадиевая | VO3– | Ванадат |
| H2WO4 | Вольфрамовая | WO42– | Вольфрамат |
| H4GeO4 или Ge(OH)4 | Германиевая кислота (Гидроксид германия (IV)) | GeO44– | Германат |
| Be(OH)2 | Гидроксид бериллия | BeO22– | Бериллат |
| H2S2O7 | Дисерная | S2O72– | Дисульфат |
| H4P2O7 | Дифосфорная | P2O74– | Пирофосфат или дифосфат (по номенклатуре IUPAC) |
| H2Cr2O7 | Дихромовая | Cr2O72– | Дихромат |
| HIO4 | Йодная | IO4– | Периодат |
| HIO | Йодноватистая | IO– | Гипоиодит |
| HI | Йодоводород (Йодоводородная кислота) | I– | Йодид |
| H2SiO3 | Кремниевая | SiO32– | Силикат |
| H2MnO4 | Марганцовистая | MnO42– | Манганат |
| HMnO4 | Марганцовая | MnO4– | Перманганат |
| HCOOH | Метановая (Муравьиная кислота) | HCOO– | Формиат |
| HBO | Метаборная | BO– | Метаборат |
| HAsO2 | Метамышьяковистая | AsO2– | Метаарсенит |
| HPO3 | Метафосфорная | PO3– | Метафосфат |
Таблица и формулы солей (2 часть):
| H2MoO4 | Молибденовая | MoO42– | Молибдат |
| H3BO3 | Ортоборная (Борная кислота) | BO33– | Бораты |
| H3AsO4 | Ортомышьяковая | AsO43– | Арсенат |
| H3AsO3 | Ортомышьяковистая | AsO33– | Ортоарсенит |
| H2PbO4 | Ортосвинцовая кислота | PbO42– | Ортоплюмбат или плюмбат |
| H3PO4 | Ортофосфорная (Фосфорная кислота) | PO43– | Фосфат |
| HNCS | Роданистоводородная (Тиоциановая кислота) | SCN– | Тиоцианат |
| C7H6O3 | Салициловая | C7H6O3– | Салицилат |
| H2SO4 | Серная | SO42– | Сульфат |
| H2SO3 | Сернистая | SO32– | Сульфит |
| H2S | Сероводород (Сероводородная кислота) | S2– | Сульфид |
| H2SO3S | Тиосерная | SO3S2– | Тиосульфат |
| H2CO3 | Угольная | CO32– | Карбонат |
| HF | Фтороводород (Плавиковая кислота) | F– | Фторид |
| HCl | Хлороводород (Соляная кислота) | Cl– | Хлорид |
| H2CrO4 | Хромовая | CrO42– | Хромат |
| HClO2 | Хлористая | ClO2– | Хлорит |
| HClO4 | Хлорная | ClO4– | Перхлорат |
| HClO3 | Хлорноватая | ClO3– | Хлорат |
| HClO | Хлорноватистая | ClO– | Гипохлорит |
| HCN | Циановодород (Синильная кислота) | CN— | Цианид |
| H2C2O4 | Этандиовая (Щавелевая кислота) | C2O42– | Оксалат |
| CH3COOH | Этановая (Уксусная кислота) | CH3COO– | Ацетат |
| C4H6O5 | Яблочная (Оксиянтарная, Гидроксибутандиовая кислота) | C4H4O52– | Малат |
Коэффициент востребованности
9 871
Знаток
(368),
закрыт
2 месяца назад
Штирлиц
Высший разум
(317565)
7 лет назад
KCl хлорид калия
KNO3 нитрат калия
KNO2 нитрит калия
K2SO3 сульфит калия
K2SO4 сульфат калия
K2S сульфид калия
К2СО3 карбонат калия
K3PO4 фосфат калия
теперь вместо К напиши Na и все будет то же, только не калия, а натрия
затем вместо К напиши Li и все будет то же, только не калия, а лития
СаCl2 хлорид кальция
Ca(NO3)2 нитрат кальция
Сa(NO2)2 нитрит кальция
CaSO3 сульфит кальция
CaSO4 сульфат кальция
Ca2S сульфид кальция
Ca3(PO4)2 фосфат кальция
вместо Са подставляй Mg – будет то же, только не кальция, а магния
аналогично и с Ва – барием
Екатерина Романова
Мастер
(1018)
7 лет назад
Берешь любой металл, например натрий и подставляешь к любому остатку, например, фторид натрия, хлорид натрия и т. д. Формулы остатков во вложении, натрий – Na, можешь еще взять магний – Mg и, к примеру, калий – K, выглядит это так: NaCl( металл всегда ПЕРЕД ОСТАТКОМ) – хлорид натрия