Как определить глицерин в пробирке
Ученик
(117),
закрыт
11 лет назад
Вахит Шавалиев
Высший разум
(762740)
11 лет назад
Прильем ко всем реактивам одинаковое количество (немного, с недостатком) гидроксида меди (II).
В глицерине, глюкозе и уксусной кислоте гидроксид растворится и появится синяя окраска.
Там, где ярко-синяя окраска находится либо глицерин, либо глюкоза, образовался комплекс с многоатомным спиртом: 4Cu(OH)2+R(OH)n->R[Cu4(OH)n+8]. Чтобы определить где находится глюкоза, где глицерин, подогреем пробирки. Глюкоза, помимо того, что спирт, еще и альдегид. При нагревании она окислится до глюконовой кислоты и восстановит гидроксид меди (II) до красного оксида меди (I), который выпадет в осадок: RCOH+2Cu(OH)2->t->RCOOH+Cu2O+2H2O. В пробирке с глицерином изменений не будет. Там, где окраска более бледная (зеленовато-голубая) – уксусная кислота – образуется смесь ацетата меди (II): Cu(OH)2+2CH3COOH->Cu(CH3COO)2+2H2O. Если есть сомнения по цвету растворов (синий или голубой) , то пробирку с кислотой можно определить по растворению в ней оксида меди (I), полученного по реакции с глюкозой.
Уксусный альдегид прореагирует при н. у. , как глюкоза при нагревании.
P.s. Вместо R подставьте соответствующие радикалы.
Экспериментальные задачи по распознаванию и получению глицерина, альдегида и глюкозы
1. Нам необходимо определить три вещества: глицерин (многоатомный спирт), альдегид, глюкозу (углевод).
Одной из характерных реакций для этих веществ является взаимодействие с Cu(OH)2.
Сначала получим гидроксид меди (II). Для этого к медному купоросу добавим немного раствора NаОН:
1) К образовавшемуся осадку прильем немного альдегида и нагреем смесь:
В результате образуется красный осадок Сu2O ↓ .
2) Теперь к Cu(OH)2 добавим по каплям глицерин и смесь взболтаем. Осадок растворяется, получается раствор ярко-синего цвета. Образуется устойчивый комплекс глицерина с медью:
3) Глюкоза по своим химическим свойствам является альдегидоспиртом, т.е. она проявляет свойства и альдегидов, и многоатомных спиртов. Как альдегид, она вступает в реакции, характерные для этого класса веществ, в частности при нагревании взаимодействует с Cu(OH)2 с образованием красно-коричневого осадка Сu2O. Как многоатомный спирт, глюкоза дает раствор ярко-синего цвета при добавлении к ней свежего осадка Cu(OH)2:
Выпадает красный осадок Сu2O.
4) для определения трех данных веществ из каждой пробирки добавим немного Cu(OH)2. В двух пробирках образуется ярко-синий раствор (глюкоза и глицерин). Теперь нагреем все три смеси: в двух пробирках выпадет красный осадок (альдегид и глюкоза). Таким образом, мы узнаем, в какой пробирке какое вещество находится.
2. Машинное масло состоит, в основном, из предельных углеводородов, а растительное масло — из жиров, образованных непредельными кислотами. Растительное масло обесцвечивает бромную воду, а машинное — нет.
3. а) для получения простого эфира проведем реакцию дегидратации этилового спирта:
Образующий эфир называется диэтиловым. данная реакция проходит лишь при определенных условиях: нагревании, в присутствии H2SO4, и при избытке спирта.
б) для получения альдегида из спирта нужно использовать слабый окислитель, например, Сu 2+ :
Образуется уксусная кислота.
4. Сахар это сложное органическое вещество, содержащее достаточно большое количество углерода. Чтобы доказать это, возьмем немного сахара и добавим к нему Н2SO4 (конц.).
Сахар под действием концентрированной серной кислоты отдаст воду и превратится в углерод:
Концентрированная серная кислота Н2SO4 забирает воду у сахара, в результате получается свободный углерод (черное вещество).
5. а) для определения крахмала существует хорошая качественная реакция с иодом. Образуется устойчивый комплекс ярко-синего цвета.
Капнем несколько капель раствора иода на картофель и белый хлеб. Если на продуктах образуется синее пятно, то они содержат крахмал.
б) для проверки яблока на содержание глюкозы приготовим несколько капель яблочного сока, добавим немного синего осадка Cu(OH)2. Если исследуемый раствор содержит глюкозу, то сначала мы получим синий растворимый комплекс глюкозы, который при нагревании разложится до красного Сu2O.
6. а) Сначала определим крахмал, добавив к каждому из трех веществ раствор иода. В пробирке с крахмалом образуется синий комплекс. Глюкозу от сахарозы можно отличить за счет альдегидных свойств. Оба вещества обладают свойствами многоатомного спирта, но только глюкоза обладает еще и свойствами альдегида. добавим в обе пробирки Cu(OH)2, образуется синий раствор. Но только при нагревании с глюкозой выпадает красный осадок Сu2O (т.е. происходит окисление альдегидной группы).
б) Сначала определим крахмал с помощью иода. Образуется синий комплекс.
Теперь проверим кислотности растворов мыла и глицерина. Глицерин имеет слабокислую среду, а мыло — щелочную.
Глицерин также образует с Cu(OH)2 синий раствор (свойство многоатомных спиртов).
7. Нагреем полученные растворы. В одной из пробирок выпадет белый осадок — происходит денатурация белка. С глицерином при нагревании ничего не происходит.
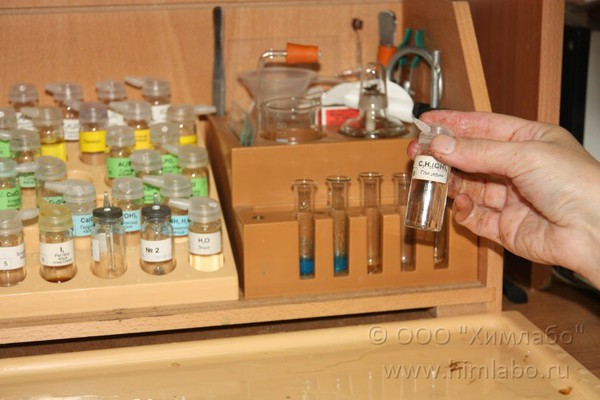
Качественная реакция на глицерин
При проведении опыта используем Микролабораторию для химического эксперимента
Цель опыта: изучить качественную реакцию на глицерин.
Оборудование: пробирки (2 шт.).
Реактивы: раствор гидроксида натрия NaOH, раствор сульфата меди(II) CuSO4, глицерин C3H5(OH)3.
Ход работы
1. В две пробирки вносим по 20-25 капель сульфата меди(II).
2. Добавляем к нему избыток гидроксида натрия.
3. Образуется осадок гидроксида меди(II) голубого цвета.
4. В одну пробирку по каплям добавляем глицерин.
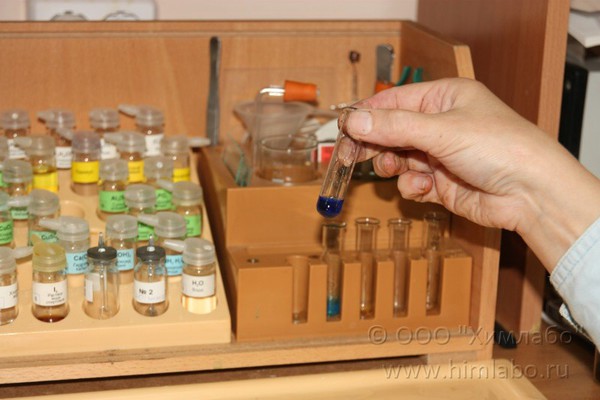
5. Встряхиваем пробирку до исчезновения осадка и образования темно-синего раствора глицерата меди(II).
6. Сравниваем окраску раствора с окраской гидроксида меди(II) в контрольной пробирке.
Вывод:
Качественной реакцией на глицерин является его взаимодействие с гидроксидом меди (II).
Оказываем содействие в подготовке технических требований для тендерной документации.
Внимание! Изображение товара может отличаться от полученного Вами товара. Производитель оставляет за собой право изменять комплектацию и технические характеристики товара без предварительного уведомления без ухудшения функциональных и качественных показателей. Информация о товаре носит справочный характер и не является публичной офертой, определяемой Статьей 437 ГК РФ.
Убедительная просьба, при покупке учебного оборудования согласовывать с менеджером важные для Вас характеристики, комплектацию и цену учебного оборудования.
как химическим путем доказать, что в пробирке находится раствор глицерина?
Опишите действия и наблюдения запишите уравнения необходимых реакций.
1, Качественной реакцией на глицерин является образование ярко-синего раствора глицерата меди ,
Налить в пробирку 2 мл раствора гидроксида натрия и добавить немного раствора сульфата меди (II) до выпадения осадка. К голубому осадку прилить немного глицерина – будем наблюдать растворение осадка и ярко синее окрашивание раствора.
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 – голубой осадок
Сu(OH)2 + CH2(OH) -CH(OH) – CH2(OH) = CH2(OH) – CH(O-Cu-O)CH2 + 2H2O –
ярко синий раствор глицерата меди
[spoiler title=”источники:”]
http://www.himlabo.ru/experiments/kachestvennaya-reaktsiya-na-glitserin
http://sprashivalka.com/tqa/q/22817501
[/spoiler]
в двух пробирках находятся глицерин и сахароза. как определить,что где?
Если речь идёт об индивидуальных веществах, то их легко можно различить по агрегатному состоянию: при комнатной температуре глицерин является жидкостью, сахароза – кристаллическим веществом.
Если речь идёт о водных растворах, то пробу надо предварительно подогреть с небольшим количеством минеральной кислоты (при этом из сахарозы образуются глюкоза и фруктоза), затем нейтрализовать и провести качественную реакцию на альдегидную группу с аммиачным раствором оксида серебра или гидроксидом меди(II). Если в исходной пробе была сахароза, то реакция на альдегидную группу будет положительной, если глицерин – отрицательной.
Сахароза
Со свежеприготовленым гидроксидом меди..
Глицерин и сахароза не восстанавливают гидроксид меди(II). Поэтому получатся практически неотличимые друг от друга тёмно-синие растворы глицерата и сахарата меди.
- Главная
- Опыты
-
Качественная реакция на глицерин
При проведении опыта используем
Микролабораторию для химического эксперимента
Цель опыта: изучить качественную реакцию на глицерин.
Оборудование: пробирки (2 шт.).
Реактивы: раствор гидроксида натрия NaOH, раствор сульфата меди(II) CuSO4, глицерин C3H5(OH)3.
Ход работы
1. В две пробирки вносим по 20-25 капель сульфата меди(II).
2. Добавляем к нему избыток гидроксида натрия.
3. Образуется осадок гидроксида меди(II) голубого цвета.
4. В одну пробирку по каплям добавляем глицерин.
5. Встряхиваем пробирку до исчезновения осадка и образования темно-синего раствора глицерата меди(II).
6. Сравниваем окраску раствора с окраской гидроксида меди(II) в контрольной пробирке.
Вывод:
Качественной реакцией на глицерин является его взаимодействие с гидроксидом меди (II).
Как определить глицерин
В состав многих парфюмерных и косметических средств входит глицерин, который оказывает благоприятное воздействие на кожу. Это различные крема, мази, моющие средства. Не менее востребован глицерин в медицинской, пищевой и химической промышленности. Представляет собой прозрачную жидкость без характерных визуальных признаков. Как же определить глицерин, если, например, этикетка от склянки утрачена?

Вам понадобится
- – пробирки;
- – глицерин;
- – щелочь (гидроксид натрия или калия);
- – сульфат меди (II).
Инструкция
Глицерин – это органическое вещество, которое относится к классу многоатомных спиртов, в частности трехатомному. Это значит, что он имеет в своем составе три гидроксильные группы. По своим физическим свойствам глицерин обладает вязкостью и не имеет запаха. Получил свое название за сладкий вкус. Слово «гликос» переводится как сладкий, потому отсюда и его название – глицерин.
Для определения глицерина достаточно провести качественную реакцию, которая достоверно укажет на наличие определяемого соединения в склянке. Для этого используют свежеприготовленный раствор гидроксида меди (II), который с глицерином дает растворение осадка, а раствор приобретает красивую синюю окраску.
Возьмите пробирку, налейте в нее 2 мл раствора сульфата меди (II), после чего понемногу добавляйте раствор гидроксида натрия или калия (щелочи). В результате реакции будете наблюдать выпадение осадка сине-голубого цвета за счет образования гидроксида меди (II).
В другую пробирку налейте 2 мл глицерина, разбавьте его 4 мл дистиллированной воды, закройте пробирку пробкой и встряхните для более качественного перемешивания. К свежеприготовленному осадку гидроксида меди (II) осторожно прилейте раствор глицерина, закройте пробирку пробкой и тщательно взболтайте полученную смесь.
Осадок практически сразу растворяется, а в результате реакции образуется раствор насыщенного ярко-синего цвета, что происходит за счет образования комплексного соединения глицерата меди (II). Это и есть самая простая качественная реакция, подтверждающая наличие глицерина.
Обратите внимание
При выполнении опыта обязательно соблюдайте правила техники безопасности, особенно при работе со щелочами. При попадании щелочи на кожу промойте пораженную поверхность большим количеством воды и обработайте слабым раствором борной или лимонной кислоты.

Связанная статья
Глицерин для красоты кожи
Источники:
- глицерин гидроксид меди
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.