| Глюкоза[1] | |
|---|---|
 |
|
| Общие | |
| Систематическое наименование |
(2R,3S,4R,5R)-2,3,4,5,6-пентагидроксигексаналь (D-глюкоза), (2S,3R,4S,5S)-2,3,4,5,6-пентагидроксигексаналь (L-глюкоза) |
| Традиционные названия | Глюкоза, декстроза |
| Хим. формула | C6H12O6 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 180,16 г/моль |
| Плотность | 1,5620 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления |
α-D-глюкоза: 146 °C (моногидрат: 83 °C) β-D-глюкоза: 148–150 °C |
| Химические свойства | |
| Растворимость | |
| • в воде |
32,3 г/100 мл (0 °C) 562 г/100 мл (90,8 °C) |
| • в 80 % этаноле | 2 г/100 мл |
Вращение ![{displaystyle [alpha ]_{D}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/429fc012b121ba581ec80c25ca5c4e5635452410) |
α-D-глюкоза: +112,2° β-D-глюкоза: +18,7° |
| Структура | |
| Дипольный момент | 14,1 Д |
| Классификация | |
| Рег. номер CAS |
50-99-7 (D-глюкоза) 921-60-8 (L-глюкоза) |
| PubChem | 5793 |
| Рег. номер EINECS | 200-075-1 |
| RTECS | LZ6600000 |
| ChEBI | 17234 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Глюко́за, или виноградный сахар, или декстроза (D-глюкоза), C6H12O6 — органическое соединение, моносахарид (шестиатомный гидроксиальдегид, гексоза), один из самых распространённых источников энергии в живых организмах[2]. Встречается в соке многих фруктов и ягод, в том числе и винограда, от чего и произошло название этого вида сахара. Глюкозное звено входит в состав полисахаридов (целлюлоза, крахмал, гликоген) и ряда дисахаридов (мальтозы, лактозы и сахарозы), которые в пищеварительном тракте быстро расщепляются на мономеры: например, сахароза — на глюкозу и фруктозу, лактоза — на глюкозу и галактозу, и т. д.
Этимология[править | править код]
Название «глюкоза» было дано в 1838 году Жаном-Батистом Дюма, в основу легло греческое слово «gleukos», что означает «сладкий»[уточнить]. Фридрих Август Кекуле предложил термин «декстроза», поскольку в водном растворе глюкозы плоскость линейно-поляризованного света повернута вправо, а «dexter» на латыни означает «правый»[3].
История[править | править код]
Вероятно, глюкоза известна человеку с древних времён, поскольку она кристаллизуется из мёда. Однако в чистом виде её выделили гораздо позже: немецкий химик Андреас Маргграф получил её в 1747 году из виноградного сока. Жозеф Луи Пруст в 1801 году осадил кристаллы α-D-глюкозы из того же виноградного сока. Благодаря этим экспериментам за глюкозой закрепилось название виноградного сахара[4].
Использование глюкозы в качестве подсластителя связано с тем, что во время Наполеоновских войн были заблокированы поставки тростникового сахара из Вест-Индии. Ещё в 1000 году до н. э. в Китае из крахмала (ферментацией риса) получали искусственный подсластитель — дисахарид мальтозу. К концу XVIII в. в Европе было известно, что крахмал можно обработать кислотой и получить сладкое вещество. Именно это позволило К. С. Кирхгофу нагреванием картофельного крахмала с серной кислотой получить сладкое сиропообразное вещество. В результате оптимизации процесса он получил сироп, который кристаллизовался при стоянии. Кроме того, была предпринята попытка прессовать получаемую массу в твёрдый продукт и в таком виде продавать. Однако организовать производство не удалось, поскольку Наполеон потерпел поражение и поставки сахара были восстановлены[4].
Процесс получения глюкозы исследовал французский химик Соссюр. Он выяснил, что крахмал подвергается гидролизу, при котором разрушаются связи между углеводными фрагментами, причём на каждый разрыв расходуется по одной молекуле воды. Также было обнаружено, что конфеты, производимые из сиропов глюкозы, не такие сладкие, как те, что получают из сахарозы. Поэтому в Германии и других странах Европы было организовано производство глюкозы[4].
В то время промышленная глюкоза была недостаточно чистой и получалась в виде сиропов. Её приходилось многократно кристаллизовать из воды или использовать органические растворители. Единственной твёрдой формой, которую выпускали в большом количестве, была литая глюкоза: сироп заливали в формы, где он затвердевал[4].
В 1923 году в США Уильям Б. Ньюкирк (англ. William B. Newkirk) запатентовал промышленный способ получения глюкозы. Этот способ отличался тщательным контролем условий кристаллизации, благодаря чему глюкоза выпадала из раствора в виде чистых, крупных кристаллов[4].
Строение молекулы[править | править код]
Глюкоза принадлежит к классу альдогексоз, то есть является полигидроксиальдегидом, содержащим шесть атомов углерода, альдегидную группу и пять гидроксильных групп. Четыре атома углерода в её структуре являются хиральными, поэтому существует 16 стереоизомерных альдогексоз: некоторые встречаются в природе, некоторые получены синтетически. Конкретную конфигурацию хиральных центров глюкозы в конце XIX в. установил немецкий химик Эмиль Фишер. Он сделал это при помощи реакций наращивания и деградации углеродной цепи сахаров. Наряду с наиболее распространённым в природе моносахаридом D-глюкозой существует также её энантиомер L-глюкоза, который в природе практически не встречается[5][6].

D-глюкоза (слева) и L-глюкоза (справа)
Часто D-глюкозу изображают в линейной форме, однако в действительности D-глюкоза существует в циклической форме, образованной в результате присоединения ОН-группы при углероде С-5 к альдегидной группе. Образующийся при этом циклический полуацеталь устойчив: в растворах и кристаллической форме D-глюкоза более чем на 99 % находится в форме полуацеталя. В общем такую форму называют пиранозной (от названия пирана — шестичленного гетероцикла с одним атомом кислорода), а циклическую D-глюкозу называют D-глюкопиранозой[7].
При описанной циклизации возникает новый стереоцентр при полуацетальном атоме углерода, поэтому D-глюкопираноза может существовать в виде двух диастереомеров, называемых аномерами: α-D-глюкопиранозы и β-D-глюкопиранозы (или кратко: α-D-глюкозы и β-D-глюкозы; α-аномера и β-аномера). Изображать циклические формы углеводов удобно при помощи проекций Хеуорса — идеализированных шестичленных циклов с заместителями над и под плоскостью цикла[7][6].
|
|
|
Наиболее близко к истине структуру молекулы глюкозы можно изобразить, используя конформацию «кресло». В таком представлении все гидроксильные группы D-глюкопиранозы находятся в экваториальных положениях (кроме аномерной, которая может находиться в экваториальном либо аксиальном положении в зависимости от аномера). Экваториальные положения более выгодны по сравнению с аксиальными: это объясняет, почему глюкоза является наиболее распространённым моносахаридом[7].
|
|
|
В растворах α-D-глюкопираноза и β-D-глюкопираноза существуют в равновесии и взаимопревращаются через образование открытоцепной формы. Равновесная доля α-аномера при 31 °C составляет 38 %, а более устойчивого β-аномера — 62 %[8]. Чистые аномеры можно получить в кристаллическом виде: α-аномер кристаллизуется из воды в виде моногидрата, а β-аномер кристаллизуется из пиридина[9].

Физические свойства[править | править код]
Глюкоза — бесцветное кристаллическое вещество без запаха. Обладает сладким вкусом. D-глюкоза представлена в виде трёх кристаллических форм: безводной α-D-глюкопиранозы, моногидрата α-D-глюкопиранозы и безводной β-D-глюкопиранозы (хотя описан также моногидрат β-D-глюкопиранозы). Безводные формы имеют орторомбические кристаллы, а гидрат — моноклинные[8]. Все три формы отличаются температурой плавления: α-аномер плавится при 146 °C, его моногидрат — при 83 °C, β-аномер — при 148—150 °C[9].
Аномеры D-глюкопиранозы оптически активны: удельное вращение α-аномера составляет +112,2°, β-аномера — +18,9°[9]. Оба аномера при растворении претерпевают мутаротацию, то есть превращаются в равновесную смесь, состоящую из 62 % β-аномера и 38 % α-аномера[8]. Удельное вращение этой смеси составляет +52,7°[9].
Получение[править | править код]
Производство глюкозных сиропов[править | править код]
Кислотный гидролиз крахмала[править | править код]

Единственным сырьём для производства глюкозы является крахмал, хотя делаются попытки использовать другой природный полимер глюкозы — целлюлозу. Основным источником крахмала является кукуруза: 100 % глюкозных подсластителей в США и 84 % в Японии производят из кукурузного крахмала. Также 70 % производимой в мире кукурузы идёт на производство глюкозы. В Европе постепенно возрастает использование пшеничного крахмала, хотя в основном используется также кукурузный крахмал. В Австралии глюкозу получают только из пшеничного крахмала. В Азии используют крахмал из саго, тапиоки и кукурузы[10].
Для получения глюкозы крахмал гидролизуют в присутствии кислот или ферментов. При этом происходит разрыв связей между глюкозными звеньями полимерных амилозы и амилопектина — компонентов крахмала — и образуется мономер (D-глюкоза) с некоторым содержанием димеров: мальтозы и изомальтозы. Для кислотного гидролиза готовят суспензию крахмала в воде (30-40 мас. %) и доводят pH до 2 или ниже. При атмосферном давлении кислотный гидролиз протекает 6 ч, однако современные установки позволяют проводить процесс при повышенном давлении и, соответственно, более высокой температуре. При давлении 415—620 кПа и температуре до 160 °C крахмал гидролизуется в течение нескольких минут. Останавливают реакцию добавлением нейтрализующего реагента (обычно карбоната натрия), и pH повышается до 4-5,5[11].
После гидролиза нерастворимые примеси, которые изначально присутствовали в крахмале, отделяют центрифугированием или фильтрованием, а растворимые примеси удаляют активированным углём и ионообменными смолами. Смолы также позволяют обесцветить полученную глюкозу. Конечный раствор упаривают. Большинство глюкозных сиропов продают в виде 70-85 % растворов, хотя их можно упарить и до твёрдого состояния[11].
Глюкозные сиропы отличаются по степени гидролиза крахмала: её оценивают по количеству присутствующих в конечном продукте восстанавливающих сахаров и выражают в декстрозных эквивалентах (DE). Интересно, что кислотный гидролиз является в целом случайным процессом, однако в данном случае при одинаковой степени конверсии получается очень воспроизводимый углеводный состав конечного продукта. В некоторых случаях этот факт является нежелательным ограничением, потому что производителю может понадобиться более гибко регулировать углеводный состав. Из-за этого в промышленности стали использовать ферментативный гидролиз крахмала[11].
Ферментативный гидролиз крахмала[править | править код]
Ферментативный гидролиз используют как дополнение к кислотному. Изначально таким способом пытались повысить степень конверсии и получить более сладкий и менее вязкий сироп с большим содержанием глюкозы. Однако ферментативный гидролиз позволяет также регулировать соотношение глюкозы и мальтозы в продукте. Для проведения ферментативного гидролиза pH повышают до 4-6, а температуру снижают до 60-70 °C, затем вносят необходимые ферменты, которые подбирают исходя из потребностей по составу. Бактериальные α-амилазы случайным образом расщепляют α-1,4-гликозидные связи в крахмале. β-Амилазы и грибковые α-амилазы расщепляют те же связи, но дают преимущественно мальтозу. Глюкоамилаза отщепляет по одной молекуле глюкозы с невосстанавливающего конца, но может расщеплять также α-1,6-связи. Пуллуланаза расщепляет α-1,6-связи. По окончании процесса ферменты дезактивируют нагреванием или изменением pH[11].
Открытие термоустойчивых α-амилаз позволило разработать полностью ферментативные процессы и ещё более точно контролировать степень конверсии и углеводный состав продукта. Ферменты вносят в суспензию крахмала при pH 6-6,5, после чего суспензию нагревают паром до 103—107 °C и выдерживают в течение 5-10 мин, а затем 1-2 ч при 95 °C. После этого проводят вторичный ферментативный гидролиз, как и в случае кислотного гидролиза[11].
Производство общего сахара[править | править код]
Большая часть глюкозы продаётся в виде сиропов, но существует небольшая потребность также в твёрдой глюкозе. Её производят как в чистом виде, так и в виде общего сахара (англ. total sugars) — отверждённого гидролизата крахмала. Общий сахар может содержать значительное количество мальтозы (DE<20), быть практически чистой глюкозой (95-99 %), а также содержать определённый процент фруктозы[12].
Производство кристаллической глюкозы[править | править код]
Изначально чистую кристаллическую глюкозу производили из крахмала, гидролизованного в кислой среде. В таких условиях удавалось добиться только 88 % содержания глюкозы, поскольку в условиях гидролиза образовывались побочные продукты, связанные с мутаротацией и изомеризацией. С 1938 года начали использовать ферментативный гидролиз, который позволил получать более чистую глюкозу[13].
Моногидрат α-D-глюкозы получают кристаллизацией из перенасыщенных сиропов с содержанием твёрдого вещества в 74-79 %, из которого глюкоза составляет 95-96 %. Такие сиропы производят ферментативным гидролизом, нацеленным на максимальную конверсию. Сироп охлаждают до 46-50 °C и смешивают с затравочными кристаллами из предыдущей партии. Сироп медленно охлаждают до 20-40 °C в течение 2-5 дней: при этом около 60 % кристаллизуется в виде моногидрата α-D-глюкозы. Маточный раствор отделяют на центрифугах, кристаллы глюкозы промывают водой и там же сушат до максимально сухого состояния (14 % влаги). Затем их досушивают потоком горячего воздуха до 8,5-9 % влаги (теоретическое содержание воды в моногидрате — 9,08 %). Кристаллизации не мешает наличие примесей, поэтому маточный раствор концентрируют и получают вторую порцию кристаллов либо объединяют его со следующей партией сиропа. Извлечение моногидрата глюкозы из сиропа достигает 87,5 %. При повторных кристаллизациях из маточного раствора степень выделения повышается до 100 %[13].
Безводную α-D-глюкозу кристаллизуют при 60-65 °C в условиях вакуума и испарения растворителя. Исходные сиропы должны быть достаточно чистые. Цикл кристаллизации значительно короче, чем для моногидрата, и составляет 6-8 ч. Выделяют и сушат кристаллы примерно так же, как описано выше. Содержание воды в конечном продукте не превышает 0,1 %[13].
Безводную β-D-глюкозу получают кристаллизацией выше 100 °C. Дополнительные сложности связаны с тем, что β-D-глюкоза значительно лучше растворима в воде, чем α-D-глюкоза (72 % против 30 % при 25 °C)[13].
Химические свойства[править | править код]
Глюкоза может восстанавливаться в шестиатомный спирт (сорбит). Окисление глюкозы в зависимости от метода окисления может приводить к трём продуктам: глюконовой кислоте (окисление альдегидной группы), глюкаровой кислоте (дополнительно окисляется первичная OH-группа) либо глюкуроновой кислоте (окисление только первичной OH-группы)[9].
Как восстанавливающий сахар, глюкоза проявляет восстановительные свойства. Это проявляется в реакциях с реактивом Толленса (аммиачным раствором оксида серебра), реактивом Бенедикта и реактивом Фелинга (реагенты на основе меди)[источник не указан 579 дней].
Глюкоза обладает также некоторыми специфическими свойствами, такими как брожение — деструктивное разложение под действием ферментов. Возможны несколько типов брожения: спиртовое (образуется этанол и углекислый газ), молочно-кислое (образуется молочная кислота), масляное (образуется бутановая кислота, водород, углекислый газ). ацетоновое (образуется бутанол, ацетон, водород, углекислый газ), лимоннокислое-кислое (образуется лимонная кислота)[источник не указан 579 дней].
Биологическая роль[править | править код]
Глюкоза — основной продукт фотосинтеза, образуется в цикле Кальвина.
В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспечения метаболических процессов. Глюкоза является субстратом гликолиза, в ходе которого она может окислиться либо до пирувата в аэробных условиях, либо до лактата в случае анаэробных условий. Пируват, полученный таким образом в гликолизе, далее декарбоксилируется, превращаясь в ацетил-КоА (ацетилкоэнзим А). Также в ходе окислительного декарбоксилирования пирувата восстанавливается кофермент НАД+. Ацетил-КоА далее используется в цикле Кребса, а восстановленный кофермент используется в дыхательной цепи.
Глюкоза депонируется у животных в виде гликогена, у растений — в виде крахмала, полимер глюкозы — целлюлоза является основной составляющей клеточных оболочек всех высших растений.
У животных глюкоза помогает пережить заморозки. Так, у некоторых видов лягушек перед зимой повышается уровень глюкозы в крови, за счёт чего их тела способны выдержать заморозку во льду.
Применение[править | править код]
В медицине[править | править код]

Глюкозу используют при интоксикации (например, при пищевом отравлении и инфекциях), вводят внутривенно струйно и капельно, так как она является универсальным антитоксическим средством.
Глюкозу используют для целей регидратации организма, как источник углеводов, в том числе при парентеральном питании.
Также препараты на основе глюкозы и сама глюкоза используются эндокринологами при определении наличия и типа сахарного диабета у человека (в виде стресс-теста на ввод повышенного количества глюкозы в организм).
Глюкозу применяют в медицине как питательное вещество и компонент кровозаменяющих противошоковых жидкостей. Кроме того, в медицине широко применяется кальциевая соль глюконовой кислоты (глюконат кальция).
Для медицинских целей глюкоза обычно используется в виде раствора для инъекций или инфузий, а также в виде таблеток.
В пищевой промышленности[править | править код]
В пищевой промышленности глюкоза применяется при выпечке хлеба, в кондитерском деле, а также при производстве сгущённого молока, мороженого, простокваша, кефир. Также для производства спирта, вин, пива.
В сельском хозяйстве[править | править код]
В сельском хозяйстве глюкоза зачастую применяется для подкормки пчёл.
В химической промышленности[править | править код]
Глюкоза используется для получения витамина C (аскорбиновая кислота), сорбита и биополимеров.
Примечания[править | править код]
- ↑ Рабинович В. А., Хавин З. Я. Краткий химический справочник. — 2-е издание. — Химия, 1978.
- ↑ Степаненко Б. Н., Городецкий В. К.; Ковалев Г. В. (фарм.). Глюкоза // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1977. — Т. 6 : Гипотиреоз — Дегенерация. — С. 197—199. — 632 с. : ил.
- ↑ Sami Dridi. Nutritional Biochemistry: From the Classroom to the Research Bench. — Bentham Science Publishers, 2022. — С. 208-209. — 287 с. — ISBN 978-981-5051-58-2. Архивная копия от 15 мая 2022 на Wayback Machine
- ↑ 1 2 3 4 5 Ullmann, 2006, p. 45–48.
- ↑ Терней, 1981, с. 444–447.
- ↑ 1 2 Робертс Дж., Касерио М. Основы органической химии / Пер. с англ. Ю. Г. Бунделя, под ред. А. Н. Несмеянова. — М. : Мир, 1978. — С. 10–27.
- ↑ 1 2 3 Терней, 1981, с. 424–429.
- ↑ 1 2 3 Ullmann, 2006, p. 48.
- ↑ 1 2 3 4 5 Химическая энциклопедия, 1988.
- ↑ Ullmann, 2006, p. 49–51.
- ↑ 1 2 3 4 5 Ullmann, 2006, p. 51–56.
- ↑ Ullmann, 2006, p. 56.
- ↑ 1 2 3 4 Ullmann, 2006, p. 56–58.
Литература[править | править код]
- Линевич Л. И. Глюкоза // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А — Дарзана. — С. 589–590. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.
- Терней А. Современная органическая химия : в 2 т.. — М. : Мир, 1981. — Т. 2.
- Schenck F. W. Glucose and Glucose-Containing Syrups (англ.) // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2006. — doi:10.1002/14356007.a12_457.pub2.
- Ельницкий А. П. Химия : учеб. для 11-го кл. учреждений общ. средн. образования с рус.яз. обучения / А. П. Ельницкий, Е. И. Шарапа. — 3-е изд., пересмотр. и доп. — Минск : Нар. асвета, 2013. — 318 с. : ил. ISBN 978-985-03-1960-9
Ссылки[править | править код]
- 1Н и 13С ЯМР-спектры α-D-глюкозы. Sigma-Aldrich. Дата обращения: 9 апреля 2019.
- ИК-спектр α-D-глюкозы. Sigma-Aldrich. Дата обращения: 9 апреля 2019.
- КР-спектр α-D-глюкозы. Sigma-Aldrich. Дата обращения: 9 апреля 2019.

Описание
D-глюкоза безводная (декстроза, D(+)-Glucose anhydrous), культуральной чистоты
Универсальный источник энергии для живых клеток. Используется как компонент питательных сред. Проходит тест на апирогенность.
По желанию клиента, в НПП “ПанЭко” можно заказать более мелкую фасовку данного продукта.
Данный продукт предназначен для исследовательских целей.
Хранить при комнатной температуре.
Срок годности 48 мес.
- Белый порошок
- Формула C6H12O6
- Молекулярная масса 180,16 г/моль
- Чистота (ВЭЖХ) 99%
Характеристики
-
Стерильность:
– -
Документы:
Для исследовательских целей -
Форма выпуска:
Порошок -
Упаковка:
1 кг, 100 г, 5 кг, 500 г -
Чистота:
Для клеточной биологии
- Фасовка: 25 кг мешки
- Квалификация: Имп. «хч»
- CAS №: 5996-10-1
- Синонимы: виноградный сахар, Глюкоза кристаллическая гидратная, 6-(гидроксиметил) оксан, -2,3,4,5-тетрол, (2R,3S,4R,5R)-6 -(гидроксиметил) тетрагидро-2H-пиран- 2,3,4,5-тетраол

- Квалификация: Имп. «хч»
- Синонимы: виноградный сахар, Глюкоза кристаллическая гидратная, 6-(гидроксиметил) оксан, -2,3,4,5-тетрол, (2R,3S,4R,5R)-6 -(гидроксиметил) тетрагидро-2H-пиран- 2,3,4,5-тетраол
- Класс опасности:
не опасна; группа упаковки III -
Гарантийный срок хранения продукта:
2 года - Производитель: Китай
-
Доп. информация:
Виноградный сахар, Глюкоза кристаллическая гидратная, 6-(гидроксиметил) оксан, -2,3,4,5-тетрол, (2R,3S,4R,5R)-6 -(гидроксиметил) тетрагидро-2H-пиран- 2,3,4,5-тетраол.
ПРИМЕНЕНИЕ:
Глюкоза 99,5% находит применение в различных отраслях:
- Пкондитерской промышленности при изготовлении мягких конфет, десертных сортов шоколада, тортов и различных диетических изделий,
- Хлебопечении глюкоза улучшает условия брожения, придает пористость и хороший вкус изделиям, замедляет очерствение,
- Производстве мороженого она занижает точку замерзания, увеличивает его твердость,
- Производстве фруктовых консервов, соков, ликеров, вин, безалкогольных напитков, так как глюкоза не маскирует аромата и вкуса,
- Молочной промышленности при изготовлении молочных продуктов и продуктов детского питания,рекомендуется использовать глюкозу в определенной пропорции с сахарозой для придания этим продуктам более высокой питательной ценности,
- Ветеринарии,
- Птицеводстве,
- Фармацевтической промышленности.
- Пищевой промышленности, как заменитель сахарозы,
- Кондитерской промышленности при изготовлении мягких конфет, десертных сортов шоколада, тортов и различных диетических изделий,
- Хлебопечении глюкоза улучшает условия брожения, придает пористость и хороший вкус изделиям, замедляет очерствение,
- Производстве мороженого она занижает точку замерзания, увеличивает его твердость,
- Производстве фруктовых консервов, соков, ликеров, вин, безалкогольных напитков, так как глюкоза не маскирует аромата и вкуса,
- Молочной промышленности при изготовлении молочных продуктов и продуктов детского питания,рекомендуется использовать глюкозу в определенной пропорции с сахарозой для придания этим продуктам более высокой питательной ценности,
- Ветеринарии,
- Птицеводстве,
- Фармацевтической промышленности.
 На сегодняшний день наша компания предлагает 2 вида глюкозы (декстроза): безводная (фармакопейная) и 1-водная (пищевая).
На сегодняшний день наша компания предлагает 2 вида глюкозы (декстроза): безводная (фармакопейная) и 1-водная (пищевая).
– Глюкоза безводная (фармакопейная) в химической промышленности более известна под названием «ангидридная декстроза». По внешним характеристикам это порошок белого цвета, состоящий из белых кристаллов. Цена безводной глюкозы 120 рублей за килограмм (2.1 доллара). Применяется в основном в медицине.
– Глюкозу пищевую (1 водная) применяют в основном в пищевой промышленности для выпекания хлеба, кондитерских изделий, производства мороженного и др. видов продукции. Состав такой глюкозы это жидкое прозрачное вещество. Стоимость пищевой глюкозы 55 рублей за килограмм (0.9 доллара).
В природе данное вещество встречается во многих живых организмах, его также получают и в лабораторных условиях путем гидролиза крахмала (картофельного и кукурузного). Остаток данного вида глюкозы является одной из составляющих следующих веществ:
- Олигосахаридов;
- Полисахаридов;
- Липополисахаридов;
- Гликопротеинов и пр.
Глюкоза ангидрид является сахаридом, широко применяется во многих сферах и отраслях.
Сферы применения глюкозы ангидрида
Наиболее значимым является использование глюкозы в производстве пищевых продуктов. Так многие предприятия пищевой промышленности приобретают глюкозу оптом для дальнейшего добавления в продукты диетического питания. Кроме того, глюкоза безводная придает мягкость кондитерским изделиям, например, батончиками и конфетам, а также усиливает их вкусовые качества. Многие производители безалкогольных напитков также используют в больших количествах глюкозу, которая является достаточно недорогим заменителем сахара.
Данное вещество также применяется в процессе производства этанола, биотина и аскорбиновой кислоты. Благодаря своим питательным свойствам ангидрид входит в состав многих жидкостей, которые используются в медицине для предотвращения кровопотерь.
Где приобрести глюкозу оптом
Наша компания предлагает ознакомиться с выгодными предложениями по продаже безводной и 1 – водной глюкозы. Продукт, представленный на нашем сайте, отвечает ГОСТу, а также сопровождается гарантией производителя. Мы предлагаем сравнительно невысокие цены на глюкозу в Москве оптом, в чем вы сможете убедиться лично. Купить декстрозу по низким ценам от производителя с доставкой очень просто! Позвоните по телефону указанному на сайту или закажите обратный звонок.
Транспортировка глюкозы возможна любыми видами транспорта и осуществляется в специальных герметичных бумажных и сварных полиэтиленовых мешках. Хранить продукт следует на складах, к которым ограничен доступ влаги.
- Фасовка: 25 кг мешки
Доставка глюкоза моногидрат,пищевая (dextrose monohydrate),рф осуществляется по Москве и МО – 1
рабочий день. По России от 2х рабочих дней.
Доставка груза в труднодоступные районы обговаривается по тел.
+7 (495) 136-20-72
Цена на глюкоза моногидрат,пищевая (dextrose monohydrate),рф
начинается от 110,0 руб/кг* . Оптовая стоимость глюкоза моногидрат,пищевая (dextrose monohydrate),рф зависит от кол-ва заказываемой
химической продукции. Для постоянных клиентов действуют хорошие скидки!
![]()
Компания «Стандарт» осуществляет продажу
глюкоза моногидрат,пищевая (dextrose monohydrate),рф физическим и юридическим лицам в Москве и
Московской области. А так же осуществляет доставку во все крупные города России:
Санкт-Петербург, Самара, Екатеринбург, Новосибирск, Казань, Омск, Волгоград,
Краснодар и многие другие на специальных условиях.
Купить глюкоза моногидрат,пищевая (dextrose monohydrate),рф оптом и в розницу или заказать
актуальный прайс вы можете позвонив по номеру телефона
+7 (495) 136-20-72
Популярные химреагенты от нашей компании
Доставка груза по всей россии
Компания ООО «Стандарт» занимается быстрой поставкой химических
реактивов, соответствующих всем требованиям ГОСТа и ТУ. У нас можно
не только купить химические реактивы около 300 наименований, но и
заказать пищевые добавки или поставку химреактивов для сельского
хозяйства и животноводства.
Вы можете купить у нас химические реактивы выгоднее, чем у других
поставщиков химической продукции, при том, что вам не придется
экономить на качестве химреактивов: компания располагает большими
вместительными складами и может позволить себе честные цены на
химреактивы.
подробнее
Спецпредложения
-
Натрий лимоннокислый Е,331 – 1,18 дол/кг
-
Натрий ацетат б/в – Е262 – 1,8 дол
-
Натрий эриторбат Е316 – 2,0 дол
-
Железо лимоннокислое – 15000,0 р/кг
-
Калий-натрий виннокислый 4-водный, е-334
-
Лактоза моногидрат (сахар молочный), пищевая
-
Натрий карбонат безводный пищевой е500i
-
Сахароза
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ
МИКРОМЕТОДОМ ХАГЕДОРНА-ИЕНСЕНА
Метод основан на реакции окисления глюкозы (и других углеводов) гексациано-(III) ферратом калия в слабощелочной среде до глюконовой кислоты. Гексациано-(III) феррат калия восстанавливается до гексациано-(II) феррата. Гексациано-(III) феррат калия берут в избытке и неиспользованный остаток его определяют иодометрически в кислой среде. К пробам прибавляют иодид калия, выделившийся иод оттитровывают тиосульфатом натрия.
Реактивы и оборудование
─ 0,045% раствор сульфата цинка.
─ 0,1 и раствор гидроксида натрия.
─ Щелочной раствор гексациано-(III) феррата калия (1,65 г K3[Fe(CN)6] и 10,6 г безводного карбоната натрия доводят водой до 1 л).
─ Реактив А (10 г сульфата цинка и 50 г хлорида натрия доводят водой до 200 мл).
─ Реактив Б (к 40 мл реактива А перед использованием добавляют 1 г иодида калия).
─ 3%-ная уксусная кислота.
─ 0,005 и тиосульфат натрия.
─ Колбы для титрования, воронки, баня водяная, пипетки, пробирки, вата гигроскопическая.
Ход работы
Подписывают 2 опытные и 2 контрольные пробирки и прибавляют реагенты по схеме, приведённой на с.30.
Содержание глюкозы рассчитывают по таблице на с. 31.
Затем из содержания глюкозы в опытной пробе вычитают содержание глюкозы в контрольной пробе и по найденной разности находят количество глюкозы в 100 мл крови:
x = разность * 100 / 0,1 (мг).
Схема прибавления реактивов для определения содержания глюкозы
| № | Операция | Опыт | Контроль |
| 1. | Дистиллированная вода | – | 0,1 мл |
| 2. | Сыворотка | 0,1 мл | – |
| 3. | 1 мл 0,1 и NaOH и 4 мл 0,45% ZnNO4 | + | + |
| 4. | Инкубация на кипящей водяной бане | 3 мин. | 3 мин. |
| 5. | Фильтрование в колбу для титрования | + | + |
| 6. | Щелочной раствор K3[Fe(CN)6] | 2 мл | 2 мл |
| 7. | Инкубация на кипящей водяной бане | 15 мин. | 15 мин. |
| 8. | Охлаждение до комнатной температуры | + | + |
| 9. | 3 мл реактива Б, 2 мл 3% уксусной кислоты, 5-6 капель раствора крахмала | + | + |
| 10. | Титрование раствором тиосульфата | + | + |
Содержание отчёта
| Объём тиосульфата натрия, израсходованного на титрование | Содержание глюкозы (мг) | |||
| опытных проб | контрольных проб | |||
| среднее | среднее | опыт | контроль | разность |
Содержание глюкозы в крови равно:
Количество миллилитров 0,005 и раствора тиосульфата и соответствующее им количество миллиграмм глюкозы при использовании 2 мл 0,005 и раствора гексациано-(III) феррата калия:
| Объём раствора тиосульфата ( в мл) | ||||||||||
| 0,00 | 0,01 | 0,02 | 0,03 | 0,04 | 0,05 | 0,06 | 0,07 | 0,08 | 0,09 | |
| 0,0 | 0,385 | 0,382 | 0,379 | 0,376 | 0,373 | 0,370 | 0,367 | 0,364 | 0,361 | 0,358 |
| 0,1 | 0,355 | 0,352 | 0,350 | 0,348 | 0,345 | 0,343 | 0,341 | 0,338 | 0,336 | 0,333 |
| 0,2 | 0,331 | 0,329 | 0,327 | 0,325 | 0,323 | 0,321 | 0,318 | 0,316 | 0,314 | 0,312 |
| 0,3 | 0,310 | 0,308 | 0,306 | 0,304 | 0,302 | 0,300 | 0,298 | 0,296 | 0,294 | 0,292 |
| 0,4 | 0,290 | 0,288 | 0,286 | 0,284 | 0,282 | 0,280 | 0,278 | 0,276 | 0,274 | 0,272 |
| 0,5 | 0,270 | 0,268 | 0,266 | 0,264 | 0,262 | 0,260 | 0,259 | 0,257 | 0,255 | 0,253 |
| 0,6 | 0,251 | 0,249 | 0,247 | 0,245 | 0,243 | 0,241 | 0,240 | 0,238 | 0,236 | 0,234 |
| 0,7 | 0,232 | 0,230 | 0,228 | 0,226 | 0,224 | 0,222 | 0,221 | 0,219 | 0,217 | 0,215 |
| 0,8 | 0,213 | 0,211 | 0,209 | 0,208 | 0,206 | 0,204 | 0,202 | 0,200 | 0,199 | 0,197 |
| 0,9 | 0,195 | 0,193 | 0,191 | 0,190 | 0,188 | 0,186 | 0,184 | 0,182 | 0,181 | 0,179 |
| 1,0 | 0,177 | 0,175 | 0,173 | 0,172 | 0,170 | 0,168 | 0,166 | 0,164 | 0,163 | 0,161 |
| 1,1 | 0,159 | 0,157 | 0,155 | 0,154 | 0,152 | 0,150 | 0,148 | 0,146 | 0,145 | 0,143 |
| 1,2 | 0,141 | 0,139 | 0,138 | 0,136 | 0,134 | 0,132 | 0,131 | 0,129 | 0,127 | 0,125 |
| 1,3 | 0,124 | 0,122 | 0,120 | 0,119 | 0,117 | 0,115 | 0,113 | 0,111 | 0,110 | 0,108 |
| 1,4 | 0,106 | 0,104 | 0,102 | 0,101 | 0, 099 | 0, 097 | 0, 095 | 0, 093 | 0, 092 | 0, 090 |
| 1,5 | 0,088 | 0,086 | 0,084 | 0,083 | 0,081 | 0,079 | 0,077 | 0,075 | 0,074 | 0,072 |
| 1,6 | 0,070 | 0,068 | 0,066 | 0,065 | 0,063 | 0,061 | 0,059 | 0,057 | 0,056 | 0,054 |
| 1,7 | 0,052 | 0,050 | 0,048 | 0,047 | 0,045 | 0,043 | 0,041 | 0,039 | 0,038 | 0,036 |
| 1,8 | 0,034 | 0,032 | 0,031 | 0,029 | 0,027 | 0,025 | 0,024 | 0,022 | 0,020 | 0,015 |
| 1,9 | 0,017 | 0,015 | 0,014 | 0,012 | 0,010 | 0,008 | 0,007 | 0,005 | 0,003 | 0,002 |
Контрольные вопросы
- Напишите уравнения реакций, на которых основано определение глюкозы методом Хагедорна-Иенсена.
- О чём может свидетельствовать пониженное или повышенное содержание глюкозы в крови?
- Механизмы гормональной регуляции уровня глюкозы в крови.
Лабораторная работа №10
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ЛИПИДЫ
Ход работы
Опыт 1. Выделение лецитина из яичного желтка
К 1/6 части яичного желтка добавляют 5-7 мл кипящего этанола и тщательно перемешивают в течение 5-10 мин. Затем жидкость фильтруют в сухую пробирку через сухой фильтр.
Опыт 2. Получение эмульсии лецитина
К 5 каплям спиртового раствора лецитина прибавляют 20-30 капель воды. Образуется эмульсия лецитина в воде.
Опыт 3. Осаждение лецитина
К 5 каплям спиртового раствора лецитина прибавить 1-2 капли насыщенного спиртового раствора хлористого кадмия. Наблюдать образование осадка нерастворимого соединения лецитина.
Опыт 4. Гидролиз лецитина
К 5-10 каплям спиртового раствора лецитина добавляют такой же объём 10% раствора NaOH и кипятят 5 мин. Лецитин при этом распадается на глицерин, жирные кислоты, холин и фосфорную кислоту. Из холина образуется триметиламин, который обнаруживается по запаху селёдочного раствора.
Опыт 5. Реакция на холестерин
К 10 каплям хлороформного раствора холестерина или растительного масла прибавляют равный объём концентрированной серной кислоты (осторожно, по стенке). При лёгком встряхивании на границе двух слоёв жидкости образуется оранжевое кольцо, которое при стоянии переходит в красное. Нижний слой серной кислоты приобретает зеленую флюоресценцию.
Содержание отчёта
Полученные результаты заносят в таблицу:
| Реакция | Наблюдаемый эффект |
Контрольные вопросы
- Перечислите представителей класса липидов, имеющих непосредственное отношение к образованию биомембран. Обьясните почему именно эти липиды.
- Напишите уравнение гидролиза лецитина.
- Почему для осаждения лецитина используется спиртовой, а не водный раствор хлорида кадмия?
- В нервной ткани относительное содержания липидов выше, чем в любой другой
- ( разумеется кроме жировой ткани). Попытайтесь дать этому факту обяьснение.
Уравнение гидролиза лецитина:
Контроль качества лекарственных средств, изготовляемых в аптеках (стр. 16 )
 |
Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |

9.5.1 Раствор глюкозы 5, 10, 20, 25% для инъекций.
Раствор глюкозы 5, 10, 20, 25% для инъекций.
Глюкозы безводной 50, 100, 200, 250 г.
Раствор кислоты хлороводородной (0,1 моль/л) до рН 3,0-4,1-5 мл
Натрия хлорида 0,26 г.
Воды для инъекций до 1 л
К раствору глюкозы прибавляют стабилизатор Вейбеля в количестве 5% от общего объема раствора состава:
Натрия хлорида 5,2 г
Кислоты хлороводородной разведенной 4,4 мл
Воды для инъекций до 1 л
Описание. Прозрачная бесцветная жидкость.
1. К 0,5 мл раствора прибвляют 3мл реактива Фелинга и нагревают до кипения. Образуется кирпично-красный осадок.
2. Помещают 2-3 капли раствора в фарфоровую чашку и выпаривают на водяной бане досуха. После охлаждения к сухому остатку прибавляют 0,01 г тимола, 5-6 капель концентрированной серной кислоты и 2 капли воды. Появляется красно-фиолетовое окрашивание.
Хлорид-ион. К 1 мл раствора прибавляют по 2-3 капли кислоты азотной разведенной и раствора серебра нитрата. Образуется белый творожистый осадок, растворимый в растворе аммиака.
Натрий-ион. Графитовую палочку, смоченную раствором, вносят в бесцветное пламя. Пламя окрашивается в желтый цвет.
1. К 2-3 мл раствора прибавляют 1 каплю раствора метилового красного. Раствор окрашивается в красный цвет.
2. К 2-3 мл раствора прибавляют 1 каплю метилового оранжевого. Раствор окрашивается в розовый цвет. рН 3,0-4,1 (потенциометрически или по универсальной индикаторной бумаге).
Глюкоза (м. м. 180,14)
Содержание глюкозы (Х) в г в 1 мл раствора вычисляют по формуле:

Содержание глюкозы в 1 мл раствора должно быть 0,0485-0,0515; 0,097-0,103; 0,194-0,206; 0,242-0,258г.
5 мл раствора помещают в мерную колбу вместимостью 25 мл и доводят водой до метки.
1 мл разведения помещают в склянку с притертой пробкой, прибавляют 2,5 мл раствора йода (0,1 моль/л) УЧ (1/2 I2), 0,5 мл раствора натрия гидроксида (1 моль/л) и оставляют в темном месте на 5 минут. Затем прибавляют 0,5 мл кислоты серной разведенной. Избыток йода оттитровывают раствором натрия тиосульфата (0,1 моль/л). Индикатор – крахмал. Параллельно проводят контрольный опыт.
Определение стабилизатора в растворе глюкозы.
К 25 мл раствора прибавляют 1 каплю метилового красного и титруют раствором натрия гидроксида (0,02 моль/л) от красного до желтого окрашивания (А мл).
1 мл раствора натрия гидроксида (0,02 моль/л) соответствует 0,0007292 г хлороводорода. Содержание раствора хлороводородной кислоты (0,1 моль/л) (Х) в 1 мл раствора вычисляют по формуле:

 ,
,
где 0,003646 – содержание хлороводорода в 1 мл раствора кислоты хлороводородной (0,1 моль/л),
а – навеска лекарственной формы (25 мл).
Натрия хлорид и кислота хлороводородная.
К 2 мл раствора прибавляют 1-2 капли раствора калия хромата и титруют раствором серебра нитрата (0,02 моль/л) до появления красноватого осадка (Б, мл).
М. м. натрия хлорида 58,44
Содержание натрия хлорида (Х) в г в 1 мл вычисляют по формуле:

К 25 мл раствора глюкозы прибавляют 1-2 капли раствора калия хромата и титруют раствором серебра нитрата (0,1 моль/л) до появления красноватого осадка.
1 мл раствора серебра нитрата (0,1 моль/л) соответствует 0,0097 г суммы натрия хлорида и кислоты хлороводородной разведенной, которых в 1 мл раствора должно быть 0,00043-0,00053 г.
Содержание суммы натрия хлорида и кислоты хлороводородной разведенной (Г∑) в г 1 мл раствора рассчитывают по формуле:

Теоретический расчет суммы натрия хлорида и кислоты хлороводородной в 1мл раствора глюкозы.
Натрия хлорид 5,2 г
Кислоты хлороводородной разведенной 4,4 мл
Воды для инъекций до 1 л
В 1 литр стабилизатора содержится 9,6 г суммы NaCl и HCl разв.
На 1 литр раствора глюкозы добавлено 50 мл стабилизатора (5%):
В 1000 мл — 9,6 г суммы NaCl и HCl разв.
В 50 мл — х г суммы NaCl и HCl разв.
х=0,48 г суммы NaCl и HCl разв. в 1 л раствора глюкозы; 0,00048 г суммы NaCl и HCl разв. в 1 мл расвора глюкозы.
Расчет среднего титра натрия хлорида и кислоты хлороводородной разведенной.
 — 0,005844 г/мл
— 0,005844 г/мл
 — 0,003646 г/мл
— 0,003646 г/мл



9.5.2 Раствор кислоты аскорбиновой 5% или 10% для инъекций.
Кислота аскорбиновая 50 г или 100 г
Натрия гидрокарбоната 23,85 г или 47,7 г
Натрия сульфита безводного 2,0 г
Воды для инъекций до 1 л
Описание. Бесцветная прозрачная жидкость.
1. К 2-3 каплям раствора прибавляют 3-5 капель воды и 2-3 капли раствора серебра нитрата. Образуется темный осадок.
2. К 1 капле раствора прибавляют 5-6 мл воды, по 1 капле раствора гексациано-(III)феррата калия и железа (III) хлорида. Появляется синее окрашивание.
К 1 мл раствора прибавляют 2-3 капли раствора бария хлорида. Образуется белый осадок, растворимый в разведенной хлороводородной кислоте.
рН 6,0-7,0 (потенциометрически или по универсальной индикаторной бумаге).
Кислота аскорбиновая (М. м. 176,12)
К 0,5 мл раствора прибавляют 0,15 мл (5-6 капель) 40% раствора формальдегида, 4 мл свежепрокипяченной и охлажденной воды, 1 мл кислоты серной разведенной и сразу же титруют раствором йода (0,1 моль/л) УЧ (1/2 I2) до синего окрашивания (индикатор – крахмал) (А, мл).
В 1 мл раствора должно быть 0,0475-0,0525 г или 0,097-0,103 г аскорбиновой кислоты.
Кислота аскорбиновая и натрия сульфит.
К 0,5 мл раствора прибавляют 4 мл свежепрокипяченной и охлажденной воды, 1 мл кислоты серной разведенной и сразу же титруют раствором йода (0,1 моль/л) УЧ (1/2 I2) до синего окрашивания (индикатор – крахмал) (Б, мл).
1 мл раствора йода (0,1 моль/л) УЧ (1/2 I2) соответствует 0,008673 г (для 5% раствора) или 0,008738 г (для 10% раствора) суммарного количества кислоты аскорбиновой и натрия сульфита, которых в 1 мл раствора должно быть 0,0493-0,0547 или 0,099-0,105 г.
Рассчитывают либо суммарное количество кислоты аскорбиновой и натрия сульфита в г в 1 мл по среднему титру, либо содержание натрия сульфита безводного в г в 1 мл.
Содержание натрия сульфита безводного (Х) в г в 1 мл раствора может быть вычислено по формуле:

1 мл раствора йода (0,1 моль/л) УЧ (1/2 I2) соответствует 0,006302 натрия сульфита безводного, которого в 1 мл раствора должно быть 0,0018-0,0022 г.
М. м. натрия сульфита водного 252,18
М. м. натрия сульфита безводного 126,04
К 0,5 мл раствора прибавляют 2,5 мл 1% раствора формальдегида, 4 мл 2% раствора кислоты хлороводородной, 0,5 мл 1% раствора калия иодида, 2мл раствора крахмала и титруют раствором калия йодата (0,1 моль/л, УЧ 1/6 KIO3) до устойчивого синего окрашивания (А, мл).
Кислота аскорбиновая и натрия сульфит.
К 0,5 мл раствора прибавляют 4 мл 2% раствора кислоты хлороводородной, 0,5 мл 1% раствора калия иодида, 2 мл раствора крахмала и титруют раствором калия йодата (0,1 моль/л, УЧ 1/6 KIO3) до устойчивого синего окрашивания (Б, мл).
Расчеты см. вар. 1.
Калия хлорида 1,5
Натрия хлорида 4,75
Натрия ацетата 3,6
Воды для инъекций до 1 л
Описание. Бесцветная прозрачная жидкость.
Хлориды. К 4-5 каплям раствора прибавляют мл разведенной азотной кислоты и 2-3 капли раствора нитрата серебра. Образуется белый творожистый осадок, растворимый в растворе аммиака.
Калий-ион. Упаривают 2 мл раствора на водяной бане до мл, прибавляют 2-3 капли разведенной уксусной кислоты и 1-2 капли гексанитро-(III)кобальтата натрия. Постепенно образуется желтый кристаллический осадок.
Натрий-ион. Микрокристаллоскопическая реакция с пикриновой кислотой.
Натрия ацетат. К 2-3 мл раствора прибавляют 3-5 капель раствора железа(III)хлорида. Появляется красно-бурое окрашивание.
рН 6,5-7,5 (потенциометрически или по универсальной индикаторной бумаге).
Натрия хлорид и калия хлорид.
1 мл раствора титруют раствором серебра нитрата (0,1 моль/л) до появления красноватого осадка) (индикатор – калия хромат).
1 мл раствора серебра нитрата соответствует 0,006164 г суммарного количественного натрия хлорида и калия хлорида, которых в 1 мл раствора должно быть 0,0059-0,0066 г.
Натрия ацетат (М. м. 136,08).
5 мл раствора титруют раствором хлороводородной кислоты (0,1 моль/л) до желтого окрашивания (индикатор – бромфеноловый синий).
1 мл раствора хлороводородной кислоты (0,1 моль/л) соответствует 0,01361 г натрия ацетата (водного), которого в 1 мл раствора должно быть 0,0035-0,0038 г.
К 5 мл раствора прибавляют 10 мл эфира, 2 капли раствора метилового оранжевого, 1 каплю метиленовой сини и титруют раствором хлороводородной кислоты (0,1 моль/л) до перехода зеленой окраски в фиолетовую с окраской в контрольном опыте.
Глюкоза количественное определение уравнение реакции
Глюкоза С6Н12O6 представляет собой наиболее распространенный и наиболее важный моносахарид — гексозу. Она является структурной единицей большинства пищевых ди- и полисахаридов.
Биологическая роль глюкозы
Глюкоза образуется в природе в процессе фотосинтеза, протекающего под действием солнечного света в листьях растений: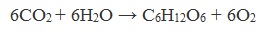
Глюкоза – ценное питательное вещество. Она является обязательным компонентом крови и тканей животных и непосредственным источником энергии для клеточных реакций. При окислении ее в тканях освобождается энергия, необходимая для нормальной жизнедеятельности организмов:
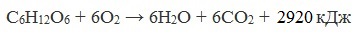
Глюкоза – необходимый компонент обмена углеводов. Она необходима для образования в печени гликогена (запасной углевод человека и животных).
Уровень содержания глюкозы в крови человека постоянен. Во всем объеме крови взрослого человека содержится 5-6 г глюкозы. Такого количества достаточно для покрытия энергетических затрат организма в течение 15 минут его жизнедеятельности.
При снижении ее уровня в крови или высокой концентрации и невозможности использования, как это происходит при сахарном диабете, наступает сонливость, может наступить потеря сознания (гипогликемическая кома).
Строение глюкозы. Изомерия
В молекуле глюкозы присутствуют альдегидная и гидроксильная группы.
Видеоопыт «Распознавание глюкозы с помощью качественных реакций»
Моносахаридам свойственна также иная структура, возникающая в результате внутримолекулярной реакции между карбонильной группой с одним из спиртовых гидроксидов. Такая реакция внутри одной молекулы сопровождается ее циклизацией.

Известно, что наиболее устойчивыми являются 5-ти и 6-ти членные циклы. Поэтому, как правило, происходит взаимодействие карбонильной группы с гидроксилом при 4-м или 5-м углеродном атоме.
В результате взаимодействия карбонильной группы с одной из гидроксильных глюкоза может существовать в двух формах: открытой цепной и циклической.
Образование циклической формы глюкозы при взаимодействии альдегидной группы и спиртового гидроксила при С5 приводит к появлению нового гидроксила у С1 называемого полуацетальным (крайний правый). Он отличается от других большей реакционной способностью, а циклическую форму в этом случае называют также полуацетальной.
В кристаллическом состоянии глюкоза находится в циклической форме, а при растворении частично переходит в открытую и устанавливается состояние подвижного равновесия.
Например, в водном растворе глюкозы существуют следующие структуры: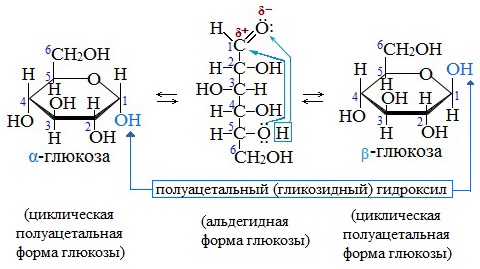
Подвижное равновесие между взаимопревращающимися структурными изомерами (таутомерами) называется таутомерией. Данный случай относится к цикло-цепной таутомерии моносахаридов.
Циклические α- и β-формы глюкозы представляют собой пространственные изомеры, отличающиеся положением полуацетального гидроксила относительно плоскости кольца.
В α-глюкозе этот гидроксил находится в транс-положении к гидроксиметильной группе -СН2ОН, в β-глюкозе – в цис-положении.
С учетом пространственного строения шестичленного цикла
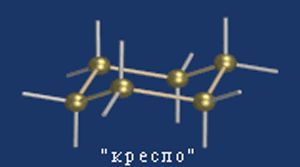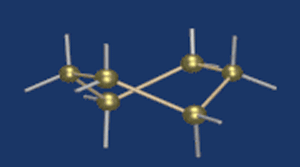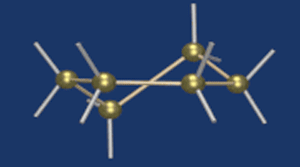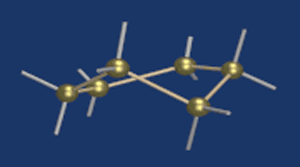
формулы этих изомеров имеют вид: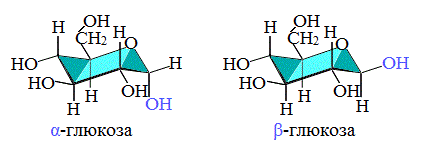
Видеофильм «Глюкоза и ее изомеры»
Аналогичные процессы происходят и в растворе рибозы: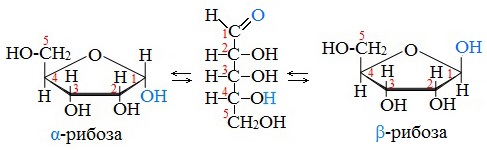
В твердом состоянии глюкоза имеет циклическое строение.
Обычная кристаллическая глюкоза – это α-форма. В растворе более устойчива β-форма (при установившемся равновесии на неё приходится более 60% молекул).
Доля альдегидной формы в равновесии незначительна. Это объясняет отсутствие взаимодействия с фуксинсернистой кислотой (качественная реакция альдегидов).
Явление существования веществ в нескольких взаимопревращающихся изомерных формах было названо А. М. Бутлеровым динамической изомерией. Позднее это явление было названо таутомерией.
Для глюкозы кроме явления таутомерии характерны структурная изомерия с кетонами (глюкоза и фруктоза – структурные межклассовые изомеры) и оптическая изомерия:
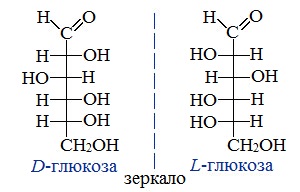
Физические свойства глюкозы
Глюкоза – бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус (лат. «глюкос» – сладкий).
Она содержится в растительных и живых организмах, особенно много ее содержится в виноградном соке (отсюда и название – виноградный сахар), в спелых фруктах и ягодах. Мед в основном состоит из смеси глюкозы с фруктозой.
В крови человека ее содержится примерно 0,1 %
Видеоопыт «Определение глюкозы в виноградном соке»
Получение глюкозы
Основным способом получения моносахаридов, имеющим практическое значения, является гидролиз ди- и полисахароидов.
1. Гидролиз полисахаридов
Глюкозу чаще всего получают гидролизом крахмала (промышленный способ получения):
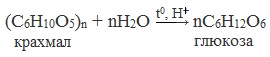 2. Гидролиз дисахаридов
2. Гидролиз дисахаридов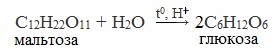
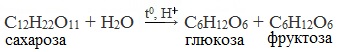 3. Альдольная конденсация формальдегида (реакция А.М. Бутлерова)
3. Альдольная конденсация формальдегида (реакция А.М. Бутлерова)
Первый синтез углеводов из формальдегида в щелочной среде осуществил А.М. Бутлеров в 1861 году.
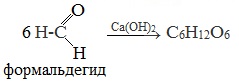
4. Фотосинтез
В природе глюкоза образуется в растениях в результате фотосинтеза:

Применение глюкозы
Глюкоза применяется в медицине в качестве укрепляющего лечебного средства при явлениях сердечной слабости, шоке, для приготовления лечебных препаратов, консервирования крови, внутривенного вливания, при самых разнообразных заболеваниях (особенно при истощении организма).
Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников и т. д.)
Глюкоза находит широкое применение в текстильной промышленности при крашении и печатании рисунков.
Глюкоза применяется в качестве исходного продукта при производстве аскорбиновых и глюконовых кислот, для синтеза ряда производных сахаров и т.д.
Она применяется в производстве зеркал и елочных игрушек (серебрение).
В микробиологической промышленности как питательная среда для получения кормовых дрожжей.
Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению.
На практике используется также спиртовое брожение глюкозы, например при производстве пива.
Фруктоза
Фруктоза (фруктовый сахар) С6Н12О6 – изомер глюкозы. Фруктоза в свободном виде содержится в фруктах, меде. Входит в состав сахарозы и полисахарида инсулина. Она слаще глюкозы и сахарозы. Ценный питательный продукт.
В отличие от глюкозы она может без участия инсулина проникать из крови в клетки тканей. По этой причине фруктоза рекомендуется в качестве наиболее безопасного источника углеводов для больных диабетом.
Как и глюкоза, она может существовать в линейной и циклических формах. В линейной форме фруктоза представляет собой кетоноспирт с пятью гидроксильными группами.
Строение ее молекулы можно выразить формулой: 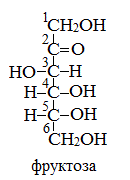
Имея гидроксильные группы, фруктоза, как и глюкоза, способна образовывать сахараты и сложные эфиры. Однако вследствие отсутствия альдегидной группы она в меньшей степени подвержена окислению, чем глюкоза. Фруктоза, также как и глюкоза, не подвергается гидролизу.
Фруктоза вступает во все реакции многоатомных спиртов, но, в отличие от глюкозы, не реагирует с аммиачным раствором оксида серебра.
[spoiler title=”источники:”]
http://pandia.ru/text/80/138/58742-16.php
[/spoiler]


- Это интересно
- СД 1 типа
- СД 2 типа
- Беременность и СД
- Технологии и гаджеты
- Исторические факты
- Книги
- Люди, которые вдохновляют
- Научные исследования
- Мифы
- Юридические аспекты
- Основы
- Инсулин
- Самоконтроль
- Гипогликемия
- Питание
- Спорт
- Жизненные ситуации
- Родителям детей с СД
- Осложнения
- Инсулиновые помпы и сенсоры
- Психология
- Сопутствующие заболевания
- Профилактика осложнений
- Основы
- Инсулин
- Самоконтроль
- Осложнения
- Питание
- Физическая активность
- Жизненные ситуации
- Таблетированные препараты
- Сопутствующие заболевания
- Психология
- Профилактика осложнений
- Гестационный диабет
- Планирование беременности при СД1
- Планирование беременности при СД2
- Беременность при СД1
- Беременность при СД2
- Послеродовый период
- Психология
Как правильно проводится глюкозотолерантный тест?
В статье речь пойдет о глюкозотолерантном тесте (ГТТ), исследовании, название которого у всех на слуху. У этого анализа множество синонимов. Вот некоторые названия, которые вы можете встретить:
- Тест с нагрузкой глюкозы
- Тест на скрытый сахар
- Пероральный (т.е. через рот) глюкозотолерантный тест (ГТТ)
- Оральный глюкозотолерантный тест (ОГТТ)
- Тест с 75 г глюкозы
- Сахарная кривая
- Сахарная нагрузка
Глюкозотолерантный тест – это лабораторный метод, оценивающий уровень глюкозы крови натощак, иногда через час и всегда – через 2 часа после «сахарной нагрузки» (приема 75 г глюкозы), позволяющий выявить сахарный диабет и состояния, которые также называют пре-диабет.
Физиологическое обоснование глюкозотолерантного теста и более глубокие подробости описали в отдельной статье
 Для чего проводится глюкозотолерантный тест?
Для чего проводится глюкозотолерантный тест?
Для выявления следующих заболеваний:
• Предиабет (скрытый диабет, нарушение толерантности к глюкозе)
• Диабет
• Гестационный сахарный диабет (диабет беременных)
Кому может быть назначен ГТТ?
• Для выявления скрытого диабета при повышенном уровне глюкозы натощак
• Для выявления скрытого диабета при нормальном уровне глюкозы натощак, но с факторами риска диабета (избыточная масса тела или ожирение, отягощенная по диабету наследственность, гипертензия, предиабет и т.д.)
• Всем при достижении 45 лет
• Для выявления гестационного сахарного диабета на 24-28 неделях беременности
 Какие правила проведения теста существуют?
Какие правила проведения теста существуют?
- Глюкозотолерантный тест проводится утром, строго натощак, после ночного голодания в течение 10-12 часов. Пить воду во время голодания можно.
- Последний вечерний прием пищи должен содержать 30-50 г углеводов. Накануне исследования, как минимум за 3 дня до проведения теста, необходимо полноценно питаться, не соблюдать диету и не ограничивать себя в углеводах. В вашем пищевом рационе при этом должно быть не менее 150 г углеводов в сутки. Фрукты, овощи, хлеб, рис, зерновые – хорошие источники углеводов.
- После забора крови натощак (первая точка), необходимо выпить специальный раствор. Его готовят из 75 г порошка глюкозы и 250-300 мл воды. Пить раствор нужно медленно, не быстрее чем за 5 минут.
 Для детей раствор готовят иначе – 1.75 г порошка глюкозы на 1 кг массы тела, но не более 75 г. Вы можете спросить: неужели детям проводят тест с глюкозой? Да, существуют показания для проведения ГТТ у детей для выявления сахарного диабета 2 типа.
Для детей раствор готовят иначе – 1.75 г порошка глюкозы на 1 кг массы тела, но не более 75 г. Вы можете спросить: неужели детям проводят тест с глюкозой? Да, существуют показания для проведения ГТТ у детей для выявления сахарного диабета 2 типа.
- Через 2 часа после нагрузки, т.е. после выпитой глюкозы, осуществляется повторный забор крови (вторая точка).
- Обратите внимание: в процессе теста нельзя курить. Лучше всего провести эти 2 часа в спокойном состоянии (например, за чтением книги).
- Тест должен проводиться по венозной плазме. Уточните этот пункт у медсестры или врача, если вам предлагают сдать кровь из пальца.
- При выполнении ГТТ беременным женщинам на сроке 24-28 недель для выявления гестационного диабета, добавляется еще одна точка. Забор крови производят через 1 час после сахарной нагрузки. Получается, кровь берут трижды: натощак, через 1 час и через 2 часа.
Ситуации, когда глюкозотолерантный тест проводить не следует:
• На фоне острого заболевания – воспалительного или инфекционного. Во время болезни наш организм борется с ней, активизируя гормоны – антагонисты инсулина. Это может вызвать повышение уровня глюкозы, но временное. Результаты теста, сделанного на фоне острого заболевания, могут быть неточными
• На фоне кратковременного приема препаратов, повышающих уровень глюкозы в крови (глюкокортикоиды, бета-адреноблокаторы, тиазидные диуретики, тиреоидные гормоны). Если вы принимаете указанные лекарства в течение длительного срока, тест проводить можно.
Результаты теста для анализа по венозной плазме:
Какие показатели ГТТ соответствуют норме?
• Натощак < 6.1 ммоль/л и
• Через 2 часа после ГТТ < 7.8 ммоль/л
Какие показатели ГТТ соответствуют сахарному диабету?
• Натощак ≥ 7.0 ммоль/л и
• Через 2 часа после ГТТ ≥ 11.1 ммоль/л
Какие показатели ГТТ соответствуют предиабету?
• Натощак от 6.1 ммоль/л до 6.9 ммоль/л (нарушенная гликемия натощак)
• Через 2 часа после ГТТ от 7.8 ммоль/л до 11.0 ммоль/л (нарушенная толерантность к глюкозе)
Какие показатели ГТТ соответствуют диабету беременных?
• Натощак ≥ 5.1, но < 7.0 ммоль/л
• Через 1 час после ГТТ < 10.0 ммоль/л
• Через 2 часа после ГТТ < 8.5 ммоль/л
Кому и зачем надо сдавать глюкозотолерантный тест?
Статья для специалистов
 Что делать, если ваши результаты ГТТ не соответствуют норме?
Что делать, если ваши результаты ГТТ не соответствуют норме?
Вам необходима консультация эндокринолога. Доктор подробно раскажет о заболевании и даст рекомендации по питанию, физической нагрузке и лекарственным препаратам. Отнеситесь серьезно и ответственно к этой информации.
Все права на материалы, размещенные на данном сайте, принадлежат проекту “Правило 15”.
Использование материалов возможно только с разрешения представителей проекта в соответствии
с условиями использования материалов проекта “Правило 15”.
Если вы желаете использовать какие-либо материалы, свяжитесь с представителями проекта.
Контактная информация в разделе “Контакты” или
воспользуйтесь обратной связью в разделе
“Чем я могу помочь проекту”, подраздел “Действием”.
Надееемся на взаимовыгодное сотрудничество.
Чтобы получить полный доступ, пожалуйста, авторизуйтесь
или
зарегистрируйтесь.




