|
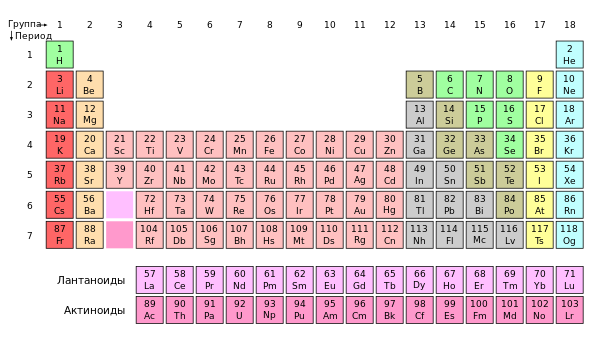
Что означают понятия “главная подгруппа” и “побочная подгруппа” в периодической таблице? Как отличить главную подгруппу от побочной подгруппы? Я упоминала о побочной и главной подгруппе в своем ответе на ваш предыдущий вопрос. Причина разделение группы на главную подгруппу (A) и побочную подгруппу (B латинская или Б русская) – различные химических свойства каждой подгруппы. Так VIIA группа представляет собой галогены – F фтор, Cl хлор, Br бром, I йод, At астат, которые являются типичными неметаллами, сильными окислителями. А вот в VIIB расположены Mn марганец, Tc технеций, Re рений, Bh борий, которые являются металлами. Вообще, все элементы побочных подгрупп являются металлами. В таблице ячейки с элементами побочных подгрупп обычно окрашивают в синий цвет, и символ пишут справа (элементы главных подгрупп – слева). автор вопроса выбрал этот ответ лучшим Ксарфакс 3 года назад Вертикальный ряд в периодической таблице Д.И. Менделеева называется группой. В короткой форме периодической таблицы каждая группа подразделяется на главную подгруппу и побочную подгруппу. В главную подгруппу входят s-элементы и p-элементы. В побочную подгруппу входят d-элементы (их также называют переходными элементами или переходными металлами). Побочная подгруппа обозначается голубым или синим цветом. Например, главная подгруппа 2 группы включает в себя элементы Be, Mg, Ca, Sr, Ba, Ra, а побочная – Zn, Cd, Hg. ** В длинной же форме периодической таблицы подгрупп нет, есть только группы. В ней все d-элементы (которые в короткой форме таблицы входят в побочную подгруппу) находятся в 3 – 12 группе. VeneraD 3 года назад Для того, чтобы ответить на вопрос, нужно посмотреть на таблицу Менделеева. Дело в том, что в этой таблице есть деление элементов. Это как раз и будет деление на главную подгруппу и побочную подгруппу. При этом есть элементы, с обозначением s и p, это и будет главная подгруппа. А есть элементы под буквой d, это побочная группа. Элементы данной группы ещё называют переходными элементами. С помощью рисунка ниже можно определить, к какой же группе относится элемент. Алиса в Стране 3 года назад Химию я в школе любила, два последние класса даже как-то умудрялась пятерки за год получить, хотя было непросто, но до этого я этот предмет как-то не воспринимала, а в 9-10 классе увлеклась, разобралась, но, конечно, я сейчас уже не очень хорошо все помню. Итак, начнем разбираться. Чтобы понять, что такое подгруппа, вспомним в начале, что такое группа в таблице Менделеева, это вертикальный ряд, у них есть номера, которые написаны сверху римскими цифрами. Так вот элементы в каждой группе делятся на главную подгруппу и побочную подгруппу, которые выделяются разными цветами – элементы побочной группы выделяются синим цветом, в побочную подгруппу входят переходные элементы (переходные металлы) – d-элементы. а в главную подгруппу – s-элементы и p-элементы. Вот на этой табличке очень наглядно все это видно: То есть определить можно по цвету. Например, в первой группе элементы побочной группы это: Cu, Ag, Au, Rg. Ладлен 3 года назад Конечно существуют различные варианты расположения элементов в периодической системе. иногда применяются разные цвета. Но честно говоря меня просто удивляют, что в интернете большинство ответов не дают реального ответа. А ведь в названии и заложен ответ на данный вопрос. Так главные подгруппы и в них химические элементы расположены слева в своей клетке, а в побочных подгруппах расположены правее. как говорится с боку. Вот как это выглядит в таблице. У элементов побочных подгрупп идет заполнение d и f уровней. А в главных подгруппах у химических элементов электроны находятся на S и P уровнях. и естественно в таблицы они изображены разными цветами. Бекки Шарп 3 года назад Деление на главную и побочную подгруппы объясняется теорией строения атома (различии в заполнении электронами энергетических уровней). Главная подгруппа состоит из s-элементов и p-элементов. Число валентных электронов на внешнем уровне такое же как номер группы. Побочные подгруппы содержат d-элементы (переходные элементы и переходные металлы). Визуально элементы побочной подгруппы синего цвета. Атомы, имеющие одинаковое строение внешнего электронного уровня относятся к одной подгруппе. В главной подгруппе одной укрупненной группы химических элементов, s и p элементы, побочная группа это элементы d. Определять их не нужно, нужно просто видеть разницу в цвете ячейки и расположение букв латинского алфавита названия элемента в главной группе буквы слева, в побочной – справа. И цвет побочной группы синий. Для это сделан таблица разноцветной, хотя можно было бы просто сделать черно-белой. Марина Вологда 3 года назад Периодическая система химических элементов или по другому “Таблица Менделеева” – это такая таблица, в которой все химические элементы классифицируются по каким-либо свойствам. Интересен тот факт, что можно встретить несколько сотен вариантов данной таблицы, но чаще всего используется двумерная таблица. Рассматривая структуру таблицы, стоит выделить группы, которые подразделяются на главные и побочные. А теперь дадим характеристику понятия “группа”. Группа состоит из главной (в таблице обозначается буквой “А”) и побочной (в таблице обозначается буквой “В”) подгрупп. А теперь рассмотрим таблицу, где видим, что каждая группа элементов подразделяется на главную и побочную подгруппы. Главные подгруппы образуют элементы малых и больших периодов, а побочные – только элементы больших периодов. На таблице это легко разобрать, ведь элементы главных подгрупп сдвинуты влево, а элементы побочных подгрупп сдвинуты в право (и ячейки окрашены в голубые цвета). В главной подгруппе – s-элементы и p-элементы, в побочной- d-элементы. Приведем пример: TheSun 3 года назад В таблице Менделеева все элементы разделены на главную и побочную подгруппу. Сначала уточним, что называется группой в таблице Менделеева. Группой называется вертикальный ряд в периодической таблице Менделеева. Каждая группа подразделяется на главную подгруппу и побочную подгруппу. Теперь ответим на вопрос, какие элементы в таблице Менделеева относятся к главной и побочной подгруппам. В главную подгруппу входят s и p-элементы, а в побочную подгруппу входят d-элементы. Для удобства определения элементов по подгруппам, элементы имеют различное цветовое обозначение в таблице Менделеева. Элементы побочная подгруппы обозначается голубым (синим) цветом. Бархатные лапки 3 года назад Все из нас знают таблицу Менделеева, она делится на главные и побочные подгруппы. Так в главную подгруппу входят s и p-элементы. Побочная подгруппа состоит из d-элементов. Определить какой элемент относится к какой подгруппе несложно, так элементы, которые относятся к побочной группе выделены синим цветом. Знаете ответ? |
ХИМИЯ! как определить главная подгруппа или побочная в хим. таблице менделеева? объясните, кто может
Залина Исаева
Мастер
(1439),
закрыт
10 лет назад
Лучший ответ
Маргарита Мосолова
Мастер
(1027)
10 лет назад
В побочной подгруппе расположены элементы d и f-семейства. Иными словами, элементы побочной подгруппы в данной таблице выделены синим и зелёным
Остальные ответы
Похожие вопросы
Гру́ппа периодической системы химических элементов — последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением.
Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) и, как правило, соответствует высшей валентности атома.
В короткопериодном варианте периодической системы группы подразделяются на подгруппы — главные (или подгруппы A), начинающиеся с элементов первого и второго периодов, и побочные (подгруппы В), содержащие d-элементы. Подгруппы также имеют названия по элементу с наименьшим зарядом ядра (как правило, по элементу второго периода для главных подгрупп и элементу четвёртого периода для побочных подгрупп). Элементы одной подгруппы обладают сходными химическими свойствами.
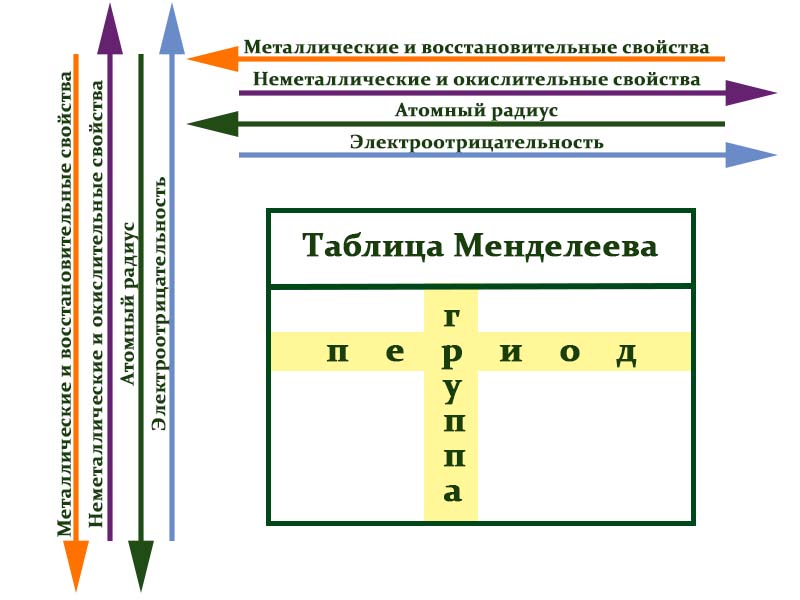
С возрастанием заряда ядра у элементов одной группы из-за увеличения числа электронных оболочек увеличиваются атомные радиусы, вследствие чего происходит снижение[источник не указан 2248 дней] электроотрицательности, усиление[источник не указан 2248 дней] металлических и ослабление[источник не указан 2248 дней] неметаллических свойств элементов, усиление восстановительных и ослабление окислительных свойств образуемых ими веществ.
Нумерация групп[править | править код]
С 1989 года Международным союзом теоретической и прикладной химии (IUPAC) в качестве основного варианта периодической системы утверждена длиннопериодная форма[1]. В связи с этим IUPAC рекомендует сплошную нумерацию групп: арабскими цифрами от 1 до 18.
Несмотря на это, продолжают применяться ставшие традиционными системы нумерации с использованием римских цифр и латинских букв, отличающиеся для Америки и Европы.
Современная система нумерации содержит следующие группы (старые системы, европейская и американская, приведены в скобках):
- Группа 1 (IA, IA): щелочные металлы
- Группа 2 (IIA, IIA): щёлочноземельные металлы
- Группа 3 (IIIB, IIIA): подгруппа скандия
- Группа 4 (IVB, IVA): подгруппа титана
- Группа 5 (VB, VA): подгруппа ванадия
- Группа 6 (VIB, VIA): подгруппа хрома
- Группа 7 (VIIB, VIIA): подгруппа марганца
- Группа 8 (VIIIВ, VIIIA): подгруппа железа
- Группа 9 (VIIIВ, VIIIA): подгруппа кобальта
- Группа 10 (VIIIВ, VIIIA): подгруппа никеля
- Группа 11 (IB, IB): подгруппа меди
- Группа 12 (IIB, IIB): подгруппа цинка
- Группа 13 (IIIA, IIIB): подгруппа бора
- Группа 14 (IVA, IVB): подгруппа углерода
- Группа 15 (VA, VB): подгруппа азота
- Группа 16 (VIA, VIB): подгруппа кислорода (халькогены)
- Группа 17 (VIIA, VIIB): галогены
- Группа 18 (VIIIA, VIIIB)[2]: инертные газы
Примечания[править | править код]
- ↑ Сайфуллин Р. С., Сайфуллин А. Р. Новая таблица Менделеева // Химия и жизнь.— 2003.— № 12.— С. 14—17.
- ↑ Подгруппа гелия (инертные газы) иногда, особенно в старых изданиях, обозначается цифрой 0.

- Периодическая система Менделеева систематизирует элементы и их свойства. В ней все элементы упорядочены с учетом их атомного числа и повторяющихся химических свойств.
- Периодический закон: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Расшифровка обозначений элементов
Каждому химическому элементу в таблице отведена одна клеточка, в которой указаны символ и название элемента, порядковый номер и относительная атомная масса.
Расшифровка обозначений элементов таблицы Менделеева:
- Обозначение: одной или двумя латинскими буквами.
- Порядковый номер элемента или атомный номер равен числу протонов в его ядре. Обычно пишется в левом верхнем углу.
- Относительная атомная масса (сумма масс протонов и нейтронов). Это усреднённая величина, для расчёта которой используются атомные массы всех изотопов элемента с учетом их содержания в природе. Поэтому обычно она является дробным числом.
- Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число.
- Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
- Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
- Электронная конфигурация — формула расположения электронов по различным электронным оболочкам атома химического элемента или молекулы.
-
Чтобы узнать количество нейтронов в ядре элемента, необходимо из относительной атомной массы (массового числа) вычесть порядковый номер.
Элементы периодической таблицы Менделеева
Металлы расположены в левом нижнем углу таблицы, неметаллы — в правом верхнем углу. Между ними находятся полуметаллы. Все периоды, кроме первого, начинается щелочным металлом. Каждый период заканчивается инертным газом.
- Металлы обладают хорошей электро- и теплопроводностью, способны отражать яркий свет, имеют высокую температуру плавления (остаются твердыми при нормальных значениях окружающей среды, исключение — ртуть).
- Неметаллы встречаются в природе в трех состояниях: газ (например, водород), жидкость (например, бром) и твердые вещества (например, фосфор). Он не способны проводить тепло и электричество. Имеют более низкую температуру плавления в сравнении с металлами, более хрупкие и ломкие. Могут иметь разнообразный внешний вид (элементы с низкой плотностью и яркостью).
- Металлоиды имеют смешанные свойства металлов и неметаллов (например, кремний). Они имеют среднюю тепло- и электропроводность. Различаются между собой по температуре плавления, плотности, цвету и форме. Внешний вид может быть схож с металлами или неметаллами.
Расшифровка групп и периодов таблицы Менделеева
В таблице химические вещества расположены в специальном порядке: слева направо по мере роста их атомных масс. Все они в периодической системе объединены в периоды и группы.
Периоды — это горизонтальные ряды в таблице. У всех элементов одного периода одинаковое количество заполненных электронами энергетических уровней.
Номер периода, в котором находится элемент, совпадает с номером его валентной оболочки. Эта валентная оболочка постепенно заполняется от начала к концу периода.
Закономерности периодов:
- Металлические свойства убывают, неметаллические и окислительные -возрастают. Каждый период начинается активным металлом и заканчивается инертным газом.
- Уменьшается атомный радиус.
- Увеличивается электроотрицательность.
Группы — это столбцы. Элементы во всех группах имеют одинаковое электронное строение внешних электронных оболочек. В каждой группе на внешнем энергетическом атома одинаковое число электронов, то есть номер группы совпадает с числом валентных электронов, которые могут участвовать в образовании химических связей. Поэтому номер группы часто совпадает с валентностью элементов. Например, номер группы совпадает с валентностью s-элементов и с наибольшей возможной валентностью p-элементов.
Закономерности групп:
- Металлические свойства увеличиваются, неметаллические и окислительные- убывают.
- Увеличивается радиус атома элементов в рамках одной группы.
- Уменьшается электроотрицательность.
Атомное число показывает, сколько протонов содержит ядро атома элемента и сколько электронов в атоме находятся вокруг него. Атом каждого последующего элемента содержит на один протон больше, чем предыдущий.
Валетность — это свойство элементов образовывать химические связи. То есть это количество химических связей, которые образует атом или число атомов, которое может присоединить или заместить атом данного элемента. Валентность бывает: постоянная и переменная (зависит от состава вещества, в которое входит элемент).
Определить валентность:
— Постоянная валентность идентична номеру группы главной подгруппы. Номера групп в таблице изображаются римскими цифрами.
— Переменная валентность (часто бывает у неметаллов) определяется по формуле: 8 вычесть № группы, в которой находится вещество.
Расшифровка периодов и групп периодической таблицы Менделеева
Каждый элемент имеет свой порядковый (атомный) номер, располагается в определённом периоде и определённой группе.
Периоды
- Малые периоды: первый, второй и третий периоды. В них содержится соответственно 2, 8 и 8 элементов;
- Большие периоды: остальные элементы. В четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент.
В таблице 7 периодов. В каждом содержится определённое число элементов:
1-й период — 2 элемента (малый период),
2-й период — 8 элементов (малый период),
3-й период — 8 элементов (малый период),
4-й период — 18 элементов (большой период),
5-й период — 18 элементов (большой период),
6-й период — 32 элемента (18+14) (большой период),
7-й период — 32 элемента (18+14) (большой период).
Группы и подгруппы
- Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов.
- Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
В Периодической таблице может использоваться разное обозначение групп. Поэтому согласно такому обозначению бывает разная расшифровка групп таблицы менделеева:
- 18 групп, пронумерованных арабскими цифрами.
- 8 групп, пронумерованных цифрами с добавлением букв A или B.
Группы A — это главные подгруппы.
Группы B — это побочные подгруппы в больших периодов. Это только металлы.
IA, VIIIA — по 7 элементов;
IIA — VIIA — по 6 элементов;
IIIB — 32 элемента (4+14 лантаноидов +14 актиноидов);
VIIIB — 12 элементов;
IB, IIB, IVB — VIIB — по 4 элемента.
Римский номер группы, как правило, показывает высшую валентность в оксидах (но для некоторых элементов не выполняется).
Элементы с порядковыми номерами 58–71 (лантаноиды) и 90–103 (актиноиды) вынесены из таблицы и располагаются под ней. Это элементы IIIB группы. Лантаноиды относятся к шестому периоду, а актиноиды — к седьмому.
Элементы главной подгруппы
1 группа главная подгруппа элементов (IA) — щелочные металлы.
Это мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним электроном на внешней оболочке и прекрасно вступают в реакцию.
Литий Li (3), Натрий Na (11), Калий K (19), Рубидий Rb (37), Цезий Cs (55), Франций Fr (87).
2 группа главная подгруппа (IIА) -щелочноземельными металлами.
Имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Кальций Ca (20), Стронций Sr (38), Барий Ba (56), Радий Ra (88).
3 группа главная подгруппа (IIIА).
Все элементы данной подгруппы, за исключением бора, металлы. Главную подгруппу составляют составляют бор, алюминий, галлий, индий и таллий. На внешнем электронном уровне элементов по три электрона. Они легко отдают эти электроны или образуют три неспаренных электрона.
4 группа главная подгруппа (IVА) .
Углерод и кремний обладают всеми свойствами неметаллов, германий и олово занимают промежуточную позицию, а свинец имеет выраженные металлические свойства. Большинство элементов подгруппы углерода — полупроводники (проводят электричество за счёт примесей, но хуже, чем металлы).
5 группа главная подгруппа (VA).
Физические свойства элементов подгруппы азота различны. Азот является бесцветным газом. Фосфор, мягкое вещество, образует несколько вариантов аллотропных модификаций — белый, красный и чёрный фосфор. Мышьяк — твёрдый полуметалл, способный проводить электрический ток. Висмут — блестящий серебристо-белый металл с радужным отливом.
6 группа главной подгруппы (VIA) .
Для завершения внешнего электронного уровня атомам этих элементов не хватает лишь двух электронов, поэтому они проявляют сильные окислительные (неметаллические) свойства.
7 группа главная подгруппа (VIIA) — галогены .
(F, Cl, Br, I, At). Имеют семь электронов на внешнем электронном слое атома. Это сильнейшие окислители, легко вступающие в реакции. Галогены («рождающие соли») назвали так потому, что они реагируют со многими металлами с образованием солей.
Самый активный из галогенов — фтор. Он способен разрушать даже молекулы воды, за что и получил своё грозное имя (слово «фтор» переводится на русский язык как «разрушительный»). А его «близкий родственник» — иод — используется в медицине в виде спиртового раствора для обработки ран.
8 группа главная подгруппа (VIIIA) — инертные (благородные) газы.
(He, Ne, Ar, Kr, Xe, Rn, Og). У них полностью заполнен внешний электронный уровень. Они практически не способны участвовать в реакциях. Поэтому их иногда называют «благородными». У инертных газов есть способность: они светятся под действием электромагнитного излучения, поэтому используются для создания ламп. Так, неон используется для создания светящихся вывесок и реклам, а ксенон — в автомобильных фарах и фотовспышках.
Элементы побочной подгруппы
Элементы побочных подгрупп кроме лантаноидов и актиноидов — переходные металлы.
Твёрдые (исключение жидкая ртуть), плотные, обладают характерным блеском, хорошо проводят тепло и электричество.
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
3 группа побочная подгруппа (IIIB) шестого и седьмого периодов — лантаноиды и актиноиды.
Для удобства их помещают под основной таблицей.
- Лантаноиды иногда называют «редкоземельными элементами», поскольку они были обнаружены в небольшом количестве в составе редких минералов и не образуют собственных руд.
- Актиноиды имеют одно важное общее свойство — радиоактивность. Все они, кроме урана, практически не встречаются в природе и синтезируются искусственно.
Неметаллы
Правый верхний угол таблицы до инертных газов -неметаллы.
Неметаллы плохо проводят тепло и электричество и могут существовать в трёх агрегатных состояниях: твёрдом (как углерод или кремний), жидком (как бром) и газообразном (как кислород и азот). Водород может проявлять как металлические, так и неметаллические свойства, поэтому его относят как к первой, так и к седьмой группе.
Кислородные и водородные соединения
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения.
Существует 8 форм кислородных соединений: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4,
где R — элемент группы.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют 4 формы водородных соединений: RH4, RH3, RH2, RH.
Характер соединений: RH — сильнокислый; RH2 — слабокислый; RH3 — слабоосновный; RH4 — нейтральный.
Любой учебник химии всегда начинается с таблицы Менделеева. И не зря: периодическая таблица рассказывает многое о строении и свойствах элементов и даже соединений, которые они образуют. В самом часто используемом варианте таблицы, коротком, имеется восемь групп. Это колонки, обозначаемые римскими цифрами. И какую же информацию они нам дают?
Для начала разберёмся, что такое главные и побочные подгруппы. С первого по третий период никаких побочных подгрупп нет, они начинаются с четвёртого периода, когда в таблице появляются так называемые d-элементы. Чтобы лучше понять, почему же вдруг в таблице образуются побочные подгруппы, посмотрим на другой вариант, длинный. Он выглядит так:
Здесь хорошо видно, что d-элементы появляются в четвёртом периоде, при этом никаких побочных подгрупп нет. А чтобы таблица была более компактной, периоды, начиная с четвёртого, укладывают в две строчки. Просто представьте, что вы сложили таблицы эдакой «гармошкой» на линии, разделяющей 10 и 11 группу в длинном варианте (или между никелем Ni и медью Cu в четвёртом периоде). Тогда и получится короткий вариант, в котором имеются побочные подгруппы. То есть побочные подгруппы – просто результат более компактного изображения таблицы, в длинном варианте их нет.
Что говорят об элементах номера групп
В группах (мы сейчас и далее будет говорить о главных подгруппах) все элементы имеют одинаковое строение внешнего электронного слоя.
У всех атомов элементов группы на внешнем слое одинаковое число электронов, равно номеру группы.
Например, у всех атомов элементов группы I (Н, Li, Na, K, Rb, Cs, Fr) на внешнем слое 1 электрон. У всех атомов элементов группы II (Be, Mg, Ca, Sr, Ba, Ra) на внешнем слое 2 электрона. И так далее вплоть до группы VIII (He, Ne, Ar, Kr, Xe, Rn) у которых на внешнем слое 8 электронов. Таким образом,
номер группы показывает, сколько электронов находится на внешнем слое атома элемента.
Номер группы определят и валентность, которая наиболее характерна для элемента. Так, элементы первой группы проявляют валентность I, элементы II группы – II и так далее. Но тут следует помнить, что элементы VII группы чаще проявляют валентность I (это связано с особенностью строения внешнего электронного слоя). А вот элементы VIII группы, имеющие полностью завершённый внешний электронный слой, на котором 8 электронов, не зря называются «благородными» или «инертными» газами. Поскольку внешний слой завершён, атомы не желают вступать в реакции, и эти газы вообще неохотно образуют соединения, у них даже молекулы одноатомные Ne, Ar, Xe в отличие от прочих газов, у которых молекулы двухатомны (N2, О2, Cl2).
Атомы с увеличением заряда ядра (а заряд ядра – это порядковый номер элемента) становятся тяжелее и больше, поскольку число электронов у них тоже увеличивается. Чтобы убедиться в этом, проследите за элементами любой группы: у верхнего будет самый маленький заряд ядра и самая маленькая масса из всех элементов группы, у нижнего – и заряд ядра, и масса будут самыми большими из всех элементов группы. По этой причине
при движении вниз по группе наблюдается усиление металлических свойств.
В это тоже легко убедиться: посмотрите, например, на IV. Там находятся элементы углерод С, кремний Si, германий Ge, олово Sn, свинец Pb. Углерод и кремний – неметаллы, а вот германий, олово и свинец – металлы. Аналогично свойства меняются в группах V, VI, VII. Отсюда следует, что элементы, стоящие выше, будут образовывать оксиды кислотные (которые при взаимодействии с водой дадут кислоты), а элементы, стоящие ниже, – основные (они, реагируя с водой, образуют гидроксиды).
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.