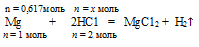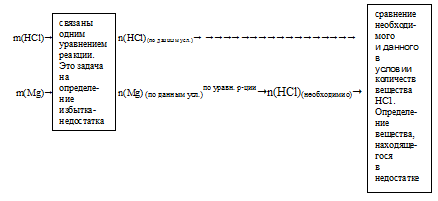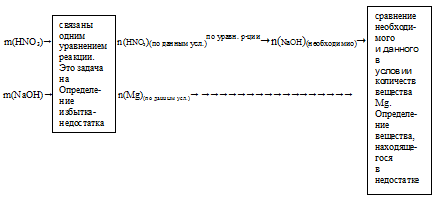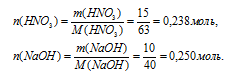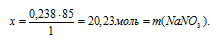“Я не сдам ЕГЭ, потому что у меня нет таланта! У Кати талант есть, у Паши – тоже есть, а у меня нет!” Сколько раз каждый из вас так думал? Много? Ха-Ха и еще раз Ха-Ха! Марк Твен говорил: «Существует тысяча причин для того, чтобы себя оправдать, но ни одной реальной». Секрет таланта и успеха на ЕГЭ я раскрою в конце статьи, а пока продолжаем изучать Стехиометрию. Сегодня разберемся с деликатной темой: избыток-недостаток в расчетах по уравнениям реакций.
В ряде задач представлены данные для обоих реагентов. Как в таких случаях выполнять расчеты по уравнения реакций? Что брать в качестве точки расчета? Давайте разбираться. Вначале определимся с понятиями.
Эквимолярное соотношение – равные количества веществ
Стехиометрическое соотношение – количества веществ в соответствии с коэффициентами в уравнении реакции
Для того, чтобы понять, в каких соотношениях представлены количества веществ-реагентов в конкретной задаче, необходимо начать анализ задачи по уже известным Четырем Заповедям. После выполнения Предварительных Расчетов (Третья Заповедь), следует выписать количества веществ над формулами реагентов в уравнении реакции и произвести пересчет количества одного вещества через количество другого. После определения избытка-недостатка дальнейшие расчеты в задаче производим по недостатку.
ПОМНИ!!!
Расчеты по уравнению реакции производятся по НЕДОСТАТКУ!
Как определить избыток-недостаток и провести дальнейшие расчеты, лучше разобрать на конкретной задаче. Читайте внимательно и попробуйте записать решение задачи на отдельном листе бумаги.
Задача 1
На 47 г оксида калия подействовали раствором, содержащим 40 г азотной кислоты. Найдите массу образовавшегося нитрата калия.
1) Первая Заповедь. Выписать данные задачи в разделе “Дано”.
2) Вторая Заповедь. Написать уравнение реакции.
Немного теории химии. Оксиды щелочных металлов проявляют ярко выраженные основные свойства. Они легко реагируют с кислотами с образованием солей.
3. Третья Заповедь. Сделать предварительные расчеты по данным условия задачи
В условии задачи представлены данные по обоим реагентам – оксиду калия и азотной кислоте, поэтому определяем количество вещества каждого участника процесса.
На этой стадии необходимо определить, кто из реагентов в избытке, а кто в недостатке. Для этого следует провести пересчет количества одного вещества через количество другого. Покажу два способа пересчета и анализа. Можете пользоваться любым, какой понятней.
1) Считаем количество вещества азотной кислоты по количеству вещества оксида калия (обычный расчет по уравнению реакции). Читайте внимательно! Я мысленно произношу: “Пусть весь оксид калия вступил в реакцию. Сколько тогда прореагирует азотной кислоты?” И делаю расчет по уравнению реакции. Азотной кислоты, по расчетам, требуется больше, чем дано, значит, азотная кислота – в недостатке.
2) Считаем количество вещества оксида калия по количеству вещества азотной кислоты (обычный расчет по уравнению реакции). Я мысленно произношу: “Пусть вся азотная кислота вступила в реакцию. Сколько тогда прореагирует оксида калия?” Оксида калия, по расчетам, требуется меньше, чем дано, значит, оксид калия в избытке.
4. Четвертая заповедь. Составить алгоритм решения задачи.
Формулизируем вопрос задачи “Найдите массу образовавшегося нитрата калия”, т.е. записываем формулу расчета массы, которая для нас, как для химиков, должна быть представлена произведением количества вещества на молярную массу. Анализируем компоненты формулы: молярную массу нитрата калия определяем по таблице Менделеева, количество вещества нитрата калия рассчитываем по уравнению реакции исключительно по недостатку!
Задача 2
Смешали 7,3 г хлороводорода и 4 г аммиака. Какая масса соли при этом образуется?
Немного теории. При смешивании хлороводорода и аммиака образуется густой белый дым (“дым без огня”) – кристаллики соли хлорида аммония.
Последовательность действия, выполняемых при решении задачи:
1) Выписать данные в разделе “Дано”
2) Написать уравнение реакции
3) Сделать предварительные расчеты.
4) Определить избыток-недостаток
5) Сделать расчет по уравнению реакции (по недостатку!)
6) Составить алгоритм решения
7) Сделать окончательный расчет
Задача 3
На 36 г алюминия подействовали 64 г серы. Найдите массу образовавшегося сульфида алюминия.
При поджигании смеси порошкообразных алюминия и серы между ними начинается интенсивная экзотермическая реакция с образованием сульфида алюминия, который полностью гидролизуется водой, поэтому не может быть получен обменными реакциями в водных растворах.
Последовательность действия, выполняемых при решении задачи:
1) Выписать данные в разделе “Дано”
2) Написать уравнение реакции
3) Сделать предварительные расчеты.
4) Определить избыток-недостаток
5) Сделать расчет по уравнению реакции (по недостатку!)
6) Составить алгоритм решения
7) Сделать окончательный расчет
Секрет таланта и успеха на ЕГЭ
Талант не дается от природы, он создается самим человеком. Это определенные способности, которые раскрываются с приобретением навыков и опыта. Успех на ЕГЭ зависит от ежедневного упорного труда и достижения мастерства в выбранном деле. Думаю, вывод не трудно сделать. Хотите добиться успеха – принимайтесь за работу!
Вы готовитесь к ЕГЭ и хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии http://repetitor-him.ru. Здесь вы найдете огромное количество задач, заданий и теоретического материала, познакомитесь с моими учениками, многие из которых уже давно работают врачами. Звоните мне +7(903) 186-74-55. Приходите ко мне на курс, на Мастер-классы “Решение задач по химии” – и вы сдадите ЕГЭ с высочайшими баллами, и станете студентом престижного ВУЗа!
PS! Если вы не можете со мной связаться из-за большого количества звонков от моих читателей, пишите мне в личку ВКонтакте, или на Facebook. Я обязательно отвечу вам.
Репетитор по химии и биологии кбн В.Богунова
Задачи на избыток и недостаток
22-Фев-2014 | комментариев 16 | Лолита Окольнова
Задачи такого типа (точнее, это может быть даже не самой задачей, а частью задачи) есть в части С ГИА, они входят в часть С ЕГЭ, теперь они появились и в части B.
Задачи на избыток и недостаток
Классический пример задачи на избыток и недостаток.
Этапы решения задачи:
1. Записываем уравнение реакции и уравниваем его:
Cu + Hg(NO3)2 → Hg + Cu(NO3)2
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(Cu) = mAr =3.2 г 63.5 гмоль = 0,05 моль
m(Hg(NO3)2) = mMr = 20 324 = 0,06 моль
3. Сравниваем количество моль веществ и определяем недостаток:
Cu + Hg(NO3)2 → Hg + Cu(NO3)2
0,05 моль 0,06 моль
по уравнению реакции меди и нитрат ртути реагируют 1:1, значит, их количество моль тоже должно быть одинаковым
0,05 моль < 0,06 моль — медь в недостатке
Задачи на избыток и недостаток всегда решаются ПО НЕДОСТАТКУ
Почему по недостатку? Это аналогично вопросу — «сколько целых яблок можно сложить из 5 половинок? «
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
Cu + Hg(NO3)2 → Hg + Cu(NO3)2
0,05 моль ——> 0,05 моль
m(Hg)= n*Ar = 0,05 моль * 200 гмоль = 10 г
______________________________________________________________________________________
Пример задачи на избыток и недостаток,
где вещества в другом соотношении:
те же самые этапы решения:
1. Записываем уравнение реакции и уравниваем его:
2N2 + 5O2 = 2N2O5
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(N2 ) = mMr = 1428=0.5 моль
n(O2) = mMr =1632=0.5 моль
3. Сравниваем количество моль веществ и определяем недостаток:
2N2 + 5O2 = 2N2O5
0.5 моль 0.5 моль
в этом уравнении все не так очевидно, как в предыдущем, поэтому нужно просто прикинуть:
- если считать по азоту (0.5 моль), то по соотношению коэффициентов (2:5) кислорода должно быть в 2.5 раза больше, т.е. (0.5*2.5) 1,25 моль, а у нас только 0.5, значит, O2 в недостатке;
- если бы количество моль азота оказалось бы меньше, значит, считали бы по азоту
4. Вычисляем массу продукта по количеству моль, соответствующему недостатку:
m(N2O5) = n*Mr = 2* 0.55 моль * 108 гмоль = 21 г
______________________________________________________________________________________
Есть задачи, очень похожие на задачи избыток-недостаток,
но это задачи на кислые и основные соли:
1. Записываем уравнение реакции и уравниваем его:
здесь у нас возможно 2 варианта — образование средней и кислой соли:
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + NaOH → NaHCO3
2. Находим количество моль тех веществ, массы которых нам даны в условии:
n(CO2 ) = V22.4 лмоль = 24.9 22.4 = 1,11 моль
n(NaOH)= mMr = 44.440 = 1,11 моль
т.к. количество моль веществ одинаково, то делаем вывод, что реакция протекает по схеме образования кислой соли:
CO2 + NaOH → NaHCO3
4. Вычисляем массу продукта по количеству моль:
m ( NaHCO3) = n*Mr = 1,11 * 84 = 93,24 г
______________________________________________________________________________________
Задачи на избыток и недостаток не трудные, зачастую они являются частью более сложных задач, поэтому все, что нужно сделать, это натренироваться — порешать как можно больше таких примеров, внимательно уравнивая и работая с коэффициентами.
Обсуждение: “Задачи на избыток и недостаток”
(Правила комментирования)
Решение задач, когда одно из веществ в избытке
(ответы и решения)
Ключевые слова конспекта: расчет массы, объема продукта реакции, если одно из реагирующих веществ дано в избытке; решение задач, когда одно из веществ в избытке.
Вещества реагируют друг с другом в строго определенных количествах. Однако исходные вещества для проведения реакции могут быть взяты в любых количествах. Таким образом, одно из реагирующих веществ может оказаться в избытке, а другое — в недостатке. В этом случае необходимо определить, какое из реагирующих веществ находится в избытке, а какое — в недостатке, и дальнейшие расчеты производить по веществу, находящемуся в недостатке. Это обусловлено тем, что вещество, находящееся в недостатке, прореагирует полностью, таким образом, количество вещества данного реагента нам будет точно известно.
Для того чтобы определить, какое из реагирующих веществ находится в избытке, а какое — в недостатке, необходимо вычислить количества вещества реагентов и сравнить их. Если количества вещества реагентов, участвующих в химической реакции, одинаковы, то в избытке будет то вещество, количество которого больше в соответствии с условиями задачи. Например, если в реакцию, уравнение которой Н2 + Сl2 = 2НСl, взять 0,2 моль водорода и 0,15 моль хлора, то в избытке будет водород, а в недостатке — хлор, так как v(H2) > v(Cl2). Расчет количества образовавшегося водорода в этом случае следует вести по количеству вещества хлора.
Если же вещества реагируют в неравных количествах, то для расчета избытка и недостатка следует учитывать коэффициенты в уравнении реакции. Например, для реакции, уравнение которой 2Н2 + O2 = 2Н2O, отношение количества веществ водорода и кислорода, реагирующих друг с другом, имеет следующий вид:
При использовании количеств веществ, соответствующих условию задачи, это выражение превращается в неравенство, которое и показывает, какое из веществ взято в реакции в избытке. Например, если в рассматриваемой реакции использовать 0,2 моль водорода и 0,15 моль кислорода, в недостатке будет водород, несмотря на то что количество вещества его больше. Это следует из соотношения: 1 • v(H2) < 2 • v(O2), или 1 • 0,2 < 2 • 0,15, учитывающего коэффициенты в уравнении реакции.
Таким образом, расчет количества образовавшейся воды в данном случае следует вести по количеству вещества водорода.
Особые трудности возникают в тех случаях, когда в зависимости от того, какой из реагентов в избытке, образуются различные продукты реакции. Например, если углекислый газ взаимодействует с избытком гидроксида кальция, образуется средняя соль — карбонат кальция:
Са(ОН)2 + СO2 = CaCO3 ↓ + Н2O.
Если же в избытке углекислый газ, то в результате реакции образуется кислая соль — гидрокарбонат кальция:
Са(ОН)2 + 2СO2 = Са(НСO3)2.
Поэтому в ряде случаев определение избытка и недостатка следует проводить еще до составления уравнения химической реакции.
В некоторых случаях вещество, взятое в избытке, взаимодействует с одним из продуктов реакции, например при восстановлении магнием оксида кремния (IV) по реакции:
взятый в избытке магний будет взаимодействовать с образовавшимся кремнием:
Такие превращения нужно также учитывать при решении задач.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Задача № 1.
Сколько граммов поваренной соли образуется при сливании растворов, содержащих 24 г гидроксида натрия и 14,6 г хлороводорода?
Посмотреть РЕШЕНИЕ

Ответ. m(NaCl) = 23,4 г.
Задача № 2.
Вычислите массу хлорида железа (III), образующегося при взаимодействии 14 г железа и 5,6 л (н. у.) хлора.
Посмотреть РЕШЕНИЕ

О т в е т. m(FeCl3) = 27,08 г.
Задача № 3.
Водород, полученный при разложении 12,6 г гидрида кальция водой, пропустили над 40 г нагретого оксида меди (II). Определите массу образовавшегося металла.
Посмотреть РЕШЕНИЕ

Ответ. m(Cu) = 32 г.
Задача № 4.
Газ, полученный при взаимодействии 19,8 г сульфата аммония и 32 г 25% -ного раствора гидроксида натрия, смешали с газом, полученным при разложении 24,5 г бертолетовой соли. Газовую смесь пропустили через 73г 5%-ного раствора соляной кислоты. Определите состав смеси газов после прохождения через раствор.
Посмотреть РЕШЕНИЕ

Ответ. V(O2) = 6,72 л, V(NH3) = 2,24 л.
Задача № 5.
Каков состав и какова масса соли, которая образуется при пропускании 26,88 л (н. у.) углекислого газа через 210 г раствора с массовой долей гидроксида калия 24% ?
Посмотреть РЕШЕНИЕ

Ответ. m(КНСO3) = 90 г.
Задача № 6.
Смешали 200 г 14% -ного раствора гидроксида натрия и 392 г 10% -ного раствора серной кислоты. Определите массовые доли солей в образовавшемся растворе.
Посмотреть РЕШЕНИЕ

Ответ. ω(NaHSO4) = 2,03%; ω(Na2SO4) = 7,2%.
Задача № 7.
Вычислите массу осадка, который образуется при прибавлении 280 г 20% -ного раствора гидроксида калия к 160,2 г 25%-ного раствора хлорида алюминия.
Посмотреть РЕШЕНИЕ
Ответ. m(А1(ОН)3) = 15,6 г.
ЗАДАЧИ с КРАТКИМ ОТВЕТОМ
- Сколько граммов осадка образуется при взаимодействии 340 г 17,5%-ного раствора нитрата серебра и 109,5 г 20% -ной соляной кислоты?
Ответ. m(AgCl) = 50,2 г.
- 29,12 л аммиака (н. у.) пропустили через 160,17мл раствора 30%-ной азотной кислоты (р = 1,18 г/мл). Определите массу образовавшейся соли.
Ответ. m(NH4NO3) = 72 г.
- Сколько граммов воды образуется при сжигании смеси, содержащей 56 л водорода (н. у.) и 56 г кислорода?
Ответ. m(Н2O) = 45 г.
- Какой объем газа (н. у.) выделится при взаимодействии 24 г смеси алюминия с кремнием, массовая доля алюминия в которой 45%, с 506,1 мл 10% -ного раствора серной кислоты (р = 1,065 г/мл)?
Ответ. V(H2) = 12,32 л.
- К 280 г 10%-ного раствора гидроксида натрия добавили 75 г медного купороса. Выпавший осадок отделили и прокалили. Определите массу образовавшегося продукта и назовите его.
Ответ. m(CuO) = 24 г, оксид меди (II).
- Через 68 г 4%-ного раствора сероводородной кислоты H2S пропустили газ, образовавшийся при сжигании 0,96 г серы в избытке кислорода. Какова масса образовавшегося осадка?
Ответ. m(S) = 2,88 г.
- Нагрели смесь, содержащую 32,5 г цинка и 11,2 г серы. После этого смесь обработали избытком соляной кислоты. Определите объем выделившегося газа (н. у.).
Ответ. V(газа) = 11,2 л.
- Газ, образовавшийся при обработке 19,2 г меди 22,79мл 94%-ной серной кислотой (р = 1,83 г/мл), пропустили через 1200 г бромной воды с массовой долей брома 4% . Будет ли раствор бесцветным после пропускания газа?
Ответ. Раствор останется окрашенным.
- 10,8 г серебра обработали 72,41 мл 30%-ной азотной кислоты (р = 1,48 г/мл). К полученному раствору добавили 18,72 г 25%-ного раствора хлорида натрия. Найдите массу образовавшегося осадка.
Ответ. m(осадка) = 11,48 г.
- Газ, полученный при обработке 26,4 г сульфида железа (II) 73 г 20%-ной соляной кислоты, пропустили через 198,6 г 25% -ного раствора нитрата свинца (II). Определите массу образовавшегося осадка.
Ответ. m(осадка) = 35,85 г.
- Определите массу и состав соли, которая образуется при пропускании 15,68 л аммиака (н. у.) через 61,25 г 40% -ного раствора серной кислоты.
Ответ. m((NH4)2SO4) = 33 г.
- Какая соль образуется при сливании 177 мл 12%-ного раствора гидроксида натрия (р = 1,13 г/мл) и 194,44 мл 14%-ного раствора фосфорной кислоты (р = 1,08 г/мл)? Какова ее масса?
Ответ. m(Na2HPO4) = 42,6 г.
- В 588 г раствора 10%-ной серной кислоты опустили кусочек цинка массой 52 г. Выделившийся водород пропустили при нагревании над 90 г оксида кобальта (II). Найдите массу образовавшегося металла.
Ответ. m(Со) 35,4 г.
- Через 224 г 20%-ного раствора гидроксида калия пропустили 13,44 л (н. у.) оксида серы (IV). Вычислите массы солей в полученном растворе.
Ответ. m(K2SO3) = 31,6 г, m(KHSO3) = 48 г.
- Какова масса осадка, выделившегося при пропускании 5,6 л (н. у.) углекислого газа через известковую воду, содержащую 11,1 г гидроксида кальция?
Ответ. m(осадка) = 5 г.
- В 200 мл воды растворили 56,8 г оксида фосфора (V). К полученному раствору прибавили
76,9 мл раствора с массовой долей NaOH 40% (р = = 1,43 г/мл). Найдите массовые доли солей в полученном растворе.
Ответ. ω(Na2HPO4) — 11,61%, ω(NaH2PO4) = 10,36%.
- Каковы объемные доли газов, образующихся при прокаливании 28,8 г углерода в присутствии 33,6 л кислорода (н. у.)?
Ответ. φ(СО) = 75%, φ(СO2) = 25%.
- После прокаливания смеси, содержащей 32,4 г алюминия и 64 г оксида железа (III), ее обработали избытком соляной кислоты. Определите объем выделившегося при этом газа (н. у.).
Ответ. V(газа) = 31,36 л.
- Какую массу кремния можно получить, прокаливая 21 г оксида кремния (IV) с 32 г кальция?
Ответ. m(Si) = 8,4 г.
- 32,5 г цинка растворили в 240 г 20%-ного раствора гидроксида натрия. К полученному раствору добавили 204,4 г 25% -ной соляной кислоты. Определите массу полученного осадка.
Ответ. m(осадка) = 39,6 г.
Задачи на количества исходных веществ и продуктов реакции (ответы и решения). Выберите дальнейшие действия:
- Перейти к следующей теме:
- Вернуться к списку конспектов по Химии.
- Проверить знания по Химии.
- Купить книгу Задачи по химии и способы их решения. 8-9 кл. / О.С. Габриелян и др. — М.: Дрофа.
Алгоритм определения избытка и недостатка
Задача 4.
В раствор, содержащий 18 г НС1, добавили 15 г Мg. Определите, какое из веществ в избытке.
Дано:
масса хлороводорода: m(НС1) = 18 г;
масса магния: m(Мg) = 15 г.
Найти:
вещество, находящееся в избытке.
Решение:
1. Все данные об исходных участниках реакции из условия задачи переводим в количество вещества.
2. Записываем уравнение реакции и уравниваем его:
Мg + 2НС1 = МgС12 + Н
n = 1 моль n = 2 моль
По коэффициентам в уравнении реакции определяем соотношение количеств веществ интересующих нас исходных реагентов.
В рассматриваемом случае из уравнения следует, что на полное растворение 1 моль Мg необходимо 2 моль НС1.
3. За основу выбираем одно из исходных веществ участников реакции (любое), по которому известны количественные данные (из первого пункта этого плана). В данном случае это будет либо Мg, либо НС1. Выберем за основу Mg. Далее, используя уравнение реакции и количественные данные по выбранному веществу, рассчитываем количество другого исходного вещества, которое необходимо для полного расходования выбранного вещества.В этой задаче нам придется рассчитать количество НС1, которое необходимо для полного расходования 0,617 моль Мg.
Составляем пропорцию:
на 0,617 моль Мg должно расходоваться х моль НС1 (по условию)
на 1 моль Мg полностью расходуется 2 моль НС1 (по уравнению р-ии)

4. Сравнение полученного по пропорции значения количества вещества с данными из условия. Выявление вещества, взятого в избытке, и вещества, взятого в недостатке.
| Количество вещества НС1, которое должно расходоваться для полного растворения всего дан- ного в условии Мg (необходимое количество, определено в третьем действии). | Количество вещества НС1, которое реально дано в условии и участву ет в реакции (из условия задачи, определено в первом действии). |
| 1,234 моль > 0,493 моль |
Из сравнения видно, что для полного растворения Мg требуется большее количество вещества НС1, чем дано в реальности. Следовательно, НС1 находится в недостатке, а Мg — в избытке.
При использовании таких количеств реагентов, которые указаны в условии данной задачи, НС1 расходуется полностью, а М§ будет израсходован не весь, и часть его останется после реакции.
Ответ: В избытке взят магний.
Схематично алгоритм определения избытка и недостатка для последней задачи можно выразить следующим образом:
В третьем действии решения мы могли выбрать за основу и НС1. Схема решения была бы немного другой, но ответ получился бы тот же:
Задача 5.
Раствор, содержащий 15 г НNО3, смешали с раствором, содержащим 10 г гидроксида натрия. Определите массу образовавшейся соли.
Дано:
масса азотной кислоты: m(НNО3) = 15 г;
масса гидроксида натрия: m(NаОН) = 10 г.
Найти:
массу образовавшейся соли.
Решение:
НNO3 + NаОН = NаNO3 + Н2О
Запишем схематично алгоритм решения.
1. Определяем количество веществ НNO3 и NаОН
2. Выберем за основу НNO3 и определим по уравнению реакции количество NаОН, которое необходимо для расходования 0,238 моль НNO3.
Составляем пропорцию:
на 0,238 моль НNO3 должно расходоваться х моль NаОН (по усл.)
на 1 моль НNO3 полностью расходуется 1 моль МаОН (по уравн. р-ции)
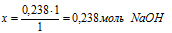
3. Определим, какое вещество в недостатке.
| n(NаОН) необходимо | n(NаОН) дано по условию |
| 0,238моль < 0,250 моль |
Гидроксид натрия находится в избытке и расходуется не весь в процессе реакции. Поэтому дальнейшие расчеты по уравнению реакции будем проводить, используя данные по НNO3.
4. По уравнению реакции определяем массу полученной соли.
Составляем пропорцию:
0,238 моль НNO3 дают х г NaNO3 (по данным условия)
1 моль НNO3 дают 85 г NaNO3 (по уравнению реакции)
Ответ: m(NаNО3) = 20,23 г.
Задачи на избыток-недостаток:
1. Определение избытка-недостатка
Как узнать в любой задаче по химии, что в избытке? плиз подскажите
Ученик
(103),
закрыт
9 лет назад
dredan
Знаток
(266)
10 лет назад
Для начала необходимо рассчитать химическое количество каждого вещества. Затем посмотреть, какое значение меньше. Но необходимо учитывать стехиометреческие коэффициенты в реакции. Например:
А + 2Б = В
Вещества А – 3 моль, а вещества Б – 4 моль. Но на каждый моль А нужно 2 моля Б. Поэтому в недостатке вещество Б.
Вот простой не химический пример. У нас есть 7 ручек и 5 колпачков к ним. Сколько мы можем сделать ручек с колпачками? Только 5.