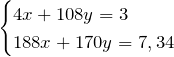Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 8 июня 2019 года; проверки требуют 2 правки.
Изотопы серебра — разновидности атомов (и ядер) химического
элемента серебра, имеющие разное содержание нейтронов в ядре.
Природное серебро является смесью двух стабильных изотопов (107Ag и 109Ag). Самым долгоживущим радиоактивным изотопом серебра является 105Ag с периодом полураспада 41,3 суток, однако ядерный изомер 108mAg имеет период полураспада 439 лет.
Таблица изотопов серебра[править | править код]
| Символ нуклида |
Z(p) | N(n) | Масса изотопа[1] (а. е. м.) |
Период полураспада[2] (T1/2) |
Канал распада | Продукт распада | Спин и чётность ядра[2] |
Распространённость изотопа в природе |
Диапазон изменения изотопной распространённости в природе |
|---|---|---|---|---|---|---|---|---|---|
| Энергия возбуждения | |||||||||
| 92Ag | 47 | 45 | 91,95971(43)# | 1# мс [>400 нс] |
β+ | 92Pd | |||
| p | 91Pd | ||||||||
| 93Ag | 47 | 46 | 92,95019(43)# | 228(16) нс | β+ | 93Pd | 9/2+# | ||
| p | 92Pd | ||||||||
| β+, p | 92Rh | ||||||||
| 94Ag | 47 | 47 | 93,94374(43)# | 27(2) мс | β+ (>99,8%) | 94Pd | 0+# | ||
| β+, p (<0,2%) | 93Rh | ||||||||
| 94m1Ag | 1350(400)# кэВ | 470(10) мс | β+ (83%) | 94Pd | (7+) | ||||
| β+, p (17%) | 93Rh | ||||||||
| 94m2Ag | 6500(550)# кэВ | 400(40) мс | β+ (~68,4%) | 94Pd | (21+) | ||||
| β+, p (~27%) | 93Rh | ||||||||
| p (4,1%) | 93Pd | ||||||||
| 2p (0,5%) | 92Rh | ||||||||
| 95Ag | 47 | 48 | 94,93569(43)# | 1,78(6) с | β+ (97,7%) | 95Pd | (9/2+) | ||
| β+, p (2,3%) | 94Rh | ||||||||
| 95m1Ag | 344,2(3) кэВ | <0,5 с | ИП | 95Ag | (1/2−) | ||||
| 95m2Ag | 2531,3(15) кэВ | <16 мс | ИП | 95Ag | (23/2+) | ||||
| 95m3Ag | 4860,0(15) кэВ | <40 мс | ИП | 95Ag | (37/2+) | ||||
| 96Ag | 47 | 49 | 95,93074(10) | 4,45(3) с | β+ (95,8%) | 96Pd | (8+) | ||
| β+, p (4,2%) | 95Rh | ||||||||
| 96m1Ag | 0(50)# кэВ | 6,9(5) с | β+ (85,1%) | 96Pd | (2+) | ||||
| β+, p (14,9%) | 95Rh | ||||||||
| 96m2Ag | 2461,4(3) кэВ | 103,2(45) мкс | ИП | 96Ag | (13-) | ||||
| 96m3Ag | 2686,7(4) кэВ | 1,561(16) мкс | ИП | 96Ag | (15+) | ||||
| 96m4Ag | 6951,8(14) кэВ | 132(17) нс | ИП | 96Ag | (19+) | ||||
| 97Ag | 47 | 50 | 96,923881(13) | 25,5(3) с | β+ | 97Pd | (9/2+) | ||
| 97mAg | 620(40) кэВ | 100# мс | (1/2-#) | ||||||
| 98Ag | 47 | 51 | 97,92156(4) | 47,5(3) с | β+ (99,99%) | 98Pd | (6)+ | ||
| β+, p (0,0012%) | 97Rh | ||||||||
| 98mAg | 107,28(10) кэВ | 161(7) нс | ИП | 98Ag | (4+) | ||||
| 99Ag | 47 | 52 | 98,917646(7) | 2,07(5) мин | β+ | 99Pd | (9/2)+ | ||
| 99mAg | 506,2(4) кэВ | 10,5(5) с | ИП | 99Ag | (1/2−) | ||||
| 100Ag | 47 | 53 | 99,916115(5) | 2,01(9) мин | β+ | 100Pd | (5)+ | ||
| 100mAg | 15,52(16) кэВ | 2,24(13) мин | ИП | 100Ag | (2)+ | ||||
| β+ | 100Pd | ||||||||
| 101Ag | 47 | 54 | 100,912684(5) | 11,1(3) мин | β+ | 101Pd | 9/2+ | ||
| 101mAg | 274,1(3) кэВ | 3,10(10) с | ИП | 101Ag | 1/2− | ||||
| 102Ag | 47 | 55 | 101,911705(9) | 12,9(3) мин | β+ | 102Pd | 5+ | ||
| 102mAg | 9,40(7) кэВ | 7,7(5) мин | β+ (51%) | 102Pd | 2+ | ||||
| ИП (49%) | 102Ag | ||||||||
| 103Ag | 47 | 56 | 102,908961(4) | 65,7(7) мин | β+ | 103Pd | 7/2+ | ||
| 103mAg | 134,45(4) кэВ | 5,7(3) с | ИП | 103Ag | 1/2− | ||||
| 104Ag | 47 | 57 | 103,908624(5) | 69,2(10) мин | β+ | 104Pd | 5+ | ||
| 104mAg | 6,90(22) кэВ | 33,5(20) мин | β+ (>99,93%) | 104Pd | 2+ | ||||
| ИП (<0,07%) | 104Ag | ||||||||
| 105Ag | 47 | 58 | 104,906526(5) | 41,29(7) сут | β+ | 105Pd | 1/2− | ||
| 105mAg | 25,468(16) кэВ | 7,23(16) мин | ИП (99,66%) | 105Ag | 7/2+ | ||||
| β+ (0,34%) | 105Pd | ||||||||
| 106Ag | 47 | 59 | 105,906663(3) | 23,96(4) мин | β+ | 106Pd | 1+ | ||
| β− (редко) | 106Cd | ||||||||
| 106mAg | 89,66(7) кэВ | 8,28(2) сут | β+ | 106Pd | 6+ | ||||
| ИП (редко) | 106Ag | ||||||||
| 107Ag | 47 | 60 | 106,9050915(26) | стабилен | 1/2− | 0,51839(8) | |||
| 107mAg | 93,125(19) кэВ | 44,3(2) с | ИП | 107Ag | 7/2+ | ||||
| 108Ag | 47 | 61 | 107,9059502(26) | 2,382(11) мин | β− (97,15%) | 108Cd | 1+ | ||
| β+ (2,85%) | 108Pd | ||||||||
| 108mAg | 109,466(7) кэВ | 439(9) лет | β+ (91,3%) | 108Pd | 6+ | ||||
| ИП (8,96%) | 108Ag | ||||||||
| 109Ag | 47 | 62 | 108,9047558(14) | стабилен | 1/2− | 0,48161(8) | |||
| 109mAg | 88,0337(10) кэВ | 39,79(21) с | ИП | 109Ag | 7/2+ | ||||
| 110Ag | 47 | 63 | 109,9061107(14) | 24,56(11) с | β− (99,7%) | 110Cd | 1+ | ||
| ЭЗ (0,3%) | 110Pd | ||||||||
| 110m1Ag | 1,112(16) кэВ | 660(40) нс | ИП | 110Ag | 2− | ||||
| 110m2Ag | 117,59(5) кэВ | 249,863(24) сут | β− (98,67%) | 110Cd | 6+ | ||||
| ИП (1,33%) | 110Ag | ||||||||
| 111Ag | 47 | 64 | 110,9052968(16) | 7,433(10) сут | β− | 111Cd | 1/2− | ||
| 111mAg | 59,82(4) кэВ | 64,8(8) с | ИП (99,3%) | 111Ag | 7/2+ | ||||
| β− (0,7%) | 111Cd | ||||||||
| 112Ag | 47 | 65 | 111,9070485(26) | 3,130(8) ч | β− | 112Cd | 2(−) | ||
| 113Ag | 47 | 66 | 112,906573(18) | 5,37(5) ч | β− | 113mCd | 1/2− | ||
| 113mAg | 43,50(10) кэВ | 68,7(16) с | ИП (64%) | 113Ag | 7/2+ | ||||
| β− (36%) | 113Cd | ||||||||
| 114Ag | 47 | 67 | 113,908823(5) | 4,6(1) с | β− | 114Cd | 1+ | ||
| 114mAg | 198,9(10) кэВ | 1,50(5) мс | ИП | 114Ag | (6+) | ||||
| 115Ag | 47 | 68 | 114,908767(20) | 20,0(5) мин | β− | 115mCd | 1/2− | ||
| 115mAg | 41,16(10) кэВ | 18,0(7) с | β− (79%) | 115Cd | 7/2+ | ||||
| ИП (21%) | 115Ag | ||||||||
| 116Ag | 47 | 69 | 115,911387(4) | 3,83(8) мин | β− | 116Cd | (0-) | ||
| 116m1Ag | 47,90(10) кэВ | 20(1) с | β− (93%) | 116Cd | (3+) | ||||
| ИП (7%) | 116Ag | ||||||||
| 116m2Ag | 129,80(22) кэВ | 9,3(3) с | β− (92%) | 116Cd | (6-) | ||||
| ИП (8%) | 116Ag | ||||||||
| 117Ag | 47 | 70 | 116,911774(15) | 73,6(14) с | β− | 117mCd | 1/2−# | ||
| 117mAg | 28,6(2) кэВ | 5,34(5) с | β− (94%) | 117mCd | 7/2+# | ||||
| ИП (6%) | 117Ag | ||||||||
| 118Ag | 47 | 71 | 117,9145955(27) | 3,76(15) с | β− | 118Cd | (2-) | ||
| 118m1Ag | 45,79(9) кэВ | ~0,1 мкс | ИП | 118Ag | 1(−) to 2(−) | ||||
| 118m2Ag | 127,63(10) кэВ | 2,0(2) с | β− (59%) | 118Cd | (5+) | ||||
| ИП (41%) | 118Ag | ||||||||
| 118m3Ag | 279,37(20) кэВ | ~0,1 мкс | ИП | 118Ag | (3+) | ||||
| 119Ag | 47 | 72 | 118,915570(16) | 6,0(5) с | β− | 119mCd | 1/2−# | ||
| 119mAg | 20(20)# кэВ | 2,1(1) с | β− | 119Cd | 7/2+# | ||||
| 120Ag | 47 | 73 | 119,918785(5) | 1,52(7) с | β− (>99,997%) | 120Cd | 4(+) | ||
| β−, n (<.003%) | 119Cd | ||||||||
| 120m1Ag | 0(50)# кэВ | 940(100) мс | (0−, 1-) | ||||||
| 120m2Ag | 203,0(10) кэВ | 384(22) мс | ИП (68%) | 120Sn | 7(−) | ||||
| β− (32%) | 120Cd | ||||||||
| 121Ag | 47 | 74 | 120,920125(13) | 777(10) мс | β− (99,92%) | 121Cd | 7/2+# | ||
| β−, n (0,076%) | 120Cd | ||||||||
| 121mAg | 20(20)# кэВ | 200# мс | 1/2-# | ||||||
| 122Ag | 47 | 75 | 121,92366(4) | 529(13) мс | β− (>99,814%) | 122Cd | (3+) | ||
| β−, n (0,186%) | 121Cd | ||||||||
| 122m1Ag | 80(50)# кэВ | 550(50) мс | β− | 122Cd | (1-) | ||||
| β−, n (редко) | 121Cd | ||||||||
| ИП (редко) | 122Ag | ||||||||
| 122m2Ag | 80(50)# кэВ | 200(50) мс | β− | 122Cd | (9-) | ||||
| β−, n (редко) | 121Cd | ||||||||
| ИП (редко) | 122Ag | ||||||||
| 122m3Ag | 171(50)# кэВ | 6,3(1) мкс | ИП | 122Ag | (1+) | ||||
| 123Ag | 47 | 76 | 122,92532(4) | 294(5) мс | β− (99,44%) | 123Cd | (7/2+) | ||
| β−, n (0,56%) | 122Cd | ||||||||
| 123m1Ag | 59,5(5) кэВ | 100# мс | β− | 123Cd | (1/2-) | ||||
| β−, n (редко) | 122Cd | ||||||||
| 123m2Ag | 1450(14)# кэВ | 202(20) нс | ИП | 123Ag | |||||
| 123m3Ag | 1472,8(8) кэВ | 393(16) нс | ИП | 123Ag | (17/2-) | ||||
| 124Ag | 47 | 77 | 123,92890(27)# | 177,9(26) мс | β− (98,7%) | 124Cd | (2-) | ||
| β−, n (1,3%) | 123Cd | ||||||||
| 124m1Ag | 50(50)# кэВ | 144(20) мс | β− | 124Cd | 9-# | ||||
| β−, n | 123Cd | ||||||||
| 124m2Ag | 155,6(5)# кэВ | 140(50) нс | ИП | 124Ag | (1+) | ||||
| 124m3Ag | 231,1(7)# кэВ | 1,48(15) мкс | ИП | 124Ag | (1-) | ||||
| 125Ag | 47 | 78 | 124,93074(47) | 160(5) мс | β− (88,2%) | 125Cd | (9/2+) | ||
| β−, n (11,8%) | 124Cd | ||||||||
| 125m1Ag | 97,1(5)# кэВ | 50# мс | (1/2-) | ||||||
| 125m2Ag | 97,1(5)# кэВ | 491(20) нс | (17/2-) | ||||||
| 126Ag | 47 | 79 | 125,93481(22)# | 52(10) мс | β− (86,3%) | 126Cd | 3+# | ||
| β−, n (13,7%) | 125Cd | ||||||||
| 126m1Ag | 100(100)# кэВ | 108,4(24) мс | 9-# | ||||||
| 126m2Ag | 97,1(5)# кэВ | 27(6) мкс | ИП | 126Ag | 1-# | ||||
| 127Ag | 47 | 80 | 126,93704(22)# | 89(2) мс | β− (85,4%) | 127Cd | (9/2+) | ||
| β−, n (14,6%) | 126Cd | ||||||||
| 127m1Ag | 20(20)# кэВ | 20# мс | (1/2-) | ||||||
| 127m2Ag | 1938(17) кэВ | 67,5(9) мс | β– (91,2%) | 127Cd | (27/2+) | ||||
| ИП (8,8%) | 127Ag | ||||||||
| 128Ag | 47 | 81 | 127,94127(32)# | 60(3) мс | β− (80%) | 128Cd | 3+# | ||
| β−, n (20%) | 127Cd | ||||||||
| 129Ag | 47 | 82 | 128,94432(43)# | 49,9(35) мс | β− (>80%) | 129Cd | 9/2+# | ||
| β−, n (<20%) | 128Cd | ||||||||
| 129mAg | 20(20)# кэВ | 10# мс | 1/2−# | ||||||
| 130Ag | 47 | 83 | 129,95073(46)# | 40,6(45) мс | β− | 130Cd | 1-# | ||
| 131Ag | 47 | 84 | 130,95625(54)# | 35(8) мс | β− | 131Cd | 9/2+# | ||
| β−, n | 130Cd | ||||||||
| β−, 2n | 129Cd | ||||||||
| 132Ag | 47 | 85 | 131,96307(54)# | 30(14) мс | β− | 132Cd | 6-# | ||
| 133Ag | 47 | 86 | 132,96878(54)# | 6-# |
Пояснения к таблице[править | править код]
- Распространённость изотопов приведена для большинства природных образцов. Для других источников значения могут сильно отличаться.
- Индексами ‘m’, ‘n’, ‘p’ (рядом с символом) обозначены возбужденные изомерные состояния нуклида.
- Символами, выделенными жирным шрифтом, обозначены стабильные продукты распада. Символами, выделенными жирным курсивом, обозначены радиоактивные продукты распада, имеющие периоды полураспада, сравнимые с возрастом Земли или превосходящие его и вследствие этого присутствующие в природной смеси.
- Значения, помеченные решёткой (#), получены не из одних лишь экспериментальных данных, а (хотя бы частично) оценены из систематических трендов у соседних нуклидов (с такими же соотношениями Z и N). Неуверенно определённые значения спина и/или чётности заключены в скобки.
- Погрешность приводится в виде числа в скобках, выраженного в единицах последней значащей цифры, означает одно стандартное отклонение (за исключением распространённости и стандартной атомной массы изотопа по данным ИЮПАК, для которых используется более сложное определение погрешности). Примеры: 29770,6(5) означает 29770,6 ± 0,5; 21,48(15) означает 21,48 ± 0,15; −2200,2(18) означает −2200,2 ± 1,8.
Примечания[править | править код]
- ↑ Данные приведены по Huang W. J., Meng Wang, Kondev F. G., Audi G., Naimi S. The Ame2020 atomic mass evaluation (I). Evaluation of input data, and adjustment procedures (англ.) // Chinese Physics C. — 2021. — Vol. 43, iss. 3. — P. 030002-1—030002-342. — doi:10.1088/1674-1137/abddb0.
- ↑ 1 2 Данные приведены по Kondev F. G., Wang M., Huang W. J., Naimi S., Audi G. The Nubase2020 evaluation of nuclear properties (англ.) // Chinese Physics C. — 2021. — Vol. 45, iss. 3. — P. 030001-1—030001-180. — doi:10.1088/1674-1137/abddae.
From Wikipedia, the free encyclopedia
|
||||||||||||||||||||||||||||||||||||||||||||||||||
| Standard atomic weight Ar°(Ag) | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
Naturally occurring silver (47Ag) is composed of the two stable isotopes 107Ag and 109Ag in almost equal proportions, with 107Ag being slightly more abundant (51.839% natural abundance). 40 radioisotopes have been characterized with the most stable being 105Ag with a half-life of 41.29 days, 111Ag with a half-life of 7.43 days, and 112Ag with a half-life of 3.13 hours.
All of the remaining radioactive isotopes have half-lives that are less than an hour, and the majority of these have half-lives that are less than 3 minutes. This element has numerous meta states, with the most stable being 108mAg (half-life 439 years), 110mAg (half-life 249.86 days) and 106mAg (half-life 8.28 days).
Isotopes of silver range in atomic weight from 91.960 u (92Ag) to 132.969 u (133Ag). The primary decay mode before the most abundant stable isotope, 107Ag, is electron capture and the primary mode after is beta decay. The primary decay products before 107Ag are palladium (element 46) isotopes and the primary products after are cadmium (element 48) isotopes.
The palladium isotope 107Pd decays by beta emission to 107Ag with a half-life of 6.5 million years. Iron meteorites are the only objects with a high enough palladium/silver ratio to yield measurable variations in 107Ag abundance. Radiogenic 107Ag was first discovered in the Santa Clara meteorite in 1978.
The discoverers suggest that the coalescence and differentiation of iron-cored small planets may have occurred 10 million years after a nucleosynthetic event. 107Pd versus 107Ag correlations observed in bodies, which have clearly been melted since the accretion of the Solar System, must reflect the presence of live short-lived nuclides in the early Solar System.
List of isotopes[edit]
| Nuclide[4] [n 1] |
Z | N | Isotopic mass (Da)[5] [n 2][n 3] |
Half-life [n 4] |
Decay mode [n 5] |
Daughter isotope [n 6][n 7] |
Spin and parity [n 8][n 4] |
Natural abundance (mole fraction) | |
|---|---|---|---|---|---|---|---|---|---|
| Excitation energy[n 4] | Normal proportion | Range of variation | |||||||
| 92Ag | 47 | 45 | 91.95971(43)# | 1# ms [>400 ns] |
β+ | 92Pd | |||
| p | 91Pd | ||||||||
| 93Ag | 47 | 46 | 92.95019(43)# | 228(16) ns | β+ | 93Pd | 9/2+# | ||
| p | 92Pd | ||||||||
| β+, p | 92Rh | ||||||||
| 94Ag | 47 | 47 | 93.94374(43)# | 27(2) ms | β+ (>99.8%) | 94Pd | 0+# | ||
| β+, p (<0.2%) | 93Rh | ||||||||
| 94m1Ag | 1350(400)# keV | 470(10) ms | β+ (83%) | 94Pd | (7+) | ||||
| β+, p (17%) | 93Rh | ||||||||
| 94m2Ag | 6500(550)# keV | 400(40) ms | β+ (~68.4%) | 94Pd | (21+) | ||||
| β+, p (~27%) | 93Rh | ||||||||
| p (4.1%) | 93Pd | ||||||||
| 2p (0.5%) | 92Rh | ||||||||
| 95Ag | 47 | 48 | 94.93569(43)# | 1.78(6) s | β+ (97.7%) | 95Pd | (9/2+) | ||
| β+, p (2.3%) | 94Rh | ||||||||
| 95m1Ag | 344.2(3) keV | <0.5 s | IT | 95Ag | (1/2−) | ||||
| 95m2Ag | 2531.3(15) keV | <16 ms | IT | 95Ag | (23/2+) | ||||
| 95m3Ag | 4860.0(15) keV | <40 ms | IT | 95Ag | (37/2+) | ||||
| 96Ag | 47 | 49 | 95.93074(10) | 4.45(3) s | β+ (95.8%) | 96Pd | (8+) | ||
| β+, p (4.2%) | 95Rh | ||||||||
| 96m1Ag | 0(50)# keV | 6.9(5) s | β+ (85.1%) | 96Pd | (2+) | ||||
| β+, p (14.9%) | 95Rh | ||||||||
| 96m2Ag | 2461.4(3) keV | 103.2(45) μs | IT | 96Ag | (13-) | ||||
| 96m3Ag | 2686.7(4) keV | 1.561(16) μs | IT | 96Ag | (15+) | ||||
| 96m4Ag | 6951.8(14) keV | 132(17) ns | IT | 96Ag | (19+) | ||||
| 97Ag | 47 | 50 | 96.923881(13) | 25.5(3) s | β+ | 97Pd | (9/2+) | ||
| 97mAg | 620(40) keV | 100# ms | (1/2-#) | ||||||
| 98Ag | 47 | 51 | 97.92156(4) | 47.5(3) s | β+ (99.99%) | 98Pd | (6)+ | ||
| β+, p (.0012%) | 97Rh | ||||||||
| 98mAg | 107.28(10) keV | 161(7) ns | IT | 98Ag | (4+) | ||||
| 99Ag | 47 | 52 | 98.917646(7) | 2.07(5) min | β+ | 99Pd | (9/2)+ | ||
| 99mAg | 506.2(4) keV | 10.5(5) s | IT | 99Ag | (1/2−) | ||||
| 100Ag | 47 | 53 | 99.916115(5) | 2.01(9) min | β+ | 100Pd | (5)+ | ||
| 100mAg | 15.52(16) keV | 2.24(13) min | IT | 100Ag | (2)+ | ||||
| β+ | 100Pd | ||||||||
| 101Ag | 47 | 54 | 100.912684(5) | 11.1(3) min | β+ | 101Pd | 9/2+ | ||
| 101mAg | 274.1(3) keV | 3.10(10) s | IT | 101Ag | 1/2− | ||||
| 102Ag | 47 | 55 | 101.911705(9) | 12.9(3) min | β+ | 102Pd | 5+ | ||
| 102mAg | 9.40(7) keV | 7.7(5) min | β+ (51%) | 102Pd | 2+ | ||||
| IT (49%) | 102Ag | ||||||||
| 103Ag | 47 | 56 | 102.908961(4) | 65.7(7) min | β+ | 103Pd | 7/2+ | ||
| 103mAg | 134.45(4) keV | 5.7(3) s | IT | 103Ag | 1/2− | ||||
| 104Ag | 47 | 57 | 103.908624(5) | 69.2(10) min | β+ | 104Pd | 5+ | ||
| 104mAg | 6.90(22) keV | 33.5(20) min | β+ (>99.93%) | 104Pd | 2+ | ||||
| IT (<0.07%) | 104Ag | ||||||||
| 105Ag | 47 | 58 | 104.906526(5) | 41.29(7) d | β+ | 105Pd | 1/2− | ||
| 105mAg | 25.468(16) keV | 7.23(16) min | IT (99.66%) | 105Ag | 7/2+ | ||||
| β+ (.34%) | 105Pd | ||||||||
| 106Ag | 47 | 59 | 105.906663(3) | 23.96(4) min | β+ | 106Pd | 1+ | ||
| β− (rare) | 106Cd | ||||||||
| 106mAg | 89.66(7) keV | 8.28(2) d | β+ | 106Pd | 6+ | ||||
| IT (rare) | 106Ag | ||||||||
| 107Ag[n 9] | 47 | 60 | 106.9050915(26) | Stable[n 10] | 1/2− | 0.51839(8) | |||
| 107mAg | 93.125(19) keV | 44.3(2) s | IT | 107Ag | 7/2+ | ||||
| 108Ag | 47 | 61 | 107.9059502(26) | 2.382(11) min | β− (97.15%) | 108Cd | 1+ | ||
| β+ (2.85%) | 108Pd | ||||||||
| 108mAg | 109.466(7) keV | 439(9) y | β+ (91.3%) | 108Pd | 6+ | ||||
| IT (8.96%) | 108Ag | ||||||||
| 109Ag[n 11] | 47 | 62 | 108.9047558(14) | Stable[n 10] | 1/2− | 0.48161(8) | |||
| 109mAg | 88.0337(10) keV | 39.79(21) s | IT | 109Ag | 7/2+ | ||||
| 110Ag | 47 | 63 | 109.9061107(14) | 24.56(11) s | β− (99.7%) | 110Cd | 1+ | ||
| EC (.3%) | 110Pd | ||||||||
| 110m1Ag | 1.112(16) keV | 660(40) ns | IT | 110Ag | 2− | ||||
| 110m2Ag | 117.59(5) keV | 249.863(24) d | β− (98.67%) | 110Cd | 6+ | ||||
| IT (1.33%) | 110Ag | ||||||||
| 111Ag[n 11] | 47 | 64 | 110.9052968(16) | 7.433(10) d | β− | 111Cd | 1/2− | ||
| 111mAg | 59.82(4) keV | 64.8(8) s | IT (99.3%) | 111Ag | 7/2+ | ||||
| β− (.7%) | 111Cd | ||||||||
| 112Ag | 47 | 65 | 111.9070485(26) | 3.130(8) h | β− | 112Cd | 2(−) | ||
| 113Ag | 47 | 66 | 112.906573(18) | 5.37(5) h | β− | 113mCd | 1/2− | ||
| 113mAg | 43.50(10) keV | 68.7(16) s | IT (64%) | 113Ag | 7/2+ | ||||
| β− (36%) | 113Cd | ||||||||
| 114Ag | 47 | 67 | 113.908823(5) | 4.6(1) s | β− | 114Cd | 1+ | ||
| 114mAg | 198.9(10) keV | 1.50(5) ms | IT | 114Ag | (6+) | ||||
| 115Ag | 47 | 68 | 114.908767(20) | 20.0(5) min | β− | 115mCd | 1/2− | ||
| 115mAg | 41.16(10) keV | 18.0(7) s | β− (79%) | 115Cd | 7/2+ | ||||
| IT (21%) | 115Ag | ||||||||
| 116Ag | 47 | 69 | 115.911387(4) | 3.83(8) min | β− | 116Cd | (0-) | ||
| 116m1Ag | 47.90(10) keV | 20(1) s | β− (93%) | 116Cd | (3+) | ||||
| IT (7%) | 116Ag | ||||||||
| 116m2Ag | 129.80(22) keV | 9.3(3) s | β− (92%) | 116Cd | (6-) | ||||
| IT (8%) | 116Ag | ||||||||
| 117Ag | 47 | 70 | 116.911774(15) | 73.6(14) s | β− | 117mCd | 1/2−# | ||
| 117mAg | 28.6(2) keV | 5.34(5) s | β− (94%) | 117mCd | 7/2+# | ||||
| IT (6%) | 117Ag | ||||||||
| 118Ag | 47 | 71 | 117.9145955(27) | 3.76(15) s | β− | 118Cd | (2-) | ||
| 118m1Ag | 45.79(9) keV | ~0.1 µs | IT | 118Ag | 1(−) to 2(−) | ||||
| 118m2Ag | 127.63(10) keV | 2.0(2) s | β− (59%) | 118Cd | (5+) | ||||
| IT (41%) | 118Ag | ||||||||
| 118m3Ag | 279.37(20) keV | ~0.1 µs | IT | 118Ag | (3+) | ||||
| 119Ag | 47 | 72 | 118.915570(16) | 6.0(5) s | β− | 119mCd | 1/2−# | ||
| 119mAg | 20(20)# keV | 2.1(1) s | β− | 119Cd | 7/2+# | ||||
| 120Ag | 47 | 73 | 119.918785(5) | 1.52(7) s | β− (>99.997%) | 120Cd | 4(+) | ||
| β−, n (<.003%) | 119Cd | ||||||||
| 120m1Ag | 0(50)# keV | 940(100) ms | (0−, 1-) | ||||||
| 120m2Ag | 203.0(10) keV | 384(22) ms | IT (68%) | 120Sn | 7(−) | ||||
| β− (32%) | 120Cd | ||||||||
| 121Ag | 47 | 74 | 120.920125(13) | 777(10) ms | β− (99.92%) | 121Cd | 7/2+# | ||
| β−, n (.076%) | 120Cd | ||||||||
| 121mAg | 20(20)# keV | 200# ms | 1/2-# | ||||||
| 122Ag | 47 | 75 | 121.92366(4) | 529(13) ms | β− (>99.814%) | 122Cd | (3+) | ||
| β−, n (.186%) | 121Cd | ||||||||
| 122m1Ag | 80(50)# keV | 550(50) ms | β− | 122Cd | (1-) | ||||
| β−, n (rare) | 121Cd | ||||||||
| IT (rare) | 122Ag | ||||||||
| 122m2Ag | 80(50)# keV | 200(50) ms | β− | 122Cd | (9-) | ||||
| β−, n (rare) | 121Cd | ||||||||
| IT (rare) | 122Ag | ||||||||
| 122m3Ag | 171(50)# keV | 6.3(1) μs | IT | 122Ag | (1+) | ||||
| 123Ag | 47 | 76 | 122.92532(4) | 294(5) ms | β− (99.44%) | 123Cd | (7/2+) | ||
| β−, n (.56%) | 122Cd | ||||||||
| 123m1Ag | 59.5(5) keV | 100# ms | β− | 123Cd | (1/2-) | ||||
| β−, n (rare) | 122Cd | ||||||||
| 123m2Ag | 1450(14)# keV | 202(20) ns | IT | 123Ag | |||||
| 123m3Ag | 1472.8(8) keV | 393(16) ns | IT | 123Ag | (17/2-) | ||||
| 124Ag | 47 | 77 | 123.92890(27)# | 177.9(26) ms | β− (98.7%) | 124Cd | (2-) | ||
| β−, n (1.3%) | 123Cd | ||||||||
| 124m1Ag | 50(50)# keV | 144(20) ms | β− | 124Cd | 9-# | ||||
| β−, n | 123Cd | ||||||||
| 124m2Ag | 155.6(5)# keV | 140(50) ns | IT | 124Ag | (1+) | ||||
| 124m3Ag | 231.1(7)# keV | 1.48(15) μs | IT | 124Ag | (1-) | ||||
| 125Ag | 47 | 78 | 124.93074(47) | 160(5) ms | β− (88.2%) | 125Cd | (9/2+) | ||
| β−, n (11.8%) | 124Cd | ||||||||
| 125m1Ag | 97.1(5)# keV | 50# ms | (1/2-) | ||||||
| 125m2Ag | 97.1(5)# keV | 491(20) ns | (17/2-) | ||||||
| 126Ag | 47 | 79 | 125.93481(22)# | 52(10) ms | β− (86.3%) | 126Cd | 3+# | ||
| β−, n (13.7%) | 125Cd | ||||||||
| 126m1Ag | 100(100)# keV | 108.4(24) ms | 9-# | ||||||
| 126m2Ag | 97.1(5)# keV | 27(6) μs | IT | 126Ag | 1-# | ||||
| 127Ag | 47 | 80 | 126.93704(22)# | 89(2) ms | β− (85.4%) | 127Cd | (9/2+) | ||
| β−, n (14.6%) | 126Cd | ||||||||
| 127m1Ag | 20(20)# keV | 20# ms | (1/2-) | ||||||
| 127m2Ag | 1938(17) keV | 67.5(9) ms | β− (91.2%) | 127Cd | (27/2+) | ||||
| IT (8.8%) | 127Ag | ||||||||
| 128Ag | 47 | 81 | 127.94127(32)# | 60(3) ms | β− (80%) | 128Cd | 3+# | ||
| β−, n (20%) | 127Cd | ||||||||
| 129Ag | 47 | 82 | 128.94432(43)# | 49.9(35) ms | β− (>80%) | 129Cd | 9/2+# | ||
| β−, n (<20%) | 128Cd | ||||||||
| 129mAg | 20(20)# keV | 10# ms | 1/2−# | ||||||
| 130Ag | 47 | 83 | 129.95073(46)# | 40.6(45) ms | β− | 130Cd | 1-# | ||
| 131Ag | 47 | 84 | 130.95625(54)# | 35(8) ms | β− | 131Cd | 9/2+# | ||
| β−, n | 130Cd | ||||||||
| β−, 2n | 129Cd | ||||||||
| 132Ag | 47 | 85 | 131.96307(54)# | 30(14) ms | β− | 132Cd | 6-# | ||
| 133Ag | 47 | 86 | 132.96878(54)# | 6-# | |||||
This table header & footer:
|
- ^ mAg – Excited nuclear isomer.
- ^ ( ) – Uncertainty (1σ) is given in concise form in parentheses after the corresponding last digits.
- ^ # – Atomic mass marked #: value and uncertainty derived not from purely experimental data, but at least partly from trends from the Mass Surface (TMS).
- ^ a b c # – Values marked # are not purely derived from experimental data, but at least partly from trends of neighboring nuclides (TNN).
- ^
Modes of decay:
- ^ Bold italics symbol as daughter – Daughter product is nearly stable.
- ^ Bold symbol as daughter – Daughter product is stable.
- ^ ( ) spin value – Indicates spin with weak assignment arguments.
- ^ Used to date certain events in the early history of the Solar System
- ^ a b Theoretically capable of spontaneous fission
- ^ a b Fission product
References[edit]
- ^ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). “The NUBASE2020 evaluation of nuclear properties” (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ “Standard Atomic Weights: Silver”. CIAAW. 1985.
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; et al. (2022-05-04). “Standard atomic weights of the elements 2021 (IUPAC Technical Report)”. Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- ^ Half-life, decay mode, nuclear spin, and isotopic composition is sourced in:
Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). “The NUBASE2020 evaluation of nuclear properties” (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae. - ^ Wang, Meng; Huang, W.J.; Kondev, F.G.; Audi, G.; Naimi, S. (2021). “The AME 2020 atomic mass evaluation (II). Tables, graphs and references*”. Chinese Physics C. 45 (3): 030003. doi:10.1088/1674-1137/abddaf.
- Isotope masses from:
- Wang, Meng; Huang, W.J.; Kondev, F.G.; Audi, G.; Naimi, S. (2021). “The AME 2020 atomic mass evaluation (II). Tables, graphs and references*”. Chinese Physics C. 45 (3): 030003. doi:10.1088/1674-1137/abddaf.
- Isotopic compositions and standard atomic masses from:
- Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). “The NUBASE2020 evaluation of nuclear properties” (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- de Laeter, John Robert; Böhlke, John Karl; De Bièvre, Paul; Hidaka, Hiroshi; Peiser, H. Steffen; Rosman, Kevin J. R.; Taylor, Philip D. P. (2003). “Atomic weights of the elements. Review 2000 (IUPAC Technical Report)”. Pure and Applied Chemistry. 75 (6): 683–800. doi:10.1351/pac200375060683.
- Wieser, Michael E. (2006). “Atomic weights of the elements 2005 (IUPAC Technical Report)”. Pure and Applied Chemistry. 78 (11): 2051–2066. doi:10.1351/pac200678112051.
- “News & Notices: Standard Atomic Weights Revised”. International Union of Pure and Applied Chemistry. 19 October 2005.
- Half-life, spin, and isomer data selected from the following sources.
- Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). “The NUBASE2020 evaluation of nuclear properties” (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- National Nuclear Data Center. “NuDat 2.x database”. Brookhaven National Laboratory.
- Holden, Norman E. (2004). “11. Table of the Isotopes”. In Lide, David R. (ed.). CRC Handbook of Chemistry and Physics (85th ed.). Boca Raton, Florida: CRC Press. ISBN 978-0-8493-0485-9.
Содержание
- Серебро и его характеристики
- Общая характеристика серебра
- Атомная и молекулярная масса серебра
- Изотопы серебра
- Ионы серебра
- Молекула и атом серебра
- Сплавы серебра
- Примеры решения задач
- Изотопы серебра
- Таблица изотопов серебра
- Примечания
- Полезное
- Смотреть что такое «Изотопы серебра» в других словарях:
- Изотопы серебра — Isotopes of silver
Серебро и его характеристики
Общая характеристика серебра
Серебро распространено в природе значительно меньше, чем, например, медь; содержание его в земной коре составляет 10 -5 % (масс.). В некоторых местах (например, в Канаде) серебро встречается в самородном состоянии, но большую часть серебра из его соединений. Самой важной серебряной рудой является серебряный блеск, или агрентит, Ag2S.
В качестве примеси серебро присутствует почти во всех медных и особенно свинцовых рудах. Из этих руд получают около 80% всего добываемого серебра.
Чистое серебро – очень мягкий, тягучий металл (рис. 1), оно лучше всех металлов проводит теплоту и электрический ток.
Серебро – малоактивный металл. В атмосфере воздуха оно не окисляется ни при комнатных температурах, ни при нагревании. Часто наблюдаемое почернение серебряных предметов – результат образования на поверхности черного сульфида серебра Ag2S.
Рис. 1. Серебро. Внешний вид.
Атомная и молекулярная масса серебра
Поскольку в свободном состоянии серебро существует в виде одноатомных молекул Ag, значения его атомной и молекулярной масс совпадают. Они равны 107,8682.
Изотопы серебра
Известно, что в природе серебро может находиться в виде двух стабильных изотопов 107 Ag и 109 Ag. Их массовые числа равны 107 и 109 соответственно. Ядро атома изотопа серебра 107 Ag содержит сорок семь протонов и шестьдесят нейтронов, а изотопа 109 Ag – такое число протонов и шестьдесят два нейтрона.
Существуют искусственные нестабильные изотопы серебра с массовыми числами от 93-х до 130-ти, а также тридцать шесть изомерных состояния ядер, среди которых наиболее долгоживущим является изотоп 104 Ag с периодом полураспада равным 69,2 минуты.
Ионы серебра
На внешнем энергетическом уровне атома серебра имеется один электрон, который является валентным:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 9 5s 2 .
В результате химического взаимодействия серебро отдает свой валентный электрон, т.е. является его донором, и превращается в положительно заряженный ион:
Молекула и атом серебра
В свободном состоянии серебро существует в виде одноатомных молекул Ag. Приведем некоторые свойства, характеризующие атом и молекулу серебра:
Энергия ионизации атома, кДж/моль
Радиус атома, нм
Сплавы серебра
На практике чистое серебро вследствие мягкости почти не применяется: обычно его сплавляют с большим или меньшим количеством меди. Сплавы серебра служат для изготовления ювелирных и бытовых изделий, монет, лабораторной посуды.
Примеры решения задач
| Задание | Вычислите массовую долю нитрата серебра в растворе, полученном при растворении соли массой 40 г в воде количеством 20 моль. |
| Решение | Найдем массу воды (молярная масса 18 г/моль): |
m (H2O)= 20 × 18 = 360 г.
Рассчитаем массу раствора нитрата серебра:
msolution(AgNO3) = 40 + 360 = 400 г.
Вычислим массовую долю нитрата серебра в растворе:
ω (AgNO3)=40 / 400 × 100% = 10%.
Ответ Массовая долю нитрата серебра в растворе равна 10%
| Задание | При растворении 3 г сплава меди и серебра в концентрированной азотной кислоте получили 7,34 г смеси нитратов. Определите массовые доли металлов в сплаве. |
| Решение | Запишем уравнения реакций взаимодействия металлов, представляющих собой сплав (медь и серебро), в концентрированной азотной кислоте: |
В результате реакции образуется смесь, состоящая из нитрата серебра и нитрата меди (II). Пусть количество вещества меди в сплаве составляет х моль, а количество вещества серебра – у моль. Тогда массы этих металлов будут равны (молярная масса меди 64 г/моль, серебра – 108 г/моль):
m (Cu) = n (Cu) × M (Cu);
m (Cu)= x × 64 = 64x.
m (Ag) = n (Ag) × M (Ag);
m (Ag)= x × 108 = 108y.
Согласно условию задачи, масса сплава равна 3 г, т.е.:
По уравнению (1) n(Cu) : n(Cu(NO3)2) = 1:1, значит n(Cu(NO3)2) = n(Cu) =х. Тогда масса нитрата меди (II) составляет (молярная масса равна 188 г/моль) 188х.
Согласно уравнению (2), n(Ag) : n(AgNO3) = 1:1, значит n(AgNO3) = n(Ag) =y. Тогда масса нитрата серебра составляет (молярная масса равна 170 г/моль) 170y.
По условию задачи масса смеси нитратов равна 7,34 г:
188 х + 170 у = 7,34.
Получили систему уравнений с двумя неизвестными:
Выразим из первого уравнения х и подставим это значение во второе уравнение, т.е. решим систему методом подстановки.
Значит количество вещества серебра равно 0,01 моль. Тогда, масса серебра в сплаве равна:
m (Ag) = n (Ag) × M (Ag) = 0,01 × 108 = 1,08г.
Не вычисляя x можно найти массу меди в сплаве:
m (Cu) = malloy– m (Ag) = 3 – 1,08 = 1,92 г.
Источник
Изотопы серебра
Изотопы серебра — разновидности атомов (и ядер) химического элемента серебра, имеющие разное содержание нейтронов в ядре.
Таблица изотопов серебра
| Символ нуклида |
Z(p) | N(n) | Масса изотопа [1] (а. е. м.) |
Период полураспада [2] (T1/2) |
Спин и чётность ядра [2] |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 93 Ag | 47 | 46 | 92,94978 | 5 мс | 9/2+ |
| 94 Ag | 47 | 47 | 93,94278 | 37 мс | 0+ |
| 94m1 Ag | 1,350 МэВ | 422 мс | 7+ | ||
| 94m2 Ag | 6,50 МэВ | 300 мс | 21+ | ||
| 95 Ag | 47 | 48 | 94,93548 | 1,74 с | 9/2+ |
| 95m1 Ag | 344,2 кэВ | 500 мс | 1/2- | ||
| 95m2 Ag | 2,531 МэВ | 16 мс | 23/2+ | ||
| 95m3 Ag | 4,859 МэВ | 40 мс | 37/2+ | ||
| 96 Ag | 47 | 49 | 95,93068 | 4,45 с | 8+ |
| 96m1 Ag | 0 кэВ | 6,9 с | 2+ | ||
| 96m2 Ag | 700 нс | ||||
| 97 Ag | 47 | 50 | 96,92397 | 25,3 с | 9/2+ |
| 97m Ag | 2,343 МэВ | 5 нс | 21/2+ | ||
| 98 Ag | 47 | 51 | 97,92157 | 47,5 с | 5+ |
| 98m Ag | 167,83 кэВ | 220 нс | 3+ | ||
| 99 Ag | 47 | 52 | 98,91760 | 124 с | 9/2+ |
| 99m Ag | 506,1 кэВ | 10,5 с | 1/2- | ||
| 100 Ag | 47 | 53 | 99,91610 | 2,01 мин | 5+ |
| 100m Ag | 15,52 кэВ | 2,24 мин | 2+ | ||
| 101 Ag | 47 | 54 | 100,91280 | 11,1 мин | 9/2+ |
| 101m Ag | 274,1 кэВ | 3,10 с | 1/2- | ||
| 102 Ag | 47 | 55 | 101,91169 | 12,9 мин | 5+ |
| 102m Ag | 9,3 кэВ | 7,7 мин | 2+ | ||
| 103 Ag | 47 | 56 | 102,908973 | 65,7 мин | 7/2+ |
| 103m Ag | 134,45 кэВ | 5,7 с | 1/2- | ||
| 104 Ag | 47 | 57 | 103,908629 | 69,2 мин | 5+ |
| 104m Ag | 6,9 кэВ | 33,5 мин | 2+ | ||
| 105 Ag | 47 | 58 | 104,906529 | 41,29 сут | 1/2- |
| 105m Ag | 25,465 кэВ | 7,23 мин | 7/2+ | ||
| 106 Ag | 47 | 59 | 105,906669 | 23,96 мин | 1+ |
| 106m Ag | 89,66 кэВ | 8,28 сут | 6+ | ||
| 107 Ag | 47 | 60 | 106,905097 | стабилен | 1/2- |
| 107m Ag | 93,125 кэВ | 44,3 с | 7/2+ | ||
| 108 Ag | 47 | 61 | 107,905956 | 2,37 мин | 1+ |
| 108m Ag | 109,440 кэВ | 418 лет | 6+ | ||
| 109 Ag | 47 | 62 | 108,904752 | стабилен | 1/2- |
| 109m Ag | 88,0341 кэВ | 39,6 с | 7/2+ | ||
| 110 Ag | 47 | 63 | 109,906107 | 24,6 с | 1+ |
| 110m1 Ag | 1,113 кэВ | 660 нс | 2- | ||
| 110m2 Ag | 117,59 кэВ | 249,950 сут | 6+ | ||
| 111 Ag | 47 | 64 | 110,905291 | 7,45 сут | 1/2- |
| 111m Ag | 59,82 кэВ | 64,8 с | 7/2+ | ||
| 112 Ag | 47 | 65 | 111,907005 | 3,130 ч | 2- |
| 113 Ag | 47 | 66 | 112,906567 | 5,37 ч | 1/2- |
| 113m Ag | 43,50 кэВ | 68,7 с | 7/2+ | ||
| 114 Ag | 47 | 67 | 113,908804 | 4,6 с | 1+ |
| 114m Ag | 199 кэВ | 1,50 мс | 7+ | ||
| 115 Ag | 47 | 68 | 114,90876 | 20,0 мин | 1/2- |
| 115m Ag | 41,16 кэВ | 18,0 с | 7/2+ | ||
| 116 Ag | 47 | 69 | 115,91136 | 2,68 мин | 2- |
| 116m Ag | 81,90 кэВ | 8,6 с | 5+ | ||
| 117 Ag | 47 | 70 | 116,91168 | 73,6 с | 1/2- |
| 117m Ag | 28,6 кэВ | 5,34 с | 7/2+ | ||
| 118 Ag | 47 | 71 | 117,91458 | 3,76 с | 1- |
| 118m1 Ag | 45,79 кэВ | 100 нс | 0- | ||
| 118m2 Ag | 127,49 кэВ | 2,0 с | 4+ | ||
| 118m3 Ag | 279,37 кэВ | 100 нс | 2+ | ||
| 119 Ag | 47 | 72 | 118,91567 | 6,0 с | 1/2- |
| 119m Ag | 20 кэВ | 2,1 с | 7/2+ | ||
| 120 Ag | 47 | 73 | 119,91879 | 1,23 с | 3+ |
| 120m Ag | 203,0 кэВ | 371 мс | 6- | ||
| 121 Ag | 47 | 74 | 120,91985 | 790 мс | 7/2+ |
| 122 Ag | 47 | 75 | 121,92353 | 529 мс | 3+ |
| 122m Ag | 80 кэВ | 1,5 с | 8- | ||
| 123 Ag | 47 | 76 | 122,92490 | 300 мс | 7/2+ |
| 124 Ag | 47 | 77 | 123,92864 | 172 мс | 3+ |
| 124m Ag | 0 кэВ | 200 мс | 8- | ||
| 125 Ag | 47 | 78 | 124,93043 | 166 мс | 7/2+ |
| 126 Ag | 47 | 79 | 125,93450 | 107 мс | 3+ |
| 127 Ag | 47 | 80 | 126,93677 | 79 мс | 7/2+ |
| 128 Ag | 47 | 81 | 127,94117 | 58 мс | |
| 129 Ag | 47 | 82 | 128,94369 | 44 мс | 7/2+ |
| 129m Ag | 0 кэВ | 160 мс | 1/2- | ||
| 130 Ag | 47 | 83 | 129,95045 | 50 мс | 0+ |
Примечания
- ↑ Данные приведены по G. Audi, A.H. Wapstra, and C. Thibault (2003). «The AME2003 atomic mass evaluation (II). Tables, graphs, and references.». Nuclear Physics A729: 337—676. DOI:10.1016/j.nuclphysa.2003.11.003.
- ↑ 12 Данные приведены по G. Audi, O. Bersillon, J. Blachot and A. H. Wapstra (2003). «The NUBASE evaluation of nuclear and decay properties». Nuclear Physics A729: 3–128. DOI:10.1016/j.nuclphysa.2003.11.001.
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Изотопы серебра» в других словарях:
Изотопы палладия — разновидности атомов (и ядер) химического элемента палладия, имеющие разное содержание нейтронов в ядре. Таблица изотопов палладия Символ нуклида Z(p) N(n) Масса изотопа[1] (а. е. м.) П … Википедия
Изотопы кадмия — Эта статья предлагается к удалению. Пояснение причин и соответствующее обсуждение вы можете найти на странице Википедия:К удалению/26 декабря 2012. Пока процесс обсуждения не завершён, статью можн … Википедия
Золото — У этого термина существуют и другие значения, см. Золото (значения). 79 Платина ← Золото → Ртуть … Википедия
Уран (элемент) — У этого термина существуют и другие значения, см. Уран. 92 Протактиний ← Уран → Нептуний … Википедия
Теллур — 52 Сурьма ← Теллур → Иод … Википедия
Медь — 29 Никель ← Медь → Цинк … Википедия
Плутоний — 94 Нептуний ← Плутоний → Америций Sm ↑ Pu … Википедия
Железо — 26 Марганец ← Железо → Кобальт … Википедия
СЕРЕБРО — Ag (argentum), химический элемент IB подгруппы периодической системы элементов, благородный металл, не подверженный коррозии в обычных условиях. Это красивый белый (в проходящем свете голубой) мягкий, удобный для обработки металл, с древности… … Энциклопедия Кольера
Олово — 50 Индий ← Олово → Сурьма … Википедия
Источник
Изотопы серебра — Isotopes of silver
Основные изотопы серебра ( 47
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес A r, стандартный (Ag) | 107,8682 (2) | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Встречающееся в природе серебро ( 47 Ag) состоит из двух стабильных изотопов 107 Ag и 109 Ag в почти равных пропорциях, причем 107 Ag немного больше (51,839% природного содержания ). Было охарактеризовано 28 радиоизотопов , наиболее стабильными из которых являются 105 Ag с периодом полураспада 41,29 дня, 111 Ag с периодом полураспада 7,45 дней и 112 Ag с периодом полураспада 3,13 часа. Все оставшиеся радиоактивные изотопы имеют период полураспада менее часа, а у большинства из них период полураспада менее 3 минут. Этот элемент имеет множество мета-состояний , наиболее стабильными из которых являются 108m Ag ( t * 418 лет), 110m Ag ( t * 249,79 дней) и 106m Ag ( t * 8,28 дней). Изотопы серебра имеют атомный вес от 92,950 ед. ( 93 Ag) до 129,950 ед. ( 130 Ag). Первичной модой распада перед наиболее распространенным стабильным изотопом 107 Ag является захват электронов, а после первичной моды — бета-распад . Первичные продукты распада до 107 Ag — изотопы палладия (элемент 46), а первичные продукты распада — изотопы кадмия (элемент 48). Изотоп палладия 107 Pd распадается бета-излучением до 107 Ag с периодом полураспада 6,5 миллионов лет. Железные метеориты — единственные объекты с достаточно высоким соотношением палладий / серебро, позволяющим измерить вариации содержания 107 Ag. Радиогенный 107 Ag был впервые обнаружен в метеорите Санта-Клара в 1978 году. Первооткрыватели предполагают, что слияние и дифференциация малых планет с железными сердцевинами могло произойти через 10 миллионов лет после нуклеосинтетического события. 107 Pd против 107 Ag корреляций в органах, которые явно были расплавленных с аккреции в Солнечной системе , должны отражать наличие живых короткоживущих нуклидов в ранней Солнечной системе. Источник Читайте также: Поднимется ли еще серебро Adblock |
Ag)
Изотопы серебра
Материал из Большого Справочника
Изотопы серебра — разновидности атомов (и ядер) химического
элемента серебра, имеющие разное содержание нейтронов в ядре.
Таблица изотопов серебра
| Символ нуклида |
Z(p) | N(n) | Масса изотопа[1] (а. е. м.) |
Период полураспада[2] (T1/2) |
Спин и чётность ядра[2] |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 93Ag | 47 | 46 | 92,94978 | 5 мс | 9/2+ |
| 94Ag | 47 | 47 | 93,94278 | 37 мс | 0+ |
| 94m1Ag | 1,350 МэВ | 422 мс | 7+ | ||
| 94m2Ag | 6,50 МэВ | 300 мс | 21+ | ||
| 95Ag | 47 | 48 | 94,93548 | 1,74 с | 9/2+ |
| 95m1Ag | 344,2 кэВ | 500 мс | 1/2- | ||
| 95m2Ag | 2,531 МэВ | 16 мс | 23/2+ | ||
| 95m3Ag | 4,859 МэВ | 40 мс | 37/2+ | ||
| 96Ag | 47 | 49 | 95,93068 | 4,45 с | 8+ |
| 96m1Ag | 0 кэВ | 6,9 с | 2+ | ||
| 96m2Ag | 700 нс | ||||
| 97Ag | 47 | 50 | 96,92397 | 25,3 с | 9/2+ |
| 97mAg | 2,343 МэВ | 5 нс | 21/2+ | ||
| 98Ag | 47 | 51 | 97,92157 | 47,5 с | 5+ |
| 98mAg | 167,83 кэВ | 220 нс | 3+ | ||
| 99Ag | 47 | 52 | 98,91760 | 124 с | 9/2+ |
| 99mAg | 506,1 кэВ | 10,5 с | 1/2- | ||
| 100Ag | 47 | 53 | 99,91610 | 2,01 мин | 5+ |
| 100mAg | 15,52 кэВ | 2,24 мин | 2+ | ||
| 101Ag | 47 | 54 | 100,91280 | 11,1 мин | 9/2+ |
| 101mAg | 274,1 кэВ | 3,10 с | 1/2- | ||
| 102Ag | 47 | 55 | 101,91169 | 12,9 мин | 5+ |
| 102mAg | 9,3 кэВ | 7,7 мин | 2+ | ||
| 103Ag | 47 | 56 | 102,908973 | 65,7 мин | 7/2+ |
| 103mAg | 134,45 кэВ | 5,7 с | 1/2- | ||
| 104Ag | 47 | 57 | 103,908629 | 69,2 мин | 5+ |
| 104mAg | 6,9 кэВ | 33,5 мин | 2+ | ||
| 105Ag | 47 | 58 | 104,906529 | 41,29 сут | 1/2- |
| 105mAg | 25,465 кэВ | 7,23 мин | 7/2+ | ||
| 106Ag | 47 | 59 | 105,906669 | 23,96 мин | 1+ |
| 106mAg | 89,66 кэВ | 8,28 сут | 6+ | ||
| 107Ag | 47 | 60 | 106,905097 | стабилен | 1/2- |
| 107mAg | 93,125 кэВ | 44,3 с | 7/2+ | ||
| 108Ag | 47 | 61 | 107,905956 | 2,37 мин | 1+ |
| 108mAg | 109,440 кэВ | 418 лет | 6+ | ||
| 109Ag | 47 | 62 | 108,904752 | стабилен | 1/2- |
| 109mAg | 88,0341 кэВ | 39,6 с | 7/2+ | ||
| 110Ag | 47 | 63 | 109,906107 | 24,6 с | 1+ |
| 110m1Ag | 1,113 кэВ | 660 нс | 2- | ||
| 110m2Ag | 117,59 кэВ | 249,950 сут | 6+ | ||
| 111Ag | 47 | 64 | 110,905291 | 7,45 сут | 1/2- |
| 111mAg | 59,82 кэВ | 64,8 с | 7/2+ | ||
| 112Ag | 47 | 65 | 111,907005 | 3,130 ч | 2- |
| 113Ag | 47 | 66 | 112,906567 | 5,37 ч | 1/2- |
| 113mAg | 43,50 кэВ | 68,7 с | 7/2+ | ||
| 114Ag | 47 | 67 | 113,908804 | 4,6 с | 1+ |
| 114mAg | 199 кэВ | 1,50 мс | 7+ | ||
| 115Ag | 47 | 68 | 114,90876 | 20,0 мин | 1/2- |
| 115mAg | 41,16 кэВ | 18,0 с | 7/2+ | ||
| 116Ag | 47 | 69 | 115,91136 | 2,68 мин | 2- |
| 116mAg | 81,90 кэВ | 8,6 с | 5+ | ||
| 117Ag | 47 | 70 | 116,91168 | 73,6 с | 1/2- |
| 117mAg | 28,6 кэВ | 5,34 с | 7/2+ | ||
| 118Ag | 47 | 71 | 117,91458 | 3,76 с | 1- |
| 118m1Ag | 45,79 кэВ | 100 нс | 0- | ||
| 118m2Ag | 127,49 кэВ | 2,0 с | 4+ | ||
| 118m3Ag | 279,37 кэВ | 100 нс | 2+ | ||
| 119Ag | 47 | 72 | 118,91567 | 6,0 с | 1/2- |
| 119mAg | 20 кэВ | 2,1 с | 7/2+ | ||
| 120Ag | 47 | 73 | 119,91879 | 1,23 с | 3+ |
| 120mAg | 203,0 кэВ | 371 мс | 6- | ||
| 121Ag | 47 | 74 | 120,91985 | 790 мс | 7/2+ |
| 122Ag | 47 | 75 | 121,92353 | 529 мс | 3+ |
| 122mAg | 80 кэВ | 1,5 с | 8- | ||
| 123Ag | 47 | 76 | 122,92490 | 300 мс | 7/2+ |
| 124Ag | 47 | 77 | 123,92864 | 172 мс | 3+ |
| 124mAg | 0 кэВ | 200 мс | 8- | ||
| 125Ag | 47 | 78 | 124,93043 | 166 мс | 7/2+ |
| 126Ag | 47 | 79 | 125,93450 | 107 мс | 3+ |
| 127Ag | 47 | 80 | 126,93677 | 79 мс | 7/2+ |
| 128Ag | 47 | 81 | 127,94117 | 58 мс | |
| 129Ag | 47 | 82 | 128,94369 | 44 мс | 7/2+ |
| 129mAg | 0 кэВ | 160 мс | 1/2- | ||
| 130Ag | 47 | 83 | 129,95045 | 50 мс | 0+ |
Примечания
- ↑ Данные приведены по Audi G., Wapstra A. H., Thibault C. The AME2003 atomic mass evaluation (II). Tables, graphs, and references (англ.) // Nuclear Physics A. — 2003. — Vol. 729. — P. 337—676. — DOI:10.1016/j.nuclphysa.2003.11.003. — Bibcode: 2003NuPhA.729..337A.
- ↑ 1 2 Данные приведены по Audi G., Bersillon O., Blachot J., Wapstra A. H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. — 2003. — Т. 729. — С. 3—128. — DOI:10.1016/j.nuclphysa.2003.11.001. — Bibcode: 2003NuPhA.729….3A.
|
||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес A r, стандартный (Ag) | 107,8682 (2) | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Встречающееся в природе серебро ( 47 Ag) состоит из двух стабильных изотопов 107 Ag и 109 Ag в почти равных пропорциях, причем 107 Ag немного больше (51,839% природного содержания ). Было охарактеризовано 28 радиоизотопов , наиболее стабильными из которых являются 105 Ag с периодом полураспада 41,29 дня, 111 Ag с периодом полураспада 7,45 дней и 112 Ag с периодом полураспада 3,13 часа.
Все оставшиеся радиоактивные изотопы имеют период полураспада менее часа, а у большинства из них период полураспада менее 3 минут. Этот элемент имеет множество мета-состояний , наиболее стабильными из которых являются 108m Ag ( t * 418 лет), 110m Ag ( t * 249,79 дней) и 106m Ag ( t * 8,28 дней).
Изотопы серебра имеют атомный вес от 92,950 ед. ( 93 Ag) до 129,950 ед. ( 130 Ag). Первичной модой распада перед наиболее распространенным стабильным изотопом 107 Ag является захват электронов, а после первичной моды – бета-распад . Первичные продукты распада до 107 Ag – изотопы палладия (элемент 46), а первичные продукты распада – изотопы кадмия (элемент 48).
Изотоп палладия 107 Pd распадается бета-излучением до 107 Ag с периодом полураспада 6,5 миллионов лет. Железные метеориты – единственные объекты с достаточно высоким соотношением палладий / серебро, позволяющим измерить вариации содержания 107 Ag. Радиогенный 107 Ag был впервые обнаружен в метеорите Санта-Клара в 1978 году.
Первооткрыватели предполагают, что слияние и дифференциация малых планет с железными сердцевинами могло произойти через 10 миллионов лет после нуклеосинтетического события. 107 Pd против 107 Ag корреляций в органах, которые явно были расплавленных с аккреции в Солнечной системе , должны отражать наличие живых короткоживущих нуклидов в ранней Солнечной системе.
Список изотопов
| Нуклид | Z | N | Изотопная масса ( Да ) | Период полураспада |
Режим распада |
Дочерний изотоп |
Спин и паритет |
Естественное изобилие (мольная доля) | |
|---|---|---|---|---|---|---|---|---|---|
| Энергия возбуждения | Нормальная пропорция | Диапазон вариации | |||||||
| 93 Ag | 47 | 46 | 92.94978 (64) # | 5 # мс [> 1,5 мкс] |
β + | 93 Pd | 9/2 + # | ||
| п | 92 Pd | ||||||||
| 94 Ag | 47 | 47 | 93.94278 (54) # | 37 (18) мс [26 (+ 26−9) мс] |
β + | 94 Pd | 0 + # | ||
| 94 мл Ag | 1350 (400) # кэВ | 422 (16) мс | β + (> 99,9%) | 94 Pd | (7+) | ||||
| β + , p (<0,1%) | 93 Rh | ||||||||
| 94м2 Ag | 6500 (2000) # кэВ | 300 (200) мс | (21+) | ||||||
| 95 Ag | 47 | 48 | 94.93548 (43) # | 1,74 (13) с | β + (> 99,9%) | 95 Pd | (9/2 +) | ||
| β + , p (<0,1%) | 94 Rh | ||||||||
| 95 мл Ag | 344,2 (3) кэВ | <0,5 с | (1 / 2-) | ||||||
| 95м2 Ag | 2531 (1) кэВ | <16 мс | (23/2 +) | ||||||
| 95 м3 Ag | 4859 (1) кэВ | <40 мс | (37/2 +) | ||||||
| 96 Ag | 47 | 49 | 95.93068 (43) # | 4,45 (4) с | β + (96,3%) | 96 Pd | (8+) | ||
| β + , p (3,7%) | 95 Rh | ||||||||
| 96 мл Ag | 0 (50) # кэВ | 6,9 (6) с | (2+) | ||||||
| 96м2 Ag | 700 (200) нс | ||||||||
| 97 Ag | 47 | 50 | 96.92397 (35) | 25,3 (3) с | β + | 97 Pd | (9/2 +) | ||
| 97 м Ag | 2343 (49) кэВ | 5 нс | (21/2 +) | ||||||
| 98 Ag | 47 | 51 | 97.92157 (7) | 47,5 (3) с | β + (99,99%) | 98 пд | (5+) | ||
| β + , p (0,0012%) | 97 Rh | ||||||||
| 98 м Ag | 167,83 (15) кэВ | 220 (20) нс | (3+) | ||||||
| 99 Ag | 47 | 52 | 98,91760 (16) | 124 (3) с | β + | 99 Pd | (9/2) + | ||
| 99m Ag | 506,1 (4) кэВ | 10,5 (5) с | ЭТО | 99 Ag | (1 / 2-) | ||||
| 100 Ag | 47 | 53 | 99,91610 (8) | 2,01 (9) мин | β + | 100 Pd | (5) + | ||
| 100 м Ag | 15.52 (16) кэВ | 2,24 (13) мин | ЭТО | 100 Ag | (2) + | ||||
| β + | 100 Pd | ||||||||
| 101 Ag | 47 | 54 | 100.91280 (11) | 11,1 (3) мин | β + | 101 Pd | 9/2 + | ||
| 101 м Ag | 274,1 (3) кэВ | 3.10 (10) с | ЭТО | 101 Ag | 1 / 2- | ||||
| 102 Ag | 47 | 55 | 101.91169 (3) | 12,9 (3) мин | β + | 102 Pd | 5+ | ||
| 102 м Ag | 9,3 (4) кэВ | 7,7 (5) мин | β + (51%) | 102 Pd | 2+ | ||||
| IT (49%) | 102 Ag | ||||||||
| 103 Ag | 47 | 56 | 102,908973 (18) | 65,7 (7) мин | β + | 103 Pd | 7/2 + | ||
| 103 м Ag | 134,45 (4) кэВ | 5,7 (3) с | ЭТО | 103 Ag | 1 / 2- | ||||
| 104 Ag | 47 | 57 год | 103.908629 (6) | 69,2 (10) мин | β + | 104 Pd | 5+ | ||
| 104 м Ag | 6.9 (4) кэВ | 33,5 (20) мин | β + (99,93%) | 104 Pd | 2+ | ||||
| ИТ (0,07%) | 104 Ag | ||||||||
| 105 Ag | 47 | 58 | 104,906529 (12) | 41.29 (7) d | β + | 105 Pd | 1 / 2- | ||
| 105 м Ag | 25,465 (12) кэВ | 7,23 (16) мин | ИТ (99,66%) | 105 Ag | 7/2 + | ||||
| β + (0,34%) | 105 Pd | ||||||||
| 106 Ag | 47 | 59 | 105,906669 (5) | 23,96 (4) мин | β + (99,5%) | 106 Pd | 1+ | ||
| β – (0,5%) | 106 кд | ||||||||
| 106 м Ag | 89.66 (7) кэВ | 8,28 (2) д | β + | 106 Pd | 6+ | ||||
| IT (4,16 × 10 −6 %) | 106 Ag | ||||||||
| 107 Ag | 47 | 60 | 106.905097 (5) | Стабильный | 1 / 2- | 0,51839 (8) | |||
| 107 м Ag | 93,125 (19) кэВ | 44,3 (2) с | ЭТО | 107 Ag | 7/2 + | ||||
| 108 Ag | 47 | 61 | 107.905956 (5) | 2,37 (1) мин | β – (97,15%) | 108 кд | 1+ | ||
| β + (2,85%) | 108 Pd | ||||||||
| 108 м Ag | 109,440 (7) кэВ | 418 (21) год | β + (91,3%) | 108 Pd | 6+ | ||||
| ИТ (8,96%) | 108 Ag | ||||||||
| 109 Ag | 47 | 62 | 108.904752 (3) | Стабильный | 1 / 2- | 0,48161 (8) | |||
| 109 м Ag | 88.0341 (11) кэВ | 39,6 (2) с | ЭТО | 109 Ag | 7/2 + | ||||
| 110 Ag | 47 | 63 | 109.906107 (3) | 24,6 (2) с | β – (99,7%) | 110 Кд | 1+ | ||
| ЭК (0,3%) | 110 пд | ||||||||
| 110 мл Ag | 1,113 кэВ | 660 (40) нс | 2− | ||||||
| 110м2 Ag | 117,59 (5) кэВ | 249.950 (24) сут | β – (98,64%) | 110 Кд | 6+ | ||||
| ИТ (1,36%) | 110 Ag | ||||||||
| 111 Ag | 47 | 64 | 110.905291 (3) | 7,45 (1) сут | β – | 111 кд | 1 / 2- | ||
| 111 м Ag | 59,82 (4) кэВ | 64,8 (8) с | IT (99,3%) | 111 Ag | 7/2 + | ||||
| β – (0,7%) | 111 кд | ||||||||
| 112 Ag | 47 | 65 | 111.907005 (18) | 3.130 (9) ч | β – | 112 кд | 2 (-) | ||
| 113 Ag | 47 | 66 | 112.906567 (18) | 5,37 (5) ч | β – | 113м кд | 1 / 2- | ||
| 113 м Ag | 43,50 (10) кэВ | 68,7 (16) с | IT (64%) | 113 Ag | 7/2 + | ||||
| β – (36%) | 113 кд | ||||||||
| 114 Ag | 47 | 67 | 113.908804 (27) | 4.6 (1) с | β – | 114 кд | 1+ | ||
| 114 м Ag | 199 (5) кэВ | 1,50 (5) мс | ЭТО | 114 Ag | (<7+) | ||||
| 115 Ag | 47 | 68 | 114,90876 (4) | 20,0 (5) мин | β – | 115м кд | 1 / 2- | ||
| 115 м Ag | 41,16 (10) кэВ | 18.0 (7) с | β – (79%) | 115 кд | 7/2 + | ||||
| IT (21%) | 115 Ag | ||||||||
| 116 Ag | 47 | 69 | 115.91136 (5) | 2,68 (10) мин | β – | 116 кд | (2) – | ||
| 116 м Ag | 81,90 (20) кэВ | 8,6 (3) с | β – (94%) | 116 кд | (5+) | ||||
| IT (6%) | 116 Ag | ||||||||
| 117 Ag | 47 | 70 | 116.91168 (5) | 73,6 (14) с [72,8 (+ 20−7) с] |
β – | 117м кд | 1/2 – # | ||
| 117m Ag | 28,6 (2) кэВ | 5,34 (5) с | β – (94%) | 117м кд | (7/2 +) | ||||
| IT (6%) | 117 Ag | ||||||||
| 118 Ag | 47 | 71 | 117.91458 (7) | 3,76 (15) с | β – | 118 кд | 1- | ||
| 118 мл Ag | 45,79 (9) кэВ | ~ 0,1 мкс | От 0 (-) до 2 (-) | ||||||
| 118м2 Ag | 127,49 (5) кэВ | 2,0 (2) с | β – (59%) | 118 кд | 4 (+) | ||||
| IT (41%) | 118 Ag | ||||||||
| 118 м3 Ag | 279,37 (20) кэВ | ~ 0,1 мкс | (2+, 3+) | ||||||
| 119 Ag | 47 | 72 | 118.91567 (10) | 6.0 (5) с | β – | 119м кд | 1/2 – # | ||
| 119m Ag | 20 (20) # кэВ | 2,1 (1) с | β – | 119 кд | 7/2 + # | ||||
| 120 Ag | 47 | 73 | 119.91879 (8) | 1,23 (4) с | β – (99,99%) | 120 кд | 3 (+ #) | ||
| β – , n (0,003%) | 119 кд | ||||||||
| 120 м Ag | 203.0 (10) кэВ | 371 (24) мс | β – (63%) | 120 кд | 6 (-) | ||||
| IT (37%) | 120 Ag | ||||||||
| 121 Ag | 47 | 74 | 120.91985 (16) | 0,79 (2) с | β – (99,92%) | 121 кд | (7/2 +) # | ||
| β – , n (0,076%) | 120 кд | ||||||||
| 122 Ag | 47 | 75 | 121.92353 (22) # | 0,529 (13) с | β – (> 99,9%) | 122 кд | (3+) | ||
| β – , n (<0,1%) | 121 кд | ||||||||
| 122 м Ag | 80 (50) # кэВ | 1,5 (5) с | β – (> 99,9%) | 122 кд | 8- # | ||||
| β – , n (<0,1%) | 121 кд | ||||||||
| 123 Ag | 47 | 76 | 122.92490 (22) # | 0,300 (5) с | β – (99,45%) | 123 кд | (7/2 +) | ||
| β – , n (0,549%) | 122 кд | ||||||||
| 124 Ag | 47 | 77 | 123.92864 (21) # | 172 (5) мс | β – (99,9%) | 124 кд | 3 + # | ||
| β – , n (0,1%) | 123 кд | ||||||||
| 124 м Ag | 0 (100) # кэВ | 200 # мс | β – | 124 кд | 8- # | ||||
| ЭТО | 124 Ag | ||||||||
| 125 Ag | 47 | 78 | 124.93043 (32) # | 166 (7) мс | β – (> 99,9%) | 125 кд | (7/2 +) # | ||
| β – , n (<0,1%) | 124 кд | ||||||||
| 126 Ag | 47 | 79 | 125.93450 (32) # | 107 (12) мс | β – (> 99,9%) | 126 кд | 3 + # | ||
| β – , n (<0,1%) | 125 кд | ||||||||
| 127 Ag | 47 | 80 | 126.93677 (32) # | 79 (3) мс | β – (> 99,9%) | 127 Кд | 7/2 + # | ||
| β – , n (<0,1%) | 126 кд | ||||||||
| 128 Ag | 47 | 81 год | 127.94117 (32) # | 58 (5) мс | β – | 128 кд | |||
| 129 Ag | 47 | 82 | 128.94369 (43) # | 44 (7) мс [46 (+ 5−9) мс] |
β – (> 99,9%) | 129 кд | 7/2 + # | ||
| β – , n (<0,1%) | 128 кд | ||||||||
| 129 м Ag | 0 (200) # кэВ | ~ 160 мс | 1/2 – # | ||||||
| 130 Ag | 47 | 83 | 129.95045 (36) # | ~ 50 мс | β – | 130 кд | 0+ | ||
| 131 Ag | 47 | 84 | 35 мс | β – | 131 кд | ||||
| 132 Ag | 47 | 85 | 28 мс | β – | 132 кд | ||||
Этот заголовок и нижний колонтитул таблицы:
|
- ^ m Ag – Возбужденный ядерный изомер .
- ^ () – Неопределенность (1 σ ) дана в сжатой форме в скобках после соответствующих последних цифр.
- ^ # – Атомная масса с пометкой #: значение и погрешность получены не из чисто экспериментальных данных, а, по крайней мере, частично из трендов по массовой поверхности (TMS).
- ^ a b c # – Значения, отмеченные знаком #, получены не только из экспериментальных данных, но, по крайней мере, частично из трендов соседних нуклидов (TNN).
-
^
Режимы распада:
- ^ Дочерний символ выделен жирным курсивом – Дочерний продукт почти стабилен.
- ^ Дочерний символ жирным шрифтом – Дочерний продукт стабилен.
- ^ () значение спина – указывает вращение со слабыми аргументами присваивания.
- ^ Используется для датирования определенных событий в ранней истории Солнечной системы.
- ^ a b Теоретически способна к спонтанному делению
- ^ a b Продукт деления
использованная литература
-
^
Meija, Juris; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)» . Чистая и прикладная химия . 88 (3): 265–91. DOI : 10,1515 / пак-2015-0305 .
- Изотопные массы из:
- Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Wapstra, Aaldert Hendrik (2003), ” Оценка ядерных свойств и свойств распада N UBASE ” , Nuclear Physics A , 729 : 3–128, Bibcode : 2003NuPhA.729 …. 3A , doi : 10.1016 / j.nuclphysa.2003.11 0,001
- Изотопные составы и стандартные атомные массы из:
- де Лаэтер, Джон Роберт ; Бёльке, Джон Карл; Де Бьевр, Поль; Хидака, Хироши; Пайзер, Х. Штеффен; Росман, Кевин-младший; Тейлор, Филип DP (2003). «Атомный вес элементов. Обзор 2000 (Технический отчет IUPAC)» . Чистая и прикладная химия . 75 (6): 683–800. DOI : 10.1351 / pac200375060683 .
- Визер, Майкл Э. (2006). «Атомный вес элементов 2005 (Технический отчет IUPAC)» . Чистая и прикладная химия . 78 (11): 2051–2066. DOI : 10,1351 / pac200678112051 . Выложите резюме .
- Данные о периоде полураспада, спине и изомерах выбраны из следующих источников.
- Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Wapstra, Aaldert Hendrik (2003), ” Оценка ядерных свойств и свойств распада N UBASE ” , Nuclear Physics A , 729 : 3–128, Bibcode : 2003NuPhA.729 …. 3A , doi : 10.1016 / j.nuclphysa.2003.11 0,001
- Национальный центр ядерных данных . «База данных NuDat 2.x» . Брукхейвенская национальная лаборатория .
- Холден, Норман Э. (2004). «11. Таблица изотопов». В Лиде, Дэвид Р. (ред.). CRC Справочник по химии и физике (85-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-0-8493-0485-9.