Йодное число
выражается количеством граммов йода,
необходимого для насыщения ненасыщенных
жирных кислот, содержащихся в 100 г жира.
Йодное
число является одним из наиболее важных
показателей для масел (жиров). Одно
позволяет судить о степени насыщенности
масла (жира), о склонности его к высыханию,
прогорканию и другим изменениям,
происходящим при хранении и переработке
пищевых и технических масел. Чем больше
содержится в жире ненасыщенных жирных
кислот, тем выше йодное число. Уменьшение
йодного числа в процессе хранения масла
является показателем его порчи.
Растительные
жиры (масла), имеющие в основном жидкую
консистенцию, содержат, главным образом,
непредельные кислоты.
Жиры
животного происхождения – в большинстве
своем твердые, так как в их состав входят
преимущественно триглицериды предельных
жирных кислот.
Принцип
метода
основан на свойстве ненасыщенных жирных
кислот присоединять галогены по месту
двойных связей.
Взаимодействие
ненасыщенных жирных кислот с йодом
протекает по уравнению
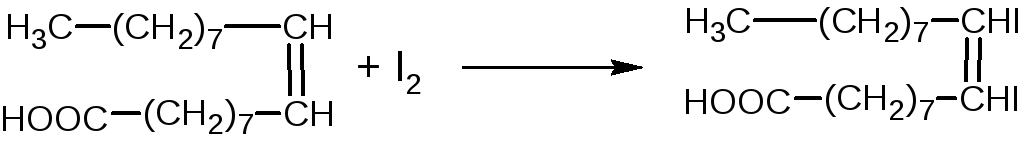
I2
+ 2Na2S2O3
=
2NaI + Na2S4O6
Непрореагировавший
йод оттитровывают 0,1 н. раствором
тиосульфата натрия.
Техника
определения:
сухую
коническую колбу со шлифом емкостью
250 см3
взвешивают
на аналитических весах, помещают туда
около 0,5 г масла и снова взвешивают
колбу. По разности масс определяют
величину навески масла. В колбу добавляют
25 см3
этилового спирта для растворения
навески. Если масло плохо растворяется,
колбу нагревают на водяной бане. Во
вторую колбу приливают 25 см3
спирта без жира «слепой опыт». В обе
колбы (опыт и контроль) прибавляют по
12,5 см3
0,2 н. спиртового раствора йода, добавляют
по 100 см3
дистиллированной воды и закрывают
пробкой. Через 5 минут содержимое колб
оттитровывают 0,1 н. раствором тиосульфата
сначала до появления слабо-желтого
окрашивания, а потом, прибавив 1 см3
раствора
крахмала, титруют до исчезновения синего
окрашивания.
Обработка
результатов:
При
расчетах учитывают, что 1 см3
0,1 н. тиосульфата натрия соответствует
1 см3
0,1 н. раствора йода. Йодное число (ИЧ)
вычисляют по формуле
![]() ,
,
где
Vк
– количество
0,1 н. раствора тиосульфата, пошедшее на
титрование контрольного опыта, см3;
Vо
– количество 0,1 н. раствора тиосульфата,
пошедшее на титрование опытного образца,
см3;
k
– поправочный коэффициент к титру
приблизительно 0,1 н. раствора тиосульфата;
0,0127 – титр
раствора тиосульфата по йоду;
m
– навеска масла, г.
2.3 Определение перекисного числа
Указанное
число показывает суммарное количество
перекисей, образовавшихся при окислении
как ненасыщенных, так и насыщенных
жирных кислот. Образование гидроперекисей
в случае насыщенных жирных кислот
происходит с меньшей скоростью в
сравнении с ненасыщенными. Однако и в
этом случае образуется свободный
перекисный радикал:

При
взаимодействии с другими жирными
кислотами свободный перекисный радикал
стабилизируется, «отрывая» от них атом
водорода:

Образовавшийся
новый радикал взаимодействует с
кислородом по прежней схеме:

Свободный перекисный
радикал может превратиться в альдегиды
путем его изомеризации с образованием
нестойкой диалкилперекиси:

Образующиеся
гидроперекиси могут также активно
превращаться в кетоны:

Доказано
также, что гидроперекиси могут
взаимодействовать с двойными связями
ненасыщенных жирных кислот с образованием
эпоксидов:

Именно
набор всех вышеуказанных соединений
с различной молекулярной массой и
обуславливает наличие в хранящемся
молочном жире таких пороков вкуса как
«салистый», «олеистый», «рыбный»,
«грибной» и т.д.
Сильнейшими
активаторами окисления являются ионы
металла.
Принцип
метода:
количественное определение перекисей
в масле основано на реакции выделения
йода перекисями из йодата калия в кислой
среде (пример циклической перекиси):

Выделившийся йод
оттитровывают раствором тиосульфата.
Техника
определения:
в конической колбе или склянке с притертой
пробкой емкостью 200 см3
отвешивают на аналитических весах около
2-3 г масла. Навеску растворяют в 20 см3
смеси ледяной уксусной кислоты и
хлороформа (2:1), прибавляют 5 см3
насыщенного раствора йодистого калия,
сосуд закрывают пробкой и ставят в
темное место на 10 минут, после чего
добавляют 50 см3
дистиллированной воды и оттитровывают
выделившийся йод 0,002 н. раствором
тиосульфата (индикатор-крахмал).
Одновременно проводят также контрольное
определение (без масла).
Обработка
результатов:
Перекисное
число (ПЧ) (количество граммов йода,
выделенного перекисями, содержащимися
в масле) рассчитывают по формуле
![]() ,
,
где
Vк
– количество 0,002 н. раствора тиосульфата,
израсходованное при титровании
контрольного образца, см3;
V0
– количество 0,002 н. раствора тиосульфата,
израсходованное при титровании опытного
образца, см3;
k
– поправочный коэффициент раствора
тиосульфата;
0,0002538
– титр 0,002 н. раствора тиосульфата по
йоду (1 см3
раствора
соответствует 0,0002538 г йода);
m
– навеска масла, г.
Таблица
1 – Показатели качества жира
|
Наименование жира |
Кислотное |
Йодное |
Перекисное число |
Стандартные |
||
|
Кислотное |
Йодное |
Перекисное число |
||||
ОБЩИЕ ВЫВОДЫ:
СПИСОК ИСПОЛЬЗУЕМОЙ
ЛИТЕРАТУРЫ
1
Химия и биохимия липидов: Методические
указания к выполнению лабораторных
работ для студентов специальностей
1-49 01 01, 1-49 01 92, 1-91 01 01 /Могилевский
государственный университет продовольствия;
сост. А.Я. Гузиков,
О.Н.Макасеева,Л.М.Ткаченко.–Могилев,2007.–41с.).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Йодное число, или так называемый коэффициент непредельности, характеризует степень ненасыщенности жира и выражается количеством йода в граммах, которое требуется для полного насыщения жирных кислот, содержащихся в 100 г жира (г I2/100 г жира). Это наиболее важная из констант жира. По величине этого показателя судят о преобладании в жирах насыщенных или ненасыщенных жирных кислот. Чем выше в жире содержание ненасыщенных жирных кислот, тем выше йодное число. Тугоплавкие жиры имеют низкое йодное число, легкоплавкие – высокое.
Йодное число дает возможность судить о склонности жира к различным изменениям (окислению, присоединению водорода и т. д.), происходящим при хранении и переработке пищевых жиров. Оно позволяет судить о чистоте и натуральности исследуемого жира. Кроме того, йодное число характеризует степень свежести жиров. При окислении жиров в процессе хранения йодное число снижается.
|
Йодное число |
г I2/100 г жира: |
|
подсолнечное масло |
– 119,0–145,0; |
|
кукурузное масло |
– 111,0–133,0; |
|
соевое масло |
– 120,0–140,0; |
|
китовый жир (покровное сало) |
– 107,4–161,5; |
|
рапсовое масло |
– 95,0–106,0; |
|
оливковое масло |
– 86,0–88,0; |
|
свиной жир |
– 46,0–66,0; |
|
молочный жир |
– 26,0–46,0; |
|
говяжий жир |
– 32,0–47,0; |
|
бараний жир |
– 31,0–46,0. |
Йодное число является показателем консистенции сливочного масла и должно учитываться при выборе температурных режимов обработки сливок в процессе их созревания и перемешивания. Этот показатель молочного жира зависит от кормовых рационов, стадии лактации, времени года, породы животного и т. д. Оно повышается летом и понижается зимой и лежит в пределах 28–45 г/100 г. Йодное число сливочного масла определяют при подозрении на наличие в нем примесей растительных масел.
Метод определения йодного числа основан на способности галогенов (йода, хлористого йода, бромистого йода) присоединяться по кратным связям. Непрореагировавший галоген оттитровывают тиосульфатом натрия в присутствии крахмала в качестве индикатора.
Кратные связи в полиненасыщенных жирных кислотах, входящих в состав жиров, насыщаются последовательно, причем время реакции присоединения возрастает по сравнению с мононенасыщенными. Насыщению галогенами в первую очередь подвержены кратные связи, наиболее удаленные от карбоксильной группы. Используя галогены, невозможно достичь полного насыщения сопряженных кратных связей. Величина йодного числа зависит:
§от числа этиленовых связей в ненасыщенных жирных кислотах (с увеличением количества этиленовых связей в углеродной цепи жирных кислот при одном и том же числе углеродных атомов йодное число увеличивается);
§от длины углеродной цепи в жирных кислотах (или от молекулярного веса);
§от положения этиленовых связей в углеродной цепи (с приближением этиленовой связи к карбоксильной группе жирных кислот их йодное число уменьшается);
§от наличия сопряженных связей (сопряженные этиленовые связи при использовании обычных методов определения йодного числа насыщаются не полностью).
Рекомендуемыми ГОСТ Р ИСО 3961–2010 «Жиры и масла животные и растительные. Определение йодного числа» являются следующие методы определения йодного числа: Гюбля (с хлорйодом), Кауфмана (с NaBr×Br2), Гануса (с бромйодом). Методы Гюбеля и Гануса дают одинаковые и близкие к теоретическим результаты. Названные методы рекомендуются для исследовательских целей, идентификации жиров и контроля производства. Метод Гануса неприемлем для анализа жиров с сопряженными кратными связями. Результаты определения йодных чисел по методу Кауфмана обычно на 1–3% выше, чем по методу Гюбля.
Метод Гюбля основан на присоединении по кратным связям хлористого йода (раствор Гюбля), который образуется при взаимодействии сулемы с йодом в спиртовых растворах:
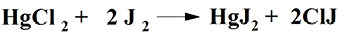
Хлористый йод практически полностью насыщает кратные связи жирнокислотных радикалов в жирах:

Избыток непрореагировавшего хлористого йода оттитровывают тиосульфатом натрия. Предварительно в реакционную среду необходимо внести йодид калия и воду для выделения эквивалентного количества йода из хлористого йода по следующей реакции:
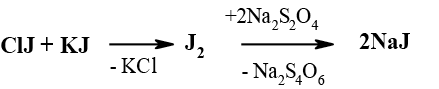
Ход анализа. В предварительно высушенную колбу для титрования вместимостью 500 мл с пришлифованной пробкой внести пробу анализируемого жира в зависимости от величины йодного числа. Пробу жира растворить в 15 мл хлороформа и добавить 25 мл (пипеткой) раствора Гюбля. Закрыть колбу пробкой, смоченной в растворе йодида калия, и оставить при температуре около 20 оС в темном месте на 18–24 часа. Время настаивания анализируемого раствора и величину навески анализируемого жира выбрать в зависимости от предполагаемой величины йодного числа (табл. 1.3.7).
Таблица 1.3.7. Рекомендуемая масса пробы и время настаивания
в зависимости от величины йодного числа
|
Значение йодного числа, г I2/100 г |
Масса пробы, г |
Время настаивания, ч |
|
от 5 до 20 включительно |
1,0 |
6 |
|
свыше 20 до 50 включительно |
0,6 |
8 |
|
свыше 50 до 100 включительно |
0,3 |
12 |
|
свыше 100 до 150 включительно |
0,2 |
18 |
|
свыше 150 до 200 включительно |
0,15 |
24 |
|
свыше 200 |
0,10 |
24 |
По истечении вышеуказанного времени до титрования в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды, смесь перемешать. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желто-соломенной окраски. В конце добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов в аналогичных условиях, но без добавления жира: 15 мл хлороформа, 25 мл раствора Гюбля. Колбу закрыть пробкой, смоченной в растворе йодида калия, и оставить в темном месте на 18–24 часа. Перед титрованием в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды и оттитровать.
Йодное число (ЙЧ, г I2/100 г или %) вычислить по формуле:
ЙЧ=VK-V0×0,01269m×100,
где VK – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование контрольного образца, мл;
VO – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование опытного образца, мл;
0, 01269 – титр 0,1 н раствора тиосульфата натрия, мг/мл;
m – масса исследуемого жира, г;
100 – коэффициент пересчета на 100 г анализируемого жира.
Метод Гануса основан на использовании бромистого йода, растворенного в безводной уксусной кислоте (реактив Гануса), который количественно присоединяется по кратным связям. Бромистый йод получают посредством смешения брома с йодом в безводной уксусной среде:
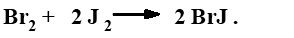
Бромистый йод присоединяется по кратным связям ненасыщенных жирных кислот.
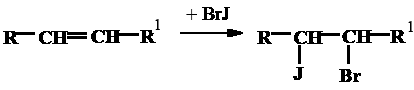
Избыток бромистого йода после введения йодида калия и воды оттитровывают тиосульфатом натрия.
Ход анализа. В колбу для титрования на 500 мл с пришлифованной пробкой внести пробу анализируемого жира в количестве 0,1–0,2 г и растворить в 15 мл хлороформа. Пипеткой внести 25 мл раствора Гануса, закрыть пробкой, смоченной в растворе йодида калия и оставить в темном месте на один час. Перед титрованием в колбу для титрования внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды.
Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный. Контрольный опыт проделать в аналогичных условиях с тем же количеством реагентов, но без добавления жира.
Метод Кауфмана основан на применении в качестве реагента непрочного соединения NaBr×Br2, которое образуется при растворении в метиловом спирте соответствующих количеств брома и бромистого натрия:
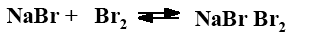
Бром из соединения NaBr×Br2 отщепляется и присоединяется к этиленовым связям жирных кислот, причем активность его недостаточна для замещения водорода:
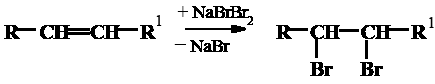
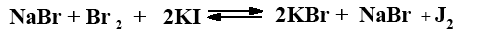
При прибавлении к раствору Кауфмана йодистого калия выделяется эквивалентное количество йода, который оттитровывают тиосульфатом натрия.
Ход анализа. Анализ аналогичен методу Гюбля. В колбу для титрования на 500 мл с пришлифованной пробкой внести пробу анализируемого жира в таких же количествах, как и в методе Гюбля и добавить 10 мл хлороформа. Пипеткой прилить 20 мл раствора Кауфмана, закрыть пробкой, смоченной в растворе йодида калия, оставить колбу с реакционной смесью в темном месте на 1–1,5 часа. Время зависит от предполагаемой величины йодного числа (на 1 час для масел с йодным числом до 100; на 1,5 часа – больше 100).
По истечении указанного времени в колбу прилить 10–15 мл 10%-го раствора йодистого калия и 50–60 мл дистиллированной воды. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов, но без добавления жира.
Метод Маргошеса является ускоренным методом определения йодного числа. Хотя он и уступает по точности вышеописанным методам, но может использоваться для анализа жиров, содержащих жирные кислоты с сопряженными кратными связями. В качестве реагента используется раствор Маргошеса, содержащий йодноватистую кислоту.
В спиртовых растворах образование из йода йодноватистой кислоты происходит в ничтожных количествах, но ускоряется в присутствии ненасыщенных связей и особенно в избытке воды. Образующаяся йодноватистая кислота взаимодействует по этиленовым связям быстрее галоидов:
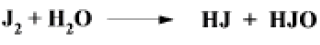

Избыток непрореагировавшего йода оттитровывают тиосульфатом натрия.
Ход анализа. В сухую колбу для титрования вместимостью 500 мл с пришлифованной пробкой взвесить на аналитических весах 0,1–0,15 г растительного масла или 0,2–0,25 г животного жира. Для растворения навески жира добавить 10 мл смеси этилового спирта и хлороформа (10:1). Если проба жира плохо растворяется, следует закрыть колбу воздушным холодильником и нагреть на водяной бане с температурой 50–60 оС в течение 15–20 минут. По истечении указанного срока колбу охладить до комнатной температуры и добавить пипеткой к анализируемой пробе 25 мл раствора Маргошеса (0,2 н спиртовой раствор йода). Оставить полученный раствор в темном месте. Спустя ровно 5 минут влить 200 мл дистиллированной воды, закрыть колбу пробкой и хорошо перемешать. Полученную смесь через 5 минут оттитровать 0,1 н раствором тиосульфата натрия до перехода коричневой окраски в желтую. Затем добавить индикатор – 1%-ный раствор крахмала – и продолжить титрование до исчезновения фиолетовой окраски (опыт).
Контрольный опыт проделать с теми же реактивами. К 10 мл смеси этилового спирта и хлороформа (10:1) добавить 25 мл 0,2 н раствора Маргошеса и оставить полученный раствор в темном месте. Спустя ровно 5 минут влить 200 мл дистиллированной воды и тщательно перемешать. Полученную эмульсию оттитровать 0,1 н раствором тиосульфата натрия в присутствии крахмала.
|
Необходимые реактивы, посуда, оборудование: §реактивы Гюбля, Гануса, Кауфмана, Маргошеса, 1%-ный раствор крахмала (индикатор), 0,1 н раствор йода, 0,1 н, 0,01 н растворы тиосульфата натрия, 10%-ный раствор йодида калия, диэтиловый эфир, хлороформ, спиртово-эфирная смесь (для рефрактометра); §колбы для титрования с пришлифованными пробками (500 мл), пипетки, бюретки, мерные цилиндры; §водяная баня, аналитические весы, термостат. |
Реактив Гюбля. В 500 мл 96%-го этанола растворить 30 г сулемы. В 500 мл 96%-го этанола растворить 25 г кристаллического йода. Растворы хранить раздельно в темной посуде, смешать за двое суток (48 часов) до анализа. При необходимости раствор сулемы перед смешением фильтруют.
Реактив Гануса. В мерной колбе на 1 л растворить 13 г кристаллического йода в 700 мл ледяной уксусной кислоты, добавить 8,2 г брома (2,61 мл, r20 = 3,14 г/мл) и довести объем раствора уксусной кислоты до метки.
Раствор бромистого натрия и брома в метиловом спирте (метод Кауфмана). В 1 л метилового спирта (перегнанного над окисью кальция) растворить 140 г бромида натрия (NaBr), высушенного при 130 °С. Раствор хорошо перемешать и оставить на 24 часа. По истечении указанного срока к раствору прибавляют 5,1 мл брома. Через 10–15 минут раствор готов к употреблению.
Раствор Маргошеса. В 1000 мл 96%-го этилового спирта растворить 25 г дважды возогнанного йода. Раствор можно использовать в течение 14 дней. К 30 дню титр раствора меняется более чем на 3%.
Йодное число масла
Йодное число является химическим показателем. Википедия трактует его как масса йода, присоединяющаяся к 100 г органического вещества. Медицинский физик И.А. Котомин объясняет расчёт йодного числа масел следующим образом: йодное число масла – это йод в граммах, которого будет достаточно, чтобы химически связать 100 г масла. Проще говоря, если йодное число взятого масла равно 110, то для того, чтобы йодировать 100 г такого масла, потребуется 110 г молекулярного йода. Физик отмечает тот факт, что это довольно много – в знакомой каждому бутылочке йода со спиртовым раствором, например, содержится всего 0,5 г чистого йода. Количество йодного числа масла позволяет нам судить о степени ненасыщенности жирных кислот, входящих в состав масла, соответственно, чем выше содержание ненасыщенных жирных кислот, тем выше йодное число, от которого и зависит степень высыхания масла. Если же масло содержит только насыщенные кислоты, то его йодное число равно нулю.
Йодное число является надежным способом выявления высыхаемости масла, т.е. по величине йодного числа можно узнать, к какой группе по степени высыхаемости относится то или иное масло.
С химической точки зрения, относительно быстроты реакции, масла разделяются:
Высыхающие масла – йодное число больше 170
Содержат много полиненасыщенных жирных кислот: линолевой, линоленовой и элеостеариновой, быстро вступают в реакцию). К ним относятся – льняное, конопляное и древесное масло.
Полувысыхающие масла – йодное число между 100 и 169
Медленно вступают в реакцию, имеют в своем составе кроме олеиновой значительное количество линолевой кислоты). К ним относятся – подсолнечное, хлопковое, маковое, соевое, кукурузное и др.
Невысыхающие – йодное число до 100
Совсем или почти не вступают в реакцию, содержат большое количество олеиновой кислоты и малый процент линолевой и линоленовой кислот). К ним относятся – оливковое, миндальное, рапсовое и др.
В данной таблице можете ознакомиться с йодное число некоторых масел:
|
Невысыхающие масла (тип олеиновой кислоты) |
|
|
Оливковое |
80–85 |
|
Арахисовое |
83–105 |
|
Рапсовое |
94 – 106 |
|
Миндальное |
93–102 |
|
Персиковое |
96–103 |
|
Касторовое |
81–90 |
|
Полувысыхающие масла (тип линолевой кислоты) |
|
|
Горчичное |
93–107 |
|
Кунжутное |
103–112 |
|
Соевое |
124 – 133 |
|
Маковое |
131–143 |
|
Хлопковое |
100–120 |
|
Подсолнечное |
119–145 |
|
Кукурузное |
117–123 |
|
Высыхающие масла (тип линоленовой кислоты) |
|
|
Конопляное |
140–175 |
|
Тунговое масло |
154 – 176 |
|
Льняное |
170 – 205 |
Почему все-таки конопляное, льняное и др. масла являются высыхающими? Т.к. в них из-за присутствия двойных связей возможна полимеризация – «сшивка» отдельных молекул с образованием нерастворимой пленки. Поэтому это свойство широко используют для приготовления натуральной олифы – растворителя для масляных красок. Немецкий автор статьи «Немецкие стратегии применения и комбинирования растительных масел – VITAZONE» Хайке Кэсер объясняет это так, что обозначения «высыхающее», «полувысыхающее» и «невысыхающее» относятся к способности масел загустевать под воздействием кислорода, то есть образовывать сухую эластичную пленку. А льняное масло имеет с ненасыщенные жиры, которые затвердевают под воздействием кислорода (полимеризуются), благодаря чему надежно защищает деревянные поверхности.
Будьте предельно внимательны при покупке разбавленного льняного масла с растительным, ведь, как мы выяснили подсолнечное масло «полувысыхающее» может так и не высохнуть, т.е. при добавлении его в льняное масло степень высыхаемости снижается. Так зачем его совсем добавлять, если льняное масло идеально для древесины? – вопрос риторический. Поэтому всегда рекомендуем читать состав масла для дерева.
На этом наш «урок химии» дошел к своему логическому концу!
Мы уверены, что информация была для Вас полезна. Теперь выбор, каким же всё-таки маслом покрывать свою любимую древесину очевиден. Правда?
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 31 октября 2017 года; проверки требуют 7 правок.
Иодное число — масса иода (в г), присоединяющегося к 100 г органического вещества.
Что характеризует иодное число[править | править код]
Иодное число, которое характеризует содержание двойных связей в ненасыщенном соединении, определяют при исследовании жиров, а также при анализе жирных кислот и установлении содержания реагирующих с иодом примесей в ароматических углеводородах.
Иодное число определяет общую ненасыщенность жиров. Чем выше иодное число, то есть тем больше иода вещество может присоединить, тем больше ненасыщенных кислот содержится в жире.
Определение иодного числа[править | править код]
В некоторых случаях при определении иодного числа устанавливают массу более легко присоединяющегося брома и вычисляют эквивалентную ему массу иода. Кроме того, существует метод определения иодного числа с использованием хлористого иода (ICl), который присоединяется по месту двойных связей, а его избыток вытесняет иод из иодида калия. В любом из методов эквивалентный избыток иода титруют раствором тиосульфата натрия[1].
Иодное число растительного масла можно вычислить по формуле: N iod = 0,86 × Oleic + 1,732 × Linolic + 2,616 × Linolenic, где Oleic, Linolic и Linolenic – это доля олеиновой, линолевой и линоленовой кислот в масле соответственно.
См. также[править | править код]
- Животные жиры
- Карбоновые кислоты
- Растительные масла
Примечания[править | править код]
- ↑ ГОСТ 7636-85
Литература[править | править код]
- ГОСТ 5475-69
- ISO 3961-2009 (fourth edition)
- Зиновьев А. А. Химия жиров. 1952
- Русский Химический Бюллетень том 33, № 12, стр. 2501—2504
Йодное число (ОФС.1.2.3.0005.15)
Государственная фармакопея 13 издание (ГФ XIII)
Йодное число (II) — количество йода, выраженное в граммах, связываемое 100 г испытуемого вещества.
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
ОФС.1.2.3.0005.15 Йодное число
Взамен ст. ГФ XI, вып.1
Йодным числом (II) называют количество йода, выраженное в граммах, связываемое 100 г испытуемого вещества. Йодное число характеризует содержание в испытуемом веществе непредельных соединений (например, непредельных жирных кислот в жирах или маслах).
Метод 1
Точную навеску испытуемого вещества в количестве, указанном в табл. 1, помещают в сухую коническую колбу с притертой пробкой вместимостью 250 мл, растворяют в 3 мл эфира или хлороформа, прибавляют 20,0 мл йода монохлорида раствора 0,1 М, закрывают колбу пробкой, смоченной 10 % раствором калия йодида, осторожно встряхивают и выдерживают в темном месте в течение 1 ч.
Прибавляют последовательно 10,0 мл калия йодида раствора 10 %, 50 мл воды и титруют натрия тиосульфата раствором 0,1 М при постоянном энергичном встряхивании до светло-желтой окраски раствора. Прибавляют 3 мл хлороформа, сильно встряхивают, затем прибавляют 1 мл раствора крахмала и продолжают титрование до обесцвечивания раствора. Проводят контрольный опыт в тех же условиях.
При анализе твердых жиров навеску испытуемого вещества растворяют в 6 мл эфира, прибавляют 20,0 мл йода монохлорида раствора 0,1 М и 25 мл воды. Дальнейшее определение проводят, как указано выше.
Таблица 1. Величина навески испытуемого вещества в зависимости от ожидаемого йодного числа

Йодное число вычисляют по формуле:

где
V1 – объем натрия тиосульфата раствора 0,1 М, израсходованный на титрование в основном опыте, мл;
V2 – объем натрия тиосульфата раствора 0,1 М, израсходованный в контрольном опыте, мл;
a – навеска испытуемого вещества, г;
0,01269 – титр натрия тиосульфата раствора 0,1 М по йоду, г/мл.
Метод 2
Точную навеску испытуемого вещества в количестве, указанном в табл. 2, помещают в сухую коническую колбу с притертой пробкой вместимостью 250 мл и растворяют в 15 мл хлороформа. Медленно прибавляют 25,0 мл раствора йода бромида. Колбу закрывают и выдерживают в темном месте в течение 30 мин, если не указано иначе в фармакопейной статье, часто встряхивая. Прибавляют последовательно 10,0 мл калия йодида раствора 10 %, 100 мл воды и титруют натрия тиосульфата раствором 0,1 М при постоянном энергичном встряхивании до светло-желтой окраски раствора. Прибавляют 5 мл раствора крахмала и продолжают титрование, прибавляя натрия тиосульфата раствор 0,1 М по каплям, до обесцвечивания раствора. Проводят контрольный опыт в тех же условиях.
Таблица 2. Величина навески испытуемого вещества в зависимости от ожидаемого йодного числа

Йодное число вычисляют по формуле, приведенной в методе 1.
