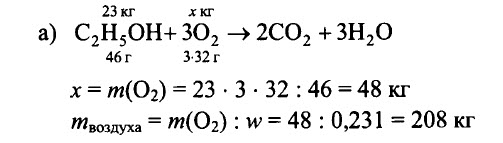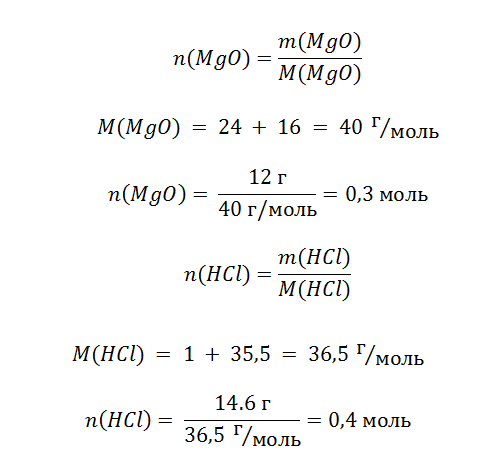Рябов Химия 8 Решение задач Кислород
Рябов Химия 8 Решение задач Кислород — это цитаты (задачи) из Главы 2 «Кислород. Горение» пособия Сборник задач и упражнений по химии: 8-9 классы: к учебникам Г.Е. Рудзитиса, Ф.Г. Фельдмана «Химия. 8 кл.», «Химия. 9 кл». ФГОС (к новым учебникам) / М.А. Рябов. — М. : Издательство «Экзамен», 2016. А также ответы и решения задач из указанного сборника.
Цитаты из вышеуказанного учебного пособия использованы на сайте в незначительных объемах, исключительно в учебных и информационных целях (пп. 1 п. 1 ст. 1274 ГК РФ), при этом цитаты переработаны в удобный для пользователя формат. При постоянном использовании задач по химии в 8 классе необходимо купить книгу: Михаил Рябов: Химия. 8-9 классы. Сборник задач и упражнений. ФГОС / М.: Экзамен, 2018. Ответы и решения расчетных задач помогут родителям проверить правильность выполнения домашних заданий.
Ответы на расчетные задачи
2.5.
Определите массу: а) 3 моль газообразного кислорода, б) 14 моль газообразного кислорода.
РЕШЕНИЕ:
Ответ: а) 96 г, б) 448 г.
2.39.
Определите массовую долю кислорода: а) в оксиде углерода(II), б) в оксиде азота(I), в) в оксиде фосфора(III), г) в оксиде кремния(IV).
РЕШЕНИЕ:
Ответ: а) 0,571, б) 0,364, в) 0,436, г) 0,533.
2.40.
Определите массовую долю кислорода: а) в серной кислоте H2SO4, б) в пероксиде водорода Н2O2, в) в карбонате кальция СаСО3, г) в сульфате меди CuSO4.
РЕШЕНИЕ:
Ответ: а) 0,653, б) 0,941, в) 0,48, г) 0,40.
2.53.
Определите массу кислорода, необходимую для окисления: а) 2 моль глюкозы, б) 45 г глюкозы.
РЕШЕНИЕ:
Ответ: а) 384 г, б) 48 г.
2.55.
Определите массу кислорода, необходимую для сжигания: а) 1 кг ацетилена, б) 3 моль ацетилена.
РЕШЕНИЕ:
Ответ: а) 3,08 кг, б) 240 г.
2.56.
Сколько (в кг) кислорода необходимо для полного сгорания: а) 80 кг метана СН4, б) 16 кг серы, в) 60 кг угля, г) 100 кг гептана С7Н16?
РЕШЕНИЕ:
Ответ: а) 320 кг, б) 16 кг, в) 160 кг, г) 176 кг.
2.59.
Какая масса кислорода была получена в ходе реакции фотосинтеза, если при этом: а) образовалось 90 г глюкозы, б) поглотилось 5 моль углекислого газа?
РЕШЕНИЕ:
Ответ: а) 96 г, б) 160 г.
2.60.
Какая масса углекислого газа поглотилась в ходе фотосинтеза, если: а) выделилось 160 г кислорода, б) образовалось 2 моль глюкозы?
РЕШЕНИЕ:
Ответ: а) 220 г, б) 528 г.
2.92.
Массовая доля кислорода в воздухе равна 0,231. Определите массу кислорода, который можно получить: а) из 1000 кг воздуха, б) из 600 г воздуха.
РЕШЕНИЕ:
Ответ: а) 231 кг, б) 139 г.
2.93.
Массовая доля кислорода в воздухе равна 0,231. Определите массу воздуха, необходимого для получения: а) 100 кг кислорода, б) 200 г кислорода.
РЕШЕНИЕ:
Ответ: а) 433 кг, б) 866 г.
2.94.
Определите массу воздуха с массовой долей кислорода, равной 0,231, необходимого для полного сгорания: а) 23 кг этилового спирта С2Н5ОН, б) 62 кг фосфора, в) 12 кг магния, г) 29 кг бутана С4Н10.
РЕШЕНИЕ:
Ответ: а) 208 кг, б) 346 кг, в) 34,6 кг, г) 442 кг.
Рябов Химия 8 Решение задач Кислород
Следующий раздел «Рябов Химия 8 Решение задач Водород»
План урока:
Основные величины и формулы их нахождения
Основные величины и формулы их нахождения
Ключевым понятием в химии является вещество. Урок 2 в данном курсе, напомнит Вам, все необходимые сведения. Формула для определения количества вещества, в зависимости от исходных данных, выражается в следующем виде.
Для веществ характерно взаимодействие друг с другом. Перед химиками стоит задача вычислить какое количество вещества необходимо для реакции с другим веществом.В химической промышленности, на производстве важно знать, какая масса или объём реагентов необходим, и сколько возможно получить в итоге реакции продукта. Вещества реагируют между собой в определённых количествах, точнее эквивалентах. Как трактовать последнее предложение. Вспомните себя маленькими, когда вы только начинали изучать количество, на примере мячиков, яблок, конфет и т.д.
Согласитесь, что самому большому шарику будет тесно в маленьком стаканчике, впрочем, как и маленькому шарику не совсем уютно будет в большом стаканчике. Т.е. мы выбираем стаканчик для шарика эквивалентно его размеру.
Возьмём, к примеру, кислород, который реакционно-способный и окисляет другие соединения.
Вспомним закон сохранения массы вещества (ЗСМВ), без которого невозможно составить химические уравнения.
Источник
Следует отметить, чтобы прореагировало 1 моль СН4, необходим кислород количеством молей 2. Снова обращаясь к базовому закону, мы видим, что реагентов и продуктов масса одинаковая, точнее 80 г. Почему именно эта цифра, и откуда она взялась. Для этого смотрим на уравнение реакции.
Другими словами, чтобы образовалось 1 моль СО2 и 2 моль Н2О, необходимо чтобы метан и кислород прореагировали пропорционально 1: 2.
Выразим массу, которая будет соответствовать этому количеству вещества.
m = n * M
Вспомним, каким образом вычисляется молярная масса.
Давайте попробуем чуть-чуть усложниться, к примеру, будет реагировать не 1 моль метана, а 2,5 моль. Сколько тогда потребуется О2?
И здесь приведём такой наглядный пример. Один килограмм конфет стоит 2 рубля. Сколько Вам понадобится денег, чтобы купить 2,5 кг. Не составит труда дать ответ, что необходимо потратить 5 рублей. А если, Вы захотите 4 кг, то придётся попросить у родителей уже 8 рублей. Вот эти размышления перенесём на наш пример.
Какое количество мы бы не взяли метана, то кислорода необходимо в 2 раза больше. Т.е. для реакции 2,5 моль СН4 необходим О2 количеством 5 моль.
Количество вещества – это уникальная величина, от которой можно перейти к другим параметрам вещества (m или V), используя основные формулы.
Рассмотрим задачи на определение массы вещества,а также объёма с помощью химических уравнений. Как и при решении, абсолютно всех задач, первое, что мы делаем, читаем внимательно условие и выписываем все известные физические величины (дано), а также определяем, что неизвестно (найти).
Задача 1. Сколько литров (н. у.) кислорода необходимо потратить для полного сгорания 8,5 г сероводорода.
Дано:
m(H2S) = 8,5 г
Найти:
V(O2) – ?
Решение.
Переведём условие задачи на химический язык, т.е. составим уравнение реакции. Важно отметить, что для удобства и лёгкости решения подчеркните те соединения, о которых идёт речь.
Теперь обратим внимание на коэффициенты в химических уравнениях, именно они отвечают за соотношение веществ.
Следует заметить, что массу (г) сероводорода необходимо выразить в количестве (моль).
Запишем мольное соотношение сероводорода и кислорода, в значение числителя подставляем коэффициенты с уравнения, а в знаменателе – что известно в условии задания.
Из пропорции определим число молей для кислорода.
Ответим на вопрос задачи (находим объём кислорода)
Ответ. V(O2) = 8.4 л
Теперь представим следующую ситуацию, Вам на день Рождения или на другой праздник подарили деньги, чтобы Вы приобрели себе желаемую вещь. К примеру, вы хотите себе наушники, карту памяти и новый чехол на телефон. Возникает закономерный вопрос, а хватит ли Вам денег. Такие задачи встречаются и в химии.
Задача 2. Хватит ли 10 л кислорода для сгорания 12 г магния и 0,6 г углерода (н.у.)?
Дано:
V(O2) = 10 л
m(Mg) = 12 г
m(C) = 0,6 г
Найти:
V(O2) – ?
Решение
Особенность этой задачи, что будет два уравнения реакции, взаимодействие О2 отдельно с магнием и углеродом. Это как покупка в двух разных магазинах. Используя алгоритм, приведённый выше, вычислим количество вещества кислорода. Следует заметить, что отдельно ведём расчёт по магнию (или по углероду), заполняя данные таблицы.
Обратите внимание, в предыдущей задаче кислород был в избытке, в объёме 10 – 6,72 = 3,28 л. Этому избытку не с чем реагировать. Представьте, что Вы помощник деда Мороза и пакуете новогодние подарки. Допустим в одном наборе должно содержаться 5 шоколадных конфет и 8 карамелек. Вам необходимо разделить 55 шоколадки и 72 карамельки. Вопрос: сколько наборов у Вас получится? Проведём нехитрые математические исчисления, знакомые Вам ещё с курса математики младшей школы.
55 : 5 = 11
72 : 8 = 9
И что получается, что шоколадки можно разместить в 11 наборов, а карамельки только в 9. Таким образом, получится 9 новогодних подарков, и 10 (5 ∙ 2 = 10) шоколадок будут лишними, они в избытке.
Расчёты по химическим уравнениям, где один из реагентов берётся в избытке (т.е. его больше, чем необходимо), проводятся аналогично, как и с одним известным веществом.
Задача 3. 48,75 цинка привели в реакцию с 5,6 л (условия нормальные) хлора. Сколько соли получилось в итоге, ответ выразите в граммах.
Дано:
V(Cl2) = 5.6 л
m(Zn) = 48.75 г
Найти:
m(ZnCl2) – ?
Решение.
Составим схему взаимодействия, не забудьте отметить количество реагирующих молей.
Теперь наша с Вами задача определить, какое вещество прореагировало полностью, а какое осталось в избытке. Вспомните пакеты с подарками, какие конфеты мы разложили полностью и почему остались шоколадные лишними. Поможет определиться с избытком, решение неравенства.
n (Zn) ? n (Cl2) ?
Расчёт для цинка производится согласно формуле:
Хлор – это газообразное вещество, поэтому нужно применить формулу:
Сравним полученные значения n(Zn) > n(Cl2), цинк находится в избытке, поэтому расчёт ведём по хлору, который прореагировал полностью количеством 0,25 моль.
Из пропорции вычислим количество образованной соли (не забываем, что числитель отвечает за коэффициенты, а знаменатель – это данные в условии).
Ответ. Масса соли равна 34 г.
Большинство химических реакций происходит в растворе. Однако при расчётах необходима масса именно растворённого вещества, которое непосредственно реагирует. Допустим, команда с 12 человек, которая на 25% состоит из девочек и 75% мальчиков, поехала на соревнования. В одном из этапов участвуют только мальчики. Ваша задача определить, сколько мальчиков поехало на соревнования.
Вот эти 9 мальчишек и участвовали в определённом туре, а девочки на данный момент были не в счёт, они были в группе поддержки.
Задача 4. На 12 г оксида магния подействовали 146 г раствора соляной кислоты, с массовой долей раствора 10%. Вычислите, сколько соли образовалось в процессе взаимодействия этих веществ?
Дано:
m(MgO) = 12 г
mр-ра(HCl) = 146 г
Wр-ра(HCl) = 10%
Найти:
m(MgCl2) – ?
Решение
Особенностью этой задачи является то, что в условии указана масса всего раствора, а необходимо знать только,сколько содержится кислоты, которая будет реагировать с MgO. Формула определения массы вещества, находящегося в растворе, выражается в следующем виде.
Обратите внимание, что из всей массы раствора (146 г) реагирует только 10%, а именно 14,6 г.
Теперь задача определить, какого из реагентов больше и он прореагирует не полностью.
Схема показывает, что для реакции 0,3 моль MgO требуется 0,6 моль кислоты. На это размышление нам указывает схема реакции. Для полного растворения оксида необходимо потратить в 2 раза больше HCl, смотрите соотношение 1:2.Однако в нашем распоряжении есть только 0,4 моль, поэтому n(MgO) >n(HCl), оксид находится в избытке, в то время как кислота прореагировала полностью и мы смело можем использовать её количество вещества для расчёта массы соли.
Снова воспользуемся пропорцией, чтобы узнать количество образованной соли.
Теперь не составит особого труда найти массу.
Ответ. m(MgCl2) = 19 г.
В желаниях человечества изобрести идеальную машину, во время работы которой не будет никаких потерь. Однако на выходе не бывает заветных 100%. Аналогично и во время химических процессов на производстве или лаборатории не удаётся получить продукт с выходом реакции 100%. При решении задач мы вычисляем так называемый теоретический выход, что должно быть в идеальной ситуации. Но мы живём в реальном мире, где есть потери: газообразные продукты могут улетучиться, осадок, образованный в процессе реакции, можно не в полной мере выделить из раствора. Поэтому практический выход всегда будет меньше теоретического.
Задача 5. В результате взаимодействия 59,5 г нитрата серебра с избытком раствора соляной кислоты, был выделен осадок массой 45 г. Определите выход реакции.
Дано:
m(AgNO3) = 59.5 г
m(осадка) = 45 г
Найти:
η – ?
Решение.
Своеобразие этого типа задач в том, что необходимо отличать теоретическую и практическую массу продукта. Маленькой подсказкой вам послужит время глагола, если видите прошедшее или настоящее время (получено, выделили), значит это практическая масса. Чтобы найти выход продукта, необходимо вычислить теоретическую массу или объём (вот за эти параметры как раз и отвечает схема реакции).
Используя привычный алгоритм, определим n нитрата серебра.
Следующим шагом будет определить количество вещества, выпавшего в осадок (AgCl).
Вычислим массу осадка, это будет теоретическая, т.е. та, которая должна получиться, если бы не было потерь.
В идеальной ситуации, мы бы получили 50,225 г, что составило бы 100%. Однако во время процесса образовалось только 45 г продукта. Получается, выход реакции будет меньше и составит:
Ответ. η = 89,6%
Особый тип задач на определение молярной массы вещества. Состав соединений мы можем узнать с химической формулы. При решении этого типа необходимо вспомнить следующие понятия– это доля (массовая) элемента и относительная плотность газов.
Однако следует заметить, что величину D мы можем использовать только для газообразных соединений.
Задача 6. Определите объём кислорода (условия нормальные), что потребуется для сжигания вещества массой 180 г, которое состоит на 26,67 % из углерода, 2,24 % водорода, а также кислорода. Известно, что равняется 45.
Дано:
DH2 = 45
W(C) = 26.67%
W(H) = 2.24%
m(CxHyOz) = 180 г
Найти:
Формула – ?
V(O2) – ?
Решение.
Чтобы решить эту, на первый взгляд, запутанную задачу, нам необходимо сначала определить, что это за соединение, чтобы была возможность составить уравнения химических реакций.
Однако в условии известно только процентный состав вещества. Но всё-таки, этих данных нам достаточно, чтобы найти формулу вещества.
Запишем выражение для нахождения количества атомов углерода (х), водорода (у) и кислорода (z). Представьте, вы купили в коробке шоколадные конфеты из трёх видов.
Следует отметить, что они имеют разную форму, начинку, как следствие и вес. Вернёмся к нашему веществу, которое состоит из 3 элементов, имеющих разнуюAr. Так вот на долю углерода выпадает 26,67% (условно допустим, что это конфета в виде сердечка), водород занимает 2,24% (конфета с воздушной начинкой), а все остальные конфеты в коробке с ореховой начинкой (в соединении их роль играют атомы кислорода). Вопрос: сколько штук занимает каждый вид конфетки? Логично узнать вес одной конфеты (в нашем случае это Ar элементов). Разделив процентное содержание на атомную массу элемента, получим их количество.
Такого же ведь количества конфет не будет в коробке, вы, наверное, слабо себе можете представить, что там будут находиться части конфет. Чтобы получить целые числа, необходимо, выбрать из этих чисел самое маленькое и каждое на него разделить.
Вычисления показывают, что соотношение элементов в данном соединении можно записать в следующем виде: СНО2. Уточним правильность наших расчётов, определив его молекулярную массу, используя величину D.
Обратите внимание, первоначальная запись формулы вещества СНО2 отвечает молярной массе
Однако, это вещество в 45 раз тяжелее водорода, что отвечает 90 г/моль.Чтобы получить её, мы сохранили соотношение элементов 1:1:2, при этом умножили количество каждого элемента на 2. Следовательно, молекулярная формула С2Н2О4.
Количество вещества, отвечающее 45 г вещества С2Н2О4, вычислим привычным методом.
Используя мольное соотношение, определим число молей кислорода, а также его объём.
Ответ. Для сгорания 45 г С2Н2О4 необходимо 5,6 л кислорода.
Обобщая всё выше сказанное, как решать расчётные задачи по химии, с улыбкой или с шоком, принимать решение только Вам. Рассмотрим ещё одну задачу.
Задача 7. Пропан (С3Н8), объёмом 84 л, который содержит 25% негорючих примесей, сожгли в 56 л кислорода. Газ, который выделился, пропустили через гидроксид бария, определите массу осадка, если выход продукта реакции составил 89%.
Дано:
V(С3H8) = 84 л
W(примеси) = 25%
V(O2) = 56 л
η = 89%
Найти:
m(осадка) – ?
Решение.
На что здесь следует обратить внимание. Пропан содержит не горючие примеси. Представьте, вам необходимо в торт 84 г очищенных орехов. Вы идёте в магазин, приобретаете необходимую массу, но придя домой обнаружили, что там 25% содержится мелких остатков скорлупы. Т.е. масса орехов не будет 84 г. Чистых орехов будет 100% – 25% = 75%.
Негорючие примеси входят в общий объём, а гореть будет только пропан. Находим, сколько же его содержится в 84 л.
Составим схему горения газа
Определим количество вещества реагирующих газов
На первый взгляд кажется, что пропан в избытке n(C3H8) > n(O2). Однако посмотрите на уравнение реакции, чтобы сгорело 2,8125 моль пропана необходимо в 5 раз больше кислорода, что составит 14 моль. По этой причине расчёт будем вести по кислороду.
Это количество СО2 пропускают через Ва(ОН)2, что можно отобразить схемой.
Найдём массу ВаСО3, которая будет в виде осадка
Теперь необходимо усчитать выход соли, который составил всего лишь 89%.
Ответ. m(BaCO3) = 263 г.
Вывод молекулярной формулы вещества по продуктам сгорания.
Задача 1.
При полном сгорании 4,6 г газообразного органического вещества получено 8,8 г СО2 и 5,4 г Н2О. Относительная плотность паров вещества по воздуху равна 1,589. Определите молекулярную формулу вещества и дайте названия всем его изомерам.
Решение.
в-во+ О2→ СО2+Н2О
в состав сгораемого вещества обязательно входят углерод и водород, но возможно наличие кислорода. Поэтому, необходимо сделать проверку на кислород:
ν(СО2)=m/M=8,8 г/44 г/моль=0,2 моль; ν(С)=0,2 моль;m(С)=2,4 г
ν(Н2О)=m/M=5,4 г/18 г/моль=0,3 моль; ν(Н)=0,6моль; m(Н)=0,6 г
m(C)+m(H)=2,4 г + 0,6 г=3 г
а вещества сгорело 4,6 г, следовательно, имеется кислород.
m(О)=4,6 г-3 г=1,6 г
ν(О)=1,6 г/16 г/моль=0,1моль
СхНyОz х:y:z= ν(C): ν(Н): ν(О)=0,2:0,6:0,1
Находим среди этих цифр самое маленькое и все делим на него, получая: х:y:z= 2:6:1
С2Н6О-простейшая формула.
D(воздуху)=M(в-ва)/М(воздуха)
М (в-ва)= D(воздуху)×М(воздуха)=1,589×29 г/моль=46 г/моль
M(С2Н6О)=12×2+6+16=46 г/моль,
что соответствует действительности.
^ Ответ: С2Н6О. Это либо этиловый спирт, либо диметиловый эфир.
Задача 2.
При сгорании углеводорода получено 0,2 моль СО2 и 0,2 моль Н2О. Определите молекулярную формулу углеводорода, если известно, что 3,64 г этого вещества занимают объем 1,456 л (н.у.).
Решение.
СхНy + (х+0,25y)О2→ хСО2 +0,5yН2О
(здесь конкретно указано, что горит углеводород).
х,y- коэффициенты перед формулами веществ в правой части – это индексы при углероде и водороде в сгоревшем веществе.
ν(СО2):ν(Н2О)=х:0,5y (по уравнению), а на самом деле как 0,2:0,2 (по условию)
ν(СО2): ν(Н2О)=х:0,5y =0,2:0,2
0,2х=0,1y, х=0,5y (1)
Раз имеется два неизвестных, то должна быть система уравнений. Второе уравнение даст молярная масса вещества:
m=М× ν
V=Vm× ν
Через объем найдем количество углеводорода, а затем его молярную массу:
ν= V/Vm=1,456 л/22,4 л/моль=0,065 моль
M=m/ν=3,64 г/0,065 моль=56 г/моль
составляем уравнение:
12х+y=56
Вместо (х) подставляем его значение из уравнения (1)
12×0,5y+y=56
7y=56, y=8, х=4
^ Ответ: С4Н8
Задача 3.
В состав вещества входят С,Н,О,S. При сжигании его навески массой 0,222 г были получены 0,396 г СО2, 0,162 г Н2О, а сера переведена в сульфат бария массой 0,3495 г. Относительная плотность паров вещества по водороду равна 74. Определить истинную формулу вещества.
Решение:
в-во+ О2→ СО2+Н2О +SО2 (любое вещество, содержащее серу, дает при сгорании диоксид серы),
SО2→ ВаSО4 (через какие реакции осуществлен данный переход – неважно, из сульфата бария надо найти массу и количества серы).
ν(СО2)=m/M=0,396 г/44 г/моль=0,009 моль;ν(С)=0,009 моль; m(С)=0,108 г;
ν(Н2О)=m/M=0,162 г/18 г/моль=0,009 моль;ν(Н)=0,018 моль; m(Н)=0,018 г;
ν(ВаSО4)=m/M=0,3495 г/233 г/моль=0,0015 моль; ν (S)=0,0015 моль; m(S)=0,048 г;
m(О)=0,222-0,108-0,018-0,048 г=0,048 г;
ν(О)=0,048 г/16 г/моль=0,003 моль;
СхНyОzSq х:y:z:q= ν(C): ν(Н): ν(О): ν (S)=0,009:0,018:0,003:0,0015
Находим среди этих цифр самое маленькое и все делим на него, получая: х:y:z:q= 6:12:2:1
С6Н12О2S-простейшая формула.
D(по водороду)=M(в-ва)/М(Н2)
М (в-ва)= D(по водороду)×М(Н2)=74×2 г/моль=148 г/моль
M(С6Н12О2S)=12×6+12+16×2+32=148 г/моль,
что соответствует действительности.
^ Ответ: С6Н12О2S.
Задача 4.
При сгорании газообразного органического вещества, не содержащего кислород, выделилось 2,24 л (н.у.) углекислого газа, 1,8 г воды и 3,65 г хлороводорода. Установите формулу сгоревшего вещества, рассчитайте его объем и массу.
Решение.
В задаче сказано, что вещество не содержит кислород, следовательно, оно состоит только из углерода, водорода и хлора:
СхНyClz + О2→ СО2 +Н2О+ НCl
в этой задаче необходимо найти количество углерода, перешедшего в углекислый газ, количество водорода, перешедшего как в воду, так и в хлороводород, количество хлора из хлороводорода:
х:y:z= ν (C): ν (Н): ν (Cl)
ν(СО2)=V/Vm=2,24 л/22,4 л/моль=0,1 моль; ν(С)=0,1 моль;
ν (Н2О)=m/M=1,8 г/18 г/моль=0,1 моль; ν (Н)=0,2 моль;
ν (НCl)=m/M=3,65 г/36,5 г/моль=0,1 моль; ν (Cl)=0,1 моль;
ν (Н)=0,1 моль
ν (Н)общее=0,1 моль+0,2 моль=0,3 моль
х:y:z= ν (C): ν (Н): ν (Cl)=0,1:0,3:0,1
Находим среди этих цифр самое маленькое и все делим на него, получая: х:y:z= 1:3:1
СН3Сl-истинная формула.
СН3Сl+ 1,5О2→ СО2 +Н2О+ НCl
Для нахождения массы и объема сгоревшего вещества, необходимо составить количественные соотношения между хлорметаном и любым продуктом реакции:
ν (СН3Сl): ν (СО2)=1:1 (по уравнению), ν (CН3Сl)=0,1 моль
m(СН3Сl)=М× ν =50,5 г/моль×0,1 моль=5,05 г
V(СН3Сl)=Vm× ν =22,4 л/моль×0,1 моль=2,24 л
^ Ответ: СН3Сl, m(СН3Сl)=5,05 г, V(СН3Сl)=2,24 л.
Задача 5.
Неизвестное органическое вещество массой 0,4 г сожгли и продукты сгорания пропустили через трубку с безводным сульфатом меди (II) и сосуд, содержащий избыток баритовой воды. Масса трубки увеличилась на 0,36 г, в сосуде образовался осадок массой 5,91 г. Установить формулу вещества.
Решение.
в-во+ О2→ СО2+Н2О
В состав сгораемого вещества обязательно входят углерод и водород, но возможно наличие кислорода. Поэтому необходимо сделать проверку на кислород.
Масса трубки с сульфатом меди (II) увеличилась за счет поглощенной воды (CuSО4 + nН2О→CuSО4×nН2О), откуда делаем вывод, что масса выделившейся воды равна 0,36 г.
С баритовой водой (Ва(ОН)2) взаимодействует СО2):
Ва(ОН)2+ СО2→ВаСО3↓+Н2О
ν(ВаСО3)=m/M=5,91 г/197 г/моль=0,03 моль;
ν(ВаСО3): ν(СО2)=1:1 (по уравнению), сл-но, ν(СО2)=0,03 моль;
ν(С)=0,03 моль, m(С)=0,36 г
ν(Н2О)=m/M=0,36 г/18 г/моль=0,02 моль; ν(Н)= 0,04 моль;
m(Н)=0,04 г
m(C)+m(H)=0,36+0,04=04 г
следовательно, кислорода нет.
СхНy х:y= ν(C): ν(Н)=0,03:0,04 (можно умножить все на 100)
х:y= 3:4
^ Ответ: С3Н4.
Задача 6*.
Смесь газов, образовавшихся при сжигании образца органического соединения Х массой 2,7 г, была пропущена последовательно через склянки с концентрированной серной кислотой и известковой водой. При этом масса первой склянки увеличилась на 3,78 г, во второй склянке образовалось 12 г осадка, а объем непоглощенного газаY составил 733 мл (250С и нормальное давление). При одновременном добавлении к такому же образцу вещества Х избытка раствора нитрита натрия и соляной кислоты выделяется вдвое больший объем газа Y. Определите неизвестное вещество Х и приведите его структурную формулу.
Решение.
Газ, который не поглощается известковой водой – это азот. Следовательно, в состав неизвестного вещества обязательно входят углерода, водород, азот и возможно, кислород.
в-во+ О2→ СО2+Н2О+ N2
Масса склянки с конц. Н2SО4 увеличивается за счет поглощения кислотой воды, m(Н2О)=3,78 г
С известковой водой взаимодействует углекислый газ:
СО2 + Са(ОН)2→СаСО3↓+Н2О
ν(СаСО3)=m/M=12 г/100 г/моль=0,12 моль;
ν(СаСО3): ν(СО2)=1:1, ν(СО2)=0,12 моль;
Проверка на кислород:
ν(СО2)=0,12 моль; ν(С)=0,12 моль;m(С)=1,44 г
ν(Н2О)=m/M=3,78 г/18 г/моль=0,21 моль; ν(Н)=0,42 моль;
m(Н)=0,42 г.
Приведем объем азота к н.у., учитывая, что Т=(273 +25)К=298 К
По «объединенному газовому закону»
V0=Р×V×Т0/Р0×Т
V0=(101,3×0,733×273)/(101,3×298)=0,672 л
ν(N2)=V/Vm=0,672 л/22,4 л/моль=0,03 моль, ν(N)=0,06 моль,
m(N)=0,84 г;
m(C)+m(H)+m(N)=1,44 г + 0,42 г+0,84=2,7 г
кислорода нет, так как вещества сгорело тоже 2,7 г.
СхНyNz х:y:z= ν(C): ν(Н): ν(N)=0,12:0,42:0,06
Находим среди этих цифр самое маленькое и все делим на него, получая: х:y:z= 2:7:1
С2Н7N-амин. Это может быть либо первичный амин С2Н5NН2, либо вторичный амин (СН3)2NН.
Установить его структуру поможет реакция с азотистой кислотой. Только первичные амины вступают в реакцию с НNО2 по уравнению:
С2Н5NН2 + NаNО2 + НCl→С2Н5ОН + N2 +NаCl+Н2О
^ Ответ: Х- C2Н2NН2– этиламин, Y-N2.
Задачи для самостоятельного решения.
1.При сжигании 3,7 г монофункционального органического вещества было получено 2,7 г воды и 3,36 л (н.у.) диоксида углерода. Какое это вещество, если при взаимодействии его с натрием выделяется водород, а водный раствор продукта реакции окрашивает лакмус в синий цвет? Составить уравнение реакции взаимодействия с натрием.
2. Относительная плотность паров органического соединения по гелию равна 25,5. При сжигании 15,3 г этого вещества образовалось 20,16 л (н.у.) углекислого газа и 18,9 г воды. Выведите молекулярную формулу органического соединения. К каким классам органических соединений может относиться данное вещество?
3.При полном сгорании 4,8 г органического вещества, плотность паров которого по водороду равна 16, получили 6,6 г диоксида углерода и 5,4 г воды. Каковы формула и названия этого вещества?
Составить не менее трех уравнений реакций получения данного вещества.
4.При полном сгорании 0,88 г органического соединения образовалось 896 мл СО2 (н.у.) и 0,72 г воды. Выведите молекулярную формулу этого вещества, если плотность паров по водороду равна 44. Укажите, к каким классам может относиться это вещество. Найти все изомеры данного вещества.
5. При сжигании вещества массой 10,7 г получили 30,8 г углекислого газа, 8,1 г воды и 1,4 г азота. Плотность паров этого вещества по воздуху равна 3,69. Определите молекулярную формулу вещества.Составить уравнение реакции данного вещества с хлороводородом, дать название образующемуся продукту.
6.При сгорании 0,9 г газообразного органического вещества выделилось 0,896 л (н.у.) углекислого газа, 1,26 г воды и 0,224 л (н.у.) азота. Плотность газообразного вещества по азоту 1,607. Установите молекулярную формулу органического вещества и приведите одно из возможных названий. Привести не менее трех уравнений реакций получения данного вещества.
7.При сгорании 0,45 г газообразного органического вещества выделилось 0,448 л углекислого газа, 0,63 г воды и 0,112 л азота.Объемы газов измерялись при нормальных условиях. Плотность газообразного вещества по азоту 1,607. Установите его молекулярную формулу и приведите одно из возможных названий этого соединения. С какими из перечисленных соединений может взаимодействовать это вещество: а) метаном; б) гидроксидом бария; в) водой; г) кислородом; д) бензолом; е) азотной кислотой. Составить уравнения данных реакций.
8.При полном сгорании 0,62 г газообразного органического вещества выделилось 0,448 л углекислого газа, 0,9 г воды и 0,224 л азота (объемы газов измерены при нормальных условиях). Плотность вещества по водороду 15,50. Установите его молекулярную формулу и назовите это соединение. Это вещество может быть получено при взаимодействии:
а) СН4 и НNО3 б) СН3NО2 и Н2 в) СН3ОН и N2
г) СН3ОН и NН3 д) CН3NН3Cl и КОН е) СН3-СН3 и NН3
Составить уравнения осуществимых реакций.
9.Сожгли 6 г вещества и получили 6,72 л углекислого газа (н.у.) и 7,2 г воды. Относительная плотность паров вещества по воздуху равна 2,07. Определить молекулярную формулу вещества. Для этого вещества характерны реакции:
а) этерификации б) поликонденсации в) нейтрализации
г) окисления д) дегидратации е) гидратации.
10.Относительная плотность паров органического вещества по водороду равна 30. При сжигании 24 г вещества образовались 35,2 г оксида углерода (IV) и 14,4 г воды. Определить молекулярную формулу вещества. Составить уравнения реакций получения данного вещества в лаборатории и промышленности.
11.Относительная плотность паров органического соединения по сернистому газу равна 2. При сжигании 19,2 г этого вещества образуется 52,8 г углекислого газа (н.у.) и 21,6 г воды. Выведите молекулярную формулу органического соединения. К каким классам органических соединений оно может относиться?
12.При сгорании вещества массой 8,5 г образовались оксид углерода (IV) массой 26,4 г и вода массой 11,7 г. Плотность паров вещества по воздуху равна 5,862. Определите формулу вещества.
Рассчитать массовую долю кислорода в соединении CH4O (метанол).
Решение задачи
Вычислим массовую долю кислорода (О) в соединении CH4O (метанол).
Напомню, что массовая доля элемента в соединении – это отношение массы элемента (mэ) к массе вещества (mв), в состав которого входит данный элемент. Массовую долю выражают в долях единицы или в процентах.
Учитывая данные таблицы Менделеева рассчитаем молярную массу метанола (CH4O):
M (CH4O) = 12 + 4 ⋅ 1 + 16 = 32 (г/моль).
Следовательно, масса метанола (CH4O) равна 32 грамма.
Рассчитаем массовую долю кислорода, входящего в состав метанола (CH4O), получаем:
Ответ:
массовая доля кислорода равна 0,5.
при полном сгорании 8,8 г органического вещества образовалось 17,6 г углекислого газа и 7,2 г воды. Относительная плотность вещества по водороду равна 36. Определи молекулярную формулу вещества.
1. Определим количества углерода в углекислом газе и водорода в воде:
n(C)=n(CO2)=17,6г44г/моль=0,4моль;
n(H)=2n(H2O)=2⋅7,2г18г/моль=0,8моль.
2. Определим, содержится ли в веществе кислород:
m(O)=m(в−ва)−m(C+H)=8,8−(0,4⋅12+0,8⋅1)=3,2г.
Значит, в сгоревшем веществе есть кислород и формулу можно записать так:
CxHyOz
.
3. Найдём количество кислорода:
n(O)=3,2г16 г/моль=0,2моль.
4. Отношение индексов в молекуле:
x:y:z=0,4моль:0,8моль:0,2моль=4:8:1.
Значит, простейшая формула вещества —
C2H4O
.
5. Определим относительную молекулярную массу вещества по его плотности и сравним с массой
C2H4O
:
Mr(CxHyOz)=DH2⋅Mr(H2)=36
·2=72.
Mr(C2H4O)=2⋅12+4⋅1+1⋅16=72.
Следовательно, простейшая и молекулярная формулы совпадают.