Расчет количества теплоты при нагревании и охлаждении:
Вы уже знаете, что изменить внутреннюю энергию тела можно передачей ему количества теплоты. Как связано изменение внутренней энергии тела, т. е. количество теплоты, с характеристиками самого тела?
Внутренняя энергия тела есть суммарная энергия всех его частиц. Значит, если массу данного тела увеличить в два или три раза, то и количество теплоты, необходимое для его нагревания на одно и то же число градусов, увеличится в два или три раза. Например, на нагревание двух килограммов воды от 20 °C до 80 °C потребуется в два раза больше теплоты, чем на нагревание одного килограмма воды (рис. 40, а).
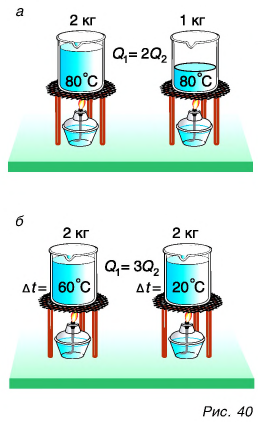
Очевидно также, что для нагревания воды на 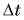
Из этих рассуждений следует подтвержденный опытами вывод. Количество теплоты, необходимое для нагревания тела, прямо пропорционально его массе и изменению температуры.
А зависит ли количество теплоты, идущее на нагревание, от рода вещества, которое нагревается?
Для ответа на этот вопрос проведем опыт. В два одинаковых стакана нальем по 150 г подсолнечного масла и воды. Поместим в них термометры и поставим на нагреватель (рис. 41).
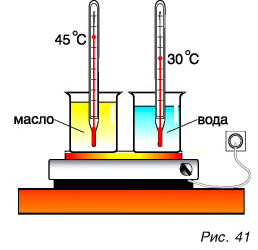
Получив за одинаковое время от нагревателя равное с водой количество теплоты, масло нагрелось больше, чем вода. Значит, для изменения температуры масла на одну и ту же величину требуется меньше теплоты, чем для изменения температуры такой же массы воды.
Поэтому для всех веществ вводят специальную величину — удельную теплоемкость вещества. Эту величину обозначают буквой с (от лат. capacite — емкость, вместимость). Теперь мы можем записать строгую формулу для количества теплоты, необходимого для нагревания:
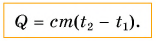
Выразим из этой формулы с: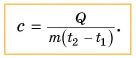
Удельная теплоемкость есть физическая величина, численно равная количеству теплоты, которое необходимо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C. Удельная теплоемкость измеряется в джоулях на килограмм-градус Цельсия 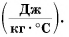
Для любознательных:
Часто формулу 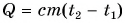 записывают в виде
записывают в виде 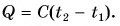 Здесь величина
Здесь величина 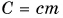 называется теплоемкостью тела (обратите внимание — не вещества). Она численно равна количеству теплоты, необходимому для нагревания всей массы тела на 1 °C. Измеряется теплоемкость тела в джоулях на градус Цельсия
называется теплоемкостью тела (обратите внимание — не вещества). Она численно равна количеству теплоты, необходимому для нагревания всей массы тела на 1 °C. Измеряется теплоемкость тела в джоулях на градус Цельсия 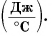
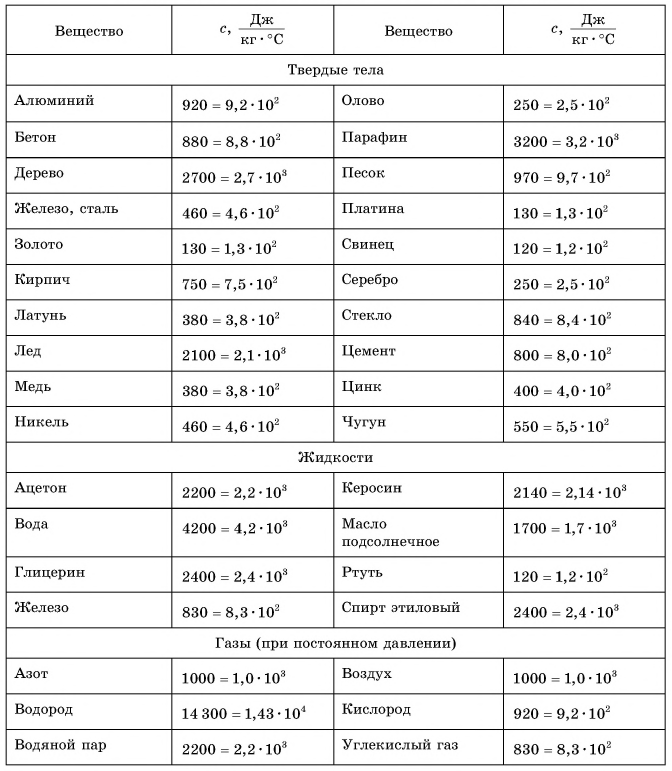
В таблице 1 представлены значения удельной теплоемкости различных веществ (в различных состояниях). Как следует из этой таблицы, среди жидкостей максимальное значение удельной теплоемкости имеет вода: для нагревания 1 кг воды на 1 °C требуется 4200 Дж теплоты — это почти в 2,5 раза больше, чем для нагревания 1 кг подсолнечного масла, и в 35 раз больше, чем для нагревания 1 кг ртути.
Формула 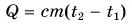 дает возможность найти и выделяемую при охлаждении тела теплоту. Так как конечная температура
дает возможность найти и выделяемую при охлаждении тела теплоту. Так как конечная температура 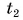 остывшего тела меньше начальной
остывшего тела меньше начальной 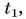 то изменение температуры оказывается отрицательным числом. Значит, и выделяемое телом количество теплоты выражается отрицательным числом, что обозначает не рост, а убыль внутренней энергии тела.
то изменение температуры оказывается отрицательным числом. Значит, и выделяемое телом количество теплоты выражается отрицательным числом, что обозначает не рост, а убыль внутренней энергии тела.
В заключение заметим, что при теплообмене двух или нескольких тел абсолютное значение количества теплоты, которое отдано более нагретым телом (телами), равно количеству теплоты, которое получено более холодным телом (телами):
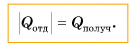
Это равенство называется уравнением теплового баланса и выражает, по сути, закон сохранения энергии. Оно справедливо при отсутствии потерь теплоты.
Таблица 1. Удельная теплоемкость некоторых веществ
Главные выводы:
- Количество теплоты, необходимое для нагревания тела (выделившееся при охлаждении), прямо пропорционально его массе, изменению температуры тела и зависит от вещества тела.
- Удельная теплоемкость вещества численно равна количеству теплоты, которое надо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C.
- При теплообмене количество теплоты, отданное более горячим телом, равно по модулю количеству теплоты, полученному более холодным телом, если нет потерь теплоты.
- Заказать решение задач по физике
Пример решения задачи:
Для купания ребенка в ванночку влили холодную воду массой 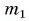 = 20 кг при температуре
= 20 кг при температуре 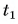 = 12 °C. Какую массу горячей воды при температуре
= 12 °C. Какую массу горячей воды при температуре 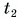 = 80 °C нужно добавить в ванночку, чтобы окончательная температура воды стала
= 80 °C нужно добавить в ванночку, чтобы окончательная температура воды стала 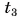 = 37 °C? Удельная теплоемкость воды с = 4200
= 37 °C? Удельная теплоемкость воды с = 4200 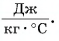
Дано:
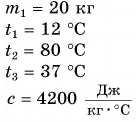
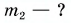
Решение
По закону сохранения энергии 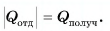
Отдавала теплоту горячая вода, изменяя свою температуру от 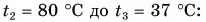
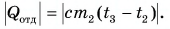
Холодная вода получила эту теплоту и нагрелась от 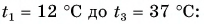
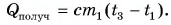
Так как нас интересует только модуль 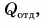 то можно записать:
то можно записать:
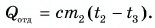
Тогда 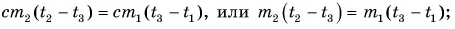
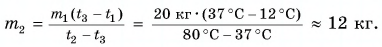
При решении мы пренебрегали потерями теплоты на нагревание ванночки, окружающего воздуха и т. д.
Возможен и другой вариант решения.
Рассчитаем сначала количество теплоты, которое было получено холодной водой:
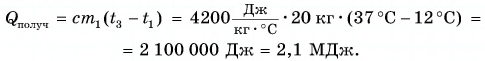
Полагая, что эта теплота отдана горячей водой, запишем: 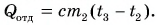 Выразим искомую массу:
Выразим искомую массу:
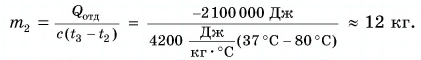
Ответ: 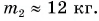
- Удельная теплота сгорания топлива
- Плавление и кристаллизация в физике
- Испарение жидкостей в физике
- Поверхностное натяжение жидкости
- Излучение тепла в физике
- Виды излучений в физике
- Инфракрасные излучения
- Количество теплоты в физике
II. Молекулярная физика
Тестирование онлайн
Термодинамика
Раздел молекулярной физики, который изучает передачу энергии, закономерности превращения одних видов энергии в другие. В отличие от молекулярно-кинетической теории, в термодинамике не учитывается внутреннее строение веществ и микропараметры.
Термодинамическая система
Это совокупность тел, которые обмениваются энергией (в форме работы или теплоты) друг с другом или с окружающей средой. Например, вода в чайнике остывает, происходит обмен теплотой воды с чайником и чайника с окружающей средой. Цилиндр с газом под поршнем: поршень выполняет работу, в результате чего, газ получает энергию, и изменяются его макропараметры.
Количество теплоты
Это энергия, которую получает или отдает система в процессе теплообмена. Обозначается символом Q, измеряется, как любая энергия, в Джоулях.
В результате различных процессов теплообмена энергия, которая передается, определяется по-своему.
Нагревание и охлаждение
Этот процесс характеризуется изменением температуры системы. Количество теплоты определяется по формуле
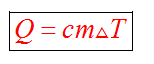
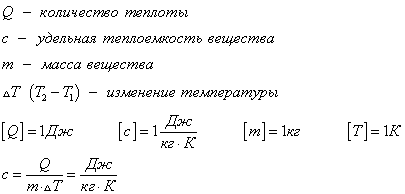
Удельная теплоемкость вещества с измеряется количеством теплоты, которое необходимо для нагревания единицы массы данного вещества на 1К. Для нагревания 1кг стекла или 1кг воды требуется различное количество энергии. Удельная теплоемкость – известная, уже вычисленная для всех веществ величина, значение смотреть в физических таблицах.
Теплоемкость вещества С – это количество теплоты, которое необходимо для нагревания тела без учета его массы на 1К.

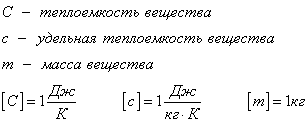
Плавление и кристаллизация
Плавление – переход вещества из твердого состояния в жидкое. Обратный переход называется кристаллизацией.
Энергия, которая тратится на разрушение кристаллической решетки вещества, определяется по формуле


Удельная теплота плавления известная для каждого вещества величина, значение смотреть в физических таблицах.
Парообразование (испарение или кипение) и конденсация
Парообразование – это переход вещества из жидкого (твердого) состояния в газообразное. Обратный процесс называется конденсацией.


Удельная теплота парообразования известная для каждого вещества величина, значение смотреть в физических таблицах.
Горение
Количество теплоты, которое выделяется при сгорании вещества

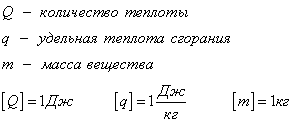
Удельная теплота сгорания известная для каждого вещества величина, значение смотреть в физических таблицах.
Для замкнутой и адиабатически изолированной системы тел выполняется уравнение теплового баланса. Алгебраическая сумма количеств теплоты, отданных и полученных всеми телами, участвующим в теплообмене, равна нулю:
Q1+Q2+…+Qn=0
Количество теплоты. Удельная теплоемкость вещества
Количеством теплоты называют количественную меру изменения внутренней энергии тела при теплообмене.
Количество теплоты — это энергия, которую тело отдает при теплообмене (без совершения работы). Количество теплоты, как и энергия, измеряется в джоулях (Дж).
Удельная теплоемкость вещества
Теплоемкость — это количество теплоты, поглощаемой телом при нагревании на $1$ градус.
Теплоемкость тела обозначается заглавной латинской буквой С.
От чего зависит теплоемкость тела? Прежде всего, от его массы. Ясно, что для нагрева, например, $1$ килограмма воды потребуется больше тепла, чем для нагрева $200$ граммов.
А от рода вещества? Проделаем опыт. Возьмем два одинаковых сосуда и, налив в один из них воду массой $400$ г, а в другой — растительное масло массой $400$ г, начнем их нагревать с помощью одинаковых горелок. Наблюдая за показаниями термометров, мы увидим, что масло нагревается быстрее. Чтобы нагреть воду и масло до одной и той же температуры, воду следует нагревать дольше. Но чем дольше мы нагреваем воду, тем большее количество теплоты она получает от горелки.
Таким образом, для нагревания одной и той же массы разных веществ до одинаковой температуры требуется разное количество теплоты. Количество теплоты, необходимое для нагревания тела и, следовательно, его теплоемкость зависят от рода вещества, из которого состоит это тело.
Так, например, чтобы увеличить на $1°$С температуру воды массой $1$ кг, требуется количество теплоты, равное $4200$ Дж, а для нагревания на $1°$С такой же массы подсолнечного масла необходимо количество теплоты, равное $1700$ Дж.
Физическая величина, показывающая, какое количество теплоты требуется для нагревания $1$ кг вещества на $1°$С, называется удельной теплоемкостью этого вещества.
У каждого вещества своя удельная теплоемкость, которая обозначается латинской буквой $с$ и измеряется в джоулях на килограмм-градус (Дж/(кг$·°$С)).
Удельная теплоемкость одного и того же вещества в разных агрегатных состояниях (твердом, жидком и газообразном) различна. Например, удельная теплоемкость воды равна $4200$ Дж/(кг$·°$С), а удельная теплоемкость льда $2100$ Дж/(кг$·°$С); алюминий в твердом состоянии имеет удельную теплоемкость, равную $920$ Дж/(кг$·°$С), а в жидком — $1080$ Дж/(кг$·°$С).
Заметим, что вода имеет очень большую удельную теплоемкость. Поэтому вода в морях и океанах, нагреваясь летом, поглощает из воздуха большое количество тепла. Благодаря этому в тех местах, которые расположены вблизи больших водоемов, лето не бывает таким жарким, как в местах, удаленных от воды.
Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении
Из вышеизложенного ясно, что количество теплоты, необходимое для нагревания тела, зависит от рода вещества, из которого состоит тело (т. е. его удельной теплоемкости), и от массы тела. Ясно также, что количество теплоты зависит от того, на сколько градусов мы собираемся увеличить температуру тела.
Итак, чтобы определить количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость тела умножить на его массу и на разность между его конечной и начальной температурами:
$Q=cm(t_2-t_1)$
где $Q$ — количество теплоты, $c$ — удельная теплоемкость, $m$ — масса тела, $t_1$ — начальная температура, $t_2$ — конечная температура.
При нагревании тела $t_2 > t_1$ и, следовательно, $Q > 0$. При охлаждении тела $t_2 < t_1$ и, следовательно, $Q < 0$.
В случае, если известна теплоемкость всего тела $С, Q$ определяется по формуле
$Q=C(t_2-t_1)$
Удельная теплота парообразования, плавления, сгорания
Теплота парообразования (теплота испарения) — количество теплоты, которое необходимо сообщить веществу (при постоянном давлении и постоянной температуре) для полного превращения жидкого вещества в пар.
Теплота парообразования равна количеству теплоты, выделяющемуся при конденсации пара в жидкость.
Превращение жидкости в пар при постоянной температуре не ведет к увеличению кинетической энергии молекул, но сопровождается увеличением их потенциальной энергии, т. к. расстояние между молекулами существенно увеличивается.
Удельная теплота парообразования и конденсации. Опытами установлено, что для полного обращения в пар $1$ кг воды (при температуре кипения) необходимо затратить $2.3$ МДж энергии. Для обращения в пар других жидкостей требуется иное количество теплоты. Например, для спирта оно составляет $0.9$ МДж.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой $1$ кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой $r$ и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты, необходимое для парообразования (или выделяющееся при конденсации). Чтобы вычислить количество теплоты $Q$, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования $r$ умножить на массу $m$:
$Q=rm$
При конденсации пара происходит выделение такого же количества теплоты:
$Q=-rm$
Удельная теплота плавления
Теплота плавления — это количество теплоты, которое необходимо сообщить веществу при постоянном давлении и постоянной температуре, равной температуре плавления, чтобы полностью перевести его из твердого кристаллического состояния в жидкое.
Теплота плавления равна тому количеству теплоты, которое выделяется при кристаллизации вещества из жидкого состояния.
При плавлении вся подводимая к веществу теплота идет на увеличение потенциальной энергии его молекул. Кинетическая энергия не меняется, поскольку плавление идет при постоянной температуре.
Изучая на опыте плавление различных веществ одной и той же массы, можно заметить, что для превращения их в жидкость требуется разное количество теплоты. Например, для того чтобы расплавить один килограмм льда, нужно затратить $332$ Дж энергии, а для того чтобы расплавить $1$ кг свинца — $25$ кДж.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой $1$ кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления измеряют в джоулях на килограмм (Дж/кг) и обозначают греческой буквой $λ$ (лямбда).
Удельная теплота кристаллизации равна удельной теплоте плавления, поскольку при кристаллизации выделяется такое же количество теплоты, какое поглощается при плавлении. Так, например, при замерзании воды массой $1$ кг выделяются те же $332$ Дж энергии, которые нужны для превращения такой же массы льда в воду.
Чтобы найти количество теплоты, необходимое для плавления кристаллического тела произвольной массы, или теплоту плавления, надо удельную теплоту плавления этого тела умножить на его массу:
$Q=λm$
Количество теплоты, выделяемое телом, считается отрицательным. Поэтому при расчете количества теплоты, выделяющегося при кристаллизации вещества массой $m$, следует пользоваться той же формулой, но со знаком «минус»:
$-Q=λm$
Удельная теплота сгорания
Теплота сгорания (или теплотворная способность, калорийность) — это количество теплоты, выделяющейся при полном сгорании топлива.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива. Обычное топливо (уголь, нефть, бензин) содержит углерод. При горении атомы углерода соединяются с атомами кислорода, содержащегося в воздухе, в результате чего образуются молекулы углекислого газа. Кинетическая энергия этих молекул оказывается большей, чем у исходных частиц. Увеличение кинетической энергии молекул в процессе горения называют выделением энергии. Энергия, выделяющаяся при полном сгорании топлива, и есть теплота сгорания этого топлива.
Теплота сгорания топлива зависит от вида топлива и его массы. Чем больше масса топлива, тем больше количество теплоты, выделяющейся при его полном сгорании.
Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой $1$ кг, называется удельной теплотой сгорания топлива.
Удельную теплоту сгорания обозначают буквой $q$ и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты $Q$, выделяющееся при сгорании $m$ кг топлива, определяют по формуле:
$Q=qm$
Чтобы найти количество теплоты, выделяющееся при полном сгорании топлива произвольной массы, нужно удельную теплоту сгорания этого топлива умножить на его массу.
Уравнение теплового баланса
В замкнутой (изолированной от внешних тел) термодинамической системе изменение внутренней энергии какого-либо тела системы $∆U_i$ не может приводить к изменению внутренней энергии всей системы. Следовательно,
$∆U_1+∆U_2+∆U_3+…+∆U_n=∑↙{i}↖{n}∆U_i=0$
Если внутри системы не совершается работа никакими телами, то, согласно первому закону термодинамики, изменение внутренней энергии любого тела происходит только за счет обмена теплом с другими телами этой системы: $∆U_i=Q_i$. Учитывая ($∆U_1+∆U_2+∆U_3+…+∆U_n=∑↙{i}↖{n}∆U_i=0$), получим:
$Q_1+Q_2+Q_3+…+Q_n=∑↙{i}↖{n}Q_i=0$
Это уравнение называется уравнением теплового баланса. Здесь $Q_i$ — количество теплоты, полученное или отданное $i$-м телом. Любое из количеств теплоты $Q_i$ может означать теплоту, выделяемую или поглощаемую при плавлении какого-либо тела, сгорании топлива, испарении или конденсации пара, если такие процессы происходят с различными телами системы, и будут определятся соответствующими соотношениями.
Уравнение теплового баланса является математическим выражением закона сохранения энергии при теплообмене.
Внутренняя энергия сосредоточена «внутри» вещества и складывается из потенциальной энергии взаимодействующих молекул (атомов) и кинетической энергии их движения:
U=∑Ek0+∑Ep0
∑Ek0 — кинетическая энергия молекул (атомов), которая зависит от скорости их движения. Она изменяется только при изменении температуры. В процессе агрегатных переходов кинетическая энергия молекул остается неизменной.
∑Ep0 — потенциальная энергия взаимодействия молекул, которая зависит от расстояния между ними. Она изменяется при изменении температуры и объема. Например, в процессе агрегатных переходов изменяется именно потенциальная энергия молекул.
Способы изменения внутренней энергии:
- Совершение работы (за счет трения или ударов).
- Испарение (в процессе испарения внутренняя энергия жидкости понижается).
- Теплопередача (приведение в соприкосновение с более холодным или более нагретым телом).
Виды теплопередачи
Выделяют три вида теплопередачи: теплопроводность, конфекцию и излучение.
Теплопроводность
Определение
Теплопроводность — способность тел переносить внутреннюю энергию без переноса вещества от более нагретых участков тела к более холодным.
При теплопроводности происходит постепенное увеличение скорости движения молекул. Это возможно только благодаря межмолекулярному взаимодействию. Поэтому теплопроводность в твердых телах происходит быстрее, чем в жидкостях. В газах она осуществляется еще медленнее. Для сохранения тепла используют пористые материалы, в которых много воздуха. Воздух — это смесь газов, поэтому он плохо переводит тепло.
Важно! В вакууме теплопроводность невозможна.
Конвекция
Определение
Конвекция — это перенос внутренней энергии, сопровождающийся переносом вещества.
При конвекции теплые слои жидкости или газа поднимаются, а холодные опускаются. Конвекция осуществляется только в жидкостях и газах.
Важно! В твердых телах и в вакууме конвекция невозможна.
Излучение
Определение
Излучение — это перенос теплоты в пространстве, осуществляемый в результате распространения электромагнитных волн, энергия которых при взаимодействии с веществом переходит в тепло.
Энергию излучают все нагретые тела. Чем больше нагрето тело, тем сильнее излучение. Теплопередача за счет излучения возможна в любой среде, в том числе и в вакууме.
Темные поверхности хорошо поглощают излучение, но быстро отдают энергию при охлаждении. Зеркальные и светлые поверхности отражают часть излучения и медленно остывают.
Количество теплоты
Определение
Количество теплоты Q (Дж) — физическая величина, которая показывает, на сколько изменяется внутренняя энергия вещества в процессе теплопередачи:
Q=±U
Если внутренняя энергия вещества увеличивается, то Q > 0. Это происходит при нагревании, плавлении и кипении.
Если внутренняя энергия вещества уменьшается, Q < 0. Это происходит при охлаждении, отвердевании и конденсации.
Нагревание и охлаждение вещества
Формула теплоты при нагревании или охлаждении
При нагревании или охлаждении вещество получает (отдает) количество теплоты, определяемое по формуле:
Q=cmΔt=cm(t−t0)
∆t — изменение температуры вещества (в оС или К), t0 — начальная температура вещества, t — конечная температура вещества, m — его масса (кг), c — удельная теплоемкость вещества (Дж/(кг∙К)).
Удельная теплоемкость вещества показывает, какое количество теплоты необходимо затратить, чтобы нагреть 1 кг вещества на 1 градус. Такое же количество теплоты выделится при охлаждении 1 кг этого вещества на 1 градус.
Внимание! Удельная теплоемкость вещества — табличная величина.
Количество теплоты также определяется формулой:
Q=CΔT
∆T — изменение температуры в Кельвинах, а C — теплоемкость вещества.
Теплоемкость вещества показывает, сколько теплоты поглощает тело при нагревании на 1 К. Измеряется в Дж/кг. Численно теплоемкость равна произведению массы вещества на его удельную теплоемкость:
C=cm
Пример №1. Температура медного образца массой 100 г увеличилась на 40 оС. Какое количество теплоты получил образец? Удельная теплоемкость меди равна 380 Дж/(кг∙К).
100 г = 0,1 кг
Q=cmΔt=380·0,1·40=1520 (Дж)
Сгорание топлива
Формула теплоты при сгорании топлива
При сгорании топлива выделяется количество теплоты, определяемое формулой:
Q=qm
m — масса сгоревшего топлива (кг), q — удельная теплота сгорания топлива (Дж/кг).
Удельная теплота сгорания показывает, какое количество теплоты выделяется при полном сгорании 1 кг данного вида топлива.
Внимание! Удельная теплота сгорания — табличная величина.
Пример №2. Сгорело 5 сухих березовых поленьев. Каждый весил 1 кг. Определить, количество выделенной теплоты, если удельная теплота сгорания березовых дров составляет 15 МДж/кг.
15МДж = 15∙109 Дж
Так как сгорело 5 поленьев по 1 кг, то всего сгорело 5 кг сухих березовых дров. Отсюда:
Q=qm=5·15·109=75·109 (Дж)=75 (МДж)
Задание EF17492
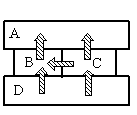 Четыре металлических бруска положили вплотную друг к другу, как показано на рисунке. Стрелки указывают направление теплопередачи от бруска к бруску. Температуры брусков в данный момент 100°С, 80°С, 60°С, 40°С. Температуру 40°С имеет брусок
Четыре металлических бруска положили вплотную друг к другу, как показано на рисунке. Стрелки указывают направление теплопередачи от бруска к бруску. Температуры брусков в данный момент 100°С, 80°С, 60°С, 40°С. Температуру 40°С имеет брусок
- A
- B
- C
- D
Алгоритм решения
- Определить тип теплопередачи.
- Вспомнить, как происходит этот тип теплопередачи.
- Сделав анализ рисунка, установить, какой брусок имеет указанную в задаче температуру.
Решение
Так как это твердые тела, поверхности которых соприкасаются друг с другом, и перенос тепла происходит без переноса вещества, то этот вид теплопередачи является теплопроводностью. Тепло всегда направлено от более нагретого тела к менее нагретому.
На рисунке видно, что самым нагретым телом является нижний брусок, так как он только отдает тепло, но не принимает его. Средний брусок справа менее нагрет, чем нижний, так как принимает от него тепло. Но он более теплый по сравнению со средним бруском слева, так как он делится с ним теплом. И оба этих бруска отдают свою энергию верхнему бруску, который сам только принимает тепло, но не отдает его. Следовательно, именно он имеет температуру +40 оС.
Ответ: A
pазбирался: Алиса Никитина | обсудить разбор
Задание EF17563
Какую массу воды можно нагреть до кипения при сжигании в костре 1,8 кг сухих дров, если в окружающую среду рассеивается 95% тепла от их сжигания? Начальная температура воды 10 оС, удельная теплота сгорания сухих дров λ = 8,3 ⋅ 106 Дж/кг.
Алгоритм решения
1.Записать исходные данные.
2.Записать формулу для расчета количества теплоты, необходимого для нагревания вещества.
3.Записать формулу для расчета количества теплоты, выделенного при сгорании топлива.
5.Подставить известные данные и произвести вычисления.
Решение
Запишем исходные данные:
• Начальная температура воды: t0 = 10 oC.
• Конечная температура воды: tкип = 100 oC.
• Масса дров: mд = 1,8 кг.
• Удельная теплота сгорания дров: λ = 8,3∙106 Дж/кг.
• Удельная теплоемкость воды: c = 4200 Дж/(кг∙К).
Вода при нагревании до температуры кипения получит следующее количество теплоты:
Q1=cmв(tкип−t0)
При полном сгорании дров выделится следующее количество теплоты:
Q2=λmд
Так как в окружающую среду выделится 95% тепла, то вода получит лишь 5%. Следовательно:
Q1=0,05Q2
Отсюда:
cmв(tкип−t0)=0,05λmд
mв=0,05λmдc(tкип−t0)
mв=0,05·8,3·106·1,84200(100−10)≈1,98 (кг)
Округлим ответ до целых и получим 2 кг воды.
Ответ: 2
pазбирался: Алиса Никитина | обсудить разбор
Задание EF17701
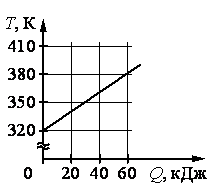 На рисунке изображён график зависимости температуры тела от подводимого к нему количества теплоты. Удельная теплоёмкость вещества этого тела равна 500 Дж/(кг⋅К). Чему равна масса тела?
На рисунке изображён график зависимости температуры тела от подводимого к нему количества теплоты. Удельная теплоёмкость вещества этого тела равна 500 Дж/(кг⋅К). Чему равна масса тела?
Ответ:
а) 1 кг
б) 2 кг
в) 3 кг
г) 4 кг
Алгоритм решения
1.Записать исходные данные и перевести единицы измерения величин в СИ.
2.По графику определить начальную температуру вещества.
3.Выбрать любую точку графика для определения количества теплоты и конечной температуры вещества.
4.Записать количество теплоты, которое получает тело при нагревании.
5.Выполнить решение в общем виде.
6.Вычислить массу, подставив данные, полученные из графика.
Решение
Запишем исходные данные и те данные, что получится выделить из графика:
• Удельная теплоемкость вещества: c = 500 Дж/(кг∙К).
• Начальная температура вещества: t0 = 320 К.
• Конечная температура вещества: t = 380 К.
• Количество полученной теплоты: Q = 60 кДж.
60 кДж = 60∙103 Дж
Количество теплоты вычисляется по формуле:
Q=cm(t−t0)
Отсюда масса вещества равна:
m=Qc(t−t0)=60·103500(380−320)=2 (кг)
Ответ: б
pазбирался: Алиса Никитина | обсудить разбор
Алиса Никитина | Просмотров: 4k
2017-08-04 ![]()
Какое количество теплоты получает одноатомный газ при нагревании в ходе процесса, изображенного на рисунке? Получает или отдает тепло газ при охлаждении? Чему равно это количество теплоты?

Решение:

Газ сначала нагревается от температуры $T_{1} = frac{2p_{0}V_{0}}{ nu R}$ до температуры $T_{3} = frac{9}{8} T_{1}$ (точка 3 на рисунке с координатами $V_{3} = frac{3}{2}V_{0}$ и $p_{3} = frac{3}{2}p_{0}$), а затем охлаждается от $T_{3}$ до $T_{2} = T_{1}$. На обоих этапах (1-3 и 3-2) газ, расширяясь, совершает работу. Работу на каждом этапе нетрудно определить как площадь соответствующей трапеции:
$A_{1-3}^{ prime} = frac{2p_{0} + 1,5p_{0}}{2} frac{V_{0}}{2} = 0,875 p_{0} V_{0}$;
$A_{3-2}^{ prime} = frac{1,5p_{0} + p_{0}}{2} frac{V_{0}}{2} = 0,625 p_{0} V_{0}$;
Изменение внутренней энергии одноатомного газа задается выражением $Delta U = frac{3}{2} nu R Delta T$, значит,
$Delta U_{1-3} = frac{3}{2} nu R (T_{3} – T_{1}) = frac{3}{16} nu RT_{1} = frac{3}{8} p_{0} V_{0}$;
$Delta U_{3-2} = frac{3}{2} nu R (T_{2} – T_{3}) = – frac{3}{8} p_{0}V_{0}$.
Мы воспользовались здесь уравнением Менделеева-Клапейрона $2p_{0}V_{0} = nu RT_{1}$. Остается лишь применить первый закон термодинамики:
$Q_{1-3} = Delta U_{1-3} + Delta U_{1-3}^{ prime} = l,25p_{0}V_{0}; Q_{3-2} = Delta U_{3-2} + A_{3-2}^{ prime} = 0,25 p_{0} V_{0}$.
Нетрудно проверить, что $Q_{1-2} = Q_{1-3} + Q_{3-2} = A_{1-3}^{ prime}$. Ведь полное изменение внутренней энергии в ходе процессе равно нулю (точки 1 и 2 лежат на одной изотерме).
Обратите внимание: газ получает теплоту при охлаждении] Ничего удивительного в этом нет: просто газ расширяется настолько быстро, что подводимой к нему теплоты недостаточно для совершения работы и газу «приходится» отдавать часть своей внутренней энергии. Заметим, что теплоемкость газа в этом процессе отрицательна (см. задачу 4001).
Ответ: $l,25 p_{0} V_{0}$; при охлаждении газ получает количество теплоты, равное $0,25p_{0}V_{0}$.
