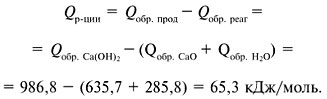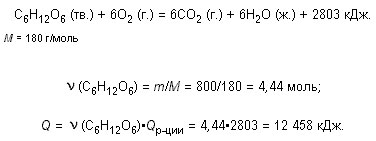ЭЛЕМЕНТЫ ТЕРМОХИМИИ
Термохимия – раздел химии, в котором рассматриваются тепловые явления, происходящие в процессе химических реакций.
Нужен репетитор по химии? Записывайтесь на занятия в каталоге TutorOnline!
Все химические реакции можно разделить на два типа: реакции, идущие с выделением теплоты, их называют экзотермические, и реакции, идущие с поглощением теплоты эндотермические. Критерием таких процессов является тепловой эффект реакции.
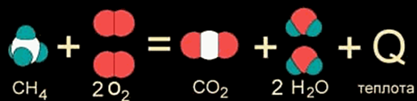
Как правило, к экзотермическим реакциям относятся реакции окисления, т.е. взаимодействия с кислородом, например сгорание метана
СН4 + 2O2 = СО2 + 2Н2О + Q (1)
а к эндотермическим реакциям – реакции разложения. Знак Q в конце уравнения указывает на то, выделяется ли теплота в процессе реакции (+ Q) или поглощается (- Q):
СаCO3 = СаO + CO2 -Q (2)
При химических процессах может выделяться или поглощаться не только тепловая, но и другие виды энергии: электрическая, световая, механическая и др.
Тепловые эффекты прямой и обратной реакций одинаковы по числу, но противоположны по знаку, например, оксид кальция (СаО) при взаимодействии с водой образует гидроксид кальция (Са(ОН)2). Процесс сопровождается выделением большого количества теплоты:
СаО + Н2О = Са(ОН) + 108 кДж (3)
А реакция разложения гидроксида кальция (Са(ОН)2) осуществляется с поглощением такого же количества теплоты извне
Са(ОН)2 = СаО + Н2О – 108 кДж (4)
Если тепловой эффект реакции определяется при постоянном давлении, температуре, то он будет соответствовать стандартной энтальпии реакции, обозначаемой ∆Н, которая противоположна по знаку величине теплового эффекта реакции. Например, если в процессе экзотермической реакции во взаимодействие вступают алюминий (Аl) и оксид железа (Fe2O3), то в конце уравнения это обозначится следующим образом:
2Аl + Fe2O3 = 2Fe + Al2O3 (+Q) или (-∆Н) (5)
А в случае эндотермической реакции значения этих тепловых величин будут иметь противоположные знаки:
С + СО2 = 2СО (-Q) или (+∆Н) (6)
Это объясняется тем, что выделяющаяся в процессе экзотермической реакции теплота как энергия, теряется системой (-∆Н), а при эндотермических процессах, наоборот – приобретается (+∆Н). Величина (Н) называется энтальпией системы. Часто её называют так же теплосодержанием или теплотой образования ∆Н данного вещества. В расчётах применяют справочные значения тепловых эффектов образования (или сгорания) одного моля вещества, отнесённые к 298К (250С) и Р = 101,325 кПа (1 атм). Эти условия считаются стандартными и поэтому используемые значения тепловых эффектов называют стандартными теплотами образования(или сгорания) вещества и обозначают как ∆Н0298. Например, тепловой эффект реакции взаимодействия графита с кислородом, выраженный через изменение энтальпии, следует записать как ∆Н0298 = – 393,6 кДж, а так как при этом из простых веществ образуется 1 моль СО2, то данный тепловой эффект является теплотой образования СО2, выраженной в кДж/моль. Главной характеристикой топлив являются их теплоты сгорания. Тепловой эффект реакции горения одного моля вещества называется теплотой сгорания данного вещества. Следовательно, исходя из вышеприведённых положений, теплота сгорания одного моля графита (12 г) составляет 393,6 кДж/моль.
Уравнение химической реакции, в котором указан тепловой эффект, называется термохимическим уравнением.
На практике это имеет большое значение. При строительстве тепловых трасс, доменных печей, котельных и т.п. теплотопотребляющих промышленных объектов, необходимо предусмотреть или приток энергии для поддержания процессов, или наоборот, отвод избытка теплоты, чтобы не было перегрева вплоть до взрыв
Расчёт теплового эффекта реакции между простыми веществами не предоставляется затруднительным. Например, для реакции образования хлористого водорода:
Н2 + Cl2 = 2НCl (7)
Энергия затрачивается на разрыв двух химических связей Н–Н и Cl – Cl. При этом энергия выделяется при образовании двух химических связей Н- Cl. Значения энергий этих связей можно найти в справочных таблицах и по разности между ними определить тепловой эффект (Q) реакции (7):
ЕН–Н = 436 кДж/моль, ЕCl–Cl = 240 кДж/моль,
ЕН–Cl = 240 кДж/моль,
Q = 2 х 430 – ( 1 х 436 – 1 х 240 ) = 184 кДж.
Приведённая в качестве примера термохимическая реакция (7) является экзотермической. Теплоты образования простых веществ при стандартных условиях приняты равными нулю.
Термохимические уравнения имеют особую форму записи. Они отличаются от обычных уравнений тем, что:
1). В термохимических уравнениях обязательно указывают агрегатные состояния веществ (жидкое, твёрдое, газообразное) Это связано с тем, что одна и та же реакция может иметь различный тепловой эффект в зависимости от фазового состояния вещества
2). Коэффициенты в термохимическом уравнении равны количеству веществ ( в молях), вступивших в реакцию. Например, дана реакция сгорания ацетилена:
2С2Н2(г) + 5О2(г) = 4СО2(г) + 2Н2О (+Q) (8)
При сгорании одного моль ацетилена С2Н2 выделяется 1257кДж теплоты. Поэтому, относительно одного моль С2Н2 необходимо все коэффициенты перед реагентами поделить на 2, тогда получим следующую запись термохимического уравнения:
С2Н2 + 5/2О2 = 2СО2 + Н2О + 1257 кДж (9)
Или другая тождественная запись:
С2Н2 + 2,5О2 = 2СО2 + Н2О + 1257 кДж (10)
Например, дано термохимическое уравнение сгорания метана:
СН4 + 2О2 = СО2 + 2Н2О + 802 кДж (11)
Необходимо вычислить, какое количество теплоты выделится при сгорании 20 г метана?
Поскольку 1 моль метана имеет массу 16 г, а 20 г метана соответственно составляют
n = m/Mr = 20:12 = 1,25 моль,
то, составив пропорцию: при сгорании
1 моль СН4 выделяется 802 кДж теплоты
1,25 СН4 ——–«——-Х кДж теплоты
Определим, что на сгорание 20г метана потребуется
Х = 1,25 х 802 / 1 = 1002,5 кДж
Приведём другой пример . Дано уравнение реакции сгорания оксида азота(+4):
4NО2(г) + O2(г) + 2H2O(г) = 4НNО3(ж) + 448 кДж (12)
Необходимо составить термохимическое уравнение относительно сгорания одного моль оксида азота. Определить: какой объём оксида азота потребуется на образование 4258 кДж теплоты в процессе данной реакции?
Для составления термохимического уравнения относительно одного моль оксида азота(+4) необходимо все коэффициенты, стоящие перед реагентами, разделить на коэффициент, стоящий перед NО2, т.е. на «4», тогда уравнение примет вид:
NО2(г) + 1/4O2(г) + 1/2H2O(г) = НNО3(ж) +112 кДж (13)
В уравнении изменится количество выделяющейся теплоты, оно станет равным 112, т.е. в четыре раза меньше, чем в приведённом уравнении. В соответствии с уравнением (13) 1 моль оксида азота(NО2) или 22,4 л в данной реакции образует 112 кДж теплоты, а Х л соответственно 4258 кДж:
22,4 моль NО2 при сгорании образуют 112 кДж теплоты.
Х л —————-«————-4258 кДж теплоты.
Хг = 22,4 х 4258 / 112 = 851,6 кДж
Важнейшим законом термохимии является закон Г.И.Гесса (1840): тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса. При помощи закона Гесса можно рассчитывать такие тепловые эффекты реакции, которые измерить трудно или невозможно. Например, теплоту образования угарного газа(СО) можно вычислить, если полное сгорание углерода
С (графит) + О2 = СО2 (∆Н1) (14)
разбить на стадии:
С (графит) + 0,5О2 = СО (∆Н2) (15)
СО + 0,5О2 = СО2 (∆Н3) (16)
Зная, что ∆Н1 = -393,6 кДж/моль и ∆Н3 = – 283,1 кДж/моль, из равенства ∆Н1 = ∆Н2 + ∆Н3
находим, что ∆Н2 = – 110,5 кДж/моль.
В качестве другого примера можно привести образование сульфата алюминия при сгорании алюминия и серы ромбической согласно реакции:
2Al(к) + 3S(ромб) + 6О2(г) = Al2(SO4)3(к) (17)
∆Н может быть найдена по тепловым эффектам отдельных стадий:
2Al + 1,5О2 = Al2O3 ∆Н1= -1670,2 кДж/моль (18)
3S + 1,5О2 = SO3 ∆Н2= -395,3 кДж/моль (19)
Al2O3 + 3SO3 = Al2(SO4)3 ∆Н3= -579,7 кДж/моль (20)
Тогда ∆Н = ∆Н1 + 3∆Н2 + ∆Н3 = (- 1670,2) – 3х (-395,3) – (579,7) = – 3435,8 кДж/моль.
На основании закона Гесса термохимические уравнения можно разбивать на отдельные стадии независимо от того, осуществимы они на практике или нет. Из закона Гесса вытекает важное следствие: тепловой эффект химической реакции равен сумме теплот образования получающихся веществ за вычетом суммы теплот образования исходный веществ:
∆Н = ∑ (𝘮 ∆Н) продукты – ∑ (𝘯 ∆Н) реагенты,
где 𝘮 и 𝘯 – число молей каждого вещества в уравнении реакции. Например, теплоту сгорания ацетилена (10) можно рассчитать, зная теплоты образования С2Н2 , СО2 и Н2О (∆Н002 = 0), как ∆Н0 = 2 ∆Н СО2 + ∆НН2О – ∆НС2Н2 = -2 х 393,6 – 281 – (+226,8) = -1295 кДж/моль.
НАЧАЛА ТЕРМОДИНАМИКИ
Среди многообразия химических реакций, термохимические занимают особое положение. Если рассуждать с точки зрения эволюции жизни на Земле, то в конечном итоге, действительно, от этих процессов зависит жизнь на нашей планете. А что касается человеческой цивилизации в целом, то здесь мы имеем прямую зависимость её развития от термохимических явлений. Ведь благодаря именно данным процессам произошёл отрыв человечества в развитии от всех других видов живых организмов, населяющих нашу планету. С древнейших времён, начиная от пассивного использования огня в качестве средства для согревания и приготовления примитивной пищи, человечество пришло к активному использованию этого явления (изготовление гончарных изделий – плавка меди, железа и других металлов – паровые двигатели – двигатели внутреннего сгорания – управление ядерными реакциями)
Если можно было бы предложить создать проект монумента человеческому прогрессу, то на его фронтоне надо было бы начертать уравнение химической реакции
С + О2 = СО2
Именно со сгорания дров, угля, торфа начался отсчёт человеческой цивилизации. В настоящее время наше с вами существование просто немыслимо без тепловых процесов. Но кроме приведённой выше реакции существует великое множество других термодинамических процессов. Почему именно углероду дано такое предпочтение? Может быть его собрату по IV-й группе – кремнию более выгоден данный процесс?
Si + О2 = SiО2
Тем более, что кремний по массе составляет 27,6% земной коры. Это несравненно больше, чем запасы древесины и её ископаемых на нашей планете. Чего же проще? Кидай в топку кремнезём! Его ведь целая планета! Правда надо оговорить тот факт, что чистого кремния в природе не существует. В наличии только его оксид – SiО2. Но на то и химики, чтобы придумать что-нибудь? А может быть для более сильного окислителя, чем кислород – фтору окисление углерода более выгодно термодинамически?
C + 2F2 = СF4
Как во всём этом разобраться? И возможно ли вообще предсказать осуществления того или иного процесса, ведь на бумаге можно написать уравнение любой химической реакции, а возможна ли она практически? Придётся начинать всё по порядку.
Одним из самых важных и очевидных законов природы является закон сохранения энергии: энергия не возникает из ничего и не исчезает бесследно, она только переходит из одной формы в другую. Аналогичным является закон сохранения массы вещества: массы веществ вступивших в реакцию равны массам веществ, образовавшихся в процессе данной реакции.
Поэтому и при экзотермической и при эндотермической обратимых реакциях одного и того же процесса как количество затрачиваемой и расходуемой энергии равны, но противоположны по знаку, так и массы веществ распадающихся и вновь образующихся равны:
СаО + Н2О = Са(ОН)2 + 108 кДж
Mr=56 Mr=18 Mr=74
Са(ОН)2 = СаО + Н2О – 108 кДж
Mr=74 Mr=56 Mr=18
Но всё дело в том, что в приведённых выше двух реакциях уже указано, какая из них экзотермическая, а какая эндотермическая. А можно ли так, как говорится «на вскидку» по одному только уравнению реакции определить: какая это реакция? В принципе, в большинстве случаев, возможно. К экзотермическим реакциям, в основном, относятся реакции соединения и как их разновидность – реакции окисления.(8,11,12,14). А к реакциям эндотермическим, соответственно – реакции разложения (2,4). Ещё раз уточним: в большинстве случаев. Поскольку реакция окисления:
0,5N2 + 0,5O2 = NО – 90 кДж
требует расхода энергии и является эндотермической, а реакция разложения нитрата натрия
2NaNO3 = 2NaNO2 + O2 (+Q)
осуществляется с выделением большого количества теплоты и является экзотермической.
Значит, принцип «на вскидку» не годится. Но каким же принципом тогда следует руководствоваться в определении реакций данного типа? В приводимых выше примерах (10), (14-20) указывалось, что стандартные теплоты образования веществ (∆Н) являются справочными данными. Такие данные скрупулёзно составлялись на протяжении десятилетий для многочисленных термодинамических реакций. С этой целью использовался прибор калориметр. Именно по этим данным в настоящее время мы можем установить, какой является та или иная реакция: экзотермической или эндотермической.
Теперь попробуем заглянуть как бы внутрь термохимической реакции. Как она начинается? Что способствует её осуществлению? В качестве примера приведём ещё раз две реакции (14) и (2):
С(графит) + О2 = СО2 + 393,3 кДж
СаСО3 = СаО + СО2 (-Q)
Представим себе, что химическими символами (С) и (О2) будут обозначаться не элемент «углерод» и простое вещество «кислород», а дрова (или уголь, торф) и воздух (атмосфера). А в качестве соединения СаСО3 – не карбонат кальция, а известное всем вещество: мел (или известняк). Первую реакцию будем проводить для того, чтобы нагреть печь и вскипятить чайник, а вторую – чтобы получить негашёную известь (СаО) в дальнейшем используемую для побелки садовых деревьев. Для разжигания печи приготовим щепки и, поместив сверху них дрова, зажжём огонь спичками.
Во втором случае, поместим в металлическое ведро мелко накрошенный мел, поставим на плиту и такими же действиями, как в случае разжигания огня в печи, разведём костёр под ведром.
Стоп! Тут что-то не так! Ведь мы установили, что первая реакция экзотермическая, протекает с выделением теплоты, а вторая реакция – эндотермическая, протекает с поглощением теплоты. А мы в обоих случаях разводим огонь, т.е. передаём этим процессам извне тепловую энергию. Значит, обе реакции эндотермические – идут с поглощением теплоты! Да, идут с поглощением теплоты, но это только на первом этапе. Некоторым экзотермическим реакциям требуется небольшой «толчок» – первоначальная подача энергии, а спустя некоторое время, когда загорятся дрова, процесс будет сопровождаться с выделением энергии в окружающую среду и во многие сотни, тысячи раз превзойдёт по величине первоначальное значение этой энергии. А второй процесс ка был так и останется эндотермическим. Ведь с прекращением подачи тепловой энергии мел перестанет разлагаться: реакция остановится. И всё-таки, почему в одних случаях процесс окисления (горения) является экзотермическим, а в других – эндотермическим процессом? И что является движущей силой эндотермических реакций, в ходе которых тепловая энергия поступает из окружающей среды? Ни у кого не вызывает удивление такое явление, как остывание со временем горячего чайника. Это нормально. А почему бы этому же чайнику, уже остывшему, холодному, взять, да и нагреться самому по себе? Вот это уже вызовет удивление.
Так вот, эта самая сила связана со стремлением любой системы к наиболее вероятному состоянию, характеризующимся максимальным беспорядком, называемым энтропией. Это одно из важнейших понятий в термодинамике. Энтропия обозначается символом «S». К примеру, при экзотермических реакциях, при проведении процессов плавления, кипения, переходов из жидкостей к газообразному состоянию, энтропия приобретает максимальное значение, поскольку при тепловых явлениях кинетическая энергия атомов, молекул, ионов возрастает, усиливаются беспорядочные колебания этих частиц. И наоборот, самый большой порядок в химических системах – в идеальном кристалле при температуре абсолютного нуля. Энтропия в данном случае равна нулю
Энтропия имеет численные значения, единицей её измерения является Дж/(моль . К); К примеру энтропия алмаза равна 2,4 Дж/(моль . К), пропана – 269,9 Дж/(моль . К). Энтропия газов значительно превышает энтропию жидких и тем более твёрдых тел. Поскольку в газообразных веществах постоянно происходит беспорядочное распределение молекул по всему объёму.
Существуют экспериментальные и теоретические методы определения энтропий различных химических соединений. Используя их, можно количественно рассчитать изменения энтропии при протекании конкретной реакции аналогично тому, как это делается для теплового эффекта реакции. Составлены специальные справочные данные, которые включают сравнительную характеристику этих величин с учётом температуры.
Подтянуть знания по химии можно записавшись на урок к онлайн-репетиторам TutorOnline
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Тепловой эффект химической реакции. Термохимические уравнения. Расчеты теплового эффекта реакции.
Любая химическая реакция сопровождается выделением или поглощением энергии в виде теплоты.
По признаку выделения или поглощения теплоты различают экзотермические и эндотермические реакции.
Экзотермические реакции – такие реакции, в ходе которых тепло выделяется (+Q).
Эндотермические реакции – реакции, при протекании которых тепло поглощается (-Q).
Тепловым эффектом реакции (Q) называют количество теплоты, которое выделяется или поглощается при взаимодействии определенного количества исходных реагентов.
Термохимическим уравнением называют уравнение, в котором указан тепловой эффект химической реакции. Так, например, термохимическими являются уравнения:
Также следует отметить, что термохимические уравнения в обязательном порядке должны включать информацию об агрегатных состояниях реагентов и продуктов, поскольку от этого зависит значение теплового эффекта.
Расчеты теплового эффекта реакции
Пример типовой задачи на нахождение теплового эффекта реакции:
При взаимодействии 45 г глюкозы с избытком кислорода в соответствии с уравнением
C6H12O6(тв.) + 6O2(г) = 6CO2(г) + 6H2O(г) + Q
выделилось 700 кДж теплоты. Определите тепловой эффект реакции. (Запишите число с точностью до целых.)
Решение:
Рассчитаем количество вещества глюкозы:
n(C6H12O6) = m(C6H12O6) / M(C6H12O6) = 45 г / 180 г/моль = 0,25 моль
Т.е. при взаимодействии 0,25 моль глюкозы с кислородом выделяется 700 кДж теплоты. Из представленного в условии термохимического уравнения следует, что при взаимодействии 1 моль глюкозы с кислородом образуется количество теплоты, равное Q (тепловой эффект реакции). Тогда верна следующая пропорция:
0,25 моль глюкозы — 700 кДж
1 моль глюкозы — Q
Из этой пропорции следует соответствующее ей уравнение:
0,25 / 1 = 700 / Q
Решая которое, находим, что:
Q = 2800 кДж
Таким образом, тепловой эффект реакции составляет 2800 кДж.
Расчёты по термохимическим уравнениям
Намного чаще в заданиях ЕГЭ по термохимии значение теплового эффекта уже известно, т.к. в условии дается полное термохимическое уравнение.
Рассчитать в таком случае требуется либо количество теплоты, выделяющееся/поглощающееся при известном количестве реагента или продукта, либо же, наоборот, по известному значению теплоты требуется определить массу, объем или количество вещества какого-либо фигуранта реакции.
Пример 1
В соответствии с термохимическим уравнением реакции
3Fe3O4(тв.) + 8Al(тв.) = 9Fe(тв.) + 4Al2O3(тв.) + 3330 кДж
образовалось 68 г оксида алюминия. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Решение
Рассчитаем количество вещества оксида алюминия:
n(Al2O3) = m(Al2O3) / M(Al2O3) = 68 г / 102 г/моль = 0,667 моль
В соответствии с термохимическим уравнением реакции при образовании 4 моль оксида алюминия выделяется 3330 кДж. В нашем же случае образуется 0,6667 моль оксида алюминия. Обозначив количество теплоты, выделившейся при этом, через x кДж составим пропорцию:
4 моль Al2O3 — 3330 кДж
0,667 моль Al2O3 — x кДж
Данной пропорции соответствует уравнение:
4 / 0,667 = 3330 / x
Решая которое, находим, что x = 555 кДж
Т.е. при образовании 68 г оксида алюминия в соответствии с термохимическим уравнением в условии выделяется 555 кДж теплоты.
Пример 2
В результате реакции, термохимическое уравнение которой
4FeS2(тв.) + 11O2(г) = 8SO2(г) + 2Fe2O3(тв.) + 3310 кДж
выделилось 1655 кДж теплоты. Определите объем (л) выделившегося диоксида серы (н.у.). (Запишите число с точностью до целых.)
Решение
В соответствии с термохимическим уравнением реакции при образовании 8 моль SO2 выделяется 3310 кДж теплоты. В нашем же случае выделилось 1655 кДж теплоты. Пусть количество вещества SO2, образовавшегося при этом, равняется x моль. Тогда справедливой является следующая пропорция:
8 моль SO2 — 3310 кДж
x моль SO2 — 1655 кДж
Из которой следует уравнение:
8 / х = 3310 / 1655
Решая которое, находим, что:
x = 4 моль
Таким образом, количество вещества SO2, образовавшееся при этом, составляет 4 моль. Следовательно, его объем равен:
V(SO2) = Vm ∙ n(SO2) = 22,4 л/моль ∙ 4 моль = 89,6 л ≈ 90 л (округляем до целых, т.к. это требуется в условии.)
Больше разобранных задач на тепловой эффект химической реакции можно найти здесь.
Приветствую вас, уважаемые читатели, на своем канале!
В данной статье разберем вопрос 27 – расчеты теплового эффекта (по термохимическим уравнениям).
Теорию по данному заданию можно посмотреть здесь.
Данное задание не претерпело изменений. Рассмотрим пять примеров.
Пример 1 (из демонстрационного варианта ЕГЭ 2022)
Синтез аммиака протекает в соответствии с термохимических уравнением реакции:
N2(г) + 3H2(г) = 2NH3(г) + 92 кДж.
Определите количество теплоты, которое выделится в результате образования 560 мл (н.у.) газообразного аммиака. (Запишите число с точностью до сотых.)
Решение
1) Перепишем уравнение реакции, укажем мольное соотношение и тепловой эффект по реакции:
2) Переведем объем в литры – 0,56 л, количество теплоты обозначим за Q. Все эти данные подпишем над уравнением реакции:
3) Так как известен объем аммиака (NH3), то по реакции объем равен: 2*22,4:
4) Составим пропорцию и решим ее:
0,56/44,8 = Q/92
Q = 1,15 кДж.
Ответ: 1,15
Пример 2 (авторы: Е.А. Дацук и A.А. Степенин 2022)
В реакцию, термохимическое уравнение которой
C2H5OH(ж) + 3O2(г) = 2CO2(г) + 3H2O(ж) + 1374 кДж,
вступило 16,1 г этанола. Вычислите количество выделившейся при этом теплоты (в кДж). Ответ запишите с точностью до десятых.
Решение
1) Перепишем уравнение реакции, укажем мольное соотношение и тепловой эффект по реакции:
2) Масса этанола (С2H5OH) равна 16,1 г; количество теплоты обозначим за Q. Все эти данные подпишем над уравнением реакции:
3) Так как известна масса этанола (С2H5OH), то по реакции масса равна: 1*46:
4) Составим пропорцию и решим ее:
16,1/46 = Q/1374
Q = 480,9 кДж.
Ответ: 480,9
Пример 3 (авторы: Е.А. Дацук и A.А. Степенин 2022)
Теплота образования оксида алюминия из простых веществ составляет 1676 кДж/моль. Вычислите объем кислорода (при н.у.), вступивший в реакцию с алюминием, если в результате получено 502,8 кДж тепла. Ответ запишите с точностью до сотых.
Решение
1) Запишем уравнение реакции и укажем тепловой эффект реакции:
Откуда взялось число 3352? В условии сказано, что для 1-го моль оксида алюминия теплота составляет 1676 кДж, соответственно, для 2-х моль – 3352 кДж.
2) Объем кислорода (O2) обозначим за V, теплота равна 502,8 кДж. Все эти данные подпишем над уравнением реакции:
3) Необходимо найти объем кислорода (O2), поэтому по реакции объем равен: 3*22,4:
4) Составим пропорцию и решим ее:
V/67,2 = 502,8/3352
V = 10,08 л.
Ответ: 10,08
Пример 4 (автор: Ю. Н. Медведев 2022)
Определите тепловой эффект реакции
2С2H2 + 5O2 = 4CO2 + 2H2O + Q,
если известно, что при сгорании 3,36 л (при н.у.) ацетилена выделяется 195,75 кДж теплоты. (Запишите число с точностью до целых.)
Решение
1) Перепишем уравнение реакции, укажем мольное соотношение и тепловой эффект по реакции:
Тепловой эффект – неизвестный параметр, который необходимо найти.
2) Известен объем ацетилена (С2H2) 3,36 л и теплота 195,75 кДж. Все эти данные подпишем над уравнением реакции:
3) Так как известен объем ацетилена (С2H2), то объем по реакции равен: 2*22,4:
4) Составим пропорцию и решим ее:
3,36/44,8 = 195,75/Q
Q = 2610 кДж.
Ответ: 2610
Пример 5 (авторы: С.И. Широкопояс и И.С. Борисов 2022)
При сгорании навески неизвестного органического вещества выделяется 560 кДж теплоты и образуется 60 л углекислого газа. Вычислите количество теплоты, выделяющееся при образовании 108 л углекислого газа в тех же условиях. (Запишите ответ с точностью до целых)
Решение
Данную задачу можно решить через пропорцию без уравнения реакции, так как даны одинаковые условия.
Составим пропорцию:
60 л – 560 кДж
108 л – Q кДж, где Q – теплота, выделяющаяся при образовании 108 л углекислого газа (CO2).
Q = 1008 кДж.
Ответ: 1008
Если есть вопросы, то пишите в комментариях.
Разборы примеров предыдущих вопросов можно посмотреть здесь:
– вопрос 1;
– вопрос 2;
– вопрос 4.
Не забываем поставить лайк этой статье и подписаться на канал!
Всем успехов в изучении химии!
2022-08-15
Вычислите количество теплоты, которое выделится при окислении 90 г глюкозы при с. у.
Решение:
Напишем уравнение реакции окисления глюкозы:
$C_{6}H_{12}O_{6} (к.) + 6O_{2} (г.) rightarrow 6CO_{2} (г.) + 6H_{2}O (ж.)$.
Определим тепловой эффект реакции в расчете на 1 моль глюкозы, пользуясь следствием из закона Гесса:
$Delta H_{p}^{ circ } =[6 Delta H_{обр}^{ circ} (CO_{2} (г.)) + 6 Delta H_{о6р}^{ circ} (H_{2}O (ж.))] – [ Delta H_{о6р}^{ circ}(C_{6}H_{12}O_{6} (к.)) + 6 Delta H_{обр}^{ circ}(O_{2} (г.))]$;
$Delta H_{p}^{ circ } = (6(-393,5) + 6(-286)) – (-1274 + 6 cdot 0) = -2803 (кДж)$.
Рассчитаем количество теплоты, выделяющейся при окислении 90 г глюкозы:
$n = frac{m}{M}; n(C_{6}H_{12}O_{6}) = frac{90 г}{180 г/моль} = 0,5 моль; Q = – Delta H_{p}^{0}$.
Согласно уравнению реакции при окислении 1 моль глюкозы выделяется 2803 кДж, следовательно, при окислении 0,5 моль выделяется 1401,5 кДж.
Ответ: $Q = 1401,5 кДж$.
И.В.ТРИГУБЧАК
Пособие-репетитор по химии
ЗАНЯТИЕ 10
10-й класс (первый год обучения)
Продолжение. Начало см. в № 22/2005; 1, 2, 3, 5, 6, 8, 9, 11, 13, 15, 16/2006
Основы термохимии. Тепловые эффекты
химических реакций
План

Экзо- и эндотермические реакции.
2. Тепловой эффект химической реакции. Понятие
об энтальпии.
3. Термохимические уравнения.
4. Закон Гесса и следствия из него.
Химические реакции протекают с выделением или
поглощением энергии (обычно в виде теплоты). Химические
реакции, протекающие с выделением теплоты,
называются экзотермическими, а реакции,
протекающие с поглощением теплоты, –
эндотермическими.
Например:
С + О2 CO2
+ Q,
СaCO3 CaO + CO2
– Q.
Количество теплоты, которое выделяется или
поглощается в результате химической реакции,
называется тепловым эффектом реакции (Q).
Тепловой эффект выражается в кДж или ккал
(1 ккал = 4,187 кДж). Для экзотермических реакций Q
> 0, для эндотермических Q < 0.
Уравнения химических реакций, в которых
записывается тепловой эффект реакции, называют термохимическими
уравнениями. Величина Q указывается в
правой части уравнения со знаком «+» в случае
экзотермической реакции и со знаком «–» в случае
эндотермической реакции. В термохимическом
уравнении принято указывать агрегатные
состояния реагентов и продуктов реакции, т.к.
тепловой эффект реакции зависит от агрегатных
состояний реагирующих веществ. По
термохимическим уравнениям можно проводить
различные расчеты, поскольку тепловой эффект
реакции относится к мольным количествам
исходных веществ и продуктов реакции. Также
термохимические уравнения можно записывать с
величиной изменения энтальпии (Н).
Энтальпия – термодинамическая функция,
определяющая общий запас энергии системы
(энергетическое состояние вещества), включая
энергию, затрачиваемую на преодоление внешнего
давления. Q = –H.
Размерность энтальпии – Дж/моль.
Например:
С + О2 CO2
– Н,
СaCO3 CaO + CO2
+ Н.
Основной закон термохимии установлен русским
ученым Г.И.Гессом в 1840 г. (закон Гесса):
тепловой эффект химической реакции зависит
только от начального и конечного состояний
веществ и не зависит от промежуточных стадий
процесса.
Например:
С + 1/2О2 CO + Q1,
СO + 1/2О2 CO2
+ Q2,
С + О2 CO2
+ Q3;
Q3 = Q1 + Q2.
Первое следствие из закона Гесса:
тепловой эффект реакции равен сумме теплот
образования продуктов реакции за вычетом сумм
теплот образования исходных веществ (с учетом
коэффициентов):
Qр-ции = Qобр. прод
– Qобр. реаг.
Теплота образования (Qобр) – это
теплота, которая выделяется или поглощается при
образовании
1 моль сложного вещества из простых веществ при
стандартных условиях. Теплоты образования
простых веществ приняты равными нулю.
Стандартные условия – давление 1 атм (101,3
кПа), Т = 298К (25 °С).
Второе следствие из закона Гесса:
тепловой эффект химической реакции равен сумме
теплот сгорания исходных веществ за вычетом
суммы теплот сгорания продуктов реакции (с
учетом коэффициентов):
Qр-ции = Qсгор. реаг –
Qсгор. прод.
Теплота сгорания (Qсгор) – это
теплота, выделяющаяся при сгорании 1 моль
вещества в кислороде при стандартных условиях с
образованием оксида элемента в высшей степени
окисления. Теплоты сгорания негорючих веществ
равны нулю.
Теплоты сгорания и образования – справочные
величины, они приводятся в справочных
термодинамических таблицах при стандартных
условиях.
Тест по теме
«Основы термохимии. Тепловые эффекты химических
реакций»

При стандартных условиях теплота образования
равна 0 для:
а) водорода;
б) воды;
в) пероксида водорода;
г) алюминия.
2. Реакция, уравнение которой
N2 + O2 = 2NO – Q,
относится к реакциям:
а) эндотермического соединения;
б) экзотермического соединения;
в) эндотермического разложения;
г) экзотермического разложения.
3. При взаимодействии 10 г натрия с водой
выделяется 36,46 кДж теплоты. Какое количество
теплоты (в кДж) выделилось, если в результате
реакции образовалось 200 г гидроксида натрия?
а) 838; б) 209,5; в) 364,6; г) 419.
4. Эндотермической является реакция:
а) горения водорода; б) разложения воды;
в) горения углерода; г) горения метана.
5. Известны тепловые эффекты следующих
процессов:
2С2Н2 (г.) + 5О2 (г.) = 4СО
(г.) + 2Н2О (ж.) + 2600 кДж,
Н2О (ж.) = Н2О (г.) – 40 кДж.
Какую массу воды (в г), находящейся при
температуре кипения, можно испарить за счет
теплоты, полученной при полном сгорании 89,6 л (н.у.)
ацетилена?
а) 72; б) 1170; в) 2340; г) 4680.
6. Какое определение неверно для данной
реакции:
2NaNO3 (тв.) = 2NaNO2 (тв.) + O2
(г.) – Q?
а) Гомогенная;
б) эндотермическая;
в) реакция соединения;
г) окислительно-восстановительная.
7. Даны теплоты реакций:
С + 1/2О2 = СО + 110 кДж,
2СО + О2 = 2СО2 + 566 кДж.
Определить теплоту образования углекислого
газа из простых веществ (в кДж/моль).
а) 346; б) 786; в) 503; г) 393.
8. Дано термохимическое уравнение:
2SO2 + O2 = 2SO3 + 198 кДж.
В результате реакции выделилось 495 кДж теплоты.
Какая масса (в г) сернистого газа прореагировала
с кислородом?
а) 160; б) 640; в) 320; г) 320.
9. Теплота сгорания ацетилена – 1300 кДж/моль.
Какое количество теплоты (в кДж) выделится при
сгорании 1л ацетилена (в пересчете на н.у.)?
а) 58; б) 116; в) 1300; г) 58 000.
10. Основным законом термохимии является
закон:
а) Гей-Люссака; б) Гесса;
в) Авогадро; г) Пруста.
Ключ к тесту
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| а, г | а | г | б | в | а, в | г | в | а |
б |
Задачи на основные
термохимические расчеты

теплоту реакции получения гидроксида кальция из
оксида кальция и воды, если теплота образования
оксида кальция равна +635,7 кДж/моль, теплота
образования воды равна +285,8 кДж/моль, а теплота
образования гидроксида кальция равна +986,8
кДж/моль.
Решение
Ответ. 65,3 кДж/моль.
2. Найти теплоту образования угарного газа,
если теплота образования углекислого газа равна
+393,8 кДж/моль, а теплота реакции получения
углекислого газа из угарного газа и кислорода
равна +283,2 кДж/моль.
Ответ. +110,6 кДж/моль.
3. Теплота сгорания графита составляет +393,8
кДж/моль, а теплота сгорания алмаза равна
+395,7 кДж/моль. Определить теплоту превращения
графита в алмаз.
Ответ. –1,9 кДж/моль.
4. Теплота образования бромоводорода равна
+36 кДж/моль, теплота образования йодоводорода
равна +12,6 кДж/моль. Рассчитать тепловой эффект
реакции взаимодействия йодоводорода с бромом.
Ответ. +23,4 кДж/моль.
5. Теплота образования углекислого газа
равна +393,8 кДж/моль, теплота образования воды
равна
+285,8 кДж/моль, теплота сгорания этилена равна +1402
кДж/моль. Вычислить теплоту образования этилена.
Ответ. –42,8 кДж/моль.
6. Определить тепловой эффект реакции
разложения 1 моль известняка, если при
образовании 10 г карбоната кальция из оксида
кальция и углекислого газа выделяется 16 кДж
теплоты.
Ответ. –160 кДж/моль.
7. Термохимическое уравнение реакции
горения метана имеет вид:
СН4 (г.) + 2О2 (г.) = СО2 (г.)
+ 2Н2О (г.),
Н = –802,2 кДж.
Найти, какое количество теплоты выделится при
сгорании 44,8 л (н.у.) метана.
Ответ. 1604,4 кДж.
8. При соединении 11,16 г железа с серой
выделилось 20,06 кДж теплоты. Определить теплоту
образования сульфида железа.
Ответ. 100,3 кДж/моль.
9. Термохимическое уравнение реакции
окисления водорода имеет вид:
Н2 (г.) + 1/2О2 (г.) = Н2О (г.),
Н = –241,8 кДж.
Определить количество теплоты, выделяющейся
при взрыве 8,4 л (н.у.) гремучего газа.
Ответ. 60,45 кДж.
10. При сгорании этилена выделилось 6226 кДж
теплоты. Найти объем (н.у.) кислорода, вступившего
в реакцию, если тепловой эффект данной реакции
составляет 1410,9 кДж. Ответ. 296,5 л.
11. Окисление глюкозы в организме может
протекать по реакции:
С6Н12О6 (тв.) + 6О2
(г.) = 6СО2 (г.) + 6Н2О (ж.),
Н = –2803 кДж.
Какое количество теплоты выделится при
окислении 800 г глюкозы?
Решение
Ответ. 12 458 кДж.
12. При стандартных условиях теплота полного
сгорания белого фосфора равна 760,1 кДж/моль, а
теплота полного сгорания черного фосфора равна
722,1 кДж/моль. Определить теплоту превращения
черного фосфора в белый при стандартных
условиях.
Ответ. –38 кДж/моль.
13. При сжигании уксусной кислоты в
кислороде выделилось 235,9 кДж теплоты и осталось 10
л непрореагировавшего кислорода (измерено при
давлении 104,1 кПа и температуре 40 °С).
Рассчитать массовые доли компонентов в исходной
смеси, если теплоты образования углекислого
газа, паров воды и уксусной кислоты равны
соответственно 393,5 кДж/моль, 241,8 кДж/моль и
484,2 кДж/моль.
Ответ. 36% СН3СООН и 64% О2.
14. 48 г минерала, содержащего 46,7% железа и 53,3%
серы по массе, сожгли в избытке кислорода, а
твердый продукт сгорания прокалили с 18,1 г
алюминия. Какое количество теплоты выделилось в
результате каждого из этих процессов, если
известно, что реакции проводились при постоянной
температуре, а теплоты образования при данной
температуре таковы: сульфид железа – 174 кДж/моль,
оксид железа(III) – 824 кДж/моль, сернистый газ – 297
кДж/моль, оксид алюминия – 1675 кДж/моль?
Ответ. 332,8 кДж и 170,2 кДж.
15. Тонко измельченную смесь алюминия и
железной окалины (термит) применяют для сварки
металлических изделий, поскольку при ее
поджигании выделяется большое количество
теплоты и развивается высокая температура.
Рассчитать минимальную массу термитной смеси,
которую необходимо взять для того, чтобы
выделилось 665,3 кДж теплоты в процессе
алюмотермии, если теплоты образования железной
окалины и оксида алюминия равны 1117 кДж/моль и 1670
кДж/моль соответственно.
Ответ. 182,4 г.