как узнать количество теплоты если известен объём нагреваемой воды и разница температур в промежутке времени?
xxx xxx
Ученик
(65),
закрыт
5 лет назад
нагревается с помощью кипятильника.
Лучший ответ
Игорь Листерман
Ученик
(54)
13 лет назад
не играет роли чем вода нагревается!
Формула кол-ва теплоты
Q=cm(t2-t1)= с*рV*(t2-t1)
с – удельная теплоемкость… для воды 4200
масса вещества m = рV (плотность на объем) плотность для воды 1000
t2-t1 – измененние температуры
Источник: собственная голова
Остальные ответы
Похожие вопросы
На прошлых двух уроках мы
узнали, что такое количество теплоты и удельная теплоёмкость. Сегодня мы сможем
узнать, как рассчитывается количество теплоты. Рассмотрим некоторые примеры.
Допустим, нам нужно нагреть чугунную сковородку массой 5 кг от 20 оС
до 200 оС. Исходя из таблицы, удельная теплоёмкость чугуна
составляет 540 Дж/кг ∙ оС .
Как мы помним, это
означает, что для нагревания 1 кг чугуна на 1 оС потребуется 540 Дж.
Для нагревания 5 кг на 1 оС потребуется в 5 раз больше. Но нам нужно
нагреть сковородку не на 1 оС, а на 180 оС.
Следовательно, потребуется в 180 раз больше энергии. Из этого мы делаем вывод: чтобы
рассчитать количество теплоты, необходимое для нагревания тела или выделяемого
им при охлаждении, нужно удельную теплоёмкость тела умножить на массу и на
разность между начальной и конечной температурами.
Получается, что
количество теплоты находится в линейной зависимости от всех трех величин,
необходимых для расчёта. Если мы сделаем проверку размерности, то убедимся, что
наш вывод был правильным:
Это вполне логично,
поскольку, если бы это было не так, то единицы измерения теплоёмкости были бы
иными.
Рассмотрим несколько
примеров решения задач на данную тему.
Задача 1. Оголённый
медный провод нагрелся до 230 ℃, после чего его выключили
из цепи. Какое количество теплоты он отдаст помещению с температурой 20 ℃,
если масса провода 2,5 кг?
Задача 2. В
алюминиевую кастрюлю массой 2 кг налили 1,5 л воды для нагревания до 80 ℃.
Начальная температура воды и кастрюли составляет 25 ℃.
Вычислите необходимое количество теплоты для нагревания. Плотность воды равна
1000 кг/м3.
Как мы помним, не все
тела нагреваются одинаково, кроме того, кастрюля и вода в данном случае имеют
разную массу. Поскольку между кастрюлей и водой происходит непрерывный
теплообмен, их температуры можно считать одинаковыми. Итак, для вычисления
необходимого количества теплоты, нам нужно рассчитать количество теплоты
отдельно для кастрюли и для воды, а потом сложить эти величины.
Задача 3. Для
охлаждения только что изготовленной стальной детали массой 12 кг, её положили в
воду. Известно, что использовали 20 л воды с начальной температурой 15 ℃.
Начальная температура детали 300 ℃.
Через некоторое время деталь вынули и измерили её температуру. Она оказалась 34
℃,
как и температура воды. Найдите количество теплоты, которое получила вода и
количество теплоты, которое потеряла деталь.
Этот результат не
случайный. Ведь теплопередача — передача энергии, поэтому, вода получила ровно
столько энергии, сколько отдала деталь.
Эта задача является
хорошим примером использования большой теплоёмкости воды: ведь масса воды не
превышала массу детали даже вдвое, в то время, как температура детали превышала
температуру воды в 20 раз.
Количество теплоты — еще один изученный нами вид энергии. Эту энергию тело получает или отдает при теплопередаче. Мы установили, что количество теплоты, необходимое для нагревания тела, зависит от массы тела, разности температур и рода вещества. Нам известен физический смысл удельной теплоемкости и некоторые ее табличные значения для разных веществ. В этом уроке мы перейдем к численному расчету количества теплоты, необходимой для нагревания тела или выделяемого им при охлаждении.
Зачем это нужно? На самом деле, на практике очень часто используют подобные расчеты.
При строительстве зданий и проектировании систем отопления важно знать, какое количество теплоты необходимо отдавать для полного обогрева всех помещений. С другой стороны, также необходима информация о том, какое количество теплоты будет уходить через окна, стены и двери.
Формула для расчета количества теплоты
Допустим, на нужно узнать, какое количество теплоты получила при нагревании железная деталь. Масса детали $3 space кг$. Деталь нагрелась от $20 degree C$ до $300 degree C$.
Возьмем значение теплоемкости железа из таблицы — $460 frac{Дж}{кг cdot degree C}$. Объясним смысл этой величины: на нагревание куска железа массой $1 space кг$ на $1 degree C$ необходимо затратить количество теплоты, равное $460 space Дж$.
- Масса детали у нас в 3 раза больше, значит, на ее нагрев потребуется в 3 раза большее количество теплоты — $1380 space Дж$
- Температура изменилась не на $1 degree C$, а на $280 degree C$
- Значит, необходимо в 280 раз большее количество теплоты: $1380 space Дж cdot 280 = 386 400 space Дж$
Тогда, формула для расчета количества теплоты, необходимой для нагревания тела или выделяемого им при охлаждении примет вид:
$Q = cm(t_2 — t_1)$,
где $Q$ — количество теплоты,
$c$ — удельная теплоемкость вещества, из которого состоит тело,
$m$ — масса тела,
$t_1$ — начальная температура тела,
$t_2$ — конечная температура тела.
Чтобы рассчитать количество теплоты, которое необходимо затратить для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость умножить на массу тела и на разность конечной и начальной температур.
Рассмотрим подробнее особенности расчета количества теплоты на примерах решения задач.
Расчет количества теплоты, затраченного на нагревание двух тел
В железный котелок массой $4 space кг$ налили воду массой $10 space кг$ (рисунок 1). Их температура $25 degree C$. Какое количество теплоты нужно затратить, чтобы нагреть котелок и воду до температуры $100 degree C$?
Обратите внимание, что нагреваться будут сразу два тела: и котелок, и вода в нем. Между постоянно будет происходить теплообмен. Поэтому их температуры мы можем считать одинаковыми.
Отметим, что массы котелка и воды различные. Также они имеют различные теплоемкости. Значит, полученные ими количества теплоты будет различными.
Теперь мы можем записать условие задачи и решить ее.
Дано:
$m_1 = 4 space кг$
$c_1 = 460 frac{Дж}{кг cdot degree C}$
$m_2 = 10 space кг$
$c_2 = 4200 frac{Дж}{кг cdot degree C}$
$t_1 = 25 degree C$
$t_2 = 100 degree C$
Q-?
Посмотреть решение и ответ
Скрыть
Решение:
Для расчета полученного количества теплоты используем формулу $Q = cm(t_2 — t_1)$.
Запишем эту формулу для количества теплоты, полученного котелком:
$Q_1 = c_1m_1(t_2 — t_1)$.
Рассчитаем это количество теплоты:
$Q_1 = 460 frac{Дж}{кг cdot degree C} cdot 4 space кг cdot (100 degree C — 25 degree C) = 1840 frac{Дж}{degree C} cdot 75 degree C = 138 000 space Дж = 138 space кДж$.
Количество теплоты, полученное водой при нагревании будет равно:
$Q_2 = c_2m_2(t_2 — t_1)$.
Подставим численные значения и рассчитаем:
$Q_2 = 4200 frac{Дж}{кг cdot degree C} cdot 10 space кг cdot (100 degree C — 25 degree C) = 42000 frac{Дж}{degree C} cdot 75 degree C = 3 150 000 space Дж = 3150 space кДж$.
Общее количество теплоты, затраченное на нагревание котелка и воды:
$Q = Q_1 +Q_2$,
$Q = 138 space кДж + 3150 space кДж = 3288 space кДж$.
Ответ: $Q = 3288 space кДж$.
Расчет количества теплоты при смешивании жидкостей
Горячую воду разбавили холодной и получили температуру смеси $30 degree C$. Горячей воды с температурой $100 degree C$ при этом было $0.3 space кг$. Холодная вода имела массу $1.4 space кг$ и температуру $15 degree C$. Рассчитайте, какое количество теплоты было отдано горячей водой при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.
Дано:
$c_1 = c_2 = c = 4200 frac{Дж}{кг cdot degree C}$
$m_1 = 0.3 space кг$
$m_2 = 1.4 space кг$
$t_1 = 100 degree C$
$t_2 = 15 degree C$
$t = 30 degree C$
$Q_1 — ?$
$Q_2 — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Запишем формулу для расчета количества теплоты, отданного горячей водой при остывании от $100 degree C$ до $30 degree C$:
$Q_1 = cm_1(t_1 — t)$.
Рассчитаем эту величину:
$Q_1 = 4200 frac{Дж}{кг cdot degree C} cdot 0.3 space кг cdot (100 degree C — 30 degree C) = 1260 frac{Дж}{degree C} cdot 70 degree C = 88 200 space Дж = 88.2 space кДж$.
Запишем формулу для расчета количества теплоты, полученного холодной водой при нагревании от $15 degree C$ до $30 degree C$:
$Q_2 = cm_2(t — t_2)$.
Рассчитаем эту величину:
$Q_1 = 4200 frac{Дж}{кг cdot degree C} cdot 1.4 space кг cdot (30 degree C — 15 degree C) = 5880 frac{Дж}{degree C} cdot 15 degree C = 88 200 space Дж = 88.2 space кДж$.
$Q_1 = Q_2 = 88.2 space кДж$.
Ответ: $Q_1 = Q_2 = 88.2 space кДж$.
В ходе решения этой задачи мы увидели, что количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой, равны. Другие опыты дают схожие результаты.
Значит,
Если между телами происходит теплоообмен, то внутренняя энергия всех нагревающихся тел увеличивается на столько, на сколько уменьшается внутренняя энергия остывающих тел.
На практике часто получается так, что отданная горячей водой энергия больше, чем полученная холодной. На самом деле, горячая вода при охлаждении передает какую-то часть своей внутренней энергии воздуху и сосуду, в котором происходит смешивание.
Есть 2 способа учесть этот фактор:
- Если мы максимально сократим потери энергии, то добьемся приблизительного равенства отданной и полученной энергий
- Если рассчитать и учесть потери энергии, то можно получить точное равенство
Расчет температуры при известной величине количества теплоты
При нагревании куска меди было затрачено $22 space кДж$. Масса этого куска составляет $300 space г$. Начальная температура была равна $20 degree C$. До какой температуры нагрели кусок меди?
Дано:
$m = 300 space г$
$t_1 = 20 degree C$
$c = 400 frac{Дж}{кг cdot degree C}$
$Q = 22 space кДж$
СИ:
$0.3 space кг$
$22 000 space Дж$
$t_2 — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Запишем формулу для расчета количества теплоты:
$Q = cm(t_2 — t_1)$.
Постепенно выразим из этой формулы искомую температуру $t_2$:
$t_2 — t_1 = frac{Q}{cm}$,
$t_2 = frac{Q}{cm} + t_1$.
Рассчитаем $t_2$:
$t_2 = frac{22 000 space Дж}{400 frac{Дж}{кг cdot degree C} cdot 0.3 space кг} + 20 degree C approx 183 degree C + 20 degree C approx 203 degree C$.
Ответ: $t_2 approx 203 degree C$.
Что такое тепло?
Начнем с вопроса одновременно легкого и сложного: что такое тепло?
Теплом называется природная энергия, которая создается беспорядочным движением частиц тела (атомов, молекул и т. п.) и проявляется в нагревании этого тела.
Такое определение не было известно людям сразу. Например, было такое предположение: теплота — это невидимая, невесомая жидкость, которая притекает в физические тела. И чем больше объем этой жидкости, тем тело горяче́е. Конечно же, эта гипотеза не нашла подтверждения.
Позже ученые обратили внимание на поведение молекул при нагревании или охлаждении тела. С ростом температуры скорость молекул возрастает, они чаще сталкиваются друг с другом. При этом растет потенциальная и кинетическая энергия, а значит, и внутренняя, что проявляется в буквальном нагревании тела. Такое хаотичное движение молекул называют тепловым движением.
Тепловое движение — процесс хаотичного движения частиц, образующих вещество.
Логично предположить: раз с ростом температуры скорость молекул увеличивается, то при понижении температуры скорость будет падать. Но возможна ли полная остановка движения? До какой температуры следует охладить тело в таком случае?
Чтобы это произошло, потребуется охладить тело до абсолютного нуля по шкале Кельвина, что соответствует −273,15 °C, или −459,67 °F. Молекулы в таких условиях прекратят движение и замрут в узлах кристаллической решетки. Но достичь такого температурного режима невозможно ни на планете Земля, ни во всей Вселенной, ни даже в лабораторных условиях.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Пятерка по физике у тебя в кармане!
Решай домашку по физике на изи. Подробные решения помогут разобраться в сложной теме и получить пятерку!

Каким образом можно нагреть вещество?
На самом деле способов больше, чем один. Телу можно передать тепло непосредственно или же изменить его внутреннюю энергию, совершив над ним работу.
Теплопередача
К видам теплопередачи относятся теплопроводность, конвекция и излучение. Чтобы лучше понять, чем отличается один тип от другого, давайте разберем примеры.
-
Теплопроводность. Представьте, что ваши руки замерзли и вы держите в руках кружку кофе, чтобы их согреть. В таком случае тепло от более нагретого тела (кружки) передается менее нагретому (вашим рукам), до тех пор пока температура двух объектов не станет одинаковой. Так, горячая вода отдает свое тепло холодной при смешивании, а суп нагревает холодную ложку, если ее оставить в тарелке. Только аккуратно, не обожгитесь!
-
Конвекция — вид теплообмена, при котором внутренняя энергия передается струями и потоками самого вещества. Проще говоря, это процесс, который происходит в жидкостях и газах, когда слои вещества разной температуры перемешиваются. На этом принципе основано отопление помещения и проветривание комнаты. Кстати, ветры, дующие над поверхностью земного шара, — это тоже пример конвекции.
-
Излучение. Догадывались ли вы, что мы сталкиваемся с этим типом теплопередачи каждый день? Именно день, ведь солнечный свет излучает тепло с помощью электромагнитных волн, что делает жизнь на планете Земля возможной. По правде говоря, любое нагретое тело может стать источником тепла (человек, животные, свеча, костер, звезды). Это можно увидеть с помощью особого прибора — тепловизора.
Совершение работы над веществом
Здесь мы тоже не обойдемся без понятного примера. Возьмем пробирку с керосином, обыкновенный шнурок и термометр. Замерим начальную температуру и начнем натирать пробирку шнурком. Что произойдет с температурой? Она начнет возрастать. Это происходит благодаря теплопередаче? Или, может, невидимое излучение заставляет керосин нагреваться? Нет, мы изменили температуру вещества, совершив над ним работу.
Итак, подведем промежуточные итоги:
-
Тепло — это энергия, которая создается тепловым движением молекул.
-
Тепловое движение — процесс хаотичного движения частиц, образующих вещество.
-
С ростом температуры растет и скорость движения молекул, а полностью остановить это движение практически невозможно.
-
Изменить температуру тела можно двумя способами: с помощью теплопередачи или изменения внутренней энергии тела при совершении над ним работы.
Понятие тепловых явлений
Тепловые явления — это физические процессы, протекающие в телах при их нагревании или охлаждении. То есть это те явления, которые происходят с телами по мере изменения их температуры.
Давайте сделаем небольшую остановку на этом физическом понятии, а потом продолжим.
Температура — мера нагретости тела. Ее можно измерить с помощью термометра, или по-простому градусника. У этого прибора есть множество разновидностей, но в быту чаще всего пользуются ртутными (для измерения температуры человеческого тела), жидкостными (для измерения температуры воздуха или жидкости) и электронными термометрами.
В мире используют несколько температурных шкал: Цельсия, Кельвина и Фаренгейта. На онлайн-уроках физики в школе Skysmart вы подробнее познакомитесь с ними и научитесь легко переводить значения из одной шкалы в другую!
Какие бывают тепловые явления?
Давайте поразмышляем о том, что может происходить с телом под действием температуры. Для этого не придется идти далеко: достанем из холодильника кубик льда, опустим его в стакан и посмотрим, что получится. Спустя какое-то время лед начнет таять (или плавиться) и превратится в воду. Но на этом мы не остановимся! Перельем воду в кастрюлю и начнем нагревать на плите. Что произойдет тогда?
Абсолютно верно! Вода начнет нагреваться, а дальше — кипеть. Если вовремя не выключить плиту или не снять с нее кастрюлю, вся вода может выкипеть — превратиться в водяной пар.
За короткий промежуток времени мы смогли пронаблюдать воду в трех агрегатных состояниях: твердом, жидком и газообразном. А можно ли обратить процесс вспять и снова получить кубик льда?
Так просто это сделать не получится: должно быть, весь водяной пар разлетелся по квартире, и его будет очень сложно собрать воедино. Но это не говорит о том, что процесс перехода из одного агрегатного состояния в другое необратим.
Предположим, нам удастся добыть целый литр водяного пара. Охлаждая его, мы заметим, как пар конденсируется — превращается в капельки жидкости. А получить лед совсем просто, если поместить полученную жидкость в морозильную камеру.
Если внимательно проанализировать опыт, вы заметите, что переход из одного агрегатного состояния в другое не происходит мгновенно. Для этого необходимо нагреть или охладить вещество до определенной температуры, причем для каждого вещества эти температуры разные. Так, лед начинает таять при 0 °С, а железо плавится аж при 1 538 °С.
А как называются процессы, связанные с повышением и понижением температуры? Сколько их всего?
Начнем с самого легкого. Процессы, связанные с нагреванием или охлаждением, так и называются. Напомним, что эти процессы не ведут к изменению агрегатного состояния, а, можно сказать, являются подготовкой к нему.
Плавление — процесс перехода из твердого состояния в жидкое. А обратный процесс, когда жидкость превращается в твердое тело, называется кристаллизацией (или затвердеванием). Для этих процессов необходимо достичь одной и той же температуры вещества. То есть лед начнет плавиться при нуле градусов, но одновременно с этим вода начнет кристаллизоваться при этой температуре.
Парообразование (кипение) — процесс перехода жидкости в газ, а конденсация — обратный процесс перехода газа в жидкость. Для этих процессов также существует одна и та же температура. Ртуть кипит при температуре 356,7 °С, и при этой же температуре пары ртути превращаются в жидкость.
Отдельно выделим процесс сгорания вещества. Это явление также является тепловым, но, к сожалению, оно необратимо.
Рассмотрим график фазовых переходов для воды:
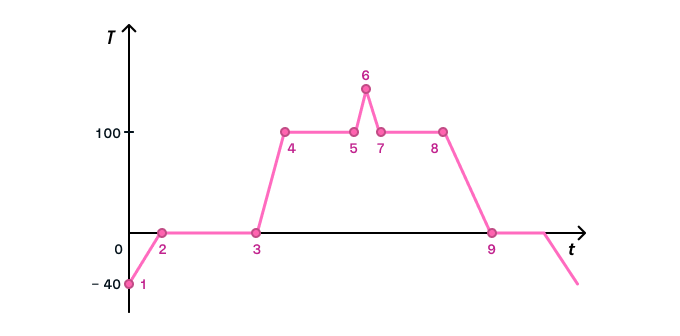
Обратите внимание на то, как одно тепловое явление сменяет другое.
Согласно графику, в начале опыта мы берем лед при температуре −40 °С и начинаем его нагревать. График этого процесса представлен наклонной прямой 1–2.
Достигнув 0 °С (точка 2), лед начинает таять. Для этого процесса не нужно увеличивать температуру, достаточно 0 °С, но понадобится время, чтобы процесс завершился. Поэтому плавление льда на графике представлено прямой линией 2–3, параллельной оси абсцисс.
Мы продолжаем нагревать воду (наклонная линия графика 3–4) до 100 °С — в этой точке начинается кипение. Если мы хотим показать на графике, что процесс кипения продолжается, от точки 100 °С мы бы провели прямую линию, параллельную оси абсцисс (4–5), а нагревание водяного пара выглядело бы как наклонная линия 5–6 (схожая с подобными процессами, уже представленными на графике).
Пойдем в обратном направлении: на графике процесс 6–7 — охлаждение пара, 7–8 — конденсация, 8–9 — охлаждение жидкости, 9–10 — кристаллизация, а дальше — охлаждение твердого тела.
Итого к тепловым явлениям относятся 7 процессов: сгорание, нагревание, охлаждение, кипение (парообразование), конденсация, плавление, кристаллизация (затвердевание).
Формулы для расчета количества теплоты
Количество теплоты, которое необходимо для возникновения процесса или выделяется при нем, можно рассчитать по формулам.
Количество теплоты, необходимое для нагревания тела или выделяющееся при охлаждении
Q = cmΔt
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества, из которого состоит тело [Дж/(кг·°C)]
m — масса тела [кг]
Δt — изменение температуры тела [°C]
Отдельно поговорим про с — удельную теплоемкость вещества. Это табличная величина, т. е. ее значение для каждого вещества различается, оно постоянно и его можно найти в конце учебника по физике или в интернете.
Количество теплоты, необходимое для плавления или выделяющееся при кристаллизации
Q = λm
Q — количество теплоты, необходимое для плавления кристаллического тела, находящегося при температуре плавления в нормальном атмосферном давлении [Дж]
m — масса тела [кг]
λ — удельная теплота плавления вещества, из которого состоит тело [Дж/кг]
Количество теплоты, необходимое для кипения или выделяющееся при конденсации
Q = Lm
Q — количество теплоты, необходимое для превращения в пар жидкости (выделяющееся при конденсации пара), находящейся при температуре кипения и нормальном атмосферном давлении [Дж]
m — масса тела [кг]
L — удельная теплота парообразования жидкости [Дж/кг]
Количество теплоты, выделяющееся при полном сгорании топлива
Q = qm
Q — количество теплоты, выделяющееся при полном сгорании топлива [Дж]
q — удельная теплота сгорания топлива [Дж/кг]
m — масса топлива [кг]
Как вы можете заметить, все формулы имеют одну и ту же логику: энергия Q прямо пропорциональна массе тела и удельным величинам. А значит, чем больше масса тела, тем больше энергии потребуется для его нагревания. Чем меньше тело, тем меньше энергии выделится при его остывании, и т. д.
Тепловые явления встроены в нашу жизнь на все сто процентов. Все — от кулинарии до погодных явлений, от медицины до промышленности — в той или иной мере зависит от процессов нагревания, плавления, кипения и других.
Мы можем плавить металлы и изготавливать из них различные предметы, повышать влажность воздуха, кипятить воду и выпекать булочки, изготавливать микросхемы и лекарства. Какой процесс ни возьмете, во всех можно отыскать примеры тепловых явлений.
Тепловые процессы в физике связаны между собой. Порой нагревание одного вещества влечет за собой плавление и даже кипение другого. Заинтригованы? Приходите на онлайн-уроки физики в школу Skysmart — там вы сможете детально разобраться в этом и других поразительных процессах.
Количество теплоты
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: количество теплоты, удельная теплоёмкость вещества, уравнение теплового баланса.
Как мы знаем, одним из способов изменения внутренней энергии является теплопередача (теплообмен). Предположим, что тело участвует в теплообмене с другими телами, и при этом не совершается механическая работа — ни самим телом, ни другими телами над этим телом.
Если в процессе теплообмена внутренняя энергия тела изменилась на величину , то говорят, что тело получило соответствующее количество теплоты:
.
Если при этом величина отрицательна, т.е. тело отдавало энергию, то говорят также, что тело отдавало тепло. Например, вместо формально верной, но несколько нелепой фразы «тело получило —5 Дж тепла» мы скажем: «тело отдало 5 Дж тепла».
Удельная теплоёмкость вещества
Предположим, что в процессе теплообмена агрегатное состояние вещества тела не изменяется (не происходит плавление, кристаллизация, парообразование или конденсация). Начальную температуру тела обозначим , конечную температуру —
.
Опыт показывает, что количество теплоты, полученное телом, прямо пропорционально массе тела и разности конечной и начальной температур:
Коэффициент пропорциональности c называется удельной теплоёмкостью вещества тела. Удельная теплоёмкость не зависит от формы и размеров тела. Удельные теплоёмкости различных веществ можно найти в таблицах.
Введя обозначение , получим также:
Чтобы понять физический смысл удельной теплоёмкости, выразим её из последней формулы:
Мы видим, что удельная теплоёмкость численно равна количеству теплоты, которое необходимо для нагревания 1кг данного вещества на (или, что то же самое, на
). Измеряется удельная теплоёмкость в Дж/(кг·
C) или в Дж/(кг·K).
Чем больше удельная теплоёмкость вещества, тем большее количество теплоты требуется для нагревания тела данной массы на заданное количество градусов.
В задачах часто фигурируют вода и лёд. Их удельные теплоёмкости желательно помнить.
Вода: Дж/(кг·
C).
Лёд: Дж/(кг·
C).
Произведение удельной теплоёмкости вещества на массу тела называется теплоёмкостью тела и обозначается :
Соответственно, для количества теплоты имеем:
Уравнение теплового баланса
Рассмотрим два тела (обозначим их 1 и 2), которые образуют замкнутую систему. Это означает, что данные тела могут обмениваться энергией только друг с другом, но не с другими телами. Считаем также, что механическая работа не совершается — внутренняя энергия тел меняется только в процессе теплообмена.
Имеется фундаментальный закон природы, подтверждаемый всевозможными экспериментами — закон сохранения энергии. Он гласит, что полная энергия замкнутой системы тел не меняется со временем.
В данном случае закон сохранения энергии утверждает, что внутренняя энергия нашей системы будет оставаться одной и той же: . Если изменение внутренней энергии первого тела равно
, а изменение внутренней энергии второго тела равно
, то суммарное изменение внутренней энергии будет равно нулю:
Но — количество теплоты, полученное первым телом в процессе теплообмена; аналогично
— количество теплоты, полученное вторым телом в процессе теплообмена. Стало быть,
(1)
Попросту говоря, сколько джоулей тепла отдало одно тело, ровно столько же джоулей получило второе тело. Так как система замкнута, ни один джоуль наружу не вышел. Соотношение (1) называется уравнением теплового баланса. В общем случае, когда тел образуют замкнутую систему и обмениваются энергией только с помощью теплопередачи, из закона сохранения энергии с помощью тех же рассуждений получаем общее уравнение теплового баланса:
(2)
В качестве простого примера применения уравнения теплового баланса рассмотрим следующую задачу.
Смешали г воды при температуре
и
г воды при температуре
. Найти установившуюся температуру смеси.
Обозначим искомую установившуюся температуру через . Запишем уравнение теплового баланса (1):
где — удельная теплоёмкость воды. Раскрываем скобки и находим:
Благодарим за то, что пользуйтесь нашими материалами.
Информация на странице «Количество теплоты» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из разделов нашего сайта.
Публикация обновлена:
08.05.2023
