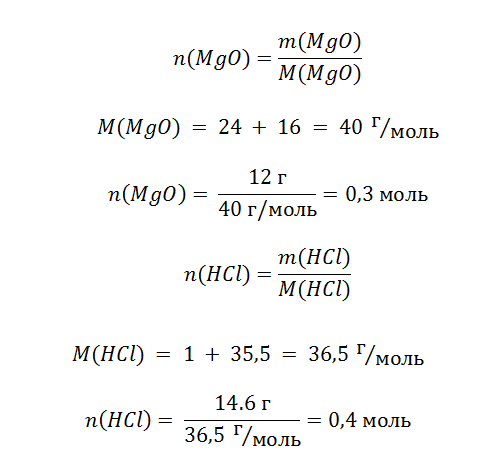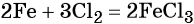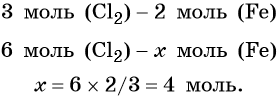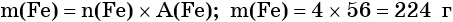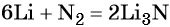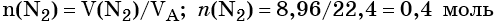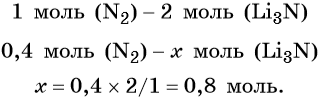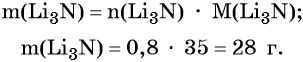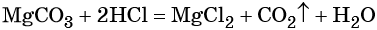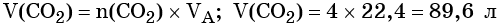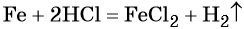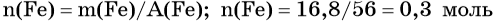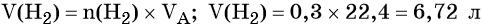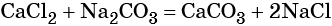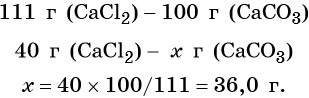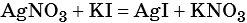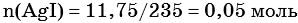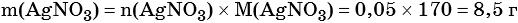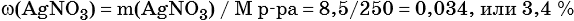Задача 22.
Существует всего три типа задач, которые встречаются в этом задании, но все они решаются по уравнению реакции, в вычислениях используют определенный набор формул:
Для каждого из типов представлен алгоритм решения задач.
Первый тип задач.
Дана масса раствора исходного вещества и его массовая доля. Определить массу образовавшегося осадка.
1. Составить уравнение реакции, т.е. записать формулы веществ вступающих в реакцию и продуктов, образующихся в результате реакции. Расставить коэффициенты!
2. По таблице растворимости определить в правой части реакции осадок, обозначить его ↓.
3. Рассчитать массу вещества в растворе по формуле:
m(ве-ва) = m(ра-ра)∙ω.
4. Рассчитать количество вещества по формуле: n = m/M.
5. По уравнению реакции определить количество вещества того вещества, которое выпало в осадок.
6. Рассчитать массу осадка по формуле: m =M·n.
Пример 1. К 60 г раствора с массовой долей гидроксида калия 15% добавили избыток раствора нитрата меди (II). Определите массу выпавшего осадка.
Решение: 1. Записываем уравнение реакции, пользуясь таблицей растворимости устанавливаем вещество, которое выпадает в осадок:
2. Найдем массу гидроксида калия (m(ве-ва)):
m(ве-ва) = m(ра-ра)∙ω
m(КОН) = 60*15/100% = 9 г
3. Найдем количество вещества КОН:
n = m/M
nКОН = 9/56 = 0, 16 моль
4. По уравнению реакции найдем количество вещества Cu(OH)2:
2 моль КОН – 1 моль Cu(OH)2
0,16 моль КОН – х моль Cu(OH)2
х = 0,16*1/2 = 0,8 моль
5. Найдем массу осадка:
m =M·n
mCu(OH)2 = 98*0,8 = 78,4 г
Ответ: 78,4 г.
Второй тип задач.
Дана масса раствора вещества или продукта реакции. Вычислить массовую долю вещества или продукта реакции.
1. Составить уравнение реакции, т.е. записать формулы веществ, вступающих в реакцию и продуктов, образующихся в результате реакции. Расставить коэффициенты!
2. Вычисляем количество исходного вещества (или продукта) реакции по формуле: n = m/M, если дан объем газа, то по формуле: n =V*Vm .
3. Вычисляем массу исходного вещества (или продукта) реакции по формуле: m = n*M.
4.Знаем массу исходного вещества (продукта) – нашли в предыдущем действии. Знаем массу раствора – дана в условии. Находим массовую долю по формуле: ω = m(вещества)/m(раствора)∙.
Пример2: К 85 г раствора серной кислоты добавили порцию карбоната калия. При этом выделилось 0,896 л газа. Вычислите массовую долю исходного раствора серной кислоты.
Решение: 1. Записываем уравнение реакции:
2. Найдем количество вещества CO2:
n = V/Vm
nCO2 = 0,896/22,4 = 0, 04 моль
3.По уравнению реакции найдем количество вещества Н2SO4:
nCO2 = nН2SO4 = 0,04 моль
1. Найдем массу серной кислоты (m(ве-ва)):
m(Н2SO4) = n*M
m(Н2SO4) = 0,04*98 = 3,92 г
5. Найдем массовую долю серной кислоты в растворе:
ω (Н2SO4) = 3,92/85*100% = 4,6%
Ответ: 4,6%
Третий тип задач.
Дана массовая доля раствора исходного вещества. Определить массу исходного вещества в растворе.
1. Составить уравнение реакции, т.е. записать формулы веществ вступающих в реакцию и продуктов, образующихся в результате реакции. Расставить коэффициенты!
2. Рассчитать количество вещества образовавшегося осадка или выделившегося газа по формуле:
n = m/M или n = V/Vm
3. По уравнению реакции рассчитать количество вещества, массу которого необходимо найти в вопросе задачи.
4. Рассчитать массу вещества в растворе по формуле:
m(Na2SO4) = n*M
5. Найдем масcу растворa:
m(ра-ра) = m(ве-ва) /ω.
Пример 3: К раствору сульфата натрия с массовой долей 9% добавили избыток раствора нитрата бария. В результате образовался осадок массой 9,85г. Определите массу исходного раствора сульфата натрия.
Решение: 1. Записываем уравнение реакции, пользуясь таблицей растворимости устанавливаем вещество, которое выпадает в осадок:
2. Найдем количество вещества BaSO4:
n = m/M
nBaSO4 = 9,85/230 = 0,04 моль
3.По уравнению реакции найдем количество вещества Na2SO4:
n BaSO4 = nNa2SO4 = 0,04 моль
4. Найдем массу вещества сульфата натрия (m(ве-ва)):
m(Na2SO4) = n*M
m(Н2SO4) = 0,04*119 = 4,76 г
5. Найдем масcу растворa сульфата натрия:
m(ра-ра) = m(ве-ва) /ω.
m(ра-ра) = 4,76*100% /9 = 52,89 г
Ответ: 52,89 г
Задачи для самостоятельного решения.
1. К 160 г раствора с массовой долей нитрата серебра 5% добавили избыток раствора хлорида натрия. Определите массу выпавшего осадка.
2. К 80 г раствора с массовой долей нитрата бария 9% добавили избыток раствора серной кислоты. Определите массу выпавшего осадка.
3. К 180 г раствора с массовой долей гидроксида натрия 10% добавили избыток раствора хлорида железа (III). Определите массу выпавшего осадка.
4. К 150 г раствора соляной кислоты добавили раствор сульфида калия. При этом выделилось 8,96 л газа. Вычислите массовую долю исходного раствора соляной кислоты.
5. К 75 г раствора серной кислоты добавили порцию карбоната кальция. При этом выделилось 2, 24 л газа. Вычислите массовую долю исходного раствора серной кислоты.
6. К 125 г раствора соляной кислоты добавили порцию сульфита калия. При этом выделилось 4,48 л газа. Вычислите массовую долю исходного раствора соляной кислоты.
7. К раствору сульфата калия с массовой долей 6% добавили избыток раствора хлорида бария. В результате образовался осадок массой 8,95г. Определите массу исходного раствора сульфата калия.
8. К раствору фосфата натрия с массовой долей 12% добавили избыток раствора нитрата серебра. В результате образовался осадок массой 12,45г. Определите массу исходного раствора фосфата натрия.
9. К раствору хлорида кальция с массовой долей 8% добавили избыток раствора нитрата серебра. В результате образовался осадок массой 9,85г. Определите массу исходного раствора хлорида кальция.
Как найти массу осадка
Часто бывает так, что в ходе химической реакции образуется малорастворимое вещество, выпадающее в осадок (к примеру, сульфат бария, фосфат кальция, хлорид серебра и т.д.). Предположим, химику поставлена задача: определить массу этого осадка. Каким образом можно это сделать?

Инструкция
Если вам неизвестны точные количества исходных веществ, то придется действовать опытным путем. То есть сначала отделите осадок от раствора (путем фильтрования или на обычной воронке, или с использованием воронки Бюхнера). После чего тщательно высушите его и взвесьте на аналитических весах. Так вы получите достаточно точный результат.
Ну а если вам известны точные количества веществ, вступавших в реакцию, то все будет гораздо проще. Например, изначально было 28,4 грамма сульфата натрия и 20,8 грамма хлорида бария. Сколько граммов осадка образовалось?
Напишите правильное уравнение химической реакции: Na2SO4 + BaCl2 = BaSO4 + 2NaCl.В результате этой реакции образуется практически нерастворимое вещество – сульфат бария, мгновенно выпадающий в виде плотного белого осадка.
Вычислите, какое из веществ было взято в недостатке, а какое – в избытке. Для этого подсчитайте молярные массы исходных реагентов:46 + 32 + 64 = 142 г/моль – молярная масса сульфата натрия;
137 + 71 = 208 г/моль – молярная масса хлорида бария.То есть в реакцию вступали 0,2 моля сульфата натрия и 0,1 моля хлорида бария. Сульфат натрия был взят в избытке, следовательно, весь хлорид бария прореагировал.
Подсчитайте количество образовавшегося осадка. Для этого разделите молекулярную массу сульфата бария на молекулярную массу хлорида бария и результат умножьте на количество исходного вещества:20,8 * 233/208 = 23,3 грамма.
А если бы сульфат натрия был в недостатке? Предположим, в реакцию вступило бы не 28,4 грамма этой соли, а в 5 раз меньше – всего 5,68 грамма. И тут нет абсолютно ничего сложного. 5,68 грамма сульфата натрия составляют 0,04 моля. Следовательно, в реакцию с таким количеством этой соли могло вступить также всего 0,04 моля хлорида бария, то есть 0,04 х 208 = 8,32 грамма. Прореагировало только 8,32 грамма из исходных 20,8 граммов.
Умножив эту величину на соотношение молярных масс сульфата бария и хлорида бария, получите ответ: 8,32 * 233/208 = 9,32 грамма осадка.
Источники:
- как найти массу осадка в растворе
- Вычисление молярной массы эквивалента
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
План урока:
Основные величины и формулы их нахождения
Основные величины и формулы их нахождения
Ключевым понятием в химии является вещество. Урок 2 в данном курсе, напомнит Вам, все необходимые сведения. Формула для определения количества вещества, в зависимости от исходных данных, выражается в следующем виде.
Для веществ характерно взаимодействие друг с другом. Перед химиками стоит задача вычислить какое количество вещества необходимо для реакции с другим веществом.В химической промышленности, на производстве важно знать, какая масса или объём реагентов необходим, и сколько возможно получить в итоге реакции продукта. Вещества реагируют между собой в определённых количествах, точнее эквивалентах. Как трактовать последнее предложение. Вспомните себя маленькими, когда вы только начинали изучать количество, на примере мячиков, яблок, конфет и т.д.
Согласитесь, что самому большому шарику будет тесно в маленьком стаканчике, впрочем, как и маленькому шарику не совсем уютно будет в большом стаканчике. Т.е. мы выбираем стаканчик для шарика эквивалентно его размеру.
Возьмём, к примеру, кислород, который реакционно-способный и окисляет другие соединения.
Вспомним закон сохранения массы вещества (ЗСМВ), без которого невозможно составить химические уравнения.
Источник
Следует отметить, чтобы прореагировало 1 моль СН4, необходим кислород количеством молей 2. Снова обращаясь к базовому закону, мы видим, что реагентов и продуктов масса одинаковая, точнее 80 г. Почему именно эта цифра, и откуда она взялась. Для этого смотрим на уравнение реакции.
Другими словами, чтобы образовалось 1 моль СО2 и 2 моль Н2О, необходимо чтобы метан и кислород прореагировали пропорционально 1: 2.
Выразим массу, которая будет соответствовать этому количеству вещества.
m = n * M
Вспомним, каким образом вычисляется молярная масса.
Давайте попробуем чуть-чуть усложниться, к примеру, будет реагировать не 1 моль метана, а 2,5 моль. Сколько тогда потребуется О2?
И здесь приведём такой наглядный пример. Один килограмм конфет стоит 2 рубля. Сколько Вам понадобится денег, чтобы купить 2,5 кг. Не составит труда дать ответ, что необходимо потратить 5 рублей. А если, Вы захотите 4 кг, то придётся попросить у родителей уже 8 рублей. Вот эти размышления перенесём на наш пример.
Какое количество мы бы не взяли метана, то кислорода необходимо в 2 раза больше. Т.е. для реакции 2,5 моль СН4 необходим О2 количеством 5 моль.
Количество вещества – это уникальная величина, от которой можно перейти к другим параметрам вещества (m или V), используя основные формулы.
Рассмотрим задачи на определение массы вещества,а также объёма с помощью химических уравнений. Как и при решении, абсолютно всех задач, первое, что мы делаем, читаем внимательно условие и выписываем все известные физические величины (дано), а также определяем, что неизвестно (найти).
Задача 1. Сколько литров (н. у.) кислорода необходимо потратить для полного сгорания 8,5 г сероводорода.
Дано:
m(H2S) = 8,5 г
Найти:
V(O2) – ?
Решение.
Переведём условие задачи на химический язык, т.е. составим уравнение реакции. Важно отметить, что для удобства и лёгкости решения подчеркните те соединения, о которых идёт речь.
Теперь обратим внимание на коэффициенты в химических уравнениях, именно они отвечают за соотношение веществ.
Следует заметить, что массу (г) сероводорода необходимо выразить в количестве (моль).
Запишем мольное соотношение сероводорода и кислорода, в значение числителя подставляем коэффициенты с уравнения, а в знаменателе – что известно в условии задания.
Из пропорции определим число молей для кислорода.
Ответим на вопрос задачи (находим объём кислорода)
Ответ. V(O2) = 8.4 л
Теперь представим следующую ситуацию, Вам на день Рождения или на другой праздник подарили деньги, чтобы Вы приобрели себе желаемую вещь. К примеру, вы хотите себе наушники, карту памяти и новый чехол на телефон. Возникает закономерный вопрос, а хватит ли Вам денег. Такие задачи встречаются и в химии.
Задача 2. Хватит ли 10 л кислорода для сгорания 12 г магния и 0,6 г углерода (н.у.)?
Дано:
V(O2) = 10 л
m(Mg) = 12 г
m(C) = 0,6 г
Найти:
V(O2) – ?
Решение
Особенность этой задачи, что будет два уравнения реакции, взаимодействие О2 отдельно с магнием и углеродом. Это как покупка в двух разных магазинах. Используя алгоритм, приведённый выше, вычислим количество вещества кислорода. Следует заметить, что отдельно ведём расчёт по магнию (или по углероду), заполняя данные таблицы.
Обратите внимание, в предыдущей задаче кислород был в избытке, в объёме 10 – 6,72 = 3,28 л. Этому избытку не с чем реагировать. Представьте, что Вы помощник деда Мороза и пакуете новогодние подарки. Допустим в одном наборе должно содержаться 5 шоколадных конфет и 8 карамелек. Вам необходимо разделить 55 шоколадки и 72 карамельки. Вопрос: сколько наборов у Вас получится? Проведём нехитрые математические исчисления, знакомые Вам ещё с курса математики младшей школы.
55 : 5 = 11
72 : 8 = 9
И что получается, что шоколадки можно разместить в 11 наборов, а карамельки только в 9. Таким образом, получится 9 новогодних подарков, и 10 (5 ∙ 2 = 10) шоколадок будут лишними, они в избытке.
Расчёты по химическим уравнениям, где один из реагентов берётся в избытке (т.е. его больше, чем необходимо), проводятся аналогично, как и с одним известным веществом.
Задача 3. 48,75 цинка привели в реакцию с 5,6 л (условия нормальные) хлора. Сколько соли получилось в итоге, ответ выразите в граммах.
Дано:
V(Cl2) = 5.6 л
m(Zn) = 48.75 г
Найти:
m(ZnCl2) – ?
Решение.
Составим схему взаимодействия, не забудьте отметить количество реагирующих молей.
Теперь наша с Вами задача определить, какое вещество прореагировало полностью, а какое осталось в избытке. Вспомните пакеты с подарками, какие конфеты мы разложили полностью и почему остались шоколадные лишними. Поможет определиться с избытком, решение неравенства.
n (Zn) ? n (Cl2) ?
Расчёт для цинка производится согласно формуле:
Хлор – это газообразное вещество, поэтому нужно применить формулу:
Сравним полученные значения n(Zn) > n(Cl2), цинк находится в избытке, поэтому расчёт ведём по хлору, который прореагировал полностью количеством 0,25 моль.
Из пропорции вычислим количество образованной соли (не забываем, что числитель отвечает за коэффициенты, а знаменатель – это данные в условии).
Ответ. Масса соли равна 34 г.
Большинство химических реакций происходит в растворе. Однако при расчётах необходима масса именно растворённого вещества, которое непосредственно реагирует. Допустим, команда с 12 человек, которая на 25% состоит из девочек и 75% мальчиков, поехала на соревнования. В одном из этапов участвуют только мальчики. Ваша задача определить, сколько мальчиков поехало на соревнования.
Вот эти 9 мальчишек и участвовали в определённом туре, а девочки на данный момент были не в счёт, они были в группе поддержки.
Задача 4. На 12 г оксида магния подействовали 146 г раствора соляной кислоты, с массовой долей раствора 10%. Вычислите, сколько соли образовалось в процессе взаимодействия этих веществ?
Дано:
m(MgO) = 12 г
mр-ра(HCl) = 146 г
Wр-ра(HCl) = 10%
Найти:
m(MgCl2) – ?
Решение
Особенностью этой задачи является то, что в условии указана масса всего раствора, а необходимо знать только,сколько содержится кислоты, которая будет реагировать с MgO. Формула определения массы вещества, находящегося в растворе, выражается в следующем виде.
Обратите внимание, что из всей массы раствора (146 г) реагирует только 10%, а именно 14,6 г.
Теперь задача определить, какого из реагентов больше и он прореагирует не полностью.
Схема показывает, что для реакции 0,3 моль MgO требуется 0,6 моль кислоты. На это размышление нам указывает схема реакции. Для полного растворения оксида необходимо потратить в 2 раза больше HCl, смотрите соотношение 1:2.Однако в нашем распоряжении есть только 0,4 моль, поэтому n(MgO) >n(HCl), оксид находится в избытке, в то время как кислота прореагировала полностью и мы смело можем использовать её количество вещества для расчёта массы соли.
Снова воспользуемся пропорцией, чтобы узнать количество образованной соли.
Теперь не составит особого труда найти массу.
Ответ. m(MgCl2) = 19 г.
В желаниях человечества изобрести идеальную машину, во время работы которой не будет никаких потерь. Однако на выходе не бывает заветных 100%. Аналогично и во время химических процессов на производстве или лаборатории не удаётся получить продукт с выходом реакции 100%. При решении задач мы вычисляем так называемый теоретический выход, что должно быть в идеальной ситуации. Но мы живём в реальном мире, где есть потери: газообразные продукты могут улетучиться, осадок, образованный в процессе реакции, можно не в полной мере выделить из раствора. Поэтому практический выход всегда будет меньше теоретического.
Задача 5. В результате взаимодействия 59,5 г нитрата серебра с избытком раствора соляной кислоты, был выделен осадок массой 45 г. Определите выход реакции.
Дано:
m(AgNO3) = 59.5 г
m(осадка) = 45 г
Найти:
η – ?
Решение.
Своеобразие этого типа задач в том, что необходимо отличать теоретическую и практическую массу продукта. Маленькой подсказкой вам послужит время глагола, если видите прошедшее или настоящее время (получено, выделили), значит это практическая масса. Чтобы найти выход продукта, необходимо вычислить теоретическую массу или объём (вот за эти параметры как раз и отвечает схема реакции).
Используя привычный алгоритм, определим n нитрата серебра.
Следующим шагом будет определить количество вещества, выпавшего в осадок (AgCl).
Вычислим массу осадка, это будет теоретическая, т.е. та, которая должна получиться, если бы не было потерь.
В идеальной ситуации, мы бы получили 50,225 г, что составило бы 100%. Однако во время процесса образовалось только 45 г продукта. Получается, выход реакции будет меньше и составит:
Ответ. η = 89,6%
Особый тип задач на определение молярной массы вещества. Состав соединений мы можем узнать с химической формулы. При решении этого типа необходимо вспомнить следующие понятия– это доля (массовая) элемента и относительная плотность газов.
Однако следует заметить, что величину D мы можем использовать только для газообразных соединений.
Задача 6. Определите объём кислорода (условия нормальные), что потребуется для сжигания вещества массой 180 г, которое состоит на 26,67 % из углерода, 2,24 % водорода, а также кислорода. Известно, что равняется 45.
Дано:
DH2 = 45
W(C) = 26.67%
W(H) = 2.24%
m(CxHyOz) = 180 г
Найти:
Формула – ?
V(O2) – ?
Решение.
Чтобы решить эту, на первый взгляд, запутанную задачу, нам необходимо сначала определить, что это за соединение, чтобы была возможность составить уравнения химических реакций.
Однако в условии известно только процентный состав вещества. Но всё-таки, этих данных нам достаточно, чтобы найти формулу вещества.
Запишем выражение для нахождения количества атомов углерода (х), водорода (у) и кислорода (z). Представьте, вы купили в коробке шоколадные конфеты из трёх видов.
Следует отметить, что они имеют разную форму, начинку, как следствие и вес. Вернёмся к нашему веществу, которое состоит из 3 элементов, имеющих разнуюAr. Так вот на долю углерода выпадает 26,67% (условно допустим, что это конфета в виде сердечка), водород занимает 2,24% (конфета с воздушной начинкой), а все остальные конфеты в коробке с ореховой начинкой (в соединении их роль играют атомы кислорода). Вопрос: сколько штук занимает каждый вид конфетки? Логично узнать вес одной конфеты (в нашем случае это Ar элементов). Разделив процентное содержание на атомную массу элемента, получим их количество.
Такого же ведь количества конфет не будет в коробке, вы, наверное, слабо себе можете представить, что там будут находиться части конфет. Чтобы получить целые числа, необходимо, выбрать из этих чисел самое маленькое и каждое на него разделить.
Вычисления показывают, что соотношение элементов в данном соединении можно записать в следующем виде: СНО2. Уточним правильность наших расчётов, определив его молекулярную массу, используя величину D.
Обратите внимание, первоначальная запись формулы вещества СНО2 отвечает молярной массе
Однако, это вещество в 45 раз тяжелее водорода, что отвечает 90 г/моль.Чтобы получить её, мы сохранили соотношение элементов 1:1:2, при этом умножили количество каждого элемента на 2. Следовательно, молекулярная формула С2Н2О4.
Количество вещества, отвечающее 45 г вещества С2Н2О4, вычислим привычным методом.
Используя мольное соотношение, определим число молей кислорода, а также его объём.
Ответ. Для сгорания 45 г С2Н2О4 необходимо 5,6 л кислорода.
Обобщая всё выше сказанное, как решать расчётные задачи по химии, с улыбкой или с шоком, принимать решение только Вам. Рассмотрим ещё одну задачу.
Задача 7. Пропан (С3Н8), объёмом 84 л, который содержит 25% негорючих примесей, сожгли в 56 л кислорода. Газ, который выделился, пропустили через гидроксид бария, определите массу осадка, если выход продукта реакции составил 89%.
Дано:
V(С3H8) = 84 л
W(примеси) = 25%
V(O2) = 56 л
η = 89%
Найти:
m(осадка) – ?
Решение.
На что здесь следует обратить внимание. Пропан содержит не горючие примеси. Представьте, вам необходимо в торт 84 г очищенных орехов. Вы идёте в магазин, приобретаете необходимую массу, но придя домой обнаружили, что там 25% содержится мелких остатков скорлупы. Т.е. масса орехов не будет 84 г. Чистых орехов будет 100% – 25% = 75%.
Негорючие примеси входят в общий объём, а гореть будет только пропан. Находим, сколько же его содержится в 84 л.
Составим схему горения газа
Определим количество вещества реагирующих газов
На первый взгляд кажется, что пропан в избытке n(C3H8) > n(O2). Однако посмотрите на уравнение реакции, чтобы сгорело 2,8125 моль пропана необходимо в 5 раз больше кислорода, что составит 14 моль. По этой причине расчёт будем вести по кислороду.
Это количество СО2 пропускают через Ва(ОН)2, что можно отобразить схемой.
Найдём массу ВаСО3, которая будет в виде осадка
Теперь необходимо усчитать выход соли, который составил всего лишь 89%.
Ответ. m(BaCO3) = 263 г.
Вычисление количества вещества, массы или объема вещества по количеству веществ, массе или объему одного из реагентов или продуктов реакции
Основой для проведения количественных расчётов в химии является закон сохранения массы. Согласно этому закону масса реагентов равна массе продуктов реакции.
Отсюда следует, что для любой химической реакции массы реагентов и продуктов реакции относятся между собой как молярные массы веществ, умноженные на их стехиометрические коэффициенты.
Для расчёта по химическим уравнениям можно использовать два эквивалентных способа: через количество вещества или через пропорцию. Подчеркнём ещё раз: официального запрета на использование метода пропорций при решении задач на ОГЭ и ЕГЭ нет!
Для определения массы (или количества вещества) продуктов реакции или исходных веществ по уравнениям химических реакций вначале составляют уравнение химической реакции и устанавливают стехиометрические коэффициенты; затем определяют молярную массу, массу и количество вещества известных реагентов химической реакции; составляют и решают пропорцию, в которую в зависимости от условий задачи вводят числовые значение величин: молярные массы, массы, количества веществ или их объёмы (для газов).
При этом в одном столбце пропорций должны находиться одинаковые характеристики вещества с одной и той же размерностью.
Пример 1. Масса железа, вступившего в реакцию с 6 моль хлора, равна _________ г. (Ответ запишите с точностью до целого числа.)
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что 3 моль Cl2 реагируют с 2 моль Fe, т. е.:
Определяем массу железа:
Пример 2. Масса нитрида лития, образовавшегося в результате его реакции с азотом объёмом 8,96 л, равна_______________ г.
Решение. Составляем уравнение химической реакции:
Определяем количество вещества азота, вступившего в реакцию:
Из уравнения реакции следует, что из 1 моль N2 образуется 2 моль Li3N, т. е.:
Определим массу Li3N:
Пример 3. Объём углекислого газа, образовавшегося в результате разложения карбоната магния количеством вещества 4 моль избытком соляной кислоты, равен________ л.
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что количество вещества углекислого газа и карбоната магния равны между собой, т. е. n(CO2) = 4 моль.
Определим V(CO2):
Пример 4. Объём водорода, который выделится при растворении 16,8 г железа в избытке разбавленной соляной кислоты, равен _________ л.
Решение. Составляем уравнение химической реакции:
Определим количество вещества железа:
Количество вещества железа и водорода в данном уравнении реакции равны между собой. Следовательно, количество вещества водорода также равно 0,3 моль.
Вычислим объём водорода:
Пример 5. Масса осадка, который образуется в результате взаимодействия 40,0 г хлорида кальция с избытком карбоната натрия, равна _________г.
Решение. Составляем уравнение реакции:
Согласно уравнению химической реакции составим пропорцию и решим её:
Пример 6. 250 г раствора нитрата серебра смешали с избытком раствора йодида калия. Выпал осадок массой 11,75 г. Вычислите массовую долю нитрата серебра в исходном растворе.
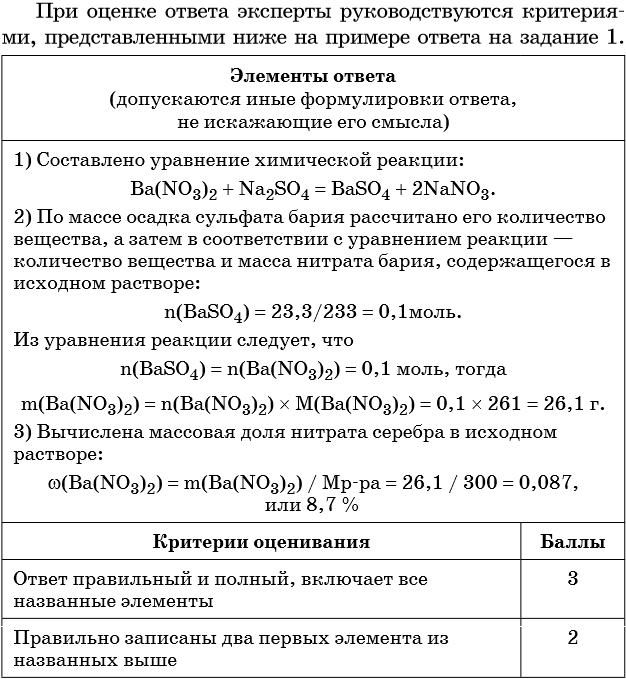
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысла)
1) Составлено уравнение химической реакции:
2) По массе осадка йодида серебра рассчитано его количество вещества, а затем в соответствии с уравнением реакции — количество вещества и масса нитрата серебра, содержащегося в исходном растворе:
Из уравнения реакции следует, что n(AgI) = n(AgNO3) = 0,05 моль, тогда:
3) Вычислена массовая доля нитрата серебра в исходном растворе:
| Критерии оценивания | Баллы |
| Ответ правильный и полный, включает все названные элементы | 3 |
| Правильно записаны два первых элемента из названных выше | 2 |
| Правильно записан один из названных выше элементов (1-й или 2-й) | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
Тренировочные задания
1. К 300 г раствора нитрата бария прибавили избыток раствора сульфата натрия. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
2. К 150 г раствора сульфата натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
3. К 300 г раствора силиката натрия прибавили избыток раствора нитрата кальция. Масса выпавшего осадка составила 12,0 г. Определите концентрацию соли в исходном растворе.
4. К 150 г раствора карбоната калия прибавили избыток раствора соляной кислоты. При этом выделился газ объёмом 3,36 л (н. у.). Определите концентрацию соли в исходном растворе.
5. К 250 г раствора гидрокарбоната натрия прибавили избыток раствора бромоводородной кислоты. При этом выделился газ объёмом 5,6 л. Определите концентрацию соли в исходном растворе.
6. К 50 г раствора карбоната натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
7. К 200 г раствора хлорида бария прибавили избыток раствора карбоната калия. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
8. К 200 г раствора хлорида железа (II) прибавили избыток раствора гидроксида калия. Масса выпавшего осадка составила 18,0 г. Определите концентрацию соли в исходном растворе.
9. К 400 г раствора нитрата свинца прибавили избыток раствора йодида натрия. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
10. К 300 г раствора йодида натрия прибавили избыток раствора нитрата свинца. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
11. Определите массу осадка, который выпадет при взаимодействии 150 г 14,8%-ного раствора хлорида кальция с избытком раствора карбоната натрия.
12. Определите объём газа (н. у.), который выделится при взаимодействии 120 г 8,8%-ного раствора карбоната натрия с избытком раствора соляной кислоты.
13. Определите массу соли, которая выпадет в осадок при взаимодействии 140 г 13,5%-ного раствора нитрата цинка с избытком раствора сульфида натрия.
14. Определите массу осадка, который выделится при взаимодействии 200 г 18,8%-ного раствора нитрата меди с избытком раствора сульфида натрия.
15. Определите массу осадка, который выпадет при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора хлорида цинка.
16. Определите массу осадка, который выделится при взаимодействии 200 г 12,7%-ного раствора хлорида железа (II) с избытком раствора сульфида натрия.
17. Определите массу осадка, который выделится при взаимодействии 50 г 17%-ного раствора нитрата серебра с избытком раствора бромида калия.
18. Определите массу осадка, который образуется при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора нитрата кальция.
19. Определите массу осадка, который образуется при взаимодействии 50 г 5,8%-ного раствора хлорида магния с избытком раствора фосфата натрия.
20. Определите объём газа, который выделится при взаимодействии 200 г 6,9%-ного раствора карбоната калия с избытком раствора соляной кислоты.
21. Оксид фосфора (V) массой 21,3 г растворили в растворе гидроксида калия, в результате чего был получен раствор средней соли массой 500 г. Определите концентрацию фосфата калия в конечном растворе.
22. Раствор хлорида железа (II) полностью прореагировал со 120 г раствора гидроксида натрия, в результате чего образовалось 6,0 г осадка. Определите массовую долю гидроксида натрия в исходном растворе.
23. Какой объём аммиака (н. у.) может полностью прореагировать со 150 г 20%-ного раствора серной кислоты с образованием средней соли?
24. В 200 г 20%-ного раствора соляной кислоты растворили магний до прекращения выделения газа. Определите объём выделившегося при этом водорода (н. у.).
25. Аммиак объёмом 10 л (н. у.) пропустили через раствор серной кислоты с массовой долей 8% до образования средней соли. Определите массу исходного раствора.
26. Определите объём сероводорода (н. у.), который необходимо пропустить через 130 г 6%-ного раствора хлорида меди (II) до полного осаждения сульфида меди (II).
27. Сероводород объёмом 3,36 л (н. у.) пропустили через раствор гидроксида натрия, в результате чего получили 180 г раствора сульфида натрия. Определите массовую долю соли в полученном растворе.
28. Алюминий массой 8,1 г может нацело прореагировать с 250 г раствора серной кислоты. Определите массовую долю серной кислоты в исходном растворе.
29. К 250 г раствора нитрата серебра добавили раствор хлорида калия до прекращения выделения осадка, масса которого составила 14,35 г. Определите массовую долю нитрата серебра в исходном растворе.
30. К 300 г 5%-ного раствора хлорида магния добавили избыток раствора фосфата калия. Вычислите массу выпавшего при этом осадка.
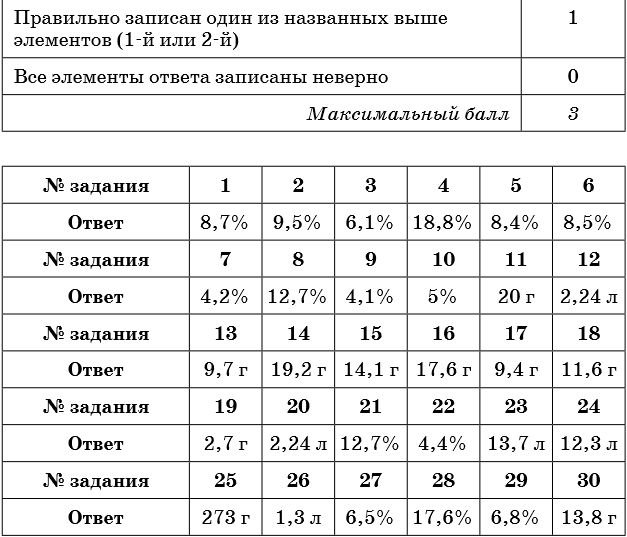
Ответы

Найти количество вещества осадка,образовавшегося при взаимодействии сульфата калия с 52г 40%-ого раствора хлорида бария
Светило науки – 717 ответов – 6315 раз оказано помощи
Дано: Решение:
m(р)(BaCI₂) = 52 г K₂SO₄ + BaCI₂ = BaSO₄↓ + 2KCI
ω(BaCI₂) = 40% 1) Найдем массу соли:
Найти: 52 × 0.4 = 20.8 г
n(BaSO₄)=? 2) Найдем молярную массу соли и осадка:
М(BaCI₂) = 137 + 35 × 2 = 207 г/моль
М(BaSO₄) = 137 + 32 + 16 × 4 = 233 г/моль
3) По пропорции найдем массу осадка:
20.8 г = Х г ⇒ Х = 20.8 × 233 = 23.41 г
207 г/моль = 233 г/моль ⇒ 207
4) Найдем количество осадка:
n(BaSO₄) = m/M = 23.41/233 = 0.1 моль
Ответ: n(BaSO₄) = 0.1 моль