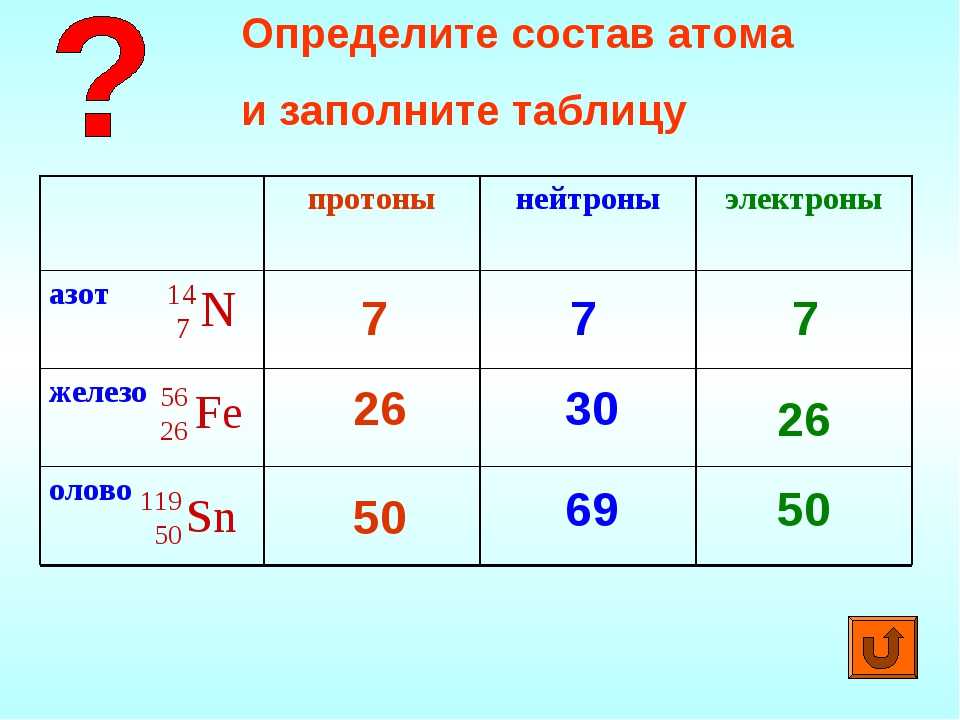
Изучая атом, можно заметить, что он состоит из трех основных частиц: протонов, электронов и нейтронов. Каждая из частиц играет важную роль в создании замечательного мира, которым мы живем. При этом нейтроны несут на себе половину массы всего атома. Изучение и понимание данного компонента чрезвычайно важно для работы химиков, физиков и других научных специалистов, цель которых – раскрыть тайну устройства нашей Вселенной.
В работе данной статьи мы познакомим вас с различными методами, доступными для определения числа нейтронов в атоме химического элемента. Мы обсудим простые расчеты и теоретические основы, а также рассмотрим физические тесты и эксперименты. Кроме того, мы предоставим несколько примеров для более наглядного представления материала.
Теперь не останется никаких вопросов насчет количества нейтронов в атоме и вы сможете вниз глубже погрузиться в захватывающую науку АТОМНОЙ структурой и иными замечательными явлениями, населяющими наш мир. Вы готовы? Тогда мы начинаем!
Необходимость и значение нейтронов в химии
Влияние нейтронов на химическую и isotopicow stability
Изначально атомы из одних и тех же химических элементов, но с разной активностью нейтронов, полностью эквивалентны в химическом отношении и называют стабильными изотопами. Это значит что химические свойства атома, в основном определяемые его наружным процессом электронов, не зависят от средней инерции нейтрона в ядре. Никогда находит проблемы в некоторых радиоизотопах с избытком нейтронов или протонов, когда их ядро находится не в состоянии достичь стабильности, что приводит к радиоактивным реакциям с выделением энергии и испусканием далеких частиц и гамма-квантов.
Неутронные реакции как инструмент химического анализа
Нейтроны с их способностью взаимодействовать с атомными ядрами малого веса способны служить важным инструментом для исследований с использованием нитроновых реакций. Эта техника, называемая нейтронно-активационным анализом (NAA), основана на облучении проб афтертонами и последующем измерении излучения оцененной пробы после ее рекомбинации. Неутронный активационный анализ имеет очень высокую чувствительность и способность идентифицировать очень низкие содержание элементов, что позволяет использовать эту технику для обнаружения различных примесей и загрязнений в материалах, а также для изучения геохимических и биологических систем.
| Тип нейтронного взаимодействия | Результат |
|---|---|
| распаде навертона | формирование атома с меньшим atomic number |
| активации нейтрона | формирование атомов с большим атомным весом |
| протон радиация | излучение гамма-квантов с опреденнавыми энергиями |
Таким образом, нейтроны являются основой для необратимо ряда важных химических процессов и находках, обеспечивая стабильность атомов и предоставляя полезные методики анализа.
Атомная и массовая числа
Атомное число (Значение в периодтической таблице слева от названия элемента) указывает количество протонов в ядре атома данного элемента. Это число уникально для каждого химического элемента и определяет его простую электронную конфигурацию и его химические свойства.
Массовое число

Массовое число – сумма протонов и нейтронов в ядре атома. Это число используется для изучения относительной атомной массы элемента. Иногда оно может немного отличаться в разных источниках, так как некоторые химические элементы могут иметь различные стабильные изотопы с разной массами.
Нейтроны в атоме
Нейтроны – незаряженные частицы, находящиеся в ядре атома. Их количество можно определить, отдельно используя массовую и атомную числа атома. Для этого просто вычтите атомное число из массового числа дляATOMNEUTRONS = массовое число – атомное число
Нейтроны играют ключевую роль в стабильности атомов и экзотических ядерных реакциях. Они влияют на массу атома, иногда приводя к значительным изменениям в его химических и физических свойствах.
В итоге, в зависимости от количества нейтронов в ядре атома, могут и не значимо меняться некоторые химические или физические свойства атома (некоторые изотопы к примеру могут относиться к радиоактивным продуктам). Поэтому изучение атомных и массовых чисел является важной составляющей любого химического образования и исследования.
Умный подход к расчету нейтронов
| Элемент | Атомный номер (Z) | Массовое число (A) | Количество нейтронов (N) |
|---|---|---|---|
| Гелий-4 | 2 | 4 | 2 (A – Z) |
| Бор-11 | 5 | 11 | 6 (A – Z) |
| Углерод-12 | 6 | 12 | 6 (A – Z) |
Как вы можете заметить из этой таблицы, для расчета числа нейтронов достаточно вычесть атомный номер из массового числа. Атомный номер – это количество протонов в атомном ядре, и он определяет, какой именно элемент является. Массовое число, в свою очередь, показывает количество протонов и нейтронов в ядре элемента.
Таким образом, после вычитания атомного номера из массового числа мы получаем количество нейтронов в ядре: N = A – Z.
Обратите внимание, что атомные номера собраны в таблице Менделеева. Если у вас нет доступа к этой таблице, способ найти необходимое число заключается в анализе информации из справочника химических элементов. В случае отсутствия таких ресурсов, вы можете использовать надежное источник в интернете, такое как упрощенная форма таблицы Менделеева, чтобы узнать атомный номер.
Некоторые распространенные элементы имеют изотопы, различающиеся числом нейтронов. В таких случаях к названию элемента прибавляется знак деления и массовое число изотопа:
Boron-10 и Boron-11 (второй вариант является изотопом бора с большим количество нейтронов, но не относящимся к стабильным)
Метод, который описывается здесь, будет работать для большинства элементов и изотопов, хотя он не применим для бета- распада или электронного захвата, потому что в таких случаях количество нейтронов меняется.
Этот умный подход к расчетам нейтронов поможет вам быстрее и надежно избегать ошибок в будущем, если вам необходимо будет определить количество нейтронов в атомах различных элементов.
Опыты в мастерской: поиск нейтронов
Определение кол-ва нейтронов по периодной таблице
Одним из наиболее доступных способов определения числа нейтронов в атоме является обращение к периодической таблице химических элементов. Каждый химический элемент имеет свой атомный номер, который соответствует числу протонов в атомном ядре. Учитывая, что это число протонов в неизменном состоянии для каждого элемента, можно определить число нейтронов, подсчитав разницу между атомным номером и массовым числом.
Пример:
Возьмем кальций (Ca) со следующими характеристиками:
– Атомный номер: 20
– Массовое число: 40
Делаем вычисления:
Число нейтронов = Массовое число – Атомный номер
Число нейтронов = 40 – 20 = 20
Определение количества нейтронов с использованием масс-спектрометра
Для более точного определения числа нейтронов в атоме может быть использован масс-спектрометр. Масс-спектрометр использует масс-спектрометрию для измерения масс поступающих ионов и их изотопов. Полученная информация позволяет точно вычислить массовое число частицы, а таким образом и число нейтронов.
Ограничения:
Несмотря на то, что масс-спектрометр обеспечивает более точные данные, его использование может потребовать дополнительного оборудования и навыков, которые могут быть недоступными во всех случаях.
Внимание: при работе с радиоактивными веществами необходимо соблюдать все меры предосторожности для защиты вас и окружающих.
В заключении можно выделить, что если вы стремитесь найти число нейтронов в атоме, вам будут нужны как фундаментальные знания химии, так и спецтехника. Легкодоступный способ – используя периодическую таблицу и простые арифметические операции. Однако, для более точной идентификации и решения вопросов, связанных с изотопными смесями или радиоактивными веществами, может потребоваться использование детальных методов анализа, таких как масс-спектрометрия.
Периодическая таблица как ключ к непонятиям
Когда речь заходит о нейтронах, периодическая таблица является незаменимым аппаратом для понимания их роли в атомной структуре. Периодическая таблица определяет атомный номер и массовое число каждого элемента.
Объясним фундаментальные понятия:
- Атомный номер: Это то, насколько простыми числами раздельно заряжен протонов в ядре атома.
- Массовое число: Это общее число протонов и нейтронов в ядре элемента.
- Нейтронов: Это нейтральные частицы, которые являются неотъемлемой частью атомного ядра, но не имеют протиелектрического заряда.
Итак, чтобы определить количество нейтронов в атоме, их количеством служит разница между массовым числом и атомным номером данного элемента. Достаточно иметь доступ к периодической таблице, и вы сможете быстро определить кол-во нейтронов для каждого элемента спокойно и уверенно.
Итак, как найти кол-во нейтронов с периодической таблицы?
- Найдите нужный элемент в периодической таблице.
- Запишите атомный номер элемента.
- Запишите массовое число элемента.
- Посчитайте количество нейтронов, вычитая атомный номер из массового числа. Например, углерод имеет атомный номер 6 и массовое число равно 12, поэтому нейтронов во внешней части атома: 12 – 6 = 6 нейтронов.
Необходимо отметить, что этот процесс найдет количество нейтронов для обычной, стабильной изотопной формы элемента, который гораздо более распространены в природных состояниях. Но существует также множество стабильных и радиоактивных изотопов элементов, которые могут аварировать распределение протонов и нейтронов в ядре этого элемента.
Таким образом, периодическая таблица играет огромную роль в атомной и ядерной физике, используется для научных исследований, в медицине, военных целях, а в отдельный период времени и для других определенных целей. В данном случае, она является ключом к таким непростым вещам, как нейтроны, и помогает найти их количество, построенным прелестно данной схемой.
Изучая почему как нейтроны влияют на свойства веществ
Нейтроны и стабильность атома
Нейтроны – незаряженные частицы, которые вместе с протонами составляют ядро атома. Они занимаются поддержанием стабильности атома благодаря прочной связи с протонами.
Нейтроны влияют на стабильность атома, обеспечивая противовес положительному заряду протонов и предотвращая тем самым распад атома. Взаимодействие нейтронов с протонами также является причиной появления различных изотопов, а следовательно и разных химических свойств.
Нейтроны и давление ядра

Давление ядра – один из основных факторов, управляющих стабильностью атома. Измерие
Вопрос-ответ:
Как определить количество нейтронов в атомном ядре элемента, используя периодическую таблицу?
Для определения количества нейтронов в атомном ядре необходимо найти массовое число атома (которое равно сумме количества протонов и нейтронов) и вычесть из него число протонов, которое равно атомным номеру элемента (отображенному слева от названия элемента в таблице Менделеева). Например, углерод-12 имеет атомный номер 6 и массовое число 12, так что количество нейтронов равно 12 – 6 = 6.
Могут ли нейтроны быть непосредственно определены в атоме без использования периодической таблицы или других справочников?
Нет, нейтроны являются субатомными частицами, и непосредственное их наблюдение или измерение в атоме невозможно с помощью простых инструментов или методов. Чтобы определить количество нейтронов, необходимо использовать периодическую таблицу элементов, справочные источники, или для более точных измерений – применить методологии ядерной физики, такие как ядерная спектроскопия, рентгеновская флуоресценция или гамма-спектрометрия.
Что если я хочу узнать количество нейтронов в атоме, но у меня недоступна периодическая таблица? Есть ли другие способы?
Если периодическая таблица недоступна, существуют другие пути для получения информации о количестве нейтронов в атоме. Один из способов – использование информационных технологий, таких как поисковые системы и электронные базы данных, специально предназначенные для индексирования информации о химических элементах. Также, вы можете обратиться к специалистам, имеющим необходимую информацию, или посмотреть учёбные материалы и пособия по химии и ядерной физике, где обычно приводятся таблицы элементов с количеством нейтронов.