СО называют монооксидом углерода, так как ближайшее соединение есть всем хорошо известный диоксид углерода, или СО².
Разница в токсичности между СО и СО² колоссальная.
Угарный газ или окись углерода не имеет ни цвета, ни запаха.
Газ полностью лишен каких либо физических меток, определяющих его наличие в помещение человеком.
В жилом помещение концентрации CO можно уловить благодаря датчикам, метеостанция с функцией контроля воздуха или газовыми анализаторами различного типа.
Как образуется угарный газ ( CO ).
Угарный газ это продукт сгорания, выделяющийся при горении, имеющий молярную массу 28,01 г/моль и плотность 1,25 кг/м3.
Чаще всего CO выделяется при горении, но есть ряд случаев, где газ выделяется без температурных вливаний, а непосредственно в результате химической реакции.
CO2 + C = 2CO ( с участием примерно 170 кДж тепловой энергии).
НСООН → CO + H2O серная кислота воздействует на муравьиную с получением воды и угарного газа.
H2C2O4 → CO + CO2 + H2O а щавелевая кислота распадается на угарный газ, углекислый газ и воду.
Разница в плотности углекислого газа “СО2” и угарного газа “СО” велика: при 0 цельсия она составляет 1,97 кг/м³ у углекислого и 1,25 кг/м³ у угарного газа.
Механизм разрушительного действия СО в человеческом теле обусловлен взаимодействием (СО) с двухвалентным железом (Fe²+ ) гемоглобина крови, вытесняя из оксигемоглобина (HbО²) кислород и образуя карбоксигемоглобин (HbСО).
В химии это выглядет так: НbO²+ СО = НbСО + O²
Концентрации угарного газа в PPM.
Концентрации любых газов удобно измерять не только в мгр/м³ ноти в PPM единицах и угарный не исключение из этих правил. Именно по этому на всех индикаторных трубках СО шкала обозначена в мгр/м³и в ppm.
Присутствие СО в помещение опасно для человека, и в зависимости от концентраций приводит к различным последствиям, вплоть до летального исхода.
20 ppm= 0,002%.
Чувствуется лёгкое головокружение, при условии вдыхания с такой концентрацией СО в воздухе в течение восьми часов.
40 ppm =0.004%.
СО в течении 6 часов приводит к головной боли.
Если такая концентрация влияет круглосуточно то развивается синдром тяжёлой головы.
При 100 ppm =0,01%.
Начинается легкая головная боль после 120 минут экспозиции CO.
Через 6-8 часов появляется тошнота.
200 ppm = 0,02%.
сильная головная боль после 120 мин. экспозиции.
Тошнота появляется уже через 180 мин.
400 ppm =0,04%.
приводит к сильной головной боли после одного часа вдыхания.
Тошнота приходит через 120-150 мин.
1000 ppm 0,1%.
Чувствуется головокружение и последующая тошнота а далее начинаются судороги после 30 минут экспозиции угарным газом.
1200 ppm=0.12%.
Головокружение приходит через 5-10 мин.
Тошнота через 25-30 мин.
1200 ppm CO приводит к потере сознания через 60 мин.
1600 ppm 0,16%.
После 15 минут начинается:
- головная боль,
- головокружение,
- прыгает пульс,
- летальный исход за 2 последующих часа.
Концентрация 3200 ppm = 0,32%.
- головная боль,
- головокружение,
- тошнота после 5 минут вдыхания.
- смерть через 30 минут.
6000 ppm =0,6%.
- головная боль,
- головокружение через 2 минуты экспозиции,
- начинаются нервные,
- остановка дыхания,
При таких концентрация летальный исход наступает в течении и смерть через 15-25 минут.
Где содержится много оксида углерода?
Разумеется в автомобильных выхлопах содержится большое количество угарного газа.
Любая реакция горения сопровождается выходом углекислого газа.
Опасность отравления угарным газом состоит в том, что его концентрации, которые приводят к смерти=0,1% от тобщей массы вдыхаемого воздуха.
-
- Угарный газ в выхлопах авто.
Сравнение CO и СО²
СО и СО² являются абсолютно разными по токсичности газами.
СО² – углекислый газ не является токсичным, а его концентрации в 1000 ppm ( 0,1%) вызывают переутомление при работе в офисе, например!
ПДК для угарного газа установленной в пределе 0.003 мгр/м³.
ПДК для СО² примерно 400 ppm.
Токсичность угарного газа для человека объясняется тем фактом, что кровь способна переносить как кислород, так и углекислый и угарный газ.
-
- Угарный газ купирует поступление кислорода в клетки
CO купитует доступ кислорода.
При большой концентрации угарный газ не оставляет возможности кислороду прикрепляться к гемоглобиновому белку и курирует доступ кислорода к тканям, вызывая смерть от удушья.
Самая большая опасность, что человек не замечает этот газ в помещении.
Вот почему от камина в доме можно погибнуть, не имея датчиков угарного газа.
В большинстве случаев, когда человеку становится плохо от угарного газа самостоятельно не всегда успевает покинуть помещение.
Присутствие
в воздухе паров серной кислоты H2SO4
способствует разъеданию слизистых
оболочек и разрушению легочной ткани
у человека и животных.
При
транспортировке в помещении произошел
разлив серной кислоты. Цех имеет длину
А
(м), ширину B
(м) и высоту H
(м). Необходимо рассчитать концентрацию
паров серной кислоты в цехе и сравнить
ее величину с максимально разовой
предельно допустимой концентрацией
H2SO4
(ПДКм.р. =
0,3 мг/м3),
учитывая, что масса серной кислоты
составляет M
(г), а ее испарившаяся часть равна ω
(%).
Исходные
данные для расчета по вариантам содержатся
в Таблице
14.
Ход расчета:
1.
Объем помещения (цеха) V
(м3):
V
= A
. B
. H
2.
Масса испарившейся серной кислоты
m
(г):
m
=
3.
Концентрация паров H2SO4
в цехе С
(мг/м3):
С
=
4.
Сравнение фактической и предельно
допустимой концентрации паров H2SO4
производится делением этих величин
друг на друга:
С
/ ПДКм.р.,
откуда делается
вывод о соответствии содержания паров
серной кислоты в воздухе помещения
санитарно-гигиеническим нормативам.
Таблица 14.
|
Вариант |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
М, |
150 |
200 |
250 |
300 |
350 |
400 |
450 |
500 |
550 |
600 |
|
А, |
9 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
|
B, |
5 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
H, |
3 |
2,5 |
2,5 |
2,5 |
3 |
3 |
3 |
2,5 |
3 |
3,5 |
|
ω, |
0,1 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
1,2 |
Задача 10 Определение концентрации угарного газа в закрытом помещении
Наличие
в воздухе высокой концентрации угарного
газа CO
приводит к кислородному голоданию
организма, замедляет рефлексы, вызывает
сонливость и может стать причиной потери
сознания и смерти.
Водитель
в гараже при закрытых воротах решил
проверить работу двигателя. Гараж имеет
длину А
(м), ширину B
(м) и высоту H
(м). Необходимо рассчитать, через какое
количество времени после включения
двигателя концентрация угарного газа
в гараже станет равной его максимально
разовой предельно допустимой концентрации
(ПДКм.р.
= 5 мг/м3),
если скорость заполнения гаража угарным
газом равна Q
(мг/мин).
Исходные
данные для расчета по вариантам содержатся
в Таблице
15.
Ход расчета:
1.
Объем гаража V
(м3):
V
= A
. B
. H
2.
Масса выделившегося угарного газа
m
(мг), соответствующая заполнению им
гаража до уровня ПДКм.р.:
m
= V
.
ПДКм.р.
3.
Время t
(мин) с момента включения двигателя, по
прошествии которого концентрация
угарного газа в гараже становится равной
его ПДКм.р.:
t
= m
/ Q
Таблица 15.
|
Вариант |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Q, |
20 |
25 |
35 |
40 |
45 |
50 |
55 |
60 |
65 |
70 |
|
A, |
2,5 |
3 |
2,5 |
3 |
4 |
4 |
5 |
6 |
6 |
8 |
|
B, |
4 |
4,5 |
5 |
5 |
6 |
5 |
7 |
5,5 |
6 |
7 |
|
H, |
2 |
2 |
2,5 |
2,5 |
2,5 |
2 |
2,5 |
2,5 |
2,5 |
3 |
Соседние файлы в папке Экология
- #
- #
- #
- #
19.05.2015269.52 Кб20РП.rtf
- #
Как решать задание 23 в ЕГЭ по химии в 2022-2023? Установить исходную концентрацию веществ, найти известное вещество, по которому будут проводиться расчеты. Затем провести расчеты по уравнению реакции и найти неизвестные концентрации.
Особенности задания
Как решать новое задание 23 в ЕГЭ по химии, которое появилось только в 2022 году? Разумеется, хорошенько подготовившись – аналогов этой задаче до сих пор не было, в 2023 году она будет использоваться лишь второй раз. Поэтому важно заранее получить максимум информации о том, как можно найти правильный ответ.
Прежде чем разбираться, как решать номер 23 в ЕГЭ по химии, отметим, что задание относится к повышенному уровню сложности. Соответственно, за правильное решение можно заработать два первичных балла. На выполнение отводится в среднем 5-7 минут.
В задании проверяются ваши знания и умения в следующих областях:
- Обратимые и необратимые химические реакции;
- Химическое равновесие и его смещение под воздействием различных факторов;
- Расчеты количества вещества, его массы или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.
Если вкратце: вот как делать 23 задание на ЕГЭ по химии: проанализировать исходные данные и установить известные концентрации вещества. После этого произвести расчеты по уравнению реакции и вычислить неизвестные вещества.
Демонстрационные задания
А теперь на практике покажем, как решать задачи 23 в ЕГЭ по химии – используем несколько демонстрационных вариантов. Помните, что нет никакой гарантии, что именно эти задачки попадутся в вашем комплекте заданий. Но ими можно руководствоваться как примером.
Итак, первый вариант решения 23 номера ЕГЭ по химии.
Дано:
В замкнутый реактор поместили газообразную смесь оксида азота (II) с кислородом и нагрели. В результате протекания обратимой реакции 2NO(г) + O2(г) ⇄ 2NO2(г) в системе установилось равновесие.
Используя данные, приведенные в таблице, определите равновесные концентрации оксида азота (II) (Х) и кислорода (Y).
| Реагент | NO | O2 | NO2 |
| Исходная концентрация (моль/л) | 0,5 | 0,8 | |
| Равновесная концентрация (моль/л) | 0,2 |
На основании приведенных данных рассказываем, как решать 23 задание ЕГЭ по химии:
Сначала производим базовый расчет: исходя из приведенной информации, следует, что в реакторе не было NO2, а значит, исходная концентрация NO2 равна нулю.
Известное вещество (с известной исходной и равновесной концентрацией) – это NO2, которого образовалось 0,2 моль.
Теперь переходим к стехиометрическим расчетам. Подставляем нужные цифры:
- 2NO(г) + O2(г) ⇄ 2NO2(г)
- 0,2 + 0,1 ⇄ 0,2
Из уравнения реакции становится ясно, что прореагировали 0,2 моль NO и 0,1 моль О2.
Наконец, переходим к окончательным расчетам. Еще раз представим перед собой таблицу и подставим нужные значения:
| Реагент | NO | O2 | NO2 |
| Исходная концентрация (моль/л) | 0,5 | 0,8 | 0 |
| Равновесная концентрация (моль/л) | 0,3 | 0,7 | 0,2 |
Итого, получаем следующий ответ:
- х = 0,5 – 0,2 = 0,3
- у = 0,8 – 0,1 = 0,7
Еще один разбор 23 задачи ЕГЭ по химии 2022-2023. Хороший пример, который может помочь вам разобраться.
Дано:
В реактор для синтеза метанола постоянного объема поместили водород и угарный газ. В результате протекания обратной химической реакции 2Н2(г) + СО(г) ⇄ СН3ОН(г) в системе установилось химическое равновесие.
Используя данные, приведенные в таблице, определите равновесную концентрацию угарного газа (Х) и исходную концентрацию водорода (Y).
| Реагент | Н2 | СО | СН3ОН |
| Исходная концентрация (моль/л) | Y | 2 | 0 |
| Равновесная концентрация (моль/л) | 1,2 | Х | 0,4 |
Решение демо 23 задания ЕГЭ по химии 2022 выглядит так:
Так как в первоначальный момент в системе не было метанола (а в состоянии равновесия метанола стало 0,4 моль), соответственно, изменения в ходе реакции по метанолу будет равно +0,4 моль.
Далее необходимо определить, сколько угарного газа было потрачено на реакцию. Концентрация угарного газа в ходе реакции уменьшается, из уравнения реакции следует, что n(CH3ОН):n(CO) = 1:1. Отсюда следует, что n(CO) = n(CH3ОН) = 0,4 моль.
Равновесную концентрацию угарного газа можно посчитать так: [СО]равн = [СО]исх – [CO]измен = 2 моль/л = 0,4 моль/л = 1,6 моль/л.
Первая часть разбора 23 задания ЕГЭ по химии 2022г. окончена, теперь посчитаем второе неизвестное значение:
Из уравнения реакции следует, что n(CH3ОН):n(Н2) = 1:2, отсюда следует, что n(Н2) = 2n(CH3ОН) = 2х0,4 = 0,8 моль.
Концентрация водорода в ходе реакции уменьшается. Чтобы найти исходную концентрацию водорода: [H2]исх – [H2]измен = 1,2 моль/л.
[H2]исх = [H2]измен + [H2]равн = 1,2 моль/л + 0,8 моль/л = 2 моль/л.
Ответ: х = 1,6 моль/л, у = 2 моль/л.
Как вам такое объяснение 23 задания ЕГЭ по химии 2022 года? Как видите, задачи действительно сложные – нужно знать довольно много вещей и свободно оперировать химическими формулами. Что может быть довольно сложно, если на уроках вы уделяли недостаточно внимания этим темам. Хорошо, что еще есть время на подготовку!
Решение задачи 23 в ЕГЭ по химии 2022-2023 вполне доступно каждому. Конечно, если вы понимаете смысл нужных понятий и умеете пользоваться вычислениями по химическим формулам и уравнениям. Задание это новое, поэтому лучше прорешать все доступные демонстрационные варианты перед экзаменом, чтобы хорошенько подготовиться!
Библиографическое описание:
Шахринова, Н. В. Определение содержания концентрации угарного газа вблизи автомобильных дорог (на примере села Кушнаренково Республики Башкортостан) / Н. В. Шахринова, Т. В. Соколова. — Текст : непосредственный // Молодой ученый. — 2018. — № 21 (207). — С. 199-202. — URL: https://moluch.ru/archive/207/50426/ (дата обращения: 21.05.2023).
В последнее время, в связи с интенсивным развитием промышленного производства и быстрыми темпами жизни существенно обострились проблемы воздействия на окружающую среду. С каждым годом увеличивается нагрузка антропогенной деятельности на окружающую среду.
Одним из мощных источников загрязнения воздушной среды является автомобильный транспорт, увеличение численности которого привело к насыщению легковыми автомобилями и переключению на них большей части пассажирских перевозок. Это резко ухудшает санитарные условия проживания не только в крупных городах, но и в населенных пунктах сельской местности. Транспорт является одним из важнейших компонентов общественного и экономического развития, поглощающего значительное количество ресурсов и оказывающего серьезное влияние на окружающую среду.
Автомобили сжигают огромное количество нефтепродуктов, нанося одновременно ощутимый вред окружающей среде, главным образом атмосфере. Причем, атмосферный воздух загрязняется не только вредными компонентами отработавших газов, но и обедняется кислородом. Постоянный рост количества автомобилей оказывает определенную степень отрицательного воздействия на окружающую среду и здоровье человека [1].
По своему воздействию на организм человека вещества, содержащиеся в отработанных газах, подразделяются на несколько групп. В группу нетоксичных веществ входят — азот, кислород, водяной пар, а также углекислый газ.
Группу токсичных веществ составляют оксид углерода СО, оксиды азота, многочисленная группа углеводородов, включающая парафины, ароматические соединения и т. д.
Наибольшее количество загрязняющих веществ выбрасывается при разгоне автомобиля, особенно при быстром, а также при движении с малой скоростью (из диапазона наиболее экономичных). Относительная доля (от общей массы выбросов) углеводородов и оксида углерода наиболее высока при торможении и на холостом ходу, доля оксидов азота — при разгоне. Из этих данных следует, что автомобили особенно сильно загрязняют воздушную среду при частых остановках и при движении с малой скоростью.
В отработавших газах двигателя внутреннего сгорания содержится свыше 170 вредных компонентов, из них около 160 — производные углеводородов, прямо обязанные своим появлением неполному сгоранию топлива в двигателе. Наличие в отработавших газах вредных веществ обусловлено в конечном итоге видом и условиями сгорания топлива [3].
Оксид углерода (СО) — бесцветный непахнущий ядовитый газ. Наиболее распространенными симптомами отравления угарным газом являются головная боль, тошнота, одышка, головокружение и помрачнение сознания. Высокая концентрация газа незамедлительно приводит к смерти. Низкая — вызывает гриппоподобные симптомы и обычно не распознается.
Максимальная концентрация газа наблюдается у проезжей части дороги в часы «пик» при безветренной погоде. Концентрация СО может быть рассчитана по методике Рябикова [2].
Концентрация оксида углерода рассчитывается по следующей формуле:
СО = (7,33+0,026 ∙ N) ∙К1 ∙К2, где:
СО — концетрация оксида углерода у проезжей части дороги, мг/м3;
N-интенсивность движения автомашин, авто/час (определяется путём непосредственного подсчёта);
К1 –коэффициент учёта состава транспортного потока и его средней скорости (таблица 1);
К2-коэффициент учета продольного уклона дороги (при малом уклоне К=1).
- CO =___________мг/м3
Полученная концентрация окиси углерода у проезжей части дороги сравнивается с ПДК для атмосферы жилого массива 3,0 мг/м3 (но в городах с населением более 300 тыс. жителей ПДК=0,8 ПДК, т. е. для городской местности ПДК= 2,4 мг/м3).
- Определяется кратность превышения норматива.
- Определяется ширина санитарной зоны — x м у дороги по формуле: Х=(0,5СОх-СОпдк) / 0,1 = ________ м
Результаты наблюдений за интенсивностью движения автомобилей и составом транспортного потока оформляются в виде таблицы 1.
В наших исследованиях мы проводили работу по определению содержания концентрации угарного газа вблизи автомобильных дорог. В ходе исследования были определены некоторые наиболее загруженные автотранспортом улицы села Кушнаренково, центральные их участки. Количество автомобилей определялось десять раз и для расчетов использовались средние значения. Протяженность фактической санитарной зоны определялась по минимальному в пределах участка расстоянию от проезжей части до жилых массивов. Результаты исследования отражены в таблице 1.
Таблица 1
Концентрация угарного газа вблизи автомобильных дорог села Кушнаренково
|
Время наблюдения |
Количество автомобилей (N) |
Концентрация СО (мг/м3) |
Превышение ПДК |
|
|
Место наблюдения |
Среднее количество всех автомобилей |
|||
|
1800–1900 |
ул.Садовая аллея |
39 |
7,4 |
2,4 |
|
1800–1900 |
ул.Горная |
95 |
8,7 |
2,9 |
|
1800–1900 |
ул. Октябрьская |
182 |
10,7 |
3,5 |
|
1800–1900 |
М7-Волга |
220 |
11,6 |
3,8 |
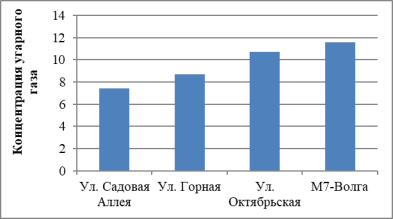
Рис. 1. Концентрация угарного газа на исследуемых участках
Таким образом, в пределах вышеперечисленных участков наблюдается явное превышение ПДК (СО), несоответствие городской планировки и загрузки улиц автотранспортом. Это определяет потенциальную угрозу воздействия угарного газа на население микрорайонов.
Угарный газ очень опасен, так как не имеет запаха и цвета, вызывает отравление и даже смерть. Класс опасности по классификации ООН — 2,3. Вторичная опасность по классификации ООН — 2,1.
Природные фоновые уровни оксида углерода колеблются в пределах от 0,01 до 0,23 мг/м3. В зоне городских автомагистралей крупных европейских городов его средние концентрации за 8 ч составляют, как правило, менее 20 мг/м3, а пиковые величины за 1 ч — ниже 60 мг/м3.
Взвешенные частицы сами по себе и в комбинации с другими загрязнителями представляют очень серьезную угрозу для здоровья человека. Они составляют 40–70 % от всей дымовой взвеси. Концентрации, значительно превышающие 100 мкг/м3 и выраженные в виде ежедневной осредненной концентрации РМ10 (массовая концентрация взвешенных частиц), начинают влиять на показатели смертности, статистику возникновения респираторных и сердечно– сосудистых заболеваний, а также на другие показатели состояния здоровья. Именно по этой причине в пересмотренном варианте критериев качества атмосферного воздуха, рекомендованных ВОЗ для стран Европы, не дается рекомендуемый критерий по краткосрочным осредненным концентрациям. Исходя из рекомендаций ВОЗ, в странах ЕС установлены пределы порогового воздействия для РМ10. Для среднесуточной концентрации не допускается превышения порогового уровня 50 мкг/м3 более чем 35 раз в течение года, среднегодовая концентрация не должна превышать уровня в 40 мкг/м3.
Во многих странах принимаются меры по снижению концентрации окиси углерода в атмосферном воздухе промышленных городов. В частности, во Франции «Plan National Santé Environnement (2004–2008)» — «Национальный план оздоровления окружающей среды на 2004–2008 годы» предусматривал уменьшить число смертей от отравления окисью углерода на 30 %. Следовательно, необходимо обеспечить качество воздуха во всех городах страны на уровне европейских показателей, а также сократить на 30 % выбросы двигателей транспортных средств в результате модернизации вновь выпускаемых автомобилей и установки специальных фильтров на уже эксплуатируемые транспортные средства.
Литература:
- Луканин В. Н., Буслаев А. П., Трофименко Ю. В. Автотранспортные потоки и окружающая среда. — М.: ИНФРА-М, 1998. — 408 с.
- Юрина С. В. Геоэкология и природопользование: методические указания. Оренбург: Изд-во ОГПУ, 2001. — 28c
- Ясаманов Н. А. Основы геоэкологии: Учебное пособие для экологических специальностей вузов. М.: Издательский центр «Академия», 2003. — 352 с.
Основные термины (генерируются автоматически): окружающая среда, угарный газ, оксид углерода, автомобиль, атмосферный воздух, проезжая часть дороги, воздушная среда, здоровье человека, малая скорость, транспортный поток.
Что такое угарный газ?
Окись углерода (CO), которую представляет собой угарный газ, возникает в результате неполного сгорания природного газа. Он не имеет выражения цветового, вкусового или запахом. Именно эти факторы являются причиной того, что отравление данным веществом может происходить незаметно.
Даже небольшие концентрации СО в воздухе, вдыхаемом человеком, способны привести к нежелательным последствиям: головные боли, удушье, приступы кашля, головокружения и др.
Если измеряемые концентрации СО превышают допустимые дозы, человек теряет сознание, наступает паралич и он довольно быстро погибает.
Источники появления угарного газа в помещении
Угарный газ может появиться на рабочем месте из различных источников, включая приборы и оборудование, работающее на горючих газах, а также из скважин или подземных каналов.
Также угарный газ может быть продуктом распада органических веществ или производства горючих газов.
Причинами повышения концентрации СО в воздухе на рабочих местах могут быть:
- отсутствие вентиляции;
- плохая циркуляция воздуха по причине засорённости вентиляционных каналов;
- отсутствие герметичности между нагревательным элементом (котлом) и дымоходом;
- неисправности в автомобиле, связанные с выхлопной трубой (утечка газа в салон, кабину);
- использование газового оборудования для обогрева помещения с нарушением норм и требований;
- нарушение требований охраны труда при покрасочных работах, связанных с веществами, содержащими дихлорметан;
- использование неисправного оборудования с открытой камерой сгорания и др.
Симптоматика при отравлении угарным газом.
Первыми и наиболее типичными симптомами при отравлении таким газом, как СО, являются:
- приступы тошноты и рвоты;
- головные боли;
- усталость и сонливость;
- боли в области живота;
- появление одышки;
- затруднённое дыхание.
Не только концентрация, но и длительность воздействия на человека данного газа имеет прямую зависимость на уровень негативного влияния. Чем дольше человек вдыхает воздух, насыщенный СО, тем серьёзнее последствия будут.
Как не допустить отравления угарным газом
Чтобы предотвратить отравление угарным газом на рабочем месте, необходимо принимать следующие меры:
- установить систему вентиляции, которая будет предотвращать накопление угарного газа в помещении;
- проводить испытания вентиляционных установок и проверку эффективности вентиляционных систем;
- обеспечить достаточное по мощности приточное воздухообменное оборудование;
- использовать системы детектора газа, чтобы определять наличие и концентрацию угарного газа на рабочем месте;
- следить за тем, чтобы приборы и оборудование были правильно подключены и исправно работали;
- использовать средства индивидуальной защиты, такие как маски и очки для защиты от угарного газа;
- ограничить доступ к помещению для лиц, не имеющих отношения к производственным процессам.
Как измерить концентрацию угарного газа в помещении?
Для измерения уровня угарного газа на рабочем месте рекомендуется использовать специальное измерительное оборудование. Современные приборы позволяют получать довольно точные показатели концентрации газов, в том числе СО.






