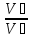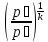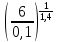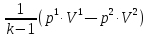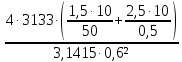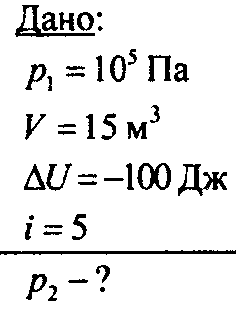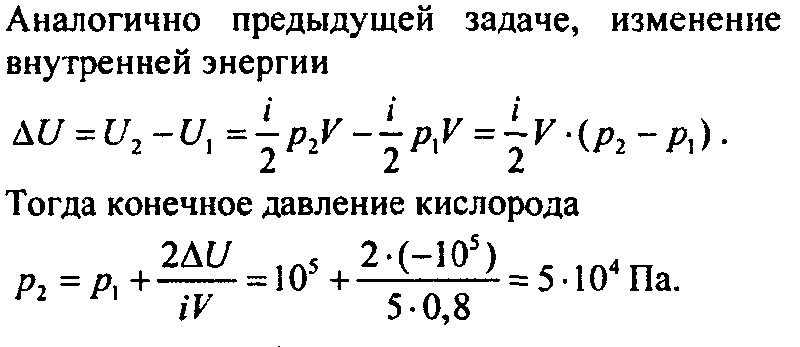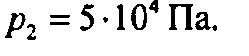найти давление кислорода?
Hasmik
Ученик
(165),
на голосовании
13 лет назад
в баллоне объемом V= 100л находится m=2,5кг сжатого кислорода при температуре t=20 C. Найти давление кислорода.
Голосование за лучший ответ
Андрей Степанов
Просветленный
(22749)
13 лет назад
Уравнение состояния идеального газа (Менделеева-Клайперона) :
PV = nRT
где n – количество молей газа, R – универсальная газовая постоянная.
Считаем что кислород – газ идеальный (ну приблизительно) .
Все составляющие даны в условии задачи. Подставляете – находите давление.
2018-09-21
Кислород, занимающий при давлении $p_{1} = 1 МПа$ объем $V_{1} = 5 л$, расширяется в $n = 3$ раза. Определите конечное давление и работу совершенную газом. Рассмотрите следующие процессы: 1) изобарный и изотермический; 3) адиабатный.
Решение:
$Q = Delta U + A$,
$A = p Delta V$,
1) Изобарный процесс
$p = const$
$p = p_{1} = 1 Мпа$
$A = p_{1} Delta V = p_{1} (V – V_{1} ) = p_{1}V_{1} (n – 1) = 10 кДж$,
2) Изотермический процесс
$T = const, p_{1}V_{1} = pV, p = frac{p_{1}V_{1} }{V} = 0,33 МПа$,
$A = int_{V_{1} }^{V_{2} } p dV = p_{1}V_{1} int_{V_{1} }^{V_{2} } frac{dV}{V} = p_{1}V_{1} ln frac{V}{V_{1} } = 5,5 кДж$,
3) Адиабатный процесс
$Q = 0, A= – Delta U, pV^{ gamma} = const$,
$p = p_{1} left ( frac{V_{1} }{V} right )^{ gamma}, gamma = frac{i + 2}{i} = 1,4, p = p_{1}n^{ – gamma} = 0,21 МПа$,
$Delta U = frac{m}{M} C_{V} (T – T_{1} ), A = frac{m}{2} frac{i}{2}R( T_{1} – T ), p_{1}V_{1} = frac{m}{M}RT_{1}$,
$pV = frac{m}{M}RT, A = frac{i}{2} ( p_{1}V_{1} – pV ) = 4,63 кДж$.
Федеральное
агентство по образованию
Пермский
государственный технический университет
|
Контрольная |
|
По предмету « |
Вариант№41
Выполнил:
студентка группы ТСП- 07
Проверил:
Селянинов Ю. А
Задача
№1
2
кг кислорода с начальным давлением
p1=6
МПа и начальной температурой t1=17
℃
расширяются до конечного давления
p2=0,1
МПа. Определить объем кислорода в начале
и в конце расширения и работу расширения.
О2
m=
2 кг
p1=6МПа
t1=17
℃
p2=
0,1 МПа = 0,1∙106
Па
V1,
V2,
ℓ=?
Для
идеального кислорода:
молярная
масса μ=32 кг/моль;
мольная
теплоемкость кислорода при постоянном
объеме ( как двухатомного газа) μ∙сυ
=20,8
кДж/(кмоль∙К) ( методичка, таблица на
стр.46);
мольная
теплоемкость кислорода при постоянном
давлении μ∙сp=29,1кДж/(кмоль∙К)
Считаем
процесс расширения кислорода адиабатным
– происходящим без теплообмена с
окружающей средой.
Уравнение
Клапейрона для начального состояния
кислорода:
p1∙V1=
m∙R∙T1
,
где R
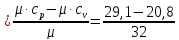
кДж/(кг∙К)=259
Дж/(кг∙К)- удельная газовая постоянная
кислорода ( можно было взять в таблице
1 приложений, ст. 67 методички), Т1=
273о+t1=273o+17o=290o–
абсолютная начальная температура
процесса; отсюда , объем кислорода в
начале расширения V1=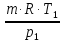
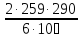
Из
уравнения адиабатного процесса
=
,где k=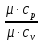
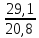
показатель адиабаты кислорода;
Найдем
конечный объем кислорода
V₂=V₁∙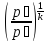
=0,466 м3
Работа
расширения ℓ=
=
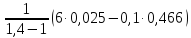
Дж = 258,5кДж.
Задача
№15
Влажный
пар с начальным давлением p1=6
МПа и степенью сухости 𝑥=0,9
расширяется изотермически до давления
𝑝₂=0,5 МПа. Определить параметры пара
в начальном и конечном состояниях,
изменение внутренней энергии, количество
переданной теплоты пару и работу
расширения. Изобразить тепловой процесс
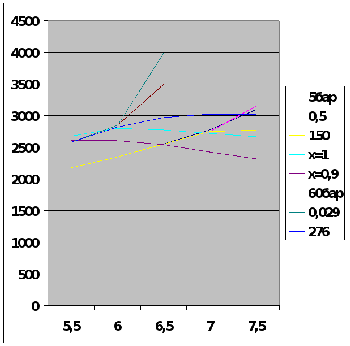
в is-диаграмме.
Влажный
пар;
𝑝₁=6МПа=
6∙10⁶Па=
60бар;
𝑥₁=0,9;
𝑝₂=0,5∙10⁶
МПа;
T=const.
Параметры
∆W,
Q
,ℓ=?
Параметры
влажного пара в начальном состоянии
1(при заданных 𝑝₁=6МПа=
60 бар и 𝑥₁=0,9)
по is-диаграмме:
Температура
t₁=276℃
(Т=549K);
Удельный
объём V₁=0,029м3/кг;
Энтальпия
i₁=2625кДж/кг;
Энтропия
s₁=
5,60 кДж/(кг∙K).
Проверка.
Параметры влажного пара в состоянии
1 по таблице3 приложений в методичке на
стр.68:
t₁=275,56℃
(Т₁=273,15+275,56=548,71K);
V₁’=0,0013185м3/кг;
V₁”=0,03243
м3/кг;
i₁’=1213,9
кДж/кг;
i₁”=2784,4
кДж/кг;
r=1570,5
кДж/кг;
s₁’=3,0276
кДж/(кг∙K);
s₁”=5,8894
кДж/(кг∙K).
Тогда
Vₓ₁=V₁”∙𝑥
–(1-𝑥)∙V₁’=0,03243∙0,9-(1-0,9)∙0,0013185=0,029
м3/кг;
iₓ₁=i₁’+r∙𝑥=1213+1570,5∙0,9=2626,5
кДж/кг;
sₓ₁=s₁’+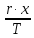
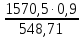
кДж/(кг∙K).
Правильность
нахождения параметров пара в начальном
состоянии, найденных по is-диаграмме,
подтверждена вычислениями этих
параметров, взятых по таблице.
При
давлении 𝑝₂=0,5
МПа=5 бар температура насыщенного пара
tn=150℃(
по is-диаграмме). Т. к. действительная
температура пара t2=t₁=276℃
>
tn
то пар будет перегретым.
Параметры
перегретого пара в конечном состоянии
2( при заданных 𝑝2=0,5МПа
и t2=276℃)
по is-диаграмме:
V2=0,50
м3/кг;
i2=3010
кДж/кг;
s2=7,38
кДж/(кг∙K).
Изменение
внутренней энергии пара ∆U=(i2−i₁)−(𝑝2V2
─
𝑝₁V₁)=
(3010─2625)∙10³ ─ ( 0,5∙0,50 ─6∙0,029)∙106=
309000 Дж/кг=309 кДж/кг
Количество
переданной пару теплоты q=T(s₁─s2)=549(
7,38─5,60)=977 кДж/кг.
Работа
расширения ℓ=q─∆V=977─309=668
кДж/кг.
Тепловой
процесс изображен на is-диаграмме:
В
области влажного пара наклонная прямая
изотермы 276℃
и изобары 60бар совпадают.
Задача
№29
20
кг. воды, находящейся в котле , нагревают
на газовой плите. Через 2 часа после
начала кипения объём воды уменьшился
вдвое. Определить количество теплоты
, поступающей в котел , и температуру
дна котла со стороны пламени, если
диаметр дна котла d=600
мм , толщина металла 𝛿₁=1,5
мм, толщина накипи 𝛿₂=0,25мм, коэффициент
теплопроводности металла 𝜆₁=50
Вт/(м∙К), коэффициент теплопроводности
накипи 𝜆₂=0,5 Вт/(м∙К),
температура дна котла со стороны кипящей
воды 𝑡ст˝=105℃
и
теплота парообразования 𝑟=2256
кДж/кг.
Н₂O;
m=20кг;
𝜏=2ч=
7,2∙103с;
V₁=
D=
600мм= 0,6 м;
𝛿₁=1,5мм=1,5∙10-3м;
𝛿₂=0,25мм=
0,25∙10-3м;
𝜆₁=50Вт/(м∙К);
𝜆₂=0,5
Вт/(м∙К);
𝑡ст˝=105℃;
𝑟=2256
кДж/кг=2,256∙106
Дж/кг.
𝑄,
𝑡ст′=?
Количество
теплоты ,поступающей в котел ( тепловой
поток),
𝑄=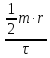
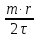
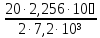
3133Дж/с=3,1 кВ
Площадь
стенки котла ( круглого дна): F=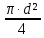
Уравнение
теплопроводности через двухслойную
стенку
𝑄=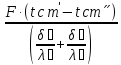
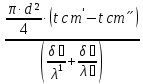
отсюда
𝑡ст′=
𝑡ст˝+
=105+
= 105+5,95=111℃.
Соседние файлы в предмете Теплотехника
- #
- #
- #
- #
- #
- #
- #
Рекомендуемые сообщения
Решение задач по фото за 30 минут! Мы онлайн – кликай!
-
- Поделиться
Помогите с последней задачкой из контрольной, пожалуйста, люди добрые!
Рассчитать давление кислорода (мм.рт.ст.) над кристаллическим оксидом по значению энергии Гиббса реакции синтеза оксида металла из элементов Fe(k)+1|2O2=FeO(k)
dG=-251кДж
Очень – очень прошу, перерыла все что было можно, но доходчивой формулы не нашла, и еще как Па перевести в мм.рт.ст.?
Ссылка на комментарий
–>
-
- Поделиться
как Па перевести в мм.рт.ст.?
P(давление)=плотность*g*высоту столба жидкости.
плотность ртути-13600кг/м^3
g=9,8м/с^2 – ускорение своьодного падения
высота столба жидкости =1мм=0,001м
P=133,3Па=1мм. рт. ст.
Ссылка на комментарий
-
- Поделиться
Помогите с последней задачкой из контрольной, пожалуйста, люди добрые!
Рассчитать давление кислорода (мм.рт.ст.) над кристаллическим оксидом по значению энергии Гиббса реакции синтеза оксида металла из элементов Fe(k)+1|2O2=FeO(k)
dG=-251кДж
Очень – очень прошу, перерыла все что было можно, но доходчивой формулы не нашла, и еще как Па перевести в мм.рт.ст.?
Надо рассмотреть обратную реакцию – разложение оксида железа
FeO(k) = Fe(k) + 0,5O2
Константа равновесия Kp этой реакции запишется так:
Kp = P0.5(O2). (1) Давления остальных веществ сюда не входят т.к. они твердые (а не газы)
Теперь надо найти Kp исходя из энергии Гиббса реакции . Энергия Гиббса прямой реакции равна с обратным знаком энергии Гиббса обратной реакции
ΔG = 251кДж
ΔG связано с Kp:
ΔG = -RTlnKp (2)
Остается найти Kp из 2 и посчитать, а затем из (1) выразить P(O2).
Ссылка на комментарий
- Автор
-
- Поделиться
Спасибо, вы даже не представляете как помогли мне!))))) да еще так быстро!!! Отдельное спасибо Wergilius, уже второй раз меня выручил!
Ссылка на комментарий
Для публикации сообщений создайте учётную запись или авторизуйтесь
Вы должны быть пользователем, чтобы оставить комментарий
Войти
Уже есть аккаунт? Войти в систему.
Войти
9. Термодинамика. §54. Внутренняя энергия. Задачи → номер 3 3. Молекулярный кислород находится под давлением 105 Па в сосуде объемом 0,8 м3. При изохорном охлаждении внутренняя энергия газа уменьшается на 100 кДж. Чему равно конечное давление кислорода? [5 ⋅ 104 Па]
3.
Решение:
Ответ: