На этой странице вы узнаете
- В чем прелесть фазовых переходов?
- Что лучше выбрать: Mercedes или BMW?
Люди научились летать в космос, покорять недра Земли и погружаться в глубины океана. Эти и другие достижения возможны благодаря способности извлекать максимум пользы из имеющихся ресурсов,а именно получать тепловую энергию различными доступными способами. Сегодня мы разберем задачи, которые заставят тепловые процессы играть на нашей стороне.
Тепловые машины и их КПД
Рекомендация: перед тем как приступить к выполнению задач неплохо было бы повторить тему «Уравнение состояния идеального газа» . Но ключевую теорию, на которой основано решение задач, сейчас разберем вместе.
Вспомним, что фазовые переходы — это переход из одного агрегатного состояния в другое. При этом может выделяться большое количество теплоты.
Именно благодаря этому они и стали такими полезными для нас. Например, в ядерных реакторах воду используют в качестве рабочего тела, то есть она нагревается вследствие энергии, полученной из ядерных реакций, доходит до температуры кипения, а затем под большим давлением уже в качестве водяного пара воздействует на ротор генератора, который вращается и дает нам электроэнергию! На этом основан принцип работы атомных электростанций.
А самый простой пример фазового перехода — образование льда на лужах в морозные ноябрьские дни. Правда о выделении тепла здесь речи не идет.
Мы не почувствуем, как испарится капелька у нас на руке, потому что это не требует много тепла от нашего тела. Но мы можем наблюдать, как горят дрова в мангале, когда мы жарим шашлык, потому что выделяется огромное количество теплоты. А зачем мы вообще рассматриваем эти фазовые переходы? Все дело в том, что именно фазовые переходы являются ключевым звеном во всех процессах, где нас просят посчитать КПД, от них нашему рабочему телу и подводится теплота нагревателя.

Человечество придумало такие устройства, которые могут переработать тепловую энергию в механическую.
Тепловые двигатели, или тепловые машины, — устройства, способные преобразовывать внутреннюю энергию в механическую.
Их устройство довольно просто: они на входе получают какую-то энергию (в основном — энергию сгорания топлива), а затем часть этой теплоты расходуется на совершение работы механизмом. Например, в автомобилях часть энергии от сгоревшего бензина идет на движение. Схематично можно изобразить так:
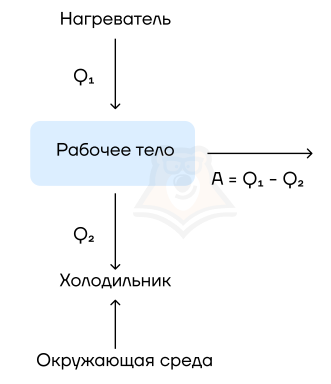
Рабочее тело — то, что совершает работу — принимает от нагревателя количество теплоты Q1, из которой A уходит на работу механизма. Остаток теплоты Q2 рабочее тело отдает холодильнику, по сути — это потеря энергии.
Физика не была бы такой загадочной, если б все в ней было идеально. Как и в любом процессе или преобразовании, здесь возможны потери, зачастую очень большие. Поэтому «индикатором качества» машины является КПД, с которым мы уже сталкивались в механике:
Коэффициент полезного действия (КПД) тепловой машины — это отношение полезной работы двигателя к энергии, полученной от нагревателя.
(eta) — КПД,
A — работа газа (Дж),
Q1 — количество теплоты, полученное от нагревателя (Дж).
Мы должны понимать, что КПД на практике никогда не получится больше 1, поскольку всегда будут тепловые потери.
Полезную работу можно расписать как Q1 — Q2 (по закону сохранения энергии). Тогда формула примет вид:
(eta = frac{Q_1 — Q_2}{Q_1} = 1 — frac{Q_2}{Q_1})
Давайте попрактикуемся в применении данной формулы на задаче номер 9 из ЕГЭ.
Задача. Тепловая машина, КПД которой равен 60%, за цикл отдает холодильнику 100 Дж. Какое количество теплоты за цикл машина получает от нагревателя? (Ответ дайте в джоулях).
Решение:
Давайте сначала вспомним нашу формулу для КПД:
(eta = frac{Q_1 — Q_2}{Q_1}),
где (Q_1) — это теплота, которую тело получает от нагревателя, (Q_2) — теплота, которая подводится к холодильнику.
Тогда отсюда можно вывести искомую теплоту нагревателя:
(eta Q_1 =Q_1-Q_2)
(eta Q_1 — Q_1= -Q_2)
(Q_1=frac{- Q_2}{eta-1}=frac{-100}{0,6-1}=250 Дж).
Ответ: 250 Дж
Цикл Карно
Мы знаем, что потери — это плохо, поэтому должны предотвращать их. Как это сделать? Нам ничего делать не нужно, за нас уже все сделал Сади Карно, французский физик, разработавший цикл, в котором машины достигают наивысшего КПД. Этот цикл носит его имя и состоит из двух изотерм и двух адиабат. Рассмотрим, как этот цикл выглядит в координатах p(V).
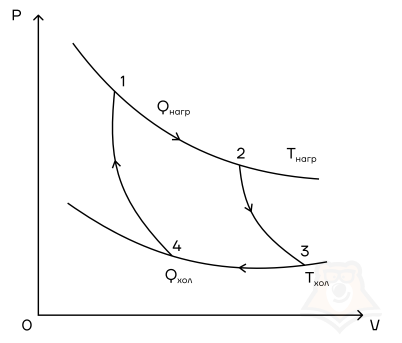
- Температура верхней изотермы 1-2 — температура нагревателя (так как теплота в данном процессе подводится).
- Температура нижней изотермы 3-4 — температура холодильника (так как теплота в данном процессе отводится).
- 2-3 и 4-1 — это адиабатические расширение и сжатие соответственно, в них газ не обменивается теплом с окружающей средой.
Цикл Карно — цикл идеальной тепловой машины, которая достигает наивысшего КПД.
Формула, по которой можно рассчитать ее КПД выражается через температуры:
T1 — температура нагревателя,
T2 — температура холодильника.
Не то круто, что красиво, а то, что по Карно работает! Поэтому присматривайте такой автомобиль, у которого высокий КПД.
Интересно, что максимальный уровень КПД двигателя внутреннего сгорания автомобилей на данный момент всего около 43%. По официальным заявлениям компания Nissan Motor с 2021 года испытывает прообраз двигателя нового поколения с планируемым КПД 50%.
Приступим к задачам
Задачи на данную тему достаточно часто встречаются в задании 27 из КИМа ЕГЭ. Давайте разберем некоторые примеры.
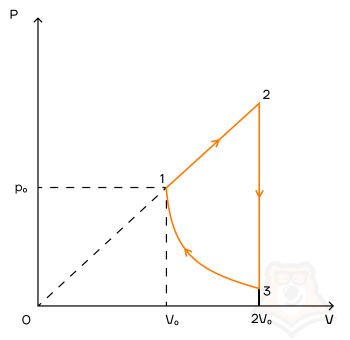
Задание 1. Одноатомный газ совершает циклический процесс, как показано на рисунке. На участке 1–2 газ совершает работу A12 = 1520 Дж. Участок 3–1 представляет собой адиабатный процесс. Количество теплоты, отданное газом за цикл холодильнику, равно |Qхол| = 4780 Дж. Найдите работу газа |A13| на адиабате, если количество вещества постоянно.
Решение:
Шаг 1. Первое, с чего лучше начинать задачи по термодинамике — исследование процессов.
Посмотрим на участок 1-2 графика: продолжение прямой проходит через начало координат, поэтому график функционально можно записать, как p = aV, где a — какое-то число, константа. Графиком является не изотерма, поскольку график изотермы в координатах p-V — гипербола. Из уравнения Менделеева-Клапейрона следует: (frac{pV}{T} = const). Отсюда можно сделать вывод, что возрастает температура, так как растут давление и объем. Температура и объем растут, значит, увеличивается и внутренняя энергия и объем соответственно.
Участок 2-3: процесс изохорный, поскольку объем постоянен, следовательно, работа газом не совершается. Рассмотрим закон Шарля: (frac{p}{T} = const). Давление в этом процессе растет, тогда растет и температура, поскольку дробь не должна менять свое значение. Делаем вывод, что внутренняя энергия тоже увеличивается.
Участок 3-1: адиабата по условию, то есть количество теплоты в этом переходе равна нулю из определения адиабатного процесса. Работа газа отрицательна, так как газ уменьшает объем.
Оформим все данные в таблицу.
Определим знаки Q, используя первый закон термодинамики: Q = ΔU + A.

Из этих данных сразу видно, что количество теплоты, отданное холодильнику — это количество теплоты в процессе 2-3.
Шаг 2. Первый закон термодинамики для процесса 1-2 запишется в виде:
Q12 = ΔU12 + A12.
Работа A12 — площадь фигуры под графиком процесса, то есть площадь трапеции:
(A_{12} = frac{p_0 + 2p_0}{2} * V0 =frac{3p_0V_0}{2}).
Запишем изменение внутренней энергии для этого процесса через давление и объем. Мы выводили эту формулу в статье «Первое начало термодинамики»:
(Delta U_{12} = frac{3}{2}(2p_0 * 2V_0 — p_0V_0) = frac{9p_0V_0}{2}).
Заметим, что это в 3 раза больше работы газа на этом участке:
(Delta U_{12} = 3A_{12} rightarrow Q_{12} = 4A_{12}).
Шаг 3. Работа цикла — площадь фигуры, которую замыкает график, тогда . A = A12 — |A31|. С другой стороны, работа цикла вычисляется как разность между энергиями нагревателя и холодильника: A = Q12 — |Q31|.
Сравним эти формулы:
Q12 -|Q31| = A12 — |A31|,
подставим выражения из предыдущего пункта:
4A12 — |Q31| = A12 — |A31| (rightarrow) |A31| = -3A12 + |Q31| = -31520 + 4780 = 220 Дж.
Ответ: 220 Дж
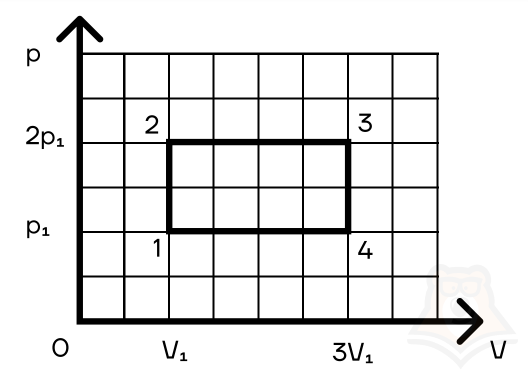
Задание 2. Найти КПД цикла для идеального одноатомного газа.
Решение:
Шаг 1. КПД цикла определим по формуле: (eta = frac{A}{Q}), где Q — количество теплоты от нагревателя, а А — работа газа за цикл. Найдем А как площадь замкнутой фигуры: A = (2p1 — p1)(3V1 — V1) = 2p1V1.
Шаг 2. Найдем процесс, который соответствует получению тепла от нагревателя. Воспользуемся теми же приемами, что и в прошлой задаче:
Посмотрим на участок 1-2 графика: давление растет, объем не меняется. По закону Шарля (frac{p}{T} = const) температура тоже растет. Работа газа равна 0 при изохорном процессе, а изменение внутренней энергии положительное.
2-3: давление не меняется, растет объем, а значит, работа газа положительна. По закону Гей-Люссака (frac{V}{T} = const) температура тоже растет, растет и внутренняя энергия.
3-4: давление уменьшается, следовательно, и температура уменьшается. При этом процесс изохорный и работа газа равна 0.
4-1: давление не меняется, объем и температура уменьшаются — работа газа отрицательна и внутренняя энергия уменьшается.
Оформим данные в таблицу:
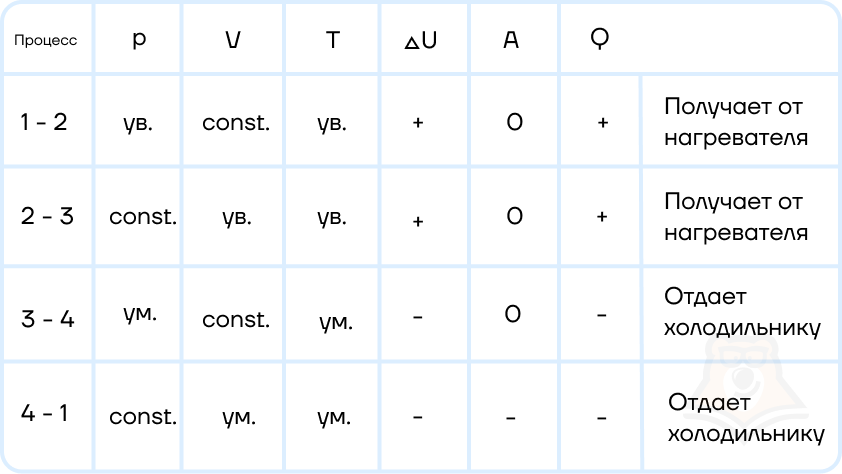
Отметим, что необходимое Q = Q12 + Q23.
Шаг 3. Запишем первый закон термодинамики для процессов 1-2 и 2-3:
(Q_{12} = U_{12} + A_{12} = Delta U_{12} = frac{3}{2}(2p_1V_1 -p_1V_1) = frac{3}{2}p_1V_1).
(Q_{23} = Delta U_{23} + A_{23}), работу газа найдем как площадь под графиком: A23 = 2p1(3V1 — V1) = 4p1V1.
(Delta U_{12} = frac{3}{2}(2p_1 * 3V_1 — 2p_1V_1) = 6p_1V_1).
(Q_{23} = Delta U_{23} + A_{23} = 10p_1V_1).
Шаг 4. Мы готовы считать КПД: (eta = frac{A}{Q} = frac{A}{Q_{12} + Q_{23}} = frac{2p_1V_1}{frac{3}{2}p_1V_1 + 10p_1V_1} = frac{4}{23} approx 0,17).
Ответ: 17%
Теперь вас не должно настораживать наличие графиков в условиях задач на расчет КПД тепловых машин. Продолжить обучение решению задач экзамена вы можете в статьях «Применение законов Ньютона» и «Движение точки по окружности».
Фактчек
- Тепловые двигатели — устройства, способные преобразовывать внутреннюю энергию в механическую.
- Тепловая машина принимает тепло от нагревателя, отдает холодильнику, а рабочим телом совершает работу.
- Коэффициент полезного действия (КПД) тепловой машины — это отношение полезной работы двигателя к энергии, полученной от нагревателя.
(eta = frac{A}{Q_1} = frac{Q_1 — Q_2}{Q_1} = 1 — frac{Q_2}{Q_1}) - Цикл Карно — цикл с максимально возможным КПД: (eta = frac{T_1 — T_2}{T_1} = 1 — frac{T_2}{T_1})
- Не забываем, что работа считается, как площадь фигуры под графиком.
Проверь себя
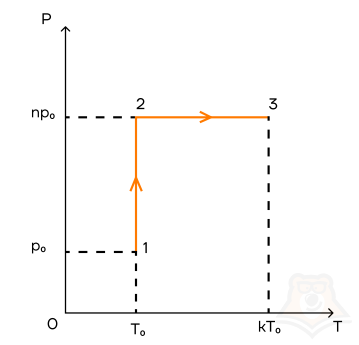
Задание 1.
1 моль идеального газа переходит из состояния 1 в состояние 2, а потом — в состояние 3 так, как это показано графике. Начальная температура газа равна T0 = 350 К. Определите работу газа при переходе из состояния 2 в состояние 3, если k = 3, а n = 2.
- 5672 Дж
- 4731 Дж
- 5817 Дж
- 6393 Дж
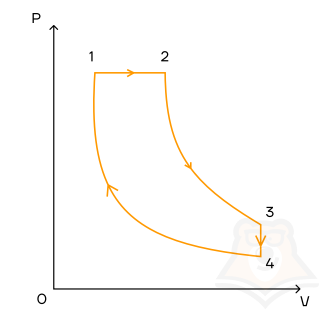
Задание 2.
1 моль идеального одноатомного газа совершает цикл, который изображен на pV-диаграмме и состоит из двух адиабат, изохоры, изобары. Модуль отношения изменения температуры газа при изобарном процессе ΔT12 к изменению его температуры ΔT34 при изохорном процессе равен 1,5. Определите КПД цикла.
- 0,6
- 0,5
- 0,8
- 1
Задание 3.
В топке паровой машины сгорело 50 кг каменного угля, удельная теплота сгорания которого равна 30 МДж/кг. При этом машиной была совершена полезная механическая работа 135 МДж. Чему равен КПД этой тепловой машины? Ответ дайте в процентах.
- 6%
- 100%
- 22%
- 9%
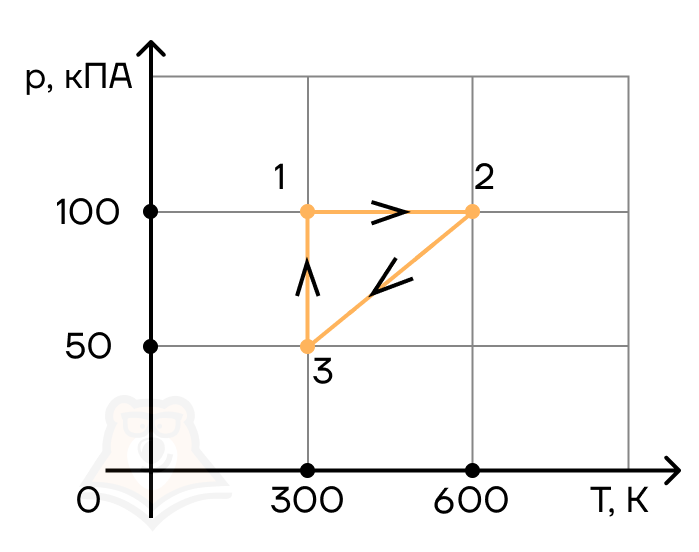
Задание 4.
С двумя молями одноатомного идеального газа совершают циклический процесс 1–2–3–1 (см. рис.). Чему равна работа, совершаемая газом на участке 1–2 в этом циклическом процессе?
- 4444 Дж
- 2891 Дж
- 4986 Дж
- 9355 Дж
Ответы:1 — 3; 2 — 1; 3 — 4; 4 — 3.
Полное условие задачи
Найдите КПД цикла, изображенного на рисунке для идеального одноатомного газа.
Краткое условие задачи
Решение задачи
КПД цикла находим по формуле:
где работа определяется как площадь прямоугольника 1234:
Для определения затраченного количества теплоты нужно выяснить, в каких процессах газ получал теплоту. Для этого воспользуемся первым законом термодинамики, формулой для изменения внутренней энергии и уравнением состояния идеального газа:
Рассмотрим каждый процесс по отдельности.
В процессе 1 – 2 начальная температура меньше конечной:
поэтому изменение внутренней энергии больше нуля:
а работа равна нулю, поскольку процесс изохорный:
Отсюда следует, что газ в процессе 1 – 2 получал тепло:
Найдем это тепло:
Разность температур найдем используя уравнение состояния идеального газа. Запишем его для состояния 1 и для состояния 2:
Вычитаем из второго уравнения первое и находим разность температур:
Подставим в формулу для теплоты:
В процессе 2 – 3 начальная температура также меньше конечной:
поэтому изменение внутренней энергии также больше нуля:
а работа в этом процессе больше нуля (газ совершает работу):
поскольку объем увеличивается:
Отсюда следует, что газ в процессе 2 – 3 тоже получал тепло:
Найдем это тепло:
Разность температур найдем используя уравнение состояния идеального газа. Запишем его для состояния 2 и для состояния 3:
Вычитаем из второго уравнения первое и находим разность температур:
Подставим в формулу для теплоты:
В процессе 3 – 4 начальная температура больше конечной:
поэтому изменение внутренней энергии меньше нуля:
а работа равна нулю, поскольку процесс изохорный:
Отсюда следует, что газ в процессе 3 – 4 отдает тепло:
В процессе 4 – 1 начальная температура также больше конечной:
поэтому изменение внутренней энергии также меньше нуля:
работа в этом процессе тоже меньше нуля (над газом совершают работу):
поскольку объем уменьшается:
Отсюда следует, что газ в процессе 4 – 1 тоже отдает тепло:
Таким образом затраченная теплота равна:
Искомый КПД равен:
Или
Ответ: 17 %.
Речь в статье пойдет о КПД различных циклов, проводимых с газом. При этом давайте помнить, что внутренняя энергия изменяется тогда, когда изменяется температура, а в адиабатном процессе передачи тепла не происходит, то есть для совершения работы в таком процессе газ “изыскивает внутренние резервы”. Кроме того, работа численно равна площади под кривой процесса, а работа за цикл – площади внутри цикла.
Задача 1.
На рисунке представлена диаграмма цикла с одноатомным идеальным газом. Участки и
– адиабаты. Вычислите КПД
данной тепловой машины и максимально возможный КПД
.

К задаче 1
КПД тепловой машины можно вычислить как
Машина получает тепло только на участке AB, и, так как работы здесь не совершается, то можно вычислить количество теплоты, полученное газом, как увеличение его внутренней энергии:
Работа численно равна площади, ограниченной циклом. Поэтому
Участк и
по условию – адиабаты, то есть передачи тепла газу на этих участках не происходит, следовательно, работа будет совершена за счет «внутренних резервов» – то есть внутренней энергии. Нужно, следовательно, найти, как она изменилась.
Задачу можно решить двумя способами. Во-первых, просто определить температуры в точках и
,
и
, это легко сделать из данных графика с помощью уравнения Менделеева-Клапейрона, и затем посчитать
. Но, так как
, а
,то изменение внутренней энергии будет равно
Определим максимальный КПД. Посчитаем его как КПД цикла Карно. Максимальная температура газа будет достигнута в точке , а минимальная – в точке
:
Ответ: ,
.
Задача 2.
Над идеальным одноатомным газом проводят цикл, включающий изобару, изохору, изотерму, при этом работа газа за цикл равна кДж. В процессе изотермического сжатия (3-1) внешние силы совершают над газом положительную работу
кДж. Найдите КПД данной тепловой машины.

К задаче 2
Работа газа в процессе 1-2– площадь под линией процесса 1-2. Работа внешних сил – площадь под циклом (под линией 3-1). Поэтому полная работа за цикл – это разность работы газа и работы внешних сил, площадь, ограниченная линиями цикла. Она будет равна 5 кДж.
Работа газа в процессе 1-2, таким образом, равна 8 кДж. А поскольку процесс изобарный, то кДж. Тогда КПД
Ответ: .
Задача 3.
КПД тепловой машины, работающей по циклу, включающему изотермический (1-2) и адиабатный (3-1) процессы, равен , причем работа, совершенная 2 моль одноатомного идеального газа в изотермическом процессе
кДж. Найдите разность
максимальной и минимальной температур газа в цикле.

К задаче 3
Полная площадь под кривой процесса 1-2 равна кДж. При этом, так как КПД машины 25%, то площадь внутри цикла равна
, а под кривой 3-1 –
. В процессе 1-2 изменения внутренней энергии не было, так как температура не менялась, а в процессе 3-1 газу не передавали тепло, следовательно, работа совершена за счет внутренней энергии. Т.е.
Ответ: 500 K.
Описание презентации по отдельным слайдам:
-

1 слайд
1
Алгоритм решения задач на определение к.п.д. теплового цикла по графику зависимости давления от объема.
-

2 слайд
2
Задача на определение коэффициента полезного действия по графику зависимости давления от объема.
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
Рассчитайте КПД тепловой машины, использующей в качестве рабочего тела одноатомный идеальный газ и работающей по циклу, изображен-ному на рисунке. -

3 слайд
3
Задача на определение коэффициента полезного действия по графику зависимости давления от объема.
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
Рассчитайте КПД тепловой машины, использующей в качестве рабочего тела одноатомный идеальный газ и работающей по циклу, изображенному на рисунке.
Подсказка№1
Подсказка№2
Алгоритм решения
Решение -

4 слайд
4
Подсказка №1
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
VСледовательно, необходимо определить в каждом процессе по изменению температуры получено, или отдано количество теплоты.
Расчет количества теплоты производят исходя из первого закона термодинамики. -

5 слайд
5
Подсказка №2
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
Работа, выполненная в каком-либо процессе, численно равна площади фигуры заключенной под графиком в координатах P(V). Площадь заштрихованной фигуры равна работе в процессе 2-3, а площадь закрашенной фигуры – работе в процессе 4-1, причем именно эта работа газа отрицательна, т.к. от 4 к 1 объём уменьшается.
Работа за цикл равна сумме этих работ. Следовательно работа газа за цикл численно равна площади этого цикла. -

6 слайд
6
Алгоритм решения задачи.
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
1. Записать формулу КПД.
2. Определить работу газа по площади фигуры процесса в координатах P,V.
3. Проанализировать в каком из процессов поглощается , а не выделяется количество теплоты.
4.Используя 1 закон термодинамики, подсчитать полученное количество теплоты.
5. Подсчитать КПД. -

7 слайд
7
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
1. Записать формулу КПД.
2. Определить работу газа по площади фигуры процесса в координатах P,V.
Решение -

8 слайд
8
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
1. Процесс1 –2 . V = const, P T Q поглощается
2. Процесс 2 – 3. P = const, V , T Q поглощается
3. Процесс 3 – 4. V = const, P , T Q выделяется
4. Процесс 4 – 1. P = const, V , T Q выделяется
3. Проанализировать в каком из процессов поглощается , а не выделяется количество теплоты. -

9 слайд
9
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
Для процесса 1-2
4. Используя 1 закон термодинамики, подсчитать полученное количество теплоты.
следовательно
Для изохорного процесса
Вычтем из нижнего уравнения верхнее -

10 слайд
10
4. Используя 1 закон термодинамики, подсчитать полученное количество теплоты.
Для процесса 2-3
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V -

11 слайд
11
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V -

12 слайд
12
P
2P0
P0
V0
0
3V0
2V0
1
2
3
4
V
5. Подсчитать КПД.
Циклический
процесс
– изменение
состояния термодинамической системы,
в результате которого система возвращается
в первоначальное состояние. Коэффициент
полезного действия тепловой машины η
(КПД):
Для
циклического процесса, совершаемого
по часовой стрелке:
![]()
Для
циклического процесса, совершаемого
против часовой стрелки: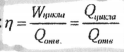
Термодинамический
цикл –
это замкнутый процесс, совершаемый
термодинамической системой, который
можно многократно повторять.
Цикл Карно
– идеальный
замкнутый процесс, состоящий из четырех
равновесных процессов – двух изотерм и
двух адиабат.
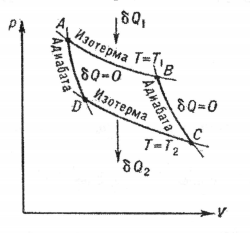
Рабочее тело
газ – последовательно изотермически
расширяется при температуре Ть
затем
адиабатически расширяется, после чего
изотермически сжимается при температуре
Т2
и, наконец, адиабатически сжимается,
возвращаясь в исходное положение.
Коэффициент
полезного действия тепловой машины η
(КПД)
в цикле Карно:
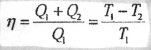
Q1 – теплота
изотермического расширения (при T1);
Q2
– теплота изотермического сжатия (при
Т2);
Т1 – температура
нагревателя;
Т2
– температура холодильника;
17.Теорема Карно. Теорема Клаузиуса. Теорема Карно-Клаузиуса. Свойства цикла Карно.
Теорема Карно–
из всех циклических процессов, совершаемых
квазистатически с идеальным газом в
качестве рабочего тела в
данном температурном интервале,
максимальным
термодинамическим КПД обладает цикл
Карно.
Теорема Клаузиуса:
КПД тепловой машины, работающей
квазистатически по циклу Карно в
данном температурном интервале
не зависит от природы рабочего тела.
Теорема
Карно-Клаузиуса:
из всех тепловых машин, работающих
квазистатически в
данном температурном интервале,
максимальным КПД независимо от природы
рабочего тела обладает машина, работающая
по циклу Карно.
Приведенная
теплота Q/T:
отношение количества теплоты к температуре
процесса.
Свойства цикла
Карно:
1. Коэффициент
полезного действия η
тепловой
машины, работающей по циклу Карно,
зависит только от разности температур
нагревателя и холодильника и не зависит
от природы рабочего тела.
2. КПД имеет
максимальное значение в данном
температурном интервале.
3. Сумма приведенных
теплот в цикле Карно равна нулю.
18.
Энтропия. Основные свойства энтропии.
Изменение энтропии как критерий
равновесия в изолированной системе.
Приведите график зависимости энтропии
от пути процесса в изолированной системе.
Как изменится энтропия (увеличится или
уменьшится) в ходе реакции: СН4(Г)
+ Н2О(г)
СО(г)
+ 3 Н2(г)
Свойства
энтропии: см. 14,15 вопрос.
Энтропия
является критерием возможности и
направления процессов, а также состояния
термодинамического равновесия в
изолированных или адиабатически-
изолированных системах. Если в
изолированной системе протекает
самопроизвольный необратимый процесс,
то энтропия возрастает ΔS>0.
Закон возрастания
энтропии (неравенство Клаузиуса): В
любой изолированной системе самопроизвольно
протекают только те процессы, которые
приводят к увеличению энтропии.
График зависимости
энтропии от пути процесса:
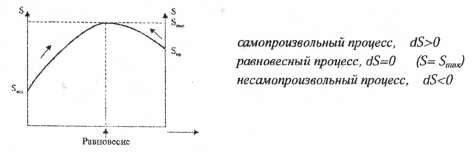
Второй закон
термодинамики для обратимых и необратимых
процессов в изолированных системах:
dS> 0
и ΔS>
О
При абсолютном
нуле (Т=0К) энтропия индивидуального
вещества, существующего в виде идеального
кристалла, равна нулю.
В ходе реакции
СН4(Г)
+ Н2О(г)
СО(г)
+ 3 Н2(г)
энтропия
увеличится.
