Согласно протонно-нейтронной модели строения атомного ядра, заряд ядра должен быть равен сумме зарядов всех протонов, которые входят в его состав. Так как заряд протона равен элементарному заряду, то можно считать, что:
(q) — заряд ядра,
(e) — элементарный заряд,
()
Z
() — количество протонов в ядре.
Количество протонов в ядре
Z
называется зарядовым числом атомного ядра.
Экспериментально было доказано, что число Z совпадает с порядковым номером химического элемента в Периодической системе Менделеева.
Обрати внимание!
Количество протонов в ядре атома совпадает с номером химического элемента в Периодической системе химических элементов и называется зарядовым числом (
Z
).
Массовое число
Количество нейтронов в ядре атома принято обозначать N. Тогда количество протонов и нейтронов в ядре атома можно вычислить как:
A=Z+N.
— количество нуклонов в атоме называется массовым числом.
Изотопы
Химические свойства атома определяются зарядовым числом, так как это число указывает на номер атома в периодической системе, т. е. определяет, какой именно это химический элемент. Физические свойства атома могут быть разными в зависимости от массового числа. Действительно, экспериментально было доказано, что ядра одного и того же химического элемента могут обладать разными массами. Например, в природе существует несколько видов атомов водорода: водород, дейтерий и тритий. Масса дейтерия приблизительно в два, а трития — в три раза больше массы водорода.
Атомы одного и того же химического элемента, но с разными массами, называются изотопами.
Так как изотопы — это атомы одного и того же химического элемента, то зарядовое число у изотопов одинаковое, а массовые числа различные. Это означает, что ядра изотопов содержат одинаковое число протонов и разное количество нейтронов.
Изотопы принято обозначать:
XZA, где
XZA — химический элемент,
A — массовое число,
Z — зарядовое число.
Пример:
— водород,
H12
— дейтерий,
H13
— тритий.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 9 ноября 2019 года; проверки требуют 4 правки.
Ма́ссовое число́ атомного ядра — суммарное количество протонов и нейтронов (называемых общим термином «нуклоны») в ядре. Обычно обозначается буквой A. Массовое число близко к атомной массе изотопа, выраженной в атомных единицах массы, но совпадает с ней только для углерода-12, поскольку атомная единица массы (а. е. м.) определяется сейчас как 1⁄12 массы атома 12С. Во всех остальных случаях атомная масса не является целым числом, в отличие от массового числа. Так, массовое число изотопа хлора 35Cl равно 35, а его атомная масса составляет 34,96885 а.е.м.
Массовое число в обозначении конкретного нуклида (вида атомных ядер) пишется верхним левым индексом, например 232Th. Нуклиды с одинаковым массовым числом называются изобарами (например, изобарами являются нуклиды 14C и 14N).
Знание массового числа позволяет оценить массу ядра и атома. Если известно массовое число, то масса М атома и его ядра оценивается из следующего соотношения М ≈ А·mN, где mN ≈ 1,67·10−27 кг — масса нуклона, то есть протона или нейтрона. Например, в состав атома алюминия-27 и его ядра входит 27 нуклонов (13 протонов и 14 нейтронов). Его масса примерно равна 27·1,67·10−27 кг ≈ 4,5·10−26 кг. Если необходимо получить массу ядра с большей точностью, то нужно учесть, что нуклоны в ядре связаны силами ядерного притяжения, и поэтому в соответствии с соотношением E = mc2 масса ядра уменьшается. В массу атома также следует добавить суммарную массу электронов на орбитах вокруг ядра. Однако все эти поправки не превышают 1 %[1].
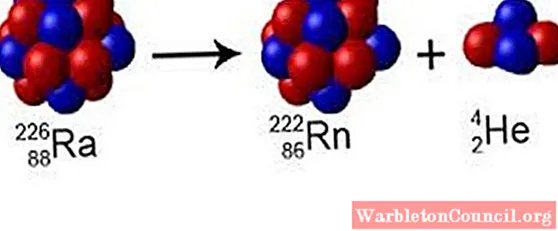
Массовое число совпадает с барионным числом ядра. Барионное число сохраняется во всех известных процессах, поэтому любые радиоактивные распады и ядерные реакции не приводят к изменению суммы массовых чисел ядер в левой и правой части реакции. Например, при альфа-распаде урана-238
в левой части массовое число начального ядра равно 238, в правой части реакции — два ядра с массовыми числами 234 и 4, что в сумме даёт 238. С учётом того, что массовое число альфа-частицы (ядра гелия-4) равно 4, альфа-распад снижает массовое число распадающегося ядра на 4 единицы. Любые типы бета-распада (бета-минус-распад, позитронный распад, электронный захват, все типы двойного бета-распада) не изменяют массовое число, поскольку в этом процессе происходит лишь превращение некоторых нуклонов ядра из одного вида в другой (протонов в нейтроны или обратно). Изомерный переход также не изменяет массовое число ядра.
Примечания[править | править код]
- ↑ «Ишханов Б. С., Капитонов И. М., Кэбин Э. И., Частицы и атомные ядра. Основные понятия, Изд. МГУ, Москва, 2009, 271 с., тираж 100 экз.» Дата обращения: 15 февраля 2011. Архивировано 25 ноября 2012 года.
Для того чтобы это сделать вам нужно знать 3 вещи:
- Как определить число протонов и нейтронов в атоме?
- Как определить общее число электронов в атоме?
- Что такое изотоп.
Вкратце напомню.
Число протонов и электронов в атоме одинаково и равно порядковому номеру элемента в периодической таблице.
Число нейтронов вычисляется по формуле:
N = A — Z
Где N — число нейтронов, A — атомная масса элемента (в целых числах), Z — заряд ядра атома (число протонов) или порядковый номер атома в периодической таблице Менделеева.
Что такое изотоп?
Изотопы это разновидности атомов химического элемента, которые имеют одинаковый заряд ядра (порядковый номер в таблице), но разные массовые числа.
Проще говоря, у изотопов в ядре атома одинаковое число протонов, но разное число нейтронов.
Таким образом, число протонов и электронов у изотопов такое же, как и у обычных атомов, разница лишь в количестве нейтронов.
Примеры
Сколько электронов, протонов и нейтронов содержит атом изотопа титана 50Ti?
Титан имеет порядковый номер 22. Значит в ядре содержится 22 протона, а в атоме 22 электрона.
Число нейтронов: N = 50 – 22 = 28 нейтронов.
Сколько электронов содержит нейтральный атом изотопа полония?
В данном случае нам даже не нужно знать массовое число изотопа, т.к. речь идет только об электронах. Порядковый номер полония 84, значит в ядре атома 84 протона, а в атоме 84 электрона.
Определите число протнов, нейтронов и электронов для изотопа 55Mn.
Порядковый номер марганца 25. Значит в ядре атома 25 протонов, а в атоме 25 электронов.
Найдем число нейтронов: N = 55 – 25 = 30 нейтронов.
Определите число протонов изотопа калия.
В этом случае массовое число изотопа не имеет значения, т.к. речь идет о протонах, число которых у изотопов одинаково. Калий имеет порядковый номер в таблице 19, значит у любого изотопа калия будет 19 протонов.
Похожие вопросы:
– Какие атомы имеют одинаковое число нейтронов?
– Как определить общее число электронов в атоме?

Содержание
- Примеры массовых чисел
- Водород
- Кислород
- Углерод
- Уран
- Как получить массовое число?
- Обозначения для атомов
- Изотопы
- Изотопы углерода
- Таблица природных изотопов углерода
- Примеры работы
- – Пример 1
- Ответить
- – Пример 2
- Ответить
- Ссылки
В массовое число Массовое число атома – это сумма количества протонов и количества нейтронов в ядре. Эти частицы взаимозаменяемо обозначаются именем нуклоны, поэтому массовое число представляет их количество.
Пусть N – количество присутствующих нейтронов, а Z – количество протонов, если мы назовем A массовым числом, тогда:
А = N + Z
Примеры массовых чисел
Вот несколько примеров массовых чисел для хорошо известных элементов:
Водород
Самый стабильный и многочисленный атом водорода также самый простой: 1 протон и один электрон. Поскольку ядро водорода не имеет нейтронов, верно, что A = Z = 1.
Кислород
В ядре кислорода 8 нейтронов и 8 протонов, поэтому A = 16.
Углерод
Жизнь на Земле основана на химии углерода, легкого атома с 6 протонами в ядре плюс 6 нейтронов, поэтому A = 6 + 6 = 12.
Уран
Этот элемент, намного тяжелее предыдущих, хорошо известен своими радиоактивными свойствами. В ядре урана 92 протона и 146 нейтронов. Тогда его массовое число A = 92 + 146 = 238.
Как получить массовое число?
Как упоминалось ранее, массовое число A элемента всегда соответствует сумме числа протонов и числа нейтронов, содержащихся в его ядре. Это тоже целое число, но … есть ли какое-нибудь правило относительно соотношения между двумя величинами?
Посмотрим: все перечисленные элементы легкие, кроме урана. Атом водорода, как мы уже сказали, самый простой. В нем нет нейтронов, по крайней мере, в его наиболее распространенной версии, а в кислороде и углероде есть равное количество протонов и нейтронов.
То же самое происходит и с другими легкими элементами, такими как азот, еще один очень важный для жизни газ, который имеет 7 протонов и 7 нейтронов. Однако по мере того, как ядро становится более сложным, а атомы становятся тяжелее, количество нейтронов увеличивается с другой скоростью.
В отличие от легких элементов, уран с 92 протонами имеет примерно в 1 ½ раза больше нейтронов: 1 ½ x 92 = 1,5 x 92 = 138.
Как видите, это довольно близко к 146 – количеству нейтронов, которое он имеет.
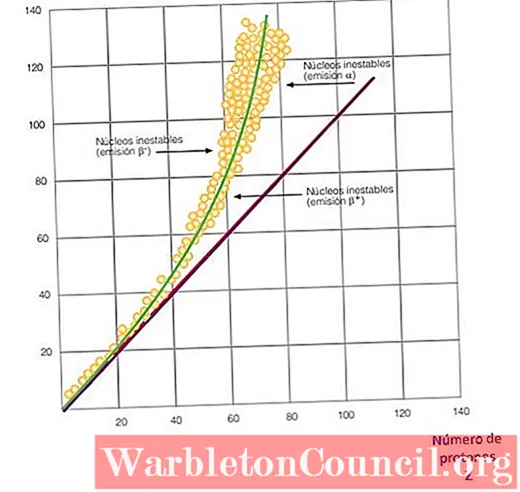
Все это становится очевидным на кривой на рисунке 2. Это график зависимости N от Z, известный каккривая ядерной устойчивости. Там вы можете увидеть, как легкие атомы имеют такое же количество протонов, что и нейтроны, и как с Z = 20 количество нейтронов увеличивается.
Таким образом, большой атом становится более стабильным, так как избыток нейтронов уменьшает электростатическое отталкивание между протонами.
Обозначения для атомов
Очень полезная запись, которая быстро описывает тип атома, следующая: символ элемента и соответствующие атомные и массовые числа записываются, как показано ниже на этой диаграмме:
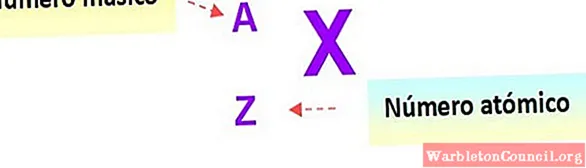
В этих обозначениях атомы в предыдущих примерах будут:

Иногда используются другие более удобные обозначения, в которых для обозначения атома используются только символ элемента и массовое число, без атомного номера. Таким образом, 12 6C просто записывается как углерод-12, 16 8Или кислород – 16 и так далее для любого элемента.
Изотопы
Число протонов в ядре определяет природу элемента. Например, каждый атом, ядро которого содержит 29 протонов, является атомом меди, несмотря ни на что.
Предположим, атом меди по какой-то причине теряет электрон, это все равно медь. Однако теперь это ионизированный атом.
Атомному ядру сложнее получить или потерять протон, но в природе это может происходить. Например, внутри звезд более тяжелые элементы непрерывно образуются из легких элементов, поскольку звездное ядро ведет себя как термоядерный реактор.
И прямо здесь, на Земле, есть феномен радиоактивный распад, в котором некоторые нестабильные атомы изгоняют нуклоны и излучают энергию, превращаясь в другие элементы.
Наконец, существует вероятность того, что атом определенного элемента имеет другое массовое число, в данном случае это изотоп.
Хороший пример – всем известный углерод-14 или радиоуглерод, который используется для датировки археологических объектов и как биохимический индикатор. Это тот же углерод с идентичными химическими свойствами, но с двумя дополнительными нейтронами.
Углерод-14 менее распространен, чем углерод-12, стабильный изотоп, а также радиоактивен. Это означает, что со временем он распадается, выделяя энергию и частицы, пока не станет стабильным элементом, которым в его случае является азот.
Изотопы углерода
Углерод существует в природе как смесь нескольких изотопов, наиболее распространенными из которых являются уже упомянутые 126С или углерод-12. А кроме углерода-14 есть 136C с дополнительным нейтроном.
Это обычное явление в природе, например, известно 10 стабильных изотопов олова. С другой стороны, из бериллия и натрия известен только один изотоп.
Каждый изотоп, природный или искусственный, имеет разную скорость превращения. Таким же образом можно создавать искусственные изотопы в лаборатории, которые, как правило, нестабильны и радиоактивно распадаются за очень короткий период долей секунды, в то время как для других требуется гораздо больше времени, равное возрасту Земли или больше.
Таблица природных изотопов углерода
| Изотопы углерода | Атомный номер Z | Массовое число A | Изобилие% |
|---|---|---|---|
| 12 6 C | 6 | 12 | 98.89 |
| 13 6 C | 6 | 13 | 1.11 |
| 14 6 C | 6 | 14 | Следы |
Примеры работы
– Пример 1
В чем разница между137 N и 147 N?
Ответить
Оба являются атомами азота, так как их атомный номер равен 7. Однако один из изотопов с A = 13 имеет на один нейтрон меньше, а 147 N – самый распространенный изотоп.
– Пример 2
Сколько нейтронов находится в ядре атома ртути, обозначаемого как 20180 Hg?
Ответить
Поскольку A = 201 и Z = 80, а также зная, что:
А = Z + N
N = А – Я = 201 – 80 = 121
И делается вывод, что в атоме ртути 121 нейтрон.
Ссылки
- Коннор, Н. Что такое нуклон – Структура атомного ядра – Определение. Получено с: period-table.org.
- Найт, р. 2017. Физика для ученых и инженерии: стратегический подход. Пирсон.
- Сирс, Земанский. 2016. Университетская физика с современной физикой. 14-го. Ред. Том 2.
- Типпенс, П. 2011. Физика: концепции и приложения. 7-е издание. Макгроу Хилл.
- Википедия. Массовое число. Получено с: en.wikipedia.org.
Физика 9 класс
Тема: Строение атома и атомного ядра. Использование энергии атомных ядер
Урок 56. Состав атомного ядра. Массовое число. Зарядовое
число. Ядерные силы
Ерюткин Евгений Сергеевич
учитель физики высшей категории ГОУ СОШ №1360
Москва
2011
Здравствуйте! Сегодняшний урок будет посвящен вопросу, связанному с обсуждением строения ядра атома, зарядовому числу, массовому числу, поговорим также о том, что такое ядерные силы. Наш урок – это подведение некоторого промежуточного итога по всем ранее изученным вопросам. Мне бы хотелось сказать то, что мы изучали вопросы, связанные со строением атома и строением ядра. Поэтому сегодня мы поговорим именно об этом. Некоторый итог предыдущим темам, предыдущим вопросам. Прежде чем мы перейдем к тому вопросу, который обозначен первым, мы поговорим вот о чем. На предыдущем уроке мы говорили, что Резерфорд в своих экспериментах установил, что существует такая частица, как протон. Через некоторое время в 1932 году Чедвик установил, что существует еще одна частица, которая называется нейтрон. После этого открытия независимо друг от друга два человека, русский ученый Иваненко и немецкий ученый Гейзенберг, предложили протонно-нейтронную модель строения ядра атома. По этой теории Иваненко – Гейзенберга, ядро любого атома содержит протоны и нейтроны. Эти протоны и нейтроны вместе, те, которые находятся в ядре атома, было решено называть нуклонами. Таким образом, «нуклон» (от лат. «ядро») – общее название для протонов и нейтронов. Те частицы, которые имеют заряд, и те частицы, которые заряд не имеют, нейтроны, эти все частицы вместе называются нуклонами. Давайте еще вот о чем поговорим. Идея о заряде ядра была впервые выдвинута в 1913 году английским ученым Генри Мозли. Он предложил, что, раз атом электронейтрален, порядковый номер элемента, умноженный на элементарный электрический заряд, это и есть заряд ядра. Каким образом Мозли пришел к такому заключению? Дело в том, что количество электронов в атоме соответствует порядковому номеру. Значит, заряд всех электронов – это произведение порядкового номера на заряд одного электрона. Поскольку в ядре сосредоточен положительный заряд, значит, то же самое можно говорить и о ядре. Давайте посмотрим на то, как пришел Мозли именно к тому, что мы называем зарядовым числом. Посмотрите:
qЯ = Z. |e|
qЯ – заряд ядра
е – заряд электрона
Z – число протонов в ядре, зарядовое число
Заряд числа, по такому утверждению, определяется как произведение порядкового номера на элементарный электрический заряд. В данном случае е – это заряд электрона, элементарный электрический заряд его называют, и взят он по модулю, потому что понятно, что заряд ядра у нас положительный. В этом случае порядковый номер стали называть зарядовым числом, порядковый номер – это число, соответствующее числу протонов в ядре. Таким образом, мы, говоря о порядковом номере, можем говорить о количестве протонов в ядре. Следующее число, о котором необходимо сказать, – это число массы. Оно, это число, обозначено буквой А, и это самое число берут то же из таблицы Менделеева и округляют его до целых. Дальше мы можем говорить о том уравнении, которое называется во всем мире уравнением Иваненко – Гейзенберга. Это уравнение состоит из трех чисел: массового числа, зарядового числа и числа нейтронов. Давайте посмотрим, как оно записывается и как обозначаются данные величины.
Уравнение Иваненко – Гейзенберга
А = Z + N
А – массовое число,
Z – порядковый номер элемента,
N – число нейтронов в ядре
Посмотрите: массовое число А говорит о том, какое количество нуклонов входит в ядро. Оказалось, что, по таблице Менделеева определяя массовое число химического элемента, мы определяем число нуклонов в ядре атома.
Z, как мы говорили, будет порядковый номер и число протонов в ядре. N в данном случае – это число нейтронов. Таким образом, мы можем из этого уравнения определить число нейтронов, число протонов, зная массовое число и порядковый номер. Здесь необходимо отметить важный момент. Дело в том, что в 1913 году еще один ученый Содди (вы помните, что этот человек работал вместе с Резерфордом) установил интересную вещь. Выяснено было, что существуют химические элементы с абсолютно одинаковыми химическими свойствами, но разным массовым числом. Такие элементы, у которых одинаковые химические свойства, но разное массовое число, стали называть изотопами. Изотопы – это химические элементы с одинаковыми химическими свойствами, но с различной массой атомных ядер.
Еще надо добавить, что у изотопов разная радиоактивность. Все это вместе привело к изучению этого вопроса. Здесь показаны изотопы легких и тяжелых элементов химических. Давайте посмотрим. Мы выбрали специально разные области таблицы Менделеева, чтобы показать, что практически все элементы химические имеют изотопы.
Изотопы:
 Н – протий
Н – протий  U
U
 H – дейтерий
H – дейтерий ![]() U
U
 Н – тритий
Н – тритий
У водорода этих изотопов три. Первый изотоп  Н называется протий. Обратите внимание, что порядковый номер ставится внизу, вот это число Z, а сверху пишется массовое число – это число А. Сверху А, внизу Z, и если мы понимаем, что
Н называется протий. Обратите внимание, что порядковый номер ставится внизу, вот это число Z, а сверху пишется массовое число – это число А. Сверху А, внизу Z, и если мы понимаем, что  это обозначает, что в ядре атома протия самый простой химический элемент, самый распространенный во вселенной. Там всего лишь 1 протон, а нейтронов в этом ядре совсем нет. Есть второй вид водорода – это дейтерий. Наверное, многие слышали такое слово. Обратите внимание: порядковый номер 1, а массовое число равно 2. Так что ядро дейтерия состоит уже из 1 протона и из одного нейтрона. И есть еще один изотоп водорода. Называется тритий. Тритий как раз (порядковый номер первый), а массовое число говорит о том, что в ядре этого изотопа находятся 2 нейтрона. И еще один элемент – это уран. Совсем другая сторона таблицы Менделеева. Это уже тяжелые элементы. У урана 2 изотопа распространенных. Это уран 235. Порядковый номер 92, а массовое число 235. Сразу можно говорить о том, чем отличается ядро одного элемента от другого. Второй изотоп: тоже порядковый номер 92, а массовое число 238. Очень часто, когда идет речь об изотопах, в частности урана, никогда не говорят порядкового номера. Просто говорят «уран», называют химический элемент и говорят его массовое число – 238. Или уран 235. Мы обсуждаем этот вопрос по той простой причине, что знаем, как сегодня этот химический элемент важен для энергетики нашей страны и вообще мировой энергетики в целом.
это обозначает, что в ядре атома протия самый простой химический элемент, самый распространенный во вселенной. Там всего лишь 1 протон, а нейтронов в этом ядре совсем нет. Есть второй вид водорода – это дейтерий. Наверное, многие слышали такое слово. Обратите внимание: порядковый номер 1, а массовое число равно 2. Так что ядро дейтерия состоит уже из 1 протона и из одного нейтрона. И есть еще один изотоп водорода. Называется тритий. Тритий как раз (порядковый номер первый), а массовое число говорит о том, что в ядре этого изотопа находятся 2 нейтрона. И еще один элемент – это уран. Совсем другая сторона таблицы Менделеева. Это уже тяжелые элементы. У урана 2 изотопа распространенных. Это уран 235. Порядковый номер 92, а массовое число 235. Сразу можно говорить о том, чем отличается ядро одного элемента от другого. Второй изотоп: тоже порядковый номер 92, а массовое число 238. Очень часто, когда идет речь об изотопах, в частности урана, никогда не говорят порядкового номера. Просто говорят «уран», называют химический элемент и говорят его массовое число – 238. Или уран 235. Мы обсуждаем этот вопрос по той простой причине, что знаем, как сегодня этот химический элемент важен для энергетики нашей страны и вообще мировой энергетики в целом.
Следующий вопрос, который мы должны затронуть, вытекает из сказанного. Как эти частицы, эти нуклоны удерживаются внутри ядра? Мы назвали различные химические элементы, изотопы различные, особенно у тяжелых элементов, там, где нуклонов, т.е. протонов и нейтронов, много. Как, каким образом они удерживаются внутри ядра? Мы знаем, что в маленьком ядре расстояния, размеры ядра очень и очень малы, бывает собрано большое количество частиц нуклонов. Как эти нуклоны там так плотно, тесно удерживаются, какими силами? Ведь за счет электростатического отталкивания эти частицы должны очень быстро распадаться, разлетаться. Мы знаем, что разноименные только заряды притягиваются, частицы, заряженные разноименными зарядами. Если частицы заряжены одноименно, понятно, что они должны отталкиваться. Внутри ядра находятся протоны. Они положительно заряжены. Размер ядра очень мал. В этом же ядре находятся еще и нейтроны, значит, должны быть силы, которые удерживают вместе те и другие частицы. Эти самые силы называют ядерными силами. Ядерные силы – это силы притяжения, действующие между нуклонами. Можно сказать, что у этих сил существуют свои особые свойства.
Первое свойство, о котором мы должны сказать, – это то, что ядерные силы должны превосходить силы электростатического отталкивания. И это так, когда удалось их определить, то выяснилось, что они в 100 раз превосходят силы электростатического отталкивания. Еще одно очень важное замечание, что действуют ядерные силы на малом расстоянии. Например, 10-15м – это и есть диаметр ядра, эти силы действуют. Но стоит только увеличиться размеру ядра до 10-14, казалось, совсем немного, то это приводит к тому, что ядро обязательно распадется. На этом расстоянии уже ядерные силы не действуют. А силы электростатического отталкивания продолжают действовать и именно они отвечают за то, что ядро распадается.
Еще можно сказать о ядерных силах то, что они не центральны, т.е. они не действуют вдоль прямой, соединяющей эти частицы. И то, что ядерные силы не зависят от того, обладает частица зарядом или не обладает, потому что в ядро входят и протоны, и нейтроны. Вместе эти частицы находятся. Таким образом, вывод: эти частицы, нуклоны, удерживаются в ядре за счет ядерных сил, и эти силы действуют только в ядре. Еще можно отметить, что ядерные силы имеют важное значение в плане стабильности ядра. Отвечают за долговременность существования этого элемента. В заключение мы можем отметить еще одно: когда мы будем говорить об энергетике, вот здесь именно ядерные силы будут играть основную роль. Об этом мы поговорим на следующих уроках. До свидания.
Задание к уроку.
1. Определите нуклонный состав ядер железа  (количество нуклонов, протонов, нейтронов).
(количество нуклонов, протонов, нейтронов).
2. В ядре атома химического элемента 22 протона и 26 нейтронов. Назовите этот химический элемент.
3. Оцените силу гравитационного взаимодействия между двумя нейтронами в ядре. Масса нейтрона примерно равна 1,7*10-27 кг, расстояние между нейтронами примите равным 10-15 м, значение гравитационной постоянной 6,67*10-11 (Н*м2)/кг2.

