4.3.1. Расчеты с использованием понятия «массовая доля вещества в растворе».
Раствором называют гомогенную смесь двух или более компонентов.
Вещества, смешением которых получен раствор, называют его компонентами.
Среди компонентов раствора различают растворенное вещество, которое может быть не одно, и растворитель. Например, в случае раствора сахара в воде сахар является растворенным веществом, а вода является растворителем.
Иногда понятие растворитель может быть применимо в равной степени к любому из компонентов. Например, это касается тех растворов, которые получены смешением двух или более жидкостей, идеально растворимых друг в друге. Так, в частности, в растворе, состоящем из спирта и воды, растворителем может быть назван как спирт, так и вода. Однако чаще всего в отношении водосодержащих растворов традиционно растворителем принято называть воду, а растворенным веществом — второй компонент.
В качестве количественной характеристики состава раствора чаще всего используют такое понятие, как массовая доля вещества в растворе. Массовой долей вещества называют отношение массы этого вещества к массе раствора, в котором оно содержится:
где ω(в-ва) – массовая доля вещества, содержащегося в растворе (г), m(в-ва) – масса вещества, содержащегося в растворе (г), m(р-ра) – масса раствора (г).
Из формулы (1) следует, что массовая доля может принимать значения от 0 до 1, то есть составляет доли единицы. В связи с этим массовую долю можно также выражать в процентах (%), причем именно в таком формате она фигурирует практически во всех задачах. Массовая доля, выраженная в процентах, рассчитывается по формуле, схожей с формулой (1) с той лишь разницей, что отношение массы растворенного вещества к массе всего раствора умножают на 100%:
Для раствора, состоящего только из двух компонентов, могут быть соответственно рассчитаны массовые доли растворенного вещества ω(р.в.) и массовая доля растворителя ω(растворителя).
Массовую долю растворенного вещества называют также концентрацией раствора.
Для двухкомпонентного раствора его масса складывается из масс растворенного вещества и растворителя:
Также в случае двухкомпонентного раствора сумма массовых долей растворенного вещества и растворителя всегда составляет 100%:
Очевидно, что, помимо записанных выше формул, следует знать и все те формулы, которые напрямую из них математически выводятся. Например:
Также необходимо помнить формулу, связывающую массу, объем и плотность вещества:
m = ρ∙V
а также обязательно нужно знать, что плотность воды равна 1 г/мл. По этой причине объем воды в миллилитрах численно равен массе воды в граммах. Например, 10 мл воды имеют массу 10 г, 200 мл — 200 г и т.д.
Для того чтобы успешно решать задачи, помимо знания указанных выше формул, крайне важно довести до автоматизма навыки их применения. Достичь этого можно только прорешиванием большого количества разнообразных задач. Задачи из реальных экзаменов ЕГЭ на тему «Расчеты с использованием понятия «массовая доля вещества в растворе»» можно порешать здесь.
Примеры задач на растворы
Пример 1
Рассчитайте массовую долю нитрата калия в растворе, полученном смешением 5 г соли и 20 г воды.
Решение:
Растворенным веществом в нашем случае является нитрат калия, а растворителем — вода. Поэтому формулы (2) и (3) могут быть записаны соответственно как:
Из условия m(KNO3) = 5 г, а m(Н2O) = 20 г, следовательно:
Пример 2
Какую массу воды необходимо добавить к 20 г глюкозы для получения 10%-ного раствора глюкозы.
Решение:
Из условий задачи следует, что растворенным веществом является глюкоза, а растворителем — вода. Тогда формула (4) может быть записана в нашем случае так:
Из условия мы знаем массовую долю (концентрацию) глюкозы и саму массу глюкозы. Обозначив массу воды как x г, мы можем записать на основе формулы выше следующее равносильное ей уравнение:
Решая это уравнение находим x:
т.е. m(H2O) = x г = 180 г
Ответ: m(H2O) = 180 г
Пример 3
150 г 15%-ного раствора хлорида натрия смешали со 100 г 20%-ного раствора этой же соли. Какова массовая доля соли в полученном растворе? Ответ укажите с точностью до целых.
Решение:
Для решения задач на приготовление растворов удобно использовать следующую таблицу:
1-й раствор
2-й раствор
3-й раствор
mр.в.
mр-ра
ωр.в.
где mр.в., mр-ра и ωр.в. — значения массы растворенного вещества, массы раствора и массовой доли растворенного вещества соответственно, индивидуальные для каждого из растворов.
Из условия мы знаем, что:
m(1)р-ра = 150 г,
ω(1)р.в. = 15%,
m(2)р-ра = 100 г,
ω(1)р.в. = 20%,
Вставим все эти значения в таблицу, получим:
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
|||
mр-ра |
150 г | 100 г | |
ωр.в. |
15% | 20% | искомая величина |
Нам следует вспомнить следующие формулы, необходимые для расчетов:
ωр.в. = 100% ∙ mр.в./mр-ра , mр.в. = mр-ра ∙ ωр.в./100% , mр-ра = 100% ∙ mр.в. /ωр.в.
Начинаем заполнять таблицу.
Если в строчке или столбце отсутствует только одно значение, то его можно посчитать. Исключение — строчка с ωр.в., зная значения в двух ее ячейках, значение в третьей рассчитать нельзя.
В первом столбце отсутствует значение только в одной ячейке. Значит мы можем рассчитать его:
m(1)р.в. = m(1)р-ра ∙ ω(1)р.в. /100% = 150 г ∙ 15%/100% = 22,5 г
Аналогично у нас известны значения в двух ячейках второго столбца, значит:
m(2)р.в. = m(2)р-ра ∙ ω(2)р.в. /100% = 100 г ∙ 20%/100% = 20 г
Внесем рассчитанные значения в таблицу:
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
22,5 г | 20 г | |
mр-ра |
150 г | 100 г | |
ωр.в. |
15% | 20% | искомая величина |
Теперь у нас стали известны два значения в первой строке и два значения во второй строке. Значит мы можем рассчитать недостающие значения (m(3)р.в. и m(3)р-ра):
m(3)р.в. = m(1)р.в. + m(2)р.в. = 22,5 г + 20 г = 42,5 г
m(3)р-ра = m(1)р-ра + m(2)р-ра = 150 г + 100 г = 250 г.
Внесем рассчитанные значения в таблицу, получим:
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
22,5 г | 20 г | 42,5 г |
mр-ра |
150 г | 100 г | 250 г |
ωр.в. |
15% | 20% | искомая величина |
Вот теперь мы вплотную подобрались к расчету искомой величины ω(3)р.в.. В столбце, где она расположена, известно содержимое двух других ячеек, значит мы можем ее рассчитать:
ω(3)р.в. = 100% ∙ m(3)р.в./m(3)р-ра = 100% ∙ 42,5 г/250 г = 17%
Пример 4
К 200 г 15%-ного раствора хлорида натрия добавили 50 мл воды. Какова массовая доля соли в полученном растворе. Ответ укажите с точностью до сотых _______%
Решение:
Прежде всего следует обратить внимание на то, что вместо массы добавленной воды, нам дан ее объем. Рассчитаем ее массу, зная, что плотность воды равна 1 г/мл:
mдоб.(H2O) = Vдоб.(H2O) ∙ ρ(H2O) = 50 мл ∙ 1 г/мл = 50 г
Если рассматривать воду как 0%-ный раствор хлорида натрия, содержащий соответственно 0 г хлорида натрия, задачу можно решить с помощью такой же таблицы, как в примере выше. Начертим такую таблицу и вставим известные нам значения в нее:
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
0 г | ||
mр-ра |
200 г | 50 г | |
ωр.в. |
15% | 0% | искомая величина |
В первом столбце известны два значения, значит можем посчитать третье:
m(1)р.в. = m(1)р-ра ∙ ω(1)р.в./100% = 200 г ∙ 15%/100% = 30 г,
Во второй строчке тоже известны два значения, значит можем рассчитать третье:
m(3)р-ра = m(1)р-ра + m(2)р-ра = 200 г + 50 г = 250 г,
Внесем рассчитанные значения в соответствующие ячейки:
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
30 г | 0 г | |
mр-ра |
200 г | 50 г | 250 г |
ωр.в. |
15% | 0% | искомая величина |
Теперь стали известны два значения в первой строке, значит можем посчитать значение m(3)р.в. в третьей ячейке:
m(3)р.в. = m(1)р.в. + m(2)р.в. = 30 г + 0 г = 30 г
1-й раствор |
2-й раствор |
3-й раствор |
|
mр.в. |
30 г | 0 г | 30 г |
mр-ра |
200 г | 50 г | 250 г |
ωр.в. |
15% | 0% | искомая величина |
Теперь можем рассчитать массовую долю в третьем растворе:
ω(3)р.в. = 30/250 ∙ 100% = 12%.
Самое главное при решении таких задач (а именно номер 27 в ЕГЭ по химии) это знать всего 3 формулы:
- массовой доли w=m(в-ва)/m(р-ра) * 100%
- молярной доли по массе М=m/v
- молярной доли по объему Vm=V/v
Вообще, основной тип этих задач – смешивание каких-либо растворов, и задача определить массовую долю вещества в получившемся растворе или масса выделившегося вещества
Алгоритм решения достаточно простой:
1) Вычислить массу растворённого вещества в каждом данном растворе
2) Вычислить общую массу смешиваемых растворов (получится новый раствор)
3) Вычислить общую массу растворённых веществ, полученных в пункте 1
4) Если требуется найти массовую долю в полученном растворе, то используя формулы, данные выше, разделить общую массу растворённых веществ (результат 3-его пункта) на массу смешиваемых растворов (результат 2-го пункта) и получить ответ.
Если же требуется получить массу какого-то побочного продукта, то надо вычесть из общей массы раствора массу данного раствора (всё это будет дано или получено, если требуется получить массу побочного продукта).
Итак, перейдём к практике:)
№1. Смешали 80 г раствора с массовой долей нитрата натрия 25 % и 20 г раствора этой же соли с массовой долей 40 %. Вычислите массовую долю соли в полученном растворе. Ответ дайте в процентах с точностью до целых.
Действуем согласно алгоритму:
1)Вычислим массу нитрата натрия в обоих растворах.
Используя формулу w=m(в-ва)/m(р-ра) * 100% , выражаем массу растворённого вещества, то есть нитрата натрия в КАЖДОМ РАСТВОРЕ:
m(в-ва1) = w(в-ва1) * m(р-ра1) : 100% = 80 г*25%:100%= 20г
m(в-ва2) = w(в-ва1) * m(р-ра2) : 100% = 20 г*40%:100%= 8г
2) Вычисляем общую массу растворов, которые смешиваем
m(р-ра) = m(р-ра1)+m(р-ра2)=80г+20г=100г
3)Вычисляем общую массу растворённых веществ
m(в-ва)=m(в-ва1)+m(в-ва2)=20г+8г=28г
4)Нам требуется получить массовую долю соли в полученном растворе. Масса соли получена в 3-ем пункте, масса раствора – во 2-м. Так что, используя формулу w=m(в-ва)/m(р-ра) * 100% вычисляем массовую долю соли в получившемся растворе.
w=m(в-ва)/m(р-ра) * 100% = 28г/100г*100%=28%
Сказано округлить до целых, но ответ уже в целых, так что так и пишем в ответе: 28%
Ответ: 28%. Задача решена.
Задача №2 будет немного другим типом, так что алгоритм немного нарушается
№2. Упариванием 500 г раствора с массовой долей соли 10 % получен раствор с массовой долей соли 14 %. Вычислите массу выпаренной при этом воды. Ответ укажите в граммах с точностью до целых.
Эта задача как раз и является тем случаем, когда нужно найти массу побочного продукта (конкретно здесь – воды)
1) Вычисляем массу соли в растворе по уже знакомой формуле
m(соли) = w(соли) * m(р-ра) : 100% = 10%*500г/100% = 50г
2) Общая масса растворов и есть данный раствор, так как фактически мы просто выделяем из него воду. Так что считать общую массу не нужно, она нам дана
3) В этой задаче действуем по другому – вычисляем раствор, который получится. То есть нам дана массовая доля соли в новом растворе, и массу этой соли мы уже знаем (1 пункт), так что мы можем вычислить массу раствора по формуле:
w=m(в-ва)/m(р-ра1) * 100%
Получается, что m(р-ра1) = m(в-ва)*100%/ w = 50г *100%/14%=примерно 357,1г.
4) Вычитаем из массы общего раствора массу получившегося раствора и получаем массу выпаренной воды, которую нам и нужно найти:
m(воды)=m(р-ра)-m(р-ра1)= 500г-357,1г=142,9г
Нам по условию нужно указать ответ с точностью до целых, то есть ответ 143 грамма.
Как видите, решать подобные задачи довольно просто. В них даже не надо знать никаких реакций, чтобы решать. Теперь вы сможете решить любую задачу на эту тему.
ПОНРАВИЛАСЬ СТАТЬЯ? ОБЯЗАТЕЛЬНО ПОДПИШИСЬ И ПОСТАВЬ ЛАЙК! ТАКЖЕ ПОДПИСЫВАЙСЯ НА МЕНЯ ВКОНТАКТЕ ПО ССЫЛКЕ: https://vk.com/hello_there_2021 Удачи!
P.S. Пишите в комментарии или в личку задачи, которые были бы Вам интересны для разбора или которые вызывают трудности. Постараюсь всем ответить!
Как определить массовую долю раствора
Массовая доля раствора – это химический термин, который может пригодиться при решении задач во время контрольной или самостоятельной работы, а также при выполнении расчетной части практических заданий. Однако не следует думать, что если золотое учебное время закончено, то больше эти знания не пригодятся. Во-первых, подрастающее поколение может подойти к родителю с вопросом по данной теме. А во-вторых, расчет массовой доли может понадобиться, например, для определения концентрации лекарственных или пищевых растворов (уксуса). Не менее важно применять знания при расчете количества удобрений.

Вам понадобится
- Ручка, бумага, калькулятор
Инструкция
Массовая доля – это отношение массы растворенного вещества к массе раствора. Причем она может измеряться или в процентах, тогда для этого полученный результат нужно умножить на 100% или в массовых долях (в этом случае единиц измерения не имеет).
Любой раствор состоит из растворителя (вода – наиболее распространенный растворитель) и растворенного вещества. Например, в любом растворе соли растворителем будет вода, а в качестве растворенного вещества будет выступать сама соль.
Для расчетов необходимо знать хотя бы два параметра – массу воды и массу соли. Это даст возможность рассчитать массовую долю вещества в растворе, которая обозначается буквой w (омега).
Пример 1. Масса раствора гидроксида калия (KOH) 150 г, масса растворенного вещества (KOH) 20 г. Найдите массовую долю щелочи (KOH) в полученном растворе.
m (KOH) = 20 г
m (KOH) = 100 г
w (KOH) – ?Существует формула, по которой можно определить массовую долю вещества.
w (KOH) = m (KOH) / m (раствора (KOH) х 100%Теперь рассчитайте массовую долю растворенного вещества гидроксида калия (KOH):
w (KOH) = 20 г / 120 г х 100% = 16,6 %
Пример 2. Масса воды 100 г, масса поваренной соли 20 г. Найдите массовую долю хлорида натрия в растворе.
m (NaCl) = 20 г
m (воды) = 100 г
w (NaCl) – ?Имеется формула, по которой можно определить массовую долю вещества.
w (NaCl) = m (NaCl) / m (раствора NaCl) х 100%Прежде чем воспользоваться данной формулой, найдите массу раствора, которая состоит из массы растворенного вещества и массы воды. Следовательно: m (раствора NaCl) = m (растворенного вещества NaCl) + m (воды)Подставьте конкретные значения
m (раствора NaCl) = 100 г + 20 г = 120 гТеперь рассчитайте массовую долю растворенного вещества:
w (NaCl) = 20 г / 120 г х 100% = 16,7 %
Полезный совет
При расчете не путайте такие понятия, как масса растворенного вещества и массовая доля растворенного вещества
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
“Только из союза двоих, работающих
вместе и при помощи друг друга, рождаются великие
вещи.”
Антуан Де Сент-Экзюпери
Математика многообразна и многогранна.
Существует ряд ситуаций в образовательном
процессе, когда при изучении какой-либо темы по
физике, химии, биологии и т.д. затрагиваются
понятия математики, например, существуют задачи,
которые решают как на уроках математики, так и на
уроках химии. Способы решения задач представляют
и учителя химии, и математики, но есть проблема:
математики знают математику, а химики – химию. И
не всегда способы совпадают.
В данной статье приводятся рекомендации по
решению химических задач на смешение растворов
разными способами: с помощью расчетной формулы,
“Правила смешения”, “Правила креста”,
графического метода, алгебраического метода.
Приведены примеры решения задач.
1. Основные химические понятия
Приведем некоторые указания к решению задач на
растворы.
Основными компонентами этого типа задач
являются:
а) массовая доля растворенного вещества в
растворе;
б) масса растворенного вещества в растворе;
в) масса раствора.
Предполагают, что:
а) все получившиеся смеси и сплавы являются
однородными;
б) смешивание различных растворов происходит
мгновенно;
в) объем смеси равен сумме объемов смешиваемых
растворов;
г) объемы растворов и массы сплавов не могут
быть отрицательными.
Определения и обозначения.
Массовая доля растворенного вещества в
растворе – это отношение массы этого вещества к
массе раствора.
![]()
где ![]() – массовая
– массовая
доля растворенного вещества в растворе;
![]() – масса
– масса
растворенного вещества в растворе;
![]() – масса
– масса
раствора.
Следствия формулы (1):
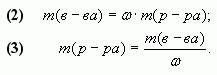
Введем обозначения:
![]() – массовая доля
– массовая доля
растворенного вещества в первом растворе;
![]() –
–
массовая доля растворенного вещества во втором
растворе;
![]() –
–
массовая доля растворенного вещества в новом
растворе, полученном при смешивании первого и
второго растворов;
m1(в-ва), m2(в-ва), m(в-ва) – массы
растворенных веществ в соответствующих
растворах;
m1(р-ра), m2(р-ра), m(р-ра) – массы
соответствующих растворов.
Основными методами решения задач на смешивание
растворов являются: с помощью расчетной формулы,
“Правило смешения”, “Правило креста”,
графический метод, алгебраический метод.
Приведем описание указанных методов.
1.1. С помощью расчетной формулы
В наших обозначениях, получим формулу для
вычисления массовой доли вещества (?) в смеси.
1. Масса полученного при смешивании раствора
равна:
m(р-ра) = m1(р-ра) + m2(р-ра).
2. Определим массы растворенных веществ в
первом и втором растворах:
m1(в-ва)= ![]() •m1(р-ра), m2(в-ва)=
•m1(р-ра), m2(в-ва)= ![]() •m2(р-ра).
•m2(р-ра).
3. Следовательно, масса растворенного вещества
в полученном растворе вычисляется как сумма масс
веществ в исходных растворах:
m(в-ва) = m1(в-ва) + m2(в-ва) = ![]() •m1(р-ра) +
•m1(р-ра) + ![]() •m2(р-ра).
•m2(р-ра).
4. Таким образом, массовая доля растворенного
вещества в полученном растворе равна:
![]()
или
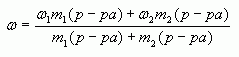
или
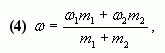
где ![]() – массы
– массы
соответствующих растворов.
Замечание: При решении задач удобно
составлять следующую таблицу.
|
1-й раствор |
2-й раствор |
Смесь двух растворов |
|
|
Масса растворов |
m1 |
m2 |
m1 + m2 |
|
Массовая доля |
|
|
|
|
Масса вещества в |
|
|
|
1.2. “Правило смешения”
Воспользуемся формулой (4): ![]()
тогда 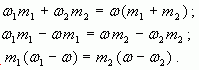
Отсюда ![]()
Таким образом, отношение массы первого
раствора к массе второго равно отношению
разности массовых долей смеси и второго раствора
к разности массовых долей первого раствора и
смеси.
Аналогично получаем, что при ![]()
Замечание: Формула (5) удобна тем, что на
практике, как правило, массы веществ не
отвешиваются, а берутся в определенном
отношении.
1.3. “Правило креста”
“Правилом креста” называют диагональную
схему правила смешения для случаев с двумя
растворами.
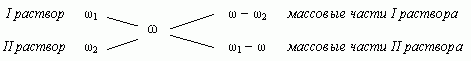
Слева на концах отрезков записывают исходные
массовые доли растворов (обычно слева
вверху-большая), на пересечении отрезков –
заданная, а справа на их концах записываются
разности между исходными и заданной массовыми
долями. Получаемые массовые части показывают в
каком отношении надо слить исходные растворы.
1.4. Графический метод
Отрезок прямой (основание графика)
представляет собой массу смеси, а на осях ординат
откладывают точки, соответствующие массовым
долям растворенного вещества в исходных
растворах. Соединив прямой точки на осях ординат,
получают прямую, которая отображает
функциональную зависимость массовой доли
растворенного вещества в смеси от массы
смешанных растворов в обратной пропорциональной
зависимости 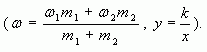
Полученная функциональная прямая позволяет
решать задачи по определению массы смешанных
растворов и обратные, по массе смешанных
растворов находить массовую долю полученной
смеси.
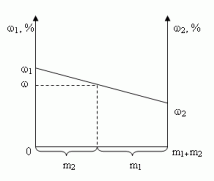
Построим график зависимости массовой доли
растворенного вещества от массы смешанных
растворов. На одной из осей ординат откладывают
точку, соответствующую массовой доли ![]() , а на другой –
, а на другой – ![]() . Обозначим на оси абсцисс
. Обозначим на оси абсцисс
точки А и В с координатами (0,0) и (m1 + m2,0),
соответственно. На графике точка А(0,0)
показывает, что массовая доля всего раствора
равна ![]() , а точка В(m1
, а точка В(m1
+ m2,0) – массовая доля всего раствора равна ![]() . В направлении от
. В направлении от
точки А к точке В возрастает содержание в
смеси 2-го раствора от 0 до m1+ m2 и
убывает содержание 1-го раствора от m1+ m2
до 0. Таким образом, любая точка на отрезке АВ будет
представлять собой смесь, имеющую одну и ту же
массу с определенным содержанием каждого
раствора, которое влияет на массовую долю
растворенного вещества в смеси.
Замечание: Данный способ является наглядным
и дает приближенное решение. При использовании
миллиметровой бумаги можно получить достаточно
точный ответ.
1.5. Алгебраический метод
Задачи на смешивание растворов решают с
помощью составления уравнения или системы
уравнений.
2. Примеры решения задач
Задача 1. (№1.43, [1])
В 100 г 20%-ного раствора соли добавили 300 г её
10%-ного раствора. Определите процентную
концентрацию раствора.
Решение:
- C помощью расчетной формулы
- Графический
- Путем последовательных вычислений
- Сколько растворенного вещества содержится:
- Сколько вещества содержится в образовавшемся
растворе? - Чему равна масса образовавшегося раствора?
- Какова процентная концентрация полученного
раствора? - Алгебраический

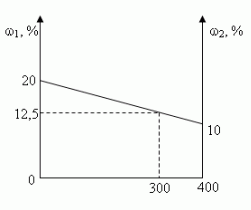
Ответ: 12,5%
а) в 100 г 20%-ного раствора; [100•0,2 = 20(г)]
б) в 300 г 10%-ного раствора? [300•0,1 = 30(г)]
20 г + 30 г = 50 г
100 г + 300 г = 400 г
(50/400)100 = 12,5(%)
Ответ: 12,5%
Пусть х – процентная концентрация
полученного раствора. В первом растворе
содержится 0,2•100(г) соли, а во втором 0,1•300(г), а в
полученном растворе х•(100 + 300)(г) соли.
Составим уравнение:
0,2•100 + 0,1•300 = х•(100 + 300);
х = 0,125 (12,5%)
Ответ: 12,5%
Задача 2. u(№10.26, [1])
Смешали 10%-ный и 25%-ный растворы соли и получили 3
кг 20%-ного раствора. Какое количество каждого
раствора в килограммах было использовано?
Решение:
- Алгебраический
- Графический.
- “Правило смешения”
- “Правило креста”
а) C помощью уравнения:
Пусть х (кг) – масса 1-го раствора, тогда 3-х (кг)
-масса 2-го раствора.
0,1•х (кг) содержится соли в 1-ом растворе,
0,25•(3-х) (кг) содержится соли в 2-ом растворе,
0,2•3 (кг) содержится соли в смеси.
Учитывая, что масса соли в 1-ом и 2-ом растворах
равна массе соли в смеси, составим и решим
уравнение:
0,1•х + 0,25•(3-х) = 0,2•3;
0,15х = 0,15;
х = 1, 1кг-масса 1-го раствора
3 – х = 3 – 1 =2 (кг) – масса 2-го раствора.
Ответ: 1 кг, 2 кг.
б) С помощью системы уравнений
Пусть х (кг) – количество первого раствора, у (кг)
– количество второго раствора. Система уравнений
имеет вид:
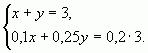
Ответ: 1 кг, 2 кг.
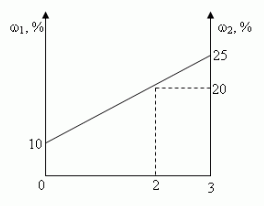
Ответ: 1кг, 2кг.

Составим диагональную схему
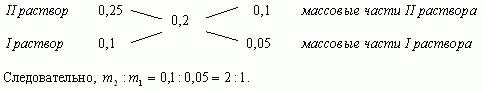
Ответ: 1кг, 2кг.
Задача 3 ([2])
Сосуд емкостью 5 л содержит 2 л р%-ного (по объёму)
раствора соли. Сколько литров 20%-ного раствора
такой же соли надо налить в сосуд, чтобы
процентное содержание соли в сосуде стало
наибольшим?
Решение (графический способ)
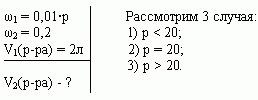
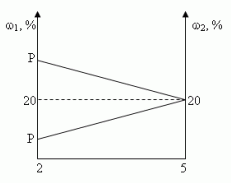
Заметим, что по условию, объём второго раствора
не превышает трёх литров.
- Ели р < 20, то для того, чтобы получить
максимальную массовую долю вещества в растворе,
необходимо добавить 3 л 20% – ного раствора соли; - Если р = 20, то при добавлении 2-го раствора,
процентное содержание соли в растворе не
изменится, следовательно, можно прилить от 0 л до 3
л 20% – ного раствора соли; - Если р > 20, то при добавлении 2-го раствора,
процентное содержание соли будет уменьшаться,
т.е. прилить нужно 0 л.
Ответ: 3 л, если 0 < р < 20, [0,3], если р = 20, 0л, если 20
< р ![]() 100.
100.
Задача 4 (работа 5, №2, [1])
В двух сосудах по 5л каждый содержится раствор
соли. Первый сосуд содержит 3л р% – ного раствора, а
второй – 4л 2р% – ного раствора одной и той же соли.
Сколько литров надо перелить из второго сосуда в
первый, чтобы получить в нем 10% – ный раствор соли?
При каких значениях р задача имеет решение?
Решение
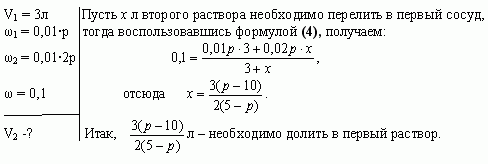
Найдем, при каких значениях р задача имеет
решение. По условию задачи 5-ти литровый сосуд
содержит 3л первого раствора, следовательно, к
нему можно прилить от 0 до 2л второго раствора.
Имеем, ![]() Решая
Решая
неравенство, получаем ![]()
Ответ: ![]()
3. Заключение
Данные рекомендации предназначены учителям
математики, желающим организовать элективные
курсы, как в девятых, так и в десятых и
одиннадцатых классах. Цель создаваемых курсов:
научить учащихся пользоваться математическим
аппаратом при решении химических задач.
Список литературы
- Галицкий и др. Сборник задач по алгебре для 8-9
классов: Учебное пособие для учащихся шк. и
классов с углубл. изуч. математики / М.Л. Галицкий,
А.М. Гольдман, Л.И. Звавич.-2-е изд. – М.:
Просвещение,1994. – 271с. - Сборник задач по математике для поступающих в
вузы: Учебное пособие/ П.Т.Дыбов, А.И.Забоев, А.С.
Иванов и др.; Под ред. А.И. Прилепко. – М.:Высш. школа,
1983. – 239 с. - Ерыгин Д.П., Шишкин Е.А. Методика решения задач по
химии: Учебное пособие для студентов пед. ин-тов
по биол. и хим. спец. – М.: Просвещение,1989. – 176с. - Хомченко Г.П., Хомченко И.Г. Задачи по химии для
поступающих в вузы: Учебное пособие. – 2-е изд..
исправ. и доп. – М.: Высш. школа, 1993. – 302 с.
Массовая доля растворённого вещества — это величина, равная отношению массы растворённого вещества к массе раствора.
Обрати внимание!
Масса раствора равна сумме масс растворённого вещества и растворителя:
Формулу для массовой доли можно записать следующим образом:
.
Массовая доля выражается в долях единицы (изменяется от (0) до (1)) или в процентах (изменяется от (0) до (100) %).
Формула для вычисления массовой доли в процентах:
%.
Пример:
или
w(HCl)=25
%.
