| Тритий | ||||
|---|---|---|---|---|
 |
||||
| Название, символ | Тритий, 3H | |||
| Альтернативные названия | сверхтяжёлый водород, T | |||
| Нейтронов | 2 | |||
| Свойства нуклида | ||||
| Атомная масса | 3,0160492777(25)[1] а. е. м. | |||
| Дефект массы | 14 949,8060(23)[1] кэВ | |||
| Удельная энергия связи (на нуклон) | 2 827,266(1)[1] кэВ | |||
| Период полураспада | 12,32(2)[2] года | |||
| Продукты распада | 3He | |||
| Спин и чётность ядра | 1/2+[2] | |||
|
||||
| Таблица нуклидов | ||||
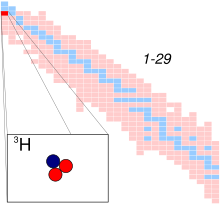
Три́тий (др.-греч. τρίτος «третий») — радиоактивный изотоп водорода. Обозначается T или 3H. Ядро трития состоит из протона и двух нейтронов, его называют тритоном.
В природе тритий образуется в верхних слоях атмосферы при соударении частиц космического излучения с ядрами атомов, например, азота[3]. В процессе распада тритий превращается в 3He с испусканием электрона и антинейтрино (бета-распад), период полураспада — 12,32 года. Доступная энергия распада очень мала (18,59 кэВ), средняя энергия электронов 5,7 кэВ.
Тритий открыт английскими учёными Эрнестом Резерфордом, Маркусом Олифантом и Паулем Хартеком в 1934 году. Название для этого изотопа было предложено на случай открытия ещё до него, 15 июня 1933 года, Юри, Мерфи и Брикведде в том же письме редактору научного журнала «The Journal of Chemical Physics», где они предложили названия для двух известных изотопов водорода — протия и дейтерия[4][5].
Используется в биологии и химии как радиоактивная метка, в экспериментах по исследованию свойств нейтрино, в термоядерном оружии как источник нейтронов и одновременно термоядерное горючее, в геологии для датирования природных вод. Промышленный тритий получают облучением лития-6 нейтронами в ядерных реакторах по следующей реакции:

Радиационная опасность трития[править | править код]
Тритий имеет период полураспада (12,32 ± 0,02) года[2]. Реакция распада трития имеет следующий вид:

При этом выделяется 18,59 кэВ энергии, из них на электрон (бета-частицу) приходится в среднем 5,7 кэВ, а на электронное антинейтрино — оставшаяся часть. Образовавшиеся бета-частицы распространяются в воздухе всего на 6,0 мм и не могут преодолеть даже верхний слой кожи человека[6].
В силу малой энергии распада трития испускаемые электроны хорошо задерживаются даже простейшими преградами типа одежды или резиновых хирургических перчаток. Тем не менее, этот изотоп представляет радиационную опасность при вдыхании, поглощении с пищей, впитывании через кожу. Единичный случай употребления тритиевой воды не приводит к длительному накоплению трития в организме, так как его период полувыведения — от 7 до 14 дней[7][8].
Производство и потребность[править | править код]
По данным отчета Institute for Energy and Environmental Research (англ.) (рус. 1996 года, в США с 1955 года было произведено около 225 кг трития[9].
В конце XX — начале XXI века наработка ведется на Watts Bar-1 путём облучения TPBAR (англ. tritium-producing burnable absorber rods), планируется также использование АЭС Секвойя. Переработку и выделение трития проводят на Tritium Extraction Facility, Саванна-Ривер[10].
В СССР и России тритий производился на реакторах АИ, АВ-3, ОК-180, ОК-190, РУСЛАН, Л-2; изотоп выделяется на заводе РТ-1 (ПО «Маяк»)[11][12].
Значительные количества трития (до 2,5—3,5 кг) для гражданских применений производит Канада на 21 тяжеловодном реакторе. Выделение изотопа — компания «Онтарио Хайдро», Дарлингтон[13].
Мировая коммерческая потребность в тритии на 1995 год составляет ежегодно около 400 г, и ещё порядка 2 кг требовалось для поддержания ядерного арсенала США[14] (7 кг для всех мировых военных потребителей). Около 4 кг трития в год образуется на АЭС, но не извлекается[15].
Большие количества трития потребуются для термоядерной энергетики: например, для запуска ITER потребуется как минимум около 3 кг трития, для запуска DEMO понадобится 4—10 кг[16]. Гипотетический тритиевый реактор потреблял бы 56 кг трития на производство 1 ГВт·года электроэнергии, тогда как всемирные запасы трития на 2003 год составляли всего 18 кг[16].
По словам Яна Беранека, политика и активиста из организации «Гринпис» и чешской партии зелёных, в 2010 году производство одного килограмма трития обходилось в 30 млн долларов[17].
Применение[править | править код]
Тритиевый брелок, свечение в темноте (снимок с длительной экспозицией)
В 2012 году канадская фирма City Labs представила радиоизотопные генераторы электричества сверхмалой мощности на базе трития, способные питать различные микроэлектронные устройства, таких как RFID-метки, автономные датчики, медицинские имплантаты. При цене порядка 1000 долларов срок службы генератора составляет около 20 лет[18].
Тритий используется в источниках подсветки в военных и гражданских приборах.
Также используется для создания начальной ионизации в ксеноновых дуговых лампах, некоторых неоновых лампах, рассчитаных на низкое напряжение работы, разрядниках. Он добавляется в рабочую смесь газов газоразрядного прибора в небольших активностях (до 0,1 мкКи).
См. также[править | править код]
- Протий
- Дейтерий
- Тяжёлая вода
- Тритиевая вода
Примечания[править | править код]
- ↑ 1 2 3 4 Audi G., Wapstra A. H., Thibault C. The AME2003 atomic mass evaluation (II). Tables, graphs, and references (англ.) // Nuclear Physics A. — 2003. — Vol. 729. — P. 337—676. — doi:10.1016/j.nuclphysa.2003.11.003. — Bibcode: 2003NuPhA.729..337A.
- ↑ 1 2 3 Audi G., Bersillon O., Blachot J., Wapstra A. H. The NUBASE evaluation of nuclear and decay properties // Nuclear Physics A. — 2003. — Т. 729. — С. 3—128. — doi:10.1016/j.nuclphysa.2003.11.001. — Bibcode: 2003NuPhA.729….3A.
- ↑ Архивированная копия. Дата обращения: 23 ноября 2014. Архивировано из оригинала 29 ноября 2014 года.
- ↑ Urey H. C., Murphy G. M., Brickwedde F. G. A Name and Symbol for H2* (англ.) // Journal of Chemical Physics : journal. — 1933. — Vol. 1. — P. 512—513. — doi:10.1063/1.1749325.
- ↑ Dan O’Leary. The deeds to deuterium (англ.) // Nature Chemistry : journal. — 2012. — Vol. 4. — P. 236. — doi:10.1038/nchem.1273.
- ↑ Nuclide safety data sheet: Hydrogen-3. ehso.emory.edu. Дата обращения: 12 июля 2014. Архивировано из оригинала 20 мая 2013 года.
- ↑ Backgrounder on Tritium, Radiation Protection Limits, and Drinking Water Standards (англ.). U.S.NRC (февраль 2011). Дата обращения: 5 октября 2012. Архивировано 14 октября 2012 года.
- ↑ R. V. Osborne. Review of the Greenpeace report: «Tritium Hazard Report: Pollution and Radiation Risk from Canadian Nuclear Facilities» (англ.) (pdf). Canadian Nuclear Association (август 2007). Дата обращения: 5 октября 2012. Архивировано 14 октября 2012 года.
- ↑ Hisham Zerriffi. Tritium: The environmental, health, budgetary, and strategic effects of the Department of Energy’s decision to produce tritium (англ.). Institute for Energy and Environmental Research (англ.) (рус. (январь 1996). Дата обращения: 15 сентября 2010. Архивировано 26 декабря 2018 года. полный текст Архивная копия от 13 ноября 2013 на Wayback Machine
- ↑ Михаил Сторожевой. Третируемый тритий. ATOMINFO.RU (28 октября 2010). Дата обращения: 13 ноября 2013. Архивировано 13 ноября 2013 года.
- ↑ Производство плутония и трития для ядерного оружия. Стратегическое ядерное вооружение СССР и России. Дата обращения: 13 ноября 2013. Архивировано из оригинала 13 ноября 2013 года.
- ↑ Бекман. 6. РЕАКТОРЫ ДЛЯ НАРАБОТКИ ТРИТИЯ. Дата обращения: 13 ноября 2013. Архивировано 13 ноября 2013 года.
- ↑ Martin В. Kalinowski, Lars С. Colschen International Control of Tritium to Prevent Horizontal Proliferation and to Foster Nuclear Disarmament Архивная копия от 13 ноября 2013 на Wayback Machine // Science & Global Security, 1994, vol. 5, рр. 131—203
- ↑ Hisham Zerriffi. Tritium: The environmental, health, budgetary, and strategic effects of the Department of Energy’s decision to produce tritium (англ.). Institute for Energy and Environmental Research (1996). Дата обращения: 13 ноября 2013. Архивировано 19 октября 2014 года.
- ↑ International Control of Tritium for Nuclear Nonproliferation and Disarmament Архивная копия от 20 января 2019 на Wayback Machine, CRC Press, 2004, page 15
- ↑ 1 2 Tritium Supply Considerations Архивная копия от 11 октября 2010 на Wayback Machine, LANL, 2003. «ITER startup inventory estimated to be ~3 Kg»
- ↑ Alasdair Cros. Is fusion power really viable? (англ.) (5 марта 2010). Дата обращения: 19 января 2019. Архивировано 26 сентября 2015 года.BBC News — Is fusion power really viable? Архивная копия от 26 сентября 2015 на Wayback Machine
- ↑ Незаменимые батарейки: Сила трития. Журнал «Популярная Механика» (27 августа 2012). — «Размерами с фалангу пальца, они используют радиоактивный распад для производства электричества – в небольших количествах, зато непрерывно в течение минимум лет двадцати. … цена остается пока на уровне 1000 долларов». Дата обращения: 13 ноября 2013. Архивировано 13 ноября 2013 года.
Ссылки[править | править код]
Дефект массы и энергия связи трития и какой процент от энергии?
энергия атома
#7745
2011-11-10 02:29 GMT
Всем привет.
Получил на дом такую задачу, прочитал условие и до сих пор не понимаю с чего тут начинать решать?
Какие тут ключевые слова в условии?
553. Найти дефект массы и энергию связи трития (^{3}_{1}H). Какой процент
от энергии покоя ядра составляет его энергия связи?
Каким тегом можно уменьшить картинку? Подскажите пожалуйста.
#7747
2011-11-10 09:52 GMT
пусть
m – масса атома трития, mp – масса протона, mn – масса нейтрона. тогда дефект масс есть
(Delta{m}=m_p+2m_n-m)
все величины табличные
Добавлено спустя 1 минута
Начинать решать надо с чтения учебника
отредактировал(а) iskander: 2011-11-10 09:53 GMT
 |
|
| General | |
|---|---|
| Symbol | 3H |
| Names | tritium, 3H, H-3, hydrogen-3, T, 3T |
| Protons (Z) | 1 |
| Neutrons (N) | 2 |
| Nuclide data | |
| Natural abundance | 10−18 in hydrogen[1] |
| Half-life (t1/2) | 12.32 years |
| Isotope mass | 3.01604928 Da |
| Spin | 1/2 |
| Excess energy | 14949.794±0.001 keV |
| Binding energy | 8481.7963±0.0009 keV |
| Decay products | 3He |
| Decay modes | |
| Decay mode | Decay energy (MeV) |
| Beta emission | 0.018590 |
| Isotopes of hydrogen Complete table of nuclides |
Tritium (from Ancient Greek τρίτος (trítos) ‘third’) or hydrogen-3 (symbol T or 3H) is a rare and radioactive isotope of hydrogen with a half-life of about 12 years. The nucleus of tritium (t, sometimes called a triton) contains one proton and two neutrons, whereas the nucleus of the common isotope hydrogen-1 (protium) contains one proton and zero neutrons, and that of hydrogen-2 (deuterium) contains one proton and one neutron.
Naturally occurring tritium is extremely rare on Earth. The atmosphere has only trace amounts, formed by the interaction of its gases with cosmic rays. It can be produced artificially by irradiating lithium metal or lithium-bearing ceramic pebbles in a nuclear reactor and is a low-abundance byproduct in normal operations of nuclear reactors.
Tritium is used as the energy source in radioluminescent lights for watches, gun sights, numerous instruments and tools, and even novelty items such as self-illuminating key chains. It is used in a medical and scientific setting as a radioactive tracer. Tritium is also used as a nuclear fusion fuel, along with more abundant deuterium, in tokamak reactors and in hydrogen bombs.
History[edit]
Tritium was first detected in 1934 by Ernest Rutherford, Mark Oliphant and Paul Harteck after bombarding deuterium with deuterons (a proton and neutron, comprising a deuterium nucleus). Deuterium is another isotope of hydrogen.[2][3] However, their experiment could not isolate tritium, which was accomplished in 1939 by Luis Alvarez and Robert Cornog, who also realized tritium’s radioactivity.[4][5] Willard Libby recognized that tritium could be used for radiometric dating of water and wine.[6]
Decay[edit]
While tritium has several different experimentally determined values of its half-life, the National Institute of Standards and Technology lists 4,500 ± 8 days (12.32 ± 0.02 years), which is approximately 5.5% of remaining tritium decaying annually.[7] It decays into helium-3 by beta decay as per this nuclear equation:
-
3
1H
→ 3
2He
+
e−
+
ν
e
and it releases 18.6 keV of energy in the process. The electron’s kinetic energy varies, with an average of 5.7 keV, while the remaining energy is carried off by the nearly undetectable electron antineutrino. Beta particles from tritium can penetrate only about 6.0 millimetres (0.24 in) of air, and they are incapable of passing through the dead outermost layer of human skin.[8] Due to their low energy compared to other beta particles, the amount of bremsstrahlung generated is also lower. The unusually low energy released in the tritium beta decay makes the decay (along with that of rhenium-187) appropriate for absolute neutrino mass measurements in the laboratory (the most recent such experiment being KATRIN).
The low energy of tritium’s radiation makes it difficult to detect tritium-labeled compounds except by using liquid scintillation counting.
Production[edit]
Lithium[edit]
Tritium is most often produced in nuclear reactors by neutron activation of lithium-6. The release and diffusion of tritium and helium produced by the fission of lithium can take place within ceramics referred to as breeder ceramics. The production of tritium from lithium-6 in such breeder ceramics is possible with neutrons of any energy, though the cross section is higher when the incident neutrons have lower energy, reaching more than 900 barns for thermal neutrons. This is an exothermic reaction, yielding 4.8 MeV.[9] In comparison, the fusion of deuterium with tritium releases about 17.6 MeV of energy. For applications in proposed fusion energy reactors, such as ITER, pebbles consisting of lithium bearing ceramics including Li2TiO3 and Li4SiO4, are being developed for tritium breeding within a helium-cooled pebble bed, also known as a breeder blanket.[10]
-
6
3Li
+
n
→ 4
2He
( 2.05 MeV ) + 3
1T
( 2.75 MeV )
High-energy neutrons can also produce tritium from lithium-7 in an endothermic (net heat consuming) reaction, consuming 2.466 MeV. This was discovered when the 1954 Castle Bravo nuclear test produced an unexpectedly high yield.[11]
-
7
3Li
+
n
→ 4
2He
+ 3
1T
+
n
Boron[edit]
High-energy neutrons irradiating boron-10 will also occasionally produce tritium:[12]
-
10
5B
+
n
→ 2 4
2He
+ 3
1T
A more common result of boron-10 neutron capture is 7
Li
and a single alpha particle.[13]
Especially in pressurized water reactors which only partially thermalize neutrons, the interaction between relatively fast neutrons and the boric acid added as a chemical shim produces small but non-negligible quantities of tritium.
Deuterium[edit]
Tritium is also produced in heavy water-moderated reactors whenever a deuterium nucleus captures a neutron. This reaction has a quite small absorption cross section, making heavy water a good neutron moderator, and relatively little tritium is produced. Even so, cleaning tritium from the moderator may be desirable after several years to reduce the risk of its escaping to the environment. Ontario Power Generation’s “Tritium Removal Facility” processes up to 2,500 tonnes (2,500 long tons; 2,800 short tons) of heavy water a year, and it separates out about 2.5 kg (5.5 lb) of tritium, making it available for other uses.[14]
CANDU reactors typically produce 130 grams (4.6 oz) of tritium per year, which is recovered at the Darlington Tritium Recovery Facility (DTRF) attached to the 3,512 MW electric Darlington Nuclear Generating Station. The total production at DTRF between 1989 and 2011 was 42.5 kilograms (94 lb) – with an activity of 409 megacuries (15,100 PBq) – which averages to about 2 kilograms (4.4 lb) per year.[15]
Deuterium’s absorption cross section for thermal neutrons is about 0.52 millibarns, whereas that of oxygen-16 (16
8O
) is about 0.19 millibarns and that of oxygen-17 (17
8O
) is about 240 millibarns. While 16
O is by far the most common isotope of oxygen in both natural oxygen and heavy water, depending on the method used for isotope separation, heavy water may be slightly to notably higher in 17
O and 18
O content. Due to both neutron capture and (n,α) reactions (the latter of which produce 14
C an undesirable long-lived beta emitter from 17
O) they are net “neutron consumers” and are thus undesirable in a moderator of a natural uranium reactor which needs to keep neutron absorption outside the fuel as low as feasible. Some facilities that remove tritium also remove (or at least reduce the content of) 17
O and 18
O, which can – at least in principle – be put to use for isotope labeling.
India, which also has a large fleet of pressurized heavy water reactors (initially CANDU technology but since indigenized and further developed IPHWR technology), also removes at least some of the tritium produced in the moderator/coolant of its reactors but due to the dual use nature of tritium and the Indian nuclear bomb program, less information about this is publicly available than for Canada.
Fission[edit]
Tritium is an uncommon product of the nuclear fission of uranium-235, plutonium-239, and uranium-233, with a production of about one atom per 10,000 fissions.[16][17] The main pathways of tritium production include ternary fission of some kind.
The release or recovery of tritium needs to be considered in the operation of nuclear reactors, especially in the reprocessing of nuclear fuels and in the storage of spent nuclear fuel. The production of tritium is not a goal, but rather a side-effect. It is discharged to the atmosphere in small quantities by some nuclear power plants.[18] Voloxidation is an optional additional step in nuclear reprocessing that removes volatile fission products (such as all isotopes of hydrogen) before an aqueous process begins. This would in principle enable economic recovery of the produced tritium but even if the tritium is only disposed and not used, it has the potential to reduce tritium contamination in the water used, reducing radioactivity released when the water is discharged since tritiated water cannot be removed from “ordinary” water except by isotope separation.
| Location | Nuclear facility | Closest waters |
Liquid (TBq) |
Steam (TBq) |
Total (TBq) |
Total (mg) |
year |
|---|---|---|---|---|---|---|---|
| Heysham nuclear power station B | Irish Sea | 396 | 2.1 | 398 | 1,115 | 2019 | |
| Sellafield reprocessing facility | Irish Sea | 423 | 56 | 479 | 1,342 | 2019 | |
| Cernavodă Nuclear Power Plant Unit 1 | Black Sea | 140 | 152 | 292 | 872 | 2018 | |
| La Hague reprocessing plant | English Channel | 11,400 | 60 | 11,460 | 32,100 | 2018 | |
| Wolseong Nuclear Power Plant and others | Sea of Japan | 211 | 154 | 365 | 1,022 | 2020[20] | |
| Maanshan Nuclear Power Plant | Luzon Strait | 35 | 9.4 | 44 | 123 | 2015 | |
| Fuqing Nuclear Power Plant | Taiwan Strait | 52 | 0.8 | 52 | 146 | 2020 | |
| Sanmen Nuclear Power Station | East China Sea | 20 | 0.4 | 20 | 56 | 2020 | |
| Bruce Nuclear Generating Station A, B | Great Lakes | 756 | 994 | 1,750 | 4,901 | 2018 | |
| Darlington Nuclear Generating Station | Great Lakes | 220 | 210 | 430 | 1,204 | 2018 | |
| Pickering Nuclear Generating Station Units 1-4 | Great Lakes | 140 | 300 | 440 | 1,232 | 2015 | |
| Diablo Canyon Power Plant Units1, 2 | Pacific Ocean | 82 | 2.7 | 84 | 235 | 2019 |
Given the specific activity of tritium at 9,650 curies per gram (357 TBq/g), one TBq is equivalent to roughly 2.8 milligrams (0.043 gr).
Fukushima Daiichi[edit]
In June 2016 the Tritiated Water Task Force released a report[21] on the status of tritium in tritiated water at Fukushima Daiichi nuclear plant, as part of considering options for final disposal of the stored contaminated cooling water. This identified that the March 2016 holding of tritium on-site was 760 TBq (equivalent to 2.1 g of tritium or 14 mL of pure tritiated water) in a total of 860,000 m3 of stored water. This report also identified the reducing concentration of tritium in the water extracted from the buildings etc. for storage, seeing a factor of ten decrease over the five years considered (2011–2016), 3.3 MBq/L to 0.3 MBq/L (after correction for the 5% annual decay of tritium).
According to a report by an expert panel considering the best approach to dealing with this issue, “Tritium could be separated theoretically, but there is no practical separation technology on an industrial scale. Accordingly, a controlled environmental release is said to be the best way to treat low-tritium-concentration water.”[22] After a public information campaign sponsored by the Japanese government, the gradual release into the sea of the tritiated water will start in 2023. The process will take “decades” to complete.[23] China reacted with protest.[24][25]
The IAEA has endorsed the plan. The water released is diluted to reduce the tritium concentration to less than 1500 Bq/L, far below the limit recommended in drinking water by the WHO.[26]
Helium-3[edit]
Tritium’s decay product helium-3 has a very large cross section (5330 barns) for reacting with thermal neutrons, expelling a proton; hence, it is rapidly converted back to tritium in nuclear reactors.[27]
Cosmic rays[edit]
Tritium occurs naturally due to cosmic rays interacting with atmospheric gases. In the most important reaction for natural production, a fast neutron (which must have energy greater than 4.0 MeV[28]) interacts with atmospheric nitrogen:
-
14
7N
+
n
→ 12
6C
+ 3
1T
Worldwide, the production of tritium from natural sources is 148 petabecquerels per year. The global equilibrium inventory of tritium created by natural sources remains approximately constant at 2,590 petabecquerels. This is due to a fixed production rate, and losses proportional to the inventory.[29]
Production history[edit]
Tritium for American nuclear weapons was produced in special heavy water reactors at the Savannah River Site until their closures in 1988. With the Strategic Arms Reduction Treaty (START) after the end of the Cold War, the existing supplies were sufficient for the new, smaller number of nuclear weapons for some time.
According to a 1996 report from Institute for Energy and Environmental Research on the US Department of Energy, only 225 kg (496 lb) of tritium had been produced in the United States from 1955 to 1996.[a] Since it continually decays into helium-3, the total amount remaining was about 75 kg (165 lb) at the time of the report,[30][11]
and about 16 kg (35 lb) as of 2023.[31]
The production of tritium was resumed with irradiation of rods containing lithium (replacing the usual control rods containing boron, cadmium, or hafnium), at the reactors of the commercial Watts Bar Nuclear Plant from 2003 to 2005 followed by extraction of tritium from the rods at the new Tritium Extraction Facility at the Savannah River Site beginning in November 2006.[32][33] Tritium leakage from the rods during reactor operations limits the number that can be used in any reactor without exceeding the maximum allowed tritium levels in the coolant.[34]
Properties[edit]
Tritium has an atomic mass of 3.01604928 u. Diatomic tritium (T2 or 3H2) is a gas at standard temperature and pressure. Combined with oxygen, it forms a liquid called tritiated water (T2O).
Compared to hydrogen in its natural composition on Earth, tritium has a higher melting point (20.62 K vs. 13.99 K), a higher boiling point (25.04 K vs. 20.27 K), a higher critical temperature (40.59 K vs. 32.94 K) and a higher critical pressure (1.8317 MPa vs. 1.2858 MPa).[35]
Tritium’s specific activity is 9,650 curies per gram (3.57×1014 Bq/g).[36]
Tritium figures prominently in studies of nuclear fusion because of its favorable reaction cross section and the large amount of energy (17.6 MeV) produced through its reaction with deuterium:
-
3
1T
+ 2
1D
→ 4
2He
+
n
All atomic nuclei contain protons as their only electrically charged particles. They therefore repel one another because like charges repel. However, if the atoms have a high enough temperature and pressure (for example, in the core of the Sun), then their random motions can overcome such electrical repulsion (called the Coulomb force), and they can come close enough for the strong nuclear force to take effect, fusing them into heavier atoms.
The tritium nucleus, containing one proton and two neutrons, has the same charge as the nucleus of ordinary hydrogen, and it experiences the same electrostatic repulsive force when brought close to another atomic nucleus. However, the neutrons in the tritium nucleus increase the attractive strong nuclear force when brought close enough to another atomic nucleus. As a result, tritium can more easily fuse with other light atoms, compared with the ability of ordinary hydrogen to do so.
The same is true, albeit to a lesser extent, of deuterium. This is why brown dwarfs (so-called ‘failed’ stars) cannot utilize ordinary hydrogen, but they do fuse the small minority of deuterium nuclei.
Radioluminescent 1.8 curies (67 GBq) 6 by 0.2 inches (152.4 mm × 5.1 mm) tritium vials are thin, tritium-gas-filled glass vials whose inner surfaces are coated with a phosphor. The vial shown here is brand-new.
Like the other isotopes of hydrogen, tritium is difficult to confine. Rubber, plastic, and some kinds of steel are all somewhat permeable. This has raised concerns that if tritium were used in large quantities, in particular for fusion reactors, it may contribute to radioactive contamination, although its short half-life should prevent significant long-term accumulation in the atmosphere.
The high levels of atmospheric nuclear weapons testing that took place prior to the enactment of the Partial Nuclear Test Ban Treaty proved to be unexpectedly useful to oceanographers. The high levels of tritium oxide introduced into upper layers of the oceans have been used in the years since then to measure the rate of mixing of the upper layers of the oceans with their lower levels.
Health risks[edit]
Tritium is an isotope of hydrogen, which allows it to readily bind to hydroxyl radicals, forming tritiated water (HTO), and to carbon atoms. Since tritium is a low energy beta emitter, it is not dangerous externally (its beta particles are unable to penetrate the skin),[29] but it can be a radiation hazard if inhaled, ingested via food or water, or absorbed through the skin.[37][38][39][40] HTO has a short biological half-life in the human body of 7 to 14 days, which both reduces the total effects of single-incident ingestion and precludes long-term bioaccumulation of HTO from the environment.[39][41] The biological half life of tritiated water in the human body, which is a measure of body water turn-over, varies with the season. Studies on the biological half life of occupational radiation workers for free water tritium in a coastal region of Karnataka, India, show that the biological half life in the winter season is twice that of the summer season.[41] If tritium exposure is suspected or known, drinking uncontaminated water will help replace the tritium from the body. Increasing sweating, urination or breathing can help the body expel water and thereby the tritium contained in it. However, care should be taken that neither dehydration nor a depletion of the body’s electrolytes results as the health consequences of those things (particularly in the short term) can be more severe than those of tritium exposure.
Environmental contamination[edit]
Tritium has leaked from 48 of 65 nuclear sites in the US. In one case, leaking water contained 7.5 microcuries (280 kBq) of tritium per liter, which is 375 times the current EPA limit for drinking water, and 28 times the World Health Organization’s recommended limit.[42] This is equivalent to 0.777 nanograms per litre (5.45×10−8 gr/imp gal) or roughly 0.8 parts per trillion.
The US Nuclear Regulatory Commission states that in normal operation in 2003, 56 pressurized water reactors released 40,600 curies (1,500,000 GBq) of tritium (maximum: 2,080 Ci (77,000 GBq); minimum: 0.1 Ci (3.7 GBq); average: 725 Ci (26,800 GBq)) and 24 boiling water reactors released 665 Ci (24.6 TBq) (maximum: 174 Ci (6,400 GBq); minimum: 0 Ci; average: 27.7 Ci (1,020 GBq)), in liquid effluents.[43] 40,600 Curie of tritium are approximately equivalent to 4.207 grams (0.1484 oz)
According to the U.S. Environmental Protection Agency, self-illuminating exit signs improperly disposed in municipal landfills have been recently[when?] found to contaminate waterways.[44]
Regulatory limits[edit]
The legal limits for tritium in drinking water vary widely from country to country. Some figures are given below:
-
Tritium drinking water limits by country[45]
Country Tritium limit
(Bq/L)Australia 76,103 [b] Japan 60,000 Finland 30,000 World Health Organization 10,000 Switzerland 10,000 Russia 7,700 Canada (Ontario) 7,000 United States 740 Norway 100 [47]
The American limit is calculated to yield a dose of 4.0 millirems (or 40 microsieverts in SI units) per year.[39] This is about 1.3% of the natural background radiation (roughly 3,000 μSv). For comparison, the banana equivalent dose (BED) is set at 0.1 μSv, so the statutory limit in the US is set at 400 BED.
Use[edit]
Biological radiometric assays[edit]
Tritium has been used for biological radiometric assays, in a process akin to radiocarbon dating. For example, in one paper, [3H] retinyl acetate was traced through the body of Sprague-Dawley rats.[48]
Self-powered lighting[edit]
The beta particles emitted by the radioactive decay of small amounts of tritium cause chemicals called phosphors to glow.
This radioluminescence is used in self-powered lighting devices called betalights, which are used for night illumination of firearm sights, watches, exit signs, map lights, navigational compasses (such as current-use M-1950 U.S. military compasses), knives and a variety of other devices.[c] As of 2000, commercial demand for tritium is 400 grams (0.88 lb) per year[11] and the cost is $30,000 per gram ($850,000/oz)[49] or more.[50]
Nuclear weapons[edit]
Tritium is an important component in nuclear weapons. It is used to enhance the efficiency and yield of fission bombs and the fission stages of hydrogen bombs in a process known as “boosting” as well as in external neutron initiators for such weapons.
Neutron initiator[edit]
These are devices incorporated in nuclear weapons which produce a pulse of neutrons when the bomb is detonated to initiate the fission reaction in the fissionable core (pit) of the bomb, after it is compressed to a critical mass by explosives. Actuated by an ultrafast switch like a krytron, a small particle accelerator drives ions of tritium and deuterium to energies above the 15 keV or so needed for deuterium-tritium fusion and directs them into a metal target where the tritium and deuterium are adsorbed as hydrides. High-energy fusion neutrons from the resulting fusion radiate in all directions. Some of these strike plutonium or uranium nuclei in the primary’s pit, initiating a nuclear chain reaction. The quantity of neutrons produced is large in absolute numbers, allowing the pit to quickly achieve neutron levels that would otherwise need many more generations of chain reaction, though still small compared to the total number of nuclei in the pit.
Boosting[edit]
Before detonation, a few grams of tritium-deuterium gas are injected into the hollow “pit” of fissile plutonium or uranium. The early stages of the fission chain reaction supply enough heat and compression to start deuterium-tritium fusion; then both fission and fusion proceed in parallel, the fission assisting the fusion by continuing heating and compression, and the fusion assisting the fission with highly energetic (14.1 MeV) neutrons. As the fission fuel depletes and also explodes outward, it falls below the density needed to stay critical by itself, but the fusion neutrons make the fission process progress faster and continue longer than it would without boosting. Increased yield comes overwhelmingly from the increase in fission. The energy released by the fusion itself is much smaller because the amount of fusion fuel is so much smaller. The effects of boosting include:
- increased yield (for the same amount of fission fuel, compared to detonation without boosting)
- the possibility of variable yield by varying the amount of fusion fuel
- allowing the bomb to require a smaller amount of the very expensive fissile material – and also eliminating the risk of predetonation by nearby nuclear explosions
- not so stringent requirements on the implosion setup, allowing for a smaller and lighter amount of high-explosives to be used
The tritium in a warhead is continually undergoing radioactive decay, hence becoming unavailable for fusion. Furthermore, its decay product, helium-3, absorbs neutrons if exposed to the ones emitted by nuclear fission. This potentially offsets or reverses the intended effect of the tritium, which was to generate many free neutrons, if too much helium-3 has accumulated from the decay of tritium. Therefore, it is necessary to replenish tritium in boosted bombs periodically. The estimated quantity needed is 4 grams (0.14 oz) per warhead.[11] To maintain constant levels of tritium, about 0.20 grams (0.0071 oz) per warhead per year must be supplied to the bomb.
One mole of deuterium-tritium gas would contain about 3.0 grams (0.11 oz) of tritium and 2.0 grams (0.071 oz) of deuterium. In comparison, the 20 moles of plutonium in a nuclear bomb consists of about 4.5 kilograms (9.9 lb) of plutonium-239.
Tritium in hydrogen bomb secondaries[edit]
Since tritium undergoes radioactive decay, and is also difficult to confine physically, the much larger secondary charge of heavy hydrogen isotopes needed in a true hydrogen bomb uses solid lithium deuteride as its source of deuterium and tritium, producing the tritium in situ during secondary ignition.
During the detonation of the primary fission bomb stage in a thermonuclear weapon (Teller-Ulam staging), the sparkplug, a cylinder of 235U/239Pu at the center of the fusion stage(s), begins to fission in a chain reaction, from excess neutrons channeled from the primary. The neutrons released from the fission of the sparkplug split lithium-6 into tritium and helium-4, while lithium-7 is split into helium-4, tritium, and one neutron. As these reactions occur, the fusion stage is compressed by photons from the primary and fission of the 238U or 238U/235U jacket surrounding the fusion stage. Therefore, the fusion stage breeds its own tritium as the device detonates. In the extreme heat and pressure of the explosion, some of the tritium is then forced into fusion with deuterium, and that reaction releases even more neutrons.
Since this fusion process requires an extremely high temperature for ignition, and it produces fewer and less energetic neutrons (only fission, deuterium-tritium fusion, and 7
3Li
splitting are net neutron producers), lithium deuteride is not used in boosted bombs, but rather for multi-stage hydrogen bombs.
Controlled nuclear fusion[edit]
Tritium is an important fuel for controlled nuclear fusion in both magnetic confinement and inertial confinement fusion reactor designs. The National Ignition Facility (NIF) uses deuterium-tritium fuel, and the experimental fusion reactor ITER will also do so. The deuterium-tritium reaction is favorable since it has the largest fusion cross section (about 5.0 barns) and it reaches this maximum cross section at the lowest energy (about 65 keV center-of-mass) of any potential fusion fuel.
The Tritium Systems Test Assembly (TSTA) was a facility at the Los Alamos National Laboratory dedicated to the development and demonstration of technologies required for fusion-relevant deuterium-tritium processing.
Analytical chemistry[edit]
Tritium is sometimes used as a radiolabel. It has the advantage that almost all organic chemicals contain hydrogen, making it easy to find a place to put tritium on the molecule under investigation. It has the disadvantage of producing a comparatively weak signal.
Electrical power source[edit]
Tritium can be used in a betavoltaic device to create an atomic battery to generate electricity.
Use as an oceanic transient tracer[edit]
Aside from chlorofluorocarbons, tritium can act as a transient tracer and has the ability to “outline” the biological, chemical, and physical paths throughout the world oceans because of its evolving distribution.[51] Tritium has thus been used as a tool to examine ocean circulation and ventilation and, for such purposes, is usually measured in Tritium Units where 1 TU is defined as the ratio of 1 tritium atom to 1018 hydrogen atoms,[51] approximately equal to 0.118 Bq/liter.[52] As noted earlier, nuclear weapons testing, primarily in the high-latitude regions of the Northern Hemisphere, throughout the late 1950s and early 1960s introduced large amounts of tritium into the atmosphere, especially the stratosphere. Before these nuclear tests, there were only about 3 to 4 kilograms of tritium on the Earth’s surface; but these amounts rose by 2 or 3 orders of magnitude during the post-test period.[51] Some sources reported natural background levels were exceeded by approximately 1,000 TU in 1963 and 1964 and the isotope is used in the northern hemisphere to estimate the age of groundwater and construct hydrogeologic simulation models.[53] Recent scientific sources have estimated atmospheric levels at the height of weapons testing to approach 1,000 TU and pre-fallout levels of rainwater to be between 5 and 10 TU.[54] In 1963 Valentia Island Ireland recorded 2,000 TU in precipitation.[55]
North Atlantic Ocean[edit]
While in the stratosphere (post-test period), the tritium interacted with and oxidized to water molecules and was present in much of the rapidly produced rainfall, making tritium a prognostic tool for studying the evolution and structure of the hydrologic cycle as well as the ventilation and formation of water masses in the North Atlantic Ocean.[51]
Bomb-tritium data were used from the Transient Tracers in the Ocean (TTO) program in order to quantify the replenishment and overturning rates for deep water located in the North Atlantic.[56]
Bomb-tritium also enters the deep ocean around the Antarctic.[57] Most of the bomb tritiated water (HTO) throughout the atmosphere can enter the ocean through the following processes:
- (a) precipitation
- (b) vapor exchange
- (c) river runoff
These processes make HTO a great tracer for time-scales of up to a few decades.[56]
Using the data from these processes for 1981, the 1 TU isosurface lies between 500 and 1,000 meters deep in the subtropical regions and then extends to 1,500–2,000 meters south of the Gulf Stream due to recirculation and ventilation in the upper portion of the Atlantic Ocean.[51] To the north, the isosurface deepens and reaches the floor of the abyssal plain which is directly related to the ventilation of the ocean floor over 10–20 year time-scales.[51]
Also evident in the Atlantic Ocean is the tritium profile near Bermuda between the late 1960s and late 1980s. There is a downward propagation of the tritium maximum from the surface (1960s) to 400 meters (1980s), which corresponds to a deepening rate of approximately 18 meters per year.[51] There are also tritium increases at 1,500 meters depth in the late 1970s and 2,500 meters in the middle of the 1980s, both of which correspond to cooling events in the deep water and associated deep water ventilation.[51]
From a study in 1991, the tritium profile was used as a tool for studying the mixing and spreading of newly formed North Atlantic Deep Water (NADW), corresponding to tritium increases to 4 TU.[56] This NADW tends to spill over sills that divide the Norwegian Sea from the North Atlantic Ocean and then flows to the west and equatorward in deep boundary currents. This process was explained via the large-scale tritium distribution in the deep North Atlantic between 1981 and 1983.[56] The sub-polar gyre tends to be freshened (ventilated) by the NADW and is directly related to the high tritium values (> 1.5 TU). Also evident was the decrease in tritium in the deep western boundary current by a factor of 10 from the Labrador Sea to the Tropics, which is indicative of loss to ocean interior due to turbulent mixing and recirculation.[56]
Pacific and Indian oceans[edit]
In a 1998 study, tritium concentrations in surface seawater and atmospheric water vapor (10 meters above the surface) were sampled at the following locations: the Sulu Sea, the Fremantle Bay, the Bay of Bengal, the Penang Bay, and the Strait of Malacca.[58] Results indicated that the tritium concentration in surface seawater was highest at the Fremantle Bay (approximately 0.40 Bq/liter), which could be accredited to the mixing of runoff of freshwater from nearby lands due to large amounts found in coastal waters.[58] Typically, lower concentrations were found between 35 and 45 degrees south latitude and near the equator. Results also indicated that (in general) tritium has decreased over the years (up to 1997) due to the physical decay of bomb tritium in the Indian Ocean. As for water vapor, the tritium concentration was approximately one order of magnitude greater than surface seawater concentrations (ranging from 0.46 to 1.15 Bq/liter).[58] Therefore, the water vapor tritium is not affected by the surface seawater concentration; thus, the high tritium concentrations in the vapor were concluded to be a direct consequence of the downward movement of natural tritium from the stratosphere to the troposphere (therefore, the ocean air showed a dependence on latitudinal change).[58]
In the North Pacific Ocean, the tritium (introduced as bomb tritium in the Northern Hemisphere) spread in three dimensions. There were subsurface maxima in the middle and low latitude regions, which is indicative of lateral mixing (advection) and diffusion processes along lines of constant potential density (isopycnals) in the upper ocean.[59] Some of these maxima even correlate well with salinity extrema.[59] In order to obtain the structure for ocean circulation, the tritium concentrations were mapped on 3 surfaces of constant potential density (23.90, 26.02, and 26.81).[59] Results indicated that the tritium was well-mixed (at 6 to 7 TU) on the 26.81 isopycnal in the subarctic cyclonic gyre and there appeared to be a slow exchange of tritium (relative to shallower isopycnals) between this gyre and the anticyclonic gyre to the south; also, the tritium on the 23.90 and 26.02 surfaces appeared to be exchanged at a slower rate between the central gyre of the North Pacific and the equatorial regions.[59]
The depth penetration of bomb tritium can be separated into three distinct layers:
- Layer 1
- Layer 1 is the shallowest layer and includes the deepest, ventilated layer in winter; it has received tritium via radioactive fallout and lost some due to advection and/or vertical diffusion and contains approximately 28% of the total amount of tritium.[59]
- Layer 2
- Layer 2 is below the first layer but above the 26.81 isopycnal and is no longer part of the mixed layer. Its two sources are diffusion downward from the mixed layer and lateral expansions outcropping strata (poleward); it contains about 58% of the total tritium.[59]
- Layer 3
- Layer 3 is representative of waters that are deeper than the outcrop isopycnal and can only receive tritium via vertical diffusion; it contains the remaining 14% of the total tritium.[59]
Mississippi River System[edit]
Nuclear fallout from Cold War weapons testing settled in the United States throughout the Mississippi River System. Tritium concentrations can be used to understand the residence times of continental hydrologic systems (as opposed to the usual oceanic hydrologic systems) which include surface waters such as lakes, streams, and rivers.[60] Studying these systems can also provide societies and municipals with information for agricultural purposes and overall river water quality.
In a 2004 study, several rivers were taken into account during the examination of tritium concentrations (starting in the 1960s) throughout the Mississippi River Basin: Ohio River (largest input to the Mississippi River flow), Missouri River, and Arkansas River.[60] The largest tritium concentrations were found in 1963 at all the sampled locations throughout these rivers and correlate well with the peak concentrations in precipitation due to the nuclear bomb tests in 1962. The overall highest concentrations occurred in the Missouri River (1963) and were greater than 1,200 TU while the lowest concentrations were found in the Arkansas River (never greater than 850 TU and less than 10 TU in the mid-1980s).[60]
Several processes can be identified using the tritium data from the rivers: direct runoff and outflow of water from groundwater reservoirs.[60] Using these processes, it becomes possible to model the response of the river basins to the transient tritium tracer. Two of the most common models are the following:
- Piston-flow approach
- tritium signal appears immediately; and
- Well-mixed reservoir approach
- outflow concentration depends upon the residence time of the basin water[60]
Unfortunately, both models fail to reproduce the tritium in river waters; thus, a two-member mixing model was developed that consists of two components: a prompt-flow component (recent precipitation – “piston”) and a component where waters reside in the basin for longer than 1 year (“well-mixed reservoir”).[60] Therefore, the basin tritium concentration becomes a function of the residence times within the basin, sinks (radioactive decay) or sources of tritium, and the input function.
For the Ohio River, the tritium data indicated that about 40% of the flow was composed of precipitation with residence times of less than one year (in the Ohio basin) and older waters consisted of residence times of about ten years.[60] Thus, the short residence times (less than one year) corresponded to the “prompt-flow” component of the two-member mixing model. As for the Missouri River, results indicated that residence times were approximately four years with the prompt-flow component being around 10% (these results are due to the series of dams in the area of the Missouri River).[60]
As for the mass flux of tritium through the main stem of the Mississippi River into the Gulf of Mexico, data indicated that approximately 780 grams of tritium has flowed out of the River and into the Gulf between 1961 and 1997,[60] an average of 7.7 PBq/yr. And current fluxes through the Mississippi River are about 1 to 2 grams per year as opposed to the pre-bomb period fluxes of roughly 0.4 grams per year.[60]
See also[edit]
- Hypertriton
- List of elements facing shortage
Footnotes[edit]
- ^ Total U.S. tritium production since 1955 has been approximately 225 kilograms, an estimated 150 kilograms of which have decayed into helium-3, leaving a current inventory of approximately 75 kilograms of tritium. — Zerriffi & Scoville (1996)[30]
- ^ This figure is derived from the guideline dose of 1 mSv per year from all sources of radiation in drinking water in The Australian Drinking Water Guidelines 6, assuming that tritium is the only radionuclide present in the water.[46]
- ^ Tritium has replaced radioluminescent paint containing radium in this application. Exposure to radium causes bone cancer, and its casual use has been banned in most countries for decades.
References[edit]
- ^
“Tritium”. britannica.com. Encyclopædia Britannica. - ^
Oliphant, M.L.; Harteck, P.; Rutherford, L. (1934). “Transmutation effects observed with heavy hydrogen”. Nature. 133 (3359): 413. Bibcode:1934Natur.133..413O. doi:10.1038/133413a0. S2CID 4078529. - ^
Oliphant, M.L.E.; Harteck, P.; Rutherford, L. (1934). “Transmutation Effects Observed with Heavy Hydrogen”. Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 144 (853): 692. Bibcode:1934RSPSA.144..692O. doi:10.1098/rspa.1934.0077. - ^
Alvarez, Luis; Cornog, Robert (1939). “Helium and Hydrogen of Mass 3”. Physical Review. 56 (6): 613. Bibcode:1939PhRv…56..613A. doi:10.1103/PhysRev.56.613. - ^
Alvarez, Luis W.; Trower, W. Peter (1987). Discovering Alvarez: Selected works of Luis W. Alvarez, with commentary by his students and colleagues. University of Chicago Press. pp. 26–30. ISBN 978-0-226-81304-2. - ^
Kaufman, Sheldon; Libby, W. (1954). “The natural distribution of tritium”. Physical Review. 93 (6): 1337. Bibcode:1954PhRv…93.1337K. doi:10.1103/PhysRev.93.1337. - ^
Lucas, L.L. & Unterweger, M. P. (2000). “Comprehensive review and critical evaluation of the half-life of tritium”. Journal of Research of the National Institute of Standards and Technology. 105 (4): 541–549. doi:10.6028/jres.105.043. PMC 4877155. PMID 27551621. - ^
Hydrogen-3 (PDF). ehso.emory.edu (Report). Nuclide safety data sheet. Archived from the original (PDF) on 20 May 2013. - ^ Rubel, M. (2019). “Fusion neutrons: tritium breeding and impact on wall materials and components of diagnostic systems”. Journal of Fusion Energy. 38 (3–4): 315–329. doi:10.1007/s10894-018-0182-1. S2CID 125723024.
- ^
Hanaor, Dorian A.H.; Kolb, Matthias H.H.; Gan, Yixiang; Kamlah, Marc; Knitter, Regina (2015). “Solution based synthesis of mixed-phase materials in the Li2TiO3–Li4SiO4 system”. Journal of Nuclear Materials. 456: 151–161. arXiv:1410.7128. Bibcode:2015JNuM..456..151H. doi:10.1016/j.jnucmat.2014.09.028. S2CID 94426898. - ^ a b c d
Zerriffi, Hisham (January 1996). Tritium: The environmental, health, budgetary, and strategic effects of the Department of Energy’s decision to produce tritium (Report). Institute for Energy and Environmental Research. Retrieved 15 September 2010. - ^
Jones, Greg (2008). “Tritium Issues in Commercial Pressurized Water Reactors”. Fusion Science and Technology. 54 (2): 329–332. Bibcode:2008FuST…54..329J. doi:10.13182/FST08-A1824. S2CID 117472371. - ^
Sublette, Carey (17 May 2006). “Nuclear Weapons FAQ Section 12.0 Useful Tables”. Nuclear Weapons Archive. Retrieved 19 September 2010. - ^
Whitlock, Jeremy. “Section D: Safety and Liability – How does Ontario Power Generation manage tritium production in its CANDU moderators?”. Canadian Nuclear FAQ. Retrieved 19 September 2010. - ^ Pearson, Richard J.; Antoniazzi, Armando B.; Nuttall, William J. (November 2018). “Tritium supply and use: a key issue for the development of nuclear fusion energy”. Fusion Engineering and Design. Elsevier. 136: 1140–1148. doi:10.1016/j.fusengdes.2018.04.090.
- ^ “Tritium (Hydrogen-3) – Human Health Fact sheet” (PDF). Argonne National Laboratory. August 2005. Archived from the original (PDF) on 8 February 2010. Retrieved 19 September 2010.
- ^
Serot, O.; Wagemans, C.; Heyse, J. (2005). “New results on helium and tritium gas production from ternary fission”. AIP Conference Proceedings. International Conference on Nuclear Data for Science and Technology. AIP Conference Proceedings. Vol. 769. American Institute of Physics. pp. 857–860. Bibcode:2005AIPC..769..857S. doi:10.1063/1.1945141. - ^
Effluent Releases from Nuclear Power Plants and Fuel-Cycle Facilities. National Academies Press (US). 29 March 2012. - ^ “Basic policy on handling of the ALPS treated water” (PDF). Ministry of Economy, Trade and Industry. 13 April 2021.
- ^ “2020년도 원전주변 환경방사능 조사 및 평가보고서” [2020 Environmental Radiation Survey and Evaluation Report Around Nuclear Power Plant]. Korea Hydro & Nuclear Power. 26 April 2021. p. 25.
- ^
Tritiated Water Task Force Report (PDF). www.meti.go.jp/english (Report). Tokyo, Japan: Ministry of Economy, Trade and Industry. - ^
“JP Gov “No drastic technology to remove Tritium was found in internationally collected knowledge”“. Fukushima Diary. December 2013. - ^ McCurry, Justin (16 April 2021). “Rosy-cheeked face of tritium dropped from Fukushima’s publicity drive”. the Guardian. p. 29.
- ^ “China to Japanese official: If treated radioactive water from Fukushima is safe, ‘please drink it’ – The Washington Post”. The Washington Post.
- ^ “Japan Faces Growing Pressure to Rethink Releasing Fukushima’s Wastewater into Ocean”.
- ^ “Why is Japan dumping radioactive water at sea?”. 13 April 2021.
- ^
“Helium-3 neutron proportional counters” (PDF). mit.edu. Cambridge, MA: Massachusetts Institute of Technology. Archived from the original (PDF) on 21 November 2004. - ^
Young, P.G. & Foster, D.G., Jr. (September 1972). “An evaluation of the neutron and gamma-ray production cross-sections for nitrogen” (PDF). Los Alamos, NM: Los Alamos Scientific Laboratory. Retrieved 19 September 2010. - ^ a b
“Tritium information section”. Physics Department. Radiation Information Network. Idaho State University. Archived from the original on 3 March 2016. - ^ a b
Zerriffi, Hisham; Scoville, Herbert Jr. (January 1996). “Tritium: The environmental, health, budgetary, and strategic effects of the Department of Energy’s decision to produce tritium” (PDF). Institute for Energy and Environmental Research. p. 5. Archived from the original (PDF) on 16 October 2014. Retrieved 6 September 2018. - ^ 27 years have passed since 1996, i.e. 2.25 half-lives, which reduce the 75kg of 1996 to 75/2^(2.25) ≈15.8 kg.
- ^
“Defense Programs”. Savannah River Site. U.S. Departmentof Energy. Retrieved 20 March 2013. - ^
“Tritium Extraction Facility” (PDF). Savannah River Site. Factsheets. U.S. Departmentof Energy. December 2007. Retrieved 19 September 2010. - ^
Horner, Daniel (November 2010). “GAO finds problems in tritium production”. Arms Control Today (Press release). - ^ PubChem. “Hazardous Substances Data Bank (HSDB) : 6467”. pubchem.ncbi.nlm.nih.gov. Retrieved 27 February 2023.
- ^
H-3. OSEH (Report). Radionuclide Safety Data Sheets. University of Michigan. Retrieved 20 March 2013. - ^ Fairlie, I. (June 2007). Tritium Hazard Report: Pollution and Radiation Risk from Canadian Nuclear Facilities (PDF) (Report). Archived from the original (PDF) on 20 May 2010. Retrieved 21 September 2008.
- ^
Osborne, R.V. (August 2007). Review of the Greenpeace report: “Tritium Hazard Report: Pollution and Radiation Risk from Canadian Nuclear Facilities” (PDF). nuclearfaq.ca (Report). - ^ a b c
Backgrounder on Tritium, Radiation Protection Limits, and Drinking Water Standards (Report). U.S. Nuclear Regulatory Commission. 15 March 2011. Retrieved 10 February 2012. - ^
Tritium Facts and Information (Report). Pennsylvania Department of Environmental Protection. Archived from the original on 15 May 2013. - ^ a b
Singh, V. P.; Pai, R. K.; Veerender, D. D.; Vishnu, M. S.; Vijayan, P.; Managanvi, S. S.; Badiger, N. M.; Bhat, H. R. (2010). “Estimation of biological half-life of tritium in coastal region of India”. Radiation Protection Dosimetry. 142 (2–4): 153–159. doi:10.1093/rpd/ncq219. PMID 20870665. - ^ Radioactive tritium leaks found at 48 US nuke sites. NBC News (21 June 2011). Retrieved on 16 October 2014.
- ^ NRC: Frequently Asked Questions About Liquid Radioactive Releases “What are normal amounts of tritium released from nuclear power plants?”
- ^ What does tritium do once it gets into the body?. U.S. Environmental Protection Agency (24 April 2012). Retrieved on 29 April 2013.
- ^
“Tritium in drinking water”. Canadian Nuclear Safety Commission. 3 February 2014. Retrieved 23 February 2017. - ^
“Australian Drinking Water Guidelines 6”. National Health and Medical Research Council, National Resource Management Ministerial Council, Commonwealth of Australia, Canberra. March 2015. p. 98. - ^
“Forskrift om visse forurensende stoffer i næringsmidler” (in Norwegian). Lovdata. 10 July 2015. Retrieved 7 January 2023. - ^ Green, Joanne Balmer; Green, Michael H. (2020). “Vitamin A Absorption Determined in Rats Using a Plasma Isotope Ratio Method”. The Journal of Nutrition. 150 (7): 1977–1981. doi:10.1093/jn/nxaa092. PMC 7330459. PMID 32271921.
- ^
Willms, Scott (14 January 2003). Tritium Supply Considerations (PDF) (Report). Los Alamos, NM: Los Alamos National Laboratory. Retrieved 1 August 2010. - ^ Jassby, Daniel (25 May 2022). “The Quest for Fusion Energy”. Inference. 7 (1).
- ^ a b c d e f g h
Jenkins, William J.; et al. (1996). “Transient Tracers Track Ocean Climate Signals”. Oceanus (Report). Woods Hole Oceanographic Institution. - ^
Stonestrom, David A.; et al. (2013). “On the conversion of tritium units to mass fractions for hydrologic applications”. Isotopes Environ Health Stud. 9 (2): 250–256. doi:10.1080/10256016.2013.766610. PMC 3664909. PMID 23464868. - ^
Maidment, David R., ed. (1993). Handbook of Hydrology. New York, NY: McGraw-Hill. pp. 6–39. ISBN 0-07-039732-5. - ^
Cossairt, J. Donald (September 2012). Background Levels of Tritium. Fermilab Environmental Safety & Health Section (Report). Environmental Protection Note. Batavia, Illinois: Fermi National Accelerator Laboratory. pp. 2–3. No. 28. - ^ Wunsch, Carl. (2015). Modern observational physical oceanography : understanding the global ocean. Princeton : Princeton University Press. p. 44 Figure 2.29. ISBN 9780691158822.
- ^ a b c d e
Doney, Scott C. (1992). “Bomb tritium in the deep north Atlantic”. Oceanography. 5 (3): 169–170. doi:10.5670/oceanog.1992.11. - ^
Michel, Robert; Williams, Peter M. (1973). “Bomb-produced tritium in the Antarctic Ocean”. Earth and Planetary Science Letters. 20 (3): 381–384. Bibcode:1973E&PSL..20..381M. doi:10.1016/0012-821X(73)90013-7. - ^ a b c d
Kakiuchi, H.; Momoshima, N.; Okai, T.; Maeda, Y. (1999). “Tritium concentration in ocean”. Journal of Radioanalytical and Nuclear Chemistry. 239 (3): 523. doi:10.1007/BF02349062. S2CID 94876087. - ^ a b c d e f g
Fine, Rana A.; Reid, Joseph L.; Östlund, H. Göte (1981). “Circulation of Tritium in the Pacific Ocean”. Journal of Physical Oceanography. 11 (1): 3–14. Bibcode:1981JPO….11….3F. doi:10.1175/1520-0485(1981)011<0003:COTITP>2.0.CO;2. - ^ a b c d e f g h i j
Michel, Robert L. (2004). “Tritium hydrology of the Mississippi River basin”. Hydrological Processes. 18 (7): 1255. Bibcode:2004HyPr…18.1255M. doi:10.1002/hyp.1403. S2CID 130033605.
External links[edit]
Wikimedia Commons has media related to Tritium.
- “Annotated bibliography for tritium”. Alsos Digital Library. Washington and Lee University. Archived from the original on 14 May 2006. Retrieved 3 March 2022.
- “Nuclear Data Evaluation Lab”.
- Review of Risks from Tritium (Report). London, UK: Health Protection Agency. November 2007. RCE-4. Archived from the original on 17 May 2013. Retrieved 3 March 2022.
- Bergeron, Kenneth D. (17 September 2004). Tritium on Ice: The dangerous new alliance of nuclear weapons and nuclear power. ISBN 9780262261722.[full citation needed]
- “Tritium production and recovery in the United States in FY2011”. Fissile Materials. February 2010.
- “Tritium removal mass transfer coefficient”. ans.org.
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,655 -
гуманитарные
33,653 -
юридические
17,917 -
школьный раздел
611,944 -
разное
16,904
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Изотоп с 2 нейтронами
 |
|
| Общее | |
|---|---|
| Символ | H |
| Имена | тритий, H -3, водород-3, T |
| Протоны | 1 |
| Нейтроны | 2 |
| Данные о нуклидах | |
| Естественное содержание | 10 в водороде |
| Период полураспада | 12,32 года |
| Продукты распада | He |
| Масса изотопа | 3,0160492 u |
| Спин | ⁄2 |
| Избыточная энергия | 14,949,794 ± 0,001 кэВ |
| Энергия связи | 8,481,821 ± 0,004 кэВ |
| Режимы распада | |
| Режим распада | Энергия распада (МэВ ) |
| Бета-излучение | 0,018590 |
| Изотопы водорода. Полная таблица нуклидов |
Тритий (или ) или водород-3 (символ T или H ) является редким и радиоактивным изотоп. Ядро трития (иногда называемое тритоном ) содержит один протон и два нейтрона, тогда как ядро обычного изотопа водо род-1 (про тий) с одержит только один протон, ядро водород-2 (дейтерий) содержит один протон и один нейтрон.
Тритий, встречающийся в природе, на планете крайне редко. атмосфера имеет только следовые количества, образованные взаимодействием ее газов с космическими лучами. Его можно получить радиоактивного облучения металлического лития или литийсодержащих керамических шариков в ядерном реакторе.
Тритий используется в качестве радиоактивного индикатора, в радиолюминесцентном источника света для часов и инструментов, а также дейтерий в качестве ядерного реактора для ядерного синтеза с применением энергии и оружии.
Название этого изотопа происходит от греческого τρίτος (trítos), что означает «третий».
Содержание
- 1 История
- 2 Распад
- 3 Производство
- 3.1 Литий
- 3.2 Бор
- 3.3 Дейтерий
- 3.4 Деление
- 3.4.1 Фукусима-дайити
- 3.5 Гелий-3
- 3.6 Космические лучи
- 3.7 История производства
- 4 Свойства
- 5 Риски для здоровья
- 6 Загрязнение окружающей среды
- 6.1 Нормативные пределы
- 7 Использование
- 7.1 Самостоятельное электрическое освещение
- 7.2 Ядерное оружие
- 7.2.1 Нейтронный инициатор
- 7.2.2 Форсирование
- 7.2.3 Тритий во вторичных элементах водородной бомбы
- 7.3 Управляемый ядерный синтез
- 7.4 Аналитическая химия
- 7.5 Источник электроэнергии
- 8 Использование в качестве индикатора переходных процессов в океане
- 8.1 Северная Атлантика
- 8.2 Тихий и Индийский океаны
- 8.3 Система реки Миссисипи
- 9 См. Также
- 10 Ссылки
- 11 Внешние ссылки
История
Тритий был впервые в 1934 году Эрнестом Резерфордом, Марком Олифантом и Полом Хартеком после бомбардировки дейтерий с дейтронами (протон и нейтрон, составляющие ядро дейтерия). Дейтерий – еще один изотоп водорода. Однако в их эксперименте не удалось получить тритий, что позже было выполнено Луисом Альваресом и Робертом Корногом, которые также осознали радиоактивность трития. Уиллард Ф. Либби признал это тритий может быть использован для радиометрического датирования воды и вина.
распада
Хотя тритий имеет несколько различных экспериментально определенных значений своего периода полураспада, Национальный институт стандартов и технологий перечисляет 4500 ± 8 дней (12,32 ± 0,02 года). Он распадается на гелий-3 в результате бета-распада, как в этом ядерном уравнении:
-
. 1H. → . 2He. + . e. + . ν. e
, и при этом выделяется 18,6 кэВ энергии. Кинетическая энергия электрона изменяется в среднем на 5,7 кэВ, в то время как оставшаяся энергия уносится почти необнаруживаемым электронным антинейтрино. Бета-частицы из трития могут проникать только около 6,0 мм воздуха, и они неспособны проходить через мертвый внешний слой кожи человека. Необычно низкая энергия, выделяемая при бета-распаде трития, делает этот распад (наряду с распадом рения-187 ) подходящим для измерения абсолютной массы нейтрино в лаборатории (последний эксперимент – KATRIN ).
Низкая энергия излучения трития затрудняет обнаружение меченых соединений, за исключением использования жидкостного сцинтилляционного счета.
Производство
16>Литий
Тритий наиболее часто используется в ядерных реакторах путем нейтронной активации лития-6. Высвобождение и диффузия трития и гелия, образующихся при делении лития, может происходить внутри керамики, называемой керамикой-размножителем. Производство трития из лития-6 с помощью воспроизводящей керамике возможно с нейтронов любой энергии и представляет собой экзотермическую реакцию, дающую 4,8 МэВ. Для сравнения, синтез дейтерия с тритием высвобождает около 17,6 МэВ энергии. Для применения предлагаемых термоядерных реакторов, таких как ITER, галька, состоящая из литийсодержащей керамики, включая Li 2 TiO 3 и Li 4 SiO 4, разрабатываются для воспроизводства трития в гелиевом слое, также известном как бланкет-размножитель.
-
. 3Li. + . n. → . 2He. ( 2,05 МэВ ) + . 1T. ( 2,75 МэВ )
Высокие- Энергетические нейтроны могут также требовать тритий из лития-7 в эндотермической ( чистое потребление тепла) реакции, потребляя 2,466 МэВ. Это было обнаружено, когда ядерное испытание Замок Браво в 1954 г. дало неожиданно высокий выход.
-
. 3Li. + . n. → . 2He. + . 1T. + . n.
Бор
нейтроны высокой энергии, облучающие бор-10, также иногда дают тритий:
-
. 5B. + . n. → 2 . 2He. + . 1T.
Более частым результатом захвата нейтронов бором-10 является. Li., и одна альфа-частица.
Дейтерий
Тритий также производит в реакторах с тяжелым водным замедлителем. всякий раз, когда ядро дейтерия захватывает нейтрон. Эта реакция имеет довольно малое сечение, что делает тяжелую воду хорошим замедлителем нейтронов, и образует относительно мало трития. Даже в этом случае очистка трития от замедлителя может потребоваться через несколько лет, чтобы снизить его утечки в глобальном мире. «Установка по удалению трития» компании Ontario Power Generation перерабатывает до 2500 тонн (2500 длинных тонн; 2800 коротких тонн) тяжелой воды в год и выделяет около 2,5 кг (5,5 фунта) трития, делает его доступным для других целей.
Сечение сечение дейтерия для тепловых нейтронов составляет около 0,52 миллибарн, тогда как сечение кислорода-16 (. 8O.) составляет около 0,19 миллибарна, а для кислород-17 (. 8O.) составляет около 240 миллибарн.
Деление
Тритий является необычным продуктом ядерного деления урана-235, плутония-239 и уран- 233 с образованием около одного атома на 10 000 делений. Выделение или извлечение топлива необходимо при эксплуатации ядерных реакторов, особенно при переработке ядерного топлива и при хранении отработавшего ядерного топлива. Производство трития – это не цель, а побочный эффект. Он выбрасывается в атмосферу в небольших количествах некоторыми атомными электростанциями.
Фукусима-дайити
В июне 2016 года Целевая группа по тритиевой воде опубликовала отчет о состоянии трития в тритиевой воде на АЭС «Фукусима-дайити», в рамках рассмотрения вариантов окончательного захоронения хранящейся загрязненной охлаждающей воды. Это показало, что запасы трития на объекте в марте 2016 г. составили 760 ТБк (что эквивалентно 2,1 г трития или 14 мл тритиевой воды) в общей сложности на 860 000 м хранимой воды. В этом отчете также указывается на уровень трития в воде, извлекаемой из зданий и т. Д. Для хранения, что десять раз снизилось за рассматриваемые пять лет (2011–2016), с 3,3 МБк / л до 0,3 МБк / л (после корректировки для 5% годового распада трития).
Согласно возможному подходу к решению проблемы, наилучший подход к решению проблемы, тритий можно использовать теоретически, но практическую методику использования в промышленных масштабах не существует отчет. Соответственно контролируемый выброс в соответствии с общепринятым методом обработки трития ».
Гелий-3
Продукт распада трития гелий-3 имеет очень большое поперечное сечение (5330 барн) для реакции с тепловыми нейтронами, вытесняя протон, поэтому он быстро превращается обратно в тритий в ядерных реакторах.
Космические лучи
Тритий возникает естественным образом из-за космических лучей, взаимодействующих с атмосферными газами. В мире мощных факторов для естественного производства быстрые нейтроны (энергия более 4,0 МэВ ) взаимодействуют с атмосферным азотом :
-
. 7N. + . n. → . 6C. + . 1T.
Во всем производстве трития из природных источников – 148 петабеккерелей в год. Глобальный равновесный запас трития, созданный из природных источников, остается постоянным на уровне 2590 петабеккерелей. Это связано с фиксированной производственной и потерями пропорциональными запасами.
История производства
Согласно отчету Института энергетических и экологических исследований за 1996 г. 249>Министерство энергетики США, с 1955 по 1996 год в США было произведено всего 225 кг (496 фунтов) трития. Оно постоянно распадается на гелий-3, общее количество составляющих около 75 кг (165 фунтов) на момент отчета отчета.
Тритий для американского ядерного оружия производился в тяжеловодных реакторах на Саванна-Ривер-Сайн до их закрытия в 1988 году. С Договором о сокращении стратегических наступательных вооружений (СНВ) после окончания холодной войны физических запасов было достаточно для нового, меньшего количества ядерного оружия когда-то.
Производство трития было возобновлено с облучением стержней, других литий (заменой обычных управляющих стержней, защит бор, кадмий, или гафний ) на реакторах промышленной АЭС Уоттс-Бар с 2003 по 2005 гг. С последующим извлечением трития из стержней на новая установка по извлечению трития на участке Саванна-Ривер начинается в ноябре 2006 года. Утечка трития из стержней во время работы реактора ограничивает количество, которое может быть использовано в любом реакторе без превышения максимально допустимых уровней трития в теплоносителе.
Триантий имеет атомную массу 3,0160492 u. Двухатомный тритий (. T. 2или. H. 2) представляет собой газ при стандартной температуре и давлении. В сочетании с кислородом он образует жидкость, называемую тритированной водой (. T. 2. O. ).
Удельная активность трития составляет 9650 кюри на грамм (3,57 × 10 Бк / г).
Тритий занимает видное место в исследованиях ядерного синтеза из-за его благоприятного воздействия факторов сечения и большого количества энергии (17,6 МэВ), выделяющегося при его реакции дейтерием :
-
. 1T. + . 1D. → . 2He. + . n.
Все атомные ядра содержат как свои единственные электрические заряженные частицы. Поэтому отталкивают друг друга, потому что отталкиваются они одинаковые заряды. Однако если атомы имеют достаточно мощное давление (например, в ядре Солнца), то их случайные движения проходят через такое электрическое отталкивание (так называемая кулоновская сила ). сильное ядерное взаимодействие начало действовать, превращая их в более тяжелые атомы.
Ядро трития испытывает такую же электростатическую силу отталкивания, когда приближается к другому ядру атома, имеет тот же заряд, что и ядро обычного водорода. Однако нейтроны в ядре трития увеличивают сильную ядерную силу притяжения, когда подносятся достаточно близко к другому атомному ядру. В результате тритий легче сливается с другими легкими атомами, чем обычный водород.
То же самое, хотя и в меньшей степени, касается дейтерия. Вот почему коричневые карлики (так называемые несостоявшиеся звезды ) не могут использовать обычный водород, но они действительно объединяют небольшую часть ядер дейтерия.

Как и другие изотопы водорода, тритий трудно удержать. Резина, пластик и некоторые виды стали в некоторой степени проницаемы. Это вызвало опасения возбудителей в больших количествах, в частности, для термоядерных реакторов, он может вызвать возбудителей радиоактивному загрязнению, хотя его короткий период полураспада должен предотвратить долгое накопление в атмосфере.
Высокие уровни атмосферных ядерных испытаний, которые имели место до вступления в силу Договора о частичном запрещении испытаний, оказались неожиданно полезными для океанографов. Высокие уровни оксида трития, внесенного в верхние слои океанов, используются с тех пор для измерения скорости смешения верхних слоев океанов с их нижними уровнями.
Риск для здоровья
Тритий – изотоп водорода, который позволяет ему легко связываться с гидроксильными радикалами, образуя воду, содержащую тритий (H TO ), и атомы углерода. Он может представлять радиационную опасность при вдыхании, поскольку он представляет собой низкоэнергетический бета-излучатель, он не опасен снаружи (его бета-частицы не проникают через кожу).. через кожу. HTO имеет короткий биологический период полураспада в организме человека, снижает общие эффекты однократного проглатывания и предотвращает длительную биоаккумуляцию HTO из окружающей среды. Биологический период полураспада тритированной воды в организме человека, который является мерой круговорота воды в организме, меняется в зависимости от сезона. Исследования биологического периода полураспада свободного трития в воде у рабочих, занимающихся профессиональной радиацией, в прибрежном районе Карнатаки, Индия, показывают, что биологический период полураспада в зимний сезон вдвое больше, чем в летний сезон.
Загрязнение окружающей среды
Тритий просочился с 48 из 65 ядерных объектов США. В одном случае протекающая вода содержала 7,5 микрокюри (280 кБк) трития на литр, что в 375 больших лимитах EPA для питьевой воды.
Комиссия по ядерному регулированию США утверждает, что в нормальных условиях В 2003 году 56 реакторов с под давлением выпустили 40 600 кюри (1,50 ПБк) трития (максимум : 2080 Ки; минимум: 0,1 Ки; в среднем: 725 Ки) и 24 реактора с кипящей водой выбросил 665 кюри (24,6 ТБк) (максимум: 174 Ки; минимум: 0 Ки; средний : 27,7 Ки) в жидких сточных водах.
По данным США Агентства по охране окружающей среды, самоуправление Недавно было обнаружено, что световые указатели выхода, неправильно размещенные на муниципальных свалках, загрязняют водные пути.
Нормативные ограничения
Законные ограничения на содержание трития в питьевой различаются от воды страны к стране. Некоторые цифры приведены ниже:
| Страна | Ограничение по тритию (Бк / л) |
|---|---|
| Австралия | 76103 |
| Япония | 60000 |
| Финляндия | 100 |
| ВОЗ | 10000 |
| Швейцария | 10000 |
| Россия | 7700 |
| Онтарио (Канада) | 7000 |
| США | 740 |
Американский предел рассчитан для получения доз 4,0 миллибэр (или 40 микрозивертов в единиц СИ ) в год. Это примерно 1,3% от естественного радиационного фона (примерно 3000 мкЗв).
Использовать
Освещение с автономным питанием

Бета-частицы, испускаемые радиоактивным распадом в небольшом количестве трития, вызывают химические вещества, называемые люминофором, чтобы светиться. радиолюминесценция используются осветительные устройства с автономным питанием, называемыми беталайтами, которые используются для ночного огнестрельного оружия часов, знаки выхода, фонарей для карт, навигационных компасов (например, використов военные компасы) США M-1950 ), ножи и множество других устройств. В этой заявке тритий заменил радиолюминесцентную краску, содержащую радий. Последний рак может вызвать кости и был запрещен в большинстве стран на десятилетии. По состоянию на 2000 год коммерческий спрос на тритий составлял 400 граммов в год, а стоимость – приблизительно 30 000 долларов США за грамм.
Ядерное оружие
Тритий является важным компонентом ядерного оружия. Он используется для повышения эффективности и мощности бомб деления и стадий деления водородных бомб в процессе, известном как «форсирование », а также в внешние нейтронные инициаторы для такого оружия.
Нейтронный инициатор
Это устройство, встроенные в ядерное оружие, которое генерирует импульс нейтронов, когда бомба взрывается, чтобы инициировать реакцию деления в делящаяся сердцевина (яма) бомбы после того, как она сжата до критической массы взрывчатыми веществами. Приводимый в действие сверхбыстрым переключателем, таким как krytron, небольшой ускоритель частиц приводит в действие ионы трития и дейтерия до энергий выше 15 кэВ или так необходим синтез дейтерия и трития, и направляет их в металлическую мишень, где тритий и дейтерий адсорбируются в виде гидридов. Термоядерные нейтроны высокой энергии от образовавшегося термоядерного синтеза излучаются во всех направлениях. Некоторые из них поражают ядро плутонию или ядро первичной обмотки, я инициируя цепную ядерную реакцию. Количество произведенных нейтронов великого ядра ядерных ядер в яме позволяет достичь больших нейтронных уровней, которые достигаются огромного количества ядер цепной реакции, хотя все еще небольшое количество ядерных ядер в яме.
Форсирование
Перед детонацией несколько граммов тритий-дейтериевого газа вводятся в полую «яму » делящегося плутония или урана. На ранних этапах цепной реакции выделяется достаточно тепла и сжатия, чтобы начать синтез дейтерия и трития, затем и деление, и синтез стимулов синтезу, продолжительная нагрузка и сжатие, помогает делению с высокоэнергетическим (14,1 МэВ) ) нейтронов. Когда топливо для деления истощается, оно заставляет процесс прогрессировать быстрее и продолжаться дольше, чем это было бы без ускорения. Повышение выхода происходит в основном за счет увеличения деления. Энергия, выделяемая самим термоядерным синтезом, намного меньше, потому что количество термоядерного топлива намного меньше. Эффекты повышения включают:
- повышенный выход (для того же количества топлива деления, по сравнению с детонацией без повышения)
- возможность переменного выхода за счет изменения количества термоядерного топлива
- позволяя бомбе потреблять меньшее количество очень дорогого расщепляющегося материала – а также исключительный риск преддетонации близлежащими ядерными взрывами
- не столь строгие требования к установке имплозии, позволяющие меньшее и меньшее количество взрывчатых веществ, используемых использования
Тритий в боеголовке постоянно подвергается радиоактивному распаду, следовательно, становится недоступным для термоядерного синтеза. Кроме того, его продукт распада, гелий-3, поглощает нейтроны при воздействии нейтронов, испускаемых ядерным делением. Этот мощный компенсирует или обращает намеченный эффект трития, который должен генерировать много свободных нейтронов, если при распаде трития накопилось слишком много гелия-3. Поэтому необходимо периодически пополнять запасы трития в бомбардировщиках. Ориентировочно необходимое количество составляет 4 грамма на боеголовку. Для поддержания постоянного уровня трития в бомбу необходимо подавать около 0,20 грамма на боеголовку в год.
Один моль дейтерий-тритиевого газа будет содержать примерно 3,0 грамма трития и 2,0 грамма дейтерия. Для сравнения: 20 молей плутония в ядерной бомбе состоят из примерно 4,5 кг плутония-239.
трития во вторичных компонентах водородной бомбы
Временный тритий подвергается радиоактивному распаду, и его трудно удерживать. физически намного больший вторичный заряд изотопов водорода, необходимый в настоящем водородной энергии, использует твердый дейтерид лития в качестве источника дейтерия и трития, производя тритий in situ во время вторичного зажигания.
Во время детонации первичной бомбы деления в термоядерном оружии (стадия Теллера-Уллама ), свеча зажигания, цилиндр из U / Pu в центре Стадия (ов) синтез начинает делиться цепной реакцией из-за избыточных нейтронов, направляющих из первичной обмотки. Нейтроны, высвобождаются при делении свечи зажигания, расщепляют литий-6 на тритий и гелий-4, а литий-7 расщепляется на гелий-4, тритий и один нейтрон. Когда используются эти реакции, стадия синтеза сжимается фотонами от первичной обмотки и деления U- или U-оболочки, окружающей стадию синтеза. Следовательно, на стадии термоядерного синтеза при взрыве устройства образуется собственный тритий. В условиях сильной жары и давления взрыва часть трития подвергается слиянию с дейтерием, и эта реакция высвобождает еще больше нейтронов.
Для этого процесса требуется высокая температура для воспламенения, и он производит все менее и менее энергичных нейтронов (чистыми производными нейтроновами являются только дейтерий-тритиевый синтез и. 3Li. расщепление), дейтерид не используется в форсированных бомбах, а скорее используется в многоступенчатых водородных бомбах.
Управляемый ядерный синтез
Три важных топливных компонента для ядерного синтеза в конструкциях реакторов как с магнитным удержанием, так и с инерционным удержанием. Экспериментальный термоядерный реактор ИТЭР и National Ignition Facility (NIF) будут использовать дейтерий-тритиевое топливо. дейтерий-тритиевая реакция является благоприятной, поскольку она имеет наибольшее сечение синтеза (около 5,0 барнс ) и достигает этого размера сечения при самой низкой энергии (около 65 кэВ центр масс) потенциального термоядерного топлива.
Испытательная сборка тритиевых систем (TSTA) была помещением в Национальной лаборатории Лос-Аламоса, предназначенным для разработки и демонстрации технологий, необходимых для термоядерного синтеза дейтерия. переработка трития.
Аналитическая химия
Тритий иногда используется в качестве радиоактивной метки. Его преимущество состоит в том, что почти все органические химические вещества содержат водород, что позволяет легко найти место для размещения трития в исследуемой молекуле. Его недостаток состоит в том, что он дает сравнительно слабый сигнал.
Источник электроэнергии
Тритий можно использовать в бетавольтаическом устройстве для создания атомной батареи для выработки электричества.
Использование как транзитный индикатор в океане
Помимо хлорфторуглеродов, тритий может действовать как временный индикатор и может «очерчивать» биологические, химические и физические пути в мировом океане из-за его развивающегося распространения. Таким образом, тритий используется в качестве инструмента изучения циркуляции и вентиляции океана и для таких целей обычно измеряется в единицах трития, где 1 TU определяется как отношение 1 атома трития к 10 атомам водорода, равное 0,118 Бк / литр.. Как отмечалось ранее, испытания ядерного оружия, в первую очередь в высокоширотных регионах Северного полушария, в конце 1950-х – начале 1960-х годов привели к попаданию большого количества трития в атмосферу, особенно в стратосферу. До этих ядерных испытаний на поверхности Земли было всего от 3 до 4 килограммов трития; но за послетестовый период эти суммы выросли на 2–3 порядка. Сообщается, что примерно естественные фоновые уровни превышены на 1000 ТЕ в 1963 и 1964 годах, и используются в северном полушарии для оценки подземных вод и построения гидрогеологических имитационных моделей. Согласно последним научным источникам, уровни в атмосфере на пике испытаний оружия приближаются к 1000 ТЕ, уровни дождевой воды до выпадения осадков составляют от 5 до 10 ТЕ. В 1963 на острове Валентия в Ирландии выпало 2000 ТЕ осадков.
Северная Атлантика
Находясь в стратосфере (период после испытаний), тритий взаимодействовал и окислялся в молекулы воды и присутствовали в большей части быстро производимых дождевых осадков, что сделало тритий прогностическим инструментом для изучения эволюции и структуры гидрологического цикла, а также вентиляции и образования водных масс в Северной Атлантике. Данные о бомбах трития были использованы из программы Transient Tracers in the Ocean (TTO) для количественной оценки скорости пополнения и опрокидывания для глубоководных источников Северной Атлантики. Бомба-тритий также попадает в глубокий океан вокруг Антарктики. Большая часть содержащегося в бомбе тритиевой воды (HTO) в атмосфере может попадать в океан в результате следующих процессов: а) осаждения, б) парообмена и в) речного стока – эти процессы делают HTO отличным индикатором для масштабов времени до нескольких десятилетий. Используя данные этих процессов за 1981 год, изоповерхность 1 TU лежит на глубине от 500 до 1000 метров в субтропических регионах, а затем простирается на 1500–2000 метров к югу от Гольфстрима из-за к рециркуляции и вентиляции верхней части Атлантического океана. К северу изоповерхности расширяется и достигается период абиссальной равнины, что связано с вентиляцией океана в течение 10–20-летних временных масштабов.
Также очевидно. в Атлантическом океане – профиль трития около Бермудских островов между концом 1960-х и концом 1980-х годов. Максимум трития распространяется вниз от поверхности (1960-е годы) до 400 метров (1980-е годы), что соответствует скорости углубления примерно 18 метров в год. Также наблюдается увеличение содержания трития на глубине 1500 метров в конце 1970-х и 2500 метров в середине 1980-х годов, оба из которых соответствуют похолоданиям на глубокой воде и не имеют их глубоководной вентиляции.
Из исследования в 1991 г. профиль трития был использован в качестве инструмента для изучения образовавшейся воды глубоководной воды Северной Атлантики (НАДВ), что соответствует увеличению трития до 4 ТЕ. Этот НАДВ тенденцию перетекать через пороги, которые отделяют Норвежское море от Северной Атлантики, а затем течет на запад и к экватору глубокими пограничными течениями. Этот процесс был объяснен крупномасштабным распределением тритии в глубинах Северной Атлантики между 1981 и 1983 годами. Субполярный круговорот тенденцию опресняться (вентилироваться) за счет NADW и напрямую с высокими значениями трития (>1,5 TU).. Также очевидным было уменьшение тритии в глубоком западном пограничном потоке в 10 раз от Лабрадорского моря до тропиков, что указывает на потерю трития в глубинах океана из-за турбулентного перемешивания. и рециркуляция.
Тихий и океанский океаны
В исследовании 1998 года пробы трития в поверхностной морской воде и атмосферном водяном паре (на высоте 10 метров над поверхностью) были взяты в следующих местах: Море Сулу, Бенгальский залив, и Малаккский пролив. Результаты показали, что приблизительно трития в поверхностной морской воде была самой высокой в заливе Фримантл (0,40 Бк / литр), что можно отнести к смешанным стокам пресной воды с близлежащими землями из-за больших количеств, обнаруженных в прибрежных водах. Как правило, более низкие уровни проявляются между 35 и 45 градусами южной широты и около экватора. Результаты также показали, что (в целом) количество трития уменьшилось с годами (до 1997 г.) из-за физического распада бомбового трития в Индийском океане. Что касается водяного пара, то есть трития примерно на порядок выше, чем была в морской воде (от 0,46 до 1,15 Бк / литр). Следовательно, на тритий в водяном паре не имеет значения морской воды на поверхности; таким образом, был сделан вывод, что влияние воздействия трития в результате прямого следствия нисходящего движения природного трития из стратосферы в тропосферу (следовательно, влияние океана зависит от широты).
В северной части Тихого океана тритий (введенный как бомбовый тритий в северном полушарии) распространился в трех измеренийх. Были отмечены подповерхностные максимумы в средних и низких широтах, что свидетельствует о латеральном перемешивании (адвекции) и диффузионных процессах вдоль потенциальной плотности (изопикнали ) в верхних слоях океана. Некоторые из этих максимумов даже хорошо коррелируют с экстремумами солености. Чтобы получить океанской циркуляции, трития были нанесены на карту на трех поверхностях с постоянной плотностью (23,90, 26,02 и 26,81). Результаты показали, что тритий был хорошо перемешан (от 6 до 7 TU) на изопикнале 26,81 в субарктическом циклоническом круговороте, и, по-видимому, имел место медленный обмен трития (по сравнению с более мелкими изопикналами) между этим круговоротом и антициклоническим круговоротом в сторону юг; кроме того, тритий на поверхностях 23.90 и 26.02, по-видимому, медленнее обменивается между центральным круговоротом северной части Тихого океана и экваториальными регионами.
Глубокое проникновение бомбового трития можно разделить на 3 отдельных слоя. Слой 1 является самым мелким слоем и включает самый глубокий вентилируемый слой зимой; он получил примерно 28% от общего количества трития. Слой 2 находится ниже первого слоя, но выше изопикны 26,81 и больше является частью смешанного слоя. Его 2 источника – это диффузия вниз от смешанного слоя и боковые расширения, обнажающие слои (к полюсу); он содержит около 58% всего трития. Слой 3 представляет воды, которые могут получать тритий только посредством вертикальной диффузии; он содержит оставшиеся 14% всего трития.
Система реки Миссисипи
Воздействие ядерных осадков ощущалось в системе Штатах по всей системе реки Миссисипи. Концентрации трития можно использовать для понимания времени пребывания континентальных гидрологических систем (в отличие от обычных океанических гидрологических систем), которые включают поверхностные воды, такие как озера, ручьи и реки. Изучение этих систем также может предоставить обществам и муниципалитетам информацию для сельскохозяйственных целей и общего качества речной воды.
В исследовании 2004 г. несколько рек были приняты во внимание при изучении концентраций трития (начиная с 1960-х гг.) В бассейне реки Миссисипи: Река Огайо (наибольший приток в реку Миссисипи). поток), река Миссури и река Арканзас. Наибольшие концентрации трития были обнаружены в 1963 году во всех местах отбора проб по всем этим рекам и хорошо коррелируют с пиковыми концентрациями в осадках, вызванными испытаниями ядерной бомбы в 1962 году. В целом самые высокие концентрации наблюдались в реке Миссури (1963 год) и превышали 1200 TU, тогда как самые низкие концентрации были обнаружены в реке Арканзас (никогда не превышали 850 TU и менее 10 TU в середине 1980-х).
Используя данные по тритию в реках, можно идентифицировать несколько процессов: прямые сток и отток воды из подземных водоемов. Используя эти процессы, становится возможным моделировать реакцию речных бассейнов на переходный индикатор трития. Двумя наиболее распространенными моделями являются следующие:
- поршневой подход – сигнал трития появляется немедленно; и
- подход с хорошо перемешанным резервуаром – концентрация оттока зависит от времени пребывания воды в бассейне
К сожалению, обе модели не могут воспроизвести тритий в речных водах; Таким образом, была разработана двухчленная модель смешения, состоящая из двух компонентов: компонента быстрого потока (недавние осадки – «поршень») и компонента, при котором воды находятся в бассейне более 1 года («хорошо перемешанный резервуар»). Следовательно, концентрация трития в бассейне становится функцией времени пребывания в бассейне, стоков (радиоактивный распад) или источников трития, а также входной функции.
Для реки Огайо данные по тритию показали, что около 40% стока составляли осадки с временем пребывания менее 1 года (в бассейне Огайо), а более старые воды имели время пребывания около 10 лет. Таким образом, короткое время пребывания (менее 1 года) соответствовало компоненту «быстрого потока» модели двухчленного смешения. Что касается реки Миссури, результаты показали, что время пребывания составляло примерно 4 года с составляющей быстрого потока около 10% (эти результаты связаны с рядом дамб в районе реки Миссури).
Что касается массового потока трития через главный ствол реки Миссисипи в Мексиканский залив, данные показали, что примерно 780 граммов трития вытекло из реки в залив между 1961 и 1997 годами.. – в среднем 7,7 ПБк / год. И текущий потоки через реку Миссисипи составляют от 1 до 2 граммов в год, в отличие от потока до периода до бомбардировки примерно 0,4 грамма в год.
См.
- Hypertriton
- Luminox
Ссылки
ние ссылки
| Викискладе есть материалы, связанные с тритием . |
- Аннотированная библиография по тритию из цифровой библиотеки Alsos
- Банк данных по опасным веществам NLM – тритий, радиоактивные
- Лаборатория анализа ядерных данных
- Обзор рисков, связанных с тритием. Отчет независимой консультативной группы по ионизирующим излучениям. Агентство по охране здоровья. Ноябрь 2007 г. РЦЭ-4.
- Тритий на льду: Опасный новый ядерное оружие и ядерной энергии, Кеннет Д. Бержерон
- Производство и извлечение трития в США в 2011 финансовом году
- Коэффициент массопереноса при удалении трития



