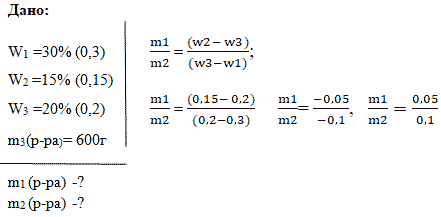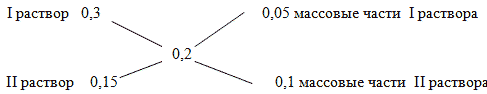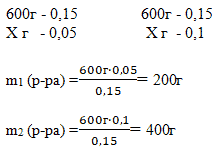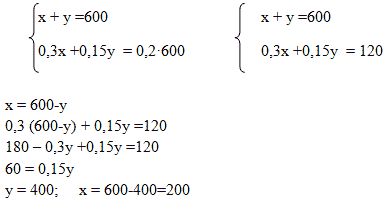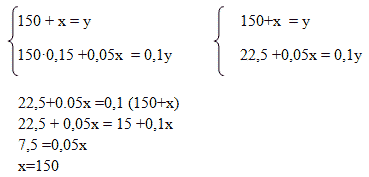Пример 5. Определите массу нитрата
натрия и воды, необходимые для приготовления
800 г раствора с ω(NaNO3) = 12%.
Решение:
Масса растворенной соли:
m(NaNO3) = ω(NaNO3)·m(р-ра) = 0,12·800 =
96 г.
m(р-ра) = m(NaNO3) + m(H2O)
Отсюда
m(H2O) = m(р-ра) – m(NaNO3) = 800 – 96
= 704 г.
Ответ: m(NaNO3) = 96 г, m(H2O) =
704 г.
Пример 6. Определите массу
кристаллогидрата CuSO4·5H2O и
воды, необходимые для приготовления
0,4 кг раствора с ω(CuSO4) = 8%.
Решение (см. пример 2):
ω(CuSO4) =
=
m(H2O) = m(р-ра) – m(CuSO4·5H2O)
m(CuSO4·5H2O) = n(CuSO4·5H2O)·M(CuSO4·5H2O)
n(CuSO4·5H2O)·= n(CuSO4) =
Находим
m(CuSO4) = ω(CuSO4)·m(р-ра) = 0,08·400
= 32 г.
n(CuSO4) =
=
0,2 моль.
Отсюда m(CuSO4·5H2O) = 0,2·250 = 50 г
Масса воды m(H2O) = 400 – 50 = 350 г
Ответ: m(CuSO4·5H2O) = 50 г,
m(H2O) = 350 г.
1. 2. Вычисление массы раствора определенной концентрации по заданной массе растворенного вещества или растворителя
Пример 7. Определить массу раствора
с массовой долей K2SO4 10%,
который можно приготовить из 200 г воды
и сульфата калия.
Решение:
m(р-ра) =
Из условия задачи m(K2SO4)
неизвестна, но известна масса воды, а
поскольку вода – один из компонентов
раствора, то:
ω(Н2О) = 100% – ω(K2SO4) =
100 – 10 = 90%
m(р-ра) =
=
= 222,2 г.
Ответ: можно приготовить 222,2 г
раствора.
Пример 8. При растворении в 400 г воды
некоторого количества CuSO4·5H2O
получен раствор с массовой долей CuSO4
5%. Рассчитать массу использованного
кристаллогидрата и массу полученного
раствора.
Решение (см. примеры 2, 6):
m(р-ра) =
=
В этом уравнении неизвестны m(р-ра) и
m(CuSO4), но
m(р-ра) = m(CuSO4·5H2O) + m(H2O)
= m(CuSO4·5H2O) + 400
Таким образом, неизвестны две величины:
m(р-ра) и m(CuSO4·5H2O).
m(CuSO4) = n(CuSO4)·m(CuSO4)
m(CuSO4·5H2O) = n(CuSO4·5H2O)·m(CuSO4·5H2O)
m(CuSO4)
= 160 г/моль, m(CuSO4·5H2O)
= 250 г/моль.
Подставим эти величины в исходную
формулу:
400 + n(CuSO4)·250 =
Решаем уравнение относительно n(CuSO4):
20 + 0,05·250· n(CuSO4) = n(CuSO4)·160,
n(CuSO4) =
= 0,136 моль.
Отсюда
m(CuSO4·5H2O) = 0,136·250 = 34 г,
m(р-ра) = 400 + 34 = 434 г.
Возможны и другие варианты решения этой
задачи:
ω(CuSO4) =
=
В этом уравнении тоже два неизвестных
– m(CuSO4) и m(CuSO4·5H2O), но
величину m(CuSO4) можно представить
в виде m(CuSO4·5H2O)·х.
Здесь х – массовая доля CuSO4 в
кристаллогидрате, она равна:
х =
=
= 0,64
С учетом исходных данных, теперь можно
записать:
0,05 =
Решаем уравнение относительно
m(CuSO4·5H2O):
20 + 0,05 m(CuSO4·5H2O) = 0,66·m(CuSO4·5H2O)
m(CuSO4·5H2O) = 34 г.
Находим m(р-ра) = 400 + 34 = 434 г.
Ответ: для приготовления раствора
используют 34 г CuSO4·5H2O, масса
полученного раствора 434 г.
1. 3. Разбавление и концентрирование растворов
При решении задач, связанных с разбавлением
и концентрированием растворов, следует
помнить, что масса растворенного
вещества остается неизменной, т.е.
m(Х) = const. Изменяется только масса
растворителя и, соответственно, масса
раствора.
Пример 9. К 50 мл раствора H2SO4
(ω1 = 48%, ρ = 1,38 г/мл) добавили 950 мл
воды. Определить массовую долю H2SO4
в полученном растворе.
Решение:
ω2(H2SO4) =
m2(р-ра) = m1(р-ра) + m(H2O)
m(H2O) = V(H2O)·ρ(H2O) = 950·1 =
950 г
m1(р-ра) = V1(р-ра)·ρ(р-ра) =
50·1,38 = 69 г
m1(H2SO4) = m1(р-ра)
ω1(H2SO4) = 69·0,48 = 33,12 г
ω2(H2SO4) =
= 0,032 или 3,2%
Ответ: ω(H2SO4) в новом
растворе 0,032 или 3,2%.
Пример 10. Какой объем воды необходимо
добавить к 100 мл раствора азотной кислоты
(ρ = 1,1 г/мл, ω1 = 20%), чтобы получить
раствор HNO3 с ω2 = 5%?
Решение:
V(H2O) =
m(H2O) = m2(р-ра) – m1(р-ра)
m1(р-ра) = V1(р-ра)·ρ(р-ра) =
100·1,1 = 110 г
Масса искомого раствора определяется
по формуле:
m2(р-ра) =
m(HNO3) = m1(р-ра)·ω1(р-ра)
= 110·0,2 = 22 г.
Отсюда масса нового раствора:
m2(р-ра) =
= 440 г
Масса и объем добавленной воды будут
равны
m(H2O) = 440 – 110 = 330 г V(H2O) =
=
330 мл
Ответ: следует добавить 330 мл воды.
Пример 11. Из 200 мл раствора сульфата
меди (ρ = 1,1 г/мл, ω1 = 8%)
выпарили
100 мл воды. Определить ω(CuSO4)
в полученном растворе.
Решение:
ω2(CuSO4) =
При концентрировании растворов масса
растворенного вещества, как и при
разбавлении, остается неизменной, т.е.
m(CuSO4) = const.
m(CuSO4) = m1(р-ра)·ω1(р-ра)
= 220·0,08 = 17,6 г
Масса раствора после упаривания
уменьшилась на 100 г:
m(H2O) = V(H2O)·ρ(H2O) = 100·1
= 100 г
Масса исходного раствора
m1(р-ра) = V1(р-ра)·ρ(р-ра) =
200·1,1 = 220 г
Следовательно, m2(р-ра) = 220 – 100 =
120 г
Отсюда ω2(CuSO4) =
= 0,147 или 14,7%
Ответ: ω(CuSO4) в полученном
растворе равна 0,147 или 14,7%.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Основные формулы для решения задач по химии
05-Авг-2012 | комментариев 450 | Лолита Окольнова
Все, все основные задачи по химии решаются с помощью
нескольких основных понятий и формул.
У всех веществ разная масса, плотность и объем. Кусочек металла одного элемента может весить во много раз больше, чем точно такого же размера кусочек другого металла.
Моль (количество моль)
обозначение: моль, международное: mol — единица измерения количества вещества. Соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов). Поэтому была введена универсальная величина — количество моль. Часто встречающаяся фраза в задачах — «было получено… моль вещества»
NA = 6,02 · 1023
NA — число Авогадро. Тоже «число по договоренности». Сколько атомов содержится в стержне кончика карандаша? Несколько миллионов. Оперировать такими величинами не удобно. Поэтому химики и физики всего мира договорились — обозначим 6,02 · 1023 частиц (атомов, молекул, ионов) как 1 моль вещества.
1 моль = 6,02 · 1023 частиц
Это была первая из основных формул для решения задач.
Молярная масса вещества
Молярная масса вещества — это масса одного моль вещества. Обозначается как M
Есть еще молекулярная масса — Mr
Находится по таблице Менделеева — это просто сумма атомных масс вещества.
Например, нам дана серная кислота — H2SO4. Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16.
Mr(H2SO4)=1•2+32+16•4=98 гмоль.
Вторая необходимая формула для решения задач —
формула массы вещества:
Т.е., чтобы найти массу вещества, необходимо знать количество моль (n), а молярную массу мы находим из Периодической системы.
Закон сохранения массы — масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.
Если мы знаем массу (массы) веществ, вступивших в реакцию, мы можем найти массу (массы) продуктов этой реакции. И наоборот.
Третья формула для решения задач по химии —
объем вещества:
Откуда взялось число 22.4? Из закона Авогадро:
в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Согласно закону Авогадро, 1 моль идеального газа при нормальных условиях (н.у.) имеет один и тот же объём Vm = 22,413 996(39) л
Т.е., если в задаче нам даны нормальные условия, то, зная количество моль (n), мы можем найти объем вещества.
Итак, основные формулы для решения задач по химии
Число Авогадро NA
6,02 · 1023 частиц
Количество вещества n (моль)
n=mM
n=V22.4 (лмоль)
Масса вещества m (г)
m=n•Mr
Объем вещества V(л)
V=n•22.4 (лмоль)
или вот еще удобная табличка:
Это формулы. Часто для решения задач нужно сначала написать уравнение реакции и (обязательно!) расставить коэффициенты — их соотношение определяет соотношение молей в процессе.
В ОГЭ и ЕГЭ по химии задач , в которых нужно было бы найти только объем массу кол-во моль нет — это обычно ЧАСТЬ решения задачи. Однако, чтобы легко решать более сложные задачи, нужно тренироваться на таких вот небольших упражнениях.
Находим количество вещества по массе
1 Какое количество вещества алюминия содержится в образце металла массой 10.8 г?2 Какое количество вещества содержится в оксиде серы (VI) массой 12 г?
3 Определите количество моль брома, содержащееся в массе 12.8 г.
Находим массу по количеству вещества:
4. Определите массу карбоната натрия количеством вещества 0.25 моль.Объем по количеству вещества:
5. Какой объем будет иметь азот при н.у., если его количество вещества 1.34 моль?6. Какой объем занимают при н.у. 2 моль любого газа?
Ответы:/p>
- 0.4 моль
- 0.15 моль
- 0.08 моль
- 26.5 г
- 30 л
- 44.8 л
Категории:
|
Обсуждение: “Основные формулы для решения задач по химии”
(Правила комментирования)
Инфоурок
›
Химия
›Другие методич. материалы›Алгоритм нахождения массы раствора
Алгоритм нахождения массы раствора
-
Настоящий материал опубликован пользователем Дударева Надежда Викторовна. Инфоурок является
информационным посредником и предоставляет пользователям возможность размещать на сайте
методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них
сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайтЕсли Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.Удалить материал
-
- На сайте: 8 лет
- Подписчики: 6
- Всего просмотров: 117744
-
Всего материалов:
65
При подготовке к экзамену в форме ЕГЭ задание 27 у обучающихся возникают вопросы по решению задач на смешивание и разбавление растворов. Эти задачи решают как на уроках математики, так и на уроках химии. Решение каждой задачи рассмотрено разными способами. Ученик может выбрать любой способ решения. Алгебраический способ решения задач на смешивание растворов учит детей строить цепочку логических рассуждений. «Конверт Пирсона» — это механический способ, который позволяет рационально проводить вычисления при решении задач на ЕГЭ.
Задачи на смешивание и разбавление растворов (по массе) можно разделить на следующие типы:
1. Задачи, связанные со смешиванием растворов, решаются по формуле:
W3,
где w3 — массовая доля растворенного вещества в конечном растворе;
m1(р.в.) — масса растворенного вещества в растворе с большей концентрацией;
m2(р.в.) — масса растворенного вещества в растворе с меньшей концентрацией;
m1(р-ра) — масса раствора с большей массовой долей растворенного вещества;
m2(р-ра) — масса раствора с меньшей массовой долей растворенного вещества.
2. Задачи на разбавление раствора, решаются по формуле:
3. Задачи на выпаривание раствора, решаются по формуле:
Для решение задач на смешивание растворов можно вывести формулу:
w3
w3 · ( m1 + m2 ) = w1·m1 + w2·m2
w3· m1+ w3· m2 = w1·m1 + w2·m2
m1· w3 – m1· w1= m2· w2- m2· w3
m1 (w3 – w1) = m2 (w2- w3)
=
,
где m1 и m2 массы исходных растворов,
w1 и w2 — соответствующие им массовые доли растворенного вещества;
m3 — масса конечного раствора;
w3 — массовая доля растворенного вещества в конечном растворе.
Таким образом: отношение массы первого раствора к массе второго равно отношению разности массовых долей второго раствора и смеси к разности массовых долей смеси и первого раствора.
Задача 1. Смешали 200 г раствора с массовой долей некоторого вещества 10 % и 150 г раствора с массовой долей этого вещества 32 %. Вычислите массовую долю растворённого вещества в полученном растворе.
350·w3 =68; w3 = 0,19 или 19%
Cпособ 2. Решим задачу, путем последовательных вычислений:
m1 (р. в.) =200г · 0,1= 20 г
m2 (р. в.) =150г · 0,32= 48 г
m3 (р. в.)= 20+48 = 68г; m3 (р-ра) = 200+150 =350 г
W = 0,19 или 19%
Ответ: массовая доля растворенного вещества в полученном растворе равна 19 %.
Способ 3. Алгебраический: пусть, х массовая доля полученного раствора;
Масса вещества в первом растворе: 200г · 0,1;
Масса вещества во втором растворе: 150г · 0,32
Масса вещества в полученном растворе: х · (200г+150г); составим уравнение:
200 · 0,1 +150 · 0,32= х · (200+150);
20 +48 = 200х +150х
68 = 350х
х=0,19 или 19%
Ответ: массовая доля растворенного вещества в полученном растворе равна 19 %
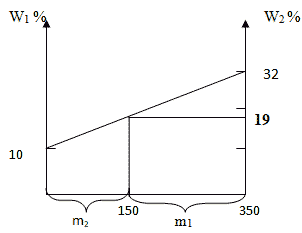
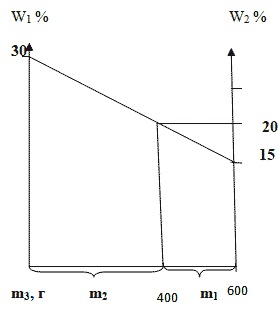
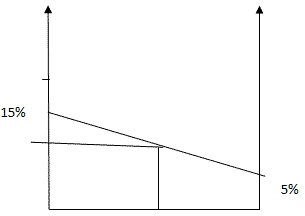
Способ 4. Графический метод
Отрезок прямой (основание графика) представляет собой массу смеси, а на осях ординат откладывают точки, соответствующие массовым долям растворенного вещества в исходных растворах. Соединив прямой точки на осях ординат, получают прямую, которая отображает функциональную зависимость массовой доли растворенного вещества в смеси от массы смешанных растворов в обратной пропорциональной зависимости. Данный способ является наглядным и дает приближенное решение.
Задача 2. Смешали 30 %-й раствор серной кислоты с 15%-ным раствором этой же кислоты и получили 600 г 20 %-го раствора.
Вычислите массу каждого раствора, необходимую для получения.
Способ 1. Решение с помощью «конверта Пирсона».
Составим диагональную схему правила смешивания для двух растворов.
Способ 2. Алгебраический
Пусть Х г – масса первого раствора; (600-х) г – масса второго раствора;
Масса вещества в первом растворе:0,3х;
Масса вещества во втором растворе: 0,15 · (600-х)
Масса вещества в полученном растворе: 0,2·600г; составим уравнение:
0,3х + 0,15 · (600-х) = 0,2·600
0,3х +90 – 0,15х = 120
0,15х = 30
Х=200 (масса первого раствора); 600-200=400 г – масса второго раствора
Способ 3. Алгебраический. Система уравнений
Пусть х г – масса первого раствора, у г – масса второго раствора. Система уравнений имеет вид:
Способ 4. Графический
Ответ: для приготовления 600 г 10 %-го раствора серной кислоты необходимо взять 200г 30 %-го раствора серной кислоты и 400г 20%-го раствора этой же кислоты.
Задача 3. К 150 г 15% раствора карбоната натрия добавили 5% раствор карбоната натрия. Какое количество 5% раствора соли надо добавить, чтобы получить 10% раствор соли?
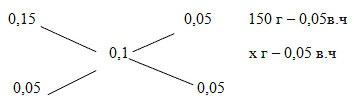
Способ 2. Решение с помощью «конверта Пирсона».
Составим диагональную схему правила смешивания для двух р-ов.
m2 (р-ра) == 150 г
Способ 3. Алгебраический
пусть Х г – масса второго раствора; (150+х) г – масса полученного раствора;
Масса вещества в первом растворе:0,15 · 150 = 22,5;
Масса вещества во втором растворе: 0,05х
Масса вещества в полученном растворе: 0,1 · (150+х); составим уравнение:
22,5 +0,05х = 0,1 · (150+х)
22,5 + 0,05х = 15 +0,1х
22,5-15= 0,1х-0,05х
7,5=0,05х
Х= 150 г
Способ 4. Алгебраический. Система уравнений
Пусть х г – масса второго раствора, у г – масса полученного раствора. Система уравнений имеет вид:
Графический способ
Ответ: чтобы получить 10% раствор соли надо добавить 150 г 5% раствора соли.
Задачи
1. Определите массовую долю кислоты в растворе, который получили смешиванием 200 г раствора с массовой долей кислоты 15% и 400г раствора с массовой долей кислоты 24% ?
2. Какие массы растворов хлороводорода с массовыми долями 12% и 28% нужно смешать для получения 480г раствора с массовой долей 22% ?
3. Сколько воды добавили к 300 граммам 30% раствора серной кислоты для получения 10% раствора серной кислоты?
4. К раствору массой 160г с неизвестной массовой долей соли добавили 80г воды. Вычислите массовую долю соли в исходном растворе, если после разбавления она равна 20%.
Литература
-
Ерыгин Д.П., Шишкин Е.А. Методика решения задач по химии׃ Учеб. пособие для студентов пед. ин-тов по биол. и хим. спец.- М.׃ Просвещение, 1989. – 176с.
формула для нахождения массы раствора
саша лайхо
Ученик
(97),
закрыт
9 лет назад
Лучший ответ
RaySa
Гуру
(3702)
10 лет назад
1. m(раствора) = масса раствор. вещества : массовая доля раствора (w)
Массовая доля измеряется в долях единицы или в процентах
2. m(раствора)= плотность * Vр-ра
Остальные ответы
Skif
Ученик
(167)
10 лет назад
Плотность раствора умножить на его объем!
Слепцов Марк Анатольевич
Мастер
(1283)
10 лет назад
Скиф сказал)
rex azimov
Ученик
(227)
5 лет назад
Массу раствора вещества: массовую долю
Похожие вопросы