Условие задачи:
На нагревание 5 кг воды от 303 К до кипения и на обращение в пар при температуре кипения некоторой её массы затрачено 2,81 МДж теплоты. Определить массу образовавшегося пара.
Задача №5.2.8 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(m=5) кг, (T=303) К, (Q=2,81) МДж, (Delta m-?)
Решение задачи:
Количество теплоты (Q) равно сумме количества теплоты (Q_1) и (Q_2):
[Q = {Q_1} + {Q_2}]
В этой формуле (Q_1) – количество теплоты, необходимое для нагревания воды массой (m) от температуры (T) до температуры кипения ((T_к=373) К), (Q_2) – количество теплоты, необходимое для превращения в пар воды массой (Delta m). Тогда:
[Q = cmleft( {{T_к} – T} right) + LDelta m]
Удельная теплоёмкость воды (c) равна 4200 Дж/(кг·°C), удельная теплота парообразования воды (L) равна 2,26 МДж/кг.
Выразим искомую массу пара (Delta m):
[Delta m = frac{{Q – cmleft( {{T_к} – T} right)}}{L}]
Произведём вычисления:
[Delta m = frac{{2,81 cdot {{10}^6} – 4200 cdot 5 cdot left( {373 – 303} right)}}{{2,26 cdot {{10}^6}}} = 0,593;кг]
Ответ: 0,593 кг.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
5.2.7 В теплоизолированном сосуде находится вода при 273 К. Выкачивая из сосуда воздух
5.2.9 Сколько было затрачено бензина в нагревателе с КПД 32%, если с его помощью 4 кг воды
5.2.10 При охлаждении 40 кг жидкого олова, взятого при температуре плавления 505 К
Расчеты, связанные с водяным паром
Задача 32.
В комнате объемом 45 м3 при температуре 25,0 °С относительная влажность воздуха равна 70% или 0,7. Определите массу водяного пара в комнате, если давление насыщенного водяного пара при этой температуре равно 3,17 кПа.
Решение:
Массу водяного пара в комнате можно определить из уравнения Менделеева-Клапейрона.
pV = (m/M . RT), где
р – давление насыщенного водяного пара; V – объем пара; М – молярная масса пара; R – газовая постоянная; Т – температура пара.
Температура, объем и молярная масса пара известны. Для определения давления водяного пара используем формулу относительной влажности.
ф = р/рн, из которой р = фрн.
При подставлении значения давления (фрн) в уравнение Клапейнона-Менделеева, то найдем массу пара m, получим:
фрнV = (m/M . RT)
откуда
m = фрнVM/RT = [0,7 . (3,17 . 103) .45 . (18 . 10-3)]/(8,31 . 298) = 0,738 кг = 738 г.
Ответ: масса водяного пара в комнате составляет 738 г.
Задача 33.
В комнате объемом 20,0 м3 температура воздуха равна 20,0 °С, а его относительная влажность составляет 20,0 %. Какое количество воды следует испарить, чтобы относительная влажность воздуха в комнате достигла 60,0 %? Известно, что при 20,0 °С давление насыщенного пара равно 2,33 кПа, молярная масса воды составляет 18,0 г/моль.
Решение:
Масса водяного пара в воздухе определяется следующими формулами:
при влажности ф1 = 20 %:
m1 = р1V, где
р1 — плотность водяного пара в воздухе при влажности 20 %; V — объем комнаты;
при влажности ф2 = 50%:
m2 = р2V, где
р2 — плотность водяного пара в воздухе при влажности 60 %.
Масса воды, которую следует испарить для повышения влажности воздуха, определяется разностью
∆m = m2 – m1, или, в явном виде, ∆m = р2V – р1V = (р2 – р1)V.
Плотность водяного пара при увеличении влажности увеличивается и определяется следующими формулами:
при влажности ф1 = 20%:
ф1 = p1M/RT, где
p1 — давление ненасыщенного водяного пара при влажности 20%; M — молярная масса водяного пара (воды); R — универсальная газовая постоянная, R = 8,31 Дж/(моль . К); T — температура воздуха, T = 273 + 20 = 293 K;
при влажности ф2 = 50%:
ф2 = p2M/RT, где
p2 — давление ненасыщенного водяного пара при влажности 60 %.
Формула для расчета искомой величины принимает вид:
∆m = p2M/RT – p1M/RT = (p2 – p1)VM/RT.
Давления ненасыщенного водяного пара найдем из формулы ф = (p . 100 %)/p0:
при влажности ф1 = 20%:
p1 = ф1p0/100%, где
р1 — первоначальная влажность воздуха, ф1 = 20%; p0 — давление насыщенного пара при температуре T = 293 К;
при влажности ф2 = 60%:
p2 = ф2p0/100%, где
ф2 — влажность воздуха после испарения некоторого количества воды, ф2 = 60 %.
Подстановка полученных выражений в формулу для ∆m дает:
∆m = (ф2 – ф1)/100% . p0VM/RT.
Вычислим:
∆m = (60,0% – 20,0%)/[100% . (2,33 . 103) . 20,0 . (18,0 . 10-3)/(8,31 / 293) = 137,8 . 10-3 кг = 137,8 г.
Ответ: Для указанного повышения влажности воздуха в комнате необходимо испарить 137,8 г воды.
Задача 34.
Определить состояние водяного пара, находящегося под давлением pп = 246660 Па, если его температура составляет:
а) t1 = 115 °С; б) t2 = 132 °С.
Решение:
Согласно табличным данным, давлению pп = 246,66 кПа соответствует температура насыщения tн = 127°С. Поскольку t1 < tн, то в первом случае пар является влажным. Для второго случая t2 > tн, т.е. пар является перегретым.
Таким образом, водяной пар при температуре 115 °С является влажным, а пар при температуре 132 °С – перегретый.
Ответ: а) влажный; б) перегретый.
Задача 35.
Водяной пар, имеющий температуру t = 150 °С, находится под давлением pп = 0,4 МПа. Определить степень его насыщенности.
Решение:
По табличным данным, применив метод интерполяции, определяем, что температуре t = 150°С соответствует давление насыщения pн = 475722 Па. Далее, использовав формулу:
ф = pп/pн, где
ф – степень насыщенности пара; pп – давление пара (плотность перегретого пара); pн – давление насыщенного пара воды (плотность насыщенного пара).
Находим степень насыщенности пара, получим:
ф = pп/pн = 400000/475722 = 0,84.
Ответ: ф = 0,84.
Как найти массу водяного пара?
В
комнате объемом 200 м3 при температуре 200 C относительная влажность воздуха равна 60 %. Определите массу
водяного пара в комнате, если давление насыщенного водяного пара при этой
температуре равно 2,33 кПа.
Решение.
Массу
водяного пара в комнате можно определить из уравнения Менделеева-Клапейрона.
Температура,
объем и молярная масса пара известны. Для определения давления водяного пара
используем формулу относительной влажности.
Если
подставить значение давления в уравнение Клапейнона-Менделеева, то найдем массу
пара m.
Ответ:
m = 2,1 кг.
Источник: Физика. Полный курс подготовки к ЦТ. Под общей редакцией проф. В.А. Яковенко.

Задание 25. В сосуде под поршнем находится пар массой 3 г под давлением 50 кПа и при температуре 100 °С. Не изменяя температуры, объём сосуда уменьшили в 6 раз. Найдите массу образовавшейся при этом воды.
Решение задачи
При температуре 100 °С давление насыщенного водяного пара равно атмосферному давлению 100 кПа, так как при 100 °С в открытом сосуде вода закипает и образуется насыщенный водяной пар. Следовательно, первоначально водяной пар насыщенный (p1 < 100 кПа), его можно считать идеальным газом.
Первоначально сжатие водяного пара приведёт к увеличению его давления до состояния насыщения: p2 = 100 кПа = 2p1. Для этого объём пара следует уменьшить в 2 раза.
Давление насыщенного водяного пара не зависит от его объёма, поэтому дальнейшее его сжатие приведёт к частичной конденсации водяных паров.
Таким образом, при уменьшении объёма насыщенного водяного пара в 3 раза произойдёт уменьшение массы водяного пара также в 3 раза.
Значит, m2 = m1 / 3 = 1 г останется пара, при этом масса образовавшейся воды равна:
mв = m1 — m2 = 2 г.
Ответ к задаче
Ответ: 2 г.
Просмотров: 4 406
(7.22) > 0) и его
где m – масса вещества; Qпл – количество теплоты, которое получает вещество при плавлении. В СИ удельную теплоту плавления измеряют в Дж/кг.
Первый закон термодинамики для процесса плавления можно записать в виде Qпл = ∆ Uпл или:
Qпл = mλ.
При плавлении вещество получает тепло (Qпл
внутренняя энергия увеличивается (∆ Uпл > 0). При кристаллизации жидкость отдает тепло (Qкр < 0) и его внутренняя энергия уменьшается (∆ Uкр < 0). Количество теплоты, которое выделяется при кристаллизации единицы массы вещества, называется удельной теплотой кристаллизации.
В процессе кристаллизации данная масса вещества отдает такое же количества теплоты, которое она получает при плавлении,
поэтому Qпл = |Qкр| и λпл = |λкр| = λ.
Парообразование и конденсация. Парообразование и конденсация – это процессы, при которых происходит изменение агрегатного состояния вещества.
Парообразование – это процесс перехода вещества из жидкого состояния в газообразное (пар).
Конденсация – это процесс перехода вещества из газообразного состояния в жидкое.
Парообразование может осуществляться в результате
испарения и кипения.
Испарение – это процесс перехода вещества из жидкого состояния в газообразное.
При испарении с поверхности жидкости или твёрдого тела вылетают частицы (молекулы, атомы), кинетическая энергия которых больше потенциальной энергии их связи между собой. Переход вещества из твердого состояния в газообразное называется сублимацией или возгонкой.
Рассмотрим процесс испарения жидкости. Испарение жидкости происходит со свободной поверхности жидкости при любой температуре.
Скорость испарения зависит от:
204
–площади свободной поверхности жидкости (чем больше эта площадь, тем выше скорость испарения);
–рода жидкости;
–температуры жидкости (чем выше температура, тем выше скорость испарения);
–давления над поверхностью жидкости, например, атмосферного (чем выше давление, тем медленнее идет процесс испарения);
–скорости движения газообразной фазы, например, воздуха над свободной поверхностью жидкости (чем больше скорость движения воздуха над поверхностью жидкости, тем быстрее идет процесс испарения).
При испарении температура жидкости понижается. Это объясняется тем, что в жидкости при любой температуре существуют молекулы с разными скоростями – « быстрые» и «медленные» молекулы. Из жидкости вылетают только «быстрые» молекулы, которые находятся вблизи её поверхности. Поэтому при испарении средняя кинетическая энергия молекул жидкости уменьшается, а это означает, что температура жидкости понижается. Испарение жидкости может происходить и более интенсивно – во всем объеме жидкости. Такой процесс называется
кипением.
Кипение – это процесс парообразования, который происходит во всем объеме жидкости при постоянной температуре.
Температура кипения – это температура, при которой кипит данная жидкость.
Рассмотрим, как происходит процесс кипения. При нагревании воды, растворенный в ней воздух выделяется на дне и стенках сосуда, образуя воздушные пузырьки. В эти пузырьки происходит испарение окружающей их жидкости, вследствие чего пузырьки наполняются паром, давление которого с повышением температуры увеличивается.
Если плотность пара внутри пузырька велика, то конденсация может происходить с той же скоростью, что и испарение, т.е. число
205
молекул, покидающих жидкость в единицу времени, равно числу молекул, возвращающихся в нее. В таком случае говорят, что пар находится в состоянии динамического равновесия со своей жидкостью.
Пар, который находится в состоянии динамического равновесия со своей жидкостью, называется насыщенным паром.
Для того, чтобы жидкость закипела, нужно довести ее температуру до такого значения, при котором давление насыщенного пара внутри содержащихся в жидкости пузырьков будет равно внешнему давлению. Условие кипения:
Жидкость закипает при такой температуре, при которой давление ее насыщенного пара равно внешнему давлению.
Таким образом, температура кипения жидкости не является фиксированной величиной. При понижении внешнего давления температура кипения уменьшается, а при повышении – увеличивается.
Например, при давлении 1 атмосфера (1 атм.= 1,013·105Па) вода закипает при 100 °C. При давлении 0,5 атмосфер вода закипит при 80 °C, а при давлении 2 атмосферы – при 120 °C.
Различные жидкости имеют разные температуры кипения при нормальном атмосферном давлении.
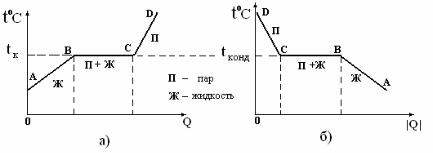
Рассмотрим изменение температуры жидкости при ее нагревании и кипении и при обратном переходе – охлаждении и конденсации (рис. 7.9а и рис. 7.9б).
Рис. 7.9. Графики процессов кипения а) и конденсации б)
При нагревании жидкости ее температура сначала повышается (рис. 7.9а, участок AB), внутренняя энергия жидкости возрастает в
206
результате увеличения средней кинетической энергии теплового движения ее молекул, а также в результате увеличения потенциальной энергии их взаимодействия. В точке В (рис. 7.9а) давление насыщенных паров внутри пузырьков становится равным внешнему давлению на свободную поверхность жидкости и начинается процесс кипения.
Количество теплоты, которое получает жидкость во время кипения, идет на увеличение ее внутренней энергии (рис. 7.9а, участок ВС). Внутренняя энергия пара, образовавшегося при температуре кипения, больше, чем внутренняя энергия жидкости при той же температуре. В процессе кипения кинетическая энергия теплового движения молекул не изменяется. Все количество получаемой теплоты идет на увеличение внутренней потенциальной энергии системы. Температура системы остается постоянной до окончания процесса парообразования (рис. 7.9, точка С). При дальнейшем нагревании пара (рис. 7.9а, участок СD) его температура опять повышается и, следовательно, увеличивается кинетическая энергия теплового движения молекул.
На рис. 7.9б показан график процесса конденсации пара. При конденсации пар отдает теплоту. Сначала температура пара понижается (рис. 7.9б, участок DС). Средняя кинетическая энергия молекул пара уменьшается, и пар начинает конденсироваться (рис. 7.9б, участок СВ). В процессе конденсации температура системы не изменяется, эта температура называется температурой конденсации
(tконд).
Температура конденсации – это температура, при которой конденсируется данный пар.
Когда весь пар сконденсируется, температура опять начинает понижаться (рис. 7.9б, участок ВА).
Из опыта известно, что температуры кипения и конденсации данного вещества равны (tкип = tконд).
Энергетической характеристикой процесса парообразования при кипении является удельная теплота парообразования (r).
Удельная теплота парообразования – это количество теплоты, необходимое для перехода единицы массы жидкости в пар при температуре кипения.
207
> 0). При
< 0) и его
|
r = |
Qкип |
, |
(7.23) |
|
|
m |
||||
|
где m – масса жидкости; |
Qкип |
– |
количество теплоты, которое |
получает жидкость при кипении. В СИ удельную теплоту парообразования измеряют в Дж/кг.
Первый закон термодинамики для процесса кипения можно
|
записать в виде ∆ Uкип = Qкип или: |
|
|
Qкип = r·m. |
(7.24) |
При кипении жидкость получает количество теплоты (Qкип > 0) и её внутренняя энергия увеличивается (∆ Uкип конденсации пар отдает количество теплоты (Qконд
внутренняя энергия уменьшается (∆ Uконд < 0). Количество теплоты, которое выделяется при конденсации единицы массы вещества,
называется удельной теплотой конденсации (rконд).
В процессе конденсации данная масса пара отдаёт такое же количества теплоты, которое получает жидкость при кипении,
поэтому Qконд = − Qкип и rконд = − rкип (| rконд | = | rкип | = r).
§ 7. ТЕРМОДИНАМИКА ПРОЦЕССА ГОРЕНИЯ
Человек использует энергию, которая выделяется при горении топлива. В качестве топлива могут служить разные вещества: дерево, каменный уголь, бензин, керосин, спирт, метан и другие. Из опыта известно, что при сгорании одинакового количества разных видов топлива выделяется разное количество теплоты. Это свойство веществ характеризуется удельной теплотой сгорания топлива (q).
Удельная теплота сгорания топлива – это количество теплоты, которое выделяется при полном сгорании единицы массы топлива.
|
q = |
Q |
, |
(7.25) |
|
m |
где m – масса топлива; Q – количество теплоты, которое выделяет топливо при сгорании. В СИ удельную теплоту сгорания топлива измеряют в Дж/кг.
208
Количество теплоты, которое выделяется при сгорании определенной массы топлива, определяют как:
Коэффициент полезного действия. Эффективность использования выделившейся при сгорании топлива теплоты (энергии) определяется коэффициентом полезного действия (КПД) нагревателя (η).
Коэффициент полезного действия нагревателя равен отношению полезно использованного количества теплоты к количеству теплоты, выделенному при полном сгорании топлива.
|
η = |
Qn |
, |
(7.27) |
||
|
m |
|||||
|
где η – |
коэффициент полезного действия (КПД) нагревателя; Qп – |
||||
|
полезно |
использованное количество |
теплоты; Q – |
количество |
теплоты, выделенное при полном сгорании топлива. Часто коэффициент полезного действия выражают в процентах, тогда:
|
η = |
Qn |
· 100 %. |
(7.29) |
|
Q |
|||
|
Коэффициент полезного действия всегда |
меньше единицы |
(η < 1) или меньше ста процентов (η < 100%), потому что всегда полезно использованное количество теплоты меньше количества теплоты, выделенного при полном сгорании топлива (Qп < Q).
ВОПРОСЫ ДЛЯ ПОВТОРЕНИЯ
1)Что такое нагревание?
2)Что такое охлаждение?
3)Увеличивается или уменьшается температура тела при нагревании?
4)Что такое плавление?
5)Что такое отвердевание?
6)Чем отличаются процессы плавления аморфных и кристаллических веществ?
7)Изменяется или нет температура в процессе плавления кристаллического вещества?
209
8)Какая температура называется температурой плавления?
9)Что такое удельная теплота плавления?
10)В каких единицах в СИ измеряют удельную теплоту плавления?
11)Что такое парообразование?
12)Что такое конденсация?
13)Что такое сублимация?
14)Что такое испарение?
15)От чего зависит скорость испарения?
16)Что такое кипение?
17) Какой пар называется насыщенным?
18)Какая температура называется температурой кипения?
19)От чего зависит температура кипения?
20)Что такое удельная теплота парообразования?
21)В каких единицах в СИ измеряют удельную теплоту парообразования?
22)Какие виды топлива вы знаете?
23)Что называется удельной теплотой сгорания топлива?
24)Как можно определить количество теплоты, которое выделяется при сгорании топлива?
25)Что называется коэффициентом полезного действия?
26)Почему коэффициент полезного действия не может быть больше 100%?
ЗАДАЧИ
Задача 1. В сосуде находится 10 кг воды при температуре 10оС. В сосуд положили кусок льда при температуре –50 оС. В результате теплообмена в сосуде образовалась ледяная масса с температурой –4 оС. Найти массу льда, который поместили в сосуд.
|
Дано: |
Решение: |
||||
|
m1 = 10 кг |
При охлаждении до 0 оС вода отдаёт |
||||
|
с1 = 4,2 кДж/(кг·K) |
количество теплоты Q1 = с1 m1(t1 – 0). Затем |
||||
|
с2 = 2,1 кДж/(кг·K) |
вода превращается в лёд и отдаёт |
||||
|
t1 = 10оС |
количество теплоты Q2 = rm1. Этот лёд |
||||
|
t2 = –50 оС |
охлаждается |
до температуры –4 оС |
и |
||
|
θ = –4 оС |
передаёт количество теплоты Q3 льду при |
||||
|
r = 0,33 МДж/кг |
температуре |
–50 оС, |
который находится |
в |
|
|
сосуде: Q3 = с2 m1(0 − |
θ). |
||||
|
m2 − ? |
|||||
|
210 |
Лёд при температуре –50 оС, который находился в сосуде, нагревается до температуры –4 оС и получает количество теплоты
Q4: Q4 = с2 m2(θ − t2).
Составим уравнение теплового баланса: Q1+Q2+Q3=Q4. Подставим полученные выражения для количеств теплоты и найдем
|
массу |
льда, |
который |
поместили |
в |
сосуд: |
|
m2= |
с1m1 (t1 − 0) + m1r + c2 m1 (0 − θ) |
= 39,4 кг. |
|||
|
c2 m2 (θ− t 2 ) |
О т в е т : m2 = 39,4 кг.
Задача 2. В нагревателе сгорает каждую минуту 3,2 г керосина. На нагреватель поставили чайник с 2 л воды при температуре 15оС и сняли через 40 минут. Какая масса воды выкипела за это время? КПД нагревателя 40%.
|
Дано: |
Решение: |
||||
|
T = 40 мин |
За время T в нагревателе сгорает |
||||
|
m = 3,2 г = 3.2 · 10−3 кг |
керосин |
и выделяется |
количество |
||
|
q = 46 · 106 Дж/кг |
теплоты: Q = qmT. Только 40% этого |
||||
|
m1 = 2 кг |
количества теплоты идет на нагревание |
||||
|
с = 4,2 · 103 Дж/(кг·K) |
и парообразование воды: Q1 = η qmT . |
||||
|
t = 15 оС |
Вода нагревается и часть воды (m2) |
||||
|
η = 40 % = 0,4 |
выкипает (переходит в пар). Для этого |
||||
|
r = 2,3 · 106 Дж/кг |
процесса |
необходимо |
количество |
||
|
tкип = 100 оС |
теплоты: Q2 = с m1(tкип – t) + rm2. |
||||
m2 – ?
При сгорании керосин отдает количество теплоты, а вода получает количество теплоты. Составим уравнение теплового баланса: Q1 = Q2. Подставим полученные выражения для количеств теплоты и найдем массу образовавшегося пара:
|
m2 |
η mqT − cm1(tкип |
− t) |
кг. |
|
= |
= 0,7 |
||
|
r |
О т в е т : m2 = 0,7 кг.
При решении задач используйте данные таблиц 1 и 2.
211
|
Таблица 1. |
||||||||||||
|
Тепловые свойства веществ |
||||||||||||
|
Твердые тела |
||||||||||||
|
Удельная |
Температура |
Удельная теплота |
||||||||||
|
Вещество |
теплоемкость, с, |
плавления, |
плавления λ, |
|||||||||
|
кДж/(кг · K) |
tпл, оС |
кДж/кг |
||||||||||
|
Алюминий |
0,89 |
660 |
380 |
|||||||||
|
Железо |
0,46 |
1400 |
82 |
|||||||||
|
Лед |
2,1 |
0 |
334 |
|||||||||
|
Медь |
0,38 |
1083 |
214 |
|||||||||
|
Олово |
0,23 |
232 |
59 |
|||||||||
|
Свинец |
0,13 |
327 |
23 |
|||||||||
|
Серебро |
0,23 |
961 |
87 |
|||||||||
|
Жидкости |
||||||||||||
|
Удельная |
Удельная теплота |
|||||||||||
|
теплоемкость, |
Температура |
|||||||||||
|
Вещество |
парообразования, |
|||||||||||
|
с, |
кипения, tкип, оС |
|||||||||||
|
кДж/(кг · K) |
r, МДж/кг |
|||||||||||
|
Вода |
4,19 |
100 |
2,3 |
|||||||||
|
Ртуть |
0,14 |
357 |
0,29 |
|||||||||
|
Спирт |
2,4 |
78 |
0,85 |
|||||||||
|
Газы |
||||||||||||
|
Удельная |
Температура |
|||||||||||
|
Вещество |
теплоемкость1, с, |
конденсации2, tконд, |
||||||||||
|
кДж/(кг · K) |
оС |
|||||||||||
|
Азот |
1,05 |
−196 |
||||||||||
|
Водород |
14,3 |
−253 |
||||||||||
|
Воздух |
1,01 |
− |
||||||||||
|
Гелий |
5,29 |
−269 |
||||||||||
|
Кислород |
0,913 |
−183 |
||||||||||
|
______________________ |
1При постоянном давлении.
2При нормальном давлении.
212
Задача 3. В сосуде находится 500 г льда при температуре 0 оС. В сосуд наливают 200 г воды при температуре 80 оС. Найти температуру, которая установится в сосуде в результате
теплообмена. Теплоёмкостью сосуда пренебречь.
О т в е т : θ = 0 оС
Задача 4. Для приготовления ванны объёмом 200 л смешали холодную воду при температуре 10 оС с горячей водой при температуре 60 оС. Какие объёмы холодной и горячей воды надо взять, чтобы в ванной установилась температура 40 оС?
О т в е т : V1 = 80 л; V2 = 120 л.
Задача 5. Для измерения температуры 66 г воды в нее поместили термометр с теплоёмкостью 1,9 Дж/K, который показал температуру 32,4 оС. До погружения в воду термометр показывал 17,8 оС. Найти начальную температуру воды.
О т в е т : t = 32,5 оС.
Задача 6: Железную деталь массой 0,5 кг при температуре 800оС помещают в 5 л воды при температуре 19оС. При этом образовалось некоторое количество пара, а вода нагрелась на 1оС. Найти массу образовавшегося пара.
О т в е т : m = 60,1 г.
Задача 7. Найти КПД нагревателя, если на нагревание чайника с 3 л воды от 10 оС до кипения было израсходовано 60 л газа.
Теплоёмкость чайника 100 Дж/K, теплота сгорания газа 36 МДж/м3.
О т в е т : η = 53 %.
Задача 8. В сосуд, содержащий 1, 5 кг воды при температуре 15 оС, впускают 200 г водяного пара при температуре 100 оС. Найти температуру в сосуде после конденсации всего пара.
О т в е т : t = 89 оС.
Задача 9. Колбу с 600 г воды при температуре 10 оС нагревают на спиртовке с КПД 35 %. Через какое время вода закипит? Сколько воды в одну секунду переходит в пар при кипении, если в одну минуту сгорает 2 г спирта? Теплоёмкость колбы 100 Дж/K.
О т в е т : T = 12 мин; m = 0,15 г.
Задача 10. В сосуде находится 2,8 л воды при температуре 20 оС. В сосуд помещают стальное тело массой 3 кг при температуре 460 оС. Вода нагревается до 60 оС, а ее часть переходит в пар. Найти массу воды, которая перешла в пар. Теплоёмкостью сосуда
пренебречь.
О т в е т : m = 33 г.
213
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
