7
Лекция 18. Элементы
физики атомного ядра
[1] гл. 32
План лекции
-
Атомное ядро.
Дефект массы, энергия связи ядра. -
Радиоактивное
излучение и его виды. Закон радиоактивного
распада. -
Законы сохранения
при радиоактивных распадах и ядерных
реакциях.
Состав атомного
ядра
Ядерная физика
– наука о строении, свойствах и превращениях
атомных ядер. В 1911 году Э. Резерфорд
установил в опытах по рассеянию -частиц
при их прохождении через вещество, что
нейтральный атом состоит из компактного
положительно заряженного ядра и
отрицательного электронного облака.
В. Гейзенберг и Д.Д. Иваненко (независимо)
высказали гипотезу о том, что ядро
состоит из протонов и нейтронов.
Атомное ядро
– центральная массивная часть атома,
состоящая из протонов и нейтронов,
которые получили общее название нуклонов.
В ядре сосредоточена почти вся масса
атома (более 99,95%). Размеры ядер порядка
10-13
– 10-12
см и зависят от числа нуклонов в ядре.
Плотность ядерного вещества как для
легких, так и для тяжелых ядер почти
одинакова и составляет около 1017
кг/м3,
т.е. 1 см3
ядерного вещества весил бы 100 млн. т.
Ядра имеют положительный электрический
заряд, равный абсолютной величине
суммарного заряда электронов в атоме.
Протон
(символ p) –
элементарная частица, ядро атома
водорода. Протон обладает положительным
зарядом, равным по величине заряду
электрона. Масса протона mp
= 1,6726 10-27
кг = 1836 me
, где me
– масса электрона.
В ядерной физике
принято выражать массы в атомных единицах
массы:
1 а.е.м. = 1,65976 10-27
кг.
Следовательно,
масса протона, выраженная в а.е.м., равна
mp
= 1,0075957 а.е.м.
Число протонов в
ядре называется зарядовым
числом
Z. Оно равно
атомному номеру данного элемента и,
следовательно, определяет место элемента
в периодической системе элементов
Менделеева.
Нейтрон
(символ n) –
элементарная частица, не обладающая
электрическим зарядом, масса которой
незначительно больше массы протона.
Масса нейтрона mn
= 1,675 10-27
кг = 1,008982 а.е.м. Число нейтронов в ядре
обозначается N.
Суммарное число
протонов и нейтронов в ядре (число
нуклонов) называется массовым
числом и
обозначается буквой А,
А = Z + N.
Для обозначения
ядер применяется символ
![]() ,
,
где Х – химический символ элемента.
Изотопы
– разновидности атомов одного и того же
химического элемента, атомные ядра
которых имеют одинаковое число протонов
(Z) и разное число нейтронов (N). Изотопами
называют также ядра таких атомов. Изотопы
занимают одно и то же место в периодической
системе элементов. В качестве примера
приведем изотопы водорода:
![]() .
.
Понятие о ядерных
силах.
Ядра атомов –
чрезвычайно прочные образования,
несмотря на то, что одноименно заряженные
протоны, находясь на очень малых
расстояниях в атомном ядре, должны с
огромной силой отталкиваться друг от
друга. Следовательно, внутри ядра
действуют чрезвычайно большие силы
притяжения между нуклонами, во много
раз превышающие электрические силы
отталкивания между протонами. Ядерные
силы представляют собой особый вид сил,
это самые сильные из всех известных
взаимодействий в природе.
Исследования
показали, что ядерные силы обладают
следующими свойствами:
-
ядерные силы
притяжения действуют между любыми
нуклонами, независимо от их зарядового
состояния; -
ядерные силы
притяжения являются короткодействующими:
они действуют между любыми двумя
нуклонами на расстоянии между центрами
частиц около 2·10-15
м и резко спадают при увеличении
расстояния (при расстояниях более
3·10-15
м они уже практически равны нулю); -
для ядерных сил
характерна насыщенность, т.е. каждый
нуклон может взаимодействовать только
с ближайшими к нему нуклонами ядра; -
ядерные силы не
являются центральными, т.е. они не
действуют вдоль линии, соединяющей
центры взаимодействующих нуклонов.
В настоящее время
природа ядерных сил изучена не до конца.
Установлено, что они являются так
называемыми обменными силами. Обменные
силы носят квантовый характер и не имеют
аналога в классической физике. Нуклоны
связываются между собой третьей частицей,
которой они постоянно обмениваются. В
1935 г. японский физик Х. Юкава показал,
что нуклоны обмениваются частицами,
масса которых примерно в 250 раз больше
массы электрона. Предсказанные частицы
были обнаружены в 1947 г. английским ученым
С. Пауэллом при изучении космических
лучей и впоследствии названы -мезонами
или пионами.
Взаимные превращения
нейтрона и протона подтверждаются
различными экспериментами.
Дефект масс
атомных ядер. Энергия связи атомного
ядра.
Нуклоны в атомном
ядре связаны между собой ядерными
силами, поэтому, чтобы разделить ядро
на составляющие его отдельные протоны
и нейтроны, необходимо затратить большую
энергию.
Минимальная
энергия, необходимая для разделения
ядра на составляющие его нуклоны,
называется энергией
связи ядра.
Такая же по величине энергия освобождается,
если свободные нейтроны и протоны
соединяются и образуют ядро.
Точные
масс-спектроскопические измерения масс
ядер показали, что масса покоя атомного
ядра меньше суммы масс покоя свободных
нейтронов и протонов, из которых
образовалось ядро. Разность между суммой
масс покоя свободных нуклонов, из которых
образовано ядро, и массой ядра называется
дефектом
массы:
![]()
Этой разности масс
m
соответствует энергия связи ядра Есв,
определяемая соотношением Эйнштейна:
![]()
или, подставив
выражение для m,
получим:
![]()
Энергию связи
обычно выражают в мегаэлектронвольтах
(МэВ). Определим энергию связи,
соответствующую одной атомной единице
массы (![]() ,
,
скорость света в вакууме
![]() ):
):
![]() .
.
Переведем полученную
величину в электронвольты:
![]()
В связи с этим на
практике удобнее пользоваться следующим
выражением для энергии связи:
![]() ,
,
где множитель m
выражен в атомных единицах массы.
Важной характеристикой
ядра служит удельная энергия связи
ядра, т.е. энергия связи, приходящаяся
на нуклон:
![]() .
.
Чем больше
![]() ,
,
тем сильнее связаны между собой нуклоны.

Рис.1
Зависимость
величины
от массового числа ядра показана на
рисунке 1. Как видно из графика, сильнее
всего связаны нуклоны в ядрах с массовыми
числами порядка 50-60 (Cr-Zn).
Энергия связи для этих ядер достигает
Соседние файлы в папке лекции
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Как найти массу ядра
Ядро атома ничтожно мало по сравнению с его общими размерами. Представить это поможет, например, такая образная модель атома водорода: если в самом центре футбольного поля положить небольшое яблоко, изображающее ядро, то орбита электрона прошла бы приблизительно по вратарской линии. Абсолютное большинство объема атома занимает пустота. И при этом столь же абсолютное большинство массы атома сосредоточено в его ядре. Достаточно сказать, что в том же атоме водорода его ядро тяжелее, чем электрон, в 1836 раз! А как же найти массу атомного ядра?

Инструкция
Упомянутый атом водорода имеет простейшее строение ядра из всех химических элементов. Оно состоит из единственной частицы, которая называется «протон». Все другие элементы имеют более сложное строение, и в состав их ядер, помимо протонов, входят так называемые «нейтроны». Запомните, что масса протона практически совпадает с массой нейтрона. Это очень важно.
За единицу измерения принята «атомная единица массы», или по-другому «Дальтон». Это масса 1/12 атома изотопа углерода. Она приблизительно равна 1,66*10^-24грамм. Именно из этой величины вам надо исходить, рассчитывая массу ядра того или иного химического элемента.
Легко можно понять, что поскольку масса электронов ничтожно мала по сравнению с массой протонов и нейтронов, ею в расчетах можно пренебречь. Разумеется, если не требуется очень высокая точность. Поэтому, решая задачу о нахождении массы ядра, можно рассматривать только «тяжелые» частицы – протоны и нейтроны. Их сумма дает вам «массовое число». Его необходимо умножить на величину атомной единицы массы и получить требуемый результат.
А как узнать массовое число? Тут на помощь придет знаменитая Таблица Менделеева. Каждому элементу в ней отведено строго определенное место, а заодно дана вся необходимая информация. В частности указана атомная масса элемента, которую можно принять за массовое число, поскольку общая масса электронов атома ничтожно мала по сравнению с массой протонов и нейтронов.
Рассмотрите конкретный пример. Вот хорошо знакомый металл – золото (Au). Его атомная масса – 196,97. Округлите ее до 197 и умножьте на величину атомной единицы массы. Получите:(197*1,66)*10^-24 = 327,02*10^-24 = 3,2*10^-22 грамм. Вот такова приблизительная масса ядра атома золота.
Видео по теме
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Основными характеристиками атомных ядер являются электрический заряд, масса, спин, энергия связи и так далее.
Заряд ядра
Ядро каждого из атомов обладает положительным зарядом. В качестве носителя положительного заряда выступает протон. По той причине, что заряд протона численно эквивалентен заряду электрона e, можно записать, что заряд ядра элемента равен +Ze (Z выражает собой целое число, которое указывает на порядковый номер химического элемента в периодической системе химических элементов Д. И. Менделеева). Значение Z также характеризует число протонов, входящих в состав ядра и количество электронов в атоме. Именно из-за этого его определяют как атомный номер ядра. Электрический заряд представляет собой одну из основных характеристик атомного ядра, от которой зависят оптические, химические и иные свойства атомов.
Масса ядра
Существует также другая значимая характеристика ядра, а именно масса. Массу атомов и ядер принято выражать в атомных единицах массы (а.е.м.), в качестве атомной единицы массы выступает 112 массы нуклида углерода C612:
где NA=6,022·1023 моль-1 обозначает число Авогадро.
Кроме того, есть другой способ выражения атомной массы: исходя из соотношения Эйнштейна E=mc2, ее выражают в единицах энергии. По той причине, что масса протона mp=1.00728 а.е.м.=938,28 МэВ, масса нейтрона mn=1.00866а.е.м.=939,57МэВ, а масса электрона me=5,49⋅10-4 а.е.м.=0,511МэВ,
Из приведенных выше значений видно, что масса электрона несущественно мала, если сравнивать ее с массой ядра, поэтому масса ядра практически эквивалентна массе всего атома и отлична от целых чисел.
Масса ядра, которая выражается в а.е.м. и округляется до целого числа носит название массового числа и обозначается с помощью буквы A. Она характеризует количество нуклонов, находящихся в составе ядра.
Количество нейтронов в ядре эквивалентно N=A−Z. В качестве обозначения ядер используют символ XZA, в котором X определяется как химический символ этого элемента.
Атомные ядра, обладающие одинаковым числом протонов, однако при этом отличающимися друг от друга массовыми числами, носят название изотопов.
В некоторых элементах количество стабильных и нестабильных изотопов достигает десятков, в качестве примера, уран обладает 14 изотопами: от U92227 до U92240. Большая часть химических элементов, которые существуют в природе, являются смесью нескольких изотопов. Как раз наличие изотопов объясняет следующее явление: некоторые природные элементы обладают массой, которая является отличной от целых чисел. В качестве примера рассмотрим природный хлор, который состоит из 75% C1735l и 24% C1737l, а его атомная масса эквивалентна 35,5 а.е.м. В большей части атомов, исключая водород, изотопы обладают практически равными физическими и химическими свойствами. Однако, за своими, исключительно ядерными свойствами, изотопы значительно отличаются друг от друга. Какие-то из них могут представлять собой стабильные изотопы, а другие – радиоактивные.
Ядра с эквивалентными массовыми числами, но отличающимися значениями Z носят название изобар, в качестве примера, A1840r, C2040a.
Ядра с одинаковым числом нейтронов определяют как изотоны.
Среди легких ядер встречаются и так называемые «зеркальные» пары ядер. Это такие пары ядер, в которых числа Z и A−Z меняются местами. В качестве примера подобных ядер можно привести C613 и N713 или H13 и H23e.
Размер атомного ядра
Принимая форму атомного ядра приблизительно сферической, мы имеем возможность ввести понятие его радиуса R. Обратим внимание на то, что в некоторых ядрах есть небольшое отклонение от симметрии в распределении электрического заряда. Более того, атомные ядра представляют собой не статические, а динамические системы, и понятие радиуса ядра нельзя представлять как радиус шара. Именно из-за этого факта, в качестве размеров атомного ядра нужно принимать ту область, в которой проявляются ядерные силы. В процессе создания количественной теории рассеивания α-частиц Э. Резерфорд исходил из тех предположений, что атомное ядро и α – частица взаимодействуют по закону Кулона, Другими словами из того, что электрическое поле вокруг ядра обладает сферической симметрией.
Это работает в отношении α – частиц, обладающих достаточно малым значением энергии E. При этом частица не имеет возможности преодолеть кулоновский потенциальный барьер и в последствии не достигает области, в которой наблюдается действие ядерных сил. Одновременно с повышением энергии частицы до некоторого граничного значения Eгр, α-частица достигает данной границы. В таком случае в рассеянии α-частиц возникает некоторое отклонение от формулы Резерфорда.
Опытным путем было определено, что радиус R ядра является зависимым от числа нуклонов, которые входят в состав ядра.
Размеры ядер определяют экспериментальным путем по рассеянию протонов, быстрых нейтронов или же электронов высоких энергий. Существует также целый список иных косвенных способов получения значений размеров ядер. Они основываются:
- на связи времени жизни α – радиоактивных ядер с энергией выпущенных ими α – частиц;
- на оптических свойствах, носящих название мезоатомов, в которых один из электронов временно захвачен мюоном;
- на сравнении энергий связи парных зеркальных атомов.
Данные способы подтверждают эмпирическую зависимость R=R0A1/3, а также благодаря таким измерениям определено значение постоянной R0=1,2-1,5·10-15 м. Обратим свое внимание также на тот факт, что за единицу расстояний в атомной физике и физике элементарных частиц принимают единицу измерения «ферми», которая равняется 10-15 м 1 ф=10-15 м. Радиусы атомных ядер определяются их массовым числом и находятся в промежутке от 2·10-15 до 10-14 м. Если из формулы R=R0A1/3 выразить R0 и записать его в следующем виде 4πR33A=const, то можно заметить, что на каждый нуклон приходится примерно одинаковый объем. Из данного факта можно сделать вывод о том, что плотность ядерного вещества для всех ядер так же приблизительно одинакова. Как можно заметить, плотность ядерного вещества довольно велика. Этот факт основывается на действие ядерных сил.
Энергия связи. Дефект масс ядер
Величину ∆m, что определяет разницу масс между массой нуклонов, которые формируют ядро, и массой ядра, называют дефектом массы ядра.
Важные сведения о свойствах ядра могут быть получены даже при отсутствии знаний о подробностях взаимодействия между нуклонами ядра, на основании закона сохранения энергии и закона пропорциональности массы и энергии. Поскольку в результате каждого изменения массы ∆m происходит соответствующее изменение энергии ∆E(∆E=∆mc2), то при образовании ядра выделяется некоторое количество энергии. Исходя из закона сохранения энергии можно сделать вывод о том, что ровно такое же количество энергии необходимо для того, чтобы разделить ядро на составляющие его элементы, другими словами отдалить нуклоны друг от друга на такие расстояния, при которых взаимодействия между ними не происходит. Данную энергию определяют как энергию связи ядра.
Заметим, что данная формула довольно неудобная в применении, так как в таблицах приводиться не массы ядер, а массы, которые относятся к массам нейтральных атомов. По этой причине ради удобства вычислений формулу преобразуют таким образом, чтобы в нее входили не массы атомов, а массы ядер. Для достижения этой цели в правой части формулы добавим и отнимем массу Z электронов (me). В таком случае Eсв=Zmp+me+A-Zmn-mя+Zmec2=ZmH11+A-Zmn-mac2 — масса атома водорода, ma — масса атома.
В ядерной физике энергию зачастую выражают в мегаэлектрон-вольтах (МэВ). Если речь идет о практическом применении ядерной энергии, то ее измеряют в джоулях. В случае сравнения энергии двух ядер используют массовую единицу энергии — соотношение между массой и энергией (E=mc2). Массовая единица энергии (le) равняется энергии, что соответствует массе в одну а.е.м. Она равняется 931,502 МэВ.
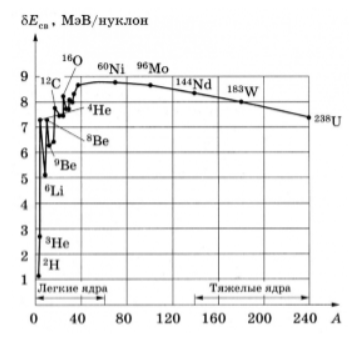
Рисунок 1
Кроме энергии, важное значение имеет удельная энергия связи ядра — энергия связи, которая припадает на один нуклон: ω=Ecв/A. Эта величина меняется сравнительно медленно по сравнению со сменой массового числа A, имея почти постоянную величину 8.6 МэВ в средней части периодической системы и уменьшается до ее краев.
Дефект массы
Энергия связи в МэВ: Eсв=∆m·931,502=0,030359·931,502=28,3 МэВ;
Удельная энергия связи: ω=EсвA=28,3 МэВ4≈7.1 МэВ.
| Ядерная физика |
|---|
 |
| Атомное ядро · Радиоактивный распад · Ядерная реакция · Термоядерная реакция |
|
Основные термины Атомное ядро · Изотопы · Изобары · Капельная модель ядра · Период полураспада · Массовое число · Составное ядро · Цепная ядерная реакция · Ядерное эффективное сечение |
|
Распад ядер Закон радиоактивного распада · Альфа-распад · Бета-распад · Кластерный распад |
|
Сложный распад Электронный захват · Двойной бета-распад · Двойной электронный захват · Внутренняя конверсия · Изомерный переход |
|
Излучения Ионизирующее излучение · Нейтронный распад · Позитронный распад · Протонный распад · Гамма излучение · Фоторасщепление |
|
Захваты Электронный захват · Нейтронный захват (r-процесс · s-процесс) · Протонный захват (p-процесс · rp-процесс) · Нейтронизация |
|
Деление ядра Спонтанное деление |
|
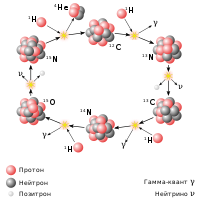
Нуклеосинтез Первичный нуклеосинтез · Протон-протонный цикл · CNO-цикл · Тройная гелиевая реакция · Гелиевая вспышка · Ядерное горение углерода · Углеродная детонация · Ядерное горение кислорода · Ядерное горение неона · Ядерное горение кремния · Реакции скалывания |
| См. также: Портал:Физика |
А́томное ядро́ — центральная часть атома, в которой сосредоточена основная его масса (более 99,9 %). Ядро заряжено положительно, заряд ядра определяет химический элемент, к которому относят атом. Размеры ядер различных атомов составляют несколько фемтометров, что более чем в 10 тысяч раз меньше размеров самого атома. Атомные ядра изучает ядерная физика.
Атомное ядро состоит из нуклонов — положительно заряженных протонов и нейтральных нейтронов, которые связаны между собой при помощи сильного взаимодействия. Протон и нейтрон обладают собственным моментом количества движения (спином), равным 
Атомное ядро, рассматриваемое как класс частиц с определённым числом протонов и нейтронов, принято называть нуклидом.
В некоторых редких случаях могут образовываться короткоживущие экзотические атомы, у которых вместо нуклона ядром служат иные частицы.
Количество протонов в ядре называется его зарядовым числом 



Как и любая квантовая система, ядра могут находиться в метастабильном возбуждённом состоянии, причём в отдельных случаях время жизни такого состояния исчисляется годами. Такие возбуждённые состояния ядер называются ядерными изомерами[1][2][3].
История[править | править код]
В 1911 году Резерфорд в своём докладе «Рассеяние α- и β-лучей и строение атома» в философском обществе Манчестера заявил[4]:
Рассеяние заряженных частиц может быть объяснено, если предположить такой атом, который состоит из центрального электрического заряда, сосредоточенного в точке и окружённого однородным сферическим распределением противоположного электричества равной величины. При таком устройстве атома α- и β-частицы, когда они проходят на близком расстоянии от центра атома, испытывают большие отклонения, хотя вероятность такого отклонения мала.
Таким образом Резерфорд открыл атомное ядро, с этого момента и ведёт начало ядерная физика, изучающая строение и свойства атомных ядер.
После обнаружения стабильных изотопов элементов, ядру самого лёгкого атома была отведена роль структурной частицы всех ядер. С 1920 года ядро атома водорода имеет официальный термин — протон. В 1921 году Лиза Мейтнер предложила[5] первую, протон-электронную, модель строения атомного ядра, согласно которой оно состоит из протонов, электронов и альфа-частиц[6]:96. Однако в 1929 году произошла «азотная катастрофа» — В. Гайтлер и Г. Герцберг установили[7], что ядро атома азота подчиняется статистике Бозе — Эйнштейна, а не статистике Ферми — Дирака, как предсказывала протон-электронная модель[8][9]:374. Таким образом, эта модель вступила в противоречие с экспериментальными результатами измерений спинов и магнитных моментов ядер[10]. В 1932 году Джеймсом Чедвиком была открыта новая электрически нейтральная частица, названная нейтроном. В том же году Иваненко[11] и, ссылаясь на работу первого[12], Гейзенберг выдвинули гипотезу о протон-нейтронной структуре ядра. В дальнейшем, с развитием ядерной физики и её приложений, эта гипотеза была полностью подтверждена[13].
Теории строения атомного ядра[править | править код]
В процессе развития физики выдвигались различные гипотезы строения атомного ядра; тем не менее, каждая из них способна описать лишь ограниченную совокупность ядерных свойств. Некоторые модели могут взаимоисключать друг друга.
Наиболее известными являются следующие:
- Капельная модель ядра — предложена в 1936 году Нильсом Бором.
- Оболочечная модель ядра — предложена в 30-х годах XX века.
- Обобщённая модель Бора — Моттельсона
- Кластерная модель ядра
- Модель нуклонных ассоциаций
- Оптическая модель ядра
- Сверхтекучая модель ядра
- Статистическая модель ядра
Ядерно-физические характеристики[править | править код]
Зарядовым числом 


Заряд[править | править код]
Число протонов в ядре 
Впервые заряды атомных ядер определил Генри Мозли в 1913 году. Свои экспериментальные наблюдения учёный интерпретировал зависимостью длины волны рентгеновского излучения от некоторой константы 
, где


Из чего Мозли сделал вывод, что найденная в его опытах константа атома, определяющая длину волны характеристического рентгеновского излучения и совпадающая с порядковым номером элемента, может быть только зарядом атомного ядра, что стало известно под названием закон Мозли[2].
Масса[править | править код]
Из-за разницы в числе нейтронов 

Кроме того, в ядерной физике часто используется энергетический эквивалент массы. Согласно соотношению Эйнштейна, каждому значению массы 
, где
— скорость света в вакууме.
Соотношение между а. е. м. и её энергетическим эквивалентом в джоулях:
,
а так как 1 электронвольт = 1,602176⋅10−19 Дж, то энергетический эквивалент а. е. м. в МэВ равен[1][3]:
.
Радиус[править | править код]
Анализ распада тяжёлых ядер уточнил оценку Резерфорда[сн 3] и связал радиус ядра 

, где
— константа.
Так как радиус ядра не является чисто геометрической характеристикой и связан прежде всего с радиусом действия ядерных сил, то значение 



Моменты ядра[править | править код]
Как и составляющие его нуклоны, ядро имеет собственные моменты.
Спин[править | править код]
Поскольку нуклоны обладают собственным механическим моментом, или спином, равным 

Несмотря на то, что число нуклонов в ядре может быть очень велико, спины ядер обычно невелики и составляют не более нескольких 
Магнитный момент[править | править код]
Измерения спинов стали возможными благодаря наличию непосредственно связанных с ними магнитных моментов. Они измеряются в магнетонах и у различных ядер равны от −2 до +5 ядерных магнетонов. Из-за относительно большой массы нуклонов магнитные моменты ядер очень малы по сравнению с магнитными моментами электронов, поэтому их измерение гораздо сложнее. Как и спины, магнитные моменты измеряются спектроскопическими методами, наиболее точным является метод ядерного магнитного резонанса.
Магнитный момент чётно-чётных пар, как и спин, равен нулю. Магнитные моменты ядер с непарными нуклонами образуются собственными моментами этих нуклонов и моментом, связанным с орбитальным движением непарного протона[10].
Электрический квадрупольный момент[править | править код]
Атомные ядра, спин которых больше или равен единице, имеют отличные от нуля квадрупольные моменты, что говорит об их не точно сферической форме. Квадрупольный момент имеет знак плюс, если ядро вытянуто вдоль оси спина (веретенообразное тело), и знак минус, если ядро растянуто в плоскости, перпендикулярной оси спина (чечевицеобразное тело). Известны ядра с положительными и отрицательными квадрупольными моментами. Отсутствие сферической симметрии у электрического поля, создаваемого ядром с ненулевым квадрупольным моментом, приводит к образованию дополнительных энергетических уровней атомных электронов и появлению в спектрах атомов линий сверхтонкой структуры, расстояния между которыми зависят от квадрупольного момента[2].
Энергия связи[править | править код]
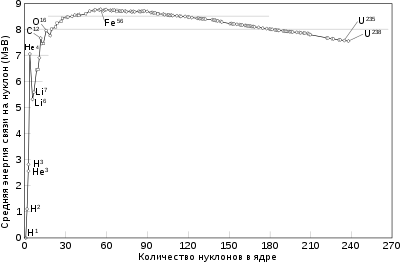
Большая энергия связи нуклонов, входящих в ядро, говорит о существовании ядерных сил, поскольку известные гравитационные силы слишком малы, чтобы преодолеть взаимное электростатическое отталкивание протонов в ядре. Связь нуклонов осуществляется чрезвычайно короткодействующими силами, которые возникают вследствие непрерывного обмена частицами, называемыми пи-мезонами, между нуклонами в ядре.
Экспериментально было обнаружено, что для всех стабильных ядер масса ядра меньше суммы масс составляющих его нуклонов, взятых по отдельности. Эта разница называется дефектом массы или избытком массы и определяется соотношением:
,
где 


Согласно принципу эквивалентности массы и энергии дефект массы представляет собой массу, эквивалентную работе, затраченной ядерными силами, чтобы собрать все нуклоны вместе при образовании ядра. Эта величина равна изменению потенциальной энергии нуклонов в результате их объединения в ядро.
Энергия, эквивалентная дефекту массы, называется энергией связи ядра и равна:
,
где 
Другим важным параметром ядра является энергия связи, приходящаяся на один нуклон ядра, которую можно вычислить, разделив энергию связи ядра на число содержащихся в нём нуклонов:
Эта величина представляет собой среднюю энергию, которую нужно затратить, чтобы удалить один нуклон из ядра, или среднее изменение энергии связи ядра, когда свободный протон или нейтрон поглощается в нём.
Как видно из поясняющего рисунка, при малых значениях массовых чисел удельная энергия связи ядер резко возрастает и достигает максимума при 



Такой характер поведения средней энергии связи указывает на свойство ядерных сил достигать насыщения, то есть на возможность взаимодействия нуклона только с малым числом «партнёров». Если бы ядерные силы не обладали свойством насыщения, то в пределах радиуса действия ядерных сил каждый нуклон взаимодействовал бы с каждым из остальных и энергия взаимодействия была бы пропорциональна 

Общая закономерность зависимости энергии связи от массового числа описывается формулой Вайцзеккера в рамках теории капельной модели ядра[1][2][14][15].
Устойчивость ядер[править | править код]
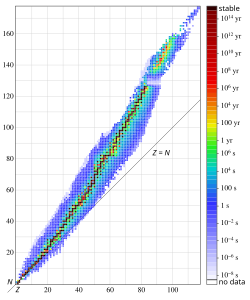
Зависимость числа нейтронов N от числа протонов Z в атомных ядрах (N=A-Z).
Из факта убывания средней энергии связи для нуклидов с массовыми числами больше или меньше 50-60 следует, что для ядер с малыми 

Детальные исследования показали, что устойчивость ядер также существенно зависит от параметра 



Если рассмотреть таблицу стабильных нуклидов, встречающихся в природе, можно обратить внимание на их распределение по чётным и нечётным значениям 







| Z | N=A-Z | A | Число нуклидов |
|---|---|---|---|
| Чётное | Чётное | Чётное | 167 |
| Чётное | Нечётное | Нечётное | 55 |
| Нечётное | Чётное | Нечётное | 53 |
| Нечётное | Нечётное | Чётное | 4 |
Таким образом, чётность числа протонов или нейтронов создаёт некоторый запас устойчивости, который приводит к возможности существования нескольких стабильных нуклидов, различающихся соответственно по числу нейтронов для изотопов и по числу протонов для изотонов. Также чётность числа нейтронов в составе тяжёлых ядер определяет их способность делиться под воздействием нейтронов[2].
Ядерные силы[править | править код]
Ядерные силы — это силы, удерживающие нуклоны в ядре, представляющие собой большие силы притяжения, действующие только на малых расстояниях. Они обладают свойствами насыщения, в связи с чем ядерным силам приписывается обменный характер (с помощью пи-мезонов). Ядерные силы зависят от спина, не зависят от электрического заряда и не являются центральными силами[2].
Уровни ядра[править | править код]
В отличие от свободных частиц, для которых энергия может принимать любые значения (так называемый непрерывный спектр), связанные частицы (то есть частицы, кинетическая энергия которых меньше абсолютного значения потенциальной), согласно квантовой механике, могут находиться в состояниях только с определёнными дискретными значениями энергий, так называемый дискретный спектр. Так как ядро — система связанных нуклонов, оно обладает дискретным спектром энергий. Обычно оно находится в наиболее низком энергетическом состоянии, называемым основным. Если передать ядру энергию, оно перейдёт в возбуждённое состояние.
Расположение энергетических уровней ядра в первом приближении:
, где:






С ростом энергии возбуждения уровни сближаются быстрее у тяжёлых ядер, также плотность уровней зависит от чётности числа нейтронов в ядре. Для ядер с чётными (особенно магическими) числами нейтронов плотность уровней меньше, чем для ядер с нечётными, при равных энергиях возбуждения первый возбуждённый уровень в ядре с чётным числом нейтронов расположен выше, чем в ядре с нечётным.
Во всех возбуждённых состояниях ядро может находиться лишь конечное время, до тех пор, пока возбуждение не будет снято тем или иным путём. Состояния, энергия возбуждения которых меньше энергии связи частицы или группы частиц в данном ядре, называются связанными; в этом случае возбуждение может сниматься лишь гамма-излучением. Состояния с энергией возбуждения, превышающей энергию связи частиц, называются квазистационарными. В этом случае ядро может испустить частицу или гамма-квант[1].
Ядерные реакции[править | править код]
Ядерная реакция — процесс превращения атомных ядер, происходящий при их взаимодействии с элементарными частицами, гамма-квантами и друг с другом.
Радиоактивность[править | править код]
Лишь небольшая часть нуклидов являются стабильными. В большинстве случаев ядерные силы оказываются неспособны обеспечить их постоянную целостность, и ядра рано или поздно распадаются. Это явление получило название радиоактивности.
Система обозначений ядер[править | править код]
Для обозначения атомных ядер используется следующая система:
Таким образом, состав ядра оказывается полностью определён, так как 
Пример такого обозначения:

Иногда, однако, для полноты вокруг обозначения элемента указывают все характеризующие ядро его атома числа:
- слева снизу — зарядовое число
, то есть, то же самое, что указано символом элемента;
- слева сверху — массовое число
;
- справа снизу — изотопическое число
[источник не указан 1369 дней (обс.)];
- если речь идёт о ядерных изомерах, к массовому числу приписывается буква из последовательности m, n, p, q, … (иногда используют последовательность m1, m2, m3, …). Иногда эту букву указывают в качестве самостоятельного индекса справа сверху.
Примеры таких обозначений:




Обозначения атомных ядер совпадают с таковыми для нуклидов.
По историческим и иным причинам, некоторые ядра имеют самостоятельные названия. Например, ядро 4He называется α-частицей, ядро дейтерия 2H (или D) — дейтроном, а ядро трития 3H (или T) — тритоном. Последние два ядра являются изотопами водорода и поэтому могут входить в состав молекул воды, давая в итоге так называемую тяжёлую воду.
Примечания[править | править код]
- Использованная литература
- ↑ 1 2 3 4 5 6 7 Бартоломей Г.Г., Байбаков В.Д., Алхутов М.С., Бать Г.А. Основы теории и методы расчета ядерных энергетических реакторов. — М.: Энергоатомиздат, 1982. — С. 512.
- ↑ 1 2 3 4 5 6 7 8 Климов А. Н. Ядерная физика и ядерные реакторы. — М.: Энергоатомиздат, 1985. — С. 352.
- ↑ 1 2 Ганев И. Х. Физика и расчёт реактора. — М.: Энергоиздат, 1981. — С. 368.
- ↑
Кудрявцев П. С. Открытие атомного ядра // Курс истории физики. — 2-е изд., испр. и доп. — М.: Просвещение, 1982. — 448 с. - ↑ Meitner, L. Über die verschiedenen Arten des radioaktiven Zerfalls und die Möglichkeit ihrer Deutung aus der Kernstruktur (нем.) // Zeitschrift für Physik : magazin. — 1921. — Bd. 4. — S. 146—156.
- ↑ Мухин К. Привлекательный мир микрофизики // Наука и жизнь. — 2015. — № 10. — С. 96—103.
- ↑ W. Heitler, G. Herzberg. Gehorchen die Stickstoffkerne der Boseschen Statistik? (нем.) // Naturwissenschaften (англ.) (рус. : magazin. — 1929. — Bd. 17. — S. 673.
- ↑ А. И. Ахиезер, М. П. Рекало. Биография элементарных частиц. — Киев: Наукова думка, 1979. — С. 18.
- ↑ Ю. А. Храмов. Физики:Биографический справочник. — 2-е изд. — М.: Наука, 1983.
- ↑ 1 2 Мухин К. Н. Экспериментальная ядерная физика. — М.: Энергоатомиздат, 1983.
- ↑ Iwanenko, D.D., The neutron hypothesis, Nature 129 (1932) 798.
- ↑ Г. А. Сарданашвили. Дмитрий Иваненко – суперзвезда советской физики. Ненаписанные мемуары. — Либроком. — 2010. — С. 12.
- ↑ Глесстон С. Атом. Атомное ядро. Атомная энергия. — М.: Изд-во иностр. лит., 1961.
- ↑ I.R.Cameron, University of New Brunswick. Nuclear fission reactors. — Canada, New Brunswick: Plenum Press, 1982.
- ↑ Камерон И. Ядерные реакторы. — М.: Энергоатомиздат, 1987. — С. 320.
- ↑ Rohlf, James William. Modern Physics from α to Z°. — John Wiley & Sons, 1994. — С. 664. — ISBN 0471572705.
Литература[править | править код]
- М. Айзенберг, В. Грайнер. Модели ядер, коллективные и одночастичные явления. — М.: Атомиздат, 1975. — 454 c.
- М. Айзенберг, В. Грайнер. Микроскопическая теория ядра. — М.: Атомиздат, 1976. — 488 с.
- К. Бракнер Теория ядерной материи. — М., Мир, 1964. — 302 с.
- О. Бор, Б. Моттельсон. Структура атомного ядра. — В 2-х т. — М.: Мир, 1971—1977.
- В. П. Крайнов. Лекции по микроскопической теории атомного ядра. — М.: Атомиздат, 1973. — 224 с.
- В. В. Маляров. Основы терии атомного ядра. 2-ое изд. — М.: Наука, 1967. — 512 с.
- Р. Натаф. Модели ядер и ядерная спектроскопия. — М.: Мир, 1968. — 404 с.
- С. М. Поликарпов. Необычные ядра и атомы. — М.: Наука, 1977. — 152 с.
- Дж. Рейнуотер. Как возникла модель сфероидальных ядер. Успехи физических наук, 1976, Том 120. Вып. 4, с. 529—541. (Нобелевская лекция по физике 1975 г.)
- А. Г. Ситенко. Теория ядерных реакций. — М.: Энергоатомиздат, 1983. — 352 с.
- А. Г. Ситенко, В. К. Тартаковский. Лекции по теории ядра. — М.: Атомиздат, 1972. — 352 с.
- Л. Слив М. И. Стрикман, Л. Л. Франкфурт. Проблемы построения микроскопической теории ядра и квантовая хромодинамика, Успехи физических наук, 1976, Том 145. Вып. 4, с. 553—592.
- В. Г. Соловьев. Теория атомного ядра. Ядерные модели. — М.: Энергоиздат, 1981. — 296с.
- В. Г. Соловьев. Теория сложных ядр. — М.: Наука, 1971. — 560 с.
- Журнал: Физика элементарных частиц и атомного ядра (ЭЧАЯ) (Архив статей с 1970 г.)
Ссылки[править | править код]
- Ядро атомное — Физическая энциклопедия
- Колебательные возбуждения ядер — Физическая энциклопедия
- Ядерные модели — Физическая энциклопедия
- Капельная модель ядра — Физическая энциклопедия
- Ядерная материя — Физическая энциклопедия
- Ядерные цепные реакции — Физическая энциклопедия
- Деформированные ядра — Физическая энциклопедия
- Б. С. Ишханов, Э. И. Кэбин, Физика ядра и частиц, XX век. МГУ, 2000.
- Ядерная энергия
Содержание
- – Как вычислять массу ядра?
- – Как найти массу атома вещества?
- – Как найти массу урана?
- – Как найти массу нуклонов?
- – Как рассчитать дефект массы?
- – Как найти массу одного электрона?
- – Сколько кг в а е м?
- – Как найти массу атома натрия?
- – Как найти массу молекулы вещества?
- – Сколько стоит 1 кг урана?
- – Как найти массу Земли по формуле?
- – Как можно найти массу небесных тел?
- – Чему равно массовое число элементов?
- – Как вычислить энергию связи?
Знание массового числа позволяет оценить массу ядра и атома. Если известно массовое число, то масса М атома и его ядра оценивается из следующего соотношения М ≈ А·mN, где mN ≈ 1,67·10−27 кг — масса нуклона, то есть протона или нейтрона.
Как вычислять массу ядра?
принимают 1/12 часть массы нуклида 12C. Следует отметить, что стандартная масса, которая обычно приводится для нуклида — это масса нейтрального атома. Для определения массы ядра нужно из массы атома вычесть сумму масс всех электронов (более точное значение получится, если учесть ещё и энергию связи электронов с ядром).
Как найти массу атома вещества?
Масса атома обозначается символом m a и может выражаться в единицах массы: килограммах или граммах. Массы атомов малы. Так, масса атома водорода равна m a ( H ) = 1,67 ⋅ 10 − 24 г , а масса атома углерода — m a ( C ) = 19,94 ⋅ 10 − 24 г .
Как найти массу урана?
Молярная масса урана равна 238,0289 г/моль.
Данное значение показывает отношение массы вещества (m) е число моль данного вещества (n), обозначается M и может быть рассчитано по формуле: M = m / n.
Как найти массу нуклонов?
Если число протонов в ядре обозначить буквой Z, а число нейтронов – буквой N, то массовое число (или число нуклонов) А = Z + N. Термин “массовое число” связан с тем, что именно количество нуклонов (протонов и нейтронов) в ядре практически полностью (с точностью обычно не хуже 1%) определяет массу атомного ядра и атома.
Как рассчитать дефект массы?
Дефект массы обусловлен энергией связи ядра Eсв, которая выделяется в результате соединения нуклонов в ядра. Массу, соответствующую энергии связи ядра (т. е. дефект массы), можно найти с помощью уравнения Эйнштейна E = mc2.
Как найти массу одного электрона?
Масса всех электронов m=N*me, где me – масса одного электрона.
Сколько кг в а е м?
1 а. е. м. = 1,660 539 066 60(50)⋅10−27 кг.
Как найти массу атома натрия?
M = m / n. В обычных условиях натрий (строение атома показано на рис. 1) представляет собой серебристо-белый металл. Он настолько мягок, что легко режется ножом.
Как найти массу молекулы вещества?
Чтобы найти массу одной молекулы, надо молярную массу разделить на число Авогадро, приблизительно будет 2,99*10 в минус 23 степени грамма.
Сколько стоит 1 кг урана?
Спотовая стоимость урана на сегодня составляют 20,02 у. е. (1155,3 руб.) за фунт, 1 грамм стоит 2,5 руб., а килограмм — 2500 рублей.
Как найти массу Земли по формуле?
Следовательно, зная, что ускорение свободного падения g=9,81мс2, G=6,673⋅10−11Н⋅м2кг2 и радиус Земли R⊕=6370км, можно по формуле M=gR2⊕G подсчитать массу Земли: M=5,97⋅1024кг. Среднюю плотность Земли можно определить, зная ее массу и объем.
Как можно найти массу небесных тел?
Массу небесного тела можно определить: а) из измерений силы тяжести на поверхности данного тела (гравиметрический способ); б) по третьему (уточненному) закону Кеплера; в) из анализа наблюдаемых возмущений, производимых небесным. телом в движениях других небесных тел.
Чему равно массовое число элементов?
Ма́ссовое число́ атомного ядра — суммарное количество протонов и нейтронов (называемых общим термином «нуклоны») в ядре. Обычно обозначается буквой A. Массовое число близко к атомной массе изотопа, выраженной в атомных единицах массы, но совпадает с ней только для углерода-12, поскольку атомная единица массы (а.
Как вычислить энергию связи?
Энергия связи ядра Eсв(A,Z) это минимальная энергия, необходимая, чтобы развалить ядро на отдельные, составляющие его нуклоны. Есв(A, Z) = [Z mp + (A – Z)mn – M(A, Z)]c2, где Z – число протонов, ( A – Z) – число нейтронов, mp – масса протона, mn – масса нейтрона, М(A,Z) – масса ядра с массовым числом А и зарядом Z.
Интересные материалы:
Что такое игла и какая она бывает?
Что такое индуктивность и от чего она зависит?
Что такое Инн компании?
Что такое int в Python?
Что такое история как наука кратко?
Что такое Ив Роше Дело Навального?
Что такое износ основных средств?
Что такое канон у Шипперов?
Что такое кэш в Вайбере?
Что такое Кешбек Ашан?

