xpout345
Вопрос по химии:
Найти массу сульфата кальция в 250 г гипса, содержащего 10% примесей.
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок – бесплатно!
Ответы и объяснения 1
vendlon289
Wcaso4= 100% – 10% = 90%
mCaSO4 = 90%*250/ 100% = 225г
Знаете ответ? Поделитесь им!
Гость ?
Как написать хороший ответ?
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете
правильный ответ; - Писать подробно, чтобы ответ был исчерпывающий и не
побуждал на дополнительные вопросы к нему; - Писать без грамматических, орфографических и
пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся
уникальные и личные объяснения; - Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не
знаю» и так далее; - Использовать мат – это неуважительно по отношению к
пользователям; - Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует?
Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие
вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи –
смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Химия,
вопрос задал faner67,
9 месяцев назад
karinapetrova709:
8 класс
Ответы на вопрос
Ответил karinapetrova709
1
Ответ:
M= 40+ 32+16×4+ 1×4 +16×2=172
Предыдущий вопрос
Следующий вопрос
Новые вопросы
Английский язык,
1 месяц назад
Нужно 8-10 предложений на английском о том как я съездил на море .
Русский язык,
1 месяц назад
Cкажите 15 слов с приставкой при- 15 слов с приставкой пре- ПОЖАЛУЙСТО СРОЧНО НАДО)…
Английский язык,
9 месяцев назад
1) Look at the sky! It … soon.
a) will rain b) is going to rain c) rains
2) Have you heard about Jake’s plans? He…across Europe next month!
a) will travel b)travels c)is going to…
История,
9 месяцев назад
Параграф «Государства и народы Африки и доколумбовой Америки». Придумать 5 вопросов к тесту параграфа.Пж, ток не списанное, откуда нибудь, у нас училка все чекает, я знаю где списано где нет…
Математика,
6 лет назад
помогите пожалуйста ребята…
Химия,
6 лет назад
Составьте молекулярные и ионные уравнения реакций, протекающих в водных растворах, объясните причины протекания реакций, назовите продукты реакций Cr2O3 + H2SO4 →
K2SO3 + H2SO4 →
Fe(OH)3 + HCl →…
Войти
Задать вопрос
Химия
Эсфира
5 января, 07:23
0
Ответы (1)
-

Филат
5 января, 08:48
0
Wcaso4 = 100% – 10% = 90%
mCaSO4 = 90%*250 / 100% = 225 г
- Комментировать
- Жалоба
- Ссылка
Знаете ответ?
Сомневаетесь в ответе?
Найдите правильный ответ на вопрос ✅ «Найти массу сульфата кальция в 250 г гипса, содержащего 10% примесей. …» по предмету 📘 Химия, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Смотреть другие ответы
Новые вопросы по химии
Придумайте необычные описания характеризующие воду.
Ответы (1)
Химия: Какие частицы входят в состав ядра атома? а). электроны б). протоны в). нейтроны г). ионы
Ответы (1)
По положению элемента #40 в табл Менделеева запишите электрон конфигур. Выделите ваоентные электронв и распредилите их по квантовым состоянием в стабильном и возбуж состояниях. Для валент электрон запишите квант числа.
Ответы (1)
CH3-CH2-CH2-Cl+KOH⇒?
Ответы (2)
Сожгли вещество, масса которого 13,8 грамм, при этом выделился оксид углерода (четырех валентный) объемом 23,52 литра, и вода массой 10,8 грамм. Плотность этого вещества по водороду 46. Установить молекулярную формулу
Ответы (2)
Главная » Химия » Найти массу сульфата кальция в 250 г гипса, содержащего 10% примесей.

Химия, опубликовано 2018-08-22 23:38:46 by Гость
Найти массу сульфата кальция полученного реакций между 300 грамм оксида кальция и 420 грам серной кислоты

Ответ оставил Гость
1)Для начала рассчитаем количество веществ каждого из реагента 1)n(CaO)=300/56=5.36моль 2)n(H2SO4)=420/98=4.3моль так как серная кислота двухосновная то при недостатке оксида кальция может образовываться гидросульфат кальция а при избытке оксида кальция образуется сульфат кальция и в 1ом и во 2 ом случае молярное соотношение реагнетов будет 1;1 и мы видим что в избытке находится оксид кальция запишем уравнение реакции CaO+H2SO4=CaSO4+H2O расчет будем вести по недостатку т е по серной кислоте тогда m(CaSO4)=136^4.3=584.8грамм

Не нашли ответа?
Если вы не нашли ответа на свой вопрос, или сомневаетесь в его правильности, то можете воспользоваться формой ниже и уточнить решение. Или воспользуйтесь формой поиска и найдите похожие ответы по предмету Химия.
Какая жесткость воды
При обработке 0,5 литров жесткой воды карбонатом натрия (Na2CO3) в осадок выпало 70 миллиграмм карбоната кальция (CaCO3). Какая жесткость воды, если она обусловлена только сульфатом кальция (CaSO4)?
Решение задачи
Запишем уравнение реакции устранения жесткости воды карбонатом натрия (Na2CO3):
![]()
Какая жесткость воды.
Найдем молярные массы веществ (смотри таблицу Менделеева):
M (CaSO4) = 40 + 32 + 4 ⋅ 16 = 136 (г/моль),
M (CaCO3) = 40 + 12 + 3 ⋅ 16 = 100 (г/моль).
По уравнению реакции найдем массу сульфата кальция (CaSO4):
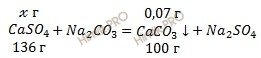
при обработке х г CaSO4 образуется 0,07 г CaCO3
при обработке 136 г CaSO4 образуется 100 г CaCO3
Откуда:
![]()
Какая жесткость воды. Вычислим молярную массу эквивалента сульфата кальция (CaSO4) по формуле:
![]()
Где:
z – число эквивалентности.
Получаем:
Mэкв. (CaSO4) = 136 / 2 = 68 (г/моль).
Какая жесткость воды. Запишем формулу нахождения жесткости воды:
![]()
Где:
Ж — жесткость воды, ммоль /л;
m — масса вещества, обусловливающего жесткость воды или применяемого для ее устранения, мг; Мэ — эквивалентная масса этого вещества, г/моль;
V — объем воды, л (дм3).
Подставляя в формулу данные из условия задачи, найдем какая жесткость воды:
Ж = 95,2 / 68 ⋅ 0,5 = 2,8 (ммоль /дм3).
Ответ:
жесткость воды 2,8 ммоль/дм3.

