Ученик
(58),
закрыт
12 лет назад
Алина Харибина
Мастер
(1377)
12 лет назад
это газ, поэтому формула m=pv не подходит
здесь надо считать через количество вещества
n = V/Vm – объем на молярный объем
также
n = m/M – масса на молярную массу
молярный объем Vm = 22,4 л
молярная масса углекислого газа M = 44 г/моль
V/Vm = m/M
m = (V * M) / Vm
m = (20 * 44) / 22,4 = 39,29 г
Валентина Вавилова(Серкова)
Гений
(62183)
12 лет назад
Из уравнения Менделеева -Клапейрона р v= m*RT / M, выразим массу:
m=p v M / R T ( p-давление, v-объем, в системе СИ =0,02 куб. м, R-универсальная газовая постоянная= 8,31 Дж / моль К, Т – абсолютная температура ( по Кельвину) , для нормальных условий = 273К, М- молярная масса углекислого газа=0,044кг/моль. ) Подставим и вычислим: m=0,04 кг. ( 40г)
Рассчитывать можно по этой формуле, для любых газов, любых объемов, температур и давлений).
Как вычислить массу газа
Довольно часто встает вопрос: как можно вычислить массу какого-либо газа, содержащегося в определенном объеме при определенных условиях (давлении, температуре)? Произвести эти вычисления несложно, надо лишь знать несколько правил.

Инструкция
Предположим, перед вами поставлена задача: надо определить массу углекислого газа, занимающего при нормальном давлении и комнатной температуре объем в 0,18 м^3. Прежде всего вспомните универсальное правило, согласно которому 1 моль любого газа при нормальных условиях занимает объем, равный 22,4 литра. (Точнее – 22, 414 литра, но для упрощения расчетов эту величину можно округлить).
Потом переведите данный вам объем в литры. 0,18м^3 – это 180 литров. Соответственно, в нем содержится 180/22,4 = 8,036 молей углекислого газа.
А теперь остается последний шаг. Формула углекислого газа – СО2. Его молярная масса: 12 + 16*2 = 44 грамма/моль. То есть в одном моле углекислого газа содержится примерно 44 грамма этого вещества. Сколько же его в 8,036 молях? Произведите умножение: 44*8,036 = 353, 58 грамма или округленно 353,6 грамма. Задача решена.
Если вам надо найти массу того же углекислого газа, но находящегося при условиях весьма отличающихся от нормальных? Например, какое-то количество этого газа поместили в герметичный сосуд объемом V, нагрели до температуры Т, измерили его давление, оказавшееся равным P. Вопрос: какая масса углекислого газа содержится в сосуде при таких условиях?
И эта задача также очень простая. Для ее решения надо всего лишь вспомнить про уравнение Менделеева-Клапейрона, названное в честь двух выдающихся ученых. Оно было выведено ими для описания состояний так называемого «идеального газа». Его формула такова: PV = MRT/m. Или в слегка видоизмененной форме: PVm = МRT, где З – давление в паскалях, V – объем в кубических метрах, m – молярная масса газа, M – его фактическая масса, T – температура в градусах Кельвина, R – универсальная газовая постоянная, примерно равная 8,31.
Легко можно видеть, что фактическая масса газа М вычисляется по формуле: М = PVm / RT. Подставив в эту формулу все известные данные, и помня, что молярная масса углекислого газа m равна 44 грамма/моль, вы легко получите ответ.
Конечно же, ни углекислый газ, ни какой-либо другой не является идеальным газом. Поэтому, уравнение Менделеева-Клапейрона не вполне точно описывает его состояние. Но, если условия не очень сильно отличаются от нормальных, погрешности вычислений малы, и ими можно пренебречь.
Источники:
- формула углекислого газа
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Известно, что масса углекислого газа (CO2) 35 грамм. Определите объём углекислого газа (CO2).
Решение задачи
Так как, углекислый газ (CO2) – газообразное вещество, то для нахождения объема углекислого газа (CO2) массой 35 г будем использовать формулу перерасчета, которая устанавливает связь между массой и объемом газа:
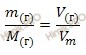
Откуда выразим объем произвольной массы газа:
![]()
Учитывая, что молярная масса углекислого газа (CO2) равна:
M (CO2) = 12 + 2 ∙ 16 = 44 (г/моль)
Рассчитаем объем углекислого газа (CO2):
![]()
Ответ:
объем углекислого газа равен 17,82 литра.
Условие задачи:
Найти массу углекислого газа в баллоне вместимостью 40 л при температуре 288 К и давлении 5,07 МПа.
Задача №4.2.2 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(V=40) л, (T=288) К, (p=5,07) МПа, (m-?)
Решение задачи:
Применим уравнение Клапейрона-Менделеева:
[pV = frac{m}{M}RT]
В этом уравнении (R) – универсальная газовая постоянная, равная 8,31 Дж/(моль·К), (M) – молярная масса углекислого газа, равная 0,044 кг/моль.
Все величины, входящие в уравнение, кроме искомой массы, известны. Выразим массу (m), тогда получим такую формулу:
[m = frac{{pVM}}{{RT}}]
Переведем объем баллона в систему СИ:
[40;л = 0,04;м^3]
Произведем вычисления:
[m = frac{{5,07 cdot {{10}^6} cdot 0,04 cdot 0,044}}{{8,31 cdot 288}} = 3,73;кг]
Ответ: 3,73 кг.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
4.2.1 Какой объем занимает 1 кг кислорода при 0 C и давлении 800 кПа?
4.2.3 В баллоне емкостью 25,6 л находится 1,04 кг азота при давлении 3,55 МПа. Определите
4.2.4 Баллон содержит 28 кг кислорода при давлении 770 кПа. Какова масса гелия, занимающего
Онисифор
10 ноября, 22:28
-

Элюня
10 ноября, 23:50
+1
M (CO2) = 12+16*2=12+32=44 г/моль
n = 5/22,4 = 0,22 моль
m=n*M = 0,22 * 44 = 9,68 г
Ответ м (CO2) = 9,68 г
- Комментировать
- Жалоба
- Ссылка
-

Найди верный ответ на вопрос ✅ «Определить массу углекислого газа (CO2), объемом 5 литров? …» по предмету 📙 Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Искать другие ответы
Главная » Химия » Определить массу углекислого газа (CO2), объемом 5 литров?
