Растворимость (Р, χ или ks) – это характеристика насыщенного раствора, которая показывает, какая масса (или объем для газов) растворенного вещества может максимально раствориться в 100 г растворителя. Размерность растворимости — г/ 100 г воды. Поскольку мы определяем массу соли, которая приходится на 100 г воды, в формулу растворимости добавляем множитель 100:
здесь mр.в. – масса растворенного вещества, г
mр-ля – масса растворителя, г
Иногда используют обозначение коэффициент растворимости kS.
Задачи на растворимость, как правило, вызывают сложности, так как эта физическая величина для школьников не очень привычна.
Как же решать задачи на растворимость? Я использую два способа. Давайте их рассмотрим на фрагменте задачи из реального ЕГЭ по химии 2019 года, где впервые появились задачи с упоминанием растворимости.
«Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната натрия к 400 мл воды.»
Первый способ.
Растворимость не показывает реальное количество соли или количество воды. Это всего лишь способ выражения концентрации в насыщенных растворах, величина, которая показывает, как соотносятся масса растворенного вещества и масса воды (или другого растворенного вещества)! Например, в условии задачи растворимость карбоната натрия 31,8 г на 100 г воды означает, что для растворения каждых 31,8 г соли необходимо 100 г воды. Зато из этих данных можно определить массовую долю растворенного вещества. Рассмотрим этот эталонный раствор, в котором содержится 31,8 г соли и 100 г воды. Массовая доля соли в таком растворе составляет:
ωр.в. = mр.в./mр-ра = 31,8 г/131,8 г = 0,2413 или 24,13%
Но в нашем, реальном растворе, который получается при растворении карбоната натрия в 400 г воды, массовая доля соли такая же!
Зная массу воды и массовую долю соли, мы без труда составим уравнение и определим массу соли в реальном растворе:
ωр.в. = mр.в./(mр.в. + mр-ра)
0,2413 = mр.в./(mр.в. + 400)
mр.в. = 127,2 г
Получается, масса нитрата натрия в реальном растворе равна 127,2 г.
Второй способ.
Используя все тот же эталонный раствор, мы можем составить пропорцию, чтобы определить массу соли в реальном растворе.
На 100 г воды приходится 31,8 г соли (по условию)
на 400 г воды будет приходиться х г соли (в реальном растворе)
Определяем х из пропорции:
х = 400 г · 31,8 г/100 г = 127,2 г нитрата натрия.
Но будьте осторожны! Пропорции можно составить далеко не для всех величин. Но соотносить массу воды и массу растворенного вещества при неизменной концентрации (массовой доле) растворенного вещества можно и иногда очень удобно. Также пропорциональны масса раствора и масса растворенного вещества, масса воды и масса раствора и т.д.
Задача 1. Массовая доля вещества в насыщенном растворе равна 24% при некоторой температуре. Определите коэффициент растворимости этого вещества при данной температуре.
Решение:
Для определения растворимости вещества примем массу раствора равной 100 г. Тогда масса соли равна:
mр.в. = mр-ра⋅ωр.в. = 100⋅0,24 = 24 г
Масса воды равна:
mводы = mр-ра – mр.в. = 100 — 24 = 76 г
Определяем растворимость:
χ = mр.в./mр-ля⋅100 = 24/76⋅100 = 31,6 г вещества на 100 г воды.
Ответ: χ = 31,6 г
Еще несколько аналогичных задач:
2. Массовая доля соли в насыщенном растворе при некоторой температуре равна 28,5%. Определите коэффициент растворимости вещества при этой температуре.
Решение:
Примем массу раствора равной 100 г. Тогда масса соли равна:
mр.в. = mр-ра⋅ωр.в. = 100⋅0,285 = 28,5 г
Масса воды равна:
mводы = mр-ра – mр.в. = 100 — 28,5 = 71,5 г
Определяем растворимость:
χ = mр.в./mр-ля⋅100 = 28,5/71,5⋅100 = 39,86 г вещества на 100 г воды.
Ответ: χ = 39,86 г вещества на 100 г воды.
3. Определите коэффициент растворимости нитрата калия при некоторой температуре, если массовая доля соли при этой температуре равна 0,48.
4. Какая масса воды и соли потребуется для приготовления 500 г насыщенного при некоторой температуре раствора нитрата калия, если его коэффициент растворимости при этой температуре равен 63,9 г соли в 100 г воды?
5. Коэффициент растворимости хлорида натрия при некоторой температуре составляет 36 г соли в 100 г воды. Определите молярную концентрацию насыщенного раствора этой соли, если плотность раствора 1,2 г/мл.
Ответ: 5,49М
6. Какая масса соли и 5% раствора её потребуется для приготовления 450г насыщенного при некоторой температуре раствора сульфата калия, если его коэффициент растворимости при этой температуре равен 439г/1000г воды?
7. Какая масса нитрата бария выделится из раствора, насыщенного при 100ºС и охлаждённого до 0ºС, если во взятом растворе было 150мл воды? Коэффициент растворимости нитрата бария при температурах 0ºС и 100ºС равен соответственно 50г и 342г в 100г воды.
8. Коэффициент растворимости хлорида калия при 90ºС равен 500г/л воды. Сколько граммов этого вещества можно растворить в 500г воды при 90ºС и какова его массовая доля в насыщенном растворе при этой температуре?
9. В 500г воды растворено при нагревании 300г хлорида аммония. Какая масса хлорида аммония выделится из раствора при его охлаждении до 50ºС, если коэффициент растворимости соли при этой температуре равен 50г/л воды?
Рассмотрим несколько примеров решения задач на растворимость из реальных ЕГЭ по химии.
10. Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната натрия к 400 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора сульфата железа(III). К раствору во второй колбе добавили 300 г раствора азотной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из второй колбы, оказался в 2 раза больше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю нитрата натрия в конечном растворе во второй колбе.
Первый этап.
Определяем массу карбоната натрия, который растворится в 400 мл воды:
На 100 г воды приходится 31,8 г соли (по условию)
на 400 г воды будет приходиться х г соли (в реальном растворе)
Определяем х из пропорции:
х = 400 г · 31,8 г/100 г = 127,2 г нитрата натрия.
n(Na2CO3) = m(Na2CO3)/M = 127,2 г/106 г/моль = 1,2 моль
Массовая доля карбоната натрия в этом растворе:
ω(Na2CO3) = m(Na2CO3)/mр-ра = 127,2 г/(127,2 г + 400 г) = 0,2413 или 24,13%
Далее раствор карбоната натрия разделили на две порции. Как решать задачи с порциями (частями)? Очень просто. Во всем исходном растворе и в порциях (частях), которые мы отделили от основного раствора, кое-что не меняется. Давайте порассуждаем, что именно.
Меняется ли масса раствора? Без сомнения, мы же разделяем раствор на части.
Меняется ли масса растворенного вещества? Также без сомнения — часть вещества попадет в одну порцию, часть в другую.
А меняется ли массовая доля растворенного вещества? Или соотношение массы растворенного вещества и воды, или другое соотношение? Конечно, не изменяется, ведь раствор — это гомогенная система, в которой вещество распределено равномерно.
Второй этап.
В первой колбе протекает реакция:
3Na2CO3 + Fe2(SO4)3 + 3H2O = 2Fe(OH)3 + 3CO2 + 3Na2SO4
Это типичный пример реакции необратимого гидролиза.
Во второй колбе протекает реакция:
Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + H2O
Пусть в первой колбе выделилось х моль углекислого газа. Количество вещества газов соотносится также, как объемы газов. Поэтому можно сказать, что во второй колбе выделится 2х моль углекислого газа.
Получается, что в первой колбе в реакцию вступает х моль карбоната натрия, а во второй колбе 2х моль карбоната натрия. Общее количество вещества карбоната натрия известно, получаем уравнение:
х + 2х = 1,2
Отсюда х = 0,4 моль.
Во второй колбе количество и масса карбоната натрия:
n2(Na2CO3) = 2х = 0,8 моль
m2(Na2CO3) = n2(Na2CO3)·M = 0,8 моль·106 г/моль = 84,8 г
Масса раствора карбоната во второй колбе (массовая доля соли в исходном растворе и в двух колбах не изменяется):
mр-ра,2(Na2CO3) = m2(Na2CO3)/ω = 84,8 г / 0,2413 = 351,47 г
Масса углекислого газа, который выделился во второй реакции:
m2(CO2) = n2(CO2)·M(СО2) = 0,8 моль·44 г/моль = 35,2 г
Масса нитрата натрия во второй колбе:
m2(NaNO3) = n2(NaNO3)·M(NaNO3) = 1,6 моль·85 г/моль = 136 г
Масса конечного раствора во второй колбе:
mр-ра,2 = mр-ра,2(Na2CO3) + mр-ра(HNO3) — m(CO2) = 351,47 г + 300 г — 35,2 г = 616,27 г
Массовая доля нитрата натрия в конечно растворе во второй колбе:
ω2(NaNO3) = m2(NaNO3)/mр-ра,2 = 136 г/616,27 г = 0,2207 или 22,07%
Ответ: ω(NaNO3) = 22,07%
11. Растворимость безводного сульфида натрия при некоторой температуре составляет 15,6 г на 100 г воды. При этой температуре приготовили 289 г насыщенного раствора сульфида натрия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора хлорида алюминия. К раствору во второй колбе добавили 100 г соляной кислоты, также взятой в избытке. При этом объём газа, выделившийся из второй колбы, оказался в 1,5 раза больше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю хлорида натрия в конечном растворе во второй колбе.
3Na2S + 2AlCl3 + 6H2O = 2Al(OH)3 + 3H2S + 6NaCl
Na2S + 2HCl = 2NaCl + H2S
Ответ: ω(NaCl) = 13,336%
12. Растворимость безводного хлорида алюминия при некоторой температуре составляет 53,4 г на 100 г воды. При этой температуре приготовили 306,8 г насыщенного раствора хлорида алюминия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора карбоната калия. К раствору во второй колбе добавили 300 г раствора аммиака, также взятого в избытке. При этом, масса осадка, выпавшего во второй колбе, оказалась в 3 раза больше массы осадка, выпавшего в первой колбе. Определите массовую долю хлорида аммония в конечном растворе во второй колбе.
2AlCl3 + 3K2CO3 + 3H2O = 2Al(OH)3 + 3CO2 + 6KCl
AlCl3 + 3NH3∙H2O = Al(OH)3 + 3NH4Cl
Ответ: ω(NH4Cl) = 19,9255%
13. Растворимость безводного карбоната аммония при некоторой температуре составляет 96 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество карбоната аммония к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток твёрдого гидроксида натрия и нагрели. К раствору во второй колбе добавили 250 г соляной кислоты, также взятой в избытке. При этом объём газа, выделившийся из второй колбы, оказался в 3 раза меньше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю соли в конечном растворе во второй колбе.
(NH4)2CO3 + 2NaOH = 2NH3 + 2H2O + Na2CO3
(NH4)2CO3 + 2HCl = 2NH4Cl + CO2 + H2O
Ответ: ω(NH4Cl) = 26,62%
14. Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. Насыщенный раствор, приготовленный при этой температуре добавлением необходимого количества карбоната натрия к 200 мл воды, разделили на две части. К первой части прилили избыток соляной кислоты. При этом выделилось 4,48 л (н.у.) газа. Ко второй части насыщенного раствора добавили 222 г 25%-ного раствора хлорида кальция. Определите массовую долю хлорида кальция в полученном растворе.
Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
Na2CO3 + CaCl2 = CaCO3 + 2NaCl
Ответ: ω(CaCl2) = 3,1%
15. Растворимость безводного сульфата железа(II) при некоторой температуре составляет 30,4 г на 100 г воды. При этой температуре приготовили 326 г насыщенного раствора сульфата железа(II). Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора хлорида бария. При этом образовалось 46,6 г осадка. К раствору во второй колбе добавили 50 г 34%-ного раствора аммиака. Определите массовую долю аммиака в конечном растворе во второй колбе.
FeSO4 + BaCl2 = BaSO4 + FeCl2
FeSO4 + 2NH3∙H2O = Fe(OH)2 + (NH4)2SO4
Ответ: ω(NH3) = 3,11%
16. Растворимость безводного сульфата алюминия при некоторой температуре составляет 34,2 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфата алюминия к 300 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора аммиака. При этом образовалось 15,6 г осадка. К раствору во второй колбе добавили 320 г 25%-ного раствора гидроксида натрия. Определите массовую долю сульфата натрия в конечном растворе во второй колбе.
Al2(SO4)3 + 6NH3∙H2O = 2Al(OH)3 + 3(NH4)2SO4
Al2(SO4)3 + 8NaOH = 2Na[Al(OH)4] + 3Na2SO4
Ответ: ω(Na2SO4) = 14,48%
17. Растворимость безводного карбоната натрия при некоторой температуре составляет 31,8 г на 100 г воды. Приготовленный при этой температуре насыщенный раствор карбоната натрия массой 395,4 г разделили на две части. К первой части прилили избыток раствора нитрата кальция. При этом образовалось 50 г осадка. Ко второй части насыщенного раствора добавили 252 г 30%-ного раствора азотной кислоты. Определите массовую долю азотной кислоты в образовавшемся растворе.
Na2CO3 + Ca(NO3)2 = CaCO3 + 2NaNO3
Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + H2O
Ответ: ω(HNO3) = 6,14%
18. Растворимость безводного сульфата железа(II) при некоторой температуре составляет 30,4 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфата железа(II) к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора гидроксида натрия. При этом образовалось 18 г осадка. К раствору во второй колбе добавили 870 г 15%-ного раствора нитрата бария. Определите массовую долю нитрата бария в конечном растворе во второй колбе.
FeSO4 + 2NaOH = Fe(OH)2 + Na2SO4
FeSO4 + Ba(NO3)2 = BaSO4 + Fe(NO3)2
Ответ: ω(Ba(NO3)2) = 5,24%
19. Растворимость безводного сульфида натрия при некоторой температуре составляет 15,6 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфида натрия к 250 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора соляной кислоты. При этом выделилось 4,48 л (н.у.) газа. К раствору во второй колбе добавили 450 г 15%-ного раствора хлорида меди(II). Определите массовую долю хлорида меди(II) в конечном растворе во второй колбе.
Na2S + 2HCl = H2S + 2NaCl
Na2S + CuCl2 = CuS + 2NaCl
Ответ: ω(CuCl2) = 4,54%
21. Растворимость безводного хлорида кальция при некоторой температуре составляет 55,5 г на 100 г воды. Насыщенный раствор, приготовленный при этой температуре добавлением необходимого количества хлорида кальция к 160 мл воды, разлили на две колбы. В первую колбу добавили избыток раствора карбоната натрия. При этом выпал осадок массой 30 г. Во вторую колбу добавили 595 г 40%-ного раствора нитрата серебра. Определите массовую долю нитрата серебра в растворе, образовавшемся во второй колбе.
CaCl2 + Na2CO3 = CaCO3 + 2NaCl
CaCl2 + 2AgNO3 = 2AgCl + Ca(NO3)2
Ответ: ω(AgNO3) = 11,2%
22. Растворимость безводного гидрокарбоната натрия при некоторой температуре составляет 12,6 г на 100 г воды. При этой температуре приготовили 450,4 г насыщенного раствора гидрокарбоната натрия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора гидроксида бария. При этом образовалось 39,4 г осадка. К раствору во второй колбе добавили 245 г 20%-ного раствора серной кислоты. При этом образовалась средняя соль. Определите массовую долю серной кислоты в конечном растворе во второй колбе.
NaHCO3 + Ba(OH)2 = BaCO3 + NaOH + H2O
2NaHCO3 + H2SO4 = Na2SO4 + 2CO2 + 2H2O
Ответ: ω(H2SO4) = 5,57%
23. Растворимость хлорида алюминия при некоторой температуре составляет 53,4 г на 100 г воды. Приготовленный при этой температуре насыщенный раствор хлорида алюминия массой 767 г разлили по двум колбам. В первую колбу добавили избыток раствора нитрата серебра, при этом выпало 344,4 г осадка. Во вторую колбу добавили 960 г 40%-ного раствора гидроксида натрия. Вычислите массовую долю хлорида натрия в растворе, образовавшемся во второй колбе.
AlCl3 + 3AgNO3 = 3AgCl + Al(NO3)3
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Ответ: ω(NaCl) = 14,83%
24. Растворимость безводного сульфата железа(II) при некоторой температуре составляет 30,4 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфата железа(II) к 400 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора аммиака. При этом образовалось 27 г осадка. К раствору во второй колбе добавили 780 г 20%-ного раствора хлорида бария. Определите массовую долю хлорида бария в конечном растворе во второй колбе.
FeSO4 + 2NH3∙H2O = Fe(OH)2 + (NH4)2SO4
FeSO4 + BaCl2 = BaSO4 + FeCl2
Ответ: ω(BaCl2) = 5,255%
25. Растворимость безводного хлорида кальция при некоторой температуре составляет 55,5 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество хлорида кальция к 300 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора нитрата серебра. При этом образовалось 143,5 г осадка. К раствору во второй колбе добавили 1272 г 10%-ного раствора карбоната натрия. Определите массовую долю карбоната натрия в конечном растворе во второй колбе.
CaCl2 + 2AgNO3 = 2AgCl + Ca(NO3)2
CaCl2 + Na2CO3 = CaCO3 + 2NaCl
Ответ: ω(Na2CO3) = 1,43%
26. Растворимость безводного сульфита натрия при некоторой температуре составляет 25,2 г на 100 г воды. При этой температуре приготовили насыщенный раствор, добавив необходимое количество сульфита натрия к 300 мл воды. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток концентрированной азотной кислоты. При этом выделился бурый газ. К раствору во второй колбе добавили 300 г раствора соляной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из второй колбы, оказался равен объёму газа, выделившемуся из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю хлорида натрия в конечном растворе во второй колбе.
Na2SO3 + 2HNO3 = Na2SO4 + 2NO2 + H2O
Na2SO3 + 2HCl = 2NaCl + SO2 + H2O
Ответ: ω(NaCl) = 8,92%
27. Растворимость безводного сульфита натрия при некоторой температуре составляет 25,2 г на 100 г воды. При этой температуре приготовили 250,4 г насыщенного раствора сульфита натрия. Раствор разлили в две колбы. К раствору в первой колбе добавили избыток раствора сульфата алюминия. К раствору во второй колбе добавили 200 г разбавленного раствора серной кислоты, также взятой в избытке. При этом, объём газа, выделившийся из второй колбы, оказался в 3 раза меньше объёма газа, выделившегося из первой колбы. (Объёмы газов измерены при одинаковых условиях). Определите массовую долю соли в конечном растворе во второй колбе. (Учитывать образование только средних солей).
3Na2SO3 + Al2(SO4)3 + 3H2O = 3SO2 + 2Al(OH)3 + 3Na2SO4
Na2SO3 + H2SO4 = Na2SO4 + SO2 + H2O
Ответ: ω(Na2SO4) = 5,54%
ЗАДАЧИ на Вычисление массы
растворенного вещества
Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей; вычисление массовой доли вещества в растворе. Элемент ЕГЭ: 4.3.1. Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе».
Расчёты с использованием понятий «растворимость»,
«массовая доля вещества в растворе»
Раствор — это гомогенная система, состоящая из двух или более веществ, содержание которых можно изменять в определенных пределах без нарушения однородности. Растворы состоят из растворителя (например, воды) и растворенного вещества.
Массовой долей растворенного вещества (ω) называют отношение его массы m(В) к массе раствора m(p).
ω(В) = m(В) : m(p)
Это безразмерная величина, поэтому выражается в долях единицы (изменяется от 0 до 1), но иногда выражается в процентах (тогда изменяется от 0 до 100 %).
Обозначение ω(В) аналогично обозначению ω(р. в-ва) или ω(в-ва);
обозначение m(В) аналогично обозначению m(р. в-ва) или m(в-ва);
обозначение m(р) аналогично обозначению m(р-ра),
где р-ра – сокращение слова «раствора», а р. в-ва и в-ва – сокращения слов «растворенного вещества».
Обратите внимание также на следующие обозначения:
m(в) — масса безводного вещества;
m(р-ля) — масса растворителя.
Соотношения между величинами, характеризующими раствор
Следует учитывать, что любой способ выражения содержания растворенного вещества в растворе дается в расчете на безводное вещество, даже если для приготовления раствора использован кристаллогидрат. Если для приготовления растворов используют не безводное вещество, а его кристаллогидрат, B • nH20, то масса растворителя (воды) рассчитывается по формуле: m(H20) = m(р) – m(кр.), где m(кр.) — масса кристаллогидрата, в граммах. Следует учитывать, что количество (моль) кристаллогидрата равно количеству (моль) безводного вещества, т.е. m(кр.) : М(кр.) = m(в) : М(в).
Молярная концентрация характеризует количество растворенного вещества, выраженное, в молях, содержащееся в 1 л раствора. Молярная концентрация вычисляется по формуле С = v / V, где С — молярная концентрация (измеряется в моль/л), v — количество вещества, V — объем раствора, измеренный в литрах. Часто размерность молярной концентрации обозначают символом М. Например, раствор с концентрацией 1 М (одномолярный раствор) содержит 1 моль растворенного вещества в 1л раствора, 0,1 М (децимолярный раствор) — 0,1 моль растворенного вещества в 1 л раствора и т. д.
Титр (Т) определяет массу растворенного вещества (в г), содержащуюся в 1 мл раствора: T = m / V.
Растворимость характеризует способность вещества растворяться в том или ином растворителе. Растворимость обозначается символом S, она равна концентрации насыщенного при данной температуре раствора. Чаще всего растворимость измеряют числом граммов вещества, способных раствориться в 100 г растворителя при данной температуре. Важно не путать растворимость с массовой долей вещества в растворе, так как растворимость показывает, сколько граммов растворенного вещества содержится в 100 г растворителя, а массовая доля — сколько граммов растворенного вещества содержится в 100 г раствора. Растворимость веществ зависит от температуры. Растворимость твердых веществ при повышении температуры, как правило, увеличивается, растворимость газов — уменьшается.
Приготовление растворов. Способы приготовления растворов: 1) Разбавление раствора водой; 2) Выпаривание воды из раствора; 3) Сливание двух растворов; 4) Выпадение кристаллов.
Способы приготовления растворов в задачах на Вычисление массы растворенного вещества
РЕШЕНИЯ ЗАДАЧ с использованием понятий «растворимость»,
«массовая доля вещества в растворе»
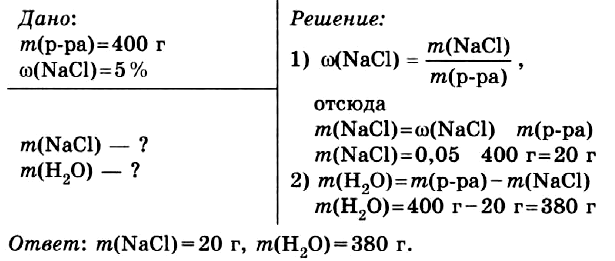
Задача № 1.
Приготовить 400 г водного раствора с массовой долей хлорида натрия в нём 5 %.
Правильный ОТВЕТ: m(NaCl) = 20 г, m(H2O) = 380 г.
Смотреть РЕШЕНИЕ задачи в тетради
Задача № 2.
Найти массовую долю растворённого вещества (в %) в растворе, полученном при смешивании 450 г воды и 50 г сахара.
Правильный ОТВЕТ: ω(сах.) = 10%.
Смотреть РЕШЕНИЕ задачи в тетради
Задача № 3.
Вычислите молярную концентрацию 4%-ного раствора поваренной соли, плотность которого равна 1,027 г/мл.
Правильный ОТВЕТ: C(NaCl) ≈ 0,7 моль/л.
Смотреть РЕШЕНИЯ заданий в тетради

Задача № 4.
Найдите массовую долю гидроксида натрия в растворе, молярная концентрация которого равна 3,08 моль/л, а плотность 1,12 г/мл.
Правильный ОТВЕТ: ω(NaOH) = 11%.
Смотреть РЕШЕНИЯ заданий в тетради

Задача № 5.
При 25 °С растворимость хлорида калия в воде составляет 25 г соли на 100 г воды. Вычислите массовую долю соли в насыщенном растворе и его молярную концентрацию, если плотность насыщенного раствора равна 1,132 г/мл.
Правильный ОТВЕТ: ω(KCl) = 20%, С(KCl) = 3,04 моль/л.
Смотреть РЕШЕНИЯ заданий в тетради
Задача № 6.
Массовая доля соли в растворе, насыщенном при температуре 40 °С, равна 35%. При охлаждении 300 г этого раствора до температуры 10 °С в осадок выпадает 45 г соли. Определите растворимость соли при 10 °С.
Правильный ОТВЕТ: S10°С = 30,77 г.
Смотреть РЕШЕНИЯ заданий в тетради
Задачи с ответами
на Вычисление массы растворенного вещества
Задача № 7.
Масса нитрата калия, которую следует растворить в 150 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%, равна ______. (Записывайте ответ с точностью до десятых.)
Правильный ОТВЕТ: 3,4 г.
Задача № 8.
Плотность 10% -ного раствора хлорида калия составляет 1,063 г/мл. Определите массу (г) хлорида калия, который содержится в 750 мл такого раствора.
Правильный ОТВЕТ: 75,0 г.
Задача № 9.
Рассчитайте массовую долю (%) нитрата натрия в растворе, полученном при смешивании 250 г 10%-ного и 750 г 15%-ного растворов этой соли.
Правильный ОТВЕТ: 13,75 %.
Задача № 10.
Найдите массовую долю гидроксида натрия в растворе, молярная концентрация которого равна 3,08 моль/л, а плотность 1,12 г/мл.
Правильный ОТВЕТ: ω(NaOH) = 11%.
Задача № 11.
В 125 г воды растворили 25 г азотной кислоты. Вычислите титр образовавшегося раствора, если его плотность равна 1,095 г/мл.
Правильный ОТВЕТ: T(HNO3) = 0,182 г/мл.
Задача № 12.
Титр раствора сульфата аммония равен 0,223 г/мл, а его плотность — 1,115 г/мл. Рассчитайте массовую долю сульфата аммония в данном растворе и молярную концентрацию раствора.
Правильный ОТВЕТ: ω((NH4)2SO4) = 20%, C((NH4)2SO4) = 1,689 моль/л.
(с) В учебных целях использованы цитаты из пособий: «Химия / Н. Э. Варавва, О. В. Мешкова. — Москва, Эксмо (ЕГЭ. Экспресс-подготовка)» и «Химия : Новый полный справочник для подготовки к ЕГЭ / Е.В. Савинкина. — Москва, Издательство АСТ».
Вы смотрели Справочник по химии «ЗАДАЧИ на Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей; вычисление массовой доли вещества в растворе». Выберите дальнейшее действие:
- Перейти к Списку конспектов по химии (по классам)
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
Здравствуйте, уважаемые читатели!
Сегодня – третья статья из серии разборов задач на растворимость из сб. И.Ю.Белавина. Задачи объединены общим химизмом – это взаимодействие СО2 с раствором щелочи или средней соли. В 341 и 342 задачах СО2 входит в состав смеси продуктов сгорания, в 343 – рассматривается как индивидуальное вещество. Помимо этого, задачи объединены и общими требованиями: необходимо найти массу выпавшего осадка и состав полученного раствора. В общий алгоритм установления массы осадка входит последовательность ряда операций: нахождение общей массы искомого вещества, расчет массы воды в растворе, определение массы растворенного вещества (по растворимости), нахождение массы осадка по разности между общей массой вещества и его массой в растворе.
Итак, задача 1 (в сборнике – № 341)
341. Продукты сгорания 3,584 л (н.у.) триметиламина в избытке кислорода растворили в 51,43 мл раствора гидроксида натрия с массовой долей щелочи 0,4 и плотностью 1,4 г/мл. Определите массу осадка и состав оставшегося раствора, если известно, что растворимости гидрокарбоната натрия и карбоната натрия в этих условиях составляют 9 г и 20 г безводной соли на 100 г воды соответственно, а карбонат натрия кристаллизуется из раствора в виде десятиводного кристаллогидрата.
Решение
1.Характеристика процесса сжигания триметиламина:
а)4С3Н9N+21О2=12СО2+18Н2О + 2N2(1)
n (С3Н9N)=3,584/22,4=0,16 моль
m1 CO2=3*0,16*44 =21,12 г
m1 Н2О =4,5*0,16*18 =12,96 г
m1 N2 =0,5*0,16*28 = 2,24 г
2.Характеристика процесса растворения продуктов сгорания щелочью:
В результате поглощения продуктов реакции раствором щелочью только 2 продукта остаются в растворе: СО2 вступает в реакцию со щелочью, Н2О -смешивается с раствором. N2 удаляется из раствора, так как практически не растворяется в воде.
а)nисх(NaOH)=51,43*0,4*1,4/40=0,72 моль, n1 CO2=0,48 моль,
б)Соотношение n(NaOH):n(CO2)=0,72:0,48=1, 5:1, т.е в растворе будут протекать реакции 2 и 3:
NaOH+CO2=NaHCO3(2)
2NaOH+CO2=Na2CO3+H2O(3)
в)Пусть n2 (NaHCO3)=x , n3 (Na2CO3)=y, тогда n2(CO2)=х, n3(CO2)=у, n2+3(CO2)=х+у=0,48 моль (4)
n2(NaOH)=х, n3(NaOH)=2у, n2+3(NaOH)=х+2у=0,72 моль (5)
Составим систему из уравнений 4 и 5:
Х+у=0,48
Х+2у=0,72, откуда х=0,24 моль, у= 0,24 моль
n1 (NaHCO3)=0,24 моль , n2 (Na2CO3)=0,24 моль,
3. Состав смеси после проведения реакции:
mисх(H2O)=51,43*1,4*0,6=43,2 г(вода в составе раствора щелочи)
mкон(H2O)= mисх(H2O)+m1(H2O)+m3(H2O)=43,2+12,96+18*0,24=60,48 г
m 2NaHCO3=84*0,24=20,16 г
m 3Na2CO3=106*0,24=25,44 г
m смеси=106,08 г
4. Установим распределение Na2CO3 между осадком и раствором :
а)Пусть в составе осадка Na2CO3*10H2O- a моль Na2CO3
В составе раствора останется- в моль Na2CO3,
Тогда а+в=0,24 (6)
б)Баланс по воде:
m Н2О в кристаллогидрате Na2CO3*10H2O=18*10а=180 а
m Н2О в растворе= 106в*100/20=530 в (на основании растворимости Na2CO3)
180а+530в=60,48 (7)
в)Составим систему из уравнений 6 и 7:
а+в=0,24
180а+530в=60,48, откуда а=0,19 моль, в= 0,05 моль
г) m Н2О в растворе=530 в=26,5 г
m осадка Na2CO3*10H2O=286*а=54,34 г
m раствNa2CO3 =106*в=5,3 г
5. Установим распределение NaНCO3 между осадком и раствором
А)Найдем m раствNaHCO3:
В 100 г Н2О- 9 г NaHCO3
В 26,5 г Н2О- с г NaHCO3, откуда с = 2,385 г=m раствNaHCO3
Б)m осадка NaHCO3= m 1NaHCO3-m раствNaHCO3 =20,16-2,385=17, 775 г
6. Характеристики конечной смеси:
m осадка=mосадка Na2CO3*10H2O+m осадка NaHCO3=54,34+17,775=72,115 г
Состав раствора:
m рра= 106,08-72,115=33,965 г
W NaHCO3=100*2,385/33,965=7,02%,
W Na2CO3=100*5,3/33,965=15,6%
Задача 2 (в сборнике №342). На мой взгляд, она – самая интересная из 341-343 задач. Задачу отличают 2 особенности:
- Недостаточность количественной информации обусловливает необходимость введения количества вещества метана в исходной смеси
- Установление количеств соотношения между метаном и кислородом в исходной смеси происходит с привлечением понятия”молярная масса смеси газов”
342. Продукты сгорания смеси метана с избытком кислорода привели к нормальным условиям и получили газовую смесь, плотность которой оказалась на 25 % больше плотности исходной смеси метана с кислородом, измеренной при тех же условиях. Полученную газовую смесь пропустили через раствор с плотностью 1,2 г/мл, содержащий гидроксид натрия с массовой долей 20 % и хлорид натрия с массовой долей 15 %, объем которого был в 672 раза меньше объема исходной газовой смеси, измеренного при нормальных условиях. Определите массовые доли веществ в полученном растворе. Коэффициенты растворимости гидрокарбоната и карбоната натрия в данных условиях составляют 95 и 220 г/л(Н2О) соответственно.
Решение
1. Найдем характеристики полученной газовой смеси:
А)СН4+2О2=СО2+2Н2О (1)
После приведения к н.у. Н2О сконденсируется и в полученной смеси будут содержаться только СО2 и непрореагировавший кислород.
Пусть n(CH4)=1 моль, nисх(О2)=х моль, тогда:
состав конечной смеси: СО2- 1 моль, О2: (х-2) моль
б)Выразим М ( смесей газов):
М исх= (16+32х)/(1+х) г/моль
М кон= (44+32(х-2))/(х-1) г/моль
Соотношение молярных масс смесей газов совпадает с соотношением плотностей этих смесей,
Согласно условию: М кон=1,25 М исх, т.е Мисх=Мкон/1,25
Составим уравнение:
(16+32х)/(1+х)= (44+32(х-2))/(1,25(х-1)), откуда х=4 моль
Т.о., мольный состав исходной смеси: φ(СН4)=1/(1+4)=0,2, φ(О2)=0,8
2.Характеристика взаимодействия полученной газовой смеси с раствором, содержащим щелочь и хлорид натрия:
а)Пусть n исходной газовой смеси = 5 моль (в т.ч. 1 моль СН4), тогда V исходной смеси=5*22,4=112 л, полученная смесь: СО2- 1 моль, О2- 2 моль (67,2 л)
б) Характеристики исходного водного раствора:
Vрра= 112л/672 =0,167 л (согласно условию), m рра=167*1,2=200 г
nисх(NaOH)=200 *0,2/40=1 моль
m(NaCl)=200*0,15=30 г
в) Согласно соотношению молей СО2 и щелочи (n(CO2): n(NaOH)=1:1, в растворе будет протекать только реакция (2):
NaOH+CO2=NaHCO3(2)
n2 NaHCO3=1 моль, m2 NaHCO3=84 г
3. Найдем состав смеси после окончания в растворе всех процессов:
а)mисх(H2O)= mкон(H2O)= 200 *(1-0,2-0,15) =130 г
m NaHCO3 (рр)=95*130/1000=12,35 г (согласно растворимости)
m NaНCO3(осадок)=84-12,35=71,65 г
m конечн рра=200+44-71,65=172,35 г
m(NaCl)= 30 г
4. W(NaНCO3)=12,35*100/172,35=7,17%
W(NaCl)=30*100/172,35=17,4%
Задача 3 (343 в сборнике)- практически, типовая.
343. В 500 мл насыщенного раствора карбоната натрия с плотностью 1,15 г/мл пропустили 20,16 л оксида углерода (IV). Определите массу выпавшего из раствора гидрокарбоната натрия и массовые доли веществ в оставшемся растворе, если в данных условиях коэффициенты растворимости карбоната и гидрокарбоната натрия равны 250 и 99 г/л(Н2О) соответственно.
Решение.
1. Характеристика процесса взаимодействия рра Na2CO3 с CO2:
а)Состав насыщенного раствора:
m рра= 500*1,15=575 г, nисх Na2CO3= 575*25/(125*106)=1,085 моль (согласно растворимости)
mисх(Н2О)=575-1,085*106=460 г
б) Na2CO3+CO2+H2O=2NaHCO3 (1)
n CO2=20,16/22,4=0,9 моль (недостаток), n Na2CO3=1,085 моль (избыток)
После протекания реакции:
n1(NaHCO3)=2n СО2=1,8 моль
nостNa2CO3=1,085- n СО2=0,185 моль
mост(Н2О)=460-18* n СО2= 443,8 г
mполуч смеси=575+0,9*44=614,6 г= 1,8*84+0,185*106+443,8
3.Найдем состав оставшегося раствора:
а)m (NaHCO3)pp = 9,9*443,8/100=43,94 г (cогласно растворимости)
mосадка(NaHCO3)=1,8*84-43,94=107,26 г
б)m ост рра= 614,6-107,26=507,34 г
W(Na2CO3)=100*106*0,185/507,34=3,87%
W(NaНCO3)=100*43,94 /507,34=8,67%
Заранее благодарна за конструктивные замечания.
Продолжаю набор школьников для подготовки к ОГЭ и ЕГЭ по химии (инд. занятия, группы). Подробности – в лс https://vk.com/id363684368
Всего доброго!
Как найти массу растворенного вещества
Бывает, что возникает такая задача: как найти массу вещества, содержащегося в том или ином объеме раствора? Ход ее решения зависит от того, какими исходными данными вы располагаете. Оно может быть и очень простым, буквально в одно действие, и более сложным.

Инструкция
Например, вам надо узнать, какое количество поваренной соли содержится в 150 миллилитрах 25%-го раствора. Решение: 25%-й раствор – это значит, что в 100 миллилитрах раствора содержится 25 грамм растворенного вещества (в данном случае поваренной соли). В 150 миллилитрах, соответственно, в полтора раза больше. Произведите умножение: 25* 1,5 = 37,5. Вот и ответ: 37,5 грамм поваренной соли.
Немного видоизмените условия задачи. Предположим, вам даны те же 150 миллилитров раствора поваренной соли. Но вместо массовой концентрации известна молярная – 1 М. Сколько поваренной соли содержится в растворе в этом случае? И здесь нет ничего сложного. Прежде всего, вспомните химическую формулу поваренной соли: NaCl. Заглянув в таблицу Менделеева, уточните атомные массы (округленные) элементов, составляющих это вещество: натрия – 23, хлора – 35,5. Следовательно, молярная масса поваренной соли – 58,5 г/моль.
А что такое молярная концентрация? Это – количество молей растворенного вещества в 1 1 литре 1-молярного раствора поваренной соли содержалось бы 58,5 грамм этого вещества. Сколько же его содержится в 150 миллилитрах? Произведя умножение, получите: 58,5* 0,15 = 8,775 г. Если вам не нужна высокая точность, можно принять результат за 8,78 грамм или за 8,8 грамм.
Предположим, вам известен точный объем раствора и его плотность, но неизвестна концентрация вещества. Как в таком случае определить его количество в растворе? Тут решение займет немного больше времени, но опять-таки не вызовет затруднений. Надо лишь найти любой справочник, где есть таблицы плотностей растворов. Для каждого показателя плотности там приведены соответствующие значения его массовой и молярной концентраций.
Например: даны 200 миллилитров водного раствора вещества Х, с плотностью 1,15 г/мл. По таблице растворимости вы выяснили, что такая плотность соответствует 30%-й концентрации раствора. Сколько вещества Х находится в растворе? Решение: если в 100 миллилитрах раствора содержалось бы 30 грамм вещества Х, то в 200 миллилитрах: 30*2 = 60 грамм.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Растворимость. Произведение растворимости
Растворение
вещества в заданном количестве
растворителя происходит до состояния
насыщения.
Насыщенный раствор
–
раствор, находящийся в динамическом
равновесии с растворяющимся веществом.
Молярная концентрация растворенного
вещества в насыщенном растворе называется
растворимостью
этого вещества при данной температуре
Р(х) = См(х).
При растворении электролита, например,
соли, в раствор переходят не молекулы,
а ионы. В этом случае в насыщенном
растворе равновесие устанавливается
между солью в кристаллическом состоянии
и ионами, перешедшими в раствор:
СаСО3(кр)
=
Ca2++
СО32-.
Константа равновесия
этого процесса:
Крав.
=
[Ca2+]
•
[СО32-]/
[СаСО3(кр)]
Концентрация
СаСО3(кр)
является величиной постоянной, тогда
Крав.
• [СаСО3(кр)]
=
[Ca2+]
•
[СО32-]
=
ПР или ПР
=
(P(x))2.
ПР – называется
произведением растворимости
труднорастворимого электролита (ТРЭ).
При постоянной
температуре в насыщенном растворе
электролита произведение концентраций
ионов с учетом стехиометрических
коэффициентов в уравнении диссоциации
есть величина постоянная при. Значения
ПР для известных ТРЭ помещены в справочник.
Для
ТРЭ типа А2В3
=
2А+3
+
3В2-
выражение для произведения растворимости
имеет вид:
ПР
=
[Аа+]2
•
[Вв-]3
=
[2Р(х)]2
•
[3Р(х)]3
= 108
Р(х)5.
Исходя из значений
ПР можно количественно оценить условия
образования и растворения осадков,
рассчитать растворимость Р(х) и молярную
концентрацию ионов электролита в его
насыщенном растворе (см. таблицу ниже).
При увеличении
концентрации одного из ионов ТРЭ в его
насыщенном растворе (например, путем
введения хорошо растворимого электролита,
содержащего тот же ион) произведение
концентраций ионов электролита (ПК)
становится больше ПР. При этом равновесие
между твердой фазой и раствором смещается
в сторону образования осадка.
Условием
образования осадка является превышение
произведения концентраций ионов
малорастворимого
электролита
над его произведением растворимости,
т.е.
ПК
> ПР.
Например,
если в насыщенный раствор AgCI
добавить сильный
электролит KCI,
то
появление в растворе одноименного иона
(CI–)
приводит к смещению равновесия в сторону
образования
осадка (←).
Когда устанавится
новое равновесие, при котором произведение
концентраций ионов электролита вновь
становится равным ПР, то в растворе
появится осадок,
концентрация ионов Ag+
будет меньше, а концентрация ионов CI–
– больше, чем было до добавления KCI.
AgCI↓
<=> AgCI <=> Ag+
+ CI–
Осадок нас.р-р
раствор
Напротив, если в
насыщенном растворе электролита
уменьшить концентрацию одного из ионов
(например, связав его каким-либо другим
ионом), произведение концентраций ионов
будет меньше значения ПР, раствор станет
ненасыщенным, а равновесие между жидкой
фазой и осадком сместится в сторону
растворения осадка (→).
Условием
растворения
осадка малорастворимого электролита
является недонасыщение раствора, т.е
при условии, когда произведение
концентраций его ионов меньше значения
ПР
т.е.
ПК
< ПР.
Пример
1.
Растворимость Аg3РО4
в воде при
20°C равна
0.0065 г/л.
Рассчитайте значение ПР (Аg3РО4).
Решение.
Растворимость Аg3РО4
или молярная концентрация соли в
насыщенном
растворе, равна:
т
(Аg3РО4)
0.0065
Р
(Аg3РО4)
= ——————————— = ——————
=
l,6
•l0-5
моль/л
М
(Аg3РО4)
• V(z)
418,58 • 1
Диссоциации
фосфата серебра идет по уравнению:
Аg3РО4
=
3Ag+
+
РО43–.
Видно,
что из
1
моля соли образуется
3
моля ионов
Ag+
и
1
моль ионов
Р043–,
поэтому [Р043–]
=
P(x), a [Ag+]
=
3Р(х).
Отсюда находим ПР:
ПР
=
[Ag+]3
•
[РО43–]
=
(3Р)3
•
Р
= (4,8 •10-5)
3
•l,6•10–5
=
1,77
•10–18.
Пример
2.
Произведение растворимости йодида
свинца при 20°С равно
8•10–9.
Вычислить
растворимость соли (в моль/л и в г/л) при
указанной
температуре.
Решение.
Обозначим искомую растворимость через
Р
(моль/л). Тогда в насыщенном растворе
РbI2
содержится
Р
моль/л ионов Рb2+
и
2Р
моль/ л ионов
I–.Отсюда
ПР(РbI2)
=
[Рb2+]
[I–]2
= Р(2Р)2
=
4 Р3
и
Р
= (
ПР(РbI2)/4
)1/3
=
(
8
•
10-9/
4)1/3
= 1,3
10-3
моль/л.
Молярная
масса РbI2
равна
461
г/моль, поэтому растворимость РbI2,
выраженная в г/л, составит 1,3
10-3
моль/ л • 461 г/ моль = 0,6
г/л.
Пример
3.
Во сколько раз растворимость оксалата
кальция СаС2О4
в
0,1
М
растворе оксалата аммония
(NH4)2С2О4
меньше, чем в воде? Диссоциацию оксалата
аммония на ионы считать полной.
Решение.
Вычислим сначала растворимость оксалата
кальция в воде. Обозначив концентрацию
соли в насыщенном растворе через
Р
(моль/ л), можем записать:
ПР(СаС2О4)
=
[Са2+]
[С2О42-]
= Р2
.
Отсюда,
используя значение ПР(СаС2О4)=
2 10-9,
Р
=
(ПР(СаС2О4)1/2
=
( 2
10-9
)1/2
=
4,5 •
10-5
моль/л.
Теперь
найдем растворимость той же соли в
0,1
М раствора (NH4)2С2О4;
обозначим ее через
Р‘.
Концентрация ионов Са2+
в насыщенном растворе тоже будет равна
Р’,
а концентрация ионов С2О42-составит
(0,1 + Р’).
Поскольку
Р‘<<0,1,
то
величиной
Р’
по сравнению с
0,1М
можно пренебречь и считать, что [С2О42-]
= 0,1
моль/л. Тогда можно записать:
ПР(СаС2О4)
= 2
•10-9
= Р’
•
0,1
и
Р’
= 2 •
10-9/
0,1
=
2 •
10-8
моль/л.
Таким
образом, в присутствии (NH4)2С2О4
растворимость СаС2О4
уменьшилась в
4,5•10-5
/
(2•10-8)
раз,т. е. приблизительно в
2200
раз.
Пример
4.
Смешаны равные объемы
0,01
М. растворов хлорида кальция и сульфата
натрия. Образуется ли осадок сульфата
кальция?
Решение.
Найдем произведение концентраций ионов
Са2+
и
SO42-
и сравним его с произведением растворимости
сульфата кальция. Исходные молярные
концентрации растворов
CaCl2
и
Na2S04
одинаковы и равны
0,01
моль/л. Поскольку при смешении исходных
растворов общий объем раствора вдвое
возрастет, то концентрации ионов [Са2+]
и
[SО42-]
вдвое уменьшатся по сравнению с исходными.
Таким
образом, [Са2+]
=
[SО42-]
=
0,005 = 5 •
10–3
моль/л.
Находим
произведение концентраций ионов ПК
= [Са2+]
[SО42-]
=
(5 •
10–3)2
= 2,5 •
10–5.
ПР(CaSO4)
=
1,3•10–4.
Найденное значение произведения
концентрации ионов меньше этой величины;
следовательно, раствор
будет
ненасыщенным относительно сульфата
кальция, и осадок не образуется.
Для решения
задач на ПР , ПК, растворимость можно
воспользоваться таблицей, приведенной
ниже.
|
Параметры го раствора |
Тип электролита |
|||
|
АВ |
А2В |
А3В |
А2В32А+3В |
|
|
См (эл-та), моль/л |
Р |
Р |
Р |
Р |
|
См (А), моль/л |
Р |
2 Р |
3 Р |
2 Р |
|
См (В), моль/л |
Р |
Р |
Р |
3 Р |
|
Масса эл-та, г/л |
М(АВ) Р |
М(А2В) |
М(А3В) |
М(А2В3) |
|
Масса (А)эл-та, |
М(А) Р |
2М(А) Р |
3М(А) Р |
2М(А) Р |
|
Масса (В), г/л |
М(В) Р |
М(В) Р |
М(В) Р |
3М(В) Р |
|
ПР электролита |
Из справочника |
Из справочника |
Из справочника |
Из справочника |
|
ПР электролита |
Р2 |
4Р3 |
27Р4 |
108Р5 |
|
Р |
(ПР)1/2 |
(ПР/4)1/3 |
(ПР/27)1/4 |
(ПР/108)1/5 |
ЗАДАЧИ
-
Вычислить
произведение растворимости РbВr2
при 25°С,
если
растворимость соли при этой температуре
равна 1,32
•
10-2
моль/л. -
В
500
мл воды при 18°С растворяется
0,0166
г
Ag2CrО4
.Чему
равно произведение растворимости этой
соли? -
Для
растворения
1,16
г РbI2
потребовалось
2
л воды. Найти
произведение
растворимости соли. -
Исходя
из произведения растворимости карбоната
кальция,
найти
массу СаСО3,
которая содержится в
100
мл его насыщенного
раствора. -
Вычислить
объем воды, необходимый для растворения
при
25°С
1
г
BaSО4. -
Рассчитайте
молярную концентрацию ионов свинца
(Pb2+)
в
насыщенном
растворе иодида свинца. ПР
(PbJ2)
= 10-8. -
Рассчитайте
ПР соли
NiC2O4,
если в
100
мл насыщенного раствора этой соли
содержится
0,001174
г ионов никеля. -
Для
растворения
0,72
г карбоната кальция потребовалось
15
л
воды.
Вычислите ПР карбоната кальция, считая,
что объем раствора равен
объему
растворителя. -
Рассчитайте,
в каком объеме насыщенного раствора
хлорида
свинца
(II)
содержится
0,1
г ионов свинца, ПР
(PbCl2)
= l,6•10-5. -
Рассчитайте
массу кальция в виде ионов Са+2
которая находится
в
500
мл насыщенного раствора сульфата
кальция, ПР (СаSО4)
= 1,3 •
10-4. -
Рассчитайте
массу кальция в виде ионов Са+2
которая находится
в
500
мл насыщенного раствора сульфата
кальция, ПР (СаSО4)
= 1,3 •
10-4. -
Сколько
литров воды потребуется для растворения
0,1
г хлорида
серебра
для получения насыщенного раствора,
ПР
(AgCl) = 1
•
10–10
. -
Выпадет
ли осадок сульфата кальция, если к
200
мл
0,002
молярного раствора хлорида кальция
добавить
2000
мл
0,00001
молярного
раствора
сульфата калия, ПР(СаSО4)
=
10–4. -
14.
Рассчитайте, в каком объеме насыщенного
раствора содержится
0.1
г иодида серебра,
ПP(AgI)=8,3•10-17. -
15.В
насыщенном растворе хромата серебра
молярная концентрация
иона
СrО-2
равна
0.0001
моль/л. Рассчитайте ПР хромата серебра
и молярную концентрацию иона серебра
в этом растворе.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #