Металлы в природе
Большая часть металлов присутствует в природе в виде руды и различных соединений: оксидов, сульфидов, карбонатов и т.д.
В малых количествах металлы присутствуют в морской воде, растениях, живых организмах, играя при этом важную роль. Известно, что организм человека на 3% состоит из металлов. Большая часть приходится на кальций (в костях) и натрий, выступающего в роли электролита в межклеточной жидкости и цитоплазме. В мышцах и нервной системе накапливается магний, в печени — медь, в крови — железо.
Добыча и обогащение
Металлы извлекают из земли в процессе добычи полезных ископаемых. Добытые руды служат относительно богатым источником необходимых элементов. Для выяснения нахождения руд в земной коре используются специальные поисковые методы, включающие разведку и исследование рудных месторождений. Месторождения руд разрабатываются открытым или карьерным способом и подземным или шахтным способом. Иногда применяется комбинированный (открыто-подземный) способ разработки рудных месторождений.
Для получения чистых металлов и дальнейшего их применения необходимо выделить их из руд и провести очистку. При необходимости проводят легирование и другую обработку металлов. Изучением этого занимается наука металлургия. Металлургия различает руды чёрных металлов (на основе железа) и цветных (в их состав не входит железо, всего около 70 элементов). Золото, серебро и платина относятся также к драгоценным (благородным) металлам.
После извлечения руд они, как правило, подвергаются обогащению. Основные процессы обогащения предназначены для выделения из исходного минерального сырья одного или нескольких полезных компонентов. Исходный материал в процессе обогащения разделяется на соответствующие продукты — концентрат(ы), промпродукты и отвальные хвосты. В процессах обогащения используют отличия минералов полезного компонента и пустой породы в плотности, магнитной восприимчивости, смачиваемости, электропроводности, крупности, форме зёрен, химических свойствах и др.
Из добытой и обогащённой руды металлы извлекаются, как правило, с помощью химического или электролитического восстановления. В пирометаллургии для преобразования руды в металлическое сырьё используются высокие температуры, в гидрометаллургии применяют для тех же целей водную химию. Используемые методы зависят от вида металла и типа загрязнения.
Когда металлическая руда является ионным соединением металла и неметалла, для извлечения чистого металла она обычно подвергается выплавлению — нагреву с восстановителем. Многие распространенные металлы, такие, как железо, плавят с использованием в качестве восстановителя углерода. Некоторые металлы, такие как алюминий и натрий, не имеют ни одного экономически оправданного восстановителя и извлекаются с применением электролиза.
Сульфидные руды не улучшаются непосредственно до получения чистого металла, но обжигаются на воздухе, с целью преобразования их в окислы.
Подготовил Евгений Лавриненко (СМ)
Получение
металлов. Нахождение их в природе
Ребята, сегодня мы
побываем с вами в местах, где получают металлы, а также узнаем, где же
встречаются металлы.
Ну что ж, начинаем
путешествие. Металлы встречаются в природе в свободном состоянии, их называют самородными
металлами, так и в виде соединений.
В самородном
состоянии в природе встречаются золото, серебро, медь, платина и ртуть.
Эти металлы обычно содержатся в небольших количествах в виде зёрен или
вкраплений в горных породах. Изредка встречаются и довольно крупные куски
металлов – самородки. Одним из самых больших месторождений чистого
серебра был так называемый «серебряный тротуар» в Канаде. Он
представлял собой глыбу почти чистого серебра длиной тридцать м, уходящую
в землю на восемнадцать м. Выработка этого месторождения дала около
двадцать т металла. А один из крупнейших самородков серебра весил почти сто
девять кг. Самый крупный самородок меди весил четыреста двадцать т, а золота –
сто двенадцать кг.
А вот распространённость
химических элементов металлов в земной коре различна. К наиболее распространённым
металлам относятся алюминий (7,45%), железо (4,20%), кальций (3,25%),
натрий (2,40%), калий (2,35%) и магний (2,35%). Содержание других металлов в
земной коре может составлять тысячные доли процента и ниже.
Некоторые историки
считают, что упадок Римской империи был обусловлен массовым отравлением
свинцом. Известно, что водопроводы Древнего Рима были из свинца.
В свинцовых чанах хранили воду и вино. Попадая в человеческий организм, свинец
вызывает поражение центральной нервной системы, приводит к изменению состава
крови.
Многие металлы являются
элементами, необходимыми для функционирования живых организмов. На долю
ионов Na+,
K+,
Mg2+,
Ca2+
в организме человека приходится 99% всех ионов металлов.
К биологически наиболее
значимым металлам относятся: K,
Na, Mg,
Ca, Fe,
Cu, Co,
Mn, Zn,
Mo.
В земной коре металлы
чаще всего встречаются в виде соединений: таких, как оксиды, силикаты,
карбонаты, сульфиды и хлориды. Эти соединения входят в состав руд и
минералов.
Рудой называют горную
породу, получение из которой чистого металла экономически выгодно.
В состав руды входят минералы и примеси в виде пустой породы. А минералы –
это природные тела, имеющие определённый химический состав. Давайте с
вами посмотрим названия и химический состав некоторых минералов.
|
Название |
Химический состав |
|
Красный железняк |
Fe2O3 |
|
Магнитный железняк |
Fe3O4 |
|
Бурый железняк |
2Fe2O3 |
|
Железный колчедан |
FeS2 |
|
Сильвин |
KCl |
|
Криолит |
Na3AlF6 |
|
Кальцит |
CaCO3 |
|
Корунд |
Al2O3 |
|
Малахит |
(CuOH)2CO3 |
|
Медный колчедан |
CuFeS2 |
|
Киноварь |
HgS |
|
Гипс |
CaSO4 |
|
Свинцовый блеск |
PbS |
|
Цинковая обманка |
ZnS |
К наиболее известным
минералам относится пирит, или железный колчедан (FeS2),
киноварь (HgS), малахит
((CuOH)2CO3).
Пирит и киноварь используют в промышленности для получения соответствующих
металлов, то есть железа и ртути, а малахит, как поделочный камень.
А теперь представьте,
что на дне водоёмов тоже есть соединения металлов, эти отложения – конкреции
– представляют собой грозди, клубни или лепёшки, густо усеивающие дно.
Плоские озёрные и болотные конкреции величиной с мелкую монету были известны
ещё в средние века, поэтому их и называли «копеечной рудой». В настоящее
время железомарганцевые конкреции, покрывающие огромные площади на дне океанов,
называют полезными ископаемыми XXI
века.
Это богатейший источник не только железа и марганца, но и кобальта, никеля,
меди и молибдена.
Представьте себя геологом
или минералогом, как же это увлекательно. Для этого сравним такие
минералы, как красный, бурый и магнитный железняк.
Цвет красного
железняка коричнево-красный, сам он прочный, плотный, если
провести образцом руды по поверхности фарфоровой ступки, то он оставляет
красно-коричневый след, не притягивается магнитом.
Бурый
железяк имеет жёлто-коричневую окраску,
сам прочный и плотный, не притягивается магнитом, оставляет на
фарфоровой ступки жёлто-бурую полосу.
Магнитный железняк
чёрного цвета, сам прочный и плотный,
притягивается магнитом, оставляет чёрный цвет черты на поверхности
фарфоровой ступки, имеет металлический блеск.
Здорово, получается, что минералы отличаются между собой окраской,
магнитными свойствами, цветом черты и некоторыми другими показателями.
В современной технике
широко используют более 75 металлов и многочисленные сплавы на их основе.
Поэтому большое значение придаётся промышленным способам получения металлов из
руд. Обычно перед получением металлов из руды её измельчают, потом
предварительно обогащают – отделяют пустую породу, примеси. В результате
образуется концентрат, служащий сырьём для металлургического производства.
Затем обогащённую руду превращают в оксид и только после этого восстанавливают
металл.
Металлургия – это наука
о методах и процессах производства металлов из руд и других металлосодержащих
продуктов, о получении сплавов и обработке металлов.
В зависимости от метода получения металла из руды (концентрата) существует
несколько видов металлургических производств.
Представьте, что из одной
т медной руды можно получить шестнадцать кг концентрата и только четыре
кг чистой меди.
Такая отрасль
металлургии, как пирометаллургия занимается переработкой руд, она
основана на химических реакциях, при чём они проходят при высоких
температурах, ведь от греч. пирос, означает огонь.
Пирометаллургические
процессы включают обжиг и плавку.
При обжиге сульфиды
переводят в оксиды, а сера удаляется в виде оксида серы
(IV).
А затем из оксида восстанавливают металл. Полученный металл или сплав
подвергают механической обработке, придают ему соответствующую форму. В
процессе выделения металлов (плавке) из оксидов в качестве
восстановителей используют углерод, оксид углерода (II),
водород, кремний или более активные металлы.
Например, ещё древние металлурги
для получения железа из его руд использовали в качестве восстановителя
углерод. Но этот способ неудобен тем, что реакция между твёрдыми
веществами идёт только в местах их соприкосновения.
2Fe2O3
+ 3C = 4Fe
+ 3CO2
В промышленных
масштабах для получения железа, цинка и других цветных
металлов из оксидов используют в качестве восстановителя оксид углерода (II).
Fe2O3
+ 3CO = 2Fe
+ 3CO2
Сейчас мы посмотрим,
как получают чугун и сталь. Восстановление железа проводят в специальных
вертикальных печах, называемых доменными, высотой до нескольких десятков
метров и внутренним объёмом до 5000 м3. Они имеют стальной корпус, а
изнутри выложены огнеупорным кирпичом. По характеру своей работы доменная печь
– аппарат непрерывного действия. Сверху в печь подаётся твёрдое сырьё
– шихта, представляющая собой смесь железной руды, кокса
(переработанного угля), известняка и других добавок, а снизу вдувается
подогретый или обогащённый кислородом воздух. В нижней части печи кокс сгорает
в горячем воздухе, образуя углекислый газ.
C
+ O2
= CO2
доменная
печь
Углекислый газ
поднимается вверх в печи и взаимодействует с новыми порциями раскалённого кокса
с образованием оксида
углерода (II).
CO2
+ C = 2CO
В результате реакций СО
с оксидом железа (III) образуется
железо.
В доменном процессе
получается железо с относительно большим (более 2%) содержанием углерода –
чугун.
Чугун превращают в
сталь, удаляя избыточный углерод путём окисления кислородом воздуха в
специальных установках – мартеновский печах, конвертерах или электропечах.
Конвертер
Для получения некоторых
металлов в качестве восстановителя используют водород.
WO3
+ 3H2
= W + 3H2O
В роли
восстановителей можно также использовать более активные металлы, способные
вытеснять другие металлы из их оксидов и солей. Этот способ получения
металлов называется металлотермией. Если используют алюминий, то говорят об алюминотермии:
Fe2O3
+ 2Al = 2Fe
+ Al2O3
Восстановление железа
методом алюминотермии до сих пор применяется при сварке рельсов.
Этот метод получения металлов был предложен русским учёным
Н.Н.
Бекетовым.
Гидрометаллургия – это
методы получения металлов, основанные на химических реакциях, происходящих в
растворе. Гидрометаллургические процессы включают стадию
перевода нерастворимых соединений металлов из руд в растворы, с последующим восстановительным
выделением металлов из полученных растворов с помощью других металлов или
электрического тока.
Электрометаллургия –
методы получения металлов, основанные на электролизе, т.е. выделение металлов
из растворов или расплавов их соединений с помощью постоянного электрического
тока. Этот метод применяют для получения активных
металлов – щелочных и щелочноземельных, алюминия, также для получения
легированных сталей. С помощью этого метода, английский химик Г. Дэви
впервые получил калий, натрий, барий и кальций.
Большое значение имеет микробиологический
метод получения металлов. В этом методе используется жизнедеятельность
некоторых бактерий. Так, тионовые бактерии способны переводить
нерастворимые сульфиды в растворимые сульфаты. Бактериальный метод применяют
для извлечения меди из её сульфидных руд. А затем полученный раствор сульфата
меди (II) подаётся на
гидрометаллургическую переработку. Кроме этого, учёные обнаружили, что
некоторые микроводоросли и бактерии накапливают на своей поверхности
отдельные металлы (например, золото) или их оксиды. Микроорганизм постепенно
обрастает «шубой» из минеральных частиц, увеличивается в размерах в десятки
раз, что позволяет легко выделить частицы из раствора.
При промышленном
производстве металлов большое значение имеют вопросы охраны окружающей среды
от загрязнений отходами производства. Охрана окружающей среды предусматривает,
прежде всего, дезактивацию выбросов, например отходящих газов при
выплавке чугуна. Здесь главную опасность представляет образующийся при
переработке сернистых руд оксид серы (IV),
который, попадая в атмосферу, может вызывать «кислотные дожди». Наряду с
комплексным использованием сырья, строительством очистных сооружений,
устройством замкнутых циклов водопользования с целью охраны окружающей среды
необходимы вывод промышленных предприятий за городскую черту, создание
лесозащитных вокруг городов и промышленных центров.
Таким образом, металлы
встречаются в природе в виде соединений или в самородном состоянии. В земной
коре металлы чаще всего встречаются в виде соединений: оксидов, силикатов,
карбонатов, сульфидов, хлоридов. Эти соединения входят в состав руд и
минералов. Для получения металлов из руд руду сначала измельчают,
обогащают, переводят в оксид и только после этого восстанавливают металл. В
качестве восстановителей используют C,
CO, H2,
Si или более
активные металлы. Металлургия занимается получением металлов и их сплавов из
руд. В зависимости от метода получения металла из руды существует несколько
видов металлургических производств: пирометаллургия, гидрометаллургия и
электрометаллургия.
Содержание
- Добыча металлов: прошлое, настоящее, будущее
- Понятие о металлургии: общие способы получения металлов
- 1. Нахождение металлов в природе
- 2. Получение активных металлов
- 3. Получение малоактивных и неактивных металлов
- 3.1. Обжиг сульфидов
- 3.2. Восстановление металлов углем
- 3.3. Восстановление металлов угарным газом
- 3.4. Восстановление металлов более активными металлами
- 3.5. Восстановление металлов из оксидов водородом
- 4. Производство чугуна
- Добавить комментарий Отменить ответ
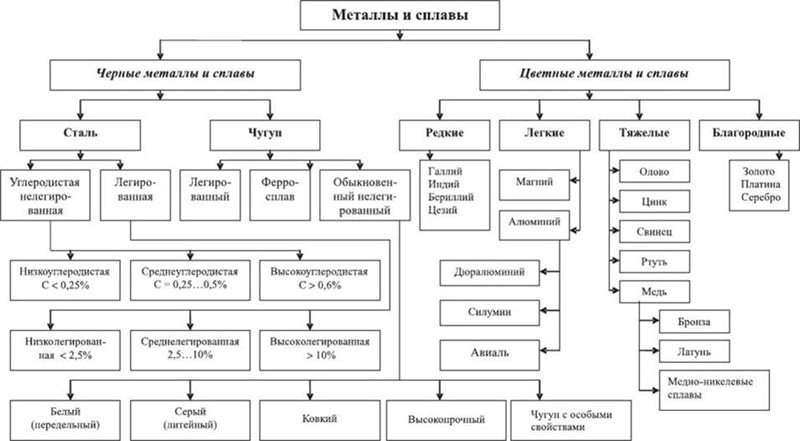
Все металлы состоят из частиц и делятся на черные и цветные. Они различаются не только по цвету, но и по составу частиц, которые определяют их химические свойства. Например, черные металлы являются более прочными и твердыми, цветные, напротив, более пластичны и податливы. Отличаются металлы и по тому, как их добывают и обрабатывают, и как их в дальнейшем используют.
Черные и цветные
Черные металлы – это железо и его сплавы. Черные металлы используются в промышленности гораздо больше, чем цветные. Из них изготавливают чугун и сталь, причем, для производства используются различные составы сплавов железа и углерода.
Цветные металлы – медь, алюминий, никель, свинец, и др., то есть все нежелезные металлы. Они более трудоемки по добыче, их меньше в целом в природе, используются они также более точечно. К примеру, добавляются к некоторым железным сплавам, для повышения стойкости производимой из них продукции.
Цветные металлы, в свою очередь, делятся на легкие и тяжелые. При этом производство тяжелых металлов требует больше затрат энергии, чем легких.
Легкие металлы – это, например, титан, алюминий, магний. Металлы очень ценные, к примеру, легкий алюминий – один из ключевых материалов для проводников, а из тугоплавких титановых сплавов производят детали и двигатели самых современных самолетов и химическое оборудование. Тяжелые металлы – медь, олово, никель, свинец, цинк. Стойкий к действию воздуха и воды никель позволяет увеличить прочность, износостойкость, коррозионную стойкость, повышает тепло- и электропроводность, улучшает магнитные и каталитические свойства, его используют практически во всех отраслях промышленности. А, скажем, из долговечного и прочного свинца изготавливают батареи и аккумуляторы. Есть также так называемые малые тяжелые металлы – ртуть, кадмий, кобальт – и легирующие – молибден, вольфрам, кремний. Легирование — это их введение в состав сталей и сплавов для придания сплавам необходимых физических, химических или механических свойств. Например, молибден повышает прокаливаемость стали.
Россия является лидером по запасам железной руды, в нашей стране огромное количество месторождений руды – например, Курская аномалия, Карельское и Костомукшское месторождения, гора Магнитная (Челябинская область), Кузбасс, Красноярский край, и др. На этих территориях, в основном, добывают ископаемые для развития черной металлургии, в данных регионах базируются металлургические предприятия черных металлургов.
Ископаемые для цветной металлургии добывают преимущественно на Урале, Северном Кавказе, в Западной и Восточной Сибири, на Дальнем Востоке. Базы по переработке «цветных» ископаемых находятся чаще всего рядом с каждым месторождением.
Ранее руды добывались исключительно путем проведения подземных горных работ, сегодня для того, чтобы их найти, используются несколько способов добычи, в том числе, шахтовый, его еще называют подземным, и открытый, или так называемый карьерный. Некоторые предприятия используют комбинированный подход.
Карьерные работы ведутся прямо на поверхности земли – с помощью экскаваторов, то есть под открытым небом. Сначала горные породы готовят к выемке – проводят вскрышные работы, отделяют эти породы от массивов, рыхлят, затем происходит непосредственно процесс добычи. Если руды надо получить из скал, производят бурильно-взрывные работы. После того, как руда получена, ее транспортируют, а «отработанную» землю рекультивируют.
Подземные работы проводятся в недрах земли, в шахтах. При применении подземного подхода месторождение сначала вскрывают, затем готовят ископаемые к выемке, затем добывают их – валовым или селективным методом (когда ископаемые сразу отделяют друг от друга).
Безусловно, сегодня, помимо людских ресурсов и тяжелой бурильной техники, для добычи руд используется современное оборудование и компьютерные технологии, которые позволяют максимально эффективно планировать и проектировать все работы по добыче ископаемых.
Как получается металл
Чтобы получился тот или иной металл, нужен различный тип руды. Можно выделить, например, руды:
• медная. Руда, позволяющая произвести черновую и рафинированную медь, а также редкие металлы, если в руде есть их примеси, серную кислоту, и др.;
• оловянная;
• медно-никелевая;
• железная. Из это руды сегодня добывается не только железо, но и другие металлы, так как в ней могут содержатся их примеси;
• свинцово-цинковая;
• вольфрамо-молибденовая – очень ценная руда, дающая возможность создавать вольфрамовые и молибденовые концентраты;
• сурьмяно-ртутная;
• золотосодержащая. Из такой руды можно получать редкие металлов и полупроводниковые материалы, а также интерметаллические соединения из них.
Это далеко не все виды руд в природе.
При этом, цветные металлы получают из обогащенной руды – так называемого рудного концентрата. В цветной металлургии есть термин «обогащение», который означает искусственное повышение содержания металлов в сырье. По сути, это способ разделения образований на металлы и минералы. Именно обогащение и позволяет повысить содержание нужного, ценного металла в разы! Для этого используются различные технологии – руду дробят, измельчают, сортируют, перерабатывают путем обезвоживания, и др. Когда металл получен из руды, далее он обрабатывается и шлифуется.
Все процессы с ископаемыми и металлами производятся на металлургических комбинатах, как правило, в различных по специализации цехах. Например, есть основные заводы, а также филиалы, которые непосредственно занимаются обработкой металлов или их прессованием. Есть также цеха, которые проверяют металл на прочность, испытывают его характеристики – растяжение, пластичность, и др.
После всех этих действий и проверок металл отправляется в другие цеха или на другие предприятия для того, чтобы из него изготавливалась продукция – трубы, станки, машины, и многое другое.
Прошлое vs настоящее
Несмотря на то, что сегодня технологии шагнули вперед, шахтовый способ руды по-прежнему остается ключевым способом нахождения ископаемых. В то же время, на металлургических предприятиях все большее распространение получают ИТ-решения, позволяющие спроектировать процесс перед тем, как провести непосредственно добывающую работу.
Карьерный способ чаще всего применяется при разработке золотых, платиновых, оловянных, вольфрамовых и других месторождений, а подземный используют для добычи глубоко залегающих руд – вплоть до глубины 1700 м. Причем для разработки небольших месторождения иногда достаточно одной шахты, в крупных же функционирует целая система шахт (до 100-150).
При этом сегодня признано, что открытый способ имеет преимущества — лучшие санитарно-гигиенические условия труда, применение более технологичного оборудования, а в результате – более эффективный бизнес-результат. По подсчетам экспертов, при открытом способе добычи ископаемых производительность труда рабочих в 5 раз выше, чем в шахте, а себестоимость добытой руды в 3 раза ниже.
Также российские предприятия часто применяют смешанный способ, в котором проводятся и подземные (шахтовые) работы, и карьерные. ИТ-технологии позволяют просчитать, где лучше применить то или иное оборудование, что позволяет металлургам экономить там, где можно обойтись без шахтовой добычи ископаемых.
Источник
Понятие о металлургии: общие способы получения металлов
Металлургия — это наука о промышленных способах получения металлов. Различают черную и цветную металлургию.
Черная металлургия — это производство железа и его сплавов (сталь, чугун и др.).
Цветная металлургия — производство остальных металлов и их сплавов.
Широкое применение находят сплавы металлов. Наиболее распространенные сплавы железа — чугун и сталь.
Чугун — это сплав железа, в котором содержится 2-4 масс. % углерода, а также кремний, марганец и небольшие количества серы и фосфора.
Сталь — это сплав железа, в котором содержится 0,3-2 масс. % углерода и небольшие примеси других элементов.
Легированные стали — это сплавы железа с хромом, никелем, марганцем, кобальтом, ванадием, титаном и другими металлами. Добавление металлов придает стали дополнительные свойства. Так, добавление хрома придает сплаву прочность, а добавление никеля придает стали пластичность.
Основные стадии металлургических процессов:
- Обогащение природной руды (очистка, удаление примесей)
- Получение металла или его сплава.
- Механическая обработка металла
Большинство металлов встречаются в природе в виде соединений. Наиболее распространенный металл в земной коре — алюминий. Затем железо, кальций, натрий и другие металлы.
| Нахождение металлов в природе | ||
| Активные металлы — в виде солей | Металлов средней активности — в виде оксидов и сульфидов | Малоактивные металлы -в виде простых веществ |
| Хлорид натрия NaCl
Активные металлы (щелочные и щелочноземельные) классическими «химическими» методами получить из соединений нельзя. Такие металлы в виде ионов — очень слабые окислители, а в простом виде — очень сильные восстановители, поэтому их очень сложно восстановить из катионов в простые вещества. Чем активнее металл, тем сложнее его получить в чистом виде — ведь он стремится прореагировать с другими веществами. Получить такие металлы можно, как правило, электролизом расплавов солей, либо вытеснением из солей другими металлами в жестких условиях. Натрий в промышленности получают электролизом расплава хлорида натрия с добавками хлорида кальция: 2NaCl = 2Na + Cl2 Калий получают пропусканием паров натрия через расплав хлорида калия при 800°С: KCl + Na = K↑ + NaCl Литий можно получить электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси): 2LiCl = 2Li + Cl2 Цезий можно получить нагреванием смеси хлорида цезия и специально подготовленного кальция: Са + 2CsCl = 2Cs + CaCl2 Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С: Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция: Барий получают из оксида восстановлением алюминием в вакууме при 1200 °C: 4BaO+ 2Al = 3Ba + Ba(AlO2)2 Алюминий получают электролизом раствора оксида алюминия Al2O3 в криолите Na3AlF6: Металлы малоактивные и неактивные восстанавливают из оксидов углем, оксидом углерода (II) СО или более активным металлом. Сульфиды металлов сначала обжигают. 3.1. Обжиг сульфидовПри обжиге сульфидов металлов образуются оксиды: 2ZnS + 3O2 → 2ZnO + 2SO2 Металлы получают дальнейшим восстановлением оксидов. Чистые металлы можно получить восстановлением из оксидов углем. При этом до металлов восстанавливаются только оксиды металлов, расположенных в ряду электрохимической активности после алюминия. Например , железо получают восстановлением из оксида углем: 2Fe2O3 + 6C → 2Fe + 6CO ZnO + C → Zn + CO Оксиды металлов, расположенных в ряду электрохимической активности до алюминия, реагируют с углем с образованием карбидов металлов: CaO + 3C → CaC2 + CO Оксид углерода (II) реагирует с оксидами металлов, расположенных в ряду электрохимической активности после алюминия. Например , железо можно получить восстановлением из оксида с помощью угарного газа: Более активные металлы вытесняют из оксидов менее активные. Активность металлов можно примерно оценить по электрохимическому ряду металлов: Восстановление металлов из оксидов другими металлами — распространенный способ получения металлов. Часто для восстановления металлов применяют алюминий и магний. А вот щелочные металлы для этого не очень подходят – они слишком химически активны, что создает сложности при работе с ними. Алюмотермия – это восстановление металлов из оксидов алюминием. Например : алюминий восстанавливает оксид меди (II) из оксида: 3CuO + 2Al = Al2O3 + 3Cu Магниетермия – это восстановление металлов из оксидов магнием. CuO + Mg = Cu + MgO Железо можно вытеснить из оксида с помощью алюминия: При алюмотермии образуется очень чистый, свободный от примесей углерода металл. Активные металлы вытесняют менее активные из растворов их солей. Например , при добавлении меди (Cu) в раствор соли менее активного металла – серебра (AgNO3) произойдет химическая реакция: 2AgNO3 + Cu = Cu(NO3)2 + 2Ag Медь покроется белыми кристаллами серебра. При добавлении железа (Fe) в раствор соли меди (CuSO4) на железном гвозде появился розовый налет металлической меди: CuSO4 + Fe = FeSO4 + Cu При добавлении цинка в раствор нитрата свинца (II) на цинке образуется слой металлического свинца: Водород восстанавливает из оксидов только металлы, расположенные в ряду активности правее алюминия. Как правило, взаимодействие оксидов металлов с водородом протекает в жестких условиях – под давлением или при нагревании. CuO + H2 = Cu + H2O 4. Производство чугунаЧугун получают из железной руды в доменных печах. Печь последовательно загружают сверху шихтой, флюсами, коксом, затем снова рудой, коксом и т.д. 1- загрузочное устройство, 2 — колошник, 3 — шахта, 4 — распар, 5 — горн, 6 — регенератор Доменная печь имеет форму двух усеченных конусов, соединенных основаниями. Верхняя часть доменной печи — колошник, средняя — шахта, а нижняя часть — распар. В нижней части печи находится горн. Внизу горна скапливается чугун и шлак и отверстия, через которые чугун и шлак покидают горн: чугун через нижнее, а шлак через верхнее. Наверху печи расположено автоматическое загрузочное устройство. Оно состоит из двух воронок, соединенных друг с другом. Руда и кокс сначала поступают в верхнюю воронку, а затем в нижнюю. Из нижней воронки руда и кокс поступают в печь. во время загрузки руды и кокса печь остается закрытой, поэтому газы не попадают в атмосферу, а попадают в регенераторы. В регенераторах печной газ сгорает. Шихта — это железная руда, смешанная с флюсами. Снизу в печь вдувают нагретый воздух, обогащенный кислородом, кокс сгорает: Образующийся углекислый газ поднимается вверх и окисляет кокс до оксида углерода (II): CO2 + С = 2CO Оксид углерода (II) (угарный газ) — это основной восстановитель железа из оксидов в данных процессах. Последовательность восстановления железа из оксида железа (III): Последовательность восстановления оксида железа (III): FeO + CO → Fe + CO2 Суммарное уравнение протекающих процессов: При этом протекает также частичное восстановление примесей оксидов других элементов (кремния, марганца и др.). Эти вещества растворяются в жидком железе. Чтобы удалить из железной руды тугоплавкие примеси (оксид кремния (IV) и др.). Для их удаления используют флюсы и плавни (как правило, известняк CaCO3 или доломит CaCO3·MgCO3). Флюсы разлагаются при нагревании: и образуют с тугоплавкими примесями легкоплавкие вещества (шлаки), которые легко можно удалить из реакционной смеси: CaO + SiO2 → CaSiO3 Добавить комментарий Отменить ответЭтот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев. Источник Adblock |
Мета́лл (в переводе с латыни означает шахта) составляет определенную категорию элементов, обладающих свойствами металлов в отличие от группы неметаллов. Около 80% процентов существующих элементов являются металлами. Алюминий является самым распространенным в земной коре. Характерной чертой является наличие особого блеска, который позволяет отличить металл от каменной породы.
На сегодняшний день насчитывается около 118 химических элементов, но не каждый завоевал официальное признание. Открытые металлы условно подразделяют на следующие элементы:
- к щелочной категории 6;
- к щелочноземельным 6;
- к переходным 38;
- к легким 11;
- полуметаллы 7;
- лантан и лантаноиды 14;
- актиноиды 14;
- бериллий и магний не относятся ни к одной категории.
Соответственно, можно сделать вывод, что из всех существующих веществ 96 можно отнести к металлам. Если рассматривать с точки зрения астрофизики, то это химические элементы, вес которых больше гелия.
Происхождение слова металл
Существует три основных теории, которые раскрывают тайну происхождения слова металл:
- в старорусский период слово было заимствовано из немецкого языка. В немецком языке слово появилось из латыни, что в переводе на русский означает рудник или металл. Латинское слово было заимствовано с греческого языка (греч metallum);
- с греческого слово означает добываю из земли. Изначально толкование предполагало природные рудники и копьи;
- в немецком языке слово появилось в переводе с латыни рудник.
Небольшая историческая справка
Впервые человек повстречал металл в виде золота, меди и серебра. Они встречаются на земле в свободной форме. Постепенно к ним стали присоединяться другие элементы, которые встречаются в круговороте природы. К соединениям, которые легко выделить, можно отнести: олово, ртуть, железо, свинец. Данные металлы известны людям с древних времен.
С точки зрения алхимии, зарождение металла происходит в недрах земли. Совершенствование происходило под планетным воздействием, а метаморфозы происходили веками. В результате появились драгоценные металлы в виде золота и серебра. Ко второй группе относились медь, олово, свинец, железо и ртуть, которые обладают свойствами благородных металлов. При этом они отличаются летучестью, жидким состоянием. Многие ученые выделяли данные элементы в особую категорию. Ртуть была причислена к элементам, из которых образовывались металлы. Именно она была носителем металлических свойств.
Цинк, висмут, сурьма и мышьяк обладают множеством схожих свойств с металлами, но ковкость в данном случае уступает реальным металлам. Поэтому была образована новая категория полуметаллов. Классификация на металлы и полуметаллы появилась еще в 18 веке. Первоначально алхимики расценивали процесс преобразования сплавов схожих по цвету с золотом, как настоящее превращение в драгоценный металл. Они считали, что достаточно поменять только цвет, чтобы свойства тоже изменились. Алхимики думали, что это вещества, которые относятся к категории сложных, состоят из серы и ртути.
Алхимики стали стараться ускорить естественный процесс созревания, поддерживая необходимые условия. Естественное превращение металлов имело прямое отождествление с обычным ростом и развитием вещей. Данная тема относилась к таинствам жизни. Именно в этот период возникла история о философском камне. Но не существует никаких точных инструкций, которые смогли бы превратить золото или серебро в камень, дающий бессмертие. Существует множество теорий. Основным борцом против идеи алхимиков считался Бойль.
С наступлением 17 века человечество узнало о том, какую роль играет воздух в процессе горения, как увеличивается массовая доля при окислении. Однако об этом знал Гебер в 8 веке. Казалось, что вопрос об элементарном составе металла будет в скором времени закрыт, но в химии появился новый раздел под названием флогистонная теория. Это привело к возникновению нового заблуждения. Процесс горения был классифицирован как разложение, то есть распад на составляющие элементы. Выделение горючего элемента происходило в форме пламени, а остальные оставались в исходном состоянии. Поэтому начали появляться противоречия. Бехер старался прийти к формированию единых понятий и предполагал, что в металле присутствует земля трех сортов: земля, горючая и ртутная. Именно при таких условиях Шталь разработал свою теорию, согласно которой причиной горючести является неизвестная, названная флогистоном. Образование металлов происходит посредством земли и флогистона. В 18 веке Ломоносов учитывал 6 металлов: Au, Ag, Cu, Sn, Fe, Pb. Ученый из России в процессе исследования металлов и неметаллов дал определение: металлом называется светлое тело, которое возможно ковать. К таким можно отнести только 6 тел: серебро, медь, золото, олово, свинец и железо. Но в этой теории была большая дыра, так как тело в процессе обжига увеличивалось в массе. В таком случае флогистон должен обладать определенным свойством в виде отрицательного тяготения. В конце 18 века данную теорию смог опровергнуть Лавуазье и доказал, что металлы являются простыми веществами. В 1789 он подготовил список простых веществ, в который включено 17 металлов. По мере прогрессирования, количество химических элементов возрастало.
Лавуазье смог установить, какую функцию воздух выполняет в процессе горения. Он показал, что увеличение веса металла при обжигании происходит в результате присоединения кислорода, который выделяется из воздуха.
В первой половине 19 века произошло новое открытие: установлены спутники Плутона, которые были получены посредством электролиза. Появились задатки классификации редкоземельных элементов, открыты новые неизвестные в процессе химического анализа минералов.
Посредством спектрального анализа появились Cs, Rb, Tl, In. Менделеев предсказал существование металлов. Например, метод ядерных превращений, начиная с середины 20 века. Искусственным методом получены радиоактивные металлы. В период 19-20 вв металлургия получила новую химико-физическую базу. В это же время появились новые исследования в области свойств металлов и сплавов, учитывая состав и строение. Такие гибриды могут иметь высокий потенциал в тепло- и энергетическом типе устойчивости. Вследствие внедрения неметаллических элементов молекулы меняют свое строение, анионы и катионы.
Нахождение металлов в природе
Основная часть всех металлов добываются из земной коры, она там расположена в виде соединений, только малоактивные, называемые благородными, встречаются в свободном формате. Обычно металлы встречаются в природе в формате руды и различных соединений.
Наличие самых распространенных металлов в коре Земли можно представить примерно таким соотношением (масс. %): алюминий 8,45; железо 4,4; кальций 3,3; натрий 2,6; калий 2,5; магний 2,1; титан 0,61.
Из металлов получаются: оксиды, сульфиды, карбонаты и другие химические вещества. Получить чистые металлы для их обработки в будущем можно только после очистки их от примесей, которые содержатся в руде. Руды скопления металлосодержащих минералов, входящих в состав горных пород. Металл в составе руды находится в окисленном состоянии, независимо от типа, поэтому основным способом получения металлов является процесс восстановления. Если в руде содержатся различные металлы, то руду подвергают расщеплению на отдельные соединения химическим методом. Таким образом, при воздействии на полиметаллические руды хлора (в присутствии восстановителя) образуются хлориды разных металлов, которые благодаря разнице степеней летучести могут отделяться один от другого и от не хлорированной части руд. Чистые хлориды ряда металлов восстанавливают активными металлами до свободных металлов.
Изредка сложные полиметаллические типы руд для выделения сложных сплавов подвергают восстановлению без предварительного разделения. Они бывают загрязненные так называемыми пустыми породами, которые затрудняют восстановление. Тогда процессу добычи металла предшествует очистка руды или ее обработка механическим, химическим, физико-химическим и другим методом. Из физико-химических наибольшее распространение получил метод флотации, в основе которого различная смачиваемость водой частиц смеси различных материалов.
Чистые оксиды металлов легче и удобнее поддаются процессу восстановления. В связи с этим водные оксиды обезвоживают, а сульфидные руды переводят в оксидные путем окислительного обжига.
Руды, в которых совсем небольшое содержание металлов подвергаются гидрометаллургической переработке водными растворами кислот или щелочей. При этом соединения некоторых металлов переходят в раствор.
Изучением этого занимается наука металлургия. Металлургия разделяет руды на чёрные металлы (на основе железа) и цветные (в их состав не входит железо, всего около 70 элементов). Исключением можно назвать около 16 элементов: т. н. благородные металлы (золото, серебро и др.), и некоторые другие (например, ртуть, медь), которые присутствуют без примесей. Золото, серебро и платина относятся также к драгоценным металлам. Кроме того, в малых количествах они присутствуют в морской воде, растениях, живых организмах (играя при этом важную роль).
Известно, что организм человека на 3 % состоит из металлов. Больше всего в наших клетках кальция и натрия, сконцентрированного в лимфатических системах. Магний накапливается в мышцах и нервной системе, медь в печени, железо в крови.
Добыча металла
Металлы часто извлекают из земли средствами горной промышленности, результат добытые руды в самородном карьере служат относительно богатым источником необходимых элементов. Для выяснения расположения руды используют специальные поисковые методы, которые включают в себя разведку руд и исследование мест рождений и окружающей среды. Месторождения, как правило, делятся на карьеры (разработки руд на поверхности), в которых добыча ведется путем извлечения грунта с использованием тяжелой техники, а также на подземные шахты.
После добычи руды ее превращают в металлы при помощи химического, а также электролитического воздействия. Самыми популярными способами распространенными способами добычи металлов считаются пирометаллургия и гидрометаллургия. Рассмотрим подробнее:
- Пирометаллургией называют восстановительную работу металлов, при которой используются углерод (карботермия), водород, металлы-восстановители (металлотермия):
WO3 + 3H2 = W + 3H2O; CuS + O2 = CuO + SO2; CuO + H2 = Cu + H2O; BeF2 + Mg = Be + MgF2.
При использовании алюминия, метод получения называется алюминотермией. Алюмотермические методы применяются в извлечении из оксидов тугоплавких металлов (ванадий, хром, молибден и др.). Иногда в качестве восстановителя требуется магний. Метод магний термии нашел применение при получении титана, циркония, тантала из хлоридов этих металлов. Углерод по своей восстановительной активности уступает многим металлам. Тем не менее, карботермия имеет широкое распространение при восстановлении металлов малой активности (медь) и средней (железо, цинк, свинец).
- Гидрометаллургией называют процесс восстановления металлов, происходит из водных растворов их солей при обычной температуре (комнатной). В этом случае восстанавливаемый металл находится в мелко раздробленном состоянии, требуются активные металлы.
- Электрометаллургией является процесс добычи под воздействием электрического тока, который пропускают через раствор или расплав соли металла:
AgNO3 + H2O → Ag + O2 + HNO3.
Электролизом водных растворов получают сравнительно малоактивные металлы (медь, серебро, никель и т. д.). А электролизом расплавов солей высокоактивные (щелочные и щелочноземельные металлы, алюминий).
Некоторые отрасли промышленности и техники нуждаются в металлах особой чистоты. Например, они востребованы при конструировании ядерных реакторов, в электронной и медицинской технике. Особо чистые металлы отличаются по своим физическим свойствам от обычных. Такие свойства, как пластичность, электро- и теплопроводность, а также сопротивление коррозии у чистых металлов имеют более высокие значения.
Сейчас проблема получения чистых и сверхчистых металлов решается различными способами.
- Электролитическое рафинирование. Это формат электролиза с использованием чернового металла в качестве анода (активного). При пропускании постоянного электрического тока через электролит черновой металл окисляется (растворяется), а на катоде, изготовленном из чистого металла, из раствора (расплава) восстанавливается (осаждается) металл.
- Термическая диссоциация летучих соединений очистка, основанная на способности некоторых соединений металлов разлагаться при высокой температуре. Например, иодиды титана и циркония, являясь летучими соединениями, при повышении температуры разлагаются на чистый металл и йод.
- Зонная плавка процесс, основанный на различной степени растворимости примесей в твердом и расплавленном состояниях. Через зону с высокой температурой медленно продвигают стержень из очищаемого металла. По мере продвижения расплавленная область, где собираются все примеси, постепенно перемещается в конец стержня, который входит в горячую зону последним. Операцию повторяют многократно, каждый раз механически отделяя от чистого металла конец стержня, содержащий примеси.
В современной технике применяют около 30 000 сплавов легкоплавких и тугоплавких, очень твердых и пластичных, с большой и малой электрической проводимостью, ферромагнитных и др. В сплавах ныне используют практически все известные металлы (кроме искусственно полученных трансплутониевых элементов). Мера использования определяется доступностью металла и содержанием в земной коре, а также степенью концентрирования в месторождениях и трудностью получения. В последние годы наблюдается тенденция некоторого снижения роли железа и увеличение использования легких металлов (Al, Mg) и наиболее доступных редких металлов (Ti, Nb, Zr).
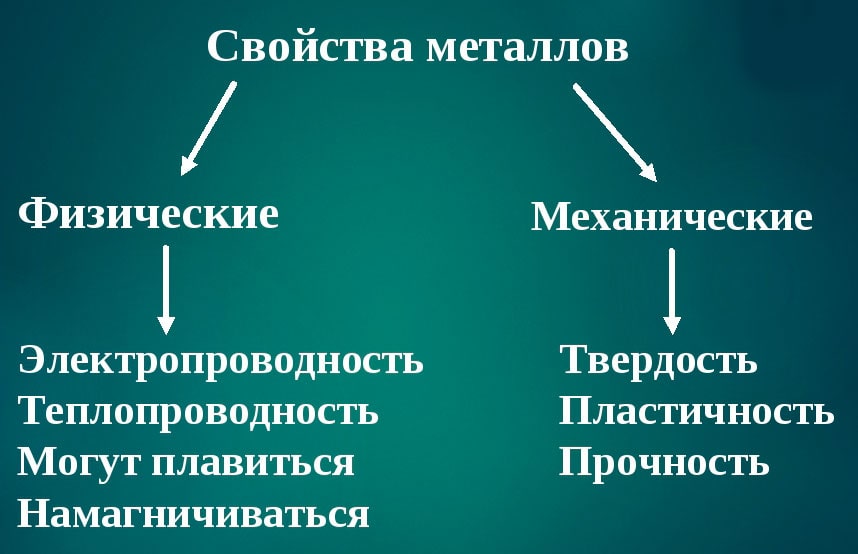
Свойства металлов
Свойства металлов можно разделить на четыре основных направления.
Характерные свойства металлов
Основные характеристики металлов:
- Металлический блеск (характерный признак не только металлов: его имеют и неметаллы азот и углерод в виде графита).
- Хорошая электропроводность всех металлов.
- Возможность легкой механической обработки (см.: пластичность; однако некоторые металлы, например германий и висмут, не пластичны).
- Высокая плотность (обычно металлы тяжелее неметаллов).
- Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы).
- Большая теплопроводность.
- В реакциях чаще всего являются восстановителями.
Атомы с промежуточными значениями степени окисления могут быть и окислителями, и восстановителями. Основные отличительные особенности металлов и неметаллов.
|
Признаки |
Металлы |
Неметаллы |
|
Положение в П. С. |
Под диагональю бор-астат |
Над ней |
|
Строение атома |
Большой атомный радиус, число электронов на последнем слое от 1 до 3 |
Маленький, от 4 до 7 соответственно |
|
Физические св-ва |
Электропроводность, теплопроводность, блеск, ковкость, пластичность, по агрегатному состоянию, в основном, твердые |
Диэлектрики, не блестящие, хрупкие, газы, жидкости и летучие твердые вещества |
|
Кристаллические решетки |
Металлическая |
Молекулярная, атомная |
|
Химические св-ва |
Восстановители |
Окислительные (иногда восстановительные) |
Физические свойства
Физические свойства металлов обусловлены металлической кристаллической решеткой и химической связью. В технике металлы принято классифицировать по различным физическим свойствам:
- плотности легкие (р < 5,0 г/см3) и тяжелые (р > 5,0 г/см3). Диапазон от 0,531 г/см3 (Li) до 22,6 г/см3 (Os). Плотность металлов связана с температурой их плавления. Легкие металлы обычно самые легкоплавкие, например, цезий с плотностью 1,87 г/см3 плавится при температуре +28 °С, а вольфрам с плотностью 19 г/см3 имеет температуру плавления, равную +3380 °С.
- температуре плавления легкоплавкие (tпл < 1000 °С) и тугоплавкие (tпл > 1000 °С). Диапазон температуры плавления от 38,87 °С (Hg) до 3380 °С (W).
Металлам характерны несколько свойств:
- Твердость сопротивление к проникновению в материал другого, более твердого тела;
- Теплота сублимации это характеристика, представляющая собой энергию, необходимую для перевода определенной массы металла в парообразное состояние. Теплота сублимации является мерой прочности связи в решетке металла. Характер изменения ее значений в побочных подгруппах аналогичен изменению температур плавления и кипения металлов.
- Износостойкость сохранение хорошего внешнего вида и физических свойств материала после сильного трения;
- Прочность стойкость к разрушению под воздействием внешней нагрузки;
- Упругость изменение формы материала под воздействием внешних сил и восстановление ее после того, как эти силы перестают на нее воздействовать;
- Теплопроводность это свойство металлов, обеспечиваемое взаимодействием электронов проводимости с ионами, находящимися в узлах кристаллической решетки. Теплопроводность металлов обусловлена в основном движением положительных электронов, поэтому коэффициент теплопроводности (3010-6.jpg) и электрической проводимости (s) металлов полностью связаны между собой соотношением 3010-7.jpg/(s•Т) = L = 2,45•10 -8 Вт•Ом/К2 (закон Видемана-Франца). Уд. коэф. теплопроводности металлов имеет значения от 425 (для Ag) до 8,41 (для Bi) Вт/(м-К).
- Пластичность изменение формы материала под внешним воздействием и сохранение ее после устранения этого воздействия;
- Усталость свойство материала выдерживать многократные нагрузки;
- Жароустойчивость сопротивление окислительным процессам при нагревании до высоких температур;
- Фотоэлектрический эффект это свойство металлов выбрасывать электроны с поверхности под действием электромагнитных волн, что обусловлено слабой связью валентных электронов с ядром.
- Полиморфизм это явление существования металла в разных формах в твердом состоянии, или способность принимать различные кристаллические формы.
- Вязкость способность материала вытягиваться под воздействием внешних сил;
- Магнитные свойства присущи фактически всем металлам, поскольку они являются магнетиками веществами, изменяющими или приобретающими магнитный момент под действием внешнего (стороннего) магнитного поля. Мерой измерения магнитных свойств металлов служат следующие величины: остаточная индукция, коэрцитивная сила и магнитная проницаемость (магнитная восприимчивость). Металлы по магнитным свойствам могут быть разделены на три основные группы:
- диамагнетики выталкиваются из магнитного поля и ослабляют его;
- парамагнетики втягиваются магнитным полем, незначительно усиливая его;
- ферромагнетики усиливают магнитное поле на порядки величин.
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твердом состоянии, однако обладают различной твердостью.
Гладкая поверхность металлов отражает большой процент света это явление называется металлическим блеском. Однако в порошкообразном состоянии большинство металлов теряют свой блеск; алюминий и магний, тем не менее, сохраняют свой блеск и в порошке. Наиболее хорошо отражают свет алюминий, серебро и палладий из этих металлов изготовляют зеркала. Для изготовления зеркал иногда применяется и родий, несмотря на его исключительно высокую цену: благодаря значительно большей, чем у серебра или даже палладия, твердости и химической стойкости, родиевый слой может быть значительно тоньше, чем серебряный.
Цвет у большинства металлов примерно одинаковый светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно желтого, красного и светло-желтого цвета.
Электрические свойства металлов
Электропроводность обусловлена присутствием в металле свободных электронов, которые направленно перемещаются при наложении электрического тока. Металлы проводники первого рода, так как проводят электрический ток без изменений своего строения. При нагревании электропроводность снижается, так как усиливается колебательное движение ионов, что затрудняет движение электронов. При охлаждении же электропроводность возрастает, близко абсолютного 0 она стремится к бесконечности это явление названо сверхпроводимостью.
Причина электрического сопротивления рассеяние электронов на любых нарушениях периодичности кристаллического строения решетки: тепловых колебаниях ионов (фононах), самих электронах, а также дефектах. К ним относятся примесные атомы, дислокации, границы кристаллов и образцов. Мерой рассеяния служит длина свободного пробега l усредненное расстояние между двумя последовательными столкновениями электронов с дефектами:
=nel/pF,
где n концентрация электронов проводимости (порядка 10221023 см3), e заряд электрона, pF=2πℏ(3n/8π)1/3 т. н. граничный фермиевский импульс. При T=300 К длина свободного пробега l порядка 106 см; с понижением T длина пробега растёт, достигая (для высококачественных образцов) 0,11 см. Соответственно возрастает электропроводность и уменьшается удельное электрич. сопротивление 1. Отношение проводимости при T=4,2 К к проводимости при T=300 К характеризует совершенство и химич. чистоту металлов.
Сопротивление сплавов значительно выше сопротивления чистых пород. В веществах с большим ρ возникает локализация электронных состояний проводимость исчезает.
При плавлении подвижные электроны в нём сохраняются, поэтому сохраняется и большая проводимость, хотя разрушение дальнего порядка приводит к скачкообразному росту сопротивления. Исключение составляют Sb,Ga,Bi, – их сопротивление при плавлении уменьшается.
Химические свойства
Во всех реакциях простые вещества металлы проявляют только восстановительные свойства.
Металлы взаимодействуют с неметаллами, образуя бинарные соединения. По правилам ИЮПАК названия этих соединений образуются в соответствии со схемой:
Так, с очень активными неметаллами (галогенами, серой) металлы образуют соединения, которые молено рассматривать, как соли бескислородных кислот: 2Na + Cl2 = 2NaCl
Если металл проявляет переменные степени окисления, подобная соль имеет состав, который зависит от окислительных свойств неметалла. Например, железо энергично взаимодействует с хлором, образуя хлорид железа(III): 2Fe + 3Сl2 = 2FeCl3
При взаимодействии железа с серой, окислительная способность которой ниже, чем у галогенов, продуктом реакции является сульфид железа(II): Fe + S = FeS
При взаимодействии металлов с кислородом образуются оксиды или пероксиды:
4Li + O2 = 2Li2O
2Na + O2 = Na2O2
Оксиды в этом случае имеют основный или амфотерный характер:
2Mg + O2 = 2MgO
4Аl + 3O2 = 2Аl2O3
Эти реакции сопровождаются выделением большого количества теплоты и очень ярким пламенем, поэтому применяются для изготовления сигнальных ракет, фейерверков, салютов и других пиротехнических средств. Поэтому обращение с ними требует строгого соблюдения правил техники безопасности.
Продуктом горения железа в кислороде является смешанный оксид :
3Fe + 2O2 = Fe3O4
Металлы простые вещества, образованные элементами IA и IIАгрупп, в полном соответствии с названием этих групп взаимодействуют с водой с образованием щелочи и водорода. В общем виде эти реакции можно записать так:
2М + 2Н2O = 2МОН + Н2↑, где М щелочной металл
М + 2Н2O = М(ОН)2 + H2↑, где М Mg или щелочноземельный металл.
Для характеристики химических свойств металлов важное значение имеет их положение в электрохимическом ряду напряжений:
К, Са, Na, Mg, Al, Zn, Fe, Sn, Pb, (H2), Cu, Hg, Ag, Au
Вспомните известные вам из курса основной школы два вывода:
- взаимодействие металлов с растворами концентрированных кислот происходит, если металл находится в ряду напряжений левее водорода. Других кислотных взаимодействий нет;
- взаимодействие металлов с растворами солей происходит, если металл находится в ряду напряжений левее металла соли.
Лабораторный способом получения водорода:
Zn + 2НСl = ZnCl2 + H2↑
Zn0 + 2H+ = Zn2+ + H20
Аналогично протекает реакция металлов и с органическими кислотами, они вступают в реакцию:
2СН3СООН + Zn > (CH3COO)2Zn + Н2↑
2СН3СООН + Zn > 2СН3СОO + Zn2+ + Н20
Реакция между цинком и раствором сульфата меди(II) протекает согласно уравнению:
Zn + CuSO4 = ZnSO4 + Cu
Zn0 + Сu2+ = Zn2+ + Сu0
Подчеркнем, что в этом случае металл может находиться в ряду напряжений и после водорода, но не после металла соли. Например, реакция замещения серебра медью:
Cu + 2AgNO3 = Сu(NО3)2 + 2Ag
Cu0 + 2Ag+ = Cu2+ + 2Ag0
В завершение рассмотрим еще одно характерное не для всех металлов свойство, которое называется металлотермия. Такие активные металлы, как алюминий, кальций, магний, литий, способны взаимодействовать с оксидами других металлов. Для того чтобы началась такая реакция, смесь активного металла и оксида металла (ее называют термитной) необходимо поджечь. После этого процесс сопровождается выделением большого количества теплоты и света (отсюда и название процесса). Металлотермию применяют для получения и более ценных металлов: 2Аl + Сr2О3 = Al2O3 + 2Сг
Классификация (виды) металлов
Есть несколько разных классификаций металлов, о которых поговорим ниже в статье. Стандарты всех металлов прописаны в ГОСТ. Каждый из стандартов определяет требования к металлическим материалам, к их индивидуальным характеристикам и сферам использования. За все эти направленности отвечает химия строения металлов. Данные критерии становятся основными при выборе материала для определенной цели.
Все металлы делятся на четыре группы:
- s-металлы (все s-элементы, кроме Н и Не) простые. Бывают щелочные металлы и щелочноземельные элементы.
- р-металлы (элементы гр. IIIа, кроме В, а также Sn, Рb, Sb, Bi, Ро) простые.
- d-металлы. Выделяют платиновые металлы.
- f-металлы.
Группа редкоземельных элементов включает как d-, так и f-металлы (подгруппа Sc и лантаноиды).
Существует также техническая классификация металлов. В известной мере она перекликается с геохимическими классификациями элементов. Обычно выделяют следующие виды, которые отличаются химически:
- черные металлы (Fe);
- тяжелые цветные металлы Сu, Pb, Zn, Ni и Sn (к этой группе примыкают т.наз. малые, или младшие, металлы Со, Sb, Bi, Hg, Cd, некоторые из них иногда относят к редким металлам);
- легкие металлы (с плотностью меньше 5 г/см3)-Аl, Mg, Ca и т.д.;
- драгоценные металлы Au, Ag и платиновые металлы;
- легирующие (или ферросплавные) металлы Mn, Cr, W, Mo, Nb, V и др.;
- редкие металлы;
- радиоактивные металлы U, Th, Pu и др.
Отличия металлов от сплавов заключается в разных визуальных признаках, например, в зернистости и гладкости поверхности. Еще сплавы имеют теплопроводность и электропроводность. Чаще всего применяются в промышленности медные, титановые, бронзовые и алюминиевые типы сплавов. Эти элементы служат сырьем для производства разного рода деталей и выливания металлоконструкций.
Для более простого восприятия, в обиходе деление происходит всего на две основные группы. Такими группами являются черные и цветные металлы. Они не имеют схожести ни по свойствам, ни по промышленному применению. Ниже в статье разберем эти группы металлов подробнее.
Черные металлы
Черные металлы получили такое наименование из-за своего цвета, который изменяется от темно-серого до практически белоснежного (серебристо-белого или белого цвета сталь, например). Они обладают высокой плотностью и температурой плавления, твердостью. Среди всех черных металлов больше всего распространено и чаще всего применяется в промышленности обычное железо.
Класс черных металлов включает в себя два основных подвида, к которым относится сталь и чугун. Стали же в свою очередь могут быть углеродистыми или легированными.
Различные виды черных сплавов получили значительное распространение в области изготовления металлопроката. Они обладают отличными рабочими свойствами, поэтому на рынке черные металлы всегда востребованы.
Добывают материалы напрямую из железной руды при помощи доменной печи, где при температуре близко к 2000 градусов протекает процесс плавления руд, из которых сразу и получают железо. На самом деле способов выработки железа множество. Также помимо доменного процесса выплавки железа, существует еще вариант прямого получения железа из предварительно измельченной железной руды с добавлением специальной глины. При таком способе железо получается сразу твердое, которое потом приходится переплавлять в мощных электропечах. Помимо видов металлов и их сплавов, существуют также и разнообразные их марки, разновидность которых указывается в буквенно-цифровом виде, например Ст4. Такого рода группировка и маркировка черных металлов, очень облегчает работу и изготовление металлопроката.
Любой металлопрокат по форме, размерам и предельным отклонениям должен строго соответствовать в России требованиям ГОСТа. К черному металлу относятся следующие виды проката: листовой, сортовый, фасонный, трубный прокат. Чугун и сталь между собой очень похожи, за исключением количества содержащегося углерода. Основные характеристики:
- Чугуны сплавы содержащие углерод свыше 2,14 % (в некоторых чугунах доля углерода доходит до 6 %). Кроме углерода в чугунах и сталях содержатся иные компоненты. Например, марганец, кремний, сера, фосфор.
- Стали сплавы железа с углеродом при содержании углерода менее 2,14 %. Стали также бывают низкоуглеродистые (содержание углерода менее 0,25%), углеродистые (0,25 0,6 %), высокоуглеродистые (более 0,6 %). Низкоуглеродистые стали легко сваривается и весьма пластичны, высокоуглеродистые же напротив очень твердые, благодаря чему применяются в агрегатах режущих инструментов.
Цветные металлы
Цветные металлы также названы благодаря цвету простых веществ. Их цвет может быть красным, желтым, белым. Например, медь красного цвета, и ее сплавы имеют красноватый оттенок. Цветным металлам свойственны также уникальные физические и химические свойства. Важнейшими продуктами цветной металлургии являются титан, вольфрам, молибден и другие металлы, которые могут использоваться в качестве специальных легирующих добавок для производства сверхтвердых, тугоплавких, устойчивых к коррозии сплавов, широко применяемых в машино и станкостроении, в обороннокосмической отрасли.
Сплавы в сравнении с металлами более пластичные, мягкие и легкоплавкие. К механической обработке цветных металлов относится штамповка, ковка, прессование, прокатка, пайка, сварка и резка.
Типы цветных металлов:
- Тяжелые цветные металлы. К ним относится свинец, медь, олово, цинк, никель, ртуть.
- Легкие цветные металлы. К ним относится: алюминий, титан, магний, бериллий, стронций, кальций, литий, барий, калий, натрий, цезий и рубидий.
- Благородные цветные металлы. Это металлы, которые уже готовы и очищены на поверхности Земли. К примеру: платина, золото, серебро, осмий, родий, рутений, палладий.
- Тугоплавкие цветные металлы. Это вольфрам и ванадий, молибден и тантал, хром и ниобий, цирконий и марганец.
- Рассеянные цветные металлы, к которым относятся: индий, таллий, германий, рений, селен, гафний и теллур.
- Радиоактивные цветные металлы. Список: уран, торий, радий, нептуний, актиний, америций, протактиний, плутоний, эйнштейний, калифорний, фермий, нобелий, менделевий и лоуренсий.
Многочисленную группу составляют редкоземельные металлы, такие как: туллий, эрбий, прометий, лютеций, церий, лантан, неодим, празеодим, европий, самарий, тербий, гадолиний, гольмий, диспрозий, иттрий и скандий.
Стоит отметить, что большая часть литых изделий, а также проволока, квадраты, шестиугольники в виде прутков и мотков, ленты и полосы, листы и фольга изготавливаются из цветных металлов. Различают по толщине, фольга бывает тонкой в несколько мм. В последнее время в производстве даже начали использоваться порошки из данных металлов.
Сплавы металлов
В твердом состоянии металлы практически не взаимодействуют друг с другом, однако в расплавленном состоянии могут иметь место и растворение, и взаимодействие. Различные расплавленные металлы в большинстве случаев смешиваются друг с другом в любых соотношениях, образуя жидкие однородные системы. Сплавами называют материалы, которые состоят из двух и более металлических компонентов. Как правило, каждый сплав состоит из основы, в нее обычно входит несколько металлов, и так называемых легирующих элементов. Легирующие добавки нужны, чтобы придать сплаву мягкость, эластичность, твердость, коррозионную стойкость и другие свойства. Чаще всего в промышленности применяются смеси с использованием железа и алюминия, но вообще существует более 5 тысяч разновидностей сплавов. Сплавы делятся на два вида: литые и порошковые. Литые сплавы получаются путем смешивания расплавленных компонентов. А порошковый метод получения сплавов подразумевает прессование порошков нескольких металлов и их последующее спекания при высоких температурах. По назначению сплавы делятся на:
- конструкционные. Конструкционные сплавы предназначены для изготовления деталей автомобилей, техники и оборудования. Это обусловлено прежде всего их высокой прочностью, однородностью и непроницаемостью для жидкостей и газов. Кроме того, меняя рецептуру сплавов, можно менять их свойства в очень широких пределах.
- инструментальные. Из технологии инструментальных сплавов, как можно понять из названия, изготавливают инструменты например, различные молотки и ножи. В качестве инструментальных материалов применяются также алмаз, нитрид бора, керамика..
- специальные. Специальные сплавы используются для изготовления деталей специального назначения например, для предотвращения трения. Металлы используются как в качестве хороших проводников электричества (медь, алюминий), так и в качестве материалов с повышенным сопротивлением для резисторов и электронагревательных элементов (нихром и т. п.)
Сплавы подразделяются на твердые и мягкие, легкоплавкие и тугоплавкие, устойчивые к воздействию кислот и щелочей.
Электро- и теплопроводность сплавов высокая. Свойства сплавов зависят от свойств веществ, входящих в его состав.
Твердость сплава, состоящего из 99% меди и 1% бериллия, в 7 раз больше твердости меди.
Сплав, состоящий из 50,1% висмута, 24,9% свинца, 14,2% олова, 10,8% кадмия, имеет температуру плавления, равную 65,5°С (тогда как висмут плавится при 271,3°С, олово 231,9°С, кадмии 320,9°С, свинец 327,4°С).
Такие металлы, как цинк, медь, алюминии не реагируют с водой, тогда как сплав, состоящий из 5% цинка, 50% меди, 45% алюминия при нормальных условиях взаимодействует с водой и вытесняет водород.
Сплавы, также как и металлы, имеют кристаллическое строение, и свойства разнятся в зависимости от строения. При кристаллизации в некоторых сплавах происходит образование химических соединений, в некоторых же сплавах, с химической точки зрения, атомы металлов связь не образуют. Такие сплавы называют нередко твердыми растворами.
Гомогенные сплавы это сплавы, состоящие из металлов, имеющих близкие величины атомного радиуса, в узлах крис-ской решетки которых возможен обмен атомов (Си-Аи, Ag-Au, Na-K, Bi-Sb).
Гетерогенные сплавы это сплавы, состоящие из металлов, имеющих различные величины атомного радиуса и в узлах кристаллической решетки которых невозможен обмен атомов (Sn-Al, Zn-Al).
Интерметаллические (межметаллические сплавы это сплавы, состоящие из металлов, электроотрицательность которых резко отличается друг от друга. В этих сплавах металлы соединяются в различных эквивалентных соотношениях, образуя химические соединения (CuZn, Cu3Al, Cu5Zn8). В отдельных случаях металлы не растворяются друг в друге и не могут образовывать сплавы (железо и свинец). В быту практически не применяются изделия, изготовленные из чистого металла. Нередко в обычной жизни можно встретить гидроксиды или каустик. Их используют при производстве целлюлозы, моющих средств (мыла, шампуней и других), в нефтепереработке, при производстве биодизельного топлива, для нейтрализации кислот во всем мире.
При изготовлении сплавов их свойства заранее должны быть известны. Кристаллическая решетка сплавов сильно отличается от кристаллической решетки чистых металлов.
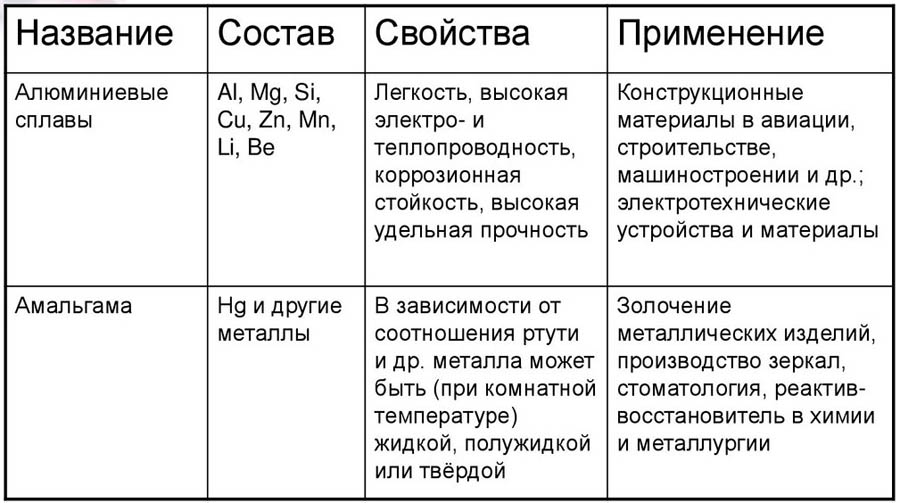
Примеры сплавов
Многие изделия станок, самолеты и ракеты, автомобили и мотоциклы, сковородки, кухонный инвентарь, ювелирные изделия делают из сплавов. Металлы-примеси (легирующие компоненты) очень часто изменяют свойства основного металла в лучшую, с точки зрения человека, сторону. Например, и железо и алюминий довольно мягкие металлы. Но, соединяясь друг с другом или с другими компонентами, они превращаются в сталь, дуралюмин и другие прочные конструкционные материалы. Рассмотрим свойства самых распространенных сплавов:
- Сталь (английский steel) это сплавы железа с углеродом, содержащие последнего до 2 %. В состав легированных сталей входят и другие химические элементы хром, ванадий, никель. Сталей производится гораздо больше, чем каких-либо других металлов и сплавов, и все виды их возможных применений трудно перечислить. Малоуглеродистая сталь (менее 0,25 % углерода) в больших количествах потребляется в качестве конструкционного материала, а сталь с более высоким содержанием углерода (более 0,55 %) идет на изготовление режущих инструментов: бритвенные лезвия, сверла и др.
- Железо составляет основу чугуна. Чугуном называется сплав железа с 24 % углерода. Важным компонентом чугуна является также кремний. Из чугуна можно отливать самые разнообразные и очень полезные изделия, например крышки для люков, трубопроводную арматуру, блоки цилиндров двигателей и др.
- Бронза сплав меди, обычно с оловом как основным легирующим компонентом, а также с алюминием, кремнием, бериллием, свинцом и другими элементами, за исключением цинка. Оловянные бронзы знали и широко использовали еще в древности. Большинство античных изделий из бронзы содержат 7590 % меди и 2510 % олова, что делает их внешне похожими на золотые, однако они более тугоплавкие. Это очень прочный сплав. Из него делали оружие до тех пор, пока не научились получать железные сплавы. С применением бронзы связана целая эпоха в истории человечества: Бронзовый век.
- Латунь это сплавы меди с Zn, Al, Mg. Это цветные сплавы с невысокой температурой плавления, их легко обрабатывать: резать, сваривать и паять.
- Мельхиор является сплавом меди с никелем, иногда с добавками железа и марганца. По внешним характеристикам мельхиор похож на серебро, но обладает большей механической прочностью. Сплав широко применяют для изготовления посуды и недорогих ювелирных изделий. Большинство современных монет серебристого цвета изготавливают из мельхиора (обычно 75 % меди и 25 % никеля с незначительными добавками марганца).
- Дюралюминий, или дюраль это сплав на основе алюминия с добавлением легирующих элементов медь, марганец, магний и железо. Он характеризуется своей стальной прочностью и устойчивостью к возможным перегрузкам. Это основной конструкционный материал в авиации и космонавтике.
Взаимодействие металлов с кислотами
Кислоты взаимодействуют с металлами, стоящими в ряду активности металлов левее водорода. Результатом такой реакции становится соль и выделение водорода. Можно сказать, что металлы, расположенные в ряду активности левее, вытесняют водород из кислот. Взаимодействие неокисляющих кислот с металлами, стоящими в электрическом ряду активности металлов до водорода
Происходит реакция замещения, которая также является окислительно-восстановительной:
Mg+2HCl=MgCl₂+H₂↑
2Al+2H3PO4=2AlPO4+3H₂↑
Взаимодействие серной кислоты H2SO4 с металлами
Окисляющие кислоты могут взаимодействовать и с металлами, стоящими в ЭРАМ после водорода:
Cu+2H₂SO4=CuSO4+SO₂↑+2H₂O
Очень разбавленная кислота реагирует с металлом по классической схеме:
Mg+H₂SO4=MgSO4+H₂↑
При увеличении концентрации кислоты образуются различные продукты:
Mg+2H2SO4=MgSO4+SO₂↑+2H₂O
3Mg+4H2SO43=3MgSO4+S↓+4H₂O
4Mg+5H2SO4=4MgSO4+ H2S↑+4H₂O
Реакции для азотной кислоты (HNO3)
Cu+4HNO3(60%)=Cu(NO3)2+2NO₂↑+2H₂O
3Cu+8HNO3(30%)=3Cu(NO3)2+2NO₂↑+4H₂O
При взаимодействии с активными металлами вариантов реакций еще больше:
Zn+4HNO3(60%)=Zn(NO3)2+2NO₂↑+2H₂O
3Zn+8HNO3(30%)=3Zn(NO3)2+2NO₂↑+4H₂O
4Zn+10HNO3(20%)=4Zn(NO3)2+N₂O↑+5H₂O
5Zn+12HNO3(10%)=5 Zn(NO3)2+N₂↑+6H₂O
4Zn+10HNO3(3%)=4Zn(NO3)2+NH4NO3+3H₂O
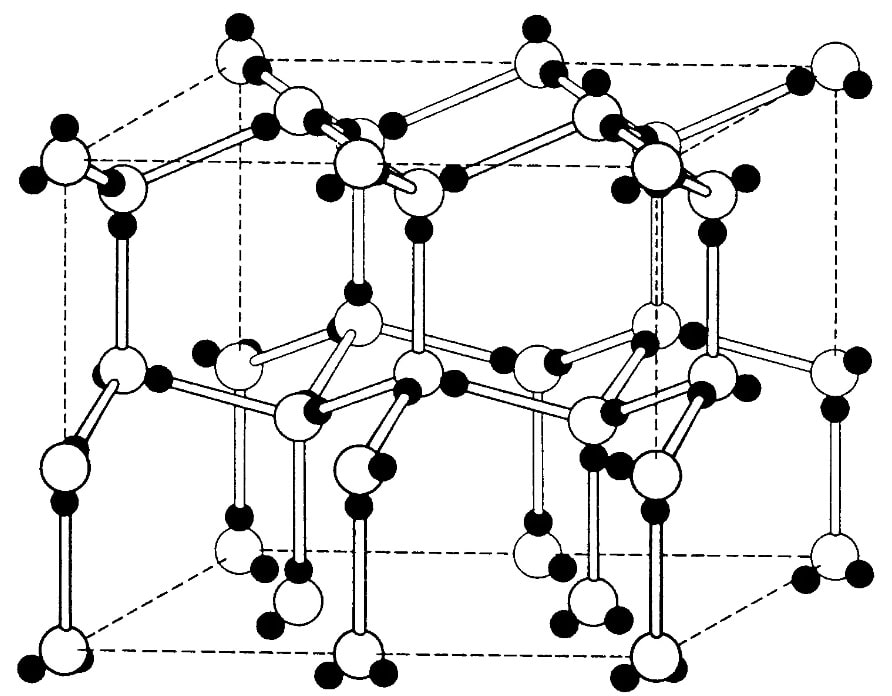
Строение металла
Металлы мы знаем из детства, в школе о них рассказывали на таких уроках, как биология, химия, физика и даже математика. Учили формулу, понятия, что такое легирование и ионная структура. Оттуда все знают, что это неорганические вещества, выдерживающие высокий температурный режим без деформации. Также есть растворимые в некоторых условиях металлы и нерастворимые. Характеристики металлов легко можно понять лишь взглянув на кристаллическую решетку.
Так как металлы в твердом состоянии имеют кристаллическое внутреннее строение, то образующие их элементарные частицы (атомы) в процессе кристаллизации из расплавленного состояния должны группироваться в определенной последовательности. Эта последовательность имеет название – кристаллическая решетка, что являет собой воображаемый элемент объема, который образуется минимальным количеством атомов, чье многократное повторение позволяет построить весь кристалл.
В каждом узле решетки металла пространственной кристаллической определенным образом расположены положительно заряженные ионы, а между ними летают свободные электроны, что представляют собой некий электронный газ. Переходя от одного катиона к другому, они осуществляют связь между ионами и превращают кристалл металла в целое вещество. Такой вид связи, называемый металлическим, возникает между атомами за счет перекрытия электронных облаков внешних электронов. Металлическая связь отлична от неполярной ковалентной в первую очередь своей ненаправленностью. В кристалле с металлической связью электроны не закрепляются между 2-мя атомами, а принадлежат всем атомам этого кристалла, другими словами. они делокализованные. К особенности структуры кристаллов металла относятся высокие координационные числа 8÷12, которым соответствует значительная твердость.
Суммарно известно четырнадцать разных видов кристаллических решеток. Металлы в основном кристаллизируются в одном из трех видов структур: объемноцентрированной кубической (ОЦК), гранецентрированной кубической (ГЦК) и гексагональной плотноупакованной (ГПУ), о которых подробнее поговорим в статье ниже. Для изображения кристаллической решетки используются упрощенные схемы. В объемно-центрированной кубической решетке содержится суммарно 9 атомов, выразить можно так: 8 расположены в вершинах куба и 1 в центре объема. Такое строение решетки у молибдена, вольфрама, ванадия и других металлов.
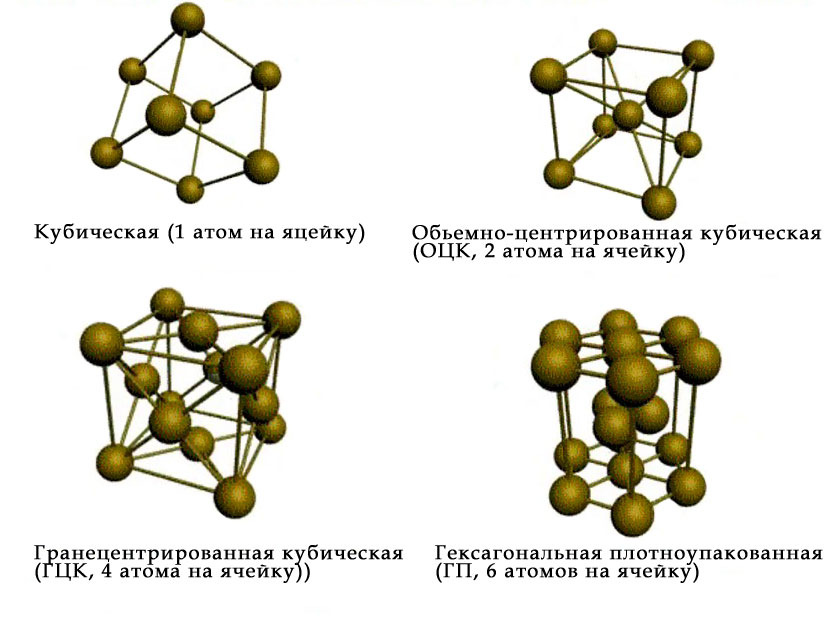
Типы кристаллических решеток
У каждого металла кристаллическая решетка содержит положительно заряженные ионы одинакового размера, что расположены по принципу довольно плотной упаковки шаров одинакового диаметра. Отличают всего 3 основных вида упаковки/кристаллической решетки.
- Объемноцентрированный кубический тип решетки с координационным числом = 8 (натрий, калий, барий). Атомы металла расположены на верхах куба, а один в центре объема. Плотность упаковки шарообразными ионами в таком варианте равна 68%.
- Гранецентрированный формат кубической решетки с координационным числом = 12 (это тип алюминия, меди, серебра). Атомы металла расположены в вершинах куба и по центру каждой из граней. Плотность упаковки 74%.
- Гексагональный тип решетки с координационным числом = 12 (магний, цинк, кадмий). Атомы металла расположены на верхах и в центре шестигранных оснований призмы, а еще три в ее средней плоскости. Плотность упаковки 74%.
Из-за разной плотности атомов в различных направлениях кристалла наблюдаются разного формата свойства. Это явление было названо анизотропия. Оно характерно для одиночного типа кристаллов монокристаллов. Однако в основном металлы в обычных условиях имеют поликристаллический тип строения, другими словами – состоят из большого количества кристаллов/зерен, каждое из которых анизотропно. Особенности кристаллических решеток обусловливают характерные физические свойства металлов.
Особенности строения
Твердость объясняется значительным количеством структурного плана дефектов (междоузельные атомы, вакансии и др.). Из-за легкой отдачи электронов есть риск окисления металлов, что в свою очередь приводит к коррозии и дальнейшему разрушению и деградации его свойств. Способность к окислению легко понять по стандартному ряду активности металлов. Это и говорить в пользу смешивания металлов в сплавы с использованием легирующих элементов химической периодической таблицы, а также применение различного рода покрытий уже готового изделия.
Для наиболее адекватного описания электронных свойств металлов стоит использовать понятие квантовой механики. В структуре всех твердых тел с достаточной симметрией уровни энергии электронов отдельных атомов перекрываются и образуют разрешенные зоны, при этом зона, которую образовали валентные электроны, имеет соответствующее название – валентная зона. Слабая связь валентных электронов в металлах приводит к тому, что валентная зона в металлах получается очень широкой, и всех валентных электронов не хватает для ее полного заполнения.
Главная особенность и отличие от остальных этой частично заполненной зоны в том, что даже при малейшем напряжении в образце запускается перестройка валентных электронов. Проще говоря, протекает электричество.
Эта же высокая подвижность электронов приводит и к высокой теплопроводности и способности зеркально отражать электромагнитное излучение (что и придает металлам характерный им блеск).
Применение металлов
Металлы активно применяют как в повседневной жизни, в быту, так и для строения зданий, оборудования и транспорта.
Применение в качестве конструкционных материалов
Сплавы, которые используются для изготовления разного формата конструкций и строений, должны быть прочны и легкообрабатываемы. В строительстве, а также в машиностроении чаще всего применяются смеси из железа и алюминия. Например, из железа получают таким образом сталь, которая славится высокой прочностью и твердостью. Из нее можно ковать детали, прессовать листы, сваривать конструкции.
Чугун популярен для отлива крупногабаритного типа конструкций и формата деталей, для которых необходима высокая прочность и устойчивость. К примеру, много лет чугун служил основой для домашних батарей центрального отопления, а также канализационных труб. Из него делают сейчас котлы, перила и опоры для мостов, лестниц. Чугун довольно тяжелый, что не позволяет его использовать в некоторых сферах. Поэтому в некоторых отраслях его заменили на сплав алюминия, который прочный, но легкий. Дюралюминий, силумин соединения алюминия, они незаменимы в построении самолетов, вагонов, а также являются основой кораблестроения. В некоторых узлах самолетов используется смесь на основе магния. Смеси магния очень легкие и устойчивые к высоким температурам.
В ракетостроительной сфере применяют легкие и термостойкие соединения титана. Для повышения показателя ударопрочности, коррозионной стойкости и износоустойчивости сплавы легируют. Например, добавление марганца делает стали ударопрочными. Чтобы получить нержавеющую сталь, в состав смеси вводят хром.
Инструментальные сплавы
Из них делают режущие инструменты, штампы и детали для точных механизмов. Эти элементы должны быть износостойкими и с высокой прочностью, причем при нагревании должны оставаться такими же. Таким требованиям соответствуют, к примеру, нержавеющие стали, которые прошли специальную обработку высокими температурами (закалку). Для придания необходимых свойств инструментальные стали, как правило, легируют вольфрамом, ванадием или хромом.
Применение в электротехнической промышленности, электронике и приборостроении
Многочисленные металлические сплавы – незаменимый материал для изготовления особо чувствительных и высокоточных приборов, разного типа датчиков и преобразователей энергии. Например, на изготовление сердечников трансформаторов и деталей реле идет смесь никеля. Некоторые составляющие электромоторов изготавливают из соединений кобальта. Сплав никеля с хромом называется нихром и отличается высоким сопротивлением. Он часто основа для нагревательных элементов печей и электроприборов, которые используются в быту. Из медных сплавов в электротехнической промышленности и в приборостроении самое широкое применение нашли для латуни и бронзы. Первые незаменимы при изготовлении приборов, деталью которых являются запорные краны ( основные детали в конструкциях подачи газа и воды). Бронза идет обычно на изготовление пружин и пружинящих контактов.
Нахождение металлов в природе
Самый распространённый в земной коре металл – алюминий. Металлы встречаются как в соединениях, так и в свободном виде.
1. Активные – в виде солей (сульфаты, нитраты, хлориды, карбонаты)
2. Средней активности – в виде оксидов, сульфидов (Fe3O4, FeS2)
3. Благородные – в свободном виде (Au, Pt, Ag)
Получение металлов
Понятие о металлургии. Способы получения металлов. Сплавы (сталь, чугун, дюралюминий, бронза). Проблема безотходных производств в металлургии и охрана окружающей среды
1. Восстановление металлов из оксидов углем или угарным газом
MеxOy + C = CO2 + Me
MеxOy + CO = CO2 + Me
2. Обжиг сульфидов с последующим восстановлением
1 стадия
MеxSy+O2=MеxOy+SO2
2 стадия
MеxOy + C = CO2 + Me
MеxOy + CO = CO2 + Me
3. Алюминотермия (восстановление более активным металлом)
MеxOy + Al = Al2O3 + Me
4. Водородотермия – для получения металлов особой чистоты
MеxOy + H2 = H2O + Me
5. Восстановление металлов электрическим током (электролиз)
1) Щелочные и щелочноземельные металлы получают в промышленности электролизом расплавов солей (хлоридов):
2NaCl =расплав, электр. ток= 2 Na + Cl2↑
CaCl2 =расплав, электр. ток= Ca + Cl2↑
расплавов гидроксидов:
4NaOH =расплав, электр. ток= 4Na + O2↑ + 2H2O
2) Алюминий в промышленности получают в результате электролиза расплава оксида алюминия в криолите Na3AlF6 (из бокситов):
2Al2O3 =расплав в криолите, электр. ток= 4Al + 3 O2↑
3) Электролиз водных растворов солей используют для получения металлов средней активности и неактивных:
2CuSO4+2H2O =раствор, электр. ток= 2Cu + O2 + 2H2SO4