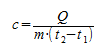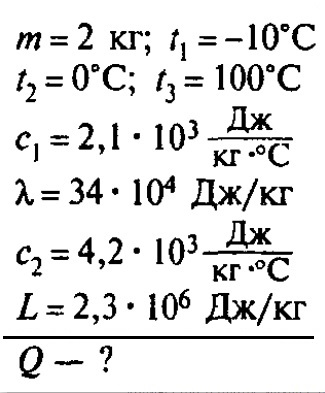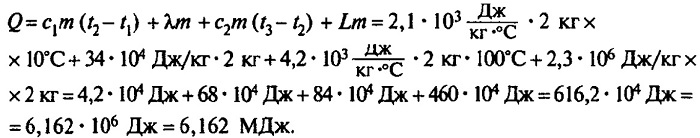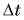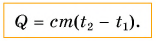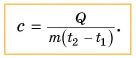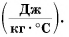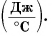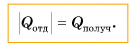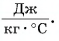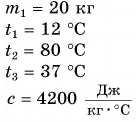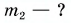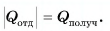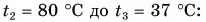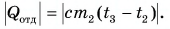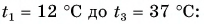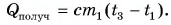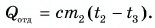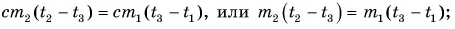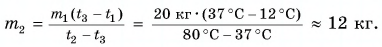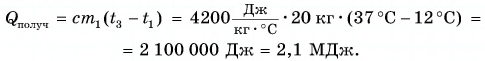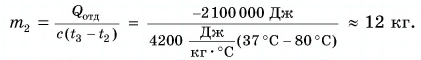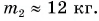Физика под удельной теплоемкостью понимает количество теплоты, которое термодинамическое вещество или система способно поглотить до повышения температуры.
Определение из учебника говорит, что это количество тепла, необходимое для создания температуры при нагревании.
Количество теплоты
Единица измерения – джоуль. Другой распространенной формой измерения является использование калорий.
Обозначается латинской буквой Q.
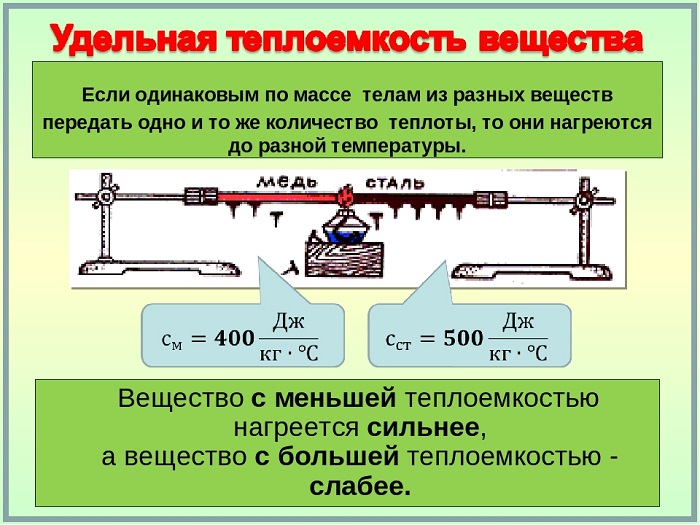
Удельная теплоемкость вещества
Это физическая величина, выражающая количество тепла, необходимое веществу на единицу массы для повышения температуры на одну единицу.
Таким образом, удельная теплоёмкость является свойством вещества, поскольку его значение является репрезентативным для каждого вещества, каждое из которых, в свою очередь, имеет различные значения в зависимости от того, в каком состоянии оно находится (жидкое, твердое или газообразное).
Удельная теплоёмкость обозначается маленькой буквой c и измеряется в Дж/кг∗°С, представляет собой коэффициент повышения температуры в одной единице всей системы или всей массы вещества.
Кроме того, удельная теплоёмкость меняется в зависимости от физического состояния вещества, особенно в случае твердых частиц и газов, поскольку его молекулярная структура влияет на теплопередачу в системе частиц. То же самое относится и к условиям атмосферного давления: чем выше давление, тем ниже удельное тепло.
Основной состав удельной теплоты вещества должен быть с = С/m, т. е. удельная теплота равна соотношению калорийности и массы. Однако когда это применяется к данному изменению температуры, говорят о средней удельной теплоемкости, которая рассчитывается на основе следующей формулы:
где:
Q – передача тепловой энергии между системой и средой (Дж);
m – масса системы (кг);
Δt или (t2 – t1) – повышение температуры, которой она подвергается (°C).
Формула для нахождения количества теплоты Q:
Q = c∗m(t2 – t1)
Чем выше удельная теплоёмкость вещества, тем больше тепловой энергии потребуется, чтобы его температура повысилась. Например, для нагрева воды (своды = 4200 Дж/кг∗°С) потребуется больше тепловой энергии, чем для нагрева свинца (ссвинца = 140 Дж/кг∗°С).
Уравнение теплового баланса:
Q отданное + Q полученное = 0.
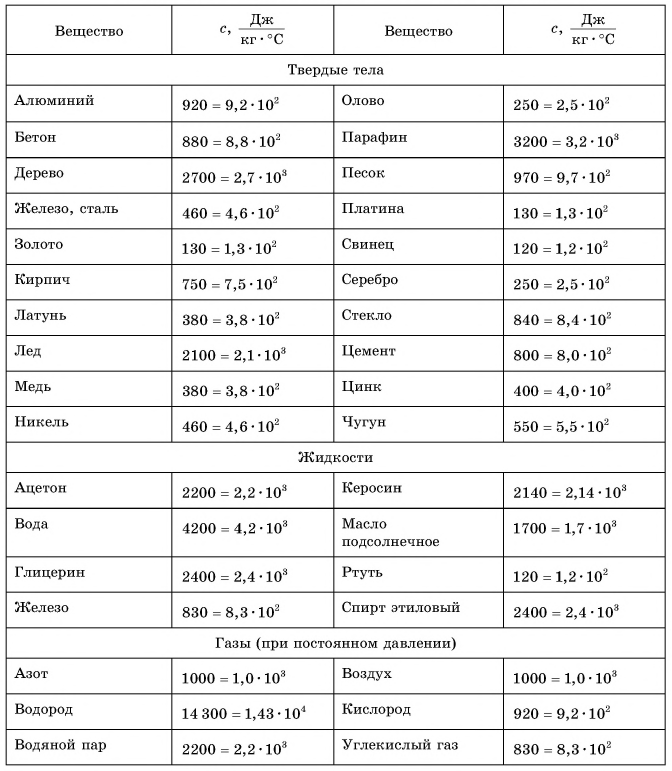
Ниже представлена таблица значений удельной теплоёмкости некоторых веществ:
Примеры решения задач
Следующие задачи покажут примеры расчета необходимого количества теплоты.
Задача №1
Сколько теплоты нужно, чтобы изо льда массой 2 кг, взятого при температуре -10°С, получить пар при 100°С?
Решение:
Ответ: чтобы изо льда массой 2 кг, взятого при температуре -10°С, получить пар при 100°С, нужно взять 6,162 мегаджоулей теплоты.
Задача №2
В железный котёл массой 5 кг налита вода массой 10 кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100°С?
Начнем решение и отметим, что нагреваться будет и котёл, и вода. Разница температур составит 1000С — 100С = 900С. Т. е. и температура котла изменится на 90 градусов, и температура воды также изменится на 90 градусов.
Количества теплоты, которые получили оба объекта (Q1
– для котла и Q2 — для воды), не будут одинаковыми. Мы найдем общее количество теплоты по формуле теплового баланса Q = Q1 + Q2.
Расчет количества теплоты при нагревании и охлаждении:
Вы уже знаете, что изменить внутреннюю энергию тела можно передачей ему количества теплоты. Как связано изменение внутренней энергии тела, т. е. количество теплоты, с характеристиками самого тела?
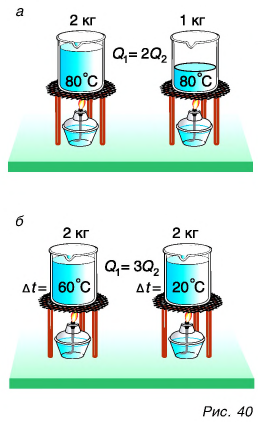
Внутренняя энергия тела есть суммарная энергия всех его частиц. Значит, если массу данного тела увеличить в два или три раза, то и количество теплоты, необходимое для его нагревания на одно и то же число градусов, увеличится в два или три раза. Например, на нагревание двух килограммов воды от 20 °C до 80 °C потребуется в два раза больше теплоты, чем на нагревание одного килограмма воды (рис. 40, а).
Очевидно также, что для нагревания воды на
Из этих рассуждений следует подтвержденный опытами вывод. Количество теплоты, необходимое для нагревания тела, прямо пропорционально его массе и изменению температуры.
А зависит ли количество теплоты, идущее на нагревание, от рода вещества, которое нагревается?
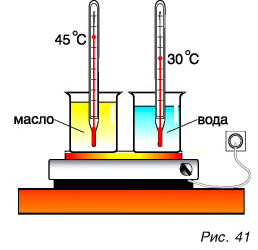
Для ответа на этот вопрос проведем опыт. В два одинаковых стакана нальем по 150 г подсолнечного масла и воды. Поместим в них термометры и поставим на нагреватель (рис. 41).
Получив за одинаковое время от нагревателя равное с водой количество теплоты, масло нагрелось больше, чем вода. Значит, для изменения температуры масла на одну и ту же величину требуется меньше теплоты, чем для изменения температуры такой же массы воды.
Поэтому для всех веществ вводят специальную величину — удельную теплоемкость вещества. Эту величину обозначают буквой с (от лат. capacite — емкость, вместимость). Теперь мы можем записать строгую формулу для количества теплоты, необходимого для нагревания:
Выразим из этой формулы с:
Удельная теплоемкость есть физическая величина, численно равная количеству теплоты, которое необходимо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C. Удельная теплоемкость измеряется в джоулях на килограмм-градус Цельсия
Для любознательных:
Часто формулу 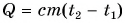
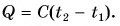
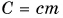
В таблице 1 представлены значения удельной теплоемкости различных веществ (в различных состояниях). Как следует из этой таблицы, среди жидкостей максимальное значение удельной теплоемкости имеет вода: для нагревания 1 кг воды на 1 °C требуется 4200 Дж теплоты — это почти в 2,5 раза больше, чем для нагревания 1 кг подсолнечного масла, и в 35 раз больше, чем для нагревания 1 кг ртути.
Формула 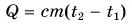
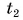
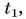
В заключение заметим, что при теплообмене двух или нескольких тел абсолютное значение количества теплоты, которое отдано более нагретым телом (телами), равно количеству теплоты, которое получено более холодным телом (телами):
Это равенство называется уравнением теплового баланса и выражает, по сути, закон сохранения энергии. Оно справедливо при отсутствии потерь теплоты.
Таблица 1. Удельная теплоемкость некоторых веществ
Главные выводы:
- Количество теплоты, необходимое для нагревания тела (выделившееся при охлаждении), прямо пропорционально его массе, изменению температуры тела и зависит от вещества тела.
- Удельная теплоемкость вещества численно равна количеству теплоты, которое надо передать 1 кг данного вещества, чтобы изменить его температуру на 1 °C.
- При теплообмене количество теплоты, отданное более горячим телом, равно по модулю количеству теплоты, полученному более холодным телом, если нет потерь теплоты.
- Заказать решение задач по физике
Пример решения задачи:
Для купания ребенка в ванночку влили холодную воду массой 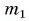
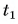
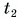
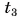
Дано:
Решение
По закону сохранения энергии
Отдавала теплоту горячая вода, изменяя свою температуру от
Холодная вода получила эту теплоту и нагрелась от
Так как нас интересует только модуль 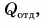
Тогда
При решении мы пренебрегали потерями теплоты на нагревание ванночки, окружающего воздуха и т. д.
Возможен и другой вариант решения.
Рассчитаем сначала количество теплоты, которое было получено холодной водой:
Полагая, что эта теплота отдана горячей водой, запишем: 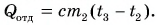
Ответ:
- Удельная теплота сгорания топлива
- Плавление и кристаллизация в физике
- Испарение жидкостей в физике
- Поверхностное натяжение жидкости
- Излучение тепла в физике
- Виды излучений в физике
- Инфракрасные излучения
- Количество теплоты в физике
Количество теплоты — еще один изученный нами вид энергии. Эту энергию тело получает или отдает при теплопередаче. Мы установили, что количество теплоты, необходимое для нагревания тела, зависит от массы тела, разности температур и рода вещества. Нам известен физический смысл удельной теплоемкости и некоторые ее табличные значения для разных веществ. В этом уроке мы перейдем к численному расчету количества теплоты, необходимой для нагревания тела или выделяемого им при охлаждении.
Зачем это нужно? На самом деле, на практике очень часто используют подобные расчеты.
При строительстве зданий и проектировании систем отопления важно знать, какое количество теплоты необходимо отдавать для полного обогрева всех помещений. С другой стороны, также необходима информация о том, какое количество теплоты будет уходить через окна, стены и двери.
Формула для расчета количества теплоты
Допустим, на нужно узнать, какое количество теплоты получила при нагревании железная деталь. Масса детали $3 space кг$. Деталь нагрелась от $20 degree C$ до $300 degree C$.
Возьмем значение теплоемкости железа из таблицы — $460 frac{Дж}{кг cdot degree C}$. Объясним смысл этой величины: на нагревание куска железа массой $1 space кг$ на $1 degree C$ необходимо затратить количество теплоты, равное $460 space Дж$.
- Масса детали у нас в 3 раза больше, значит, на ее нагрев потребуется в 3 раза большее количество теплоты — $1380 space Дж$
- Температура изменилась не на $1 degree C$, а на $280 degree C$
- Значит, необходимо в 280 раз большее количество теплоты: $1380 space Дж cdot 280 = 386 400 space Дж$
Тогда, формула для расчета количества теплоты, необходимой для нагревания тела или выделяемого им при охлаждении примет вид:
$Q = cm(t_2 — t_1)$,
где $Q$ — количество теплоты,
$c$ — удельная теплоемкость вещества, из которого состоит тело,
$m$ — масса тела,
$t_1$ — начальная температура тела,
$t_2$ — конечная температура тела.
Чтобы рассчитать количество теплоты, которое необходимо затратить для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость умножить на массу тела и на разность конечной и начальной температур.
Рассмотрим подробнее особенности расчета количества теплоты на примерах решения задач.
Расчет количества теплоты, затраченного на нагревание двух тел
В железный котелок массой $4 space кг$ налили воду массой $10 space кг$ (рисунок 1). Их температура $25 degree C$. Какое количество теплоты нужно затратить, чтобы нагреть котелок и воду до температуры $100 degree C$?
Обратите внимание, что нагреваться будут сразу два тела: и котелок, и вода в нем. Между постоянно будет происходить теплообмен. Поэтому их температуры мы можем считать одинаковыми.
Отметим, что массы котелка и воды различные. Также они имеют различные теплоемкости. Значит, полученные ими количества теплоты будет различными.
Теперь мы можем записать условие задачи и решить ее.
Дано:
$m_1 = 4 space кг$
$c_1 = 460 frac{Дж}{кг cdot degree C}$
$m_2 = 10 space кг$
$c_2 = 4200 frac{Дж}{кг cdot degree C}$
$t_1 = 25 degree C$
$t_2 = 100 degree C$
Q-?
Посмотреть решение и ответ
Скрыть
Решение:
Для расчета полученного количества теплоты используем формулу $Q = cm(t_2 — t_1)$.
Запишем эту формулу для количества теплоты, полученного котелком:
$Q_1 = c_1m_1(t_2 — t_1)$.
Рассчитаем это количество теплоты:
$Q_1 = 460 frac{Дж}{кг cdot degree C} cdot 4 space кг cdot (100 degree C — 25 degree C) = 1840 frac{Дж}{degree C} cdot 75 degree C = 138 000 space Дж = 138 space кДж$.
Количество теплоты, полученное водой при нагревании будет равно:
$Q_2 = c_2m_2(t_2 — t_1)$.
Подставим численные значения и рассчитаем:
$Q_2 = 4200 frac{Дж}{кг cdot degree C} cdot 10 space кг cdot (100 degree C — 25 degree C) = 42000 frac{Дж}{degree C} cdot 75 degree C = 3 150 000 space Дж = 3150 space кДж$.
Общее количество теплоты, затраченное на нагревание котелка и воды:
$Q = Q_1 +Q_2$,
$Q = 138 space кДж + 3150 space кДж = 3288 space кДж$.
Ответ: $Q = 3288 space кДж$.
Расчет количества теплоты при смешивании жидкостей
Горячую воду разбавили холодной и получили температуру смеси $30 degree C$. Горячей воды с температурой $100 degree C$ при этом было $0.3 space кг$. Холодная вода имела массу $1.4 space кг$ и температуру $15 degree C$. Рассчитайте, какое количество теплоты было отдано горячей водой при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.
Дано:
$c_1 = c_2 = c = 4200 frac{Дж}{кг cdot degree C}$
$m_1 = 0.3 space кг$
$m_2 = 1.4 space кг$
$t_1 = 100 degree C$
$t_2 = 15 degree C$
$t = 30 degree C$
$Q_1 — ?$
$Q_2 — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Запишем формулу для расчета количества теплоты, отданного горячей водой при остывании от $100 degree C$ до $30 degree C$:
$Q_1 = cm_1(t_1 — t)$.
Рассчитаем эту величину:
$Q_1 = 4200 frac{Дж}{кг cdot degree C} cdot 0.3 space кг cdot (100 degree C — 30 degree C) = 1260 frac{Дж}{degree C} cdot 70 degree C = 88 200 space Дж = 88.2 space кДж$.
Запишем формулу для расчета количества теплоты, полученного холодной водой при нагревании от $15 degree C$ до $30 degree C$:
$Q_2 = cm_2(t — t_2)$.
Рассчитаем эту величину:
$Q_1 = 4200 frac{Дж}{кг cdot degree C} cdot 1.4 space кг cdot (30 degree C — 15 degree C) = 5880 frac{Дж}{degree C} cdot 15 degree C = 88 200 space Дж = 88.2 space кДж$.
$Q_1 = Q_2 = 88.2 space кДж$.
Ответ: $Q_1 = Q_2 = 88.2 space кДж$.
В ходе решения этой задачи мы увидели, что количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой, равны. Другие опыты дают схожие результаты.
Значит,
Если между телами происходит теплоообмен, то внутренняя энергия всех нагревающихся тел увеличивается на столько, на сколько уменьшается внутренняя энергия остывающих тел.
На практике часто получается так, что отданная горячей водой энергия больше, чем полученная холодной. На самом деле, горячая вода при охлаждении передает какую-то часть своей внутренней энергии воздуху и сосуду, в котором происходит смешивание.
Есть 2 способа учесть этот фактор:
- Если мы максимально сократим потери энергии, то добьемся приблизительного равенства отданной и полученной энергий
- Если рассчитать и учесть потери энергии, то можно получить точное равенство
Расчет температуры при известной величине количества теплоты
При нагревании куска меди было затрачено $22 space кДж$. Масса этого куска составляет $300 space г$. Начальная температура была равна $20 degree C$. До какой температуры нагрели кусок меди?
Дано:
$m = 300 space г$
$t_1 = 20 degree C$
$c = 400 frac{Дж}{кг cdot degree C}$
$Q = 22 space кДж$
СИ:
$0.3 space кг$
$22 000 space Дж$
$t_2 — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Запишем формулу для расчета количества теплоты:
$Q = cm(t_2 — t_1)$.
Постепенно выразим из этой формулы искомую температуру $t_2$:
$t_2 — t_1 = frac{Q}{cm}$,
$t_2 = frac{Q}{cm} + t_1$.
Рассчитаем $t_2$:
$t_2 = frac{22 000 space Дж}{400 frac{Дж}{кг cdot degree C} cdot 0.3 space кг} + 20 degree C approx 183 degree C + 20 degree C approx 203 degree C$.
Ответ: $t_2 approx 203 degree C$.
Количество теплоты. Удельная теплоемкость вещества
Количеством теплоты называют количественную меру изменения внутренней энергии тела при теплообмене.
Количество теплоты — это энергия, которую тело отдает при теплообмене (без совершения работы). Количество теплоты, как и энергия, измеряется в джоулях (Дж).
Удельная теплоемкость вещества
Теплоемкость — это количество теплоты, поглощаемой телом при нагревании на $1$ градус.
Теплоемкость тела обозначается заглавной латинской буквой С.
От чего зависит теплоемкость тела? Прежде всего, от его массы. Ясно, что для нагрева, например, $1$ килограмма воды потребуется больше тепла, чем для нагрева $200$ граммов.
А от рода вещества? Проделаем опыт. Возьмем два одинаковых сосуда и, налив в один из них воду массой $400$ г, а в другой — растительное масло массой $400$ г, начнем их нагревать с помощью одинаковых горелок. Наблюдая за показаниями термометров, мы увидим, что масло нагревается быстрее. Чтобы нагреть воду и масло до одной и той же температуры, воду следует нагревать дольше. Но чем дольше мы нагреваем воду, тем большее количество теплоты она получает от горелки.
Таким образом, для нагревания одной и той же массы разных веществ до одинаковой температуры требуется разное количество теплоты. Количество теплоты, необходимое для нагревания тела и, следовательно, его теплоемкость зависят от рода вещества, из которого состоит это тело.
Так, например, чтобы увеличить на $1°$С температуру воды массой $1$ кг, требуется количество теплоты, равное $4200$ Дж, а для нагревания на $1°$С такой же массы подсолнечного масла необходимо количество теплоты, равное $1700$ Дж.
Физическая величина, показывающая, какое количество теплоты требуется для нагревания $1$ кг вещества на $1°$С, называется удельной теплоемкостью этого вещества.
У каждого вещества своя удельная теплоемкость, которая обозначается латинской буквой $с$ и измеряется в джоулях на килограмм-градус (Дж/(кг$·°$С)).
Удельная теплоемкость одного и того же вещества в разных агрегатных состояниях (твердом, жидком и газообразном) различна. Например, удельная теплоемкость воды равна $4200$ Дж/(кг$·°$С), а удельная теплоемкость льда $2100$ Дж/(кг$·°$С); алюминий в твердом состоянии имеет удельную теплоемкость, равную $920$ Дж/(кг$·°$С), а в жидком — $1080$ Дж/(кг$·°$С).
Заметим, что вода имеет очень большую удельную теплоемкость. Поэтому вода в морях и океанах, нагреваясь летом, поглощает из воздуха большое количество тепла. Благодаря этому в тех местах, которые расположены вблизи больших водоемов, лето не бывает таким жарким, как в местах, удаленных от воды.
Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении
Из вышеизложенного ясно, что количество теплоты, необходимое для нагревания тела, зависит от рода вещества, из которого состоит тело (т. е. его удельной теплоемкости), и от массы тела. Ясно также, что количество теплоты зависит от того, на сколько градусов мы собираемся увеличить температуру тела.
Итак, чтобы определить количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость тела умножить на его массу и на разность между его конечной и начальной температурами:
$Q=cm(t_2-t_1)$
где $Q$ — количество теплоты, $c$ — удельная теплоемкость, $m$ — масса тела, $t_1$ — начальная температура, $t_2$ — конечная температура.
При нагревании тела $t_2 > t_1$ и, следовательно, $Q > 0$. При охлаждении тела $t_2 < t_1$ и, следовательно, $Q < 0$.
В случае, если известна теплоемкость всего тела $С, Q$ определяется по формуле
$Q=C(t_2-t_1)$
Удельная теплота парообразования, плавления, сгорания
Теплота парообразования (теплота испарения) — количество теплоты, которое необходимо сообщить веществу (при постоянном давлении и постоянной температуре) для полного превращения жидкого вещества в пар.
Теплота парообразования равна количеству теплоты, выделяющемуся при конденсации пара в жидкость.
Превращение жидкости в пар при постоянной температуре не ведет к увеличению кинетической энергии молекул, но сопровождается увеличением их потенциальной энергии, т. к. расстояние между молекулами существенно увеличивается.
Удельная теплота парообразования и конденсации. Опытами установлено, что для полного обращения в пар $1$ кг воды (при температуре кипения) необходимо затратить $2.3$ МДж энергии. Для обращения в пар других жидкостей требуется иное количество теплоты. Например, для спирта оно составляет $0.9$ МДж.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой $1$ кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой $r$ и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты, необходимое для парообразования (или выделяющееся при конденсации). Чтобы вычислить количество теплоты $Q$, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования $r$ умножить на массу $m$:
$Q=rm$
При конденсации пара происходит выделение такого же количества теплоты:
$Q=-rm$
Удельная теплота плавления
Теплота плавления — это количество теплоты, которое необходимо сообщить веществу при постоянном давлении и постоянной температуре, равной температуре плавления, чтобы полностью перевести его из твердого кристаллического состояния в жидкое.
Теплота плавления равна тому количеству теплоты, которое выделяется при кристаллизации вещества из жидкого состояния.
При плавлении вся подводимая к веществу теплота идет на увеличение потенциальной энергии его молекул. Кинетическая энергия не меняется, поскольку плавление идет при постоянной температуре.
Изучая на опыте плавление различных веществ одной и той же массы, можно заметить, что для превращения их в жидкость требуется разное количество теплоты. Например, для того чтобы расплавить один килограмм льда, нужно затратить $332$ Дж энергии, а для того чтобы расплавить $1$ кг свинца — $25$ кДж.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой $1$ кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления измеряют в джоулях на килограмм (Дж/кг) и обозначают греческой буквой $λ$ (лямбда).
Удельная теплота кристаллизации равна удельной теплоте плавления, поскольку при кристаллизации выделяется такое же количество теплоты, какое поглощается при плавлении. Так, например, при замерзании воды массой $1$ кг выделяются те же $332$ Дж энергии, которые нужны для превращения такой же массы льда в воду.
Чтобы найти количество теплоты, необходимое для плавления кристаллического тела произвольной массы, или теплоту плавления, надо удельную теплоту плавления этого тела умножить на его массу:
$Q=λm$
Количество теплоты, выделяемое телом, считается отрицательным. Поэтому при расчете количества теплоты, выделяющегося при кристаллизации вещества массой $m$, следует пользоваться той же формулой, но со знаком «минус»:
$-Q=λm$
Удельная теплота сгорания
Теплота сгорания (или теплотворная способность, калорийность) — это количество теплоты, выделяющейся при полном сгорании топлива.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива. Обычное топливо (уголь, нефть, бензин) содержит углерод. При горении атомы углерода соединяются с атомами кислорода, содержащегося в воздухе, в результате чего образуются молекулы углекислого газа. Кинетическая энергия этих молекул оказывается большей, чем у исходных частиц. Увеличение кинетической энергии молекул в процессе горения называют выделением энергии. Энергия, выделяющаяся при полном сгорании топлива, и есть теплота сгорания этого топлива.
Теплота сгорания топлива зависит от вида топлива и его массы. Чем больше масса топлива, тем больше количество теплоты, выделяющейся при его полном сгорании.
Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой $1$ кг, называется удельной теплотой сгорания топлива.
Удельную теплоту сгорания обозначают буквой $q$ и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты $Q$, выделяющееся при сгорании $m$ кг топлива, определяют по формуле:
$Q=qm$
Чтобы найти количество теплоты, выделяющееся при полном сгорании топлива произвольной массы, нужно удельную теплоту сгорания этого топлива умножить на его массу.
Уравнение теплового баланса
В замкнутой (изолированной от внешних тел) термодинамической системе изменение внутренней энергии какого-либо тела системы $∆U_i$ не может приводить к изменению внутренней энергии всей системы. Следовательно,
$∆U_1+∆U_2+∆U_3+…+∆U_n=∑↙{i}↖{n}∆U_i=0$
Если внутри системы не совершается работа никакими телами, то, согласно первому закону термодинамики, изменение внутренней энергии любого тела происходит только за счет обмена теплом с другими телами этой системы: $∆U_i=Q_i$. Учитывая ($∆U_1+∆U_2+∆U_3+…+∆U_n=∑↙{i}↖{n}∆U_i=0$), получим:
$Q_1+Q_2+Q_3+…+Q_n=∑↙{i}↖{n}Q_i=0$
Это уравнение называется уравнением теплового баланса. Здесь $Q_i$ — количество теплоты, полученное или отданное $i$-м телом. Любое из количеств теплоты $Q_i$ может означать теплоту, выделяемую или поглощаемую при плавлении какого-либо тела, сгорании топлива, испарении или конденсации пара, если такие процессы происходят с различными телами системы, и будут определятся соответствующими соотношениями.
Уравнение теплового баланса является математическим выражением закона сохранения энергии при теплообмене.
Удельная теплоемкость вещества
Это физическая величина, выражающая количество тепла, необходимое веществу на единицу массы для повышения температуры на одну единицу.
Таким образом, удельная теплоёмкость является свойством вещества, поскольку его значение является репрезентативным для каждого вещества, каждое из которых, в свою очередь, имеет различные значения в зависимости от того, в каком состоянии оно находится (жидкое, твердое или газообразное).
Удельная теплоёмкость обозначается маленькой буквой c и измеряется в Дж/кг∗°С, представляет собой коэффициент повышения температуры в одной единице всей системы или всей массы вещества.
Кроме того, удельная теплоёмкость меняется в зависимости от физического состояния вещества, особенно в случае твердых частиц и газов, поскольку его молекулярная структура влияет на теплопередачу в системе частиц. То же самое относится и к условиям атмосферного давления: чем выше давление, тем ниже удельное тепло.
Основной состав удельной теплоты вещества должен быть с = С/m, т. е. удельная теплота равна соотношению калорийности и массы.
Однако когда это применяется к данному изменению температуры, говорят о средней удельной теплоемкости, которая рассчитывается на основе следующей формулы:
Q — передача тепловой энергии между системой и средой (Дж);
m — масса системы (кг);
Δt или (t2 — t1) — повышение температуры, которой она подвергается (°C).
Формула для нахождения количества теплоты Q:
Q = c∗m(t2— t1)
Чем выше удельная теплоёмкость вещества, тем больше тепловой энергии потребуется, чтобы его температура повысилась. Например, для нагрева воды (своды = 4200 Дж/кг∗°С) потребуется больше тепловой энергии, чем для нагрева свинца (ссвинца = 140 Дж/кг∗°С).
Уравнение теплового баланса:
Q отданное + Q полученное = 0.
Ниже представлена таблица значений удельной теплоёмкости некоторых веществ:
Самолеты, пароходы, поезда
Выше мы показали примеры относительно неподвижных, статичных предметов, которым сообщают или у которых, наоборот, отнимают определенное количество теплоты. Для объектов, в процессе работы движущихся в условиях постоянно меняющейся температуры, расчеты количества теплоты важны по другой причине.
Есть такое понятие, как «усталость металла». Включает оно в себя также и предельно допустимые нагрузки при определенной скорости изменения температуры. Представьте, самолет взлетает из влажных тропиков в замороженные верхние слои атмосферы. Инженерам приходится много работать, чтобы он не развалился из-за трещин в металле, которые появляются при перепаде температуры. Они ищут такой состав сплава, который способен выдержать реальные нагрузки и будет иметь большой запас прочности. А чтобы не искать вслепую, надеясь случайно наткнуться на нужную композицию, приходится делать много расчетов, в том числе и включающих изменения количества теплоты.
Примеры решения задач
Следующие задачи покажут примеры расчета необходимого количества теплоты.
Задача №1
Сколько теплоты нужно, чтобы изо льда массой 2 кг, взятого при температуре -10°С, получить пар при 100°С?
Ответ: чтобы изо льда массой 2 кг, взятого при температуре -10°С, получить пар при 100°С, нужно взять 6,162 мегаджоулей теплоты.
Задача №2
В железный котёл массой 5 кг налита вода массой 10 кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100°С?
Начнем решение и отметим, что нагреваться будет и котёл, и вода. Разница температур составит 100 0 С — 10 0 С = 90 0 С. Т. е. и температура котла изменится на 90 градусов, и температура воды также изменится на 90 градусов.
Количества теплоты, которые получили оба объекта (Q1 – для котла и Q2 — для воды), не будут одинаковыми. Мы найдем общее количество теплоты по формуле теплового баланса Q = Q1 + Q2.
Источник
Расчет количества теплоты, необходимого для нагревания тела и выделяемого им при охлаждении
Чтобы научиться рассчитывать количество теплоты, которое необходимо для нагревания тела, установим сначала, от каких величин оно зависит.
Из предыдущего параграфа мы уже знаем, что это количество теплоты зависит от рода вещества, из которого состоит тело (т. е. его удельной теплоемкости):
Q зависит от c.
Но это еще не все.
Если мы хотим подогреть воду в чайнике так, чтобы она стала лишь теплой, то мы недолго будем нагревать ее. А для того чтобы вода стала горячей, мы будем нагревать ее дольше. Но чем дольше чайник будет соприкасаться с нагревателем, тем большее количество теплоты он от него получит. Следовательно, чем сильнее при нагревании изменяется температура тела, тем большее количество теплоты необходимо ему передать.
Пусть начальная температура тела равна tнач, а конечная температура — tкон. Тогда изменение температуры тела будет выражаться разностью
Δt = tкон – tнач,
и количество теплоты будет зависеть от этой величины:
Q зависит от Δt.
Наконец, всем известно, что для нагревания, например, 2 кг воды требуется большее время (и, следовательно, большее количество теплоты), чем для нагревания 1 кг воды. Это означает, что количество теплоты, необходимое для нагревания тела, зависит от массы этого тела:
Q зависит от m.
Итак, для расчета количества теплоты нужно знать удельную теплоемкость вещества, из которого изготовлено тело, массу этого тела и разность между его конечной и начальной температурами.
Пусть, например, требуется определить, какое количество теплоты необходимо для нагревания железной детали массой 5 кг при условии, что ее начальная температура равна 20 °С, а конечная должна стать равной 620 °С.
Из таблицы 8 находим, что удельная теплоемкость железа с = 460 Дж/(кг*°С). Это означает, что для нагревания 1 кг железа на 1 °С требуется 460 Дж.
Для нагревания 5 кг железа на 1 °С потребуется в 5 раз больше количества теплоты, т. е. 460 Дж*5 = 2300 Дж.
Для нагревания железа не на 1 °С, а на Δt = 600 °С потребуется еще в 600 раз больше количества теплоты, т. е. 2300 Дж * 600 = 1 380 000 Дж. Точно такое же (по модулю) количество теплоты выделится и при остывании этого железа от 620 до 20 °С.
Итак, чтобы найти количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость тела умножить на его массу и на разность между его конечной и начальной температурами:
При нагревании тела tкон> tнач и, следовательно, Q > 0. При охлаждении тела tкон < tнач и, следовательно, Q < 0.
1. Приведите примеры, показывающие, что количество теплоты, получаемое телом при нагревании, зависит от его массы и изменения температуры. 2. По какой формуле рассчитывается количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении?
Как рассчитать тепловую мощность конвекторов, обогревателей и прочих отопительных приборов
Теплотехнический расчет – это вычисление требуемой толщины перекрытий в соответствии теплоизоляционных характеристик материалов и мощности нагревательных приборов. Любое помещение для создания комфортных условий в холодное время года требует определенного количества тепла, и неважно проектируется отопительная система частного дома или требуется обогреть только одну комнату – расчеты необходимы.
Все отопительные приборы независимо от типа устройства (конвекторы, радиаторные батареи, обогреватели, тепловые пушки и т.д.) и типа теплоносителя (водяные, газовые, электрические) отапливают помещения и производимое ими тепло называется тепловой мощностью. Именно эта характеристика имеет важнейшее значение при выборе обогревательного прибора.
Например невозможно обогреть мастерскую площадью 20 м 2 и построенную без теплоизоляции при -15 0 С электрическим обогревателем мощностью 1 кВт, а небольшую ванную комнату, расположенную в центре кирпичного дома запросто.
Количество тепла, которое требуется помещению для обогрева, измеряется в килокалориях, а мощности приборов в ваттах, поэтому для перевода одного значения в другое нужно килокалории поделить на 860 и получатся кВт.
Все производители отопительного оборудования обязательно указывают тепловую мощность прибора в паспорте или инструкции. Однако, следует учитывать, что указанная мощность достигается при соблюдении всех условий эксплуатации т.е. для водяных конвекторов или радиаторов имеет значение температура теплоносители, а для газовых приборов давление газа.
Поэтому помимо мощности отопления производители указывают, для каких условий эксплуатации предназначено оборудование.
Например, если у вас старая система центрального отопления с температурой нагрева 40-50 0 С, рекомендуется приобретать конвекторы для низкотемпературных систем отопления.
Единицы измерения.
Перевод единиц измерения тепла.
Калькулятор теплоты. Перевод единиц измерения теплоты (Дж, кДж, МДж, кал, ккал, Мкал, Гкал, эрг, кВт*ч и т.д.)
Введите количество теплоты (QQ)
Результат перевода единиц измерения теплоты (QQ)
Результаты работы калькулятора теплоты при переводе в другие единицы измерения теплоты:
Примеры результатов работы калькулятора теплоты:
/ 0 Гкал = 0 Дж
//
1 кал = 1.0E-9 Гкал
//
0 кВт*ч = 0 эрг
//
0 кВт*ч = 0 Мкал
//
10 кал = 4.1868E-5 МДж
//
0 кВт*ч = 0 Дж
/
Поделится ссылкой на расчет:
Простейший расчет тепловой мощности обогревателя
Существует общепринятый стандарт расчета тепловой мощности обогревателя при высоте помещения не более 3 м. На 10 метров квадратных площади устанавливается 1 кВт мощности прибора.
Эта формула неплохо работает при расчетах электрических отопительных приборов в помещениях с идеальными условиями — высокой теплоизоляцией, минимальной теплопотерей и одним окном с утепленным стеклопакетом. Но существует и примитивный вариант расчета, позволяющий учитывать и высоту комнат.
Простой расчет тепловой нагрузки (Q) помещения:
V (объем помещения/м3) х 40 Вт/1000 = Q (кВт/ч)
Эта формула не позволяет допустить ошибок, связанных с грубым расчетом по принципу 1 кВт на 10 м 2 т.к., учитывает объем комнаты включая высоту потолков. Однако и при таком расчёте легко совершить оплошность и приобрести «слабый» прибор — не учтено много важных факторов.
Пример расчетов
Вводные данные: гостиная в частном доме, ВхШхД – 4х5х6 м.
По первой формуле мы выясняем площадь помещения – 5х6 = 30 м 2 и умножаем на 1 кВт. Получается, что нам потребуется обогреватель на 3 кВт.
Но эти расчеты не гарантируют, что, купив обогреватель мощностью 3 кВт, вы получите комфортную температуру в помещении — в столь примитивном расчете даже не учитывается температура за окном. Если в средней полосе 3 кВт могут и справится с отоплением такой гостиной, но на севере с -35 за окном можете не сомневаться, разочарование от покупки и стучащие зубы вам обеспечены.
По второй формуле мы выясняем объем помещения – 4х5х6 = 120 м 3 .
Формула расчета тепловой нагрузки с учетом разницы температур
Для более точного определения требуемой тепловой мощности обогревателя или конвектора рекомендуем воспользоваться следующими формулой.
V (объем помещения) х T (разница температур) х φ (коэффициент теплопотери) = ккал/ч
- V – это упоминаемый выше объем комнаты: ширина * длину * высоты.
- Т (разница температур) – в зависимости от климатической зоны температура на улице может составлять и -5 0 С и -30 0 С. Поэтому в формулу введен параметр выражающий разницу между средней зимней температурой на улице и желаемой температурой в помещении. Пример: среднее зимнее значение на улице составляет -15 0 С, а в комнате требуется 25 0 С – получается Т = 40 0 С.
- φ – коэффициент теплопотерь помещений в зависимости от конструкции и изоляции. 3-4 – отсутствие теплоизоляции. Простые деревянные или металлические строения без изоляции.
- 2-2,9 – низкая теплоизоляция. Кладка в один кирпич, упрощенная конструкция строений, одинарные окна.
- 1-1,9 – средняя теплоизоляция. Строения с кладкой в два кирпича, стандартные здания, обычная кровля, небольшое количество окон.
- 0,6-0,9 — высокая теплоизоляция. Мало окон, сдвоенные рамы, кирпичные стены, двойная теплоизоляция, утепленная крыша и толстое основание пола.
Для получения значения мощности конвектора или обогревателя в киловаттах требуется получившееся в число разделить на 860.
Пример расчетов
Вводные данные: гостиная в частном доме, ВхШхД – 4х5х6 м. Дом построен кладкой в два кирпича, на хорошем основании (фундамент), с большим панорамным окном. Средняя температура зимой -15 0 С, желаемая температура в комнате +22 0 С.
- Выясняем объем помещения – 4х5х6х = 120 м 3 .
- Определяем разницу температур – 15+22=37 0 С.
- Подбираем коэффициент – возьмем среднее значение 1,4 т.к. несмотря на стены в два кирпича и утолщенный пол присутствует большое окно.
Подставляем данные в формулу:
V х T х φ = 120 х 37 х 1,4 = 6216 ккал .
Переводим килокалории в кВт – 6216/860= 7,2 кВт.
Получается, что для получения требуемой температуры в гостиной нам потребуется установить обогревательный прибор на 7 кВт.
Естественно в данном случае и речи не может быть об установке электрических приборов. Такие значения можно получить при установке газовых или водяных конвекторов, радиаторных батарей, тепловых пушек и т.д. Однако с учетом размеров гостиной, подобная мощность излишня — снова нет в расчете некоторых важных нюансов.
Формула расчета тепловой мощности с учетом дополнительных факторов
Несмотря на введение коэффициента потерь тепла предыдущая формула не способна отразить всевозможные нюансы помещений. Наример теплопотери квартиры расположенной на 5 этаже в центре девятиэтажного здания ниже, чем у угловой квартиры на последнем этаже. Для получения более точных данных рекомендуем воспользоваться формулой:
Q = (100 Вт/м 2 х S х φ 1 х φ 2 х φ 3 х φ 4 х φ 5 х φ 6 х φ 7)/1000
- S – площадь помещения в м 2 .
- φ 1 – потери тепла через окна: 0,85 – тройной стеклопакет;
- 1 – двойной стеклопакет;
- 1,27 – одинарный стеклопакет (стандартный).
- 0,854 – высокое;
- 1,2 – 50%;
- 1,5 – -35 0 С;
- 1,4 -4;
- 0,8 – обогреваемое;
- 1,2 – 4,5м;
Как видите в формуле расчета тепловой мощности обогревательного оборудования учтено значительно больше значений влияющих на теплопотери.
Пример расчета
Вводные данные: гостиная в частном доме, ВхШхД – 4х5х6 м. Дом построен кладкой в два кирпича, на утепленном фундаменте с большим панорамным окном, со стандартным остеклением, занимающим 50% от площади пола. Средняя температура зимой -15 0 С. На втором этаже отапливаемые спальни, две стены выходят на улицу.
Выясняем требуемые значения и коэффициенты:
- S – 30м 2 .
- φ 1 – 1,27.
- φ 2 – 1.
- φ 3 – 1,2.
- φ 4 – 0,9.
- φ 5 – 1,2.
- φ 6 – 0,8.
- φ 7 – 1,15.
Подставляем значения в формулу:
Q = (100 Вт/м 2 х S х φ 1 х φ 2 х φ 3 х φ 4 х φ 5 х φ 6 х φ 7)/1000
Q = (100 Вт/м 2 х 30 х 1,27 х 1 х 1,2 х 0,9 х 1,2 х 0,8 х 1,15)/1000 = 4,543 кВт
Исходя из этого уточненного расчета, получается, что нам нужно организовать отопление на 4,5-5 кВт.
Эта формула предпочтительна для расчета тепловой мощности отопительных систем, причем она подходит для расчета отопления в небольших жилых помещениях и в организации отопления промышленных объектов.
Важно! Для увеличения срока службы теплового оборудования и для учета непредвиденных ситуаций, рекомендуется добавлять небольшой запас в 10-15 %.к полученной тепловой мощности.
О тепловой энергии простым языком!
Человечеству известно немного видов энергии – механическая энергия (кинетическая и потенциальная), внутренняя энергия (тепловая), энергия полей (гравитационная, электромагнитная и ядерная), химическая. Отдельно стоит выделить энергию взрыва,…
…энергию вакуума и еще существующую только в теории – темную энергию. В этой статье, первой в рубрике «Теплотехника», я попытаюсь на простом и доступном языке, используя практический пример, рассказать о важнейшем виде энергии в жизни людей — о тепловой энергии и о рождающей ее во времени тепловой мощности.
Несколько слов для понимания места теплотехники, как раздела науки о получении, передаче и применении тепловой энергии. Современная теплотехника выделилась из общей термодинамики, которая в свою очередь является одним из разделов физики. Термодинамика – это дословно «теплый» плюс «силовой». Таким образом, термодинамика – это наука об «изменении температуры» системы.
Воздействие на систему извне, при котором изменяется ее внутренняя энергия, может являться результатом теплообмена. Тепловая энергия, которая приобретается или теряется системой в результате такого взаимодействия с окружающей средой, называется количеством теплоты и измеряется в системе СИ в Джоулях.
Если вы не инженер-теплотехник, и ежедневно не занимаетесь теплотехническими вопросами, то вам, столкнувшись с ними, иногда без опыта бывает очень трудно быстро в них разобраться. Трудно без наличия опыта представить даже размерность искомых значений количества теплоты и тепловой мощности. Сколько Джоулей энергии необходимо чтобы нагреть 1000 метров кубических воздуха от температуры -37˚С до +18˚С. Какая нужна мощность источника тепла, чтобы сделать это за 1 час. На эти не самые сложные вопросы способны сегодня ответить «сходу» далеко не все инженеры. Иногда специалисты даже помнят формулы, но применить их на практике могут лишь единицы!
Прочитав до конца эту статью, вы сможете легко решать реальные производственные и бытовые задачи, связанные с нагревом и охлаждением различных материалов. Понимание физической сути процессов теплопередачи и знание простых основных формул – это главные блоки в фундаменте знаний по теплотехнике!
Количество теплоты при различных физических процессах.
Большинство известных веществ могут при разных температуре и давлении находиться в твердом, жидком, газообразном или плазменном состояниях. Переход из одного агрегатного состояния в другое происходит при постоянной температуре (при условии, что не меняются давление и другие параметры окружающей среды) и сопровождается поглощением или выделением тепловой энергии. Не смотря на то, что во Вселенной 99% вещества находится в состоянии плазмы, мы в этой статье не будем рассматривать это агрегатное состояние.
Рассмотрим график, представленный на рисунке. На нем изображена зависимость температуры вещества Т от количества теплоты Q, подведенного к некой закрытой системе, содержащей определенную массу какого-то конкретного вещества.
1. Твердое тело, имеющее температуру T1, нагреваем до температуры Tпл, затрачивая на этот процесс количество теплоты равное Q1.
2. Далее начинается процесс плавления, который происходит при постоянной температуре Тпл (температуре плавления). Для расплавления всей массы твердого тела необходимо затратить тепловой энергии в количестве Q2—Q1.
3. Далее жидкость, получившаяся в результате плавления твердого тела, нагреваем до температуры кипения (газообразования) Ткп, затрачивая на это количество теплоты равное Q3— Q2.
4. Теперь при неизменной температуре кипения Ткп жидкость кипит и испаряется, превращаясь в газ. Для перехода всей массы жидкости в газ необходимо затратить тепловую энергию в количестве Q4— Q3.
5. На последнем этапе происходит нагрев газа от температуры Ткп до некоторой температуры Т2. При этом затраты количества теплоты составят Q5— Q4. (Если нагреем газ до температуры ионизации, то газ превратится в плазму.)
Таким образом, нагревая исходное твердое тело от температуры Т1 до температуры Т2 мы затратили тепловую энергию в количестве Q5, переводя вещество через три агрегатных состояния.
Двигаясь в обратном направлении, мы отведем от вещества то же количество тепла Q5, пройдя этапы конденсации, кристаллизации и остывания от температуры Т2 до температуры Т1. Разумеется, мы рассматриваем замкнутую систему без потерь энергии во внешнюю среду.
Заметим, что возможен переход из твердого состояния в газообразное состояние, минуя жидкую фазу. Такой процесс именуется возгонкой, а обратный ему процесс – десублимацией.
Итак, уяснили, что процессы переходов между агрегатными состояниями вещества характеризуются потреблением энергии при неизменной температуре. При нагреве вещества, находящегося в одном неизменном агрегатном состоянии, повышается температура и также расходуется тепловая энергия.
Применение расчетов по изменению количества теплоты
Вероятно, читатель скажет, что все это весьма познавательно, но зачем же нас так мучают в школе этими формулами. А сейчас мы приведем примеры, в каких областях человеческой деятельности они нужны непосредственно и как это касается любого в его повседневности.
Для начала посмотрите вокруг себя и посчитайте: сколько предметов из металла вас окружают? Наверняка больше десяти. Но прежде чем стать скрепкой, вагоном, кольцом или флешкой, любой металл проходит выплавку. Каждый комбинат, на котором перерабатывают, допустим, железную руду, должен понимать, сколько требуется топлива, чтобы оптимизировать расходы. А рассчитывая это, необходимо знать теплоемкость металлосодержащего сырья и количество теплоты, которое ему необходимо сообщить, чтобы произошли все технологические процессы. Так как выделяемая единицей топлива энергия рассчитывается в джоулях или калориях, то формулы нужны непосредственно.
Или другой пример: в большинстве супермаркетов есть отдел с замороженными товарами – рыбой, мясом, фруктами. Там, где сырье из мяса животных или морепродуктов превращается в полуфабрикат, должны знать, сколько электричества употребят холодильные и морозильные установки на тонну или единицу готового продукта. Для этого следует рассчитать, какое количество теплоты теряет килограмм клубники или кальмаров при охлаждении на один градус Цельсия. А в итоге это покажет, сколько электричества потратит морозильник определенной мощности.
Главные формулы теплопередачи.
Формулы очень просты.
Количество теплоты Q в Дж рассчитывается по формулам:
1. Со стороны потребления тепла, то есть со стороны нагрузки:
1.1. При нагревании (охлаждении):
m – масса вещества в кг
с – удельная теплоемкость вещества в Дж/(кг*К)
1.2. При плавлении (замерзании):
λ – удельная теплота плавления и кристаллизации вещества в Дж/кг
1.3. При кипении, испарении (конденсации):
r – удельная теплота газообразования и конденсации вещества в Дж/кг
2. Со стороны производства тепла, то есть со стороны источника:
2.1. При сгорании топлива:
q – удельная теплота сгорания топлива в Дж/кг
2.2. При превращении электроэнергии в тепловую энергию (закон Джоуля — Ленца):
I – действующее значение тока в А
U – действующее значение напряжения в В
R – сопротивление нагрузки в Ом
Делаем вывод – количество теплоты прямо пропорционально массе вещества при всех фазовых превращениях и при нагреве дополнительно прямо пропорционально разности температур. Коэффициенты пропорциональности ( c, λ , r , q ) для каждого вещества имеют свои значения и определены опытным путем (берутся из справочников).
Количество теплоты
Как известно, при различных механических процессах происходит изменение механической энергии W
meh. Мерой изменения механической энергии является работа сил, приложенных к системе:
(~Delta W_{meh} = A.)
При теплообмене происходит изменение внутренней энергии тела. Мерой изменения внутренней энергии при теплообмене является количество теплоты.
Количество теплоты
— это мера изменения внутренней энергии, которую тело получает (или отдает) в процессе теплообмена.
Таким образом, и работа, и количество теплоты характеризуют изменение энергии, но не тождественны энергии. Они не характеризуют само состояние системы, а определяют процесс перехода энергии из одного вида в другой (от одного тела к другому) при изменении состояния и существенно зависят от характера процесса.
Основное различие между работой и количеством теплоты состоит в том, что работа характеризует процесс изменения внутренней энергии системы, сопровождающийся превращением энергии из одного вида в другой (из механической во внутреннюю). Количество теплоты характеризует процесс передачи внутренней энергии от одних тел к другим (от более нагретых к менее нагретым), не сопровождающийся превращениями энергии.
Опыт показывает, что количество теплоты, необходимое для нагревания тела массой m
от температуры
T
1 до температуры
T
2, рассчитывается по формуле
(~Q = cm (T_2 — T_1) = cm Delta T, qquad (1))
где c
— удельная теплоемкость вещества;
(~c = frac{Q}{m (T_2 — T_1)}.)
Единицей удельной теплоемкости в СИ является джоуль на килограмм-Кельвин (Дж/(кг·К)).
Удельная теплоемкость
c
численно равна количеству теплоты, которое необходимо сообщить телу массой 1 кг, чтобы нагреть его на 1 К.
Теплоемкость
тела
C
T численно равна количеству теплоты, необходимому для изменения температуры тела на 1 К:
(~C_T = frac{Q}{T_2 — T_1} = cm.)
Единицей теплоемкости тела в СИ является джоуль на Кельвин (Дж/К).
Для превращения жидкости в пар при неизменной температуре необходимо затратить количество теплоты
(~Q = Lm, qquad (2))
где L
— удельная теплота парообразования. При конденсации пара выделяется такое же количество теплоты.
Для того чтобы расплавить кристаллическое тело массой m
при температуре плавления, необходимо телу сообщить количество теплоты
(~Q = lambda m, qquad (3))
где λ
— удельная теплота плавления. При кристаллизации тела такое же количество теплоты выделяется.
Количество теплоты, которое выделяется при полном сгорании топлива массой m
,
(~Q = qm, qquad (4))
где q
— удельная теплота сгорания.
Единица удельных теплот парообразования, плавления и сгорания в СИ — джоуль на килограмм (Дж/кг).