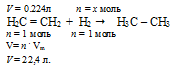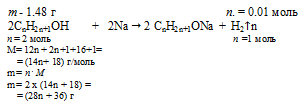Определение молекулярной формулы спирта
Наиболее распространены в тестах ЕГЭ задачи, в которых расчет ведется по уравнению реакции. Рассмотрим наиболее сложную из них.
Задача 2.6.
При взаимодействии 1,48 г предельного одноатомного спирта с металлическим натрием выделился водород в количестве, достаточном для гидрирования 224 мл этилена (н.у.). Определите молекулярную формулу спирта.
Дано:
масса предельного одноатомного спирта: m(спирта) = 1,48 г;
объем этилена (н.у.): V(С2Н4) = 224 мл.
Найти: формулу исходного спирта.
Решение:
Шаг 1. В состав предельного одноатомного спирта входят углерод, водород и один атом кислорода. Общая формула имеет вид: СnH2n+1ОН.
Шаг 2. В условии описаны две последовательные химические реакции:
2СnH2n+1ОН + 2Na —> 2СnH2n+1ОNa + H2
Водород, выделившийся в первой реакции, участвует, во взаимодействии с этиленом:
Н2С = СН2 + Н2 —> Н3С – СН3
Шаг 3 и 4. Соотношение атомов и простейшая формула спирта однозначно определяется по общей формуле, но эти данные не помогут нам при выявлении истинной формулы.
Шаг 5. Для выявления значения «n» в общей формуле спирта необходимо сопоставить массу спирта с количеством образовавшегося водорода по первому уравнению реакции. Количество образовавшегося водорода можно определить по второй реакции гидрирования.
а) Определение количества вещества водорода1:
Составляем пропорцию:
0,224 л Н2С = СН2 взаимодействуют с х моль Н2 (по условию)
22,4 л Н2С = СН2 взаимодействуют с 1 моль Н2 (по уравнению)
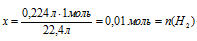
б) Водород, принявший участие в реакции с этиленом, выделился в первой реакции спирта с металлическим натрием. Следовательно, можно использовать полученные данные для сопоставления с массой исходного спирта.
Составляем пропорцию:
1,48 г СnH2n+1ОН дает 0,01 моль Н2 (по условию)
(28n + 36) г СnH2n+1ОН дает 1 моль Н2 (по уравнению)
1,48 . 1 = (28n + 36) . 0,01
Получили математическое уравнение с одним неизвестным. Решая его, получаем: n = 4.
Подставляем это значение в общую формулу спирта:
С4Н9ОН.
Ответ: С4Н9ОН.
Данная задача была осложнена двумя последовательными уравнениями реакций. Для сопоставления данных с целью определения неизвестного индекса в общей формуле нам
пришлось проводить дополнительный расчет по второму химическому уравнению. В большинстве задач ЕГЭ в условии описана лишь одна реакция и присутствуют данные о двух веществах в ней. После записи уравнения с использованием общей формулы можно сразу приступать к сопоставлению данных и выявлению неизвестных индексов.
Комментарии:
1 Объем газообразного этилена в условии выражен в миллилитрах. Для использования этого данного в пропорции необходимо перевести его в литры, т.к. молярный объем измеряется в л/моль. Ошибку, связанную с приведением данных к одним единицам измерения делают многие учащиеся.
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.
Установите молекулярную формулу предельного одноатомного спирта зная что 18, 5 г его в реакции с некоторым щелочным металлом выделяет 2, 8 л водорода (н.
У. ) ПОМОГИТЕ ПОЖАЛУЙСТААА.
На этой странице находится вопрос Установите молекулярную формулу предельного одноатомного спирта зная что 18, 5 г его в реакции с некоторым щелочным металлом выделяет 2, 8 л водорода (н?, относящийся к категории
Химия. По уровню сложности данный вопрос соответствует знаниям
учащихся 5 – 9 классов. Здесь вы найдете правильный ответ, сможете
обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С
помощью автоматического поиска на этой же странице можно найти похожие
вопросы и ответы на них в категории Химия. Если ответы вызывают
сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.

locer
+10
Решено
7 лет назад
Химия
10 – 11 классы
плотность паров спирта по кислороду равна 2,75. Определите молекулярную формулу спирта
решите , плиз
Смотреть ответ
1
Ответ
5
(2 оценки)
2
DashaNikitina451
7 лет назад
Светило науки – 459 ответов – 0 раз оказано помощи
Формула спирта общая: CnH2n+1OH
M(CnH2n+1OH) = D(по кислороду)*M(O2) = 2,75*32 = 88 г/моль
12n+2n+1+16+1 = 88
14n = 70
n = 5 => C5H11OH
12,1,16 – атомные массы соответственно C ,H,O из таблицы Менделеева. n – их количество.
(2 оценки)
https://vashotvet.com/task/8691883
Предельные одноатомные спирты

4.6
Средняя оценка: 4.6
Всего получено оценок: 454.
4.6
Средняя оценка: 4.6
Всего получено оценок: 454.
Вещества, образованные от предельных углеводородов и содержащие гидроксильную группу (-ОН), называются насыщенными или предельными одноатомными спиртами. Названия спиртов совпадают с названиями алканов в гомологическом ряду с суффиксом «-ол».
Строение
Общая формула предельных одноатомных спиртов – CnH2n+1-OH. Гидроксил является функциональной группой и определяет физические и химические свойства спиртов.
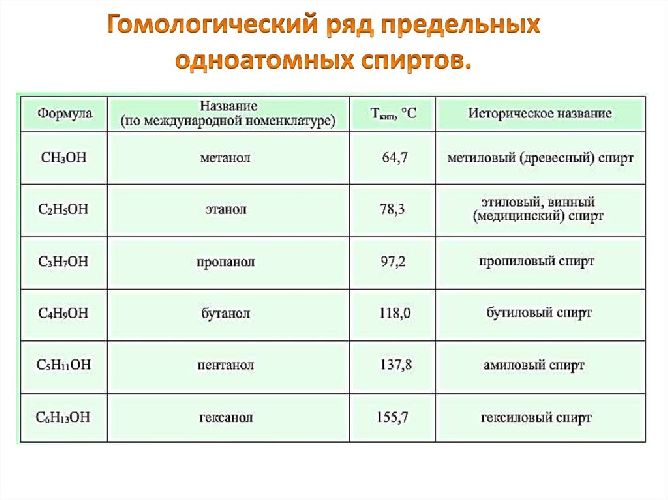
Основные одноатомные спирты (гомологический ряд метанола):
- метанол или метиловый спирт – CH3OH;
- этанол или этиловый спирт – C2H5OH;
- пропанол – C3H7OH;
- бутанол – C4H9OH;
- пентанол – C5H11OH.
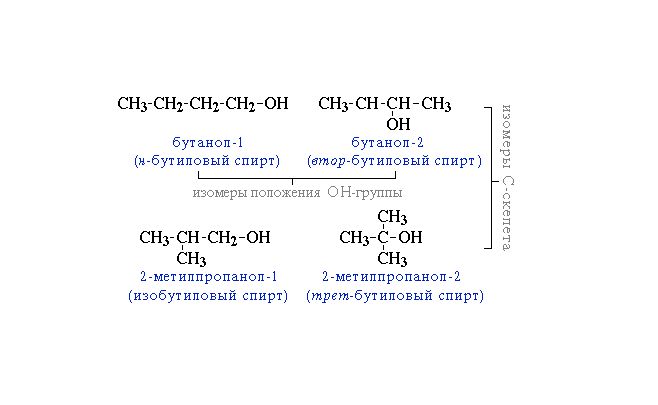
Насыщенным спиртам свойственна структурная и межклассовая изомерия. В зависимости от расположения гидроксильной группы в молекуле вещества различают:
- первичные спирты – гидроксил прикреплён к первому атому углерода;
- вторичные спирты – гидроксил находится у второго атома углерода;
- третичные спирты – гидроксил соединён с третьим атом углерода.
Начиная с бутанола, наблюдается изомерия углеродного скелета. В этом случае название спирта записывается с двумя цифрами: первая указывает на положение метильной группы, вторая – гидроксила.
Одноатомные спирты образуют межклассовые изомеры с простыми эфирами – этиловый спирт (CH3CH2-OH), диметиловый эфир (CH3-O-CH3).
Несмотря на то, что пропанол содержит три атома углерода, он может образовывать только два изомера по гидроксильной группе – пропанол-1 и пропанол-2.
Свойства
В зависимости от количества атомов углерода меняется агрегатное состояние одноатомных спиртов. Если в молекуле до 15 атомов углерода, то это жидкость, больше 15 – твёрдое вещество. Хорошо смешиваются с водой первые два спирта из гомологического ряда – метанол и этанол, а также структурный изомер пропанол-2.
Все спирты плавятся и кипят при высоких температурах.
Активность спиртов объясняется наличием О-Н и С-О связей, которые легко разрываются. Основные химические свойства одноатомных спиртов приведены в таблице.
|
Реакция |
Описание |
Уравнение |
|
С металлами |
Реагируют только со щелочными и щелочноземельными металлами с разрывом связи О-Н |
2C2H5OH + 2К → 2С2Н5ОК + Н2 |
|
С кислородом |
Горят в присутствии перманганата или дихромата калия (KMnO4, K2Cr2O7) |
C2H5OH + 3O2 → 2CO2 + H2O |
|
C галогеноводородами |
Гидроксильная группа вытесняется галогеном |
C2H5OH + HBr → C2H5Br + H2O |
|
С кислотами |
Реагируют с минеральными и органическими кислотами с образованием сложных эфиров |
C2H5OH + CH3COOH → CH3COOC2H5 |
|
С оксидами металлов |
Качественная реакция с образование альдегида |
C2H5OH + CuO → CH3COH + H2O + Cu |
|
Дегидратация |
Протекает в присутствии сильной кислоты при высокой температуре |
C2H5OH → C2H4 + H2O |
|
С карбоновыми кислотами |
Реакция этерификации – образование сложных эфиров |
C2H5OH + CH3COOH → CH3COOC2H5 + H2O |
Одноатомные спирты имеют широкое применение в промышленности. Наиболее активно применяется этанол. Его используют для изготовления парфюмерии, уксусной кислоты, лекарств, лаков, красителей, растворителей и других веществ.
Что мы узнали?
Из урока химии узнали, что предельные или насыщенные одноатомные спирты являются производными предельных углеводородов с одной гидроксильной группой (гидроксилом). Это жидкости или твёрдые вещества в зависимости от количества атомов углерода. Одноатомные спирты образуют изомеры по гидроксильной, метильной группе и с простыми эфирами. Предельные одноатомные спирты реагируют со щелочными металлами, кислотами, оксидами. Используются для изготовления лекарств, растворителей, кислот.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
-
Лидия Маслова
5/5
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 454.
А какая ваша оценка?