Molar mass of C6H5OH = 94.11124 g/mol
Convert grams Phenol to moles
or
moles Phenol to grams
Molecular weight calculation:
12.0107*6 + 1.00794*5 + 15.9994 + 1.00794
Percent composition by element
Element: Hydrogen
Symbol: H
Atomic Mass: 1.00794
# of Atoms: 6
Mass Percent: 6.426%
Element: Carbon
Symbol: C
Atomic Mass: 12.0107
# of Atoms: 6
Mass Percent: 76.573%
Element: Oxygen
Symbol: O
Atomic Mass: 15.9994
# of Atoms: 1
Mass Percent: 17.001%
Calculate the
molecular weight of a chemical compound
More information
on molar mass and molecular weight
In chemistry, the formula weight is a quantity computed by multiplying the atomic weight (in atomic mass units) of each element in a chemical formula by the number of atoms of that element present in the formula, then adding all of these products together.
Formula weights are especially useful in determining the relative weights of reagents and products in a chemical reaction. These relative weights computed from the chemical equation are sometimes called equation weights.
A common request on this site is to convert grams to moles. To complete this calculation, you have to know what substance you are trying to convert. The reason is that the molar mass of the substance affects the conversion. This site explains how to find molar mass.
Finding molar mass starts with units of grams per mole (g/mol). When calculating molecular weight of a chemical compound, it tells us how many grams are in one mole of that substance. The formula weight is simply the weight in atomic mass units of all the atoms in a given formula.
Using the chemical formula of the compound and the periodic table of elements, we can add up the atomic weights and calculate molecular weight of the substance.
The atomic weights used on this site come from NIST, the National Institute of Standards and Technology. We use the most common isotopes. This is how to calculate molar mass (average molecular weight), which is based on isotropically weighted averages. This is not the same as molecular mass, which is the mass of a single molecule of well-defined isotopes. For bulk stoichiometric calculations, we are usually determining molar mass, which may also be called standard atomic weight or average atomic mass.
If the formula used in calculating molar mass is the molecular formula, the formula weight computed is the molecular weight. The percentage by weight of any atom or group of atoms in a compound can be computed by dividing the total weight of the atom (or group of atoms) in the formula by the formula weight and multiplying by 100.
| Фенол | ||
|---|---|---|
|
||
| Общие | ||
| Систематическое наименование |
Гидроксибензол | |
| Традиционные названия | Фенол, карболовая кислота, карбо́лка, бензоло́л; оксибензо́л | |
| Хим. формула | C6H6O | |
| Рац. формула | C6H5OH | |
| Физические свойства | ||
| Состояние | Твёрдое | |
| Молярная масса | 94,11 г/моль | |
| Плотность | 1,07 г/см³ | |
| Энергия ионизации | 8,5 ± 0,1 эВ[1] | |
| Термические свойства | ||
| Температура | ||
| • плавления | 41 °C | |
| • кипения | 181,84 °C | |
| • вспышки | 79 (в закрытом тигле), 85 (в открытом) °C | |
| Пределы взрываемости | 1,8 ± 0,1 об.%[1] | |
| Мол. теплоёмк. | 134,7 (кр.) Дж/(моль·К) | |
| Энтальпия | ||
| • образования | −162,944 кДж/моль | |
| Давление пара | 0,4 ± 0,1 мм рт.ст.[1] | |
| Химические свойства | ||
Константа диссоциации кислоты  |
9,89 ± 0,01[2] | |
| Растворимость | ||
| • в воде | 6,5 г/100 мл | |
| Структура | ||
| Гибридизация | sp2-гибридизация | |
| Классификация | ||
| Рег. номер CAS | 108-95-2 | |
| PubChem | 996 | |
| Рег. номер EINECS | 203-632-7 | |
| SMILES |
OC1=CC=CC=C1 |
|
| InChI |
InChI=1S/C6H6O/c7-6-4-2-1-3-5-6/h1-5,7H ISWSIDIOOBJBQZ-UHFFFAOYSA-N |
|
| RTECS | SJ3325000 | |
| ChEBI | 15882 | |
| Номер ООН | 1671 | |
| ChemSpider | 971 | |
| Безопасность | ||
| ЛД50 | 140 мг/кг (морская свинка, внутрижелудочно) | |
| Токсичность | Токсичен, весьма едкий, является сильным ирритантом | |
| Фразы риска (R) | R23/24/25, R34, R48/20/21/22, R68 | |
| Фразы безопасности (S) | S24/25, S26, S28, S36/37/39, S45 | |
| Краткие характер. опасности (H) |
H301, H311, H331, H314, H341, H373 |
|
| Меры предостор. (P) |
P260, P301+P310, P303+P361+P353, P305+P351+P338, P361, P405, P501 |
|
| Сигнальное слово | опасно | |
| Пиктограммы СГС |
|
|
| NFPA 704 |
2 3 0 |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | ||

Игольчатые кристаллы фенола

Сильно окислившийся при длительном хранении фенол
Фено́л (гидро́ксибензо́л, от устар. «карбо́ловая кислота́», химическая формула — C6H6O или C6H5OH) — органическое соединение, возглавляющее класс фенолов.
При стандартных условиях фенол — это бесцветные игольчатые кристаллы, розовеющие на воздухе, с характерным запахом. Токсичен, является сильным ирритантом.
Соли и эфиры фенола называются феноля́тами.
История[править | править код]
Фенол был обнаружен в 1834 году Фридлибом Фердинандом Рунге, который извлёк его (в нечистом виде) из каменноугольной смолы[3]. Рунге назвал фенол «Karbolsäure» (угольно-масляная кислота, карболовая кислота). Каменноугольная смола оставалась основным источником получения фенола до развития нефтехимической промышленности. В 1841 году французский химик Огюст Лоран получил фенол в чистом виде[4].
В 1836 году Огюст Лоран придумал название «фен» для бензола[5], это корень слов «фенол» и «фенил». В 1843 году французский химик Шарль Герхардт придумал название «фенол»[6].
Антисептические свойства фенола использовал сэр Джозеф Листер (1827—1912) в своей пионерской технике антисептической хирургии. Листер решил, что сами раны должны быть тщательно очищены. Затем он покрыл раны кусочком тряпки или ворса[7], покрытого фенолом или «карболовой кислотой», как он её называл. Раздражение кожи, вызванное постоянным воздействием фенола, в конечном итоге привело к внедрению асептических методов в хирургию.
Физические свойства[править | править код]
Представляет собой бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к образованию окрашенных веществ (это связано с промежуточным образованием хинонов). Обладает специфическим запахом (таким, как запах гуаши, так как в состав гуаши входит фенол).
Умеренно растворим в воде (6 г на 100 г воды), в растворах щелочей, в спирте, в бензоле, в ацетоне. 5%-й раствор в воде — антисептик, широко применявшийся в медицине в прошлом.
Химические свойства[править | править код]
Из-за наличия ароматического кольца и гидроксильной группы фенол проявляет химические свойства, характерные как для спиртов, так и для ароматических углеводородов.
По гидроксильной группе:
- Обладает слабыми кислотными свойствами (более сильными, чем у спиртов), при действии щелочей образует соли — феноляты (например, фенолят натрия — C6H5ONa)[8]:
Фенол — настолько слабая кислота, что даже угольная кислота вытесняет его из фенолятов:
Более интенсивно феноляты разлагаются под действием сильных кислот, например, под действием серной кислоты:
Взаимодействие с металлическим натрием:
Фенол непосредственно не этерифицируется карбоновыми кислотами, эфиры можно получить при взаимодействии фенолятов с ангидридами или галогенангидридами кислот:
Образование простых эфиров. Для получения простых эфиров фенола действуют галогеналканами или галогенпроизводными аренов на феноляты. В первом случае получают смешанные жирно-ароматические простые эфиры:
Во втором случае получают чисто-ароматические простые эфиры:
Реакция проводится в присутствии порошкообразной меди, которая служит катализатором.
При перегонке фенола с цинковой пылью происходит замещение гидроксильной группы водородом[9]:
Фенол вступает в реакции электрофильного замещения по ароматическому кольцу. Гидроксогруппа, являясь одной из самых сильных донорных групп (вследствие уменьшении электронной плотности на функциональной группе), увеличивает реакционную способность кольца к этим реакциям и направляет замещение в орто- и пара-положения[10]. Фенол с лёгкостью алкилируется, ацилируется, галогенируется, нитруется и сульфируется.
Реакция Кольбе — Шмитта служит для синтеза салициловой кислоты и её производных (ацетилсалициловой кислоты и других).
Взаимодействие с бромной водой (качественная реакция на фенол):
Образуется 2,4,6-трибромфенол — твёрдое вещество белого цвета.
Взаимодействие с концентрированной азотной кислотой:
Взаимодействие с хлоридом железа(III) (качественная реакция на фенол[11]):
Реакция присоединения: гидрирование фенола в присутствии металлических катализаторов приводит к образованию циклогексанола и циклогексанона:
Окисление фенола: вследствие наличия гидроксильной группы в молекуле фенола устойчивость к окислению намного ниже, чем у бензола. В зависимости от природы окислителя и условия проведения реакции получаются различные продукты. Так, под действием пероксида водорода в присутствии железного катализатора образуется небольшое количество двухатомного фенола — пирокатехина:
При взаимодействии более сильных окислителей (хромовая смесь, диоксид марганца в кислой среде) образуется пара-хинон.
Получение[править | править код]
В настоящее время производство фенола в промышленном масштабе осуществляется тремя способами:
- кумольный метод. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол. 95 % всего производимого в мире фенола производят этим методом. Способ был изобретён советскими учёными П. Г. Сергеевым, Н. М. Горнасталевой, Р. Ю. Удрисом, Б. Д. Кружаловым. По сравнению с большинством других процессов, процесс кумола использует относительно мягкие условия синтеза и относительно недорогое сырьё. Однако, чтобы работать экономно, должен быть спрос как на фенол, так и на ацетон[12][13]. В 2010 году мировой спрос на ацетон составлял примерно 6,7 миллиона тонн, 83 процента из которых были удовлетворены ацетоном, полученным кумольным методом;
- окисление толуола, с промежуточным образованием бензойной кислоты (около 3 %);
- выделением из каменноугольной смолы.
Фенол также можно получить восстановлением хинона.
Биологическая роль[править | править код]
Протеиногенная аминокислота тирозин является структурным производным фенола и может быть рассмотрена как пара-замещённый фенол или α-замещённый пара-крезол. В природе распространены и другие фенольные соединения, в том числе полифенолы.
В свободном виде фенол встречается у некоторых микроорганизмов и находится в равновесии с тирозином. Равновесие поддерживает фермент тирозин-фенол-лиаза (КФ 4.1.99.2).
Биологическое значение фенола обычно рассматривается в рамках его воздействия на окружающую среду. Фенол — один из промышленных загрязнителей. В чистом виде фенол довольно токсичен для животных и человека. Фенол губителен для многих микроорганизмов, поэтому промышленные сточные воды с высоким содержанием фенола плохо поддаются биологической очистке.
Применение[править | править код]
Мировое производство фенола на 2006 год составляет 8,3 млн т/год. По объёму производства фенол занимает 33-е место среди всех выпускаемых химической промышленностью веществ и 17-е место среди органических веществ[источник не указан 1672 дня]. По данным на 2006 год мировое потребление фенола имеет следующую структуру:
- 43 % фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбонатов и эпоксидных смол;
- 30 % фенола расходуется на производство фенолформальдегидных смол;
- 12 % фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон — нейлона и капрона[14];
- в России большое количество фенола используется в нефтепереработке, в частности, для селективной очистки масел на технологических установках типа 37/1 и А-37/1. Фенол проявляет высокую селективность и эффективность при удалении из масел смолистых веществ, различных полициклических ароматических углеводородов с короткими боковыми цепями, а также соединений, содержащих серу[15];
- остальной фенол расходуется на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ — полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов. Раствор 1,4 % фенола применяется в медицине (орасепт) как обезболивающее и антисептическое средство[16].
Фенол и его производные обусловливают консервирующие свойства коптильного дыма.
В косметологии — как химический пилинг (токсично).
- в скотоводстве — дезинфекция животных растворами фенола и его производных.
- в косметологии — для проведения глубокого пилинга.
Токсические свойства[править | править код]
Фенол — токсичное вещество. По степени воздействия на человеческий организм фенол относится к высокоопасным веществам (Класс опасности 2). При вдыхании вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу, вызывая химические ожоги. Доказательства канцерогенности фенола для людей отсутствуют[17].
Предельно допустимые концентрации (ПДК) фенола[18][19]
[20][21]:
- ПДКр.з. = 1 мг/м³ (2 класс опасности)
- ПДКр.с. = 0,3 мг/м³ (2 класс опасности)
- ПДКм.р. = 0,01 мг/м³
- ПДКс.с. = 0,006 мг/м³
- ПДКв. = 0,001 мг/л.
Попадая на кожу, фенол очень быстро всасывается даже через неповреждённые участки и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом — паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжелые случаи отравления характеризуются бессознательным состоянием, синюшностью, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Смертельная доза для человека при попадании внутрь — 1—10 г, для детей — 0,05—0,5 г[22].
Охрана труда[править | править код]
ПДК в воздухе рабочей зоны — 1 мг/м³ (максимально-разовая) и 0,3 мг/м³ (среднесменная). Порог восприятия запаха фенола у разных людей разный; и он может достигать (среднее значение в группе) 5,8-7,5 мг/м³[23]. А у отдельных работников он может быть значительно больше среднего значения. По этой причине можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками) приведёт к чрезмерному воздействию паров фенола на, по крайней мере, часть работников, и причинить вред их здоровью[24] — из-за запоздалой замены противогазных фильтров. Для защиты от фенола следует использовать более эффективные изменение технологии и средства коллективной защиты.
Фенольная катастрофа в Уфе[править | править код]
Наглядным примером воздействия фенола на окружающую среду стал случай весной 1990 года в Уфе. В результате техногенной аварии на предприятии ПО «Уфахимпром» произошла утечка большого количества фенола в речку Шугуровка, впадающую в более крупную реку Уфу, являющуюся источником хозяйственно-питьевого водоснабжения города Уфы. Загрязнение воды в районе Южного водозабора превышало ПДК более чем в 100 раз. Опасность загрязнения питьевой воды фенолом проявляется в том, что при очистке вод использовался хлор, который, взаимодействуя с фенолом, образовывал хлорпроизводные (смесь хлорфенолов) — более токсичные вещества (некоторые в 100—250 раз превышают токсичность самого фенола). Население Уфы было оповещено об опасности употребления водопроводной воды для питья. Общая численность населения, потреблявшего питьевую воду, загрязненную фенолом из Южного водозабора Уфы, составила 672 876 человек[25].
Примечания[править | править код]
- ↑ 1 2 3 (unspecified title)
- ↑ Binas (нидерл.) — 2 — Noordhoff Uitgevers, 1986. — ISBN 978-90-01-89351-4
- ↑ F. F. Runge (1834) «Ueber einige Produkte der Steinkohlendestillation» Архивная копия от 29 апреля 2021 на Wayback Machine (On some products of coal distillation), Annalen der Physik und Chemie, 31: 65-78. On page 69 of volume 31, Runge names phenol «Karbolsäure» (coal-oil-acid, carbolic acid). Runge characterizes phenol in: F. F. Runge (1834) “Ueber einige Produkte der Steinkohlendestillation, ” Архивная копия от 3 марта 2021 на Wayback Machine Annalen der Physik und Chemie, 31: 308—328.
- ↑ Auguste Laurent (1841) «Mémoire sur le phényle et ses dérivés» Архивная копия от 27 октября 2019 на Wayback Machine (Memoir on benzene and its derivatives), Annales de Chimie et de Physique, series 3, 3: 195—228. On page 198, Laurent names phenol «hydrate de phényle» and «l’acide phénique».
- ↑ Auguste Laurent (1836) “Sur la chlorophénise et les acides chlorophénisique et chlorophénèsique, ” Annales de Chemie et de Physique, vol. 63, pp. 27-45, see p. 44 Архивная копия от 20 марта 2015 на Wayback Machine: Je donne le nom de phène au radical fondamental des acides précédens (φαινω, j’éclaire), puisque la benzine se trouve dans le gaz de l’éclairage. (I give the name of «phène» (φαινω, I illuminate) to the fundamental radical of the preceding acid, because benzene is found in illuminating gas.)
- ↑ Gerhardt, Charles (1843) “Recherches sur la salicine, ” Архивная копия от 6 ноября 2018 на Wayback Machine Annales de Chimie et de Physique, series 3, 7: 215—229. Gerhardt coins the name «phénol» on page 221.
- ↑ Lister, Joseph. Antiseptic Principle Of The Practice Of Surgery (англ.). — 1867. Архивная копия от 15 сентября 2014 на Wayback Machine
- ↑ Smith, Michael B. & March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1, <https://books.google.com/books?id=JDR-nZpojeEC&printsec=frontcover> Архивная копия от 24 декабря 2019 на Wayback Machine
- ↑ Roscoe, Henry. A treatise on chemistry, Volume 3, Part 3 (англ.). — London: Macmillan & Co., 1891. — P. 23.
- ↑ Organic Chemistry 2nd Ed. John McMurry ISBN 0-534-07968-7
- ↑ Качественная реакция на фенол Архивная копия от 31 мая 2014 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ Phenol — The essential chemical industry online (11 января 2017). Дата обращения: 2 января 2018. Архивировано 3 января 2018 года.
- ↑ Direct Routes to Phenol. Дата обращения: 9 апреля 2007. Архивировано из оригинала 9 апреля 2007 года.
- ↑ Plotkin, Jeffrey S. What’s New in Phenol Production? American Chemical Society (21 марта 2016). Дата обращения: 2 января 2018. Архивировано из оригинала 27 октября 2019 года.
- ↑ Яушев Р. Г., Усманов Р. М. Интенсификация процесса селективной очистки масел фенолом. — М.: ЦНИИТЭнефтехим, 1988. — 76 с. — (Переработка нефти).
- ↑ Phenol spray. drugs.com. Дата обращения: 27 октября 2019. Архивировано 11 июля 2017 года.
- ↑ U.S. Department of Health and Human Services. «How can phenol affect my health?» Архивная копия от 28 июня 2013 на Wayback Machine Toxicological Profile for Phenol: 24.
- ↑ s:Гигиенические нормативы ГН 2.2.5.1313—03. «Предельно допустимые концентрации (ПДК) вредных веществ воздухе рабочей зоны»
- ↑ (Роспотребнадзор). № 535. Гидроксибензол (фенол) // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» / утверждены А.Ю. Поповой. — М., 2018. — С. 39. — 170 с. — (Санитарные правила). Архивная копия от 12 июня 2020 на Wayback Machine
- ↑ s:Гигиенические нормативы ГН 2.1.6.1338—03. «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест»
- ↑ s:Гигиенические нормативы ГН 2.1.5.1315—03. «Предельно допустимые концентрации (ПДК) химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования»
- ↑ Неотложная помощь при острых отравлениях. Справочник по токсикологии. Под ред. Голикова С. Н. — М.: Медицина, 1977. — С. 174.
- ↑ Herbert Kohler und Willem Jan Homans. Kombination von Olfactometer und Flammenionisationsdetektor zur Bestimmung von Geruchsschweilwerten – Einsatz der mcBmethodik in der Praxis (нем.) // Staub, Reinhaltung der Luft. — Düsseldorf: VDI-Verlag GmbH, 1980. — August (Bd. 40, H. 8). — S. 331—335. — ISSN 0039-0771.
- ↑ Волкова З.А., Муратов В.К., Проказова Н.В. Фенолы // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б.В. Петровский. — 3 изд. — Москва : Советская энциклопедия, 1985. — Т. 26. Углекислые воды – Хлор. — 560 с. — 150 000 экз.
- ↑ 1990 год — загрязнение питьевой воды г. Уфы фенолом Архивировано 15 января 2005 года.
Ссылки[править | править код]
Вычисление молярной массы
To calculate molar mass of a chemical compound enter its formula and click ‘Compute’. В химической формуле, вы можете использовать:
- Любой химический элемент. Capitalize the first letter in chemical symbol and use lower case for the remaining letters: Ca, Fe, Mg, Mn, S, O, H, C, N, Na, K, Cl, Al.
- Функциональные группы:D, Ph, Me, Et, Bu, AcAc, For, Ts, Tos, Bz, TMS, tBu, Bzl, Bn, Dmg
- круглые () и квадратные [] скобки.
- Общие составные имена.
Примеры расчета молярной массы:
NaCl,
Ca(OH)2,
K4[Fe(CN)6],
CuSO4*5H2O,
water,
nitric acid,
potassium permanganate,
ethanol,
fructose.
Molar mass calculator also displays common compound name, Hill formula, elemental composition, mass percent composition, atomic percent compositions and allows to convert from weight to number of moles and vice versa.
Вычисление молекулярной массы (молекулярная масса)
Для того, чтобы рассчитать молекулярную массу химического соединения, введите её формулу, указав его количество массы изотопа после каждого элемента в квадратных скобках.
Примеры молекулярные вычисления веса:
C[14]O[16]2,
S[34]O[16]2.
Определение молекулярной массы, молекулярный вес, молекулярная масса и молярная масса
- Молекулярная масса ( молекулярной массой ) это масса одной молекулы вещества, выражающаяся в атомных единицах массы (и). (1 и равна 1/12 массы одного атома углерода-12)
- Молярная масса ( молекулярной массой ) является масса одного моля вещества и выражается в г / моль.
Массы атомов и изотопов с NIST статью .
См. также: молекулярные массы аминокислот
Random converter
фенол: состав и молярная масса
Химическая формула
Молярная масса C6H5OH, фенол 94.11124 г/моль
12,0107·6+1,00794·5+15,9994+1,00794
Массовые доли элементов в соединении
| Элемент | Символ | Атомная масса | Число атомов | Массовая доля |
|---|---|---|---|---|
| Carboneum | C | 12.0107 | 6 | 76.574% |
| Hydrogenium | H | 1.00794 | 6 | 6.427% |
| Oxygenium | O | 15.9994 | 1 | 17.001% |
Использование калькулятора молярной массы
- Химические формулы нужно вводить с учетом регистра
- Индексы вводятся как обычные числа
- Точка на средней линии (знак умножения), применяемая, например, в формулах кристаллогидратов, заменяется обычной точкой.
- Пример: вместо CuSO₄·5H₂O в конвертере для удобства ввода используется написание CuSO4.5H2O.
Калькулятор молярной массы

Моль
Молярная масса
Молярная масса элементов и соединений
Молекулярная масса
Расчет молярной массы
Моль
Все вещества состоят из атомов и молекул. В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ. Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
Постоянная Авогадро NA = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³.
Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Один моль чистого углерода-12 равен точно 12 г.
Молярная масса
Молярная масса — физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях. Говоря иначе, это масса одного моля вещества. В системе СИ единицей молярной массы является килограмм/моль (кг/моль). Однако химики привыкли пользоваться более удобной единицей г/моль.
молярная масса = г/моль

Горение — высокотемпературная экзотермическая окислительно-восстановительная реакция.
Молярная масса элементов и соединений
Соединения — вещества, состоящие из различных атомов, которые химически связаны друг с другом. Например, приведенные ниже вещества, которые можно найти на кухне у любой хозяйки, являются химическими соединениями:
- соль (хлорид натрия) NaCl
- сахар (сахароза) C₁₂H₂₂O₁₁
- уксус (раствор уксусной кислоты) CH₃COOH
Молярная масса химических элементов в граммах на моль численно совпадает с массой атомов элемента, выраженных в атомных единицах массы (или дальтонах). Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 1 × 2 + 16 = 18 г/моль.
Молекулярная масса

Молекулярная масса (старое название — молекулярный вес) — это масса молекулы, рассчитанная как сумма масс каждого атома, входящего в состав молекулы, умноженных на количество атомов в этой молекуле. Молекулярная масса представляет собой безразмерную физическую величину, численно равную молярной массе. То есть, молекулярная масса отличается от молярной массы размерностью. Несмотря на то, что молекулярная масса является безразмерной величиной, она все же имеет величину, называемую атомной единицей массы (а.е.м.) или дальтоном (Да), и приблизительно равную массе одного протона или нейтрона. Атомная единица массы также численно равна 1 г/моль.
Расчет молярной массы
Молярную массу рассчитывают так:
- определяют атомные массы элементов по таблице Менделеева;
- определяют количество атомов каждого элемента в формуле соединения;
- определяют молярную массу, складывая атомные массы входящих в соединение элементов, умноженные на их количество.
Например, рассчитаем молярную массу уксусной кислоты
CH₃COOH
Она состоит из:
- двух атомов углерода
- четырех атомов водорода
- двух атомов кислорода
Расчет:
- углерод C = 2 × 12,0107 г/моль = 24,0214 г/моль
- водород H = 4 × 1,00794 г/моль = 4,03176 г/моль
- кислород O = 2 × 15,9994 г/моль = 31,9988 г/моль
- молярная масса = 24,0214 + 4,03176 + 31,9988 = 60,05196 g/mol
Наш калькулятор выполняет именно такой расчет. Можно ввести в него формулу уксусной кислоты и проверить что получится.
Вы затрудняетесь в переводе единицы измерения с одного языка на другой? Коллеги готовы вам помочь. Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
Другие конвертеры
Конвертеры единиц измерения, используемых при измерении скорости передачи данных, в типографике и обработке изображений, для измерения объема лесоматериалов, а также десятичные приставки и калькулятор молярной массы химических соединений
Вычисление молярной массы
Молярная масса — физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях, то есть, это масса одного моля вещества.
Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении.
Использование конвертера «Вычисление молярной массы»
На этих страницах размещены конвертеры единиц измерения, позволяющие быстро и точно перевести значения из одних единиц в другие, а также из одной системы единиц в другую. Конвертеры пригодятся инженерам, переводчикам и всем, кто работает с разными единицами измерения.
Пользуйтесь конвертером для преобразования нескольких сотен единиц в 76 категориях или несколько тысяч пар единиц, включая метрические, британские и американские единицы. Вы сможете перевести единицы измерения длины, площади, объема, ускорения, силы, массы, потока, плотности, удельного объема, мощности, давления, напряжения, температуры, времени, момента, скорости, вязкости, электромагнитные и другие.
Примечание. В связи с ограниченной точностью преобразования возможны ошибки округления. В этом конвертере целые числа считаются точными до 15 знаков, а максимальное количество цифр после десятичной запятой или точки равно 10.
Для представления очень больших и очень малых чисел в этом калькуляторе используется компьютерная экспоненциальная запись, являющаяся альтернативной формой нормализованной экспоненциальной (научной) записи, в которой числа записываются в форме a · 10x. Например: 1 103 000 = 1,103 · 106 = 1,103E+6. Здесь E (сокращение от exponent) — означает «· 10^», то есть «…умножить на десять в степени…». Компьютерная экспоненциальная запись широко используется в научных, математических и инженерных расчетах.
Мы работаем над обеспечением точности конвертеров и калькуляторов TranslatorsCafe.com, однако мы не можем гарантировать, что они не содержат ошибок и неточностей. Вся информация предоставляется «как есть», без каких-либо гарантий. Условия.
Если вы заметили неточность в расчётах или ошибку в тексте, или вам необходим другой конвертер для перевода из одной единицы измерения в другую, которого нет на нашем сайте — напишите нам!
Канал Конвертера единиц TranslatorsCafe.com на YouTube
ГДЗ (ответы) Химия 10 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А., 2019, §13 Фенол
Во всех упражнениях
красным цветом приводится решение,
а фиолетовым ― объяснение.
Задание 1
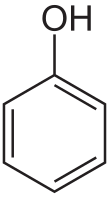
Приведите молекулярную и структурную формулы фенола.
Молекулярная формула фенола: C6H5OH.
Структурная формула фенола: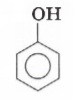
Найдите черты сходства и различия в строении молекул фенола и этанола.
Сходство: молекулы имеют в своём составе гидроксильную группу ОН, которая связана с атомом углерода.
Различия: в молекуле фенола гидроксильная группа связана с ароматическим радикалом, а в этаноле ― с алкильным радикалом.
Задание 2 Как взаимное влияние фенильного радикала и гидроксильной группы отражается на свойствах фенола? Ответ проиллюстрируйте уравнениями химических реакций.
Влияние фенильного радикала –C6H5 на гидроксильную группу выражается в значительном усилении кислотных свойств, так, например, фенол, в отличие от спиртов, вступает в реакцию нейтрализации со щелочами:
C6H5OH + NaOH ⟶ C6H5ONa + H2O
Влияние гидроксильной группы на фенильный радикал –C6H5 выражается в значительном облегчении протекания реакции по фенильному радикалу, так, например, для бромирования фенола, в отличие от бензола, не требуется катализатор и замещаются сразу три атома водорода в положениях 2, 4 и 6 с образованием белого нерастворимого осадка 2,4,6-трибромфенола: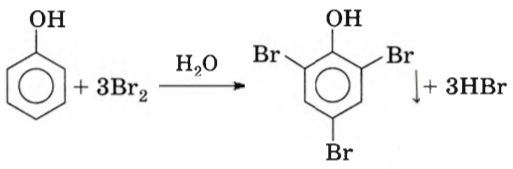
Задание 3
В настоящее время вместо фенола в качестве дезинфицирующего средства используют 2,4,6-трихлорфенол. Предложите способ его получения исходя из бензола. Напишите уравнения соответствующих реакций.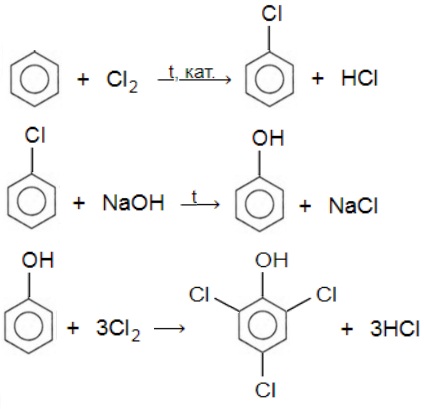
или
С6H6 + Cl2t,кат.⟶ C6H5Cl + HCl
C6H5Cl + NaOH t⟶ C6H5OH + NaCl
C6H5OH + 3Cl2 ⟶ C6H2Cl3OH + 3HCl
Задание 4
В результате взаимодействия 47 г водного раствора фенола с бромной водой выпало 1,655 г осадка. Рассчитайте массовую долю фенола в исходном растворе.
Дано: m(раствора)=47 г, m(C6H2Br3OH)=1,655 г
Найти: ω(C6H5OH)—?
Решение
1. Количество вещества осадка рассчитываем по формуле: n=m/M, где M ― молярная масса.
M(C6H2Br3OH)=331 г/моль
n(C6H2Br3OH)=m(C6H2Br3OH)/M(C6H2Br3OH)=1,655 г : 331 г/моль=0,005 моль
2. Составим химическое уравнение:
C6H5OH + 3Br2 = C6H2Br3OH↓ + 3HBr
По уравнению реакции n(C6H5OH):n(C6H2Br3OH)=1:1, количество вещества одинаковое, поэтому
n(C6H5OH)=n(C6H2Br3OH)=0,005 моль
3. Рассчитываем массу фенола количеством вещества 0,005 моль по формуле: m=n•M, где M ― молярная масса.
M(C6H5OH)=94 г/моль
m(C6H5OH)=n(C6H5OH)•M(C6H5OH)=0,005 моль • 94 г/моль=0,47 г
4. Рассчитываем массовую долю фенола в растворе:
ω(C6H5OH)=(m(C6H5OH):m(раствора))•100%=(0,47 г : 47 г) •100%=1%
Ответ: 1%
Задание 5
В трёх пробирках без подписи находятся водные растворы пропанола-1, глицерина и фенола. С помощью каких реагентов можно определить каждый из растворов?
Качественной реакцией на фенол является реакция с бромной водой при комнатной температуре, в результате образуется белый осадок.
Качественной рекцией на глицерин (мноатономный спирт) является реакция со свежеполученным осадком гидроксида меди (II), в результате которой образуется раствор ярко-синего цвета.
Определить раствор пропанола-1 можно при помощи оксида меди (II), при его добавлении, наблюдается окисление спирта до альдегида, и раствор приобретает фруктовый запах.
Задание 6
Фенолят натрия взаимодействует с углекислым газом с образованием гидрокарбоната натрия и фенола согласно уравнению C6H5ONa + CO2 + H2O ⟶ C6H5OH + NaHCO3 Какой вывод относительно кислотных свойств фенола и угольной кислоты можно сделать на основании этой реакции? Фенол является слабой кислотой, при этом кислотные свойства фенола настолько слабые, что даже такая слабая кислота, как угольная, вытесняет фенол из раствора его солей.
Задание 7
Опишите физические свойства фенола.
Фенол ― бесцветные кристаллы, розовеющие при хранении на воздухе, с температурой плавления 41°C и температурой кипения 181,2°C, летучие, имеют специфический стойкий запах (запах гуаши, или так называемый «карболовый запах»). При комнатной температуре фенол растворим в воде незначительно, а при нагревании до 70°С растворяется полностью.
Найдите в Интернете данные о растворимости фенола в воде при различных температурах. Постройте график температурной зависимости растворимости фенола в воде.
В справочнике химика нашли, що 1 г кристаллического фенола растворяется в 15 г воды при 200С, поэтому в 100 г воды при 200С растворится 6,6 г фенола, следовательно первая координата (20;6,6). Остальные координаты берем из других справочников в интернете: (16;6,2); (36;8); (50;10,71); (60;14,97).
Построили график температурной зависимости растворимости фенола в воде: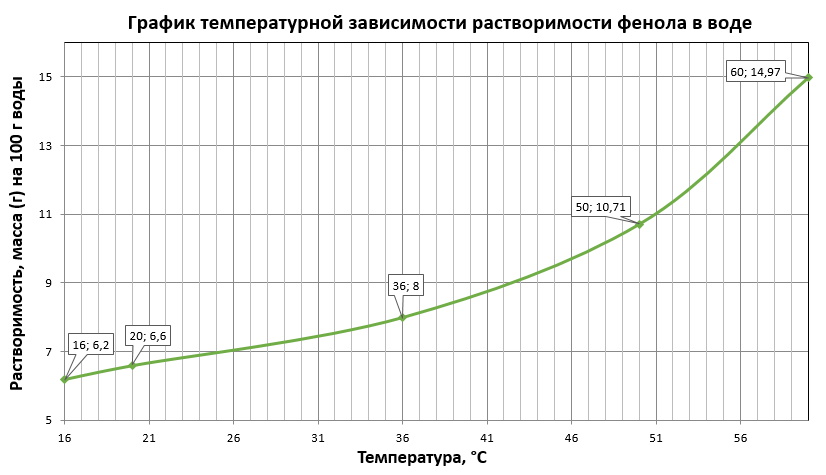








![{displaystyle {mathsf {C_{6}H_{5}ONa+C_{6}H_{5}Cl{xrightarrow[{}]{Cu}}C_{6}H_{5}OC_{6}H_{5}+NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6bc5440e942ad1032d9bac43b770cdead2e43681)

![{displaystyle {mathsf {C_{6}H_{5}OH+CO_{2}{xrightarrow[{}]{NaOH}}C_{6}H_{4}OH(COONa)}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8746d83f76859c5bf80d5bc833151804dc210186)



![{displaystyle {mathsf {6C_{6}H_{5}OH+FeCl_{3}rightarrow H_{3}[Fe(C_{6}H_{5}O)_{6}]+3HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/298928dbc2a7b0fca344f5d84657a2595c0b18e1)

![{displaystyle {mathsf {C_{6}H_{5}OH+2H_{2}O_{2}{xrightarrow[{-H_{2}O}]{kat:Fe}}C_{6}H_{4}(OH)_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a3412295398fa56c30b01ef5f9cc5de7c91fdae7)
