Загрузить PDF
Загрузить PDF
Молярность — это соотношение между молями растворенного вещества и объемом раствора.[1]
Чтобы получить подробное представление о том, как найти молярность раствора, когда даны моли, литры, граммы и/или миллилитры, читайте далее.
-

1
Запомните основную формулу для вычисления молярности. Молярность равна количеству молей вещества, поделенному на объем раствора в литрах.[2]
Следовательно, ее можно записать в следующем виде: молярность = моли растворенного вещества / литры раствора.- Пример: какова молярность раствора, содержащего 0,75 моль NaCl в 4,2 литрах?
-

2
Проанализируйте пример. Чтобы найти молярность, нужно знать количество молей и литров. Если в задаче даны оба этих значения, никаких предварительных расчетов делать не нужно.
- Пример:
- Моли = 0,75 моль NaCl
- Объем = 4,2 л
- Пример:
-

3
Разделите количество молей на количество литров. Получившееся соотношение даст вам количество молей на литр раствора, также известное как молярность.
- Пример: молярность = моли растворенного вещества / литры раствора = 0,75 моль / 4,2 л = 0,17857142
-

4
Запишите ответ. Округлите получившееся число до сотых или тысячных, в зависимости от требований вашего преподавателя. Когда вы записываете ответ, сокращайте «молярность» буквой «M» и указывайте химическую формулу растворенного вещества.
- Пример: 0,179 M NaCl
Реклама
-

1
Запомните основную формулу для вычисления молярности. Молярность выражают отношением количества молей растворенного вещества к литрам раствора, или его объему. В виде формулы молярность выражается следующим образом: молярность = моли растворенного вещества / литры раствора.[3]
- Пример: какова молярность раствора, полученного растворением 3,4 г KMnO4 в 5,2 л воды?
-

2
Проанализируйте задачу. Чтобы найти молярность, необходимо знать количество молей и количество литров. Если количество молей не дано, но известны объем раствора и масса растворенного вещества, то для того, чтобы продолжить решение, вам нужно рассчитать количество молей растворенного вещества.
- Пример:
- Масса = 3,4 г KMnO4
- Объем = 5,2 л
- Пример:
-

3
Найдите молярную массу растворенного вещества. Чтобы найти число молей, зная массу, или граммы, использованного растворенного вещества, нужно сначала определить его молярную массу.[4]
Это можно сделать, сложив отдельные молярные массы всех элементов, входящих в состав растворенного вещества. Найдите молярные массы элементов с помощью таблицы Менделеева.[5]
Сделайте это с каждым элементом.- Пример:
- Молярная масса K = 39,1 г
- Молярная масса Mn = 54,9 г
- Молярная масса O = 16,0 г
- Общая молярная масса = K + Mn + O+ O +O + O = 39,1+ 54,9 + 16,0 + 16,0 + 16,0 + 16,0 =158,0 г
- Пример:
-

4
Преобразуйте граммы в моли. Теперь, когда у вас есть молярная масса растворенного вещества, вам нужно умножить количество граммов растворенного вещества на коэффициент пересчета его формульной (молярной) массы.[6]
- Пример: граммы растворенного вещества * (1/молярная масса растворенного вещества) =3,4 г * (1 моль / 158 г) = 0,0215 моль
- Как видно в приведенном примере выше, граммы сокращаются и остаются только моли.
-

5
Разделите количество молей на количество литров. Теперь, когда у вас есть количество молей, вы можете разделить это значение на количество литров раствора для того, чтобы найти молярность.
- Пример: молярность = моли растворенного вещества / литры раствора = 0,0215 моль / 5,2 л = 0,04134615
-

6
Запишите полученный ответ. Следует округлить число до такого количества знаков после запятой, которого требует от вас ваш преподаватель. Обычно это два или три знака. Кроме того, когда вы записываете ответ, сокращайте «молярность» буквой «M» и указывайте растворенное вещество.
- Пример: 0,004 M KMnO4
Реклама
-

1
Запомните основную формулу. Чтобы найти молярность, нужно вычислить количество молей растворенного вещества в литре раствора. Миллилитры использовать нельзя. Общая формула, используемая для выражения молярности, имеет следующий вид: молярность = моли растворенного вещества / литры раствора.[7]
- Пример: какова молярность раствора, содержащего 1,2 моля CaCl2 в 2905 миллилитрах?
-

2
Проанализируйте задачу. Для вычисления молярности нужно знать количество молей и количество литров. Если объем дан в миллилитрах, а не в литрах, тогда вам придется перевести объем в литры, прежде чем продолжить расчет.
- Пример:
- Моли = 1,2 моль CaCl2
- Объем = 2905 мл
- Пример:
-

3
Переведите миллилитры в литры.[8]
Найдите количество литров, разделив количество миллилитров на 1000, так как в 1 литре содержится 1000 миллилитров. Обратите внимание, что вы также можете переместить запятую на три знака влево.- Пример: 2905 мл * (1 л / 1000 мл) = 2,905 л
-

4
Разделите количество молей на количество литров. Теперь, когда у вас есть количество литров, вы можете разделить количество молей растворенного вещества на это значение, чтобы получить молярность раствора.
- Пример: молярность = моли растворенного вещества / литры раствора = 1,2 моль CaCl2 / 2,905 л = 0,413080895
-

5
Запишите ответ. Округлите ответ в соответствии с требованиями вашего преподавателя (обычно до второго или третьего знака). Когда вы записываете ответ, сокращайте «молярность» буквой «M» и указывайте растворенное вещество.
- Пример: 0,413 M CaCl2
Реклама
-

1
Найдите молярность раствора, полученного растворением 5,2 г NaCl в 800 мл воды. Определите значения, данные в задаче: масса в граммах и объем в миллилитрах.
-
- Масса = 5,2 г NaCl
- Объем = 800 мл воды
-
-

2
Найдите молярную массу NaCl. Для этого сложите молярную массу натрия, Na, и хлора,Cl.
- Молярная масса Na = 22,99 г
- Молярная масса Cl = 35,45 г
- Молярная масса NaCl = 22,99 + 35,45 =58,44 г
-

3
Умножьте массу растворенного вещества на коэффициент пересчета его молярной массы. В данном примере молярная масса NaCl равна 58,44 г, соответственно, коэффициент пересчета будет равен 1 моль / 58,44 грамм.
- Моли NaCl = 5,2 г NaCl * (1 моль / 58,44 г) = 0,08898 моль = 0,9 моль
-

4
Разделите 800 мл воды на 1000. Поскольку в литре содержится 1000 мл, то, чтобы найти количество литров, вам нужно будет разделить количество миллилитров в этой задаче на 1000.
- Это действие также можно рассмотреть как умножение 800 мл на коэффициент пересчета 1 л / 1000 мл.
- Для ускорения процесса вы можете просто переместить десятичную запятую на три знака влево, ничего не перемножая и не деля.
- Объем = 800 л * (1 л / 1000 мл) = 800 мл / 1000 мл = 0,8 л
-

5
Разделите количество молей растворенного вещества на количество литров раствора. Чтобы найти молярность, вам необходимо разделить 0,09 моль, количество молей растворенного NaCl, на объем растворенного вещества в литрах.
- молярность = моли растворенного вещества / литры раствора = 0,09 моль / 0,8 л =0,01125 моль/л.
-

6
Приведите ответ в порядок. Округлите полученный ответ до двух или трех знаков после запятой и сократите молярность буквой «M».
- Ответ: 0,11 M NaCl
Реклама
Об этой статье
Эту страницу просматривали 111 946 раз.
Была ли эта статья полезной?
В уроке 15 «Моляльность и молярность» из курса «Химия для чайников» рассмотрим понятия растворитель и растворенное вещество научимся выполнять расчет молярной и моляльной концентрации, а также разбавлять растворы. Невозможно объяснить что такое моляльность и молярность, если вы не знакомы с понятием моль вещества, поэтому не поленитесь и прочитайте предыдущие уроки. Кстати, в прошлом уроке мы разбирали задачи на выход реакции, посмотрите если вам интересно.

Химикам нередко приходится работать с жидкими растворами, так как это благоприятная среда для протекания химических реакций. Жидкости легко смешивать, в отличие от кристаллических тел, а также жидкость занимает меньший объем, по сравнению с газом. Благодаря этим достоинствам, химические реакции могут осуществляться гораздо быстрее, так как исходные реагенты в жидкой среде часто сближаются и сталкиваются друг с другом. В прошлых уроках мы отмечали, что вода относится к полярным жидкостям, и потому является неплохим растворителем для проведения химических реакций. Молекулы H2O, а также ионы H+ и OH—, на которых вода диссоциирована в небольшой степени, могут способствовать запуску химические реакций, благодаря поляризации связей в других молекулах или ослаблению связи между атомами. Вот почему жизнь на Земле зародилась не на суше или в атмосфере, а именно в воде.
Содержание
- Растворитель и растворенное вещество
- Расчет концентрации раствора
- Молярная концентрация
- Моляльная концентрация
- Разбавление растворов
Растворитель и растворенное вещество
Раствор может быть образован путем растворения газа в жидкости или твердого тела в жидкости. В обоих случаях жидкость является растворителем, а другой компонент — растворенное вещество. Когда раствор образован путем смешивания двух жидкостей, растворителем считается та жидкость, которая находится в большем количестве, иначе говоря имеет бОльшую концентрацию.
Расчет концентрации раствора
Молярная концентрация
Концентрацию можно выражать по разному, но наиболее распространенный способ — указание его молярности. Молярная концентрация (молярность) — это число молей растворенного вещества в 1 литре раствора. Единица молярности обозначается символом M. Например два моля соляной кислоты на 1 литр раствора обозначается 2 М HCl. Кстати, если на 1 литр раствора приходится 1 моль растворенного вещества, тогда раствор называется одномолярным. Молярная концентрация раствора обозначается различными символами:
- cx, Смx, [x], где x — растворенное вещество
Формула для вычисления молярной концентрации (молярности):
- См = n/V, моль/л
где n — количество растворенного вещества в молях, V — объем раствора в литрах.
Пару слов о технике приготовления растворов нужной молярности. Очевидно, что если добавить к одному литру растворителя 1 моль вещества, общий объем раствора будет чуть больше одного литра, и потому будет ошибкой считать полученный раствор одномолярным. Чтобы этого избежать, первым делом добавляем вещество, а только потом доливаем воду, пока суммарный объем раствора не будет равным 1 л. Полезно будет запомнить приближенное правило аддитивности объемов, которое гласит, что объем раствора приближенно равен сумме объемов растворителя и растворенного вещества. Растворы многих солей приближенно подчиняются данному правилу.

Пример 1. Химичка дала задание растворить в литре воды 264 г сульфата аммония (NH4)2SO4, а затем вычислить молярность полученного раствора и его объем, основываясь на предположении об аддитивности объемов. Плотность сульфата аммония равна 1,76 г/мл.
Решение:
Определим объем (NH4)2SO4 до растворения:
- 264 г / 1,76 г/мл = 150 мл = 0,150 л
Пользуясь правилом аддитивности объемов, найдем окончательный объем раствора:
- 1,000 л + 0,150 л = 1,150 л
Число молей растворенного сульфата аммония равно:
- 264 г / 132 г/моль = 2,00 моля (NH4)2SO4
Завершающий шаг! Молярность раствора равна:
- 2,000 / 1,150 л = 1,74 моль/л, т.е 1,74 М (NH4)2SO4
Приближенным правилом аддитивности объемов можно пользоваться только для грубой предварительной оценки молярности раствора. Например, в примере 1, объем полученного раствора на самом деле имеет молярную концентрацию равную 1,8 М, т.е погрешность наших расчетов составляет 3,3%.
Моляльная концентрация
Наряду с молярностью, химики используют моляльность, или моляльную концентрацию, в основе которой учитывается количество использованного растворителя, а не количество образующегося раствора. Моляльная концентрация — это число молей растворенного вещества в 1 кг растворителя (а не раствора!). Моляльность выражается в моль/кг и обозначается маленькой буквой m. Формула для вычисления моляльной концентрации:
- m = n/m
где n — количество растворенного вещества в молях, m — масса растворителя в кг
Для справки отметим, что 1 л воды = 1 кг воды, и еще, 1 г/мл = 1 кг/л.

Пример 2. Химичка попросила определить моляльность раствора, полученного при растворении 5 г уксусной кислоты C2H4O2 в 1 л этанола. Плотность этанола равна 0,789 г/мл.
Решение:
Число молей уксусной кислоты в 5 г равно:
- 5,00 г / 60,05 г/моль = 0,833 моля C2H4O2
Масса 1 л этанола равна:
- 1,000 л × 0,789 кг/л = 0,789 кг этанола
Последний этап. Найдем моляльность полученного раствора:
- 0,833 моля / 0,789 кг растворителя = 0,106 моль/кг
Единица моляльности обозначается Мл, поэтому ответ также можно записать 0,106 Мл.
Разбавление растворов
В химической практике часто занимаются разбавлением растворов, т.е добавлением растворителя. Просто нужно запомнить, что число молей растворенного вещества при разбавлении раствора остается неизменным. И еще запомните формулу правильного разбавления раствора:
- Число молей растворенного вещества = c1V1 = c2V2
где с1 и V1 — молярная концентрация и объем раствора до разбавления, с2 и V2 — молярная концентрация и объем раствора после разбавления. Рассмотрите задачи на разбавление растворов:

Пример 3. Определите молярность раствора, полученного разбавлением 175 мл 2,00 М раствора до 1,00 л.
Решение:
В условие задача указаны значения с1, V1 и V2, поэтому пользуясь формулой разбавления растворов, выразим молярную концентрацию полученного раствора с2
- с2 = c1V1 / V2 = (2,00 М × 175 мл) / 1000 мл = 0,350 М
Пример 4 самостоятельно. До какого объема следует разбавить 5,00 мл 6,00 М раствора HCl, чтобы его молярность стала 0,1 М?
Ответ: V2 = 300 мл
Без сомнения, вы и сами догадались, что урок 15 «Моляльность и молярность» очень важный, ведь 90% все лабораторных по химии связаны с приготовлением растворов нужной концентрации. Поэтому проштудируйте материал от корки до корки. Если у вас возникли вопросы, пишите их в комментарии.
Молярная концентрация (молярность), Сm – это характеристика раствора, способ выражения концентрации растворенного вещества в растворе. Молярная концентрация равна отношению количества растворенного вещества к объему раствора:

где νр.в. – количество растворенного вещества, моль
Vр-ра – объем раствора, л
Иногда молярную концентрацию вещества А обозначают так: [A].
Молярная концентрация измеряется в моль/л или М.
Несколько задач на молярную концентрацию.
1. Определите молярную концентрацию раствора азотной кислоты, если в 500 мл раствора содержится 6,3г азотной кислоты. Ответ: 0,2М
Решение: молярная концентрация — это отношение количества растворенного вещества к объему раствора в литрах. Количество азотной кислоты:
ν(HNO3) = m/M(HNO3) = 6,3 г/ 63 г/моль = 0,1 моль
С(HNO3) = ν(HNO3)/Vр-ра = 0,1 моль/ 0,5 л = 0,2 моль/л
2. Определить молярную концентрацию раствора серной кислоты, если в 2л раствора содержится 0,98г кислоты. Ответ: 0,005М
3. Какую массу хлорида натрия надо растворить в воде, чтобы получить 1л раствора с молярной концентрацией соли 0,02моль/л? Ответ: 1,17г
4. Какое количество вещества (в моль) гидроксида калия содержится в 200мл раствора, если молярная концентрация щёлочи равна 0,9моль/л? Ответ: 0,18моль
5. Какая масса хлороводорода содержится в 250мл раствора соляной кислоты с молярной концентрацией 1 моль/л? Ответ: 9,125г
6. В каком объёме раствора серной кислоты с концентрацией 1 моль/л содержится 4,9г серной кислоты? Ответ: 50мл
7. Смешали 400мл раствора хлорида натрия с молярной концентрацией 1 моль/л и 600мл раствора хлорида натрия с концентрацией соли 2 моль/л. Определить количество вещества хлорида натрия в получившемся растворе и молярную концентрацию этого раствора. Ответ: 1,6М
Раствор представляет собой смесь соединений, в результате чего одно из них – растворенное вещество – распределяется по всему другому, известному как растворитель. Растворитель – это всегда соединение, которое составляет большую часть смеси, а в большинстве реальных ситуаций растворителем является вода. Свойства раствора изменяются с концентрацией растворенного вещества, поэтому химикам нужны единицы измерения концентрации для его измерения. Наиболее важной единицей концентрации является молярность, которая представляет собой число молей растворенного вещества на литр раствора. Молярность обозначается заглавной М, а М в химии означает следующее:
Молярность (М) = (моль растворенного вещества) ÷ (литры раствора).
Чтобы рассчитать количество родинок растворенного вещества, вам понадобятся две части информации, которые вам, возможно, придется извлечь из других данных. Первый – это химическая формула растворенного вещества, а второй – масса растворенного вещества. Затем вы вычисляете молярность, измеряя объем раствора, переводя его в литры и деля это число на число молей.
Что такое крот?
Помимо пушистых роющих животных, родинка является одной из центральных единиц измерения в химии. Он основан на числе Авогадро, которое составляет 6, 02 x 10 23. Это количество атомов в образце углерода-12, которое весит ровно 12.000 грамм. Такое же количество частиц любого другого соединения представляет собой моль этого соединения. Один моль любого соединения имеет характерную массу в граммах, которая оказывается точно такой же, как его атомная масса в атомных единицах массы (amu). Например, атомная масса водорода составляет 1, 008 а.е.м., поэтому моль водорода весит 1, 008 грамма.
Вы можете посмотреть атомные массы в периодической таблице, и вы можете рассчитать молекулярную массу соединения на основе его химической формулы. Как только вы узнаете атомную массу соединения, вы сразу узнаете массу моль этого соединения (молярную массу). Если у вас есть образец соединения под рукой, просто взвесьте его и разделите на молярный вес, чтобы найти количество родинок, которые у вас есть.
Пример: образец гидроксида натрия (NaOH) весит 32 грамма. Сколько родинок это?
Из таблицы Менделеева, атомные массы натрия, кислорода и водорода составляют 22, 990, 15, 999 и 1, 008 а.е.м. соответственно. Округляя до целого числа, их молярные массы составляют 23, 16 и 1 грамм соответственно. Сложите их вместе, чтобы получить молярную массу гидроксида натрия, которая оказывается 40 грамм. Разделите это число на количество, которое вы имеете под рукой, чтобы найти число родинок:
32 г / 40 г = 0, 8 моль.
Как найти молярность
Пока у вас есть способ измерения массы растворенного вещества, вы можете рассчитать его молярность путем измерения объема раствора. Будьте осторожны, потому что молярность всегда выражается в молях / литр, поэтому, если вы измеряете объем в любых других единицах, вы должны пересчитать в литры. Вот некоторые факторы конверсии, которые вы найдете полезными:
1 литр = 0, 001 кубометра = 1000 миллилитров = 0, 264 галлона США = 33, 81 унции жидкости.
Пример
Вы наливаете 12 грамм соли (NaCl) в стакан, содержащий 20 унций воды. Какова молярность соли в растворе?
Вы можете решить эту проблему в три простых шага:
-
Найти количество молей соли
-
Преобразовать объем в литры
-
Рассчитать молярность
При округлении до одного десятичного знака масса одного моля натрия (Na) составляет 23, 0 грамма, а хлора (Cl) – 35, 5 грамма, поэтому один моль NaCl имеет массу 58, 5 грамма. У вас есть 12 грамм, что равно 12 / 58, 5 = 0, 21 моль.
Если 33, 81 унции соответствует 1 литру, 20 унций равны 20 / 33, 81 = 0, 59 литра.
Разделите количество молей NaCl на объем раствора, чтобы получить молярность.
0, 21 моль ÷ 0, 59 л =
0, 356 м.
Определение молярности раствора
Молярность (molarity) – способ выражения концентрации, показывающей количество растворенного вещества (n, моль) в единице объема раствора (1 литр). В отличие от массовой и мольной доли, молярность имеет единицы измерения. В случае использования в качестве меры объема литров, молярность измеряется в «моль/литр»1. Обозначается молярность — «См».
Для вычисления молярной концентрации раствора (молярности) используется формула:
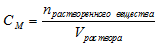
Задача 1.
24 г чистой серной кислоты растворили в 85 г воды. Определить молярную концентрацию серной кислоты в полученном растворе, если его плотность составляет 1,155 г/мл.
Дано:
масса серной кислоты: m(Н2SО4) = 24 г;
масса воды: m(Н2О) = 85 г;
плотность раствора: рр-ра = 1,155 г/мл.
Найти:
молярную концентрацию серной кислоты в растворе.
Решение:
Для определения молярной концентрации необходимо вычислить количество (п, моль) растворенного вещества (Н2SО4) и объем раствора.
Схематично алгоритм решения можно представить следующим образом:
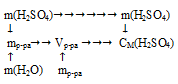
1. Определим количество вещества серной кислоты:
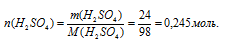
2. Определим объем раствора:
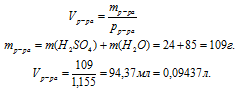
Объем, выраженный в других единицах, для определения молярной концентрации всегда необходимо переводить в литры.
Подставим в формулу для вычисления молярной концентрации полученные данные:
CМ = n(H2SO4)/V(p-pa) = 0,245/0,09437 = 2,6 моль/л.
Ответ: СМ(Н2SO4) = 2,6 моль/л.
Задача 2.
Определить массу гидроксида натрия в 700 г 14,ЗМ раствора NаОН в воде (рр-ра = 1,43 г/мл).
Дано:
масса раствора гидроксида натрия в воде : mр-ра = 700 г;
молярная концентрация гидроксида натрия в растворе: См(NаОН) = 14,3 моль/л,
плотность раствора: рр-ра= 1,43 г/мл.
Найти:
массу гидроксида натрия.
Решение:
Схематично алгоритм решения можно представить так:
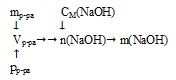
1. Определим объем 700 г раствора
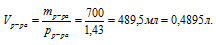
Обращайте, пожалуйста, внимание на согласованность единиц измерения величин, подставляемых в формулу. Если плотность выражена в г/мл или г/см3, то объем необходимо использовать в миллилитрах, а массу в граммах. Для использования молярной концентрации объем необходимо переводить в литры.
2. Используя соотношение для молярной концентрации, определим количество вещества NаОН в 0,4895 л раствора.
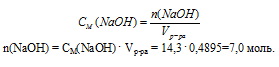
3. Определим массу 7 моль NаОН:
m(NaOH) = n(NaOH) . M(NaOH) = 7 . 40 =280 г.
Ответ: m(NaOH) = 280 г.
Задача 3.
3 г поваренной соли (NаС1) растворили в 200 г воды. Определить молярную концентрацию полученного раствора.
Дано:
масса поваренной соли: m(NаС1) = 3 г;
масса воды: m(Н2О) = 200 г.
Найти:
молярную концентрацию поваренной соли в растворе.
Решение:
Схематично алгоритм решения можно представить следующим образом:
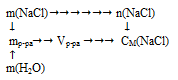
1 . Определяем количество вещества NаС1:
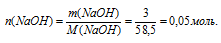
2. Для вычисления молярной концентрации необходимо знать объем раствора. Но по данным из условия задачи, возможно определить только его массу:
mр-ра = m(NаС1) + mН2О) = 3 + 200 = 203 г.
3. Для нахождения объема раствора требуется плотность. При необходимости очень точного расчета можно воспользоваться справочником физико-химических величин. В случае решения обычной задачи разумно принять плотность разбавленного водного раствора равной плотности воды2.
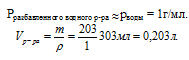
Определим молярную концентрацию NаС1 в растворе:
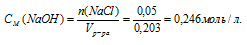
Ответ: 0,24моль/л.
Комментарии:
1Иногда для сокращения записи после значения молярной концентрации вместо размерности записывают заглавную букву (М). Например, запись « 0.03М раствор NаОН в воде» следует понимать так: молярная концентрация NаОН в воде равна 0,03 моль/л.
2Справочное значение плотности данного раствора равно 1,009 г/мл.
