Недавно
мы говорили о размерах молекул и выяснили, что они очень малы. Как вы
понимаете, измерять массу молекул в обычных единицах массы, таких как
килограммы или граммы, крайне неудобно. Поэтому люди придумали относительную
молекулярную массу. Относительная молекулярная (или атомная) масса вещества —
это отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода.
Дело
в том, что углерод входит в множество веществ, и по международному соглашению
было решено использовать углеродную шкалу атомных масс. Нетрудно догадаться,
что относительная молекулярная масса — это безразмерная величина, поскольку
она показывает во сколько раз масса данной молекулы (или атома) больше массы
одной двенадцатой атома углерода. Тем не менее, молекулярную массу
условились измерять в атомных единицах массы (а. е. м.).
Относительные
массы всех химических элементов измерены с высокой точностью, и их можно найти
в таблице Менделеева.
Например,
относительная атомная масса водорода равна 1, относительная атомная масса гелия
равна 4 и так далее.
Зная
атомные массы можно вычислить и молекулярную массу. Например, относительная
молекулярная масса соляной кислоты равна
Аналогичным
способом можно вычислить массы других молекул. Например, молекула серной кислоты
состоит из двух атомов водорода, одного атома серы и четырех атомов кислорода.
Таким образом, относительная молекулярная масса серной кислоты равна .
Еще
одно понятие, с которым необходимо ознакомиться при изучении
молекулярно-кинетической теории — это количество вещества. Можно,
конечно, определить количество вещества, как количество молекул, содержащихся в
данном теле. Но, как мы уже убедились, это количество просто огромно для любого
макроскопического тела, поэтому нам снова нужно ввести специальную величину.
Эта величина так и называется «количество вещества» и обозначается буквой ν.
Единицей измерения количества вещества является моль: .
1
моль — это количество вещества, в котором содержится столько же молекул или
атомов, сколько содержится атомов в 12 г углерода.
Это
число было определено Амедео Авогадро еще в 19 веке. Один моль любого вещества
содержит 6,02 х 1023 молекул. Это число называется числом
Авогадро или постоянной Авогадро.
Таким
образом, зная число молекул в теле, можно определить количество вещества:
С
постоянной Авогадро связана и другая величина, которая называется молярной
массой — это масса данного вещества, взятого в количестве 1 моль.
Исходя
из этого, можно заключить, что молярная масса вещества равна .
Как
видно из этого уравнения, молярная масса измеряется .
Заметим, что массу любого вещества можно представить, как произведение массы
молекулы этого вещества и количества молекул, содержащегося в данном веществе:
Тогда
можно записать:
Необходимо
отметить, что молярную массу можно также взять из таблицы Менделеева, как и
молекулярную массу. Они численно равны, но следует понимать, что они обозначают
различные величины, а потому измеряются в различных единицах измерения. В
таблице Менделеева молярная масса указана в г/моль, поэтому нельзя забывать
переводить её в кг/моль при решении задач по физике.
Пример
решения задачи.
Задача
1. Определите
массу 3 моль углекислого газа.
Основные положения МКТ. Масса и размер молекул. Количество вещества. Молекулярная физика
- Подробности
- Обновлено 07.10.2018 21:04
- Просмотров: 1192
МКТ – это просто!
«Ничто не существует, кроме атомов и пустого пространства …» – Демокрит
«Любое тело может делиться до бесконечности» – Аристотель
Основные положения молекулярно-кинетической теории (МКТ)
Цель МКТ – это объяснение строения и свойств различных макроскопических тел и тепловых явлений, в них протекающих, движением и взаимодействием частиц, из которых состоят тела.
Макроскопические тела – это большие тела, состоящие из огромного числа молекул.
Тепловые явления – явления, связанные с нагреванием и охлаждением тел.
Основные утверждения МКТ
1. Вещество состоит из частиц (молекул и атомов).
2. Между частицами есть промежутки.
3. Частицы беспорядочно и непрерывно движутся.
4. Частицы взаимодействуют друг с другом (притягиваются и отталкиваются).
Подтверждение МКТ:
1. экспериментальное
– механическое дробление вещества; растворение вещества в воде; сжатие и расширение газов; испарение; деформация тел; диффузия; опыт Бригмана: в сосуд заливается масло, сверху на масло давит поршень, при давлении 10 000 атм масло начинает просачиваться сквозь стенки стального сосуда;
– диффузия; броуновское движение частиц в жидкости под ударами молекул;
– плохая сжимаемость твердых и жидких тел; значительные усилия для разрыва твердых тел; слияние капель жидкости;
2. прямое
– фотографирование, определение размеров частиц.

Броуновское движение
Броуновское движение – это тепловое движение взвешенных частиц в жидкости (или газе).
Броуновское движение стало доказательством непрерывного и хаотичного (теплового) движения молекул вещества.
– открыто английским ботаником Р. Броуном в 1827 г.
– дано теоретическое объяснение на основе МКТ А. Эйнштейном в 1905 г.
– экспериментально подтверждено французским физиком Ж. Перреном.
Масса и размеры молекул
Размеры частиц
Диаметр любого атома составляет около ![]() см.
см.

Число молекул в веществе

где V – объем вещества, Vo – объем одной молекулы
Масса одной молекулы

где m – масса вещества,
N – число молекул в веществе
Единица измерения массы в СИ: [m]= 1 кг
В атомной физике массу обычно измеряют в атомных единицах массы (а.е.м.).
Условно принято считать за 1 а.е.м. :

Относительная молекулярная масса вещества
Для удобства расчетов вводится величина – относительная молекулярная масса вещества.
Массу молекулы любого вещества можно сравнить с 1/12 массы молекулы углерода.

где числитель – это масса молекулы, а знаменатель – 1/12 массы атома углерода
![]() – это величина безразмерная, т.е. не имеет единиц измерения
– это величина безразмерная, т.е. не имеет единиц измерения
Относительная атомная масса химического элемента

где числитель – это масса атома, а знаменатель – 1/12 массы атома углерода
![]() – величина безразмерная, т.е. не имеет единиц измерения
– величина безразмерная, т.е. не имеет единиц измерения
Относительная атомная масса каждого химического элемента дана в таблице Менделеева.
Другой способ определения относительной молекулярной массы вещества
Относительная молекулярная масса вещества равна сумме относительных атомных масс химических элементов, входящих в состав молекулы вещества.
Относительную атомную массу любого химического элемента берем из таблицы Менделеева!)
Количество вещества
Количество вещества (ν) определяет относительное число молекул в теле.

где N – число молекул в теле, а Na – постоянная Авогадро
Единица измерения количества вещества в системе СИ: [ν]= 1 моль
1 моль – это количество вещества, в котором содержится столько молекул (или атомов), сколько атомов содержится в углероде массой 0,012 кг.
Запомни!
В 1 моле любого вещества содержится одинаковое число атомов или молекул!
Но!
Одинаковые количества вещества для разных веществ имеют разную массу!
Постоянная Авогадро
Число атомов в 1 моле любого вещества называют числом Авогадро или постоянной Авогадро:

Молярная масса
Молярная масса (M) – это масса вещества, взятого в одном моле, или иначе – это масса одного моля вещества.

где
![]() – масса молекулы
– масса молекулы
![]() – постоянная Авогадро
– постоянная Авогадро
Единица измерения молярной массы: [M]=1 кг/моль.
Формулы для решения задач
Эти формулы получаются в результате подстановки вышерассмотренных формул.
Масса любого количества вещества

и формула для 7 класса

Количество вещества
![]()
Число молекул в веществе

Молярная масса

Масса одной молекулы

Связь между относительной молекулярной массой и молярной массой

Молекулярная физика. Термодинамика – Класс!ная физика
Основные положения МКТ. Масса и размер молекул. Количество вещества. —
Взаимодействие молекул. Строение твердых тел, жидкостей и газов. —
Идеальный газ. Основное уравнение МКТ. —
Температура. Тепловое равновесие. Абсолютная шкала температур. —
Уравнение состояния идеального газа. —
Изопроцессы. Газовые законы. —
Взаимные превращения жидкостей и газов. Влажность воздуха. —
Твердые тела. Кристаллические тела. Аморфные тела.
Масса молекул. Количество вещества
Физика10 класс
Материалы к уроку
-
25. Масса молекул. Количество вещества.doc
58.5 KBСкачать
-
25. Масса молекул. Количество вещества.ppt
9.18 MBСкачать
Конспект урока
Рассмотрим основные понятия молекулярно-кинетической теории: относительная молекулярная масса, количество вещества, постоянная АвогАдро, молярная масса.
Так как массы молекул очень малы, удобно использовать в расчетах не абсолютные значения масс, а относительные. По международному соглашению массы всех атомов и молекул сравниваются с 1/12 массы атома углерода. Массу частицы, измеренную в а.е.м. (атомная единица массы), принято называть относительной атомной (или молекулярной) массой. Значения относительных атомных масс приведены в периодической системе химических элементов Дмитрия Ивановича Менделеева. Относительная молекулярная масса молекулы вещества равна сумме относительных атомных масс атомов, составляющих данную молекулу. Относительные атомные массы всех химических элементов точно измерены. Относительная молекулярная масса (Mr) – отношение массы молекулы данного вещества к 1/12 массы атома углерода (m0c).
Складывая относительные массы элементов, входящих в состав молекулы вещества, можно вычислить относительную молекулярную массу вещества. Например, относительная молекулярная масса углекислого газа СО2 приблизительно равна 44, так как относительная атомная масса углерода точно равна 12, а кислорода примерно 16: к 12+2*16=44
Количество вещества – это физическая величина, характеризующая число структурных единиц в теле (атомов в атомарном веществе, молекул – в молекулярном).
Единицей количества вещества в СИ является моль. Один моль равен количеству вещества, в котором содержится столько же атомов или молекул, сколько атомов содержится в чистом углероде массой 0,012 кг. Такое число атомов называется числом Авогадро в честь итальянского ученого.
Для определения постоянной Авогадро надо найти массу одного атома углерода. Постоянную Авогадро можно определить, если разделить массу углерода, взятого в количестве одного моля на массу атома углерода:
Количество вещества равно отношению числа частиц в теле (атомов – в атомарном веществе, молекул – в молекулярном) к числу молекул в одном моле вещества, т.е. к числу Авогадро.
Если два разных тела состоят из одного и того же числа частиц (хотя и разных), то эти тела содержат одинаковое количество вещества (при этом массы тел могут не совпадать). Слева атомы углерода, справа атомы водорода.
Молярная масса M равна массе вещества, взятого в количестве один моль. Единица молярной массы – кг/моль.
Молярные массы веществ, молекулы которых состоят из одного атома, приведены в Периодической системе Д.И.Менделеева.
Например, информация в клетке с углеродом, помимо порядкового номера 6 углерода в Периодической системе, задает его молярную массу в г/моль 12,011. Молярная масса углерода в СИ равна 0,012 кг/моль. Для веществ, молекулы которых состоят из двух атомов (например, О2), молярная масса составит удвоенную цифру, взятую из Периодической системы.
Для молекул более сложного состава при расчете учитывается число атомов всех химических элементов в молекуле.
Если массу одной молекулы вещества обозначить через m0 (эм нулевое), то молярную массу можно трактовать как массу постоянной Авогадро (Nа) молекул. Масса любого количества вещества равна произведению массы одной молекулы на число молекул в теле. Заменив постоянное Авогадро и число молекул в теле их выражениями, получим, что количество вещества равно отношению массы вещества к его молярной массе.
Масса молекулы может быть рассчитана на основе молярной массы и числа Авогадро.
Масса одного атома водорода, например, составляет 1,67·10-27 кг, молекулы водорода Н2 в 2 раза больше, масса атома углерода в 12 раз, а молекулы кислорода в 32 раза больше массы атома водорода.
Размер молекулы a может быть оценен как размер кубика, в котором содержится одна молекула, исходя из плотности твердых или жидких веществ и массы одной молекулы.
Для воды диаметр а = 3·10-10 м. Для газов, в которых молекулы разделены друг от друга зазором, как показано на рисунке, такая оценка дает среднее расстояние между молекулами.
Часто при решении той или иной задачи важнее знать не число частиц вещества, а их концентрацию. Концентрация (n) показывает, сколько частиц содержится в единице объема (чаще всего – в одном кубическом метре) данного вещества.
Рассмотрим задачи.
Определим молярную массу воды.
Решение. В молекуле воды Н2О 2 атома водорода и 1 атом кислорода. Атомная масса водорода = 1, а кислорода – 16. Следовательно молекулярная масса воды равна 2* 1 + 16 = 18 атомных единиц массы, а молярная масса воды =0,018 кг/моль.
Какое количество вещества содержится в воде массой 200 г?
Для решения задачи переведем массу в систему СИ. Запишем формулу для определения количества вещества.
Чтобы иметь возможность воспользоваться ей, надо найти молярную массу воды.
Теперь подставим наши результаты в исходную формулу и получим ответ.
В воде массой 200 г содержится 11,1 моль вещества.
Остались вопросы по теме? Наши педагоги готовы помочь!
Подготовим к ЕГЭ, ОГЭ и другим экзаменам
Найдём слабые места по предмету и разберём ошибки
Повысим успеваемость по школьным предметам
Поможем подготовиться к поступлению в любой ВУЗ
Молярная масса
Массу одного моля вещества называют молярной массой.
Молярная масса обозначается 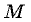 и в системе СИ измеряется в кг/моль.
и в системе СИ измеряется в кг/моль.
Таким образом, молярная масса 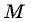 связана с массой образца
связана с массой образца 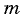 соотношением
соотношением 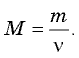 Поэтому, зная массу образца и молярную массу, можно определить, сколько молей вещества содержит данный образец, по формуле
Поэтому, зная массу образца и молярную массу, можно определить, сколько молей вещества содержит данный образец, по формуле 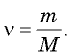
Поскольку в одном моле вещества содержится 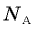 молекул, молярная масса связана с массой
молекул, молярная масса связана с массой 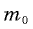 одной молекулы соотношением
одной молекулы соотношением 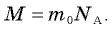
- Примеры
- Как связано число молекул с массой вещества и его молярной массой?
Молекулярная физика и термодинамика.
2014




