- Относительная молекулярная масса HCl: 36.46094
- Молярная масса HCl: 36.46094 г/моль (0.03646 кг/моль)
| Элемент | Всего атомов | Атомная масса, а.е.м. | Общая масса атомов, а.е.м. |
|---|---|---|---|
| H (водород) | 1 | 1.00794 | 1.00794 |
| Cl (хлор) | 1 | 35.453 | 35.453 |
| 36.46094 |
Расчёт молярной и относительной молекулярной массы HCl
- Mr[HCl] = Ar[H] + Ar[Cl] = 1.00794 + 35.453 = 36.46094
- Молярная масса (в кг/моль) = Mr[HCl] : 1000 = 36.46094 : 1000 = 0.03646 кг/моль
Расчёт массовых долей элементов в HCl
- Массовая доля водорода (H) = 1.00794 : 36.46094 * 100 = 2.764 %
- Массовая доля хлора (Cl) = 35.453 : 36.46094 * 100 = 97.236 %
Калькулятор массы
Ученик
(117),
закрыт
2 года назад
Вячек
Высший разум
(391245)
9 лет назад
смотришь в таблицу Менделеева и находишь там атомные массы этих элементов, складываешь их, вот и будет молекулярная масса! А она численно равна молярной массе!
Вычисление молярной массы
To calculate molar mass of a chemical compound enter its formula and click ‘Compute’. В химической формуле, вы можете использовать:
- Любой химический элемент. Capitalize the first letter in chemical symbol and use lower case for the remaining letters: Ca, Fe, Mg, Mn, S, O, H, C, N, Na, K, Cl, Al.
- Функциональные группы:D, Ph, Me, Et, Bu, AcAc, For, Ts, Tos, Bz, TMS, tBu, Bzl, Bn, Dmg
- круглые () и квадратные [] скобки.
- Общие составные имена.
Примеры расчета молярной массы:
NaCl,
Ca(OH)2,
K4[Fe(CN)6],
CuSO4*5H2O,
water,
nitric acid,
potassium permanganate,
ethanol,
fructose.
Molar mass calculator also displays common compound name, Hill formula, elemental composition, mass percent composition, atomic percent compositions and allows to convert from weight to number of moles and vice versa.
Вычисление молекулярной массы (молекулярная масса)
Для того, чтобы рассчитать молекулярную массу химического соединения, введите её формулу, указав его количество массы изотопа после каждого элемента в квадратных скобках.
Примеры молекулярные вычисления веса:
C[14]O[16]2,
S[34]O[16]2.
Определение молекулярной массы, молекулярный вес, молекулярная масса и молярная масса
- Молекулярная масса ( молекулярной массой ) это масса одной молекулы вещества, выражающаяся в атомных единицах массы (и). (1 и равна 1/12 массы одного атома углерода-12)
- Молярная масса ( молекулярной массой ) является масса одного моля вещества и выражается в г / моль.
Массы атомов и изотопов с NIST статью .
См. также: молекулярные массы аминокислот
| Соляная кислота | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование |
Хлороводородная кислота |
| Хим. формула | HCl |
| Физические свойства | |
| Состояние | Жидкость |
| Молярная масса | 36.46 г/моль |
| Плотность | 1.19 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -30 °C |
| • кипения | 48 °C |
| Энтальпия | |
| • образования | -605.22 кДж/моль |
| Давление пара | 190 гПа[3] |
| Химические свойства | |
Константа диссоциации кислоты  |
-10 |
| Растворимость | |
| • в воде | Растворима |
| Классификация | |
| Рег. номер CAS | 7647-01-0 |
| Рег. номер EINECS | 933-977-5 |
| Кодекс Алиментариус | E507 |
| RTECS | MW4025000 |
| Безопасность | |
| Предельная концентрация | 5 мг/м³[1] |
| Токсичность | 3 класс опасности[2] |
| Пиктограммы СГС |
|
| NFPA 704 |
0 3 1 ACID |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Соля́ная кислота́ (также хлороводоро́дная, или хлористоводоро́дная кислота, химическая формула — HCl) — сильная химическая неорганическая кислота. Раствор хлороводорода в воде.
При стандартных условиях — это сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около 0,5 % присутствует в желудке человека. Соли соляной кислоты называются хлоридами.
История[править | править код]
Впервые хлороводород получил алхимик Василий Валентин, нагрев гептагидрат сульфата железа с поваренной солью и назвав полученное вещество «духом соли» (лат. spiritus salis). Иоганн Глаубер в XVII веке получил соляную кислоту из поваренной соли и серной кислоты. В 1790 году британский химик Гемфри Дэви получил хлороводород из водорода и хлора, таким образом установив его состав. Возникновение промышленного производства соляной кислоты связано с технологией получения карбоната натрия: на первой стадии этого процесса поваренную соль вводили в реакцию с серной кислотой, в результате чего выделялся хлороводород. В 1863 году в Англии был принят закон «Alkali Act», согласно которому запрещалось выбрасывать этот хлороводород в воздух, а необходимо было пропускать его в воду. Это привело к развитию промышленного производства соляной кислоты. Дальнейшее развитие произошло благодаря промышленным методам получения гидроксида натрия и хлора путём электролиза растворов хлорида натрия[4].
Физические свойства[править | править код]
Физические свойства соляной кислоты сильно зависят от концентрации растворённого хлороводорода:
| Концентрация (вес), мас. % | Концентрация (г/л), кг HCl/м³ | Плотность, кг/л | Молярность, M, или моль/л | Водородный показатель (pH) | Вязкость, мПа·с | Удельная теплоемкость, кДж/(кг·К) | Давление пара, кПа | Температура кипения, °C | Температура плавления, °C |
|---|---|---|---|---|---|---|---|---|---|
| 10 % | 104,80 | 1,048 | 2,87 | −0,4578 | 1,16 | 3,47 | 1,95 | 103 | −18 |
| 20 % | 219,60 | 1,098 | 6,02 | −0,7796 | 1,37 | 2,99 | 1,40 | 108 | −59 |
| 30 % | 344,70 | 1,149 | 9,45 | −0,9754 | 1,70 | 2,60 | 2,13 | 90 | −52 |
| 32 % | 370,88 | 1,159 | 10,17 | −1,0073 | 1,80 | 2,55 | 3,73 | 84 | −43 |
| 34 % | 397,46 | 1,169 | 10,90 | −1,0374 | 1,90 | 2,50 | 7,24 | 71 | −36 |
| 36 % | 424,44 | 1,179 | 11,64 | −1,06595 | 1,99 | 2,46 | 14,50 | 61 | −30 |
| 38 % | 451,82 | 1,189 | 12,39 | −1,0931 | 2,10 | 2,43 | 28,30 | 48 | −26 |
При 20 °C, 1 атм (101,325 кПа)
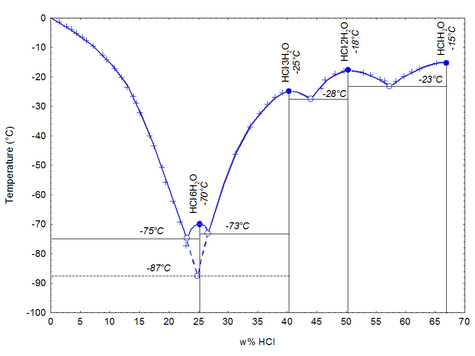
При низкой температуре хлороводород с водой даёт кристаллогидраты составов 




Химические свойства[править | править код]
- Взаимодействие с металлами, стоящими в ряду электрохимических потенциалов до водорода, с образованием соли и выделением газообразного водорода:
-
,
,
.
- Взаимодействие с оксидами металлов с образованием растворимой соли и воды:
-
,
,
.
- Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):
-
,
,
.
- Взаимодействие с солями металлов, образованных более слабыми кислотами, например, с угольной кислотой:
-
.
- Взаимодействие с сильными окислителями (перманганат калия, диоксид марганца) с выделением газообразного хлора:
-
.

Соляная кислота (в стакане) взаимодействует с аммиаком
- Взаимодействие с аммиаком с образованием густого белого дыма, состоящего из мельчайших кристаллов хлорида аммония[6]:
-
.
- Качественная реакция на соляную кислоту и её соли — взаимодействие кислоты с нитратом серебра, при котором образуется белый творожистый осадок хлорида серебра, нерастворимый в азотной кислоте[7]:
-
.
Получение[править | править код]
Соляную кислоту получают растворением газообразного хлороводорода (HCl) в воде. Хлороводород получают сжиганием водорода в хлоре, полученная таким способом кислота называется синтетической. Также соляную кислоту получают из абгазов — побочных газов, образующихся при различных процессах, например, при хлорировании углеводородов. Хлороводород, содержащийся в этих газах, называется абгазным, а полученная таким образом кислота — абгазной. В последние десятилетия доля абгазной соляной кислоты в объёме производства постепенно увеличивается, вытесняя кислоту, полученную сжиганием водорода в хлоре. Но полученная методом сжигания водорода в хлоре соляная кислота содержит меньше примесей и применяется при необходимости высокой чистоты.
В лабораторных условиях используется разработанный алхимиками способ, заключающийся в действии концентрированной серной кислоты на твёрдую поваренную соль:
-
.
При температуре выше 550 °C и избытке поваренной соли возможно взаимодействие:
-
.
Получение путём гидролиза хлоридов магния, алюминия (производится нагревание гидратированной соли):
-
,
.
Эти реакции могут идти не до конца с образованием основных хлоридов (оксихлоридов) переменного состава, например:
-
[8]
В промышленности хлороводород получают реакцией горения водорода в хлоре:
Хлороводород хорошо растворим в воде. Так, при 0 °C один объём воды может поглотить 507 объёмов 

Применение[править | править код]

Промышленность[править | править код]
- Применяется в гидрометаллургии и гальванопластике (травление, декапирование), для очистки поверхности металлов при пайке и лужении, для получения хлоридов цинка, марганца, железа и др. металлов. В смеси с поверхностно-активными веществами используется для очистки керамических и металлических изделий (тут необходима ингибированная кислота) от загрязнений и дезинфекции.
- В пищевой промышленности зарегистрирована как регулятор кислотности (пищевая добавка E507). Применяется для изготовления сельтерской (содовой) воды.
Медицина[править | править код]
- Естественная составная часть желудочного сока человека. В концентрации 0,3—0,5 %, обычно в смеси с ферментом пепсином, назначается внутрь при недостаточной кислотности.
Особенности обращения[править | править код]
![]()


Соляная кислота относится к веществам III класса опасности[2]. Рекомендуемая ПДК в рабочей зоне — 5 мг/м³[1].
Высококонцентрированная соляная кислота представляет собой едкое вещество. При попадании на кожу вызывает сильные химические ожоги. Особенно опасным считается попадание в глаза (в значительном количестве). Для нейтрализации ожогов применяют раствор слабого основания, или соли слабой кислоты, обычно пищевой соды.
При открывании сосудов с концентрированной соляной кислотой пары хлороводорода, притягивая влагу воздуха, образуют туман, раздражающий глаза и дыхательные пути человека.
Реагируя с сильными окислителями (хлорной известью, диоксидом марганца, перманганатом калия), образует токсичный газообразный хлор.
В РФ оборот соляной кислоты концентрации 15 % и более — ограничен[9].
Примечания[править | править код]
- ↑ 1 2 ГОСТ 12.1.005-76 “Воздух рабочей зоны. Санитарно-гигиенические требования”.
- ↑ 1 2 ГОСТ 12.1.007-76 “Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности”.
- ↑ https://gestis.dguv.de/data?name=520030
- ↑ Ullmann, 2000, p. 191.
- ↑ Ullmann, 2000, p. 194.
- ↑ Дым без огня: взаимодействие аммиака с хлороводородом Архивная копия от 4 марта 2016 на Wayback Machine — видеоопыт в Единой коллекции цифровых образовательных ресурсов
- ↑ Ходаков Ю.В., Эпштейн Д. А., Глориозов П. А. § 82. Соляная кислота // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 195—196. — 240 с. — 1 630 000 экз.
- ↑ page-book.ru — Реми Г. Курс неорганической химии (Том 1): Стр.301. Дата обращения: 23 августа 2012. Архивировано из оригинала 11 мая 2013 года.
- ↑ Постановление Правительства Российской Федерации от 3 июня 2010 года № 398 Архивировано 30 июня 2016 года.
Ссылки[править | править код]
- Austin S., Glowacki A. Hydrochloric Acid (англ.) // Ullmann’s Encyclopedia of Industrial Chemistry. — Wiley, 2000. — doi:10.1002/14356007.a13_283.
Molar mass of HCl = 36.46094 g/mol
This compound is also known as Hydrochloric Acid.
Convert grams HCl to moles
or
moles HCl to grams
Molecular weight calculation:
1.00794 + 35.453
Percent composition by element
Element: Chlorine
Symbol: Cl
Atomic Mass: 35.453
# of Atoms: 1
Mass Percent: 97.236%
Element: Hydrogen
Symbol: H
Atomic Mass: 1.00794
# of Atoms: 1
Mass Percent: 2.764%
Calculate the
molecular weight of a chemical compound
More information
on molar mass and molecular weight
In chemistry, the formula weight is a quantity computed by multiplying the atomic weight (in atomic mass units) of each element in a chemical formula by the number of atoms of that element present in the formula, then adding all of these products together.
If the formula used in calculating molar mass is the molecular formula, the formula weight computed is the molecular weight. The percentage by weight of any atom or group of atoms in a compound can be computed by dividing the total weight of the atom (or group of atoms) in the formula by the formula weight and multiplying by 100.
Using the chemical formula of the compound and the periodic table of elements, we can add up the atomic weights and calculate molecular weight of the substance.
The atomic weights used on this site come from NIST, the National Institute of Standards and Technology. We use the most common isotopes. This is how to calculate molar mass (average molecular weight), which is based on isotropically weighted averages. This is not the same as molecular mass, which is the mass of a single molecule of well-defined isotopes. For bulk stoichiometric calculations, we are usually determining molar mass, which may also be called standard atomic weight or average atomic mass.
A common request on this site is to convert grams to moles. To complete this calculation, you have to know what substance you are trying to convert. The reason is that the molar mass of the substance affects the conversion. This site explains how to find molar mass.
Formula weights are especially useful in determining the relative weights of reagents and products in a chemical reaction. These relative weights computed from the chemical equation are sometimes called equation weights.
Finding molar mass starts with units of grams per mole (g/mol). When calculating molecular weight of a chemical compound, it tells us how many grams are in one mole of that substance. The formula weight is simply the weight in atomic mass units of all the atoms in a given formula.