как вычислить молярную массу водорода?
Профи
(975),
закрыт
8 лет назад
Ирина Владимировна
Ученик
(128)
8 лет назад
Итак начнём наше путешествие по изучению малярной массы водорода
Первое – Водород – легчайший газ, первый и простейший элемент таблицы Менделеева. Атом его наиболее распространенного изотопа протия состоит из единственного протона и единственного электрона. Водород – самое массовое вещество во Вселенной. Именно из него, главным образом, состоят звезды. Этот элемент находит широкое применение в разных отраслях промышленности. Часто возникает необходимость вычислить массу какого-то количества водорода.
А теперь сам дальше перейди по ссылке и изучи материал сам : http://www.kakprosto.ru/kak-130149-kak-vychislit-massu-odnogo-molya-vodoroda
Антон Кочуг
Профи
(914)
8 лет назад
Этот газ всегда имеет эмпирическую формулу H2, по таблице смотришь атомную массу (она в данном случае равна 1) и умножаешь на кол-во атомов ( в данном у нас два атома), поэтому молярная масса равна 2

Масса водорода в 1 л воды равна ( М(H2O)=18*10^-3 кг/моль, М(Н2)=2*10^-3 кг/моль, р воды=10^3 кг/м^3 )
P.S.Это молекулярная физика, поэтому все нужно переводить в кг
Комментарии



Светило науки – 1118 ответов – 8179 раз оказано помощи
M(молярная масса)=m₀(масса молекулы)*Na(число Авогадро);m₀=M/Na;
m(масса вещества)=m₀*N(число молекул вещества);
N=m/m₀=m*Na/M; Найдем количество молекул H₂O в 1 литре воды(1 литр-1 кг, т.к. плотность воды 1000 кг/м³)
В каждой молекуле H₂O содержится два атома H, значит масса H₂ будет равна m=m₀(H₂)*N(H₂O);
m(H₂)=1/9≈0.1 кг
Ответ:m(H₂)≈0.1 кг
Моль — условное количество вещества
Добавлено: 3 октября 2021 в 12:58

Химия — наука, изучающая взаимодействие веществ на атомном и молекулярном уровнях. Эти процессы значительно отличаются от привычного нам макроуровня и поэтому требуют специфических подходов, в том числе к «подсчету» и «взвешиванию».
Школьный курс химии включает понятия «моль» и «молярной массы». Они кажутся сложными, но если разобраться, то вы без труда поймете сущность этих понятий и научитесь ими пользоваться при решении задач.
Моль
Понятие «моль» попытаемся разобрать и, самое главное, понять на примере всем знакомой реакции взаимодействия кислорода и водорода. Когда одна молекула O2 соединяется с двумя молекулами H2, получается две молекулы H2O:
- O2 + 2H2 = 2H2O
То есть, чтобы максимально полно провести химическую реакцию, мы должны взять на каждую молекулу кислорода две молекулы водорода. Итак, у нас есть 100 г кислорода.
Сколько понадобится водорода для протекания процесса? И тут возникает первый вопрос: сколько молекул в 100 г кислорода? Наверное, миллиарды или даже миллиарды миллиардов? И сколько их в 100 г водорода? Уж точно в не в 2 раза меньше.
Как вообще подсчитать молекулы, ведь они бывают совершенно разными, «тяжелыми» и «легкими». Этими вопросами задавались и люди, закладывавшие основу современной химической науки.
Был найден простой выход, который помогает легко и изящно решить проблему. Химики решили взять за единицу измерения не одну молекулу, а определенное их количество, причем очень большое. Таким образом эта единица измерения приводит микроуровень к макроуровню. Она называется «моль».
Моль — это количество вещества из 6,02214076⋅1023 атомов или молекул. Оно не имеет физического смысла и изначально было привязано к массе определенного количества (12 граммов) углерода-12, но позже переопределено, как и многие другие единицы системы СИ.
В школьных расчетах количество структурных единиц в моле, которое также называется постоянной Авогадро, обычно округляют до 6,022⋅1023 и обозначают NA.
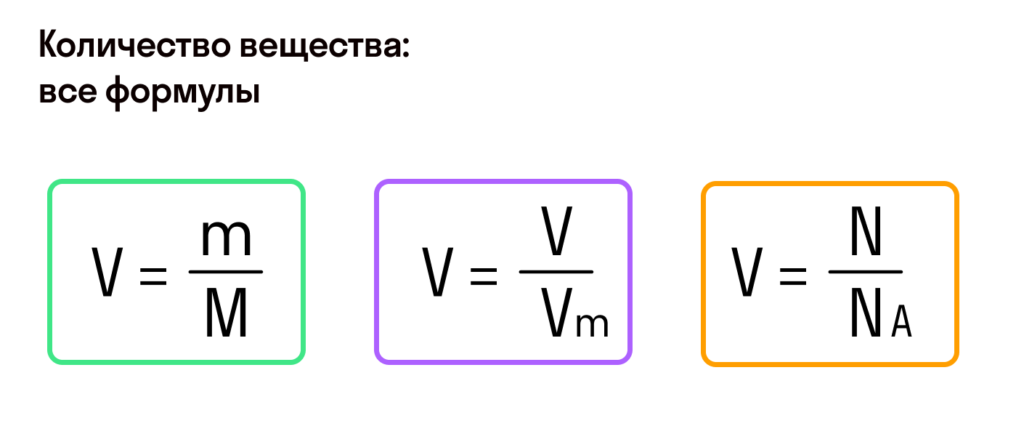
С этой величиной связано другое химическое понятие — «количество вещества», то есть количество структурных единиц в определенной его порции. Оно обозначается буквой ν (ню).
Примеры
В стакане содержится 2 моль воды. Сколько молекул воды находится в стакане?
- N = ν⋅ NA =2 ⋅ 6,022⋅1023 = 12,044⋅1023 молекул воды.
Также можно решить обратную задачу. Сколько молей вещества составляют 24,088⋅1023 молекул воды?
- ν⋅ = N / NA = 24,088⋅1023 / 6,022⋅1023 = 4 моля.
Что называется молярной массой
Итак, мы поняли, что моль — условное количество вещества, выбранное для удобства химиков. Это даже не миллиарды миллиардов, как мы предположили ранее, а миллиарды триллионов, что никак не облегчает задачу подсчета этих структурных единиц.
Как же все-таки узнать, сколько атомов или молекул в 100 граммах того или иного вещества? Теперь хорошо бы связать количество вещества и его массу, ведь это не одно и то же. Нам поможет «молярная масса» — 1 моль вещества или 6,022⋅1023 структурных единиц этого вещества.
Итак, масса вещества равна массе порции вещества m к количеству молекул ν в его порции:
- М = m / ν.
Вооружившись этим знанием, мы можем переводить граммы в число молекул и наоборот. При этом следует учесть, что молярная масса численно идентична молекулярной массе (то есть массе молекулы), выраженной в атомных единицах массы, и относительной молекулярной массе.
Пример
Найдем массу 5 моль воды.
Чтобы решить эту задачу, обратимся к формуле молярной массы и выразим из нее массу:
- m = М ⋅ ν
В этой формуле мы знаем количество вещества ν = 5 моль, а молярную массу сложной молекулы нужно определить, как сумму молярных масс составляющих ее химических элементов:
- M (H2O) = 2 ⋅M (H) + M (O)
Где взять молярные массы кислорода и водорода (в соединение входит два атома водорода, поэтому его молярную массу умножаем на 2)?
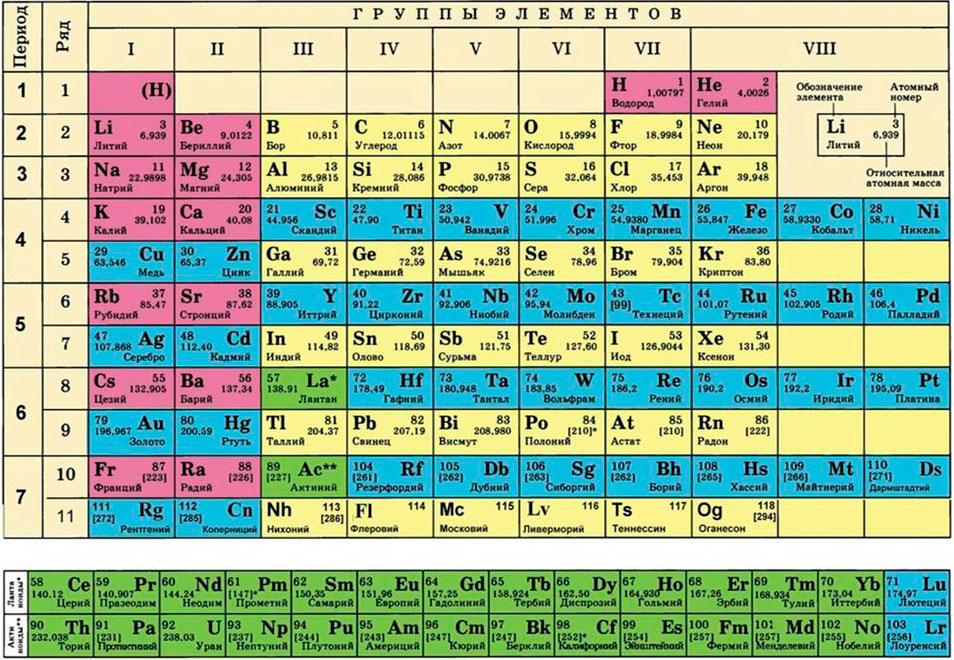
Для этого нам понадобится таблица Менделеева и значение «относительной атомной массы», которая, как мы уже знаем, идентична молекулярной. Это значение приведено для каждого химического элемента и для водорода равно 1,00797 (то есть близко к 1), для углерода — близко к 6, для кислорода — около 16.
Подставим соответствующие значения в исходную формулу и получим:
- M (H2O) = 2 ⋅M (H) + M (O) = 2 ⋅ 1 + 16 = 18 г/моль.
То есть вес 1 моль воды составляет 18 граммов. Теперь можем подсчитать массу 5 моль воды:
- m = М ⋅ ν = 18 ⋅ 5 = 90 г.
Аналогичным образом мы можем подсчитать количество вещества, которое содержится в определенном образце заданной массы. Для примера возьмем оксид алюминия Al2O3 и узнаем, сколько моль в 400 граммах этого вещества. Для этого выразим количество вещества через молярную массу и подставим исходные данные:
- ν = m / М = 400 / (2 ⋅ М (Al) + 3 ⋅ (O)) = 400 / (2 ⋅ 75 + 3 ⋅ 16) = 400 / (150 + 48) = 400 / 198 ≈ 2,02 моль.
Занимайтесь на курсах ЕГЭ и ОГЭ в паре TwoStu и получите максимум баллов на экзамене:

Эксперт по подготовке к ЕГЭ, ОГЭ и ВПР
Задать вопрос
Закончил Московский физико-технический институт (Физтех) по специальности прикладная физика и математика. Магистр физико-математических наук. Преподавательский стаж более 13 лет. Соучредитель курсов ЕГЭ и ОГЭ в паре TwoStu.
Читайте также:
В химии определение массового процента элемента в соединении может показаться сложным, но расчет прост. Например, чтобы определить массовую долю водорода в воде (H2O), разделите молярную массу водорода на общую молярную массу воды, а затем умножьте результат на 100. Вся необходимая информация находится в таблице Менделеева.
TL; DR (слишком длинный; Не читал)
Массовая доля водорода в воде составляет 11,19%.
Молярная масса элементов
Для любого соединения вы определяете общую молярную массу, складывая молярные массы каждого элемента. Когда вы просматриваете элемент в периодической таблице, число вверху – это атомный номер, а цифра под символом элемента – это средняя атомная масса, выраженная в атомных единицах массы (а.е.м.). Для любых атомов, которые встречаются в молекуле более одного раза, умножьте молярную массу на количество элемента в химической формуле. Например, в молекуле воды два атома водорода, поэтому умножьте атомную массу водорода на 2.
Молярная масса воды
Атомная масса водорода, взятая из периодической таблицы, равна 1,008. Поскольку в молекуле два атома водорода, умножьте 1,008 на 2, чтобы получить 2,016. Атомная масса кислорода составляет 16,00, а в молекуле только один атом кислорода, поэтому общая масса кислорода остается 16,00. Складываем 2,016 к 16,00, получаем 18,016. Это общая молярная масса воды.
Массовый процент водорода
Чтобы найти массовый процент водорода в воде, возьмите молярную массу водорода в молекуле воды, разделите на общую молярную массу воды и умножьте на 100. Разделив 2,016 на 18,016, вы получите 0,1119. Умножьте 0,1119 на 100, чтобы получить ответ: 11,19 процента.
Массовый процент кислорода
Вы можете использовать два метода, чтобы определить массовый процент кислорода в воде. Из приведенного выше расчета вы знаете, что процентное содержание водорода составляет 11,19 процента, а в воде есть только водород и кислород, поэтому два сложенных вместе должны равняться 100 процентам. Вычтем 11,19 из 100, чтобы получить 88,81 процента. Второй метод такой же, как и для определения массового процента водорода. Из предыдущих расчетов вы знаете, что общая молярная масса кислорода в воде составляет 16,00. Разделите 16,00 на общую молярную массу воды 18,016, чтобы получить 0,8881. Умножьте 0,8881 на 100, чтобы получить процентное значение: 88,81 процента.
Соотношение масс
Поскольку в молекуле воды ровно два элемента, вы можете использовать уже вычисленные числа для определения соотношения масс. Например, чтобы найти отношение массы водорода к массе кислорода в воде, разделите общую молярную массу водорода 2,016 на молярную массу кислорода 16,00 и получите 0,126. Чтобы найти отношение кислорода к водороду, разделите 16,00 на 2,016 и получите 7,937. Это означает, что в воде кислород почти в 8 раз превышает водород.
Масса водорода
На нашей планете содержится около 1,4 * 10 18 тонн воды (H2O). Какова масса водорода (H2), содержащегося в этом количестве воды (H2O)?
Решение задачи
Учитывая, что молекулярная масса воды (H2O) равна:
Mr (H2O) = 2 ∙ 1 + 16 = 18.
Следовательно, молярная масса воды (H2O) равна 18 г/моль.
Молярная масса вещества, имеющего молекулярную структуру, численно равна относительной молекулярной массе.
Значит, один моль воды (H2O) равен по массе 18 г.
Учитывая, что в 1 грамме 10-6 тонн, найдем массу водорода (H2), содержащегося в 1,4 * 10 18 тонн воды (H2O). Составим соотношение:
в H2O массой 18 ∙ 10-6 т содержится водород массой 2 ∙ 10-6 т
в H2O массой 1,4 * 10 18 т содержится водород массой х т
Откуда:
Значит, масса водорода (H2), содержащегося в 1,4 * 10 18 тонн воды (H2O) равна 1,56 ∙ 1017 тонн.
Ответ:
масса водорода равна 1,56 ∙ 1017 тонн.