О тепловой энергии простым языком!
Опубликовано 13 Окт 2013
Рубрика: Теплотехника | 117 комментариев

…энергию вакуума и еще существующую только в теории – темную энергию. В этой статье, первой в рубрике «Теплотехника», я попытаюсь на простом и доступном языке, используя практический пример, рассказать о важнейшем виде энергии в жизни людей — о тепловой энергии и о рождающей ее во времени тепловой мощности.
Несколько слов для понимания места теплотехники, как раздела науки о получении, передаче и применении тепловой энергии. Современная теплотехника выделилась из общей термодинамики, которая в свою очередь является одним из разделов физики. Термодинамика – это дословно «теплый» плюс «силовой». Таким образом, термодинамика – это наука об «изменении температуры» системы.
Воздействие на систему извне, при котором изменяется ее внутренняя энергия, может являться результатом теплообмена. Тепловая энергия, которая приобретается или теряется системой в результате такого взаимодействия с окружающей средой, называется количеством теплоты и измеряется в системе СИ в Джоулях.
Если вы не инженер-теплотехник, и ежедневно не занимаетесь теплотехническими вопросами, то вам, столкнувшись с ними, иногда без опыта бывает очень трудно быстро в них разобраться. Трудно без наличия опыта представить даже размерность искомых значений количества теплоты и тепловой мощности. Сколько Джоулей энергии необходимо чтобы нагреть 1000 метров кубических воздуха от температуры -37˚С до +18˚С?.. Какая нужна мощность источника тепла, чтобы сделать это за 1 час?.. На эти не самые сложные вопросы способны сегодня ответить «сходу» далеко не все инженеры. Иногда специалисты даже помнят формулы, но применить их на практике могут лишь единицы!
Прочитав до конца эту статью, вы сможете легко решать реальные производственные и бытовые задачи, связанные с нагревом и охлаждением различных материалов. Понимание физической сути процессов теплопередачи и знание простых основных формул – это главные блоки в фундаменте знаний по теплотехнике!
Количество теплоты при различных физических процессах.
Большинство известных веществ могут при разных температуре и давлении находиться в твердом, жидком, газообразном или плазменном состояниях. Переход из одного агрегатного состояния в другое происходит при постоянной температуре (при условии, что не меняются давление и другие параметры окружающей среды) и сопровождается поглощением или выделением тепловой энергии. Не смотря на то, что во Вселенной 99% вещества находится в состоянии плазмы, мы в этой статье не будем рассматривать это агрегатное состояние.
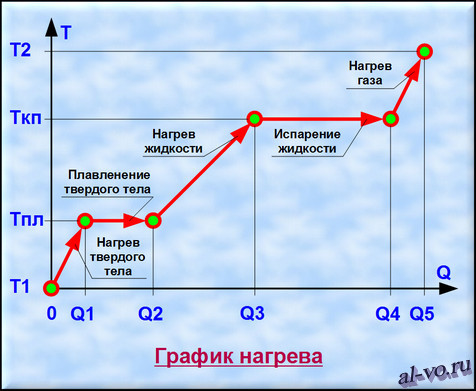
Рассмотрим график, представленный на рисунке. На нем изображена зависимость температуры вещества Т от количества теплоты Q, подведенного к некой закрытой системе, содержащей определенную массу какого-то конкретного вещества.
1. Твердое тело, имеющее температуру T1, нагреваем до температуры Tпл, затрачивая на этот процесс количество теплоты равное Q1.
2. Далее начинается процесс плавления, который происходит при постоянной температуре Тпл (температуре плавления). Для расплавления всей массы твердого тела необходимо затратить тепловой энергии в количестве Q2— Q1.
3. Далее жидкость, получившаяся в результате плавления твердого тела, нагреваем до температуры кипения (газообразования) Ткп, затрачивая на это количество теплоты равное Q3–Q2.
4. Теперь при неизменной температуре кипения Ткп жидкость кипит и испаряется, превращаясь в газ. Для перехода всей массы жидкости в газ необходимо затратить тепловую энергию в количестве Q4–Q3.
5. На последнем этапе происходит нагрев газа от температуры Ткп до некоторой температуры Т2. При этом затраты количества теплоты составят Q5–Q4. (Если нагреем газ до температуры ионизации, то газ превратится в плазму.)
Таким образом, нагревая исходное твердое тело от температуры Т1 до температуры Т2 мы затратили тепловую энергию в количестве Q5, переводя вещество через три агрегатных состояния.
Двигаясь в обратном направлении, мы отведем от вещества то же количество тепла Q5, пройдя этапы конденсации, кристаллизации и остывания от температуры Т2 до температуры Т1. Разумеется, мы рассматриваем замкнутую систему без потерь энергии во внешнюю среду.
Заметим, что возможен переход из твердого состояния в газообразное состояние, минуя жидкую фазу. Такой процесс именуется возгонкой, а обратный ему процесс – десублимацией.
Итак, уяснили, что процессы переходов между агрегатными состояниями вещества характеризуются потреблением энергии при неизменной температуре. При нагреве вещества, находящегося в одном неизменном агрегатном состоянии, повышается температура и также расходуется тепловая энергия.
Главные формулы теплопередачи.
Формулы очень просты.
Количество теплоты Q в Дж рассчитывается по формулам:
1. Со стороны потребления тепла, то есть со стороны нагрузки:
1.1. При нагревании (охлаждении):
Q=m*c*(Т2–Т1)
Здесь и далее:
m – масса вещества в кг
с – удельная теплоемкость вещества в Дж/(кг*К)
1.2. При плавлении (замерзании):
Q=m*λ
λ – удельная теплота плавления и кристаллизации вещества в Дж/кг
1.3. При кипении, испарении (конденсации):
Q=m*r
r – удельная теплота газообразования и конденсации вещества в Дж/кг
2. Со стороны производства тепла, то есть со стороны источника:
2.1. При сгорании топлива:
Q=m*q
q – удельная теплота сгорания топлива в Дж/кг
2.2. При превращении электроэнергии в тепловую энергию (закон Джоуля — Ленца):
Q=t*I*U=t*R*I^2=(t/R)*U^2
t – время в с
I – действующее значение тока в А
U – действующее значение напряжения в В
R – сопротивление нагрузки в Ом
Делаем вывод – количество теплоты прямо пропорционально массе вещества при всех фазовых превращениях и при нагреве дополнительно прямо пропорционально разности температур. Коэффициенты пропорциональности (c, λ, r, q) для каждого вещества имеют свои значения и определены опытным путем (берутся из справочников).
Тепловая мощность N в Вт – это количество теплоты переданное системе за определенное время:
N=Q/t
Чем быстрее мы хотим нагреть тело до определенной температуры, тем большей мощности должен быть источник тепловой энергии – все логично.
В жизни бывает часто необходимо сделать быстрый оценочный расчет, чтобы понять – имеет ли смысл продолжать изучение темы, делая проект и развернутые точные трудоемкие расчеты. Сделав за несколько минут расчет даже с точностью ±30%, можно принять важное управленческое решение, которое будет в 100 раз более дешевым и в 1000 раз более оперативным и в итоге в 100000 раз более эффективным, чем выполнение точного расчета в течение недели, а то и месяца, группой дорогостоящих специалистов…
Условия задачи:
В помещение цеха подготовки металлопроката размерами 24м х 15м х 7м завозим со склада на улице металлопрокат в количестве 3т. На металлопрокате есть лед общей массой 20кг. На улице -37˚С. Какое количество теплоты необходимо, чтобы нагреть металл до +18˚С; нагреть лед, растопить его и нагреть воду до +18˚С; нагреть весь объем воздуха в помещении, если предположить, что до этого отопление было полностью отключено? Какую мощность должна иметь система отопления, если все вышесказанное необходимо выполнить за 1час? (Очень жесткие и почти не реальные условия – особенно касающиеся воздуха!)
Расчет выполним в программе MS Excel или в программе OOo Calc.
С цветовым форматированием ячеек и шрифтов ознакомьтесь на странице «О блоге».
Исходные данные:
1. Названия веществ пишем:
в ячейку D3: Сталь
в ячейку E3: Лед
в ячейку F3: Лед/вода
в ячейку G3: Вода
в ячейку G3: Воздух
2. Названия процессов заносим:
в ячейки D4, E4, G4, G4: нагрев
в ячейку F4: таяние
3. Удельную теплоемкость веществ c в Дж/(кг*К) пишем для стали, льда, воды и воздуха соответственно
в ячейку D5: 460
в ячейку E5: 2110
в ячейку G5: 4190
в ячейку H5: 1005
4. Удельную теплоту плавления льда λ в Дж/кг вписываем
в ячейку F6: 330000
5. Массу веществ m в кг вписываем соответственно для стали и льда
в ячейку D7: 3000
в ячейку E7: 20
Так как при превращении льда в воду масса не изменяется, то
в ячейках F7 и G7: =E7=20
Массу воздуха находим произведением объема помещения на удельный вес
в ячейке H7: =24*15*7*1,23=3100
6. Время процессов t в мин пишем только один раз для стали
в ячейку D8: 60
Значения времени для нагрева льда, его плавления и нагрева получившейся воды рассчитываются из условия, что все эти три процесса должны уложиться в сумме за такое же время, какое отведено на нагрев металла. Считываем соответственно
в ячейке E8: =E12/(($E$12+$F$12+$G$12)/D8)=9,7
в ячейке F8: =F12/(($E$12+$F$12+$G$12)/D8)=41,0
в ячейке G8: =G12/(($E$12+$F$12+$G$12)/D8)=9,4
Воздух также должен прогреться за это же самое отведенное время, читаем
в ячейке H8: =D8=60,0
7. Начальную температуру всех веществ T1 в ˚C заносим
в ячейку D9: -37
в ячейку E9: -37
в ячейку F9: 0
в ячейку G9: 0
в ячейку H9: -37
8. Конечную температуру всех веществ T2 в ˚C заносим
в ячейку D10: 18
в ячейку E10: 0
в ячейку F10: 0
в ячейку G10: 18
в ячейку H10: 18
Думаю, вопросов по п.7 и п.8 быть недолжно.
Результаты расчетов:
9. Количество теплоты Q в КДж, необходимое для каждого из процессов рассчитываем
для нагрева стали в ячейке D12: =D7*D5*(D10-D9)/1000=75900
для нагрева льда в ячейке E12: =E7*E5*(E10-E9)/1000= 1561
для плавления льда в ячейке F12: =F7*F6/1000= 6600
для нагрева воды в ячейке G12: =G7*G5*(G10-G9)/1000= 1508
для нагрева воздуха в ячейке H12: =H7*H5*(H10-H9)/1000= 171330
Общее количество необходимой для всех процессов тепловой энергии считываем
в объединенной ячейке D13E13F13G13H13: =СУММ(D12:H12) = 256900
В ячейках D14, E14, F14, G14, H14, и объединенной ячейке D15E15F15G15H15 количество теплоты приведено в дугой единице измерения – в ГКал (в гигакалориях).
10. Тепловая мощность N в КВт, необходимая для каждого из процессов рассчитывается
для нагрева стали в ячейке D16: =D12/(D8*60)=21,083
для нагрева льда в ячейке E16: =E12/(E8*60)= 2,686
для плавления льда в ячейке F16: =F12/(F8*60)= 2,686
для нагрева воды в ячейке G16: =G12/(G8*60)= 2,686
для нагрева воздуха в ячейке H16: =H12/(H8*60)= 47,592
Суммарная тепловая мощность необходимая для выполнения всех процессов за время t рассчитывается
в объединенной ячейке D17E17F17G17H17: =D13/(D8*60) = 71,361
В ячейках D18, E18, F18, G18, H18, и объединенной ячейке D19E19F19G19H19 тепловая мощность приведена в дугой единице измерения – в Гкал/час.
На этом расчет в Excel завершен.
Выводы:
Обратите внимание, что для нагрева воздуха необходимо более чем в два раза больше затратить энергии, чем для нагрева такой же массы стали.
При нагреве воды затраты энергии в два раза больше, чем при нагреве льда. Процесс плавления многократно больше потребляет энергии, чем процесс нагрева (при небольшой разности температур).
Нагрев воды в десять раз затрачивает больше тепловой энергии, чем нагрев стали и в четыре раза больше, чем нагрев воздуха.
Мы вспомнили понятия «количество теплоты» и «тепловая мощность», рассмотрели фундаментальные формулы теплопередачи, разобрали практический пример. Надеюсь, что мой язык был прост и понятен.
Ссылка на скачивание файла: raschet-teplovoy-moshchnosti (xls 19,5KB).
Другие статьи автора блога
На главную
Статьи с близкой тематикой
Отзывы
Расчет мощности тэна, необходимой для поддержания заданной температуры в том или ином помещении,
рассмотрен в п.1 «Справочных данных».
1. Для проверки соответствия данных маркировки реальным параметрам
ТЭН необходимо проверить его сопротивление Омметром в горячем виде. В этом случае можно пренебречь различными коэффициентами.
Р=U*U/R,
где P — мощность, которую необходимо найти, Вт;
U — рабочее напряжение, В;
R — измеренное сопротивление тэн в горячем виде, Ом.
Например:
Напряжение в сети 220 Вольт, измеренное сопротивление равно 22 Ом. Тогда мощность тэна имеет значение: Р=220*220/22=2200 Вт=2.2 кВт.
2. Для расчета времени за которое тэн нагреет воду, используем формулу теплодинамики.
При этом для простоты будем считать, что окружающая среда, переходные процессы, емкость и т.д. не влияют на нашу систему ТЭН — жидкость:
А=С(T1-T2)m,
где А -работа, которую необходимо проделать, чтобы изменить температуру жидкости массой «m» с Т1 до Т2.
С — удельная теплоемкость жидкости;
и формулу работы электрического тока:
А=Рt,
где А — работа электрического тока,
Р — мощность установки (в нашем случае — ТЭНов), Вт,
t — время работы электрического тока, сек.
Пример: За какое время тэн мощностью 2.0 кВт согреет воду массой 1.0 кг. с 20 до 80 градусов?
Справочное данное: С для воды = 4200 Дж/кг*градус.
С(Т1-Т2)m=Рt, отсюда t=C(T1-T2)m/P=4200*(80-20)*1.0/2000=126 секунд.
Ответ: вода массой 1.0 кг нагреется тэном мощностью 2 кВт с 20 до 80 градусов за 2 минуты и 6 секунд.
3.Подбор обогревательного устройства с оптимальной мощностью.
Мощность обогревателя определяет его способность поддерживать определенную температуру в помещении. Вторая величина, от которой это зависит, — объем помещения. При этом есть одно условие — теплоизоляция помещения должна быть приемлемой для данной климатической зоны.
Для стандартной высоты жилых помещений в России в 2.2-2.5 метра соотношение мощности к площади равна 1:10, т.е. нагреватель мощностью 1 кВт может обогреть помещение в 10 кв. метров.
Если высота помещения превышает указанное выше значение, тогда необходимо использовать поправочный коэффициент. Например, если высот помещения 3 метра, тогда: К = 3 метра/2.5 метра=1,2. Т.е. в этом случает соотношение мощности прибора и отапливаемой площади будет 1,2 кВт : 10 квадратных метров.
4. Зависимость объема теплоносителя (жидкости) системы отопления от мощности.
Приблизительный расчет объема теплоносителя системы отопления можно произвести используя следующее соотношение: для отопительной системы с котлом мощностью 1кВт требуется 15 литров теплоносителя. Соответственно объем отопительной системы с котлом мощностью 10 кВт приблизительно составит 150 литров.+
Данные, полученные при таком подсчете объема теплоносителя в системе отопления, не учитывают особенностей конкретной отопительной системы и являются всего лишь приблизительными
Нагреватель – калориметр
Cтраница 3
В измерительную схему прибора входят потенциометр постоянного тока, гальванометр, блоки холодных спаев БХС1, БХС2 и переключатели. Силовая часть состоит из блока питания, нагревателей калориметров, нагревателя адиабатной оболочки и тумблеров. Измерительная и силовая части схемы являются общими для обоих калориметров, так как прибор рассчитан на их поочередное использование. Подключение электрической схемы к соответствующему калориметру осуществляется переключателем.
[31]
Электрические соединения от внешней измерительной цепи к нагревателю калориметра и термистору проходят через выводы из трубки 4 в верхней части оболочки. Вводимую в калориметр мощность измеряют потенцио-метрической схемой.
[33]
Такое автоматическое включение и выключение нагревателя осуществляется в течение всего опыта; частота переключений зависит от скорости выделения теплоты. При этом счетчик 58 суммирует время, когда нагреватель калориметра не работает. Та же самая схема компенсации используется при десорбции, сопровождающейся поглощением тепла.
[34]
Собственно измерение производится после достижения стабильного режима парообразования в калориметре, о чем свидетельствует неизменность показаний калориметрического термометра. Мощность нагревателя калориметра расчитывается по измеренным напряжению на нагревателе калориметра и падению напряжения на эталонном сопротивлении I м, включенном последовательно в цепь на-128 гревателя.
[35]
Функция W ( т) в общем случае не является линейной и зависит от конкретных особенностей калориметра, так как в широком диапазоне рабочих температур сказывается температурная зависимость параметров Ся. В интересующем нас интервале температур от – 150 до 400 С близкий к линейному разогрев удается получать, питая нагреватель калориметра от источника с линейно возрастающим напряжением.
[36]
Время работы нагревателя регистрируется печатающим хронографом с погрешностью, не превышающей 0 01 сек. Вычитая показание хронографа, отвечающее моменту включения нагревателя, из показания, соответствующего моменту выключения нагревателя, получают время, в течение которого нагреватель калориметра был включен. Сдвоенный выключатель 33 обеспечивает одновременное включение питания нагревателя и хронографа.
[37]
Перед опытом необходимо включить вентилятор-эксгаустер и автоматический потенциометр. Запись температур на ленте потенциометра будет свидетельствовать, что температура входящего в калориметр воздуха равна температуре выходящего воздуха. Затем следует включить нагреватель калориметра и наблюдать на ленте потенциометра возрастание температуры воздуха на выходе из калориметра.
[38]
В процессе работы вакуумная линия загрязняется парами адсорбированных веществ и вакуум снижается. Сопротивление термистора на калориметре меньше, чем термистора сравнения, разница компенсируется магазином сопротивлений. Чувствительность измерительной схемы составляет 5 Ю-4 К. Теплота парообразования компенсируется электрическим током, пропускаемым через нагреватель калориметра. Для питания нагревателя используют батарею аккумуляторов, которая находится под постоянной нагрузкой. В течение 90 мин до начала измерений пропускают ток через балластное сопротивление, равное сопротивлению нагревателя калориметра.
[39]
В процессе работы вакуумная линия загрязняется парами адсорбированных веществ и вакуум снижается. Изменение температуры калориметра относительно окружающей медной оболочки измеряют двумя термисторами, связанными мостовой схемой с двумя сопротивлениями по 4000 Ом. Сопротивление термистора на калориметре меньше, чем термистора сравнения, разница компенсируется магазином сопротивлений. Чувствительность измерительной схемы составляет 5 10 4 К. Теплота парообразования компенсируется электрическим током, пропускаемым через нагреватель калориметра. Для питания нагревателя используют батарею аккумуляторов, которая находится под постоянной нагрузкой. В течение 90 мин до начала измерений пропускают ток через балластное сопротивление, равное сопротивлению нагревателя калориметра.
[41]
Электрические соединения от внешней измерительной цепи к нагревателю калориметра и термистору проходят через выводы из трубки 4 в верхней части оболочки. Вводимую в калориметр мощность измеряют потенцио-метрической схемой. К нуль-детектору присоединено записывающее устройство, управляющее фотоячейкой передающей цепи. Последняя включает и выключает счетчик времени и нагреватель калориметра в зависимости от температуры, показываемой тер-мистором.
[42]
В процессе работы вакуумная линия загрязняется парами адсорбированных веществ и вакуум снижается. Сопротивление термистора на калориметре меньше, чем термистора сравнения, разница компенсируется магазином сопротивлений. Чувствительность измерительной схемы составляет 5 Ю-4 К. Теплота парообразования компенсируется электрическим током, пропускаемым через нагреватель калориметра. Для питания нагревателя используют батарею аккумуляторов, которая находится под постоянной нагрузкой. В течение 90 мин до начала измерений пропускают ток через балластное сопротивление, равное сопротивлению нагревателя калориметра.
[43]
Две серии концентрических тонких ( 0 2 мм) медных пластинок способствуют установлению теплового равновесия в образце. Платиновый термометр сопротивления расположен в центральной стенке. Калориметр внутри заполнен небольшим количеством гелия, способствующим увеличению теплопередачи между образцом, нагревателем, термометром и калориметрической ячейкой. Калориметр окружен полированной медной ширмой толщиной 0 4 мм, на которой размещены нагреватели, поддерживающие постоянную разность температур между ширмой и калориметром. Охлаждение достигается погружением камеры в жидкий водород, азот, твердую углекислоту, лед или воду в зависимости от необходимой температурной области. Температура платинового термометра измеряется мостом Мюллера. Электрическая мощность, подаваемая в нагреватель калориметра, определяется на Основании измерений силы тока и напряжения. Интересный вариант такого калориметра разработан Пассалио и Кеворкианом ( 1963), которые уменьшили тепловое значение калориметра с 85 до 5 % от общей теплоемкости. Это достигнуто за счет использования в качестве калориметра самого полимера.
[44]
В процессе работы вакуумная линия загрязняется парами адсорбированных веществ и вакуум снижается. Изменение температуры калориметра относительно окружающей медной оболочки измеряют двумя термисторами, связанными мостовой схемой с двумя сопротивлениями по 4000 Ом. Сопротивление термистора на калориметре меньше, чем термистора сравнения, разница компенсируется магазином сопротивлений. Чувствительность измерительной схемы составляет 5 10 4 К. Теплота парообразования компенсируется электрическим током, пропускаемым через нагреватель калориметра. Для питания нагревателя используют батарею аккумуляторов, которая находится под постоянной нагрузкой. В течение 90 мин до начала измерений пропускают ток через балластное сопротивление, равное сопротивлению нагревателя калориметра.
[45]
Страницы:
1
2
3
4
Плавление и отвердевание
ОпределениеПлавление — переход вещества из твердого состояния в жидкое.
Для расчета количества теплоты, необходимого для процесса плавления, следует применять формулу:
Q=λm
m — масса вещества, λ (Дж/кг) — удельная теплота плавления.
Плавление каждого вещества происходит при определенной температуре, которую называют температурой плавления. Все проводимое тепло идет на разрушение кристаллической решетки, при этом увеличивается потенциальная энергия молекул. Кинетическая энергия остается без изменения и температура в процессе плавления не изменяется.
Удельная теплота плавления показывает, какое количество теплоты необходимо сообщить 1 кг данного вещества, чтобы перевести его из твердого состояния в жидкое при условии, что оно уже нагрето до температуры плавления. В процессе отвердевания 1 кг данной жидкости, охлажденной до температуры отвердевания, выделится такое же количество теплоты.
Внимание! Удельная теплота плавления — табличная величина.
Определение
Отвердевание, или кристаллизация — переход состояния из жидкого состояния в твердое (это процесс, обратный плавлению).
Отвердевание происходит при той же температуре, что и плавление. В процессе отвердевания температура также не изменяется. Количество теплоты, выделяемое в процессе отвердевания:
Q=−λm
Продолжаем подготовку к олимпиадам. Сегодня рассматриваем тему “мощность теплопередачи”. Задачи интересные, и в школе эту тему не дают, заимствованы на «Фоксфорде» – спасибо составителям за удовольствие от решения.
Мощность теплопередачи – количество теплоты, отданное системой за время .
Эта мощность зависит от разности температур (если горячее тело вынести на мороз, остывает быстрее, чем если такое же тело вынести на жару), от площади поверхности тела (чем она больше, тем быстрее остынет), от расстояния, на которое тепло передают:
Задача 1. Ведро воды удалось нагреть кипятильником мощностью 800 Вт лишь до С. За какое время ведро остынет до С после выключения кипятильника? Масса воды 10 кг.
Задача на прямое применение данной выше формулы. Ведро остывает на 1 градус, следовательно,
Ответ: 52,5 с.
Задача 2. Петя заметил, что на морозе вода в стакане остывает от С до С за 3 мин, а от С до С за 6 мин. Чему равна температура окружающей среды ? Считайте, что мощность теплопередачи пропорциональна разности температур стакана и окружающей среды.
Вода и в первом, и во втором случае отдает одно и то же количество теплоты, так как остывает в обоих случаях на три градуса. Тогда
Но, с другой стороны,
и -средняя температура воды в первом и во втором случаях. Коэффициент учитывает все остальные параметры: длины, площади и пр.
Поделим уравнения друг на друга
Или
Ответ:
Задача 3. На плите стоит кастрюля с водой. При нагревании температура воды увеличилась от C до C за одну минуту. Какая доля теплоты, получаемой водой при нагревании, рассеивается в окружающем пространстве, если время остывания той же воды от C до C равно 9,0 минутам?
Кастрюлю подогревают – но это не значит, что она не остывает! Вот такой парадокс. Тепло кастрюля все равно отдает, всегда, когда она теплее, чем окружающие предметы. Просто, если кастрюля нагревается, то это означает, что тепло, которое она получает от плитки, больше, чем то, которое она рассеивает.
Поэтому при нагреве
А при пассивном остывании
Тогда
Искомая величина:
Задача 4. В палатке, покрытой сверху шерстяными одеялами, пол застелен толстым теплонепроницаемым войлоком. Одинокий спящий индеец начинает мерзнуть в такой палатке при уличной температуре воздуха С. Два спящих индейца начинают мерзнуть в такой палатке при уличной температуре воздуха С. При какой температуре воздуха индейцы начинают пользоваться палатками? При какой температуре в той же палате будет холодно трем индейцам? Какому количеству индейцев никогда не будет холодно в палатке? Считайте, что тепловая мощность, передаваемая через тент палатки, пропорциональна разности температур внутри и снаружи.
Индеец теплый, теплее окружающей среды. Он отдает тепло наружному холодному воздуху. Если температура воздуха , мощность теплоотдачи индейца . Потому что если на улице другая температура, то и мощность уже другая, индеец остывает или быстрее, или медленнее. Пусть температура вокруг индейца, при которой индеец начинает замерзать, . Это может быть и температура наружного воздуха, и температура в палатке. Тогда двое индейцев имеют мощность теплоотдачи , трое – и так далее. Пусть коэффициент учитывает площадь поверхности индейца, рост, материал, из которого индеец состоит… Тогда
Разделим второе на первое:
Разделим третье на первое:
Разделим четвертое на первое:
Тогда, если температура на улице , то
Таким образом, 48-49 индейцев не должны замерзнуть даже при абсолютном нуле.
Задача 5. Система охлаждения нагревателя состоит из нескольких одинаковых теплопроводящих стержней, соединенных небольшими шариками. Температура нагревателя С, температура холодильника С. Чему равна разность температур шарика K и шарика B () в установившемся режиме? Приток тепла в системе осуществляется только от нагревателя, а отвод только через холодильник. Мощность теплопередачи через стержень пропорциональна разности температур на его концах.
Рисунок 1
Расставим направления потоков тепла. В центре все понятно: все стрелки направлены от горячего к холодному «очагу» – холодильнику. А что по верхним правому и левому углам?
Рисунок 2
Точка ближе к холодильнику, чем , поэтому направление потока логично будет выбрать от к .
Рисунок 3
Точка дальше от нагревателя, чем , поэтому ставим стрелку от к .
Рисунок 4
Теперь определим величины этих потоков. Если от к направлен поток , то от к – тоже . Но тогда от к холодильнику – , так как в силу симметрии в левой части расстановка потоков такая же.
Рисунок 5
Если теперь пройти от точки к холодильнику по красной стрелке, наберется , следовательно, поток от точки к холодильнику тоже . Тогда от нагревателя к точке будет течь поток , и в левой части аналогично.
Рисунок 6
Следовательно, если пройти от нагревателя к холодильнику через точку по стрелке, поток будет равен . Тогда и “напрямки” тоже .
Но температура холодильника и нагревателя отличается на , поэтому
Тогда расставляем температуры узлов: в точке и симметричной ей слева , в точке , в точке .
Определяем искомое:
Ответ: .
Парообразование и конденсация
ОпределениеПарообразование, или кипение — переход вещества из жидкого состояния в газообразное.
Количество теплоты, необходимое для процесса кипения, вычисляют по формуле:
Q=rm
m — масса вещества, r (Дж/кг) — удельная теплота парообразования.
Парообразование происходит при определенной температуре, которую называют температурой кипения. В отличие от испарения, процесс парообразования идет со всего объема жидкости. Несмотря на то, что к кипящему веществу подводят тепло, температура не изменяется. Все затраты энергии идут на увеличение промежутком между молекулами. Температура кипения зависит от рода вещества и внешнего атмосферного давления.
Удельная теплота парообразования показывает, какое количество теплоты необходимо затратить, чтобы перевести в пар 1 кг жидкости, нагретой до температуры кипения. Такое же количество теплоты выделится в процессе конденсации 1 кг пара, охлажденного до температуры конденсации.
Внимание! Удельная теплота парообразования — табличная величина.
Определение
Конденсация — процесс, обратный кипению. Это переход вещества из газообразного состояния в жидкое.
Конденсация происходит при температуре кипения, которая также не изменяется во время всего процесса. Количество теплоты, выделяемое в процессе конденсации:
Q=−rm
06-в. Количество теплоты и калориметр
- Главная
- Справочник
- Физика
- Введение в термодинамику
- Книги, лекции и конспекты по физике
- Физика 7 класс
- 06-в. Количество теплоты и калориметр
§ 06-в. Количество теплоты и калориметр
В этом параграфе мы изучим несколько новых терминов. Определим их. Теплообмен
– это явление перехода внутренней энергии одного тела во внутреннюю энергию другого тела без совершения механической работы.
Количество теплоты
– это энергия, перешедшая от одного тела к другому при теплообмене.
На рисунке показан калориметр
– прибор для измерения количества теплоты.
Простейший калориметр состоит из двух стаканов: внутреннего алюминиевого и внешнего пластмассового, которые разделены воздушным промежутком.
Рассмотрим пример. Во внутренний стакан нальём 100 г воды. Измерим её температуру: 20 °С. Погрузим в воду горячее тело – металлический цилиндрик. Внутри калориметра начнётся теплообмен, и некоторое количество теплоты перейдёт от цилиндрика к воде
, в результате чего её температура повысится (см. рисунок). Вычислим изменение температуры воды:
Δt°
воды = 60 °С – 20 °С = 40 °С .
Зная, что масса воды 100 г, инженер-теплотехник скажет: вода получила 100 г · 40 °С = 4000 калорий теплоты. В отличие от теплотехники, в физике количество теплоты выражают в джоулях
(как и любую другую энергию). Для этого применяют специальную формулу:
Формула для подсчета количества теплоты, поглощаемого телом при нагревании или выделяющегося при его охлаждении. Формула читается так: «Ку равно цэ эм дэльта тэ».
| Q = c·m·Δt° | Q
– количество теплоты, Дж |
Удельная теплоёмкость вещества
– физическая величина, показывающая количество теплоты, необходимое для изменения температуры 1 кг этого вещества на 1 °С.
Используя таблицу (см. далее), легко подсчитать, что вода внутри калориметра получила от цилиндрика 16,8 кДж теплоты:
Q
воды = 4200 Дж/(кг°С) · 0,1 кг · 40 °С = 16800 Дж .
Формулу Q = cmΔt°
применяют не только в том случае, когда вещество нагревается. Её также используют для подсчёта количества теплоты, которое
отдают охлаждающиеся тела
. Например, вода внутри отопительных батарей в квартире или классе.
Удельные теплоёмкости всех веществ измерены и занесены в специальные таблицы. Например, для воды в жидком состоянии с = 4200 Дж/(кг°С). Это значение показывает, что для нагревания 1 кг воды на 1 °С потребуется 4200 Дж теплоты. Можно сказать и иначе: каждый килограмм воды, остывая на 1 °С, отдаёт окружающим телам 4200 Дж тепловой энергии.
Удельная теплоемкость показывает количество теплоты, которое необходимо для нагревания 1 кг вещества на 1 градус. Или, что то же самое, – количество теплоты, которое выделится при охлаждении 1 кг этого вещества на 1 градус.
| Удельные теплоёмкости некоторых веществ, Дж/(кг°С) | ||||
| Алюминий | 920 | Вода | 4200 | |
| Железо | 460 | Лёд | 2100 | |
| Латунь | 400 | Масло подсолн. | 1700 |
Поясним, почему в определении теплообмена присутствуют слова «без совершения механической работы». Вспомним, что в § 5-е мы рассмотрели опыт с манометром и горячей гирей. Тогда внутренняя энергия гири уменьшалась. Часть этой энергии превращалась в механическую работу – удлинялся «столбик» жидкости в манометре. В опыте с калориметром внутренняя энергия цилиндрика также уменьшалась. Однако теперь она превращалась во внутреннюю энергию воды без совершения работы (см. рисунок; для наглядности цилиндрик изображён вне калориметра).
Калориметрические измерения показывают, что теплообмен всегда протекает так, что убыль внутренней энергии одних тел сопровождается таким же приращением внутренней энергии других тел, участвующих в теплообмене.
Это – одно из проявлений закона сохранения и превращения энергии.
Введение в термодинамикуФормулы Физика Теория 7 класс
Источник
Источник информации
Тепловые процессы при нагревании и охлаждении
Все фазовые переходы, а также процессы нагревания и остывания вещества можно отобразить графически. Посмотрите на график фазовых переходов вещества:
Он показывает зависимость температуры вещества от времени в процессе его нагревания и остывания. Опишем процессы, отображаемые на графике, в таблице.
| Процесс | Что происходит | Количество выделенной теплоты |
| 1–2 | Нагревание твердого тела | Q=cтm(tпл−t0)
ст — удельная теплоемкость вещества в твердом состоянии. |
| 2–3 | Плавление при температуре плавления (tпл) | Q=λm |
| 3–4 | Нагревание жидкости | Q=cжm(tкип−tпл)
сж — удельная теплоемкость вещества в жидком состоянии. |
| 4–5 | Кипение при температуре кипения (tкип) | Q=rm |
| 5–6 | Нагревание пара | Q=cпm(t−tкип)
сп — удельная теплоемкость вещества в газообразном состоянии. |
| 6–7 | Охлаждение пара | Q=cпm(tкип−t) |
| 7–8 | Кипение при температуре кипения (tкип) | Q=−rm |
| 8–9 | Охлаждение жидкости | Q=cжm(tпд−tкип) |
| 9–10 | Отвердевание при температуре плавления (tпл) | Q=−λm |
| 10–11 | Охлаждение твердого тела | Q=cтm(t0−tпл) |
Внимание! На участках 2–3 и 9–10 вещество частично находится в жидком и твердом состояниях, а на 4–5 и 7–8 — в жидком и газообразном.
Частные случаи тепловых процессов
| Что происходит | График | Формула количества теплоты |
| Полностью растопили лед, имеющий отрицательную температуру. | Q=cлm(tпл−tл)+λm
cл — удельная теплоемкость льда, tл — начальная температура льда. |
|
| Лед, взятый при отрицательной температуре, превратили в воду при комнатной температуре. | Q=cлm(tпл−tл)+λm+cвm(tв−tпл)
cв — удельная теплоемкость воды. |
|
| Взяли лед при температуре 0 оС и полностью испарили. | Q=λm+cвm(tкип−tпл)+rm | |
| Взяли воду при комнатной температуре и половину превратили в пар. | Q=cвm(tкип−tв)+rm2.. |
Подсказки к задачам
| Единицы измерения | Температуру можно оставлять в градусах Цельсия, так как изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах. |
| Кипяток | Вода, которая при нормальном атмосферном давлении имеет температуру в 100 оС. |
| Объем воды 5 л | m = 5 кг, так как: m=ρV=103· 5·10−3м3=5 кг Внимание! Равенство V (л) = m (кг) справедливо только для воды. |
Пример №1. Какое количество теплоты нужно сообщить льду массой 2 кг, находящемуся при температуре –10 оС, чтобы превратить его в воду и нагреть ее до температуры +30 оС?
Можно выделить три тепловых процесса:
- Нагревание льда до температуры плавления.
- Плавление льда.
- Нагревание воды до указанной температуры.
Поэтому количество теплоты будет равно сумме количеств теплоты для каждого из этих процессов:
Q=Q1+Q2+Q3
Q=cлm(0−t1)+λm+cвm(t2−0)
Удельные теплоемкости и удельную теплоту плавления смотрим в таблицах:
- Удельная теплоемкость льда = 2050 Дж/(кг∙К).
- Удельная теплоемкость воды = 4200 Дж/(кг∙К).
- Удельная теплота плавления льда = 333,5∙103 Дж/кг.
Отсюда:
Q=2050·2(0−(−10))+333,5·103·2+4220·2·30=961200 (дж)=961,2 (кДж)
Взаимные превращения механической и внутренней энергии
Если в тексте задачи указан процент одного вида энергии, перешедший в другой, то он указывается в виде десятичной дроби перед этой энергией, которой тело обладало вначале.
Частные случаи закона сохранения энергии
| При неупругом ударе о стенку пуля нагрелась | mv22..=cmΔt |
| Тело падает с некоторой высоты и в момент падения нагревается | mgh=cmΔt |
| В результате того, что пуля пробивает стену, ее скорость уменьшается, 50% выделившейся при этом энергии идет на нагревание пули | 0,5(mv202..−mv22..)=cmΔt |
| Летящая пуля при ударе о стенку расплавилась. Начальная температура пули меньше температуры плавления | mv22..=cmΔt+λm |
| Капля воды, падая с некоторой высоты, в момент удара испарилась. Температура капли у поверхности земли меньше температуры кипения. На нагрев пошло 60% выделившейся механической энергии | 0,6mgh=cmΔt+rm |
| Вследствие сгорания топлива ракета поднялась на некоторую высоту | qmтоп=mрgh |
| Вследствие сгорания топлива снаряд приобрел некоторую скорость, и на это было затрачено 25% энергии | 0,25qmтопmсv22.. |
Пример №3. Свинцовая дробинка, летящая со скоростью 100 м/с, попадает в доску и входит в нее. 52% кинетической энергии дробинки идет на ее нагревание. На сколько градусов нагрелась дробинка? Удельная теплоемкость свинца 130 Дж/(кг∙К).
Запишем закон сохранения энергии для этого случая:
0,52mv22..=cmΔt
Δt=0,52v22c..=0,52·10022·130..=20 (К)
Полностью заполненный водой калориметр с электронагревателем имеет комнатную температуру t0. Нагреватель включают, и через время T = 30 с температура калориметра увеличивается на величину Δt. Затем воду из калориметра быстро выливают, вместо нее наливают такое же количество воды комнатной температуры и снова включают нагреватель. Чтобы теперь нагреть калориметр до температуры требуется время
После этого воду из калориметра снова быстро выливают, а наливают такое же количество воды с температурой на величину Δt ниже комнатной. Сколько понадобится времени, чтобы нагреть калориметр тем же нагревателем до комнатной температуры? Считать, что калориметр не отдает тепло в окружающее пространство. Температуры воды и калориметра уравниваются очень быстро.
Спрятать решение
Решение.
Пусть теплоемкость воды в калориметре — C, теплоемкость калориметра — C0, мощность нагревателя — P. Тогда уравнение теплового баланса для первого нагревания (начальные температуры воды и калориметра равны t1) имеем
где T — время нагревания, Δt — увеличение температуры калориметра при нагревании. После того как воду вылили, заполнили калориметр водой комнатной температуры, в калориметре установилась температура, большая, чем комнатная. При этом, поскольку потерь энергии нет, то количество необходимой для нагревания теплоты можно вычислить как количество теплоты, необходимое для нагревания воды (но не калориметра) от комнатной температуры на величину Δt. Поэтому уравнение теплового баланса для второго нагревания дает
Вычитая (**) и (*), получим
Количество теплоты, необходимое для третьего нагревания можно посчитать так. В третьем процессе вода должна нагреться на величину Δt (от температуры на Δt ниже комнатной до комнатной), а калориметр остыть на величину Δt (от температуры на Δt выше комнатной до комнатной). Поэтому уравнение теплового баланса дает
где T1 — искомое время. Используя формулы (**) и (***), получим
Ответ: 20 сек.
Спрятать критерии
Критерии проверки:
| Критерии по заданию | Баллы |
|---|---|
| Правильная идея решения — использование уравнения
теплового баланса с калориметром и без калориметра |
0,5 |
| Найдено соотношение теплоемкости калориметра и
воды в калориметре |
0,5 |
| Правильное уравнение теплового баланса для третьего случая | 0,5 |
| Правильный ответ | 0,5 |
Классификатор: МКТ и термодинамика. Тепловая мощность