как определить число неспаренных электронов в атоме
Ученик
(122),
закрыт
6 лет назад
rafael ahmetov
Высший разум
(122431)
9 лет назад
Используя правило Клечковского написать электронную формулу. По электронной формуле это определяется легко. Например, электронная формула углерода 1s2 2s2 2p2, видим что на s-орбиталях по 2 электрона, т. е. они спарены. На p- орбиталях 2 электрона, но 2-р орбиталей три. Значит по правилу Гунда, 2 электрона займут 2 разных р-орбитали, и у углерода – 2 неспаренных электрона. Аналогично рассуждая видим, что у атома азота 1s2 2s2 2p3 – 3 неспаренных электрона. У кислорода 1s2 2s2 2p4 – на р-орбиталях 4 электрона. 3 электрона расположились по одному на разных р-орбиталях, а четвертому отдельного места нет. Поэтому он идет в пару к одному из трех, а два остаются неспаренными. Аналогично у фтора 1s2 2s2 2p5 – один неспаренный электрон, а у неона 1s2 2s2 2p6 нет неспаренных электронов.
Совершенно аналогично нужно рассматривать и d- и f- орбитали (если они задействованы в электронной формуле, и не забывать, что d-орбиталей пять, а f-орбиталей семь.
Вадим Беленецкий
Просветленный
(36367)
9 лет назад
неадо расписать любой элемент и тогда будет видно,естьнеспаренные электроны или нет Напимер у алюминия заряд +13. а распределение по уровнням -2.8.3.Уже видно ,что р-электрон на последнем слое неспаренный.И таким же способом проверь у всех элементов.
Приветствую вас, уважаемые читатели, на своем канале!
В данной статье разберем основное и возбужденное состояния атомов и электронные формулы ионов.
Предыдущие статьи по вопросу 1 можно посмотреть здесь:
Основное и возбужденное состояния атомов
Валентность – это способность атома химического элемента образовывать с другими атомами химические связи за счет отдачи или принятия электронов. Валентность определяется числом неспаренных электронов в обычном и возбужденном состоянии атома.
Когда мы строим электронные конфигурации атомов по ПС, то это основное состояние (т.е. состояние с минимальной энергией).
Иногда, некоторые атомы, когда получают энергию извне, могут переходить в возбужденное состояние.
Возбужденное состояние атома – это состояние, при котором электрон из электронной пары с предыдущего подуровня с меньшей энергией “расспаривается” и переходит на следующий подуровень с большей энергией.
Например, рассмотрим электронные оболочки атомов углерода и серы в основном и возбужденном состояниях.
Возбужденное состояние характерно для таких атомов, которые имеют свободную орбиталь. Например, мы знаем, что третий уровень характеризуются тремя подуровнями, независимо от их заполнения (например, как у серы).
Атомы азота (N), кислорода (O), фтора (F) и неона не могут переходить в возбужденное состояние, так как нет свободных орбиталей и второй уровень характеризуется только двумя подуровнями.
Атом азота (N):
– количество неспаренных электронов 3;
-валентность: 3.
Атом кислорода (O):
– количество неспаренных электронов: 2;
-валентность: 2.
Атом фтора (F):
– количество неспаренных электронов: 1;
-валентность 1.
Атом неона (Ne):
– количество неспаренных электронов: 0;
– валентность: 0.
Электронные формулы ионов
Если атом отдает или принимает электрон, он превращается в ион.
Например, переход железа в состояние Fe(3+) связано с отдачей трех электронов:
Fe(0) → Fe(3+) (атом отдал 3е) =>
26Fe …3d(6)4s(2) Fe(3+) …3d(5) (катион).
В первую очередь атом отдает электроны с более высокого энергетического уровня и подуровня.
S(0) → S(2-) (атом принял 2е) =>
16S …3s(2)3p(4) S(2-) …3s(2)3p(6) (анион).
Электронная конфигурация иона S(2-) аналогична электронной конфигурации атома аргона.
Связь электронного строения атома с положением элемента в ПС
1. Число энергетических уровней в атоме, на которых расположены электроны, равно номеру периода.
2. У элементов главных подгрупп число электронов на внешнем энергетическом уровне равно номеру группы ПС. У элементов главных подгрупп электроны внешнего энергетического уровня являются валентными.
3. У элементов побочных подгруппы III – VIII групп общее число электронов на s-подуровне внешнего энергетического уровня атома и d-подуровне предпоследнего уровня равно номеру группы.
Например:
25Mn 1s(2)2s(2)2p(6)3s(2)3p(6)3d(5)4s(2)
26Fe 1s(2)2s(2)2p(6)3s(2)3p(6)3d(6)4s(2)
У элементов побочных подгрупп валентными могут быть электроны внешнего энергетического уровня и d-подуровня предпоследнего уровня.
4. У элементов побочных подгрупп I и II групп d-подуровень предпоследнего энергетического уровня завершен (d(10)), а на внешнем энергетическом уровне число электронов равно номеру группы.
Например:
29Cu 1s(2)2s(2)2p(6)3s(2)3p(6)3d(10)4s(1)
30Zn 1s(2)2s(2)2p(6)3s(2)3p(6)3d(10)4s(2)
Если есть вопросы по данной статье, то пишите в комментариях!
Разборы заданий второй части реальных вариантов ЕГЭ 2021 смотрим ниже.
Решение заданий 30 и 31 разных вариантов можно посмотреть здесь:
Решение заданий 32 разных вариантов можно посмотреть здесь:
Решение заданий 33 разных вариантов можно посмотреть здесь:
Решение заданий 34 разных вариантов можно посмотреть здесь:
Решение заданий 35 разных вариантов можно посмотреть здесь:
Не забываем поставить лайк этой статье и подписаться на канал!
Всем успехов в изучении химии!
Как определить неспаренные и спаренные электроны?
Ева Р.
25 октября 2018 · 89,9 K
Если на орбитали находится один электрон, то он называется неспаренным, а если два – то это спаренные электроны. Легче всего определить, какие они, при помощи графической формулы. Эта схема размещения электронов в квантовых ячейках, которые являются графическим изображением атомной орбитали. Дляего составления следует знать:
1. Порядковый номер элемента, т.е. заряд его ядра и соответствующее ему число электронов в атоме.
2. Номер периода, определяющий число энергетических уровней атома.
3. Квантовые числа и связь между ними.
65,9 K
Комментировать ответ…Комментировать…
Имею естественно научное образование, в юношестве прикипел к литературе, сейчас активно… · 25 янв 2019
Число электронов определяется исходя из номера элемента, далее исходя из количества нужно рисовать уровни, на каждом уровне может быть 2 электрона, они будут спаренными, если на последнем уровне останется 1 электрон, то он и будет неспаренным.
40,6 K
Комментировать ответ…Комментировать…
Атомно-молекулярное учение
Мы приступаем к изучению химии – мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными
формулами элементов.
Атом (греч. а – отриц. частица + tomos – отдел, греч. atomos – неделимый) – электронейтральная частица вещества микроскопических
размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется “планетарной” и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos – первый) – положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов
элементов. Нейтрон (лат. neuter – ни тот, ни другой) – нейтральная (0) элементарная частица, присутствующая в ядрах всех
химических элементов, кроме водорода.
Электрон (греч. elektron – янтарь) – стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома –
порядковый номер в таблице Менделеева – равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20)
в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило:
порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим
электроны занимают различные энергетические уровни.
Энергетические уровни подразделяются на несколько подуровней:
- Первый уровень
- Второй уровень
- Третий уровень
- Четвертый уровень
Состоит из s-подуровня: одной “1s” ячейки, в которой помещаются 2 электрона (заполненный электронами – 1s2)
Состоит из s-подуровня: одной “s” ячейки (2s2) и p-подуровня: трех “p” ячеек (2p6), на которых
помещается 6 электронов
Состоит из s-подуровня: одной “s” ячейки (3s2), p-подуровня: трех “p” ячеек (3p6) и d-подуровня:
пяти “d” ячеек (3d10), в которых помещается 10 электронов
Состоит из s-подуровня: одной “s” ячейки (4s2), p-подуровня: трех “p” ячеек (4p6), d-подуровня:
пяти “d” ячеек (4d10) и f-подуровня: семи “f” ячеек (4f14), на которых помещается 14
электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число
электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а
также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: “s”, “p” и “d”, которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или
атомным орбиталям, движутся электроны, создавая определенный “рисунок”.
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь – клеверный лист.

Правила заполнения электронных орбиталей и примеры
Существует ряд правил, которые применяют при составлении электронных конфигураций атомов:
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной “ячейке”) не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются
еще одним электроном с противоположным направлением - Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было
бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и
серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода – 6, у серы – 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.

Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил.
А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся
одним электроном дополнили первую ячейку.
Таким образом, электронные конфигурации наших элементов:
- Углерод – 1s22s22p2
- Серы – 1s22s22p63s23p4
Внешний уровень и валентные электроны
Количество электронов на внешнем (валентном) уровне – это число электронов на наивысшем энергетическом уровне, которого достигает элемент. Такие электроны называются валентными: они могут быть спаренными или неспаренными. Иногда
для наглядного представления конфигурацию внешнего уровня записывают отдельно:
- Углерод – 2s22p2 (4 валентных электрона)
- Сера -3s23p4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью – способностью атомов образовывать определенное число химических связей.

- Углерод – 2s22p2 (2 неспаренных валентных электрона)
- Сера -3s23p4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных
электронов. Ниже будет дано наглядное объяснение этой задаче.

Запишем получившиеся электронные конфигурации магния и скандия:
- Магний – 1s22s22p63s2
- Скандий – 1s22s22p63s23p64s23d1
В целом несложная и интересная тема электронных конфигураций отягощена небольшим исключением – провалом электрона, которое только подтверждает общее
правило: любая система стремится занять наименее энергозатратное состояние.
Провал электрона
Провалом электрона называют переход электрона с внешнего, более высокого энергетического уровня, на предвнешний, энергетически более
низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций.
Подобное явление характерно лишь для некоторых элементов: медь, хром, серебро, золото, молибден. Для примера выберем хром, и рассмотрим
две электронных конфигурации: первую “неправильную” (сделаем вид, будто мы не знаем про провал электрона) и вторую правильную, написанную
с учетом провала электрона.
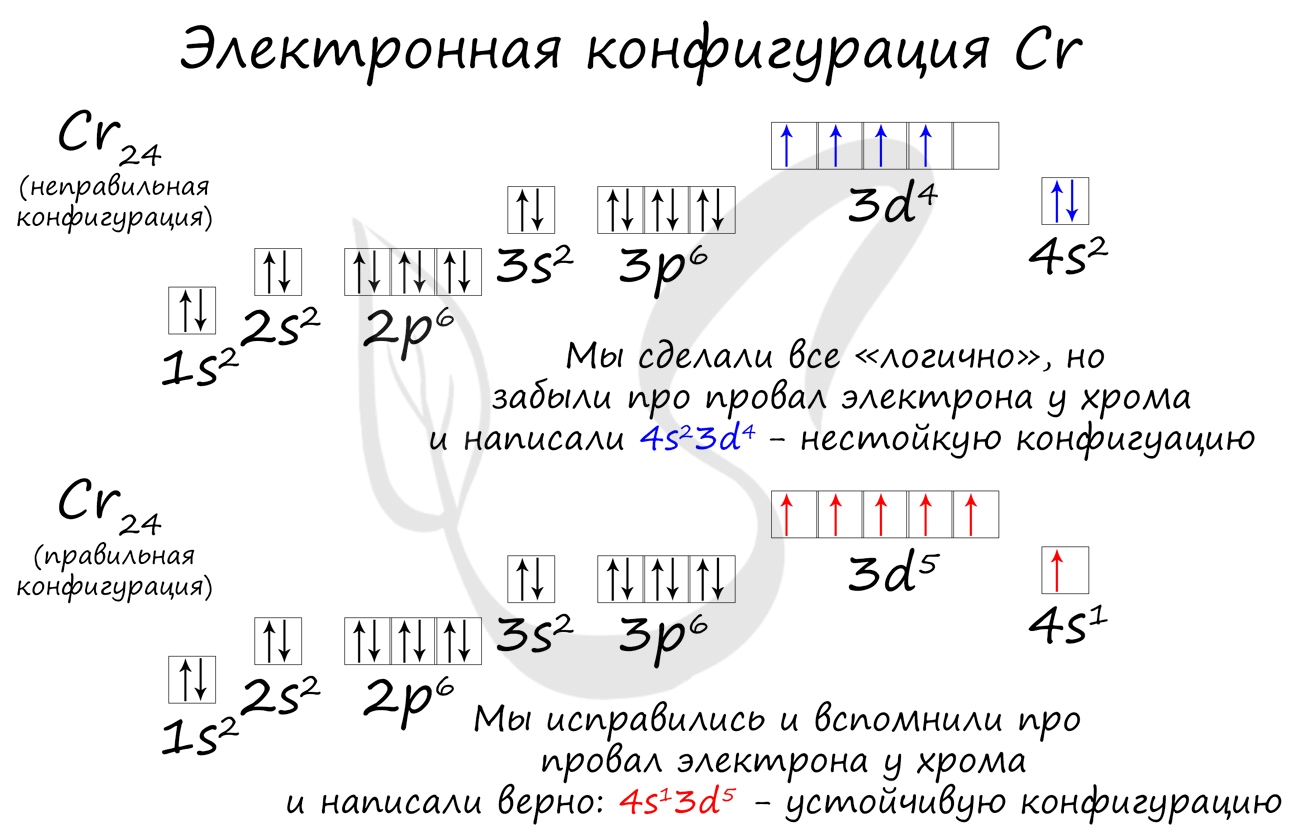
Теперь вы понимаете, что кроется под явлением провала электрона. Запишите электронные конфигурации хрома и меди самостоятельно еще раз и
сверьте с представленными ниже.

Основное и возбужденное состояние атома
Основное и возбужденное состояние атома отражаются на электронных конфигурациях. Возбужденное состояние связано с движением электронов
относительно атомных ядер. Говоря проще: при возбуждении пары электронов распариваются и занимают новые ячейки.
Возбужденное состояние является для атома нестабильным, поэтому долгое время в нем он пребывать не может. У некоторых атомов: азота,
кислорода , фтора – возбужденное состояние невозможно, так как отсутствуют свободные орбитали (“ячейки”) – электронам некуда перескакивать, к тому
же d-орбиталь у них отсутствует (они во втором периоде).
У серы возможно возбужденное состояние, так как она имеет свободную d-орбиталь, куда могут перескочить электроны. Четвертый энергетический
уровень отсутствует, поэтому, минуя 4s-подуровень, заполняем распаренными электронами 3d-подуровень.
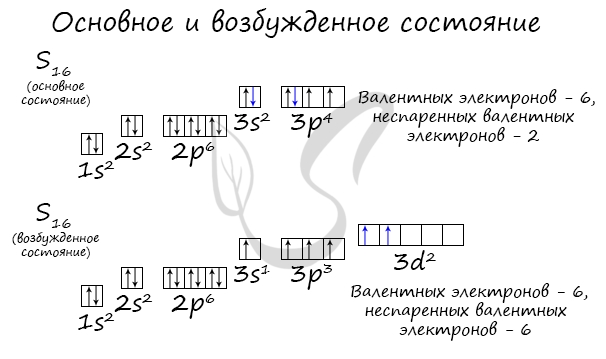
По мере изучения основ общей химии мы еще не раз вернемся к этой теме, однако хорошо, если вы уже сейчас запомните, что возбужденное состояние
связано с распаривание электронных пар.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Определите, какие элементы имеют в основном состоянии одинаковое количество неспаренных электронов. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Спрятать решение
Решение.
Выпишем валентные электроны в атоме каждого из элементов:
1. — 3d54s1.
2. — 3s23p2.
3. — 3d14s2.
4. — 2s22p4.
5. — 2s22p3.
Чтобы определить, сколько неспаренных электронов в основном состоянии имеет элемент, нужно знать как заполняются электронные слои. Если одну орбиталь занимает один электрон, то он называется неспаренным, а если на одной орбитали два электрона, то их называют спаренными.
Рассмотрим элементы, находящиеся в главных подруппах — кремний, кислород, азот. На p-подуровне — 3 орбитали, на одной орбитали располагается два электрона, всего 6 электронов на подуровне: электроны вначале заполняют каждую из орбиталей по одному. Соответственно, у азота — 3 неспаренных электрона, у кремния и кислорода — 2 неспаренных электрона.
Ответ: 24.
