Как определить число нуклонов в ядре атома?
Число нуклонов в ядре атома равно массовому числу атома (относительная атомная масса химического элемента) или сумме протонов и нейтронов.
Как определить число протонов в атоме?
Число протонов в атоме равно заряду его ядра (обозначается как Z) или порядковому номеру элемента в периодической таблице Менделеева.
Как определить число нейтронов в атоме?
Очень просто!
N = A – Z
Где N – число нейтронов, A – атомная масса элемента (в целых числах), Z – заряд ядра атома или порядковый номер атома в периодической таблице Менделеева.
Развернутый ответ
Масса атома складывается из двух величин: масса протонов + масса нейтронов. Дело в том, что масса электронов пренебрежимо мала.
Масса нейтрона = 1,674 927 498 04(95)⋅10⁻²⁷ кг= 1,008 664 915 60(57) а.е.м.
Масса протона = 1,672 621 923 69(51)⋅10⁻²⁷ кг = 1,007276466621(53) а.е.м.
Масса электрона = 9,109383 7015(28)⋅10⁻³¹ кг = 0,000548579909065 а.е.м.
То есть даже 100 электронов дадут в сумме всего 0,0548579909065 а.е.м.
Первоначально Д. И. Менделеев в построении своей периодической таблицы исходил из атомных весов элементов. Однако, дальнейшее развитие науки показало, что свойства химических элементов находятся в прямой зависимости не от атомной массы химического элемента, а от заряда ядра его атома. Таким образом, в периодической таблице химические элементы выстроены в порядке возрастания заряда ядра атома и номер элемента в таблице соответствует заряду его ядра. А заряд ядра равен сумме протонов. То есть № (элемента) = Z (заряд ядра или число протонов).
Остаток массы ядра приходится на нейтроны. Поэтому чтобы определить число нейтронов в атоме нужно всего лишь вычесть из атомной массы число протонов, которое равно заряду ядра или порядковому номеру элемента в таблице Менделеева.
Примеры
Сколько протонов и нейтронов в атоме натрия?
Ar (Na) = 23 а.е.м.
Z (Na) = 11 (протонов)
N = Ar (Na) – Z (Na) = 23 – 11 = 12 (нейтронов)
Ответ: число протонов в атоме натрия равно 11, а число нейтронов в атоме натрия равно 12.
Сколько протонов и нейтронов в атоме фосфора?
Ar (P) = 31 а.е.м.
Z (P) = 15 (протонов)
N = Ar (P) – Z (P) = 31 – 15 = 16 (нейтронов)
Ответ: число протонов в атоме фосфора равно 15, а число нейтронов в атоме фосфора равно 16.
Сколько протонов и нейтронов в атоме золота?
Ar (Au) = 197 а.е.м.
Z (Au) = 79 (протонов)
N = Ar (Au) – Z (Au) = 197 – 79 = 118 (нейтронов)
Ответ: число протонов в атоме золота равно 79, а число нейтронов в атоме золота равно 118.
Сколько протонов и нейтронов в атоме кремния?
Ar (Si) = 28 а.е.м.
Z (Si) = 14 (протонов)
N = Ar (Si) – Z (Si) = 28 – 14 = 14 (нейтронов)
Ответ: число протонов и нейтронов в атоме кремния равно 14.
Сколько протонов и нейтронов в атоме углерода?
Ar (C) = 12 а.е.м.
Z (C) = 6 (протонов)
N = Ar (C) – Z (C) = 12 – 6 = 6 (нейтронов)
Ответ: число протонов и нейтронов в атоме углерода равно 6.
Сколько протонов и нейтронов в атоме калия?
Ar (K) = 39 а.е.м.
Z (K) = 19 (протонов)
N = Ar (K) – Z (K) = 39 – 19 = 20 (нейтронов)
Ответ: число протонов в атоме калия равно 19, а число нейтронов в атоме калия равно 20.
Сколько протонов и нейтронов в атоме железа?
Ar (Fe) = 39 а.е.м.
Z (Fe) = 19 (протонов)
N = Ar (Fe) – Z (Fe) = 56 – 26 = 30 (нейтронов)
Ответ: число протонов в атоме железа равно 19, а число нейтронов в атоме железа равно 30.
Сколько протонов и нейтронов в атоме алюминия?
Ar (Al) = 27 а.е.м.
Z (Al) = 13 (протонов)
N = Ar (Al) – Z (Al) = 27 – 13 = 14 (нейтронов)
Ответ: число протонов в атоме алюминия равно 13, а число нейтронов в атоме алюминия равно 14 .
Сколько протонов и нейтронов в атоме фтора?
Ar (F) = 19 а.е.м.
Z (F) = 9 (протонов)
N = Ar (F) – Z (F) = 19 – 9 = 10 (нейтронов)
Ответ: число протонов в атоме фтора равно 9, а число нейтронов в атоме фтора равно 10.
Сколько протонов и нейтронов в атоме хлора?
Ar (Cl) = 35 а.е.м.
Z (Cl) = 17 (протонов)
N = Ar (Cl) – Z (Cl) = 35 – 17 = 18 (нейтронов)
Ответ: число протонов в атоме хлора равно 17, а число нейтронов равно 18.
Сколько протонов и нейтронов в атоме кислорода?
Ar (O) = 16 а.е.м.
Z (O) = 8 (протонов)
N = Ar (O) – Z (O) = 16 – 8 = 8 (нейтронов)
Ответ: число протонов и нейтронов в атоме кислорода равно 8.
Сколько протонов и нейтронов в атоме серы?
Ar (S) = 32 а.е.м.
Z (S) = 16 (протонов)
N = Ar (S) – Z (S) = 32 – 16 = 16 (нейтронов)
Ответ: число протонов и нейтронов в атоме серы равно 16.
Сколько протонов и нейтронов в атоме магния?
Ar (Mg) = 32 а.е.м.
Z (Mg) = 16 (протонов)
N = Ar (Mg) – Z (Mg) = 24 – 12 = 12 (нейтронов)
Ответ: число протонов в атоме магния равно 16, а число нейтронов равно 12.
Сколько протонов и нейтронов в атоме цинка?
Ar (Zn) = 65 а.е.м.
Z (Zn) = 30 (протонов)
N = Ar (Zn) – Z (Zn) = 65 – 30 = 35 (нейтронов)
Ответ: число протонов в атоме цинка равно 30, а число нейтронов в атоме цинка равно 35.
Похожие вопросы:
– Какие атомы имеют одинаковое число нейтронов?
– Как определить общее число электронов в атоме?
Укажите нуклонное число элемента с порядковым номером 13.
Решение задачи
Напомню, что ядра атомов химических элементов состоят из протонов и нейтронов, общее название которых нуклоны.
Протон и
нейтрон – элементарные частицы, обладающие практически одинаковой массой, но
различным зарядом.
Химические элементы в таблице Д.И. Менделеева расположены в порядке возрастания положительного заряда их ядер, выраженного в относительных единицах, а положительный заряд ядра определяется числом протонов в нем, поэтому
порядковый номер химического элемента указывает число протонов в ядре (Z).
Надо помнить, что округленное значение относительной атомной массы Ar химического элемента равно общему числу нуклонов (нуклонное число) в ядре.
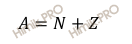
Где:
N – число нейтронов
в ядре;
A – округленное значение Ar (нуклонное число);
Z – число протонов в
ядре.
В таблице Д.И. Менделеева элемент с порядковым номером 13 – это алюминий (Al).
Так как округленное значение относительной атомной массы алюминия (Al) равно 27, следовательно нуклонное число элемента алюминий (Al) равно 27:
А (Al) = 27.
Ответ:
нуклонное число 27.
Как найти количество протонов, электронов,нуклонов и нейтронов?Напишите формулы и разьясните что к чему.
Daria
Знаток
(258),
закрыт
9 лет назад
Алла Калінчук
Мыслитель
(5437)
12 лет назад
число протонов=числу электронов =номеру в таблице Менделеева
чтоб найти число нейтронов, надо от массы-номер
напимер., Литий№3,масса 7.протонов, электронов будет по 3,нейтронов 7-3=4
Нуклоны это протоны+нейтроны (они в ядре) число нуклонов=массе, у лития 7
Урок 41
Тема: строение атома. Состав атомных ядер. Протонное и
нуклонное число
Цель:
повторить строение атома, ознакомить учащихся со строением атомных ядер, дать
понятие протон, нейтрон, протонне , нуклонне число; научиться рассчитывать
число протонов и нейтронов в ядрах атомов, находить в ПС протонне и нуклонне
числа для каждого элемента, знать их значение.
Оборудование:
ПСХЕ, таблица „ Строение атома”
Тип
урока: ВНМ ( д )
Формы
работы: лекция, беседа, химическая разминка, собственные примеры
Ход
урока:
И.
организация класса
ИИ.
Объявление темы и цели урока
III.
Актуализация опорных знаний. Химическая разминка по основным вопросам темы. Эти
вопросы, как обычно записаны на доске.
*
Периодический закон дополняем по ходу урока
*
Периодическая система-ядро
*
Период-электрон
•
Виды периодов – протон
*
Группа-нейтрон
•
Подгруппы – протонне число
*
Главная п / г – нуклонное число
•
Побочная п/г
В
это время несколько учеников на доске выполняют домашнее задание
IV.
Мотивация учебной деятельности.
Начинаем
мотивацию с задания:
Знайте
в ПС случаи несоответствия положения элемента со значением его относительной
атомной массы. Ученики находят и учитель объясняет, что ко времени открытия
периодического закона уровень развития такой науки, как физика был низок,
строение атома еще не было изучено. Учитель рассказывает о исследования Е.
Резерфорда по изучению строения атома и объясняет, что только после изучения
его строения было объяснено причину периодического повторения свойств
элементов.
V.
изучение нового материала.
1.
Рассказ учителя об опыте Э. Резерфорда, ядерная модель атома.
2.
Вспоминаем с учащимися строение атома, схемку ,которую мы изучили еще в 7
классе.
АТОМ
ЯДРО ЭЛЕКТРОНЫ
(+) (- )
протоны нейтроны
( + ) ( 0 )
Напоминаем,
что атом электронейтральный, потому что положительный заряд ядра атома
уравновешивается суммарным отрицательным зарядом всех электронов.
3.
Объясняем, что номер, под которым элемент стоит в ПС , указывает на заряд ядра
его атома. Например, если Натрий стоит под порядковым номером 11, то заряд ядра
его атома + 11, Кальций под номером 20 , то и заряд ядра его атома + 20 и т.д.
4.
Объясняем, что ядро состоит из протонов и нейтронов, даем понятие, какая
частица является протоном и нейтроном.
5.
Объясняем , что такое протонне число и нуклонне число. Учим учеников находить в
ПСХЕ протонные и нуклонные числа элементов, записывать их.
Объясняем
понятия и обозначения „ нуклид”.
Нуклонное число 23 относительная атомная масса (а)
Na
Протонне число 11 Порядковый номер (Z )
16
нуклид Оксиген-16, или O
6.
Учим учеников рассчитывать число протонов и нейтронов в ядрах атомов по формуле
A = Z + N, где А – число нуклонне
Z – протонне число
N-нейтроны
Итак,
чтобы рассчитать количество нейтронов в ядрах атомов надо от нуклонного числа
вычесть протонное число: N = A – Z . Например, в ядре атома натрия будет 23 –
11= 12 нейтронов.
VI.
Закрепление изученного. „ Свои примеры”
1.
Учитель записывает на доске запись и предлагает ученикам прокомментировать ее и
привести собственные примеры.
24
Mg
12
2.
Учитель рассчитывает количество нейтронов в ядре любого элемента и предлагает
учащимся привести свои примеры.
VII.
Подведение итогов урока.
Делаем вывод, что химические элементы расположены у ПС по возрастанию зарядов
их атомных ядер, а не по возрастанию относительной атомной массы.
VIII.
Домашнее задание.
Введённое нами понятие атома рассматривает его как систему, в которой положительно заряженное ядро (состоит из протонов и нейтронов) окружено вращающимися вокруг него электронами. Рассмотрим само ядро (рис. 1). Контуры ядра не настолько округлые, но всё же ядром можно назвать область пространства в условном геометрическом центре ядра, где сосредоточены протоны и нейтроны. Протон — положительно заряженная частица, нейтрон — нейтральная частица. Вместе их удерживают внутриядерные силы (лучше пока о них много не знать) и внеядерное присутствие отрицательно заряженных электронов.

Рис. 1. Ядро
Ядра различных веществ содержат различное количество протонов. Данный факт является основой для таблицы Менделеева. В данной таблице у водорода () — первый элемент таблицы, присутствует один протон, далее ядро гелия (
) — второй элемент, имеет два протона и так далее. При этом количество нейтронов в одном и том же веществе может быть разным.
Введём некоторые понятия ядерной физики:
Количество нуклонов — суммарное количество протонов и нейтронов.
Изотопы — ядра одного и того же вещества, имеющие одно и то же количество протонов, но разное количество нейтронов.

Рис. 2. Обозначение ядра
Для рассмотрения элементов в курсе ядерной физики вводят специальные обозначения (рис. 2). Рассмотрим гипотетический элемент . В предложенной форме записи число снизу указывает на количество протонов, а сверху — количество нуклонов (протонов+нейтронов).
Примеры:
— ядро лития, состоящее из 3 протонов и 7-3=4 нейтронов,
— ядро алюминия, состоящее из 13 протонов и 27-13=14 нейтронов,
— ядро меди, состоящее из 29 протонов и 63-29=34 нейтронов.
Таким образом, исходя из таблицы Менделеева, можно сформировать внешний вид элемента (рис. 2) или, исходя из внешнего вида, определить сам элемент.
Исходя из введённых нами понятий и изображений, в ядерной физике школьного уровня выделяют три типа задач:
- задачи на уравнение радиоактивного распада
- задачи на ядерные реакции
- задачи, касающиеся энергии ядерных реакций
