Рассчитать объем азота.
Рассчитать объем азота (газа) при нормальных условиях, если известна его масса, можно по формуле: V = m · Vm / M = ν · Vm. Рассчитать объем азота (газа), если известна его масса, температура и давление, можно по формуле: V = m · R · T / (p · M) = ν · R · T / p.
Химическая формула азота N₂.
Расчет объема азота (газа)
Теория расчета объема газа
Пример: Рассчитайте объем для 140 кг азота
Рассчитать объем газа: азота, водорода, воздуха, гелия, озона, кислорода, углекислого газа, хлора
Рассчитать объем азота (газа) при нормальных условиях:
Рассчитать объем азота (газа):
Теория:
Рассчитать объем азота (газа) при нормальных условиях, если известна его масса, можно по формуле:
V = m · Vm / M = ν · Vm,
где
V – объем газа, л,
ν – количество вещества, моль,
Vm – молярный объем газа, л/моль, Vm = 22,4 л/моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(N₂) = 2·14 = 28 г/моль.
Нормальные условия: 0 оС (или 273,15 К), 101,325 кПа или 1 атм.
Рассчитать объем азота (газа), если известна его масса, температура и давление, можно по формуле:
V = m · R · T / (p · M) = ν · R · T / p,
где
V – объем газа, л,
ν – количество вещества, моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(N2) = 2·14 = 28 г/моль,
R – универсальная газовая постоянная, R ≈ 8,314 Дж/(моль⋅К),
T – термодинамическая температура, К.
P – давление, кПа.
Пример: Рассчитайте объем для 140 кг азота:
Рассчитайте объем для 140 кг азота (газа) при нормальных условиях.
V = m · Vm / M = 140 000 грамм · 22,4 л/моль / 28 г/моль = 112 000 литров или 112 м3.
Рассчитайте объем для 140 кг азота (газа) при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = m · R · T / p · M = 140 000 грамм · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа · 28 г/моль) = 420 064,85 литров или 420,06485 м3.
Рассчитать объем газа: азота, водорода, воздуха, гелия, озона, кислорода, углекислого газа, хлора
Коэффициент востребованности
2 181
Как найти объем газа (азота или водорода), если мне известен вес данного газа?
Профи
(827),
закрыт
16 лет назад
Елена Баровик
Мастер
(2438)
16 лет назад
молярный объем любого газа – 22,4 л/моль. Посчитайте, сколько моль газа, если известна его химическая формула, потом умножайте кол-во моль на 22,4. Нормальные условия (20 по цельсию, одна атмосфера)
Паралипоменонов-Навуходоносоров
Мыслитель
(8427)
16 лет назад
Собственно, газ может принимать любой объём, зная один только вес (P=mg), объём не определить. Газ весом, например 20 ньютон может находиться и в 10 мл ампуле и в 10000 л цистерне. Давление бы ещё и температуру знать
Источник: Голова моя глупая, безногая, безрукая
Валерий Меренков
Оракул
(54289)
16 лет назад
Наверное, не ВЕС, а МАССА?
Если так, то нгаз может занимать любой объём (будет меняться лишь давление) Чтобы найти объём, занимаемый газом при нормальных условиях надо массу газа, разделить на его молярную массу и умножить на 22,4 л. – средний объём моля любого газа при нормальных условиях.
Молярный
объём – это объём 1 моль вещества. Понятие молярного
объема применимо для газов. Например, если взять 1 моль воды, то мы
не взвешиваем на весах 18 г воды, т.к. это совершенно неудобно, а зная, что
плотность воды 1 г/мл, мы измеряем её объем цилиндром или мензуркой.
Молярный
объем воды в таком случае будет равен 18 мл/моль. Молярный
объём твёрдых веществ и жидкостей зависит от их плотности. Молярный
объём воды, кислоты, сахара и соли отличается между собой, потому что и
плотности их тоже отличаются.
Если
взять 1 моль кислорода, 1 моль углекислого газа, 1 моль водорода, то при
одинаковых нормальных условиях они будут занимать одинаковый объем,
равный 22,4 л. Эти газы также будут содержать и одинаковое число частиц,
т.е. 6,02 · 1023. Нормальными условиями или н.у. принято
считать температуру 0 0С (градусов по Цельсию) и давление 760 мм.
рт. ст. (миллиметров ртутного столба) или 101,3 кПа (килопаскаля).
Следовательно,
молярный объём – это объём газа количеством 1 моль. Обозначается молярный
объём, как и любой другой объем, но с символом Vm.
Кроме
того, молярный объём – это физическая величина, равная отношению объёма
вещества к количеству вещества. Это можно записать в виде формулы:
Vm
=
V
–
это объём газа, n
–
это количество вещества.
Из
этого выражения можно найти и V.
V=
n
· Vm
Единицей
измерения молярного объёма является л/моль, и т.к. это величина
постоянная при нормальных условиях, то молярный объём равен 22,4 л/моль.
Объём
1 кмоля называют киломолярным объёмом и измеряют в м3/кмоль,
т.е. он равен 22,4 м3/кмоль, а объём 1 ммоля называют миллимолярным
объёмом, измеряют его в мл/ммоль, т.е. миллимолярный объём равен 22,
4 мл/ммоль.
Используя
новые формулы, решим задачи.
1.
Найдите объём азота (N2)
количеством 2 моль.
Найдем объем азота (N2)
количеством 2 моль. По условию нам дано количество вещества азота – 2 моль.
Найти необходимо его объем. Для решения задачи используем формулу нахождения
объема газа через количество вещества, т.е. нужно молярный объем умножить на
количество вещества. Подставляем значения в формулу, т.е. 22,4 литра на моль
умножаем на 2 моль, в результате получаем 44,8 литра. Следовательно, 2 моль
азота занимает объем 44,8 л.
2.
Найдите количество вещества озона (O3)
объёмом 67,2 л.
По
условию задачи нам дан объем озона – 67,2 литра, найти нужно количество
вещества озона. Для решения задачи используем формулу: объем, разделенный на
молярный объем, подставим значения в формулу, т.е. 67,2 литра делим на 22,4
литра на моль, получаем результат – 3 моль. Поэтому 3 моль озона занимают объем
67,2 л.
Рассчитайте количество вещества, массу и объём (н. у.) порции азота
N
2
, содержащей
9
,
03
∗
10
23
атомов азота.

reshalka.com
ГДЗ Химия 8 класс класс Габриелян. §19. Примените свои знания. Номер №8
Решение
Дано:
N (N) =
9
,
03
∗
10
23
Найти:
n − ?
m − ?
V − ?
Решение:
Зная количество атомов, найдем количество вещества: n = N : Na.
n (
N
2
) =
9
,
03
∗
10
23
:
6
,
02
∗
10
23
= 1,5 моль
Зная количества азота, можем найти массу: m = n * M.
m (
N
2
) = 1,5 моль * 28 г/моль = 42 г
Зная количество вещества, найдем объем газа: V = n * Vm.
V (
N
2
) = 1,5 моль * 22,4 л/моль = 33,6 л
Ответ: n = 1,5 моль; m = 42 г; V = 33,6 л.
Молярный объем газа


4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
Для того, чтобы узнать состав любых газообразных веществ необходимо уметь оперировать такими понятиями, как молярный объем, молярная масса и плотность вещества. В данной статье рассмотрим, что такое молярный объем, и как его вычислить?
Количество вещества
Количественные расчеты проводят с целью, чтобы в реальности осуществить тот или иной процесс или узнать состав и строение определенного вещества. Эти расчеты неудобно производить с абсолютными значениями массы атомов или молекул из-за того, что они очень малы. Относительные атомные массы также в большинстве случаев невозможно использовать, так как они не связаны с общепринятыми мерами массы или объема вещества. Поэтому введено понятие количество вещества, которое обозначается греческой буквой v (ню) или n. Количество вещества пропорционально числу содержащихся в веществе структурных единиц (молекул, атомных частиц).
Единицей количества вещества является моль.
моль – это такое количество вещества, которое содержит столько же структурных единиц, сколько атомов содержится в 12 г изотопа углерода.
Масса 1 атома равна 12 а. е. м., поэтому число атомов в 12 г изотопа углерода равно:
Na= 12г/12*1,66057*10в степени-24г=6,0221*10 в степени 23
Физическая величина Na называется постоянной Авогадро. Один моль любого вещества содержит 6,02*10 в степени 23 частиц.

Молярный объем газа
Молярный объем газа – это отношение объема вещества к количеству этого вещества. Эту величину вычисляют при делении молярной массы вещества на его плотность по следующей формуле:
Vm=M/p,
где Vm – молярный объем, М – молярная масса, а p – плотность вещества.
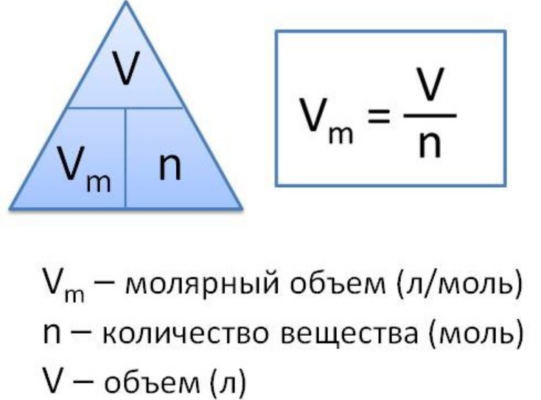
В международной системе Си измерение молярного объема газообразных веществ осуществляется в кубических метрах на моль (м3 /моль)
Молярный объем газообразных веществ отличается от веществ, находящихся в жидком и твердом состоянии тем, что газообразный элемент количеством 1 моль всегда занимает одинаковый объем (если соблюдены одинаковые параметры).
Объем газа зависит от температуры и давления, поэтому при расчетах следует брать объем газа при нормальных условиях. Нормальными условиями считается температура 0 градусов и давление 101,325 кПа. Молярный объем 1 моля газа при нормальных условиях всегда одинаков и равен 22,41 дм3 /моль. Этот объем называется молярным объемом идеального газа. То есть, в 1 моле любого газа (кислород, водород, воздух) объем равен 22,41 дм3 /м.

Таблица «молярный объем газов»
В следующей таблице представлен объем некоторых газов:
| Газ | Молярный объем, л |
| H2 | 22,432 |
| O2 | 22,391 |
| Cl2 | 22,022 |
| CO2 | 22,263 |
| NH3 | 22,065 |
| SO2 | 21,888 |
| Идеальный | 22,41383 |

Что мы узнали?
Молярный объем газа, изучаемый по химии (8 класс) наряду с молярной массой и плотностью являются необходимыми величинами для определения состава того или иного химического вещества. Особенностью молярного газа является то, что в одном моле газа всегда содержится одинаковый объем. Этот объем называется молярным объемом газа.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
-

Аэлита Коробка
5/5
-

Александр Котков
5/5
-

Настя Бабич
5/5
-

Александр Котков
5/5
Оценка доклада
4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
А какая ваша оценка?
